Клинический разбор в общей медицине №3 2023
Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia
omekan@mail.ru
Abstract
The drastic increase in life expectancy of the population, referred to as “silver tsunami” and demanding the development of such an entirely new branch of medical science as “anti-age medicine”, is one of the most pressing issues of modern demography. It is believed that aging of the body is inevitably associated with reduced quality of life, however, this postulate is currently urgently refuted, that is why the term “successful growing-up” is most relevant for the 21st century. There is a number of scientific studies focused on certain mechanisms underlying cellular senescence, which should be the therapeutic targets for prediction of age-related disorders. Thus, it is necessary to summarize the scientific evidence available and structure the modern approaches that contribute to “successful growing-up” under the innovation anti-aging concept.
Key words: anti-age, anti-aging, cellular senescence, successful growing-up.
For citation: Orazov M.R., Dolgov E.D. Inevitable aging or successful growing-up? Anti-aging medicine: the abstract in concrete terms. Clinical review for general practice. 2023; 4 (3): 67–76. DOI: 10.47407/kr2023.4.3.00226
Разработка революционных фармакологических препаратов, инновационного оборудования, внедрение в практику генетического обследования и других медицинских технологий поспособствовали существенному увеличению общемирового показателя продолжительности жизни. В 2012 г. средняя продолжительность жизни в Российской Федерации составляла 70,2 года, в 2017 г. показатель преодолел отметку в 72,7 года, а уже к 2024 г. прогнозируется повышение продолжительности жизни до 78 лет [1]. Говоря о демографии, мы подразумеваем две противоборствующие силы – прирост населения и депопуляцию. И в последнее время мы наблюдаем неоспоримую тенденцию увеличения численности населения: в 2013 г. население Земли составило 7,3 млрд человек, в 2023 г. показатель уже превысил
8 млрд, а согласно прогнозам к 2030 и 2050 г. показатель численности населения достигнет 8,5 и 9,6 млрд человек соответственно [2, 3]. Однако столь существенный демографический прирост обусловлен отнюдь не значительным повышением рождаемости, а повышением продолжительности жизни. Кроме того, на сегодняшний день людей старше 65 лет стало больше, чем детей младше 5 лет [3]. И это, безусловно, является самым настоящим демографическим парадоксом, которого ранее мир еще не видел. Важно отметить, что фокус эволюции медицинской науки должен динамически изменяться исходя из сегодняшних потребностей. Согласно весьма актуальной градации Всемирной организации здравоохранения, пожилой возраст начинается в 60 лет и заканчивается в 74 года, а старческий соответствует интервалу от 75 до 90 лет, все остальные люди, прожившие 90 и более лет, приписаны в ранг долгожителей. Однако становится очевидным тот факт, что не за горами то время, когда людей в возрасте старше 90 лет будут относить как минимум к группе старческого возраста. Более того, прогнозируется, что к 2030 г. каждому шестому жителю планеты будет более 60 лет, а к 2050 г. – и вовсе каждому пятому [4]! Данную ситуацию современные демографы как раз и именуют «серебряным цунами XXI века». Данный феномен привел нас к тому, что сейчас доля пожилого возраста в структуре человеческой жизни составит ни много ни мало 20–30%, что весьма остро ставит перед нами вопрос о необходимости введения такого понятия, как «успешное взросление». И если сейчас в наших руках повышение продолжительности жизни, то не менее важным остается вопрос качества той самой продленной жизни, которое, к сожалению, нередко страдает.
Долгое время философы всего мира размышляют о смысле жизни. Данный вопрос, стоящий на «повестке дня» далеко не одно столетие, до сих пор находится в «подвешенном» состоянии. Однако расширение и модернизация взглядов современного населения помогли человечеству отойти от унифицированного подхода к решению самых незаурядных вопросов. И сейчас мы хорошо понимаем, что смысл жизни, как и понятие счастья, у каждого свои. Однако любые ценности и потребности каждого конкретного человека успешно укладываются в общепринятое понятие качества жизни, о котором сейчас не говорит только ленивый.
И в данном контексте мы акцентируем внимание на том, что реализация «высшего смысла» в целом и счастья в частности невозможна без достижения должного уровня качества жизни. А человек пожилого и старческого возраста также имеет много целей и планов, для реализации которых ему необходима эмоциональная и физическая гармония.
Принято считать, что старение организма неизбежно приводит к развитию возраст-ассоциированных заболеваний и снижению качества жизни. Однако, как мы отметили выше, человек «60+» стремится к активной деятельности, не желая оставаться «за кулисами жизни». Исходя из этого медицина сделала «идеологический кульбит» и стала базироваться на принципах четырех «П»: предикция, превенция, партисипативность и персонализация. И в этой связи важно отметить, что современная медицина располагает ресурсом максимального сглаживания перехода из периода среднего возраста в пожилой. Предупреждение развития мультиорганных заболеваний, нейродегенерации, поддержание физической активности и восполнение нутриентных дефицитов – все это входит в основу современной концепции «успешного взросления» или так называемого «антиэйджинга», которая позволит женщине успешно «повзрослеть» и вовсе не ощущать на себе груз прожитых лет. Целью данной статьи была демонстрация современных подходов anti-age-медицины и возможностей предикции ряда возраст-ассоциированных заболеваний.
Наиболее распространенной концепцией «молекулярного старения» является теория укорочения теломер. Хорошо известно, что пролиферативный потенциал каждой соматической клетки определяется так называемым пределом Хейфлика, который отражает максимальное число возможных делений до того момента, пока клеточный цикл не остановится. Как правило, предел Хейфлика составляет 48–50 клеточных делений. Остановка клеточного цикла, в свою очередь, обуславливается двумя процессами: критическим укорочением теломерных участков, а также активацией экспрессии онкосупрессорных локусов, блокирующих дальнейшее клеточное деление. В ходе каждой репликации ДНК теряется от 50 до 200 пар теломерных оснований, что обусловлено невозможностью ДНК-полимеразы «обработать» весь хроматин. После достижения «точки невозврата» высвобождается так называемый секреторный комплекс, ассоциированный с клеточным старением (SASP), включающий провоспалительные цитокины, хемокины, факторы роста, протеазы и ангиогенные факторы, сигнализирующие клетке о критическом повреждении ДНК, что индуцирует экспрессию ингибиторов клеточного цикла p16INK4A и p21CIP1 и, как следствие, блокирование активности циклинзависимых протеинкиназ [5, 6]. Более того, все факторы, входящие в состав SASP-комплекса, обладают ауто- и паракринной активностью, активируя аналогичные процессы старения во всех рядом расположенных клетках. Аналогичный внутриклеточный каскад активируется и в случае появления экзо- и эндогенных триггеров, опосредованно приводящих через активацию p16INK4A/p21CIP1 к остановке клеточного цикла [7].
Не менее важным механизмом клеточного старения является оксидативный стресс, который возникает вследствие снижения утилизации организмом активных форм кислорода (пероксид водорода, супероксид-радикал и гидроксид-радикал). Повышение концентрации данных метаболитов приводит к повреждению ДНК и реализации типового механизма сигнализации, о котором мы упомянули выше [7].
Особое внимание в последние годы уделяется дисбалансу кишечного микробиома, реализующего воспалительные изменения стенки кишки и повышение ее проницаемости. Безусловно, прямые доказательства влияния дисбактериоза на развитие возраст-ассоциированных заболеваний отсутствуют. Однако ряд научных исследований выявили изменения кишечного микробиома при сахарном диабете 2-го типа (СД 2), ишемической болезни сердца, сердечной недостаточности, а также ряде онкологических заболеваний. Доказано, что кишечный микробиом регулирует целый ряд необходимых физиологических процессов: ферментирование и модификацию питательных веществ, синтез витаминов, стимуляцию антиоксидантных механизмов, а также стимуляцию иммунной системы и предупреждение процессов клеточного старения [26–30]. Хорошо известно, что с возрастом происходят существенные изменения как количественного, так и качественного состава кишечной микробиоты, проявляющиеся истощением пула лакто- и бифидобактерий. Кроме того, важно отметить, что исследователями был выявлен один из потенциальных механизмов реализации механизмов старения, ассоциированных с изменениями микробиома. Так, метилглиоксаль, являясь одним из метаболитов бактериального происхождения, способствует активации старения кожных фибробластов и реализации ассоциированных с онкогенными агентами процессов клеточного старения [6, 8]. Исходя из этого становится совершенно очевидным факт ассоциации дисбактериоза с рядом нозологий и ключевыми механизмами старения, что также должно являться потенциальной терапевтической мишенью у пациенток пожилого возраста.
Таким образом, необходимо отметить, что все описанные процессы приводят к снижению регенераторного и пролиферативного потенциала клеток, что и лежит в основе клеточного старения. Данные механизмы и будут являться основными точками приложения для современной концепции anti-age-медицины, которая позволит не только замедлить процессы старения, но и обратить их вспять.
Исследователи обнаружили, что в кардиомиоцитах пожилых людей как с ожирением, так и без него длина теломерных повторов оказалась на 30% ниже стандартного показателя, при этом аналогичная ситуация отмечалась и у молодых людей, однако степень редукции теломер была несколько ниже. Оказалось, что укорочение теломер у лиц с верифицированным ожирением ассоциировано с повышением активности фактора теломерного повтора-1 (TRF-1), ингибирующего активность теломеразы, ответственной за удлинение теломерных участков. Кроме того, провоспалительные изменения, индуцированные ожирением, способствуют активации пролиферации лейкоцитарного звена в периферических тканях, также способствующего опосредованному сокращению теломерных участков [6]. Также необходимо отметить, что кроме влияния на TRF-1 ожирение способствует накоплению SASP-комплексов за счет повышенной продукции адипоцитами провоспалительных цитокинов и адипокинов, опосредованно накладывающих арест на клеточный цикл через стандартный и описанный нами выше механизм. Также была выявлена прямая взаимосвязь между ожирением и развитием СД 2. Так, описанные комплексы SASP кроме сигнализации о повреждении ДНК приводят к снижению антиоксидантной активности и митохондриальной дисфункции, что неизбежно затрагивает гепатоциты и β-клетки поджелудочной железы. Вследствие развития клеточной метаболической дисфункции нарушаются процессы окисления жирных кислот и снижается эндокринная функция поджелудочной железы, что способствует развитию инсулинорезистентности [10].
Резюмируя вышесказанное, необходимо отметить исключительно важную роль ожирения в реализации ключевых процессов клеточного старения. А исходя из имеющихся научных данных, мы формируем главный тезис: «Неважно, сколько пациентке лет, важно то, есть ли у нее ожирение». Мы акцентируем внимание на том, что основным звеном клинического менеджмента таких пациенток является не их стратификация исходя из возрастного показателя, а верификация у нее избыточной массы тела, потенцирующей ключевые механизмы клеточного старения, что демонстрирует актуальность anti-ageing-концепции не только у женщин пожилого/старческого возраста, но и у пациенток средней возрастной когорты. Именно на этом принципе должен основываться клинический менеджмент в рамках anti-ageing-концепции, ведь ожирение – это уникальная нозология, создающая огромную пропасть между фактическим и биологическим возрастом пациентки.
Важно отметить, что основные расстройства постменопаузы определяются именно преимущественной локализацией рецепторов к эстрогенам. Наиболее ранним расстройством постменопаузы является климактерический синдром, включающий приливы жара, нейровегетативную симптоматику, а также психоэмоциональные девиации, которые способствуют существенному снижению качества жизни пациентки. Следующим «испытанием» в этот период является генитоуринарный менопаузальный синдром (ГУМС), характеризующийся появлением урогенитальной атрофии и дебютированием ряда характерных симптомов: зуд, сухость, жжение, диспареуния, дизурия и недержание мочи [13]. Кроме того, снижение толщины эпителиального компартмента вульвовагинальной зоны приводит к снижению pH и содержания лактобактерий, а также активации размножения условно-патогенной флоры, что приводит к развитию рецидивирующих воспалительных заболеваний [14, 15]. Однако наиболее грозными и отдаленными расстройствами постменопаузы являются снижение минеральной плотности костной ткани – МПКТ (остеоартриты, остеопороз), неврологические нарушения (болезнь Альцгеймера, когнитивный дефицит), сердечно-сосудистые заболевания – ССЗ (атеросклероз и ассоциированные с ним состояния), а также менопаузальный метаболический синдром [16]. Важно отметить, что кроме эндогенных проявлений эстрогенодефицита отмечаются и внешние признаки «репродуктивного старения», такие как дряблость кожи, морщины, а также изменения качества и структуры волос [17].
Таким образом, важно отметить, что менопауза является поистине важным событием в жизни женщины, к которому необходимо быть готовой. «Распознать и устранить» – вот главная задача клинициста в ходе менеджмента пациенток с климактерическим синдромом и другими расстройствами постменопаузы. Менопауза является достоверным предвестником общего старения организма, что необходимо учитывать в рамках концепции антиэйджинга.
Как мы выше отметили, в основе старения женского организма лежат изменения, связанные с менопаузой. С целью прогнозирования менопаузальных расстройств необходимо использование модифицированной шкалы STRAW+10, согласно которой клиницист может провести тщательную стратификацию пациенток и отнести каждую из них к определенной стадии: стадия -1 соответствует поздней переходной фазе, стадия +1 – ранней постменопаузе, подразделяющейся на три этапа (+1a, +1b, +1c), а стадия +2 соответствует поздней постменопаузе. Основными инструментами стратификации пациенток по данной шкале являются определение характера менструального цикла, а также маркеров овариального резерва (концентрации фолликулостимулирующего, антимюллерова гормонов, ингибина B, числа антральных фолликулов) [18]. Определение «репродуктивной стадии» согласно шкале STRAW+10 позволит спрогнозировать развитие возможных менопаузальных расстройств и вовремя начать мероприятия в рамках anti-ageing-концепции.
Также необходимо отметить инструменты объективизации расстройств постменопаузы, к которым относятся специальные оценочные шкалы. С целью верификации и объективизации климактерического синдрома возможно использование шкалы Грина, включающей ряд вазомоторных, нейровегетативных и психоэмоциональных симптомов. Согласно данной шкале возможна стратификация пациенток в зависимости от тяжести климактерического синдрома: результат в 1–11 баллов соответствует климактерическому синдрому легкой степени тяжести, 12–19 баллов – средней степени, а 20 и более баллов – тяжелой степени [19].
Наиболее актуальными методами объективизации ГУМС являются измерение индекса вагинального здоровья (по G. Bachmann) и использование шкалы D. Barlow для определения тяжести симптоматики ГУМС [20].
Не менее важным является верификация снижения МПКТ. Так, «золотым стандартом» определения МПКТ, отраженным в отечественных рекомендациях по ведению пациенток в постменопаузе, является двуволновая рентгеновская абсорбциометрия, по результатам которой определяется так называемый Т-критерий. О наличии остеопороза свидетельствует величина Т-критерия от -2,5 и менее [21].
Также необходимо отметить важность оценки состояния сердечно-сосудистой системы, поскольку именно острые сердечно-сосудистые события приводят к выраженной инвалидизации пациенток, а нередко бывают фатальны. Наиболее удобным и простым методом оценки состояния сердечно-сосудистой системы является измерение артериального давления на обеих руках с целью верификации атеросклеротических поражений сосудов. С этой же целью возможно измерение лодыжечно-плечевого индекса (норма >0,9). Не менее важным является определение нарушений в показателях липидограммы: повышение общего холестерина, триглицеридов, липопротеинов низкой плотности и снижение содержания липопротеинов высокой плотности [22] – и определение антропометрических показателей, таких как масса тела, индекс массы тела (норма – до 25 кг/м2) и окружность талии (норма – до 80 см). Одним из наиболее современных методов диагностики ожирения является биоимпедансометрия – метод определения процентного содержания жира в организме путем прохождения электрической волны через ткани организма [23]. Данный метод является крайне актуальным, поскольку на данный момент у многих пациенток отмечается так называемое «скрытое» ожирение, когда отсутствуют внешние признаки ожирения и при этом существенно повышается объем перивисцеральной жировой ткани. Исходя из этого необходимо отметить, что своевременная верификация и лечение ожирения позволят не только профилактировать заболевания сердечно-сосудистой системы, но и замедлить процессы клеточного старения.
Дополнительными методами обследования в рамках anti-age-концепции являются осмотр и пальпация молочных желез, а также проведение скрининговой маммографии 1 раз в 2 года после 40 лет [24]. Верификация заболеваний молочных желез является крайне актуальной в рамках концепции антиэйджинга, поскольку нередко они свидетельствуют о возрастной перестройке гормонального фона пациенток.
Кроме того, в рамках anti-age-концепции необходимо определение микронутриентного профиля у пациентки с определением концентраций витаминов и минералов, наиболее важными из которых являются витамин D и железо, о которых будет упомянуто ниже [25].
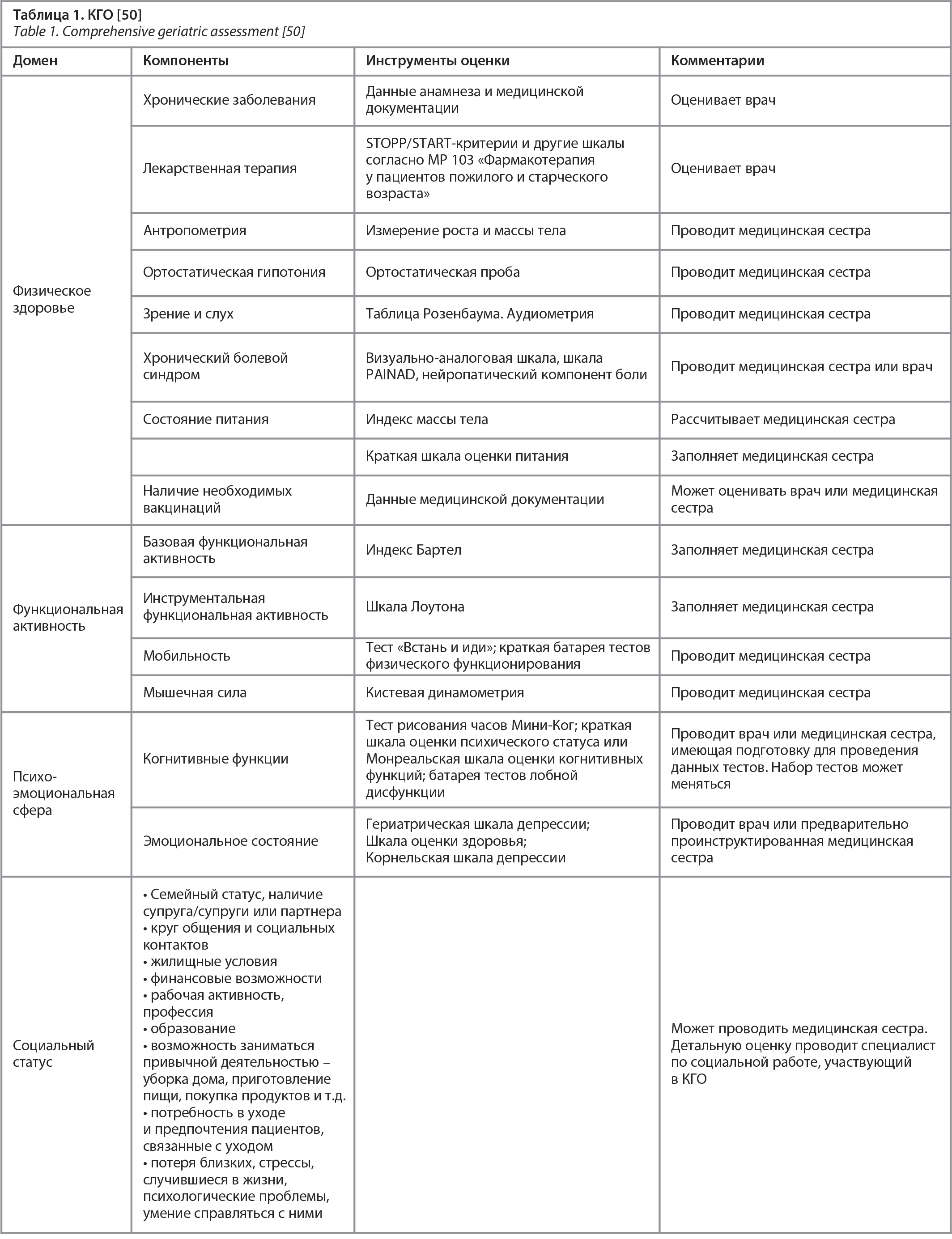
Однако кроме выявления предпосылок к развитию возраст-ассоциированных заболеваний необходимо сделать особый акцент на оценку показателей качества жизни пациентки и перейти к не менее главному этапу anti-age-скрининга. В данном контексте возможно проведение так называемой комплексной гериатрической оценки (КГО) с использованием ряда объективизирующих оценочных шкал, с помощью которой клиницист описывает текущее состояние пациентки путем оценивания 4 основных доменов: физическое здоровье, функциональная активность, психоэмоциональная сфера и социальный статус (табл. 1). На основании КГО клиницист определяет ключевые проблемы, снижающие функциональный статус и качество жизни пациенток, а в дальнейшем разрабатывает индивидуальный план мероприятий для их коррекции [50].
Таким образом, вопрос комплексного обследования пациентки в рамках программы антиэйджинга является чрезвычайно важным. Клеточное старение неизбежно приводит к снижению функции различных органов и систем, что диктует необходимость междисциплинарного подхода не только к обследованию в рамках anti-age-концепции, но и для осуществления антиэйджинг-мероприятий. В этой связи необходимо отметить, что сама концепция anti-age-медицины подразумевает формирование «anti-age-команды», состоящей из акушера-гинеколога, эндокринолога, кардиолога, геронтолога и других специалистов, для осуществления эффективного клинического менеджмента пациенток.
Рекомендуется назначение менопаузальной гормональной терапии (МГТ) женщинам в пери- и постменопаузе для лечения вазомоторных симптомов умеренной и тяжелой степени, симптомов ГУМС, сексуальной дисфункции, а также с целью профилактики постменопаузального остеопороза. МГТ является эффективным методом предикции потери костной массы, при этом наиболее выраженный эффект отмечается при раннем начале терапии (уровень убедительности рекомендаций – УУР А) [21].
Рекомендуется назначение локальной гормональной терапии на основе препаратов эстриола у пациенток с симптомами ГУМС и сексуальной дисфункции (УУР С) [21].
Рекомендуется назначение альтернативных методов терапии у пациенток при наличии противопоказаний или нежелания использовать МГТ. Одними из главных альтернативных методов терапии и предикции климактерического синдрома являются: коррекция образа жизни и снижение массы тела, использование когнитивно-поведенческой терапии, а также иглорефлексотерапия и гипноз (УУР А) [21].
Рекомендуется использование лубрикантов в качестве альтернативы локальной гормональной терапии у пациенток с симптомами ГУМС (УУР B) [21].
Рекомендуется поддерживать адекватный уровень регулярной физической активности с целью профилактики когнитивных расстройств [39].
Рекомендуется выполнение физических упражнений с осевыми нагрузками (ходьба, бег, танцы, подвижные игры) с целью поддержания МПКТ у здоровых пожилых людей (УУР С) [31].
Рекомендуется проведение умеренных силовых тренировок (пилатес, тай-чи, плавание и др.) для укрепления мышечного каркаса и улучшения координации у пожилых людей с переломами в анамнезе или с диагностированным остеопорозом (УУР B) [31].
Рекомендуется поддержание адекватного уровня психической и социальной активности с целью профилактики развития когнитивных расстройств [39]. Важно отметить, что социализация необходима для «успешного взросления» пациенток, поскольку она не позволяет им закрыться в себе. Актуальными являются любые виды социальной и умственной активности: разгадывание кроссвордов, лингвистические групповые занятия, чтение книг, йога, пилатес и др.
Рекомендуется соблюдение принципов здорового питания для профилактики когнитивных расстройств (УУР С) [39].
Рекомендуется соблюдение принципов правильного питания. Включение в рацион жирной и в высокой степени переработанной пищи способствует избыточному образованию продуктов гликирования и перекисного окисления липидов, повышающих риски возникновения СД и ССЗ. Диета с низким содержанием данных продуктов приводит к снижению инсулинорезистентности у людей с СД 2. В этой связи предпочтительно включение в рацион продуктов с низким содержанием жиров, сложных углеводов (бобовые, овощи, фрукты, цельные злаки), а также молочных продуктов с низким содержанием жира (УУР D) [33].
Рекомендуется употребление не менее 0,8 г белка на килограмм массы тела всем людям пожилого возраста (Европейское управление по безопасности пищевых продуктов); УУР С. Наиболее выраженное истощение физических и когнитивных ресурсов отмечается после 50 лет, однако адекватное потребление белка поможет замедлить процессы клеточного старения, прогрессирование потери костной и мышечной массы, а также профилактировать развитие когнитивного дефицита [38].
Рекомендуется прекращение курения для снижения риска развития когнитивных расстройств (УУР B) [39].
Рекомендуется сокращение употребления алкоголя для снижения риска развития когнитивных расстройств (УУР B) [39].
В качестве профилактики развития когнитивного дефицита и снижения риска развития деменции рекомендуется мультимодальный подход с коррекцией имеющихся факторов риска (УУР B). Основными факторами риска когнитивных расстройств являются: артериальная гипертензия, снижение слуха и ожирение в среднем возрасте; курение, депрессия, гиподинамия, социальная изоляция и СД у лиц старше 65 лет. Успешная коррекция ключевых факторов риска способна снизить вероятность развития деменции на 35% [39].
Рекомендуется использование витамина D (колекальциферола) в терапевтических дозах с целью коррекции дефицита или в профилактических дозах для его предупреждения (УУР А) [31]. Доказана важная роль витамина D в абсорбции кальция и усилении минерализации костной ткани. Более того, по данным ряда исследований отмечается, что адекватная концентрация витамина D способствует нормализации ключевых процессов клеточного цикла и пролиферативного потенциала клеток, а также удлинению теломерных участков, подавляя ключевой механизм клеточного старения. Также имеются данные о том, что витамин D способствует предикции СД 2, снижая уровень гликированного гемоглобина и инсулинорезистентность [25].
Рекомендуется использование активных метаболитов витамина D (альфакальцидол, кальцитриол) у пациенток с высоким риском падений в качестве монотерапии или в качестве дополнения к антирезорбтивной терапии для повышения МПКТ (УУР А) [31].
Рекомендуется достаточное потребление кальция с продуктами питания или использование препаратов кальция в качестве дополнения к пищевому рациону (УУР А) [31].
Рекомендуется использование препаратов витамина E в качестве меры профилактики и замедления клеточного старения (УУР D) [25]. Имеются данные, свидетельствующие о высокой антиоксидантной активности токоферола. Витамин Е успешно подавляет ключевые процессы старения эндотелиальных и фибробластных клеток за счет блокирования ингибиторов клеточного цикла. В свою очередь, дефицит витамина Е приводил к укорочению теломерных участков лейкоцитов, что свидетельствует о его таргетном влиянии на основные механизмы клеточного старения [25].
Рекомендуется назначение препаратов железа лицам из групп риска развития латентного железодефицита и железодефицитной анемии, а также при верификации данных состояний (УУР С) [32]. Распространенность дефицита железа у лиц пожилого возраста остается на высоком уровне. В основе развития железодефицитной анемии у людей пожилого возраста лежат снижение его доступности вследствие хелатирования и нарушение всасывания. Кроме того, было выявлено, что железо активно накапливается в стареющих клетках и повышает порог их выживаемости.
Рекомендуется использование метформина в качестве приоритетного препарата при СД 2 с целью снижения уровня глюкозы (уровень доказательности А). Имеется ряд научных исследований, доказывающих предиктивное влияние метформина на развитие ССЗ. Кроме того, важно отметить, что метформин имеет грандиозный потенциал в отношении блокирования ключевых механизмов клеточного старения: ингибирование процессов онкогенеза, реализация антиоксидантного эффекта, активация гена SIRT1, активация бактерий, продуцирующих короткоцепочечные жирные кислоты, регулирующие сигнальные пути mTOR, что приводит к замедлению процессов клеточного старения, а также позитивное влияние на массу тела пациенток [40–42].
Рекомендуется использование добавок селена для стимуляции антиоксидантных, иммуномодулирующих и противовоспалительных процессов (УУР D) [36].
Рекомендуется использование профилактических доз витаминов группы B (B1, B2, B3, B9, B12) с целью профилактики гипергомоцистеинемии и, как следствие, предикции развития когнитивного дефицита у пациенток пожилого возраста согласно результатам ряда рандомизированных клинических исследований (УУР D). Отмечается, что использование комплекса вышеуказанных витаминов приводит к замедлению прогрессирования возраст-ассоциированного когнитивного дефицита [45, 46].
Рекомендуется использование мелатонина в качестве антиоксиданта с целью замедления процессов клеточного старения. Отмечается, что мелатонин обладает мощным антиоксидантным действием и является одним из ключевых митохондриальных протекторов за счет активации ряда ферментов: супероксиддисмутазы, каталазы, глутатионпероксидазы и глутатионредуктазы. Не менее важным является и противовоспалительный эффект мелатонина, обусловленный его отрицательным влиянием на экспрессию провоспалительных цитокинов, ряда ферментов и молекул клеточной адгезии (УУР D) [35]. Все вышеописанные эффекты мелатонина характеризуют его выраженный предиктивный потенциал в отношении развития нейродегенеративных заболеваний, а именно болезни Альцгеймера и болезни Паркинсона [43].
Рекомендуется использование ресвератрола в качестве ингибитора гликирования для профилактики инсулинорезистентности. Кроме того, имеются данные лабораторных исследований, свидетельствующих о позитивном влиянии ресвератрола на поддержание МПКТ (УУР D) [33, 34].
Рекомендуется использование альфа-кетоглутарата в качестве антиоксиданта с целью замедления процессов клеточного старения (УУР D). Имеются данные, свидетельствующие о выраженном антиоксидантном эффекте альфа-кетоглутарата за счет повышения утилизации активных форм кислорода. Кроме того, отмечается, что альфа-кетоглутарата может обладать потенциальным эффектом снижения калорийности рациона, также способствующим реализации позитивных anti-age-эффектов [44].
Рекомендуется использование добавок аминокислот с разветвленной цепью с целью реализации антиоксидантного эффекта и митохондриальной протекции (УУР D). Отмечается, что использование данных добавок приводит к улучшению общего состояния здоровья, а также замедлению потери костной и мышечной массы и профилактике саркопении [47].
Рекомендуется использование эпигаллокатехин-3-галлата для реализации антиоксидантного и противовоспалительного эффекта с целью предикции нейродегенеративных заболеваний (УУР D). Также отмечается, что эпигаллокатехин-3-галлат ингибирует агрегацию амилоида и усиливает его деградацию, что играет важную роль в профилактике развития болезни Альцгеймера [48].
Важно отметить, что все патогенетические механизмы старения организма, начиная с угасания циклических изменений в женском организме и заканчивая ожирением, крайне тесно взаимосвязаны. Этот весьма сложный молекулярно-биологический механизм напоминает паутину, в которой каждая новая нить переплетается с предыдущими. И в этой связи мы констатируем, что невозможно вычленить главный триггер старения, ведь старение – то комплексный механизм. Данный постулат напрямую отражается и в клиническом менеджменте пациенток, лишь готовящихся вступить в период благородного возраста. Диагностический чекап в рамках концепции антиэйджинга должен охватывать большинство систем организма женщины с целью прогнозирования и предикции возраст-ассоциированных заболеваний и скрытых микронутриентных дефицитов.
Аналогичный подход был отражен и в предложенной нами anti-age-концепции ведения пациенток. Мероприятия, направленные на купирование возрастных изменений, крайне обширны и также направлены на терапевтический охват наиболее важных потенциальных последствий клеточного старения. Одним из наиважнейших мероприятий в рамках концепции антиэйджинга является модификация образа жизни, в рамках которой необходимы коррекция и поддержание нормальной массы тела, а также адекватная и, самое главное, ежедневная физическая активность. Ведь важно помнить, что каждый дополнительно сделанный шаг – это путь к успешному взрослению и активному долголетию! Кроме того, уже сейчас имеется внушительный пул данных, свидетельствующих о высоких перспективах использования генной терапии для купирования возраст-ассоциированных изменений.
Таким образом, важно отметить, что anti-age-медицина – это не просто очередной раздел классической медицинской науки, это всеобъемлющий массив мероприятий, требующий высокой степени отдачи не только клиницистов совершенно различных профилей, но и прежде всего самой пациентки. Мы полагаем, что на настоящий момент в XXI в. не должно существовать такого понятия, как старость. Есть лишь один путь к счастью и высокому уровню качества жизни – успешное взросление. Безусловно, в рамках anti-age-медицины нам еще предстоит очень многое узнать. Однако уже сейчас мы способны сделать определенные конкретные шаги в менеджменте пациенток, заботящихся о качестве своей жизни.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Сonflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах / Information about the authors
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-1767-5536
Mekan R. Orazov – D. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru;
ORCID: 0000-0002-1767-5536
Долгов Евгений Денисович – клинический ординатор каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: 1586dolgde@gmail.com; ORCID: 0000-0001-6709-5209
Evgenii D. Dolgov – clinical resident, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: 1586dolgde@gmail.com;
ORCID: 0000-0001-6709-5209.
Поступила в редакцию / Received: 22.02.2023
Поступила после рецензирования / Revised: 13.03.2023
Принята к публикации / Accepted: 30.03.2023
Клинический разбор в общей медицине №3 2023
Неизбежное старение или успешное взросление? Anti-ageing-медицина: конкретно об абстрактном
Номера страниц в выпуске:67-76
Аннотация
Одним из наиболее актуальных вопросов современной демографии является стремительное повышение продолжительности жизни населения, именуемое «серебряным цунами» и диктующее необходимость развития такого совершенно нового раздела медицинской науки, как anti-age-медицина. Принято считать, что старение организма неизбежно ассоциировано со снижением качества жизни, однако сейчас данный постулат опровергается, и в этой связи наиболее актуальным для XXI в. термином является «успешное взросление». Существует большое количество научных исследований, освещающих те или иные механизмы клеточного старения, которые должны являться терапевтическими мишенями с целью предикции возраст-ассоциированных заболеваний. И в этой связи необходимо обобщить имеющиеся научные данные и структурировать современные подходы, способствующие «успешному взрослению» в рамках инновационной anti-ageing-концепции.
Ключевые слова: anti-age, антиэйджинг, клеточное старение, успешное взросление.
Для цитирования: Оразов М.Р., Долгов Е.Д. Неизбежное старение или успешное взросление? Anti-ageing-медицина: конкретно об абстрактном. Клинический разбор в общей медицине. 2023; 4 (3): 67–76. DOI: 10.47407/kr2023.4.3.00226
Одним из наиболее актуальных вопросов современной демографии является стремительное повышение продолжительности жизни населения, именуемое «серебряным цунами» и диктующее необходимость развития такого совершенно нового раздела медицинской науки, как anti-age-медицина. Принято считать, что старение организма неизбежно ассоциировано со снижением качества жизни, однако сейчас данный постулат опровергается, и в этой связи наиболее актуальным для XXI в. термином является «успешное взросление». Существует большое количество научных исследований, освещающих те или иные механизмы клеточного старения, которые должны являться терапевтическими мишенями с целью предикции возраст-ассоциированных заболеваний. И в этой связи необходимо обобщить имеющиеся научные данные и структурировать современные подходы, способствующие «успешному взрослению» в рамках инновационной anti-ageing-концепции.
Ключевые слова: anti-age, антиэйджинг, клеточное старение, успешное взросление.
Для цитирования: Оразов М.Р., Долгов Е.Д. Неизбежное старение или успешное взросление? Anti-ageing-медицина: конкретно об абстрактном. Клинический разбор в общей медицине. 2023; 4 (3): 67–76. DOI: 10.47407/kr2023.4.3.00226
Inevitable aging or successful growing-up? Anti-aging medicine: the abstract in concrete terms
Mekan R. Orazov, Evgenii D. DolgovPatrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia
omekan@mail.ru
Abstract
The drastic increase in life expectancy of the population, referred to as “silver tsunami” and demanding the development of such an entirely new branch of medical science as “anti-age medicine”, is one of the most pressing issues of modern demography. It is believed that aging of the body is inevitably associated with reduced quality of life, however, this postulate is currently urgently refuted, that is why the term “successful growing-up” is most relevant for the 21st century. There is a number of scientific studies focused on certain mechanisms underlying cellular senescence, which should be the therapeutic targets for prediction of age-related disorders. Thus, it is necessary to summarize the scientific evidence available and structure the modern approaches that contribute to “successful growing-up” under the innovation anti-aging concept.
Key words: anti-age, anti-aging, cellular senescence, successful growing-up.
For citation: Orazov M.R., Dolgov E.D. Inevitable aging or successful growing-up? Anti-aging medicine: the abstract in concrete terms. Clinical review for general practice. 2023; 4 (3): 67–76. DOI: 10.47407/kr2023.4.3.00226
Первое цунами в демографии: прогнозируем «вызовы природы»
С самых древних времен алхимики пытались найти материю, обладающую невероятной силой и способную не только обращать любой металл в золото, но и получить столь желанный «эликсир вечной жизни». Долгое время знаменитый алхимик Николя Фламель проводил исследования и пытался добыть заветный философский камень. И существует множество легенд, говорящих о том, что у него это получилось, и о том, что он жив до сих пор. Однако спорная судьба одного человека в масштабе мира не столь показательна, а истории о поиске философского камня попадают лишь в ранг «неизданных легенд». Сейчас же современное человечество переживает совершенно уникальное время, когда стандартный поход в «магазин напротив» стал архаизмом, а темпы развития искусственного интеллекта опережают все мыслимые пределы.Разработка революционных фармакологических препаратов, инновационного оборудования, внедрение в практику генетического обследования и других медицинских технологий поспособствовали существенному увеличению общемирового показателя продолжительности жизни. В 2012 г. средняя продолжительность жизни в Российской Федерации составляла 70,2 года, в 2017 г. показатель преодолел отметку в 72,7 года, а уже к 2024 г. прогнозируется повышение продолжительности жизни до 78 лет [1]. Говоря о демографии, мы подразумеваем две противоборствующие силы – прирост населения и депопуляцию. И в последнее время мы наблюдаем неоспоримую тенденцию увеличения численности населения: в 2013 г. население Земли составило 7,3 млрд человек, в 2023 г. показатель уже превысил
8 млрд, а согласно прогнозам к 2030 и 2050 г. показатель численности населения достигнет 8,5 и 9,6 млрд человек соответственно [2, 3]. Однако столь существенный демографический прирост обусловлен отнюдь не значительным повышением рождаемости, а повышением продолжительности жизни. Кроме того, на сегодняшний день людей старше 65 лет стало больше, чем детей младше 5 лет [3]. И это, безусловно, является самым настоящим демографическим парадоксом, которого ранее мир еще не видел. Важно отметить, что фокус эволюции медицинской науки должен динамически изменяться исходя из сегодняшних потребностей. Согласно весьма актуальной градации Всемирной организации здравоохранения, пожилой возраст начинается в 60 лет и заканчивается в 74 года, а старческий соответствует интервалу от 75 до 90 лет, все остальные люди, прожившие 90 и более лет, приписаны в ранг долгожителей. Однако становится очевидным тот факт, что не за горами то время, когда людей в возрасте старше 90 лет будут относить как минимум к группе старческого возраста. Более того, прогнозируется, что к 2030 г. каждому шестому жителю планеты будет более 60 лет, а к 2050 г. – и вовсе каждому пятому [4]! Данную ситуацию современные демографы как раз и именуют «серебряным цунами XXI века». Данный феномен привел нас к тому, что сейчас доля пожилого возраста в структуре человеческой жизни составит ни много ни мало 20–30%, что весьма остро ставит перед нами вопрос о необходимости введения такого понятия, как «успешное взросление». И если сейчас в наших руках повышение продолжительности жизни, то не менее важным остается вопрос качества той самой продленной жизни, которое, к сожалению, нередко страдает.
Долгое время философы всего мира размышляют о смысле жизни. Данный вопрос, стоящий на «повестке дня» далеко не одно столетие, до сих пор находится в «подвешенном» состоянии. Однако расширение и модернизация взглядов современного населения помогли человечеству отойти от унифицированного подхода к решению самых незаурядных вопросов. И сейчас мы хорошо понимаем, что смысл жизни, как и понятие счастья, у каждого свои. Однако любые ценности и потребности каждого конкретного человека успешно укладываются в общепринятое понятие качества жизни, о котором сейчас не говорит только ленивый.
И в данном контексте мы акцентируем внимание на том, что реализация «высшего смысла» в целом и счастья в частности невозможна без достижения должного уровня качества жизни. А человек пожилого и старческого возраста также имеет много целей и планов, для реализации которых ему необходима эмоциональная и физическая гармония.
Принято считать, что старение организма неизбежно приводит к развитию возраст-ассоциированных заболеваний и снижению качества жизни. Однако, как мы отметили выше, человек «60+» стремится к активной деятельности, не желая оставаться «за кулисами жизни». Исходя из этого медицина сделала «идеологический кульбит» и стала базироваться на принципах четырех «П»: предикция, превенция, партисипативность и персонализация. И в этой связи важно отметить, что современная медицина располагает ресурсом максимального сглаживания перехода из периода среднего возраста в пожилой. Предупреждение развития мультиорганных заболеваний, нейродегенерации, поддержание физической активности и восполнение нутриентных дефицитов – все это входит в основу современной концепции «успешного взросления» или так называемого «антиэйджинга», которая позволит женщине успешно «повзрослеть» и вовсе не ощущать на себе груз прожитых лет. Целью данной статьи была демонстрация современных подходов anti-age-медицины и возможностей предикции ряда возраст-ассоциированных заболеваний.
Ключевые механизмы клеточного старения
В XXI в. количество научных исследований, раскрывающих молекулярные основы старения, растет в геометрической прогрессии. Наиболее актуальными концепциями «патогенеза старения» являются теории стареющих теломер, митохондриальной дисфункции, генетических детерминантов, а также онкогенной активации и дисбактериоза.Наиболее распространенной концепцией «молекулярного старения» является теория укорочения теломер. Хорошо известно, что пролиферативный потенциал каждой соматической клетки определяется так называемым пределом Хейфлика, который отражает максимальное число возможных делений до того момента, пока клеточный цикл не остановится. Как правило, предел Хейфлика составляет 48–50 клеточных делений. Остановка клеточного цикла, в свою очередь, обуславливается двумя процессами: критическим укорочением теломерных участков, а также активацией экспрессии онкосупрессорных локусов, блокирующих дальнейшее клеточное деление. В ходе каждой репликации ДНК теряется от 50 до 200 пар теломерных оснований, что обусловлено невозможностью ДНК-полимеразы «обработать» весь хроматин. После достижения «точки невозврата» высвобождается так называемый секреторный комплекс, ассоциированный с клеточным старением (SASP), включающий провоспалительные цитокины, хемокины, факторы роста, протеазы и ангиогенные факторы, сигнализирующие клетке о критическом повреждении ДНК, что индуцирует экспрессию ингибиторов клеточного цикла p16INK4A и p21CIP1 и, как следствие, блокирование активности циклинзависимых протеинкиназ [5, 6]. Более того, все факторы, входящие в состав SASP-комплекса, обладают ауто- и паракринной активностью, активируя аналогичные процессы старения во всех рядом расположенных клетках. Аналогичный внутриклеточный каскад активируется и в случае появления экзо- и эндогенных триггеров, опосредованно приводящих через активацию p16INK4A/p21CIP1 к остановке клеточного цикла [7].
Не менее важным механизмом клеточного старения является оксидативный стресс, который возникает вследствие снижения утилизации организмом активных форм кислорода (пероксид водорода, супероксид-радикал и гидроксид-радикал). Повышение концентрации данных метаболитов приводит к повреждению ДНК и реализации типового механизма сигнализации, о котором мы упомянули выше [7].
Особое внимание в последние годы уделяется дисбалансу кишечного микробиома, реализующего воспалительные изменения стенки кишки и повышение ее проницаемости. Безусловно, прямые доказательства влияния дисбактериоза на развитие возраст-ассоциированных заболеваний отсутствуют. Однако ряд научных исследований выявили изменения кишечного микробиома при сахарном диабете 2-го типа (СД 2), ишемической болезни сердца, сердечной недостаточности, а также ряде онкологических заболеваний. Доказано, что кишечный микробиом регулирует целый ряд необходимых физиологических процессов: ферментирование и модификацию питательных веществ, синтез витаминов, стимуляцию антиоксидантных механизмов, а также стимуляцию иммунной системы и предупреждение процессов клеточного старения [26–30]. Хорошо известно, что с возрастом происходят существенные изменения как количественного, так и качественного состава кишечной микробиоты, проявляющиеся истощением пула лакто- и бифидобактерий. Кроме того, важно отметить, что исследователями был выявлен один из потенциальных механизмов реализации механизмов старения, ассоциированных с изменениями микробиома. Так, метилглиоксаль, являясь одним из метаболитов бактериального происхождения, способствует активации старения кожных фибробластов и реализации ассоциированных с онкогенными агентами процессов клеточного старения [6, 8]. Исходя из этого становится совершенно очевидным факт ассоциации дисбактериоза с рядом нозологий и ключевыми механизмами старения, что также должно являться потенциальной терапевтической мишенью у пациенток пожилого возраста.
Таким образом, необходимо отметить, что все описанные процессы приводят к снижению регенераторного и пролиферативного потенциала клеток, что и лежит в основе клеточного старения. Данные механизмы и будут являться основными точками приложения для современной концепции anti-age-медицины, которая позволит не только замедлить процессы старения, но и обратить их вспять.
Ожирение и клеточное старение: ставим знак равенства
Однако одной из самых дискуссионных тем последнего десятилетия остается ожирение. Согласно данным Всемирной организации здравоохранения, по состоянию на 2016 г. этим поистине грозным заболеванием страдали около 13% взрослого населения, а 39% людей старше 18 лет имели избыточный вес [9]. И эпидемиологическая ситуация со временем отнюдь не улучшается. Одной из главных проблем ожирения на современном этапе является его достоверная ассоциация с реализацией злокачественных гиперпролиферативных заболеваний как органов репродуктивной системы (аденокарцинома эндометрия, рак молочной железы в постменопаузе, рак яичников), так и других (рак желудка, колоректальный рак, гепатоцеллюлярная карцинома, менингиома, множественная миелома, рак желчного пузыря и щитовидной железы) [49]. Важно отметить, что коррекция массы тела играет важную роль в антиэйджинг-концепции, достоверно снижая вероятность развития онкологических заболеваний. Однако в рамках данной тематики наиболее парадоксальным является то, что ожирение независимо от возраста индуцирует ключевые механизмы старения. Так, было выявлено, что ожирение и связанные с ним гипергликемия и состояние так называемого метаболического стресса приводят к старению различных популяций клеток. Однако наиболее важным в данном контексте является негативное влияние ожирения на длину теломерных участков.Исследователи обнаружили, что в кардиомиоцитах пожилых людей как с ожирением, так и без него длина теломерных повторов оказалась на 30% ниже стандартного показателя, при этом аналогичная ситуация отмечалась и у молодых людей, однако степень редукции теломер была несколько ниже. Оказалось, что укорочение теломер у лиц с верифицированным ожирением ассоциировано с повышением активности фактора теломерного повтора-1 (TRF-1), ингибирующего активность теломеразы, ответственной за удлинение теломерных участков. Кроме того, провоспалительные изменения, индуцированные ожирением, способствуют активации пролиферации лейкоцитарного звена в периферических тканях, также способствующего опосредованному сокращению теломерных участков [6]. Также необходимо отметить, что кроме влияния на TRF-1 ожирение способствует накоплению SASP-комплексов за счет повышенной продукции адипоцитами провоспалительных цитокинов и адипокинов, опосредованно накладывающих арест на клеточный цикл через стандартный и описанный нами выше механизм. Также была выявлена прямая взаимосвязь между ожирением и развитием СД 2. Так, описанные комплексы SASP кроме сигнализации о повреждении ДНК приводят к снижению антиоксидантной активности и митохондриальной дисфункции, что неизбежно затрагивает гепатоциты и β-клетки поджелудочной железы. Вследствие развития клеточной метаболической дисфункции нарушаются процессы окисления жирных кислот и снижается эндокринная функция поджелудочной железы, что способствует развитию инсулинорезистентности [10].
Резюмируя вышесказанное, необходимо отметить исключительно важную роль ожирения в реализации ключевых процессов клеточного старения. А исходя из имеющихся научных данных, мы формируем главный тезис: «Неважно, сколько пациентке лет, важно то, есть ли у нее ожирение». Мы акцентируем внимание на том, что основным звеном клинического менеджмента таких пациенток является не их стратификация исходя из возрастного показателя, а верификация у нее избыточной массы тела, потенцирующей ключевые механизмы клеточного старения, что демонстрирует актуальность anti-ageing-концепции не только у женщин пожилого/старческого возраста, но и у пациенток средней возрастной когорты. Именно на этом принципе должен основываться клинический менеджмент в рамках anti-ageing-концепции, ведь ожирение – это уникальная нозология, создающая огромную пропасть между фактическим и биологическим возрастом пациентки.
Менопауза – основной индуктор «женского взросления»
Точкой «финиша» менструальной функции как основного циклического процесса, лежащего в основе регуляции функционирования репродуктивной системы женщины, является менопауза, средний возраст наступления которой составляет 51 год. Хорошо известно, что одними из главных гормонов женского организма являются эстрогены, рецепторы к которым лоцируются в большинстве органов и тканей: мышцы тазового дна, связочный аппарат органов малого таза, уретра, влагалище, вульва, молочная железа, нервная ткань, а также сердце и сосуды [11, 12]. Поддержание оптимальной концентрации эстрогенов в организме женщины обеспечивается их продукцией растущим фолликулом в течение менструального цикла. Однако с течением времени овариальный резерв неизбежно истощается, что приводит к закономерному снижению уровня эстрогенов, являющихся универсальным фактором пролиферации в организме женщины. В этой связи включается компенсаторная активация внегонадного синтеза эстрогенов жировой тканью, что приводит к ее гиперплазии и ожирению, опосредованно способствующему развитию клеточного старения. Кроме того, снижение концентрации эстрогенов приводит к снижению пролиферативного и регенераторного потенциала клеток, лежащих в основе менопаузальных расстройств и, как следствие, системного старения женского организма.Важно отметить, что основные расстройства постменопаузы определяются именно преимущественной локализацией рецепторов к эстрогенам. Наиболее ранним расстройством постменопаузы является климактерический синдром, включающий приливы жара, нейровегетативную симптоматику, а также психоэмоциональные девиации, которые способствуют существенному снижению качества жизни пациентки. Следующим «испытанием» в этот период является генитоуринарный менопаузальный синдром (ГУМС), характеризующийся появлением урогенитальной атрофии и дебютированием ряда характерных симптомов: зуд, сухость, жжение, диспареуния, дизурия и недержание мочи [13]. Кроме того, снижение толщины эпителиального компартмента вульвовагинальной зоны приводит к снижению pH и содержания лактобактерий, а также активации размножения условно-патогенной флоры, что приводит к развитию рецидивирующих воспалительных заболеваний [14, 15]. Однако наиболее грозными и отдаленными расстройствами постменопаузы являются снижение минеральной плотности костной ткани – МПКТ (остеоартриты, остеопороз), неврологические нарушения (болезнь Альцгеймера, когнитивный дефицит), сердечно-сосудистые заболевания – ССЗ (атеросклероз и ассоциированные с ним состояния), а также менопаузальный метаболический синдром [16]. Важно отметить, что кроме эндогенных проявлений эстрогенодефицита отмечаются и внешние признаки «репродуктивного старения», такие как дряблость кожи, морщины, а также изменения качества и структуры волос [17].
Таким образом, важно отметить, что менопауза является поистине важным событием в жизни женщины, к которому необходимо быть готовой. «Распознать и устранить» – вот главная задача клинициста в ходе менеджмента пациенток с климактерическим синдромом и другими расстройствами постменопаузы. Менопауза является достоверным предвестником общего старения организма, что необходимо учитывать в рамках концепции антиэйджинга.
Диагностика старения: очередная эфемерность или практическая необходимость?
Современная концепция anti-age-медицины подразумевает замедление прогрессирования или остановку ключевых процессов клеточного старения. Однако в данном тексте остро встает вопрос: а когда же нужно начать антиэйджинг-терапию? На данный момент не существует ни одного международного или отечественного гайдлайна, регламентирующего мероприятия в рамках anti-ageing-концепции. В этой связи необходимо отметить уже имеющиеся диагностические инструменты, которые помогут выявить признаки возраст-ассоциированной системной дегенерации.Как мы выше отметили, в основе старения женского организма лежат изменения, связанные с менопаузой. С целью прогнозирования менопаузальных расстройств необходимо использование модифицированной шкалы STRAW+10, согласно которой клиницист может провести тщательную стратификацию пациенток и отнести каждую из них к определенной стадии: стадия -1 соответствует поздней переходной фазе, стадия +1 – ранней постменопаузе, подразделяющейся на три этапа (+1a, +1b, +1c), а стадия +2 соответствует поздней постменопаузе. Основными инструментами стратификации пациенток по данной шкале являются определение характера менструального цикла, а также маркеров овариального резерва (концентрации фолликулостимулирующего, антимюллерова гормонов, ингибина B, числа антральных фолликулов) [18]. Определение «репродуктивной стадии» согласно шкале STRAW+10 позволит спрогнозировать развитие возможных менопаузальных расстройств и вовремя начать мероприятия в рамках anti-ageing-концепции.
Также необходимо отметить инструменты объективизации расстройств постменопаузы, к которым относятся специальные оценочные шкалы. С целью верификации и объективизации климактерического синдрома возможно использование шкалы Грина, включающей ряд вазомоторных, нейровегетативных и психоэмоциональных симптомов. Согласно данной шкале возможна стратификация пациенток в зависимости от тяжести климактерического синдрома: результат в 1–11 баллов соответствует климактерическому синдрому легкой степени тяжести, 12–19 баллов – средней степени, а 20 и более баллов – тяжелой степени [19].
Наиболее актуальными методами объективизации ГУМС являются измерение индекса вагинального здоровья (по G. Bachmann) и использование шкалы D. Barlow для определения тяжести симптоматики ГУМС [20].
Не менее важным является верификация снижения МПКТ. Так, «золотым стандартом» определения МПКТ, отраженным в отечественных рекомендациях по ведению пациенток в постменопаузе, является двуволновая рентгеновская абсорбциометрия, по результатам которой определяется так называемый Т-критерий. О наличии остеопороза свидетельствует величина Т-критерия от -2,5 и менее [21].
Также необходимо отметить важность оценки состояния сердечно-сосудистой системы, поскольку именно острые сердечно-сосудистые события приводят к выраженной инвалидизации пациенток, а нередко бывают фатальны. Наиболее удобным и простым методом оценки состояния сердечно-сосудистой системы является измерение артериального давления на обеих руках с целью верификации атеросклеротических поражений сосудов. С этой же целью возможно измерение лодыжечно-плечевого индекса (норма >0,9). Не менее важным является определение нарушений в показателях липидограммы: повышение общего холестерина, триглицеридов, липопротеинов низкой плотности и снижение содержания липопротеинов высокой плотности [22] – и определение антропометрических показателей, таких как масса тела, индекс массы тела (норма – до 25 кг/м2) и окружность талии (норма – до 80 см). Одним из наиболее современных методов диагностики ожирения является биоимпедансометрия – метод определения процентного содержания жира в организме путем прохождения электрической волны через ткани организма [23]. Данный метод является крайне актуальным, поскольку на данный момент у многих пациенток отмечается так называемое «скрытое» ожирение, когда отсутствуют внешние признаки ожирения и при этом существенно повышается объем перивисцеральной жировой ткани. Исходя из этого необходимо отметить, что своевременная верификация и лечение ожирения позволят не только профилактировать заболевания сердечно-сосудистой системы, но и замедлить процессы клеточного старения.
Дополнительными методами обследования в рамках anti-age-концепции являются осмотр и пальпация молочных желез, а также проведение скрининговой маммографии 1 раз в 2 года после 40 лет [24]. Верификация заболеваний молочных желез является крайне актуальной в рамках концепции антиэйджинга, поскольку нередко они свидетельствуют о возрастной перестройке гормонального фона пациенток.
Кроме того, в рамках anti-age-концепции необходимо определение микронутриентного профиля у пациентки с определением концентраций витаминов и минералов, наиболее важными из которых являются витамин D и железо, о которых будет упомянуто ниже [25].
Однако кроме выявления предпосылок к развитию возраст-ассоциированных заболеваний необходимо сделать особый акцент на оценку показателей качества жизни пациентки и перейти к не менее главному этапу anti-age-скрининга. В данном контексте возможно проведение так называемой комплексной гериатрической оценки (КГО) с использованием ряда объективизирующих оценочных шкал, с помощью которой клиницист описывает текущее состояние пациентки путем оценивания 4 основных доменов: физическое здоровье, функциональная активность, психоэмоциональная сфера и социальный статус (табл. 1). На основании КГО клиницист определяет ключевые проблемы, снижающие функциональный статус и качество жизни пациенток, а в дальнейшем разрабатывает индивидуальный план мероприятий для их коррекции [50].

Таким образом, вопрос комплексного обследования пациентки в рамках программы антиэйджинга является чрезвычайно важным. Клеточное старение неизбежно приводит к снижению функции различных органов и систем, что диктует необходимость междисциплинарного подхода не только к обследованию в рамках anti-age-концепции, но и для осуществления антиэйджинг-мероприятий. В этой связи необходимо отметить, что сама концепция anti-age-медицины подразумевает формирование «anti-age-команды», состоящей из акушера-гинеколога, эндокринолога, кардиолога, геронтолога и других специалистов, для осуществления эффективного клинического менеджмента пациенток.
Лечить нельзя профилактировать: ставим запятую правильно
Исходя из описанных механизмов старения женского организма, мы представляем свою anti-age-концепцию, направленную на предикцию развития возраст-ассоциированных заболеваний и на повышение качества жизни пациенток «старшего переходного возраста», основанную на имеющихся отечественных и международных гайдлайнах и результатах ряда научных исследований.Рекомендуется назначение менопаузальной гормональной терапии (МГТ) женщинам в пери- и постменопаузе для лечения вазомоторных симптомов умеренной и тяжелой степени, симптомов ГУМС, сексуальной дисфункции, а также с целью профилактики постменопаузального остеопороза. МГТ является эффективным методом предикции потери костной массы, при этом наиболее выраженный эффект отмечается при раннем начале терапии (уровень убедительности рекомендаций – УУР А) [21].
Рекомендуется назначение локальной гормональной терапии на основе препаратов эстриола у пациенток с симптомами ГУМС и сексуальной дисфункции (УУР С) [21].
Рекомендуется назначение альтернативных методов терапии у пациенток при наличии противопоказаний или нежелания использовать МГТ. Одними из главных альтернативных методов терапии и предикции климактерического синдрома являются: коррекция образа жизни и снижение массы тела, использование когнитивно-поведенческой терапии, а также иглорефлексотерапия и гипноз (УУР А) [21].
Рекомендуется использование лубрикантов в качестве альтернативы локальной гормональной терапии у пациенток с симптомами ГУМС (УУР B) [21].
Рекомендуется поддерживать адекватный уровень регулярной физической активности с целью профилактики когнитивных расстройств [39].
Рекомендуется выполнение физических упражнений с осевыми нагрузками (ходьба, бег, танцы, подвижные игры) с целью поддержания МПКТ у здоровых пожилых людей (УУР С) [31].
Рекомендуется проведение умеренных силовых тренировок (пилатес, тай-чи, плавание и др.) для укрепления мышечного каркаса и улучшения координации у пожилых людей с переломами в анамнезе или с диагностированным остеопорозом (УУР B) [31].
Рекомендуется поддержание адекватного уровня психической и социальной активности с целью профилактики развития когнитивных расстройств [39]. Важно отметить, что социализация необходима для «успешного взросления» пациенток, поскольку она не позволяет им закрыться в себе. Актуальными являются любые виды социальной и умственной активности: разгадывание кроссвордов, лингвистические групповые занятия, чтение книг, йога, пилатес и др.
Рекомендуется соблюдение принципов здорового питания для профилактики когнитивных расстройств (УУР С) [39].
Рекомендуется соблюдение принципов правильного питания. Включение в рацион жирной и в высокой степени переработанной пищи способствует избыточному образованию продуктов гликирования и перекисного окисления липидов, повышающих риски возникновения СД и ССЗ. Диета с низким содержанием данных продуктов приводит к снижению инсулинорезистентности у людей с СД 2. В этой связи предпочтительно включение в рацион продуктов с низким содержанием жиров, сложных углеводов (бобовые, овощи, фрукты, цельные злаки), а также молочных продуктов с низким содержанием жира (УУР D) [33].
Рекомендуется употребление не менее 0,8 г белка на килограмм массы тела всем людям пожилого возраста (Европейское управление по безопасности пищевых продуктов); УУР С. Наиболее выраженное истощение физических и когнитивных ресурсов отмечается после 50 лет, однако адекватное потребление белка поможет замедлить процессы клеточного старения, прогрессирование потери костной и мышечной массы, а также профилактировать развитие когнитивного дефицита [38].
Рекомендуется прекращение курения для снижения риска развития когнитивных расстройств (УУР B) [39].
Рекомендуется сокращение употребления алкоголя для снижения риска развития когнитивных расстройств (УУР B) [39].
В качестве профилактики развития когнитивного дефицита и снижения риска развития деменции рекомендуется мультимодальный подход с коррекцией имеющихся факторов риска (УУР B). Основными факторами риска когнитивных расстройств являются: артериальная гипертензия, снижение слуха и ожирение в среднем возрасте; курение, депрессия, гиподинамия, социальная изоляция и СД у лиц старше 65 лет. Успешная коррекция ключевых факторов риска способна снизить вероятность развития деменции на 35% [39].
Рекомендуется использование витамина D (колекальциферола) в терапевтических дозах с целью коррекции дефицита или в профилактических дозах для его предупреждения (УУР А) [31]. Доказана важная роль витамина D в абсорбции кальция и усилении минерализации костной ткани. Более того, по данным ряда исследований отмечается, что адекватная концентрация витамина D способствует нормализации ключевых процессов клеточного цикла и пролиферативного потенциала клеток, а также удлинению теломерных участков, подавляя ключевой механизм клеточного старения. Также имеются данные о том, что витамин D способствует предикции СД 2, снижая уровень гликированного гемоглобина и инсулинорезистентность [25].
Рекомендуется использование активных метаболитов витамина D (альфакальцидол, кальцитриол) у пациенток с высоким риском падений в качестве монотерапии или в качестве дополнения к антирезорбтивной терапии для повышения МПКТ (УУР А) [31].
Рекомендуется достаточное потребление кальция с продуктами питания или использование препаратов кальция в качестве дополнения к пищевому рациону (УУР А) [31].
Рекомендуется использование препаратов витамина E в качестве меры профилактики и замедления клеточного старения (УУР D) [25]. Имеются данные, свидетельствующие о высокой антиоксидантной активности токоферола. Витамин Е успешно подавляет ключевые процессы старения эндотелиальных и фибробластных клеток за счет блокирования ингибиторов клеточного цикла. В свою очередь, дефицит витамина Е приводил к укорочению теломерных участков лейкоцитов, что свидетельствует о его таргетном влиянии на основные механизмы клеточного старения [25].
Рекомендуется назначение препаратов железа лицам из групп риска развития латентного железодефицита и железодефицитной анемии, а также при верификации данных состояний (УУР С) [32]. Распространенность дефицита железа у лиц пожилого возраста остается на высоком уровне. В основе развития железодефицитной анемии у людей пожилого возраста лежат снижение его доступности вследствие хелатирования и нарушение всасывания. Кроме того, было выявлено, что железо активно накапливается в стареющих клетках и повышает порог их выживаемости.
Рекомендуется использование метформина в качестве приоритетного препарата при СД 2 с целью снижения уровня глюкозы (уровень доказательности А). Имеется ряд научных исследований, доказывающих предиктивное влияние метформина на развитие ССЗ. Кроме того, важно отметить, что метформин имеет грандиозный потенциал в отношении блокирования ключевых механизмов клеточного старения: ингибирование процессов онкогенеза, реализация антиоксидантного эффекта, активация гена SIRT1, активация бактерий, продуцирующих короткоцепочечные жирные кислоты, регулирующие сигнальные пути mTOR, что приводит к замедлению процессов клеточного старения, а также позитивное влияние на массу тела пациенток [40–42].
Рекомендуется использование добавок селена для стимуляции антиоксидантных, иммуномодулирующих и противовоспалительных процессов (УУР D) [36].
Рекомендуется использование профилактических доз витаминов группы B (B1, B2, B3, B9, B12) с целью профилактики гипергомоцистеинемии и, как следствие, предикции развития когнитивного дефицита у пациенток пожилого возраста согласно результатам ряда рандомизированных клинических исследований (УУР D). Отмечается, что использование комплекса вышеуказанных витаминов приводит к замедлению прогрессирования возраст-ассоциированного когнитивного дефицита [45, 46].
Рекомендуется использование мелатонина в качестве антиоксиданта с целью замедления процессов клеточного старения. Отмечается, что мелатонин обладает мощным антиоксидантным действием и является одним из ключевых митохондриальных протекторов за счет активации ряда ферментов: супероксиддисмутазы, каталазы, глутатионпероксидазы и глутатионредуктазы. Не менее важным является и противовоспалительный эффект мелатонина, обусловленный его отрицательным влиянием на экспрессию провоспалительных цитокинов, ряда ферментов и молекул клеточной адгезии (УУР D) [35]. Все вышеописанные эффекты мелатонина характеризуют его выраженный предиктивный потенциал в отношении развития нейродегенеративных заболеваний, а именно болезни Альцгеймера и болезни Паркинсона [43].
Рекомендуется использование ресвератрола в качестве ингибитора гликирования для профилактики инсулинорезистентности. Кроме того, имеются данные лабораторных исследований, свидетельствующих о позитивном влиянии ресвератрола на поддержание МПКТ (УУР D) [33, 34].
Рекомендуется использование альфа-кетоглутарата в качестве антиоксиданта с целью замедления процессов клеточного старения (УУР D). Имеются данные, свидетельствующие о выраженном антиоксидантном эффекте альфа-кетоглутарата за счет повышения утилизации активных форм кислорода. Кроме того, отмечается, что альфа-кетоглутарата может обладать потенциальным эффектом снижения калорийности рациона, также способствующим реализации позитивных anti-age-эффектов [44].
Рекомендуется использование добавок аминокислот с разветвленной цепью с целью реализации антиоксидантного эффекта и митохондриальной протекции (УУР D). Отмечается, что использование данных добавок приводит к улучшению общего состояния здоровья, а также замедлению потери костной и мышечной массы и профилактике саркопении [47].
Рекомендуется использование эпигаллокатехин-3-галлата для реализации антиоксидантного и противовоспалительного эффекта с целью предикции нейродегенеративных заболеваний (УУР D). Также отмечается, что эпигаллокатехин-3-галлат ингибирует агрегацию амилоида и усиливает его деградацию, что играет важную роль в профилактике развития болезни Альцгеймера [48].
Будущее anti-age-медицины
Однако кроме достижений настоящего уже сформирован ряд дальнейших перспектив, определяющих вектор развития концепции anti-age-медицины. Наиболее инновационным и таргетным методом купирования возраст-ассоциированных изменений является генная терапия, которая с каждым годом набирает все большие обороты. Главной точкой приложения генетических методик являются теломерные участки хромосом, стимуляция роста которых обеспечивается таргетным переносом гена, кодирующего обратную транскриптазу теломеразы (hTERT), с помощью специфических плазмидных векторов. Было показано, что использование данной технологии позволяет увеличить длину теломерных участков и повысить число возможных клеточных делений как минимум на 20 митозов. Однако здесь возникают и определенные трудности: ингибирование репликативного старения клеток приводит к повышению рисков развития онкологических заболеваний. Еще одной целью anti-age генной терапии является ген Klotho, низкая экспрессия которого способствует прогрессированию возраст-ассоциированных нейродегенеративных заболеваний, таких как болезнь Альцгеймера. Стимуляция экспрессии данного гена с помощью воздействия на промоторную область данного гена известной системы CRISPR-dCas9, обеспечивающей таргетное воздействие на гены, может поспособствовать улучшению когнитивных функций и профилактике демиелинизирующих и нейродегенеративных заболеваний [37].Итоги настоящего. Перспективы будущего
Целью данной статьи являлось освещение весьма непростого вопроса, касающегося современных методик anti-age-медицины. Антиэйджинг – это то, о чем говорят все, однако на данный момент не существует общепринятого и универсального гайдлайна, который выступил бы успешным ассистентом для современного клинициста, занимающегося проблемами антиэйджинга.Важно отметить, что все патогенетические механизмы старения организма, начиная с угасания циклических изменений в женском организме и заканчивая ожирением, крайне тесно взаимосвязаны. Этот весьма сложный молекулярно-биологический механизм напоминает паутину, в которой каждая новая нить переплетается с предыдущими. И в этой связи мы констатируем, что невозможно вычленить главный триггер старения, ведь старение – то комплексный механизм. Данный постулат напрямую отражается и в клиническом менеджменте пациенток, лишь готовящихся вступить в период благородного возраста. Диагностический чекап в рамках концепции антиэйджинга должен охватывать большинство систем организма женщины с целью прогнозирования и предикции возраст-ассоциированных заболеваний и скрытых микронутриентных дефицитов.
Аналогичный подход был отражен и в предложенной нами anti-age-концепции ведения пациенток. Мероприятия, направленные на купирование возрастных изменений, крайне обширны и также направлены на терапевтический охват наиболее важных потенциальных последствий клеточного старения. Одним из наиважнейших мероприятий в рамках концепции антиэйджинга является модификация образа жизни, в рамках которой необходимы коррекция и поддержание нормальной массы тела, а также адекватная и, самое главное, ежедневная физическая активность. Ведь важно помнить, что каждый дополнительно сделанный шаг – это путь к успешному взрослению и активному долголетию! Кроме того, уже сейчас имеется внушительный пул данных, свидетельствующих о высоких перспективах использования генной терапии для купирования возраст-ассоциированных изменений.
Таким образом, важно отметить, что anti-age-медицина – это не просто очередной раздел классической медицинской науки, это всеобъемлющий массив мероприятий, требующий высокой степени отдачи не только клиницистов совершенно различных профилей, но и прежде всего самой пациентки. Мы полагаем, что на настоящий момент в XXI в. не должно существовать такого понятия, как старость. Есть лишь один путь к счастью и высокому уровню качества жизни – успешное взросление. Безусловно, в рамках anti-age-медицины нам еще предстоит очень многое узнать. Однако уже сейчас мы способны сделать определенные конкретные шаги в менеджменте пациенток, заботящихся о качестве своей жизни.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Сonflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах / Information about the authors
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-1767-5536
Mekan R. Orazov – D. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru;
ORCID: 0000-0002-1767-5536
Долгов Евгений Денисович – клинический ординатор каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: 1586dolgde@gmail.com; ORCID: 0000-0001-6709-5209
Evgenii D. Dolgov – clinical resident, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: 1586dolgde@gmail.com;
ORCID: 0000-0001-6709-5209.
Поступила в редакцию / Received: 22.02.2023
Поступила после рецензирования / Revised: 13.03.2023
Принята к публикации / Accepted: 30.03.2023
Список исп. литературыСкрыть список1. Улумбекова Г.Э., Прохоренко Н.Ф., Гиноян А.Б., Калашникова А.В. Системный подход к достижению общенациональной цели по увеличению ожидаемой продолжительности жизни до 78 лет к 2024 году. Экономика. Налоги. Право. 2019; 12 (2): 19–30.
[Ulumbekova G.E., Prokhorenko N.F., Ginoian A.B., Kalashnikova A.V. Sistemnyi podkhod k dostizheniiu obshchenatsional'noi tseli po uvelicheniiu ozhidaemoi prodolzhitel'nosti zhizni do 78 let k 2024 godu. Ekonomika. Nalogi. Pravo. 2019; 12 (2): 19–30 (in Russian).]
2. https://www.worldometers.info/ru/
3. Степанова Н.М., Сергуладзе С.Ю. Естественные патофизиологические процессы старения сердца как фактор развития сердечно-сосудистых заболеваний. Креативная кардиология. 2021; 15 (1): 72–86.
[Stepanova N.M., Serguladze S.Iu. Estestvennye patofiziologicheskie protsessy stareniia serdtsa kak faktor razvitiia serdechno-sosudistykh zabolevanii. Kreativnaia kardiologiia. 2021; 15 (1): 72–86 (in Russian).]
4. World Health Organization. 2021. Ageing and Health. https://www.who.int/news-room/fact-sheets/detail/ageing-and-health
5. Di Micco R et al. Cellular senescence in ageing: from mechanisms to therapeutic opportunities. Nat Rev Mol Cell Biol 2021; 22 (2): 75–95.
6. Rubio-Tomás T, Rueda-Robles A, Plaza-Díaz J, Álvarez-Mercado AI. Nutrition and cellular senescence in obesity-related disorders. J Nutr Biochem 2022; 99: 108861.
7. Mylonas A, O’Loghlen A. Cellular senescence and ageing: mechanisms and interventions. Frontiers Aging 2022; 3.
8. Sharma R. Emerging interrelationship between the gut microbiome and cellular senescence in the context of aging and disease: perspectives and therapeutic opportunities. Probiotics Antimicrobial Proteins 2022; 14 (4): 648–63.
9. World Health Organization. https://www.who.int/ru/news-room/fact-sheets/detail/obesity-and-overweight
10. Narasimhan A, Flores RR, Camell CD et al. Cellular Senescence in Obesity and Associated Complications: a New Therapeutic Target. Curr Diabetes Rep 2022; 22 (11): 537–48.
11. Mueck AO, Ruan X, Prasauskas V et al. Treatment of vaginal atrophy with estriol and lactobacilli combination: a clinical review. Climacteric 2018; 21 (2): 140–7.
12. Tang ZR, Zhang R, Lian ZX et al. Estrogen-receptor expression and function in female reproductive disease. Cells 2019; 8 (10): 1123.
13. Scavello I et al. Sexual health in menopause. Medicina 2019; 55 (9): 559.
14. Auriemma RS et al. The vaginal microbiome: a long urogenital colonization throughout woman life. Front Cell Infect Microbiol 2021; 11: 613.
15. The 2020 genitourinary syndrome of menopause position statement of The North American Menopause Society. Menopause 2020; 27 (9): 976–92. DOI: 10.1097/GME.0000000000001609
16. Дворянский С.А., Емельянова, Д.И., Яговкина Н.В. Климактерический синдром: современное состояние вопроса. Вятский медицинский вестник. 2017; 1 (53): 7–15.
[Dvorianskii S.A., Emel'ianova, D.I., Iagovkina N.V. Klimaktericheskii sindrom: sovremennoe sostoianie voprosa. Viatskii meditsinskii vestnik. 2017; 1 (53): 7–15 (in Russian).]
17. Zouboulis CC, Blume-Peytavi U, Kosmadaki M et al. Skin, hair and beyond: the impact of menopause. Climacteric 2022; 25 (5): 434–42.
18. Подзолкова Н.М., Подзолков В.И., Брагина А.Е., Роговская С.И. Современные возможности диагностики, лечения и профилактики возрастзависимых заболеваний у женщин. М.: ГЭОТАР-Медиа, 2019; c. 1226–35.
[Podzolkova N.M., Podzolkov V.I., Bragina A.E., Rogovskaia S.I. Sovremennye vozmozhnosti diagnostiki, lecheniia i profilaktiki vozrastzavisimykh zabolevanii u zhenshchin. M.: GEOTAR-Media, 2019; c. 1226–35. (in Russian).]
19. Fait T. Menopause hormone therapy: latest developments and clinical practice. Drugs Context 2019; 8.
20. Bachmann G. Urogenital ageing: an old problem newly recognized. Maturitas 1995; 22: S1–S5.
21. Федеральные клинические рекомендации «Менопауза и климактерическое состояние у женщины». 2021.
[Federal guidelines "Menopause and climacteric condition in women". 2021 (in Russian).]
22. Федеральные клинические рекомендации «Артериальная гипер тензия у взрослых». 2022.
[Federal clinical guidelines "Arterial hypertension in adults". 2022 (in Russian).]
23. Di Vincenzo O, Marra M, Sacco AM et al. Bioelectrical impedance (BIA)-derived phase angle in adults with obesity: A systematic review. Clinical Nutrition 2021; 40 (9): 5238–48.
24. Федеральные клинические рекомендации «Доброкачественная дисплазия молочной железы». 2020.
[Federal clinical guidelines "Benign breast dysplasia". 2020 (in Russian).]
25. Diwan B, Sharma R. Nutritional components as mitigators of cellular senescence in organismal aging: a comprehensive review. Food Sci Biotechn 2022; 31 (9): 1089–109.
26. Sirisinha S. The potential impact of gut microbiota on your health: current status and future challenges. Asian Pac J Allergy Immunol 2016; 34 (4): 249–64. DOI: 10.12932/AP0803. PMID: 28042926.
27. Nehra V, Allen JM, Mailing LJ et al. Gut Microbiota: Modulation of Host Physiology in Obesity. Physiology (Bethesda) 2016; 31 (5): 327–35. DOI: 10.1152/physiol.00005.2016. PMID: 27511459.
28. Zhang X, Zheng X, Yuan Y. Treatment of insulin resistance: straight from the gut. Drug Discov Today 2016; 21 (8): 1284–90. DOI: 10.1016/j.drudis.2016.06.016. PMID: 27326909.
29. Rivière A, Selak M, Lantin D et al. Bifidobacteria and Butyrate-Producing Colon Bacteria: Importance and Strategies for Their Stimulation in the Human Gut. Front Microbiol 2016; 7: 979. DOI: 10.3389/fmicb.2016.00979. PMID: 27446020.
30. Patel R, DuPont HL. New approaches for bacteriotherapy: prebiotics, new-generation probiotics, and synbiotics. Clin Infect Dis 2015; 60 (Suppl 2): S108–21. DOI: 10.1093/cid/civ177. PMID: 25922396.
31. Федеральные клинические рекомендации «Остеопороз». 2021.
[Federal clinical guidelines "Osteoporosis". 2021 (in Russian).]
32. Федеральные клинические рекомендации «Железодефицитная анемия». 2021.
[Federal clinical guidelines "Iron deficiency anemia". 2021 (in Russian).]
33. Del Castillo MD, Iriondo-DeHond A, Iriondo-DeHond M et al. Healthy eating recommendations: good for reducing dietary contribution to the body’s advanced glycation/lipoxidation end products pool? Nutrition Res Rev 2021; 34 (1): 48–63.
34. Tresguerres IF, Tamimi F, Eimar H et al. Resveratrol as anti-aging therapy for age-related bone loss. Rejuvenation Res 2014; 17 (5): 439–45.
35. Bantounou M, Plascevic J, Galley HF. Melatonin and related compounds: Antioxidant and anti-inflammatory actions. Antioxidants 2022; 11 (3): 532.
36. Bjørklund G, Shanaida M, Lysiuk R et al. Selenium: an antioxidant with a critical role in anti-aging. Molecules 2022; 27 (19): 6613.
37. Vaiserman A, De Falco E, Koliada A et al. Anti-ageing gene therapy: Not so far away? Ageing Res Rev 2019; 56: 100977.
38. PROMISS Project. https://www.promiss-vu.eu
39. Федеральные клинические рекомендации «Когнитивные расстройства у лиц пожилого и старческого возраста». 2021.
[Federal clinical guidelines "Cognitive disorders in the elderly and senile age". 2021 (in Russian).]
40. Федеральные клинические рекомендации «Сахарный диабет
2 типа у взрослых». 2022.
[Federal clinical guidelines "Type 2 diabetes mellitus in adults". 2022 (in Russian).]
41. Soukas AA, Hao H, Wu L. Metformin as anti-aging therapy: is it for everyone? Trends Endocrinol Metab 2019; 30 (10): 745–55.
42. Yerevanian A, Soukas AA. Metformin: mechanisms in human obesity and weight loss. Curr Obesity Rep 2019; 8: 156–64.
43. Wongprayoon P, Govitrapong P. Melatonin as a mitochondrial protector in neurodegenerative diseases. Cell Mol Life Sci 2017; 74: 3999–4014.
44. Bayliak MM, Gospodaryov DV, Lushchak VI. Mimicking caloric restriction for anti-aging effects: the pro-oxidant role of alpha-ketoglutarate. Curr Opin Toxicol 2022.
45. Gil Martínez V, Avedillo Salas A, Santander Ballestín S. Vitamin supplementation and dementia: a systematic review. Nutrients 2022; 14 (5): 1033.
46. Nguyen HD, Kim MS. The role of mixed B vitamin intakes on cognitive performance: modeling, genes and miRNAs involved. J Psychiatric Res 2022; 152: 38–56.
47. Buondonno I, Sassi F, Carignano G et al. From mitochondria to healthy aging: The role of branched-chain amino acids treatment: MATeR a randomized study. Clin Nutr 2020; 39 (7): 2080–91.
48. Payne A, Nahashon S, Taka E et al. Epigallocatechin-3-Gallate (EGCG): New therapeutic perspectives for neuroprotection, aging, and neuroinflammation for the modern age. Biomolecules 2022; 12 (3): 371.
49. Avgerinos KI, Spyrou N, Mantzoros CS, Dalamaga M. Obesity and cancer risk: Emerging biological mechanisms and perspectives. Metabolism 2019; 92: 121–35.
50. Федеральные клинические рекомендации «Старческая астения». 2020.
[Federal clinical guidelines "Senile asthenia". 2020 (in Russian).]

