Клинический разбор в акушерстве, гинекологии и репродуктологии № 3-4 2022
Клинический разбор в акушерстве, гинекологии и репродуктологии № 3-4 2022
Беременность при аденоме гипофиза со смешанной секрецией
Аннотация
Современные медицинские технологии позволяют сохранять беременность при разнообразных сопутствующих заболеваниях матери, в том числе имеется возможность проводить хирургические вмешательства прямо во время беременности, сохраняя здоровье матери и плода. В статье представлен клинический случай аденомы гипофиза, секретирующей гормон роста, пролактин и адренокортикотропный гормон. У пациентки наблюдался относительно мягкий вариант течения заболевания. При наличии сглаженной, но характерной клинической картины за прошедшие 10 лет по месту жительства врачи не установили гормональную активность аденомы гипофиза.
За период существования опухоли у пациентки дважды наступала беременность. Оба раза беременность была прервана: в первый раз прервать беременность рекомендовал гинеколог, во второй раз это было решением пациентки на фоне манифестации акромегалии и гиперкортицизма. При обращении наблюдалось параселлярное распространение аденомы гипофиза с прорастанием ее в кавернозный синус. Было проведено оперативное лечение, удалена доступная часть опухоли с фрагментом аденогипофиза, далее была проведена лучевая терапия. Возможным последствием лечения являются развитие вторичного гипогонадизма и невозможность наступления спонтанной беременности. Учитывая намерение женщины родить ребенка, целесообразно было бы организовать коллегиальное ведение пациентки гинекологами, эндокринологами, хирургами и анестезиологами. Такое сотрудничество могло бы позволить пациентке реализовать свою репродуктивную функцию.
Ключевые слова: клинический случай, беременность, акромегалия, гиперкортицизм, аденома гипофиза, смешанная секреция.
Для цитирования: Гусова А.А. Беременность при аденоме гипофиза со смешанной секрецией. Клинический разбор в акушерстве, гинекологии и репродуктологии. 2022; 3–4: 22–27. DOI: 10.47407/kragr2022.2.34.000038
Современные медицинские технологии позволяют сохранять беременность при разнообразных сопутствующих заболеваниях матери, в том числе имеется возможность проводить хирургические вмешательства прямо во время беременности, сохраняя здоровье матери и плода. В статье представлен клинический случай аденомы гипофиза, секретирующей гормон роста, пролактин и адренокортикотропный гормон. У пациентки наблюдался относительно мягкий вариант течения заболевания. При наличии сглаженной, но характерной клинической картины за прошедшие 10 лет по месту жительства врачи не установили гормональную активность аденомы гипофиза.
За период существования опухоли у пациентки дважды наступала беременность. Оба раза беременность была прервана: в первый раз прервать беременность рекомендовал гинеколог, во второй раз это было решением пациентки на фоне манифестации акромегалии и гиперкортицизма. При обращении наблюдалось параселлярное распространение аденомы гипофиза с прорастанием ее в кавернозный синус. Было проведено оперативное лечение, удалена доступная часть опухоли с фрагментом аденогипофиза, далее была проведена лучевая терапия. Возможным последствием лечения являются развитие вторичного гипогонадизма и невозможность наступления спонтанной беременности. Учитывая намерение женщины родить ребенка, целесообразно было бы организовать коллегиальное ведение пациентки гинекологами, эндокринологами, хирургами и анестезиологами. Такое сотрудничество могло бы позволить пациентке реализовать свою репродуктивную функцию.
Ключевые слова: клинический случай, беременность, акромегалия, гиперкортицизм, аденома гипофиза, смешанная секреция.
Для цитирования: Гусова А.А. Беременность при аденоме гипофиза со смешанной секрецией. Клинический разбор в акушерстве, гинекологии и репродуктологии. 2022; 3–4: 22–27. DOI: 10.47407/kragr2022.2.34.000038
Pregnancy in patient with mixed secreting pituitary adenoma
Anna A. Gusova
Abstract
Contemporary medical technologies make it possible to maintain pregnancy in mothers with various concomitant disorders. Among other things it is possible to perform surgery right during pregnancy without disturbing pregnancy, and maintaining maternal and fetal health. The paper reports the clinical case of pituitary adenoma, secreting growth hormone, prolactin, and ACTH. The female patient had a rather mild course of the disease. Provided that the patient had vague but typical clinical manifestations, hormonal activity of pituitary adenoma has not been determined for ten years in the community clinic. During the period of the tumor existence two pregnancies occurred. Pregnancy was terminated both times: at the first time pregnancy termination was recommended by gynecologist, and at the second time it was the patient herself who made a decision due to the acromegaly and hypercortisolism manifestations. The patient presented with the extension of pituitary adenoma invading the cavernous sinus. Surgery was performed in order to remove the accessible part of the tumor together with a fragment of adenohypophysis, then the patient received radiation therapy. The development of secondary hypogonadism and impossibility of spontaneous pregnancy are the possible treatment effects. Thus, taking into account the woman's intention to have a child, the team efforts of gynecologists of all levels, endocrinologists, surgeons and anesthesiologists, focused on maintaining pregnancy in women with pituitary adenomas would be appropriate. Such cooperation might allow the patient to implement her reproductive function.
Key words: clinical case, pregnancy, acromegaly, hypercortisolism, pituitary adenoma, mixed secretions.
For citation: Gusova A.A. Pregnancy in patient with mixed secreting pituitary adenoma. Clinical analysis in obstetrics, gynecology and reproductology. 2022; 3–4: 22–27. DOI: 10.47407/kragr2022.2.34.000038
Актуальность
Аденомы гипофиза – нередкий вариант образований головного мозга. Популяционная частота аденом гипофиза по разным данным составляет около 20% [1]. Гормонально-активные аденомы гипофиза встречаются в популяции с частотой 0,1%, наиболее частым вариантом гормональной активности является гиперпролактинемия [1–3]. В последние десятилетия было показано, что опухоли, секретирующие пролактин, в большинстве случаев поддаются успешному медикаментозному лечению. При этом другие, более редкие варианты гормональной активности аденом гипофиза – гиперсекреция соматотропного гормона (СТГ) и адренокортикотропного гормона (АКТГ), вызывающие у взрослых соответственно акромегалию и болезнь Иценко–Кушинга (БИК), часто являются заболеваниями, в меньшей степени поддающимся медикаментозному воздействию. Эти патологии приводят к существенному ухудшению качества жизни и здоровья, инвалидизации пациентов [3–5].
Особым вариантом аденом гипофиза являются опухоли со смешанной гормональной секрецией. Считается, что варианты сочетаний гормональной активности клеток аденомы связаны с источником опухолевых клеток и со степенью их дифференцировки. Наиболее частым вариантом смешанной гормональной активности аденом гипофиза является сочетание гиперпролактинемии и гиперсекреции СТГ, при этом любой вариант аденомы гипофиза со смешанной секрецией обладает более агрессивным ростом, чем аденома, секретирующая один гормон. Сочетание секреции аденомой СТГ и АКТГ наблюдается редко и характеризуется частыми рецидивами и неблагоприятным прогнозом [2–4].
Наступление беременности при гиперпролактинемиях на фоне медикаментозной терапии хорошо изучено и описано во многих руководствах [6–8]. Беременности при активных акромегалии и гиперкортицизме, наоборот, являются достаточно редкими и вызывают много вопросов и затруднений у гинекологов первичного звена.
Клинический случай
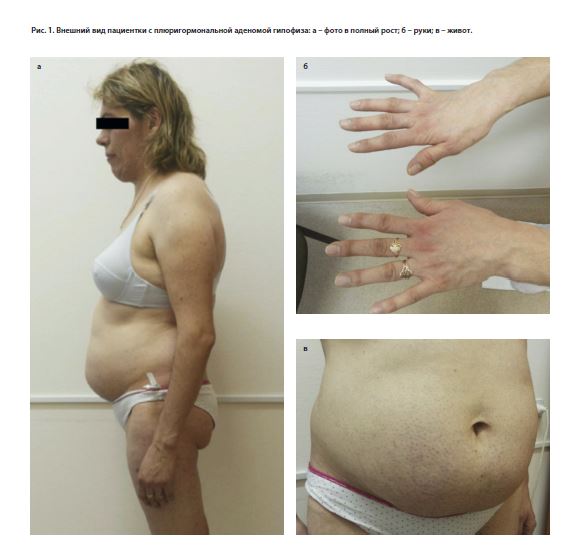
Пациентка З. 38 лет обратилась с жалобами на повышение артериального давления (АД) до 180/100 мм рт. ст., головные боли и изменение распределения жировой клетчатки – отложение жировой клетчатки в области живота, на спине, плечах и лице, похудение конечностей (рис. 1). Из анамнеза известно, что 16 лет назад впервые были выявлены эндоселлярная аденома гипофиза, гиперпролактинемия до 3053 мМЕ/л (при норме до 727) и снижение тиреотропного гормона (ТТГ) – 0,01 МЕ/л (норма 0,4–4,0) при отсутствии изменений при ультразвуковом исследовании (УЗИ) щитовидной железы (объем железы 14,4 мл). Был назначен бромокриптин 2,5 мг в день, на фоне лечения пролактин снизился до 1679 нмоль/л, терапию было рекомендовано продолжить, однако приверженность терапии была низкой.
 Из представленной медицинской документации известно, что снижение ТТГ до 0,037–0,1 МЕ/л (норма от 0,4) при нормальном уровне тироксина свободного (Т4св) – 18,2–21,1 пмоль/л (норма 10–23,2) систематически выявлялось при обследовании 6 и 12 лет назад, рекомендовался прием тиреостатиков в дозе 5 мг/сут, пациентка препарат не принимала. За год до обращения при обследовании – эутиреоз, объем щитовидной железы 23 мл.
Из представленной медицинской документации известно, что снижение ТТГ до 0,037–0,1 МЕ/л (норма от 0,4) при нормальном уровне тироксина свободного (Т4св) – 18,2–21,1 пмоль/л (норма 10–23,2) систематически выявлялось при обследовании 6 и 12 лет назад, рекомендовался прием тиреостатиков в дозе 5 мг/сут, пациентка препарат не принимала. За год до обращения при обследовании – эутиреоз, объем щитовидной железы 23 мл.
С 2010 г. периодически выявлялось умеренное повышение кортизола – 742–1002 нмоль/л (норма до 690) при высоконормальном или повышенном АКТГ – 43,6–59,6 пг/мл (норма до 46). За год до обращения АКТГ 23,1 пг/мл (при норме до 58,2), кортизол 590 нмоль/л (при норме до 600), дальнейшее тестирование по поводу эндогенного гиперкортицизма не проводилось.
В возрасте 32 лет впервые выявлено нарушение толерантности к углеводам, которое через 2 года прогрессировало в сахарный диабет. На момент осмотра пациентка получала интенсифицированную инсулинотерапию препаратами гларгин и аспарт, диету не соблюдала, при самоконтроле гликемия натощак 7–8 ммоль/л, в течение дня до 11–12 ммоль/л, гликированный гемоглобин 8,8%.
С 34 лет отметила периодическое повышение АД до 130/80 мм рт. ст., в течение года до обращения – повышение АД до 180/100 мм рт. ст., при этом постоянной антигипертензивной терапии пациентка не получала. За 3 мес до обращения при обследовании – снижение ТТГ -0,04 МЕ/л при нормальном Т4св – 18,2 пмоль/л (норма 10,5–24,5), был назначен тиамазол 5–10 мг/сут. В связи с выявленной гормональной активностью аденомы гипофиза (повышение инсулиноподобного фактора роста 1 – ИФР-1 1104 нг/мл при норме до 307, СТГ 2,08 нг/мл при норме 0–8, кортизол 486 нмоль/л при норме до 600, АКТГ и пролактин в норме) в течение месяца принимала бромокриптин 2,5 мг на ночь. Менархе в 15 лет, цикл установился сразу, с 26 лет отметила нарушения менструального цикла по типу олигоопсоменореи. В течение 3 лет до обращения цикл относительно регулярный с периодическими задержками. Замужем, в течение длительного времени планировали деторождение. За 4 года до обращения во ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Мин-здрава России наступила беременность, однако в связи с повышенным уровнем пролактина по месту жительства было рекомендовано прервать беременность, что пациентка и сделала. Результаты физикального, лабораторного и инструментального обследования пациентки в ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». При физикальном обследовании: пациентка повышенного питания, индекс массы тела 28,7 кг/м2. Кожные покровы умеренно гиперемированы, цианотичны, неравномерно пигментированы, ливедо (см. рис. 1). На коже живота обнаруживаются тонкие белесые полосы растяжения. Перераспределение подкожной жировой клетчатки с преимущественным отложением на животе и спине. Гирсутизм – избыточный рост волос на животе, лице, груди, бедрах. Незначительно выраженный экзофтальм, симптом Мебиуса положителен, остальные глазные симптомы отрицательные. При лабораторном обследовании: пролактин 218 мМЕ/л (норма 40–530), СТГ 4,73 нг/мл (до 8), ИФР-1 1023 нг/мл (до 307), ТТГ<0,01 мМЕ/л, Т4св 15,1 пмоль/л (11,5–22,7), кортизол 588 МЕд/л (норма до 690). Проведен ночной подавляющий тест с 1 мг дексаметазона. После приема дексаметазона проведены исследования: кортизол – 828 нмоль/л, АКТГ – 56,8 пг/мл (норма до 46). При УЗИ щитовидной железы: объем железы 38,6 мл, в левой доле анэхогенные образования 5 и 7 мм. По данным магнитно-резонансной томографии – эндолатеро(D)селлярная аденома гипофиза, супраселлярная цистерна свободна. При обследовании у офтальмолога с проведением компьютерной периметрии нарушений со стороны зрения не выявлено. На основании данных обследования установлен диагноз: аденома гипофиза смешанной секреции (СТГ-АКТГ-пролактинсекретирующая). БИК средней тяжести. Акромегалия, активная фаза. Сахарный диабет, ассоциированный с гиперкортицизмом и акромегалией. Назначен каберголин внутрь 3 мг/нед, внутрь кетоконазол 200 мг/сут, октреотид продленного действия 20 мг внутримышечно 1 раз в 28 дней, интенсифицированная инсулинотерапия терапия под контролем гликемии. Рекомендовано трансназальное транссфеноидальное нейрохирургическое лечение по поводу макроаденомы гипофиза. Незадолго до даты госпитализации пациентка обратилась с просьбой перенести госпитализацию в связи с наступлением у нее беременности и желанием прервать беременность по месту жительства согласно настоятельным рекомендациям гинекологов. Несмотря на многочисленные беседы о возможности сохранения беременности и проведения операции по поводу аденомы гипофиза на фоне беременности с использованием методик и препаратов, разрешенных при беременности, а также разъяснения о возможном развитии вторичного гипогонадизма и потере фертильности как последствии проведения радикальной операции удаления макроаденомы гипофиза, пациентка прервала беременность на сроке 10 нед. Еще через 3 мес пациентка была госпитализирована в ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко» для проведения оперативного лечения. При лабораторном контроле до операции на фоне консервативной терапии отмечалось некоторое снижение гормональной активности опухоли: СТГ 2,57 нг/мл, ИФР-1 629 нг/мл (норма до 284), АКТГ 21,5 пг/мл (до 46), кортизол 235 нмоль/л (119–618), пролактин 17 МЕ/мл (59–619). Лечение. Через полгода после первичного обращения, в возрасте 38 лет, в ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко» была проведена операция эндоскопического эндоназального транссфеноидального частичного удаления эндолатеро(R)селлярной аденомы гипофиза. Согласно протоколу оперативного вмешательства, опухоль была кремового цвета, плотной консистенции, занимала всю полость турецкого седла и распространялась в правый кавернозный синус. При операции удалена доступная часть опухоли. По данным патоморфологического исследования удаленной опухоли: аденома гипофиза с инфильтрацией капсулы и фрагмент аденогипофиза. После операции была отмечена нормализация гликемии, отменена сахароснижающая терапия. Через 3 мес после операции гормональная активность аденомы, согласно лабораторным данным, сохранялась, было рекомендовано проведение лучевой терапии. В течение года после операции пациентка не получала терапии, направленной на снижение гормональной активности аденомы гипофиза. Через год после операции, в 39 лет, при гормональном обследовании подтверждено сохранение гормональной активности опухоли: пролактин 178 мМЕ/л (норма 59–619), СТГ 3,17 нг/мл (до 8), ИФР-1 1023 нг/мл (до 307), ТТГ 0,02 мМЕ/л, Т4св 16,6 пмоль/л (11,5–22,7), кортизол 461 МЕд/л (до 618), в ночном подавляющем тесте с 1 мг дексаметазона кортизол 107 нмоль/л (<50), свободный кортизол в суточной моче 835 нмоль/сут (380–940), гликированный гемоглобин 6,2%. Менструальная функция у пациентки была сохранена, индекс массы тела 26,5 кг/м2. С учетом наличия остатков опухоли и ее гормональной активности было проведено лучевое лечение в ФГАУ «НМИЦ нейрохирургии им. акад.
Н.Н. Бурденко». После лучевого лечения было рекомендовано возобновить терапию октреотидом продленного действия 20 мг внутримышечно 1 раз в 28 дней и каберголином внутрь 3 мг/нед, а также вновь назначен метформин 2000 мг/сут под контролем гормональных показателей и гликемии. Исход и результаты последующего наблюдения. Для оценки эффективности проведенного лечения необходима оценка гормонального статуса в отдаленном периоде, однако пациентка стала наблюдаться по месту жительства и не приехала для динамического контроля. С учетом проведения лучевого лечения у пациентки возможно развитие гипопитуитаризма, в том числе вторичного гипогонадизма. Может быть необходима терапия для снижения гормональной активности остаточной ткани опухоли. С учетом возраста пациентки это может помешать реализации ее репродуктивных планов. Что касается функции щитовидной железы, то в данном случае, очевидно, наблюдалось изолированное снижение ТТГ на фоне наличия активной БИК, что позволяет предположить нормализацию показателей при ликвидации эндогенного гиперкортицизма [9].
Обсуждение
Данный клинический случай представляет особый интерес, так как и при гиперпролактинемии, и при акромегалии, и при гиперкортицизме обычно наблюдается нарушение овуляторной функции и фертильность существенно снижается. А у описываемой пациентки на фоне плюригормональной гиперфункции гипофиза дважды самопроизвольно развилась беременность.
Основными эндокринными нарушениями, определяющими прогноз и тяжесть состояния пациентки, являлись эндогенный гиперкортицизм (БИК) и акромегалия, при этом гиперпролактинемия могла быть следствием масс-эффекта макроаденомы на ножку гипофиза.
В большинстве случаев у пациенток с акромегалией не наблюдается ухудшения течения заболевания при беременности. Считается, что беременность не стимулирует секрецию СТГ аденомой, продукция СТГ аденомой остается автономной. При этом в начале беременности под действием эстрогенов развивается относительная резистентность гепатоцитов к действию СТГ, что проявляется исходным снижением уровня ИФР-1 в крови с дальнейшим повышением его концентрации за счет плацентарного ИФР-1, однако обычно уровень ИФР-1 во время беременности не возрастает более чем на 50% [3, 10]. В сериях наблюдений у большинства пациенток с акромегалией при беременности размеры аденомы оставались неизменными даже без медикаментозного лечения [4, 8, 11, 12].
При наличии активного гиперкортицизма планирование беременности не рекомендуется. Более того, активные акромегалия и гиперкортицизм являются показаниями для искусственного прерывания беременности по медицинским показаниям [13]. Однако в настоящее время накоплен клинический опыт ведения беременности у таких пациенток, который позволяет сохранить жизнь и здоровье матери и ребенка. Ведение такой беременности рекомендуется проводить мультидисциплинарной командой врачей [8, 12, 14].
По данным С.А. Григорьянц и соавт. [15], у беременных женщин с БИК ремиссии удалось добиться в 69% случаев. У пациенток наблюдалась высокая частота осложнений беременности – 77–92%. Наиболее часто регистрировались внутриутробная задержка развития плода, преждевременные роды (более 50% случаев), перинатальная смертность (до 25%). Однако до 70% рожденных детей были практически здоровы, а выявленные отклонения – неспецифичны [3, 4, 15, 16].
Согласно данным зарубежных авторов, за историю существования PubMed до июня 2020 г. было описано 62 случая беременности при достоверно диагностированной БИК [12, 14, 17]. При этом более чем в 50% случаев беременность сопровождалась неблагоприятными материнскими или перинатальными исходами. На фоне хирургического и медикаментозного лечения, которое проводилось в 40% случаев, исходы беременности были лучше. Предпочтительным вариантом лечения является трассфеноидальное удаление аденомы гипофиза, при этом варианте наблюдалось более 85% благоприятных перинатальных исходов. Наилучшим временем для проведения операции считается начало II триместра беременности. Еще одним вариантом является медикаментозная терапия, которая назначается во время II и III триместров беременности [17]. При этом препаратом выбора при беременности является метирапон, в то время как кетоконазол обладает тератогенным эффектом и рекомендован только в крайнем случае при непереносимости метирапона [5].
Вне зависимости от гормональной активности опухоли женщинам с макроаденомами гипофиза (более
1 см) во время беременности рекомендована оценка полей зрения для своевременного выявления отрицательной динамики и проведения соответствующего лечения при необходимости [4, 8, 11, 12]. В нашем случае не наблюдалось супраселлярного роста аденомы гипофиза и риск развития хиазмального синдрома на фоне гиперплазии гипофиза во время беременности был минимальным.
Важнейшими параметрами, оказывающими основное влияние на течение беременности как при акромегалии, так и при гиперкортицизме, являются симптоматические нарушения – артериальная гипертензия и сахарный диабет [4, 8, 11, 12].
Динамика симптомов заболевания, а также изолированное снижение ТТГ в дебюте заболевания при небольшой эндоселлярной аденоме гипофиза позволяют предположить, что опухоль исходно продуцировала АКТГ [10]. При этом, исходя из клиники, выраженность гиперкортицизма была незначительной и обнаружить его можно было только при проведении диагностических проб, которые не были выполнены в течение первых 16 (!) лет после выявления аденомы гипофиза. Тем не менее с точки зрения осуществления репродуктивных планов первая беременность была наиболее благоприятной.
Заключение
Таким образом, за время от дебюта заболевания до операции удаления аденомы пациентка дважды беременела. И несмотря на наличие репродуктивных планов, оба раза было принято решение о прерывании беременности. При этом, согласно современным представлениям, наличие гиперпролактинемии и аденомы гипофиза не является противопоказанием для беременности. Более того, в большинстве случаев во время беременности не происходит прогрессирования пролактинсекретирующих опухолей гипофиза [7]. Наличие аденомы гипофиза, секретирующей гормон роста, а тем более АКТГ, является крайне неблагоприятным фоном для развития беременности, однако с учетом существующих способов лечения также не является абсолютным противопоказанием для беременности и родов. При сохранении нарушения функции тиреотрофов со снижением ТТГ на фоне гиперкортицизма при беременности вести пациентку следует исходя из принципов ведения беременных с вторичным гипотиреозом.
У данной пациентки наиболее благоприятным в отношении перинатальных исходов представляется сохранение первой беременности, в период минимальной выраженности артериальной гипертензии и сахарного диабета, ухудшающих прогноз.
Дополнительная информация
Согласие пациентки. Пациентка добровольно подписала информированное согласие на публикацию персональной медицинской информации в обезличенной форме.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Сonflict of interests. The author declares that there is not conflict of interests.
Гусова Анна Аузбиевна – канд. мед. наук, ФГБУ ФНКЦСМ ФМБА России. E-mail: agusova@mail.ru
Anna A. Gusova – Cand. Sci. (Med.), Federal Research and Clinical Center of Sports Medicine and Rehabilitation of the Federal Medical Biological Agency of Russia. Е-mail: agusova@mail.ru
Anna A. Gusova
Abstract
Contemporary medical technologies make it possible to maintain pregnancy in mothers with various concomitant disorders. Among other things it is possible to perform surgery right during pregnancy without disturbing pregnancy, and maintaining maternal and fetal health. The paper reports the clinical case of pituitary adenoma, secreting growth hormone, prolactin, and ACTH. The female patient had a rather mild course of the disease. Provided that the patient had vague but typical clinical manifestations, hormonal activity of pituitary adenoma has not been determined for ten years in the community clinic. During the period of the tumor existence two pregnancies occurred. Pregnancy was terminated both times: at the first time pregnancy termination was recommended by gynecologist, and at the second time it was the patient herself who made a decision due to the acromegaly and hypercortisolism manifestations. The patient presented with the extension of pituitary adenoma invading the cavernous sinus. Surgery was performed in order to remove the accessible part of the tumor together with a fragment of adenohypophysis, then the patient received radiation therapy. The development of secondary hypogonadism and impossibility of spontaneous pregnancy are the possible treatment effects. Thus, taking into account the woman's intention to have a child, the team efforts of gynecologists of all levels, endocrinologists, surgeons and anesthesiologists, focused on maintaining pregnancy in women with pituitary adenomas would be appropriate. Such cooperation might allow the patient to implement her reproductive function.
Key words: clinical case, pregnancy, acromegaly, hypercortisolism, pituitary adenoma, mixed secretions.
For citation: Gusova A.A. Pregnancy in patient with mixed secreting pituitary adenoma. Clinical analysis in obstetrics, gynecology and reproductology. 2022; 3–4: 22–27. DOI: 10.47407/kragr2022.2.34.000038
Актуальность
Аденомы гипофиза – нередкий вариант образований головного мозга. Популяционная частота аденом гипофиза по разным данным составляет около 20% [1]. Гормонально-активные аденомы гипофиза встречаются в популяции с частотой 0,1%, наиболее частым вариантом гормональной активности является гиперпролактинемия [1–3]. В последние десятилетия было показано, что опухоли, секретирующие пролактин, в большинстве случаев поддаются успешному медикаментозному лечению. При этом другие, более редкие варианты гормональной активности аденом гипофиза – гиперсекреция соматотропного гормона (СТГ) и адренокортикотропного гормона (АКТГ), вызывающие у взрослых соответственно акромегалию и болезнь Иценко–Кушинга (БИК), часто являются заболеваниями, в меньшей степени поддающимся медикаментозному воздействию. Эти патологии приводят к существенному ухудшению качества жизни и здоровья, инвалидизации пациентов [3–5].
Особым вариантом аденом гипофиза являются опухоли со смешанной гормональной секрецией. Считается, что варианты сочетаний гормональной активности клеток аденомы связаны с источником опухолевых клеток и со степенью их дифференцировки. Наиболее частым вариантом смешанной гормональной активности аденом гипофиза является сочетание гиперпролактинемии и гиперсекреции СТГ, при этом любой вариант аденомы гипофиза со смешанной секрецией обладает более агрессивным ростом, чем аденома, секретирующая один гормон. Сочетание секреции аденомой СТГ и АКТГ наблюдается редко и характеризуется частыми рецидивами и неблагоприятным прогнозом [2–4].
Наступление беременности при гиперпролактинемиях на фоне медикаментозной терапии хорошо изучено и описано во многих руководствах [6–8]. Беременности при активных акромегалии и гиперкортицизме, наоборот, являются достаточно редкими и вызывают много вопросов и затруднений у гинекологов первичного звена.
Клинический случай
Пациентка З. 38 лет обратилась с жалобами на повышение артериального давления (АД) до 180/100 мм рт. ст., головные боли и изменение распределения жировой клетчатки – отложение жировой клетчатки в области живота, на спине, плечах и лице, похудение конечностей (рис. 1). Из анамнеза известно, что 16 лет назад впервые были выявлены эндоселлярная аденома гипофиза, гиперпролактинемия до 3053 мМЕ/л (при норме до 727) и снижение тиреотропного гормона (ТТГ) – 0,01 МЕ/л (норма 0,4–4,0) при отсутствии изменений при ультразвуковом исследовании (УЗИ) щитовидной железы (объем железы 14,4 мл). Был назначен бромокриптин 2,5 мг в день, на фоне лечения пролактин снизился до 1679 нмоль/л, терапию было рекомендовано продолжить, однако приверженность терапии была низкой.
С 2010 г. периодически выявлялось умеренное повышение кортизола – 742–1002 нмоль/л (норма до 690) при высоконормальном или повышенном АКТГ – 43,6–59,6 пг/мл (норма до 46). За год до обращения АКТГ 23,1 пг/мл (при норме до 58,2), кортизол 590 нмоль/л (при норме до 600), дальнейшее тестирование по поводу эндогенного гиперкортицизма не проводилось.
В возрасте 32 лет впервые выявлено нарушение толерантности к углеводам, которое через 2 года прогрессировало в сахарный диабет. На момент осмотра пациентка получала интенсифицированную инсулинотерапию препаратами гларгин и аспарт, диету не соблюдала, при самоконтроле гликемия натощак 7–8 ммоль/л, в течение дня до 11–12 ммоль/л, гликированный гемоглобин 8,8%.
С 34 лет отметила периодическое повышение АД до 130/80 мм рт. ст., в течение года до обращения – повышение АД до 180/100 мм рт. ст., при этом постоянной антигипертензивной терапии пациентка не получала. За 3 мес до обращения при обследовании – снижение ТТГ -0,04 МЕ/л при нормальном Т4св – 18,2 пмоль/л (норма 10,5–24,5), был назначен тиамазол 5–10 мг/сут. В связи с выявленной гормональной активностью аденомы гипофиза (повышение инсулиноподобного фактора роста 1 – ИФР-1 1104 нг/мл при норме до 307, СТГ 2,08 нг/мл при норме 0–8, кортизол 486 нмоль/л при норме до 600, АКТГ и пролактин в норме) в течение месяца принимала бромокриптин 2,5 мг на ночь. Менархе в 15 лет, цикл установился сразу, с 26 лет отметила нарушения менструального цикла по типу олигоопсоменореи. В течение 3 лет до обращения цикл относительно регулярный с периодическими задержками. Замужем, в течение длительного времени планировали деторождение. За 4 года до обращения во ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Мин-здрава России наступила беременность, однако в связи с повышенным уровнем пролактина по месту жительства было рекомендовано прервать беременность, что пациентка и сделала. Результаты физикального, лабораторного и инструментального обследования пациентки в ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». При физикальном обследовании: пациентка повышенного питания, индекс массы тела 28,7 кг/м2. Кожные покровы умеренно гиперемированы, цианотичны, неравномерно пигментированы, ливедо (см. рис. 1). На коже живота обнаруживаются тонкие белесые полосы растяжения. Перераспределение подкожной жировой клетчатки с преимущественным отложением на животе и спине. Гирсутизм – избыточный рост волос на животе, лице, груди, бедрах. Незначительно выраженный экзофтальм, симптом Мебиуса положителен, остальные глазные симптомы отрицательные. При лабораторном обследовании: пролактин 218 мМЕ/л (норма 40–530), СТГ 4,73 нг/мл (до 8), ИФР-1 1023 нг/мл (до 307), ТТГ<0,01 мМЕ/л, Т4св 15,1 пмоль/л (11,5–22,7), кортизол 588 МЕд/л (норма до 690). Проведен ночной подавляющий тест с 1 мг дексаметазона. После приема дексаметазона проведены исследования: кортизол – 828 нмоль/л, АКТГ – 56,8 пг/мл (норма до 46). При УЗИ щитовидной железы: объем железы 38,6 мл, в левой доле анэхогенные образования 5 и 7 мм. По данным магнитно-резонансной томографии – эндолатеро(D)селлярная аденома гипофиза, супраселлярная цистерна свободна. При обследовании у офтальмолога с проведением компьютерной периметрии нарушений со стороны зрения не выявлено. На основании данных обследования установлен диагноз: аденома гипофиза смешанной секреции (СТГ-АКТГ-пролактинсекретирующая). БИК средней тяжести. Акромегалия, активная фаза. Сахарный диабет, ассоциированный с гиперкортицизмом и акромегалией. Назначен каберголин внутрь 3 мг/нед, внутрь кетоконазол 200 мг/сут, октреотид продленного действия 20 мг внутримышечно 1 раз в 28 дней, интенсифицированная инсулинотерапия терапия под контролем гликемии. Рекомендовано трансназальное транссфеноидальное нейрохирургическое лечение по поводу макроаденомы гипофиза. Незадолго до даты госпитализации пациентка обратилась с просьбой перенести госпитализацию в связи с наступлением у нее беременности и желанием прервать беременность по месту жительства согласно настоятельным рекомендациям гинекологов. Несмотря на многочисленные беседы о возможности сохранения беременности и проведения операции по поводу аденомы гипофиза на фоне беременности с использованием методик и препаратов, разрешенных при беременности, а также разъяснения о возможном развитии вторичного гипогонадизма и потере фертильности как последствии проведения радикальной операции удаления макроаденомы гипофиза, пациентка прервала беременность на сроке 10 нед. Еще через 3 мес пациентка была госпитализирована в ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко» для проведения оперативного лечения. При лабораторном контроле до операции на фоне консервативной терапии отмечалось некоторое снижение гормональной активности опухоли: СТГ 2,57 нг/мл, ИФР-1 629 нг/мл (норма до 284), АКТГ 21,5 пг/мл (до 46), кортизол 235 нмоль/л (119–618), пролактин 17 МЕ/мл (59–619). Лечение. Через полгода после первичного обращения, в возрасте 38 лет, в ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко» была проведена операция эндоскопического эндоназального транссфеноидального частичного удаления эндолатеро(R)селлярной аденомы гипофиза. Согласно протоколу оперативного вмешательства, опухоль была кремового цвета, плотной консистенции, занимала всю полость турецкого седла и распространялась в правый кавернозный синус. При операции удалена доступная часть опухоли. По данным патоморфологического исследования удаленной опухоли: аденома гипофиза с инфильтрацией капсулы и фрагмент аденогипофиза. После операции была отмечена нормализация гликемии, отменена сахароснижающая терапия. Через 3 мес после операции гормональная активность аденомы, согласно лабораторным данным, сохранялась, было рекомендовано проведение лучевой терапии. В течение года после операции пациентка не получала терапии, направленной на снижение гормональной активности аденомы гипофиза. Через год после операции, в 39 лет, при гормональном обследовании подтверждено сохранение гормональной активности опухоли: пролактин 178 мМЕ/л (норма 59–619), СТГ 3,17 нг/мл (до 8), ИФР-1 1023 нг/мл (до 307), ТТГ 0,02 мМЕ/л, Т4св 16,6 пмоль/л (11,5–22,7), кортизол 461 МЕд/л (до 618), в ночном подавляющем тесте с 1 мг дексаметазона кортизол 107 нмоль/л (<50), свободный кортизол в суточной моче 835 нмоль/сут (380–940), гликированный гемоглобин 6,2%. Менструальная функция у пациентки была сохранена, индекс массы тела 26,5 кг/м2. С учетом наличия остатков опухоли и ее гормональной активности было проведено лучевое лечение в ФГАУ «НМИЦ нейрохирургии им. акад.
Н.Н. Бурденко». После лучевого лечения было рекомендовано возобновить терапию октреотидом продленного действия 20 мг внутримышечно 1 раз в 28 дней и каберголином внутрь 3 мг/нед, а также вновь назначен метформин 2000 мг/сут под контролем гормональных показателей и гликемии. Исход и результаты последующего наблюдения. Для оценки эффективности проведенного лечения необходима оценка гормонального статуса в отдаленном периоде, однако пациентка стала наблюдаться по месту жительства и не приехала для динамического контроля. С учетом проведения лучевого лечения у пациентки возможно развитие гипопитуитаризма, в том числе вторичного гипогонадизма. Может быть необходима терапия для снижения гормональной активности остаточной ткани опухоли. С учетом возраста пациентки это может помешать реализации ее репродуктивных планов. Что касается функции щитовидной железы, то в данном случае, очевидно, наблюдалось изолированное снижение ТТГ на фоне наличия активной БИК, что позволяет предположить нормализацию показателей при ликвидации эндогенного гиперкортицизма [9].
Обсуждение
Данный клинический случай представляет особый интерес, так как и при гиперпролактинемии, и при акромегалии, и при гиперкортицизме обычно наблюдается нарушение овуляторной функции и фертильность существенно снижается. А у описываемой пациентки на фоне плюригормональной гиперфункции гипофиза дважды самопроизвольно развилась беременность.
Основными эндокринными нарушениями, определяющими прогноз и тяжесть состояния пациентки, являлись эндогенный гиперкортицизм (БИК) и акромегалия, при этом гиперпролактинемия могла быть следствием масс-эффекта макроаденомы на ножку гипофиза.
В большинстве случаев у пациенток с акромегалией не наблюдается ухудшения течения заболевания при беременности. Считается, что беременность не стимулирует секрецию СТГ аденомой, продукция СТГ аденомой остается автономной. При этом в начале беременности под действием эстрогенов развивается относительная резистентность гепатоцитов к действию СТГ, что проявляется исходным снижением уровня ИФР-1 в крови с дальнейшим повышением его концентрации за счет плацентарного ИФР-1, однако обычно уровень ИФР-1 во время беременности не возрастает более чем на 50% [3, 10]. В сериях наблюдений у большинства пациенток с акромегалией при беременности размеры аденомы оставались неизменными даже без медикаментозного лечения [4, 8, 11, 12].
При наличии активного гиперкортицизма планирование беременности не рекомендуется. Более того, активные акромегалия и гиперкортицизм являются показаниями для искусственного прерывания беременности по медицинским показаниям [13]. Однако в настоящее время накоплен клинический опыт ведения беременности у таких пациенток, который позволяет сохранить жизнь и здоровье матери и ребенка. Ведение такой беременности рекомендуется проводить мультидисциплинарной командой врачей [8, 12, 14].
По данным С.А. Григорьянц и соавт. [15], у беременных женщин с БИК ремиссии удалось добиться в 69% случаев. У пациенток наблюдалась высокая частота осложнений беременности – 77–92%. Наиболее часто регистрировались внутриутробная задержка развития плода, преждевременные роды (более 50% случаев), перинатальная смертность (до 25%). Однако до 70% рожденных детей были практически здоровы, а выявленные отклонения – неспецифичны [3, 4, 15, 16].
Согласно данным зарубежных авторов, за историю существования PubMed до июня 2020 г. было описано 62 случая беременности при достоверно диагностированной БИК [12, 14, 17]. При этом более чем в 50% случаев беременность сопровождалась неблагоприятными материнскими или перинатальными исходами. На фоне хирургического и медикаментозного лечения, которое проводилось в 40% случаев, исходы беременности были лучше. Предпочтительным вариантом лечения является трассфеноидальное удаление аденомы гипофиза, при этом варианте наблюдалось более 85% благоприятных перинатальных исходов. Наилучшим временем для проведения операции считается начало II триместра беременности. Еще одним вариантом является медикаментозная терапия, которая назначается во время II и III триместров беременности [17]. При этом препаратом выбора при беременности является метирапон, в то время как кетоконазол обладает тератогенным эффектом и рекомендован только в крайнем случае при непереносимости метирапона [5].
Вне зависимости от гормональной активности опухоли женщинам с макроаденомами гипофиза (более
1 см) во время беременности рекомендована оценка полей зрения для своевременного выявления отрицательной динамики и проведения соответствующего лечения при необходимости [4, 8, 11, 12]. В нашем случае не наблюдалось супраселлярного роста аденомы гипофиза и риск развития хиазмального синдрома на фоне гиперплазии гипофиза во время беременности был минимальным.
Важнейшими параметрами, оказывающими основное влияние на течение беременности как при акромегалии, так и при гиперкортицизме, являются симптоматические нарушения – артериальная гипертензия и сахарный диабет [4, 8, 11, 12].
Динамика симптомов заболевания, а также изолированное снижение ТТГ в дебюте заболевания при небольшой эндоселлярной аденоме гипофиза позволяют предположить, что опухоль исходно продуцировала АКТГ [10]. При этом, исходя из клиники, выраженность гиперкортицизма была незначительной и обнаружить его можно было только при проведении диагностических проб, которые не были выполнены в течение первых 16 (!) лет после выявления аденомы гипофиза. Тем не менее с точки зрения осуществления репродуктивных планов первая беременность была наиболее благоприятной.
Заключение
Таким образом, за время от дебюта заболевания до операции удаления аденомы пациентка дважды беременела. И несмотря на наличие репродуктивных планов, оба раза было принято решение о прерывании беременности. При этом, согласно современным представлениям, наличие гиперпролактинемии и аденомы гипофиза не является противопоказанием для беременности. Более того, в большинстве случаев во время беременности не происходит прогрессирования пролактинсекретирующих опухолей гипофиза [7]. Наличие аденомы гипофиза, секретирующей гормон роста, а тем более АКТГ, является крайне неблагоприятным фоном для развития беременности, однако с учетом существующих способов лечения также не является абсолютным противопоказанием для беременности и родов. При сохранении нарушения функции тиреотрофов со снижением ТТГ на фоне гиперкортицизма при беременности вести пациентку следует исходя из принципов ведения беременных с вторичным гипотиреозом.
У данной пациентки наиболее благоприятным в отношении перинатальных исходов представляется сохранение первой беременности, в период минимальной выраженности артериальной гипертензии и сахарного диабета, ухудшающих прогноз.
Дополнительная информация
Согласие пациентки. Пациентка добровольно подписала информированное согласие на публикацию персональной медицинской информации в обезличенной форме.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Сonflict of interests. The author declares that there is not conflict of interests.
Гусова Анна Аузбиевна – канд. мед. наук, ФГБУ ФНКЦСМ ФМБА России. E-mail: agusova@mail.ru
Anna A. Gusova – Cand. Sci. (Med.), Federal Research and Clinical Center of Sports Medicine and Rehabilitation of the Federal Medical Biological Agency of Russia. Е-mail: agusova@mail.ru
29 декабря 2022
Количество просмотров: 2263

