Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2009
Эффективность современных антипсихотических средств при длительной поддерживающей терапии шизофрении (противорецидивное действие, качество и структура ремиссий) №06 2009
Номера страниц в выпуске:4-13
В основе большинства современных стандартов лечения шизофрении лежит представление о равной эффективности всех антипсихотических средств и их различии только в спектре побочных эффектов. В качестве препаратов выбора предлагается использовать атипичные нейролептики нового поколения, редко вызывающие неврологические расстройства . Традиционные нейролептики рассматриваются как средства второго ряда из-за частого возникновения двигательных нарушений и выраженного затормаживающего действия. Указывается, что клозапин должен использоваться в последнюю очередь (препарат резерва) в связи с возможностью развития ряда осложнений. Несмотря на всю привлекательность идеи, лежащей в основе предложенного подхода (высокая эффективность и хорошая переносимость), представленная дифференцированная схема терапии шизофрении имеет ряд недостатков.
Введение
В основе большинства современных стандартов лечения шизофрении лежит представление о равной эффективности всех антипсихотических средств и их различии только в спектре побочных эффектов [13, 22–25, 30]. В качестве препаратов выбора предлагается использовать атипичные нейролептики нового поколения, редко вызывающие неврологические расстройства [10, 12, 14, 20, 21, 26]. Традиционные нейролептики рассматриваются как средства второго ряда из-за частого возникновения двигательных нарушений и выраженного затормаживающего действия. Указывается, что клозапин должен использоваться в последнюю очередь (препарат резерва) в связи с возможностью развития ряда осложнений.
Несмотря на всю привлекательность идеи, лежащей в основе предложенного подхода (высокая эффективность и хорошая переносимость), представленная дифференцированная схема терапии шизофрении имеет ряд недостатков. Они связаны со «спорностью» некоторых теоретических данных, которые стали основой для ее разработки, и с определенными трудностями ее применения в клинической практике. В последнее время все чаще высказывается мнение о «предварительности» результатов исследований, свидетельствующих о высокой эффективности атипичных нейролептиков [1, 11, 15, 16, 18, 29, 31]. При их приеме часто развиваются побочные эффекты, которые могут представлять серьезную угрозу для здоровья пациентов, значительно ухудшают качество жизни, приводят к стигматизации и несоблюдению медицинских рекомендаций (метаболические и эндокринные нарушения, пируэтная тахикардия) [2, 17, 19, 24, 28, 32, 34]. До сих пор не определены профили избирательного антипсихотического эффекта атипичных нейролептиков, что связано с распространившейся недавно, но весьма спорной точкой зрения о равной эффективности всех нейролептиков и отсутствии «специфичности» их действия [13, 22, 23, 25, 27, 30, 33]. Не проведено сопоставление «специфичности» действия различных атипичных и типичных антипсихотических средств. Все это значительно затрудняет возможность дифференцированного выбора терапии. На практике его часто приходится осуществлять на основании личных предпочтений специалиста, что часто приводит к длительному «перебору» различных препаратов без достижения необходимого терапевтического эффекта.
Необходимо отметить дискутабельность вопроса об отнесении клозапина и высокопотентных традиционных средств к препаратам резерва. Недавно нами было высказано мнение о рациональности использования этих средств у ряда больных уже на ранних стадиях эндогенного процесса даже в ущерб хорошей переносимости лечения [5–8]. Оно основывается на данных сравнительных исследований эффективности различных нейролептиков при основных формах шизофрении, в которых показано, что применение клозапина намного эффективнее, чем терапия другими нейролептиками, особенно атипичными средствами нового поколения [3, 4, 7, 9].
Настоящее исследование является одним из этапов проводимой нами работы, направленной на изучение эффективности атипичных нейролептиков при лечении шизофрении. Его цель состояла в сравнении противорецидивной эффективности, качества и структуры ремиссий при проведении длительной поддерживающей терапии шизофрении клозапином, рисперидоном, оланзапином, кветиапином и высокопотентными типичными нейролептиками.
Материалы и методы
Под длительным амбулаторным наблюдением находились 267 пациентов. Их включали в исследование после завершения купирующей терапии. Из них 97 больных (36,3%) страдали непрерывной параноидной шизофренией, 85 (31,85%) – приступообразной шизофренией (шубообразная, рекуррентная), у 85 (31,85%) больных процесс протекал вяло. Их состояние соответствовало лекарственным ремиссиям различного качества, которое определялось особенностями заболевания и индивидуальной эффективностью предшествующей купирующей терапии. Наблюдались случаи как практически полного отсутствия продуктивной симптоматики, так и ее большой выраженности.
Все пациенты были разделены на 5 групп. Все группы были сопоставимы по демографическим характеристикам. Количество наблюдений в первых 3 группах составило 80, 69 и 67. Первые 3 группы были сопоставимы по числу больных с различными формами шизофрении. В 1-й группе было 27 случаев непрерывной параноидной шизофрении, 31 случай шизофрении, протекающей приступообразно, и 22 случая вялотекущей шизофрении. Во 2-й группе таких наблюдений было 20, 29 и 20 соответственно. В 3-й группе число больных с этими формами заболевания составило 20, 25 и 22. В 4-ю группу вошел 21 пациент, страдающий только вялотекущей шизофренией, а 5-я группа состояла из 30 больных параноидной шизофренией.
Всем больным назначали поддерживающую антипсихотическую терапию – клозапином (1-я группа), рисперидоном (2-я группа), оланзапином (3-я группа), кветиапином (4-я группа) или традиционными нейролептиками (5-я группа). Пациенты продолжали принимать тот нейролептик, которым проводилась предшествующая купирующая терапия. Дозы подбирали индивидуально с учетом тяжести состояния и его динамики. Дозы клозапина составляли от 25 до 500 мг/сут, рисперидона (per os) – от 0,5 до 6 мг/сут, микросфер рисперидона – от 25 до 50 мг в 2 нед, оланзапина – от 2,5 до 25 мг/сут, кветиапина – от 25 до 400 мг/сут, галоперидола (per os) – от 10 до 30 мг/сут, галоперидол-деканоата – от 50 до 150 мг в 3–4 нед, трифлуоперазина – от 15 до 25 мг/сут, флуфеназин-деканоата – от 25 до 50 мг в 2 нед. Поддерживающую терапию обычно проводили амбулаторно. В отдельных случаях допускали госпитализацию больных по социальным показаниям.
Обследование больных проводили комплексно с использованием традиционных способов оценки состояния и методов, основанных на принципах доказательной медицины. Состояние больных оценивали клиническим методом и при помощи стандартизированных шкал (PANSS). Длительность наблюдения составила 3 года. Развитие при приеме поддерживающей терапии обострения (острого приступа) болезни рассматривали в качестве критерия исключения из дальнейшего наблюдения.
Статистический анализ полученных данных проводили при помощи методов параметрической (расчет 95% доверительного интервала) и непараметрической (c2, c2 с поправкой Йетса, метод Фишера) статистики.
Результаты
Повторные обострения в обследованной группе развивались в течение всего периода наблюдения (табл. 1).
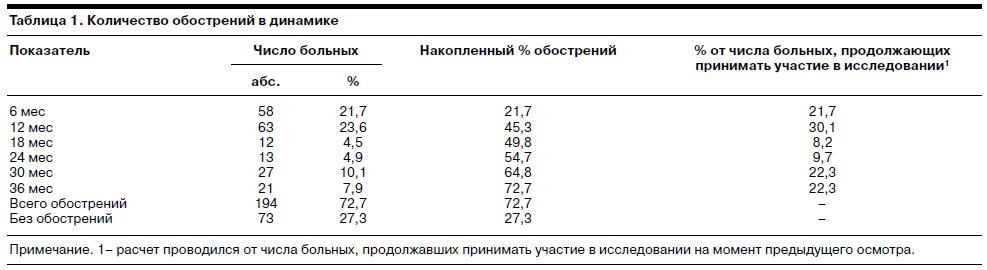
В течение 1-го года амбулаторной терапии их частота была максимальной, а именно: 21,7% через 6 мес и 23,6% через 12 мес (от общего числа больных). В течение 2-го года наблюдения частота обострений значительно снижалась. Через 18 и 24 мес ухудшение состояния наблюдали у 4,5 и 4,9% пациентов. Затем количество рецидивов вновь возрастало: 10,1 и 7,9% через 30 и 36 мес. Иными словами, через год после начала амбулаторного лечения устойчивые ремиссии сохранялись в 54,7%, через 2 года – в 45,3% и через 3 года – только в 27,3% случаев.
В табл. 1 также приведен показатель частоты обострений от числа больных, продолжавших принимать участие в исследовании. Его использование при описании полученных результатов, особенно при сравнении относительных частот в группах больных, принимавших различные нейролептики, представляется методически более правильным, чем применение показателей «% от исходного количества больных» или «накопленный % больных». Это связано с тем, что развитие обострений болезни при проведении поддерживающей терапии рассматривали в качестве одного из критериев исключения больных из исследования (неэффективность лечения). В этом случае возникала необходимость пересмотра схемы лечения с возобновлением купирующей терапии и больного исключали из дальнейшего статистического сравнения. Поэтому показатель «доля больных от их числа, продолжающих принимать участие в исследовании» часто будет использоваться при дальнейшем анализе полученных данных.
При оценке частоты обострений при приеме разных нейролептиков были выявлены значительные различия (табл. 2).
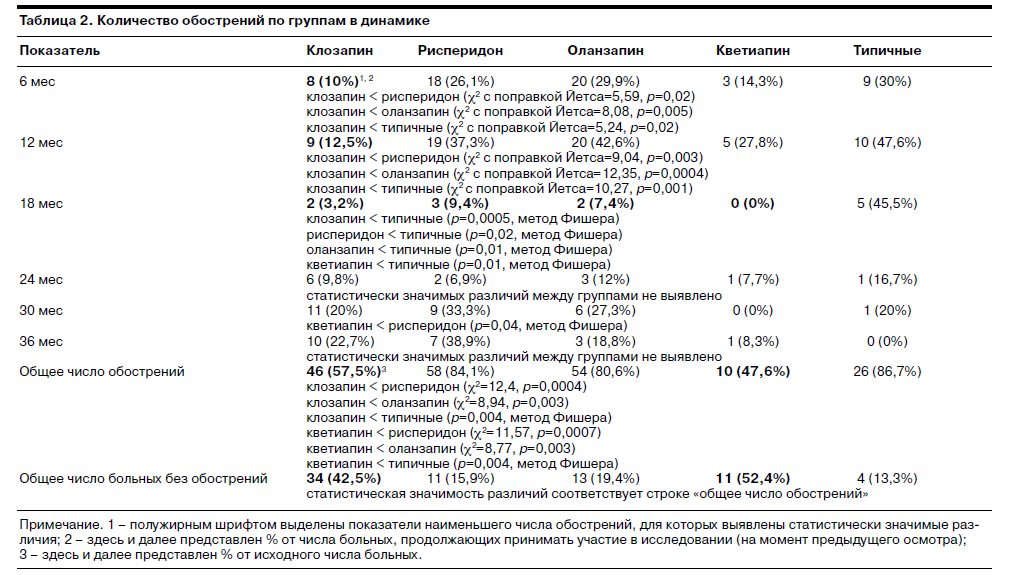
Необходимо оговориться, что представленная в табл. 2 статистически значимая разница является безоговорочной только в отношении групп больных, принимавших клозапин, рисперидон и оланзапин, поскольку они были сопоставимы по представленности основных форм заболевания (параноидная, шубообразная и рекуррентная, вялотекущая). Статистически значимая разница по сравнению с группами пациентов, которым был рекомендован прием кветиапина и типичных нейролептиков, условна, поскольку к ним относились соответственно только случаи вялотекущей и параноидной шизофрении. Это приводило к фактической несопоставимости этих групп между собой и с другими группами.
Более показательно сравнение эффективности терапии при отдельных формах заболевания. При параноидной шизофрении наибольшая длительность ремиссий достигалась при приеме клозапина, особенно на ранних сроках амбулаторного лечения (табл. 3). Эффективность рисперидона и оланзапина была примерно сопоставимой. Применение высокопотентных типичных нейролептиков чаще приводило к формированию длительных ремиссий, чем рисперидона. Статистически значимые различия между группами были выявлены в течение первых 18 мес наблюдения. Через 6 мес частота обострений при приеме клозапина была статистически значимо меньшей (7,4%), чем при лечении рисперидоном (40%), оланзапином (50%) и типичными средствами (30%). Спустя 12 мес наблюдения состояние пациентов, лечившихся клозапином, также ухудшалось значительно реже (8%), чем при терапии рисперидоном (91,7%), оланзапином (70%) и традиционными нейролептиками (47,6%). В этот период прием типичных нейролептиков был более эффективен, чем применение рисперидона (47,6% против 91,7%). Через 18 мес статистически значимые различия были выявлены при сравнении групп больных, принимавших клозапин (0%) и рисперидон (100%); клозапин (0%) и типичные нейролептики (45,5%). В дальнейшем различия между группами становились менее выраженными, что проявлялось отсутствием статистически значимой разницы между ними. Группа больных, принимавших рисперидон, через 18 мес наблюдения была полностью исключена из сравнения из-за ухудшения состояния во всех случаях. Примечательно, что наибольшее число обострений при приеме клозапина приходилось на отдаленные этапы ремиссии (3-й год наблюдения), тогда как при лечении другими нейролептиками состояние больных обычно ухудшалось в течение 1-го года. Это означает, что длительность ремиссий при приеме клозапина была значительно продолжительнее, чем при лечении рисперидоном, оланзапином и типичными средствами, что было связано с более высоким качеством ремиссий и лучшим соблюдением режима терапии. За весь период наблюдения частота обострений составила 66,7, 100, 95 и 86,7% соответственно обследованным группам. Интересно, что общее число обострений при сравнении групп больных, принимавших клозапин и типичные нейролептики, типичные нейролептики и рисперидон, было сопоставимым. Однако это не означает равную эффективность этих средств, поскольку статистически значимые различия между группами были выявлены в процессе наблюдения (6, 12 и 18 мес).
Клиническое наблюдение и статистическая обработка полученных данных свидетельствуют, что при шизофрении, протекающей в форме приступов (шубообразная и рекуррентная), наиболее длительные ремиссии также формировались при приеме клозапина (см. табл. 3).
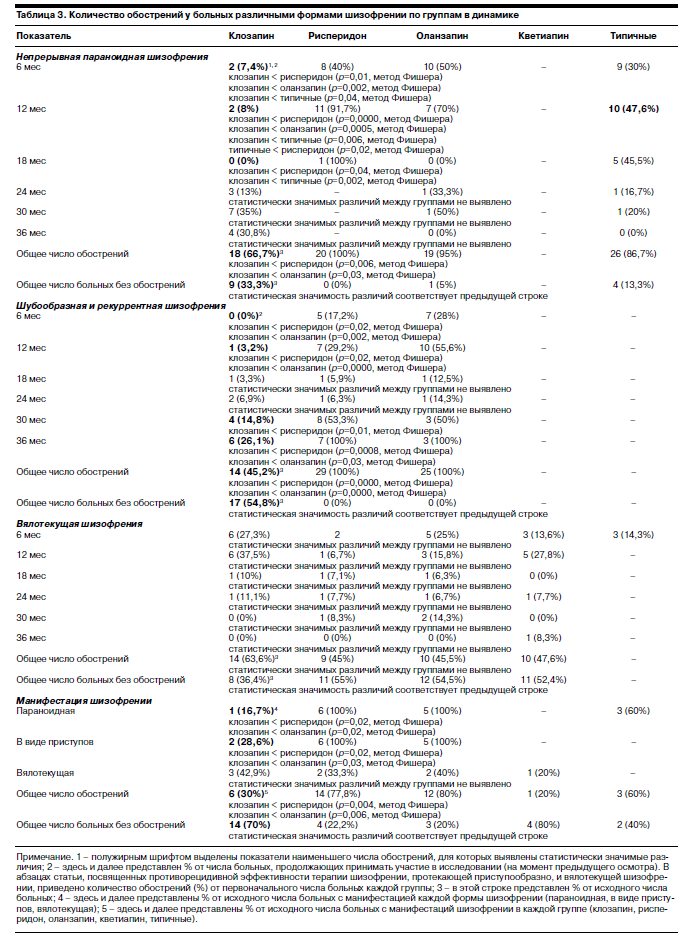
Всего в 3,2% случаев их длительность составила менее 1 года. Через 2 года повторные приступы развились еще у 9,7% больных (от общего их числа в этой группе). В течение 3-го года состояние ухудшалось у 32,3% пациентов. При терапии рисперидоном и оланзапином ремиссии были менее устойчивыми. В течение 1-го года приема этих нейролептиков состояние ухудшалось у 41,4 и 68% пациентов. Через 2 года повторные приступы развивались еще в 6,9 и 8% случаев соответственно. В течение 3-го года повторные психозы наблюдали у 51,7 и 24% больных. За 3-летний период состояние ухудшилось у всех пациентов, принимавших рисперидон (100%) и оланзапин (100%), что значительно превышало количество повторных приступов при приеме клозапина (45,2%). В процессе наблюдения статистически значимые различия между группами были выявлены через 6 и 12, 30 и 36 мес. В течение 2-го года терапии (13–24-й месяцы) частота повторных приступов во всех группах была сопоставимой. Примечательно, что при приеме клозапина наибольшее количество рецидивов наблюдали на поздних сроках ремиссии (в течение 3-го года) обычно из-за появления у больных убежденности в выздоровлении. При приеме других нейролептиков максимальное число обострений отмечено в течение 1-го года после выписки больных из стационара. Это было связано с более низким качеством сформированных ремиссий в этих группах, а значит, с более слабым осознанием пациентами болезненности своего состояния и несоблюдением режима приема лекарств.
При вялотекущей шизофрении в отличие от других форм заболевания частота обострений в течение всего периода наблюдения во всех группах была сопоставимой (см. табл. 3). Ремиссии длительностью менее 1 года были сформированы у 54,5, 30, 27,3 и 38,1% от общего числа больных, принимавших клозапин, рисперидон, оланзапин и кветиапин. Причем в этот период частота обострений во всех группах была максимальной. В течение 2-го года наблюдения состояние ухудшалось еще в 9,1, 10, 9,1 и 4,8% случаев. В течение 3-го года повторные обострения развились у 0, 5, 9,1 и 4,8% больных. За весь период наблюдения устойчивость ремиссии нарушалась у 63,6, 45, 45,5 и 47,6% пациентов, принимавших соответственно клозапин, рисперидон, оланзапин и кветиапин. Несмотря на отсутствие статистически значимых различий между группами, обращает внимание меньшая длительность ремиссий у больных, которым рекомендовался прием клозапина, и высокая частота обострений в этой группе в течение 1-го года амбулаторной терапии. Необходимо подчеркнуть, что эта закономерность не отражала силу «истинной» противорецидивной эффективности клозапина, а была связана с субъективным отношением пациентов к такой терапии. Больные вялотекущей шизофренией, особенно при преобладании ипохондрической и психопатоподобной симптоматики, субъективно тяжело воспринимали даже легкие побочные эффекты, часто развивающиеся при приеме клозапина, нарушали режим терапии, что приводило к ухудшению их состояния. При приеме других атипичных нейролептиков субъективно тягостные побочные эффекты были менее выражены, как следствие пациенты лучше выполняли назначения врача. Это наблюдение свидетельствует о необходимости противопоставления понятий «эффективность лечебного процесса» («эффективность лечения»), которая зависит от целого комплекса факторов, и «эффективность нейролептика», которая отражает мощность антипсихотического эффекта и его спектр.
Прием клозапина при манифестации параноидной шизофрении обеспечивал формирование ремиссий длительностью более 3 лет у 83,3% больных. Напротив, за этот период обострения болезни развивались во всех случаях приема рисперидона и оланзапина. Между группами были выявлены статистически значимые различия. При приеме типичных нейролептиков состояние больных ухудшалось чаще (60%), чем при лечении клозапином (16,7%), и реже, чем при терапии рисперидоном (100%) и оланзапином (100%). Однако эти различия не достигали статистической значимости.
При шизофрении, протекающей в форме приступов, длительность ремиссий у всех больных, принимавших рисперидон и оланзапин, не превышала 3 лет. При лечении клозапином таких больных было значительно меньше – всего 28,6%. Между группами выявлены статистически значимые различия.
При вялотекущей шизофрении количество обострений в течение 3 лет было сопоставимым во всех группах и составило 42,9, 33,3, 40 и 20% соответственно.
Необходимо отметить, что эффективность поддерживающей терапии зависела не только от особенностей лечения, но, безусловно, и от особенностей патологического процесса. Это доказывалось тем, что на ранних сроках ремиссии обострения при непрерывной параноидной и вялотекущей шизофрении развивались чаще, чем при ее приступообразном течении (табл. 4).
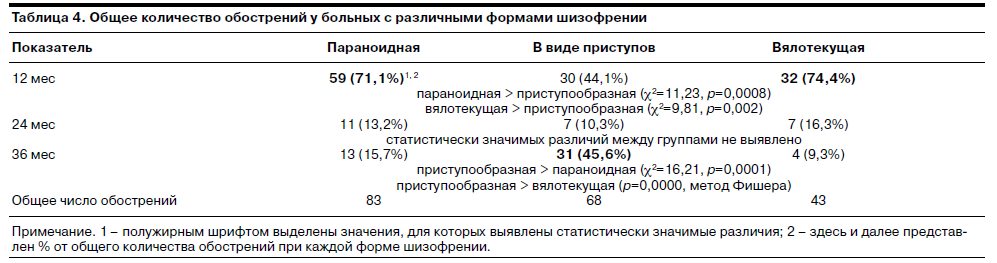
Это было связано с более тяжелым протеканием непрерывных форм по сравнению с приступообразными (худшее качество ремиссий, меньшее осознание пациентами болезненности состояния, большая распространенность отсутствия терапевтического сотрудничества). При шубообразной и рекуррентной шизофрении большинство обострений развивалось на отдаленных этапах ремиссии (3-й год наблюдения).
Как было отмечено, в течение 1-го года наблюдения при приеме клозапина, рисперидона, оланзапина и типичных нейролептиков обострения параноидной шизофрении развились в 14,8, 95, 85 и 63,3% случаев соответственно. Это привело к утрате сопоставимости групп больных, принимавших разные нейролептики. Поэтому при этой форме заболевания сравнить качество ремиссий в различных группах не удалось. Длительная оценка динамики состояния была проведена только у больных, получавших клозапин. Качество ремиссий изучали у 20 таких пациентов, у которых в течение 2 лет не отмечено развития повторных обострений. Все эти случаи относились к среднепрогредиентному течению эндогенного процесса.
Клиническое наблюдение показало, что после «отзвучания» обострения в период последующей ремиссии непрерывно текущей параноидной шизофрении состояние больных, принимавших клозапин, продолжало улучшаться. Это проявлялось в очень медленном, постепенном ослаблении продуктивной симптоматики. Наблюдали дальнейшую дезактуализацию бредовых идей и психических автоматизмов. Во многих случаях обращало внимание ослабление нарушений стройности мышления. Примечательно, что у некоторых длительно болеющих появлялось сознание болезни, ощущение чуждости или субъективной тягостности переживаний, хотя полноценная критика у них не формировалась. В наиболее тяжелых случаях можно было говорить об «эмоциональной инкапсуляции» продуктивных расстройств, при которой сохранявшиеся переживания все в меньшей степени определяли поведение больных. Пациенты становились безучастными к ним, условно «сторонними наблюдателями».
Стандартизированная оценка доказывала результаты приведенного клинического наблюдения (табл. 5).
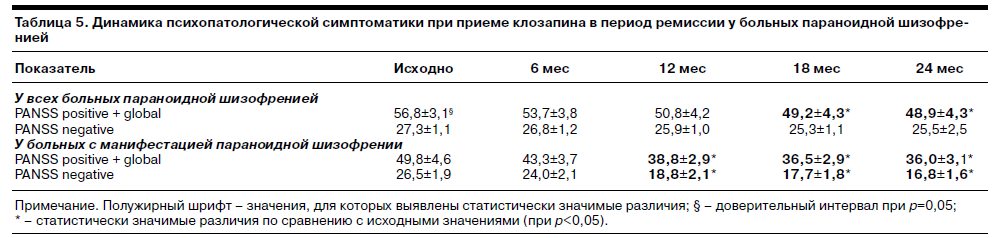
В течение 2 лет отмечено снижение среднего суммарного балла по подшкалам, отражающим продуктивные расстройства. Причем через 18 и 24 мес наблюдения эти различия были статистически значимыми по сравнению с исходным уровнем (р<0,05). В течение 2 лет наблюдения тяжесть продуктивных и негативных расстройств снизилась на 7,9 и 1,8 балла.
Клиническое наблюдение показало, что сформированные у больных параноидной шизофренией ремиссии относились к параноидному, психопатоподобному типу и типу Verschrobene. Таких наблюдений было 12 (60%), 2 (10%) и 6 (30%) соответственно. При параноидном варианте состояние больных определялось переплетением собственно дефицитарной симптоматики в виде эмоционально-волевого обеднения и продуктивных расстройств, проявляющихся бредовыми идеями различной степени выраженности. В легких случаях наблюдали бредовую настроенность в виде подозрительности, настороженности, недоверчивости. Затем шли случаи инкапсулированного или диссимулируемого бреда. В редких случаях при большей тяжести состояния бредовые расстройства были довольно выражены. У всех больных были заметны нарушения стройности мышления. Параноидные ремиссии формировались при активном течении шизофрении длительностью более 1 года – 2 лет и на этапе затухания активности патологического процесса (формирование дефекта). Психопатоподобный (псевдопсихопатический) тип ремиссий проявлялся сочетанием эмоционально-волевого обеднения и психопатоподобной симптоматики в виде легкого возникновения вспышек гнева, возбудимости, взрывчатости, деструктивного поведения, особенно в ответ на субъективно неприятные для больного внешние события, эгоцентризма, дурашливости. Такую картину наблюдали у больных с длительным течением патологического процесса на этапе его «выгорания». При этом симптоматика более высоких регистров (бред, нарушения стройности мышления) могла входить в структуру описываемого симптомокомплекса, но не была определяющей. Пациенты с ремиссиями типа Verschrobene будут описаны чуть ниже.
Довольно интересны данные о динамике состояния больных с манифестацией параноидной шизофрении. Несмотря на то что таких наблюдений было всего 6, полученные результаты важны для понимания закономерностей развития патологического процесса и его чувствительности к лечению. Характеризуя эту группу, необходимо отметить, что ее составили случаи болезни, начавшейся в зрелом возрасте, длительностью течения не более 1 года (на момент начала предшествующей купирующей терапии), с признаками, позволяющими прогнозировать среднюю прогредиентность течения. Длительная терапия клозапином приводила к значительному улучшению состояния таких больных. Это проявлялось в существенном ослаблении психопатологических расстройств (см. табл. 5). При суммарной оценке по подшкалам PANSS positive и PANSS global их тяжесть уменьшилась на 11 и 13,8 балла от исходного уровня через 12 и 24 мес. Терапия клозапином была эффективна в отношении не только продуктивных, но и негативных расстройств, что доказывалось статистически значимыми различиями при их оценке в процессе наблюдения по сравнению с исходным уровнем (р<0,05). Выраженность негативной симптоматики по PANSS negative через 12 и 24 мес снизилась на 7,7 и 9,7 балла. Эти различия значительно превышали средние показатели в группе больных параноидной шизофренией. Обращает внимание, что лечение клозапином манифестации непрерывной параноидной шизофрении и шизофрении, протекающей приступообразно, приводило к тому, что тяжесть психопатологической симптоматики в этих группах больных становилась сопоставимой (сравнение данных табл. 5, 6).
Ремиссии, сформированные спустя 1–2 года после начала терапии у больных с манифестацией параноидной шизофрении, характеризовались довольно высоким качеством с практически полной редукцией психотической симптоматики. Наблюдали лишь бредовую настроенность в виде подозрительности, настороженности, некоторого недоверия. Наиболее отчетливо это проявлялось в общении с окружающими. Больные были критичны к переживаниям, перенесенным во время предшествующего психоза. Выявлялись невыраженные нарушения мышления по эндогенному типу, однако они скорее входили в структуру дефекта, а не текущего процесса. В целом состояние больных можно было расценить как ремиссии типа Verschrobene с полной остановкой прогрессирования болезни на время лечения. Имеющиеся расстройства грубо не нарушали социальную адаптацию больных. Все это свидетельствует, что интенсивная терапия клозапином начального этапа параноидной шизофрении приводит к переходу ее течения из непрерывного в условно приступообразное (лекарственный патоморфоз).
Прежде всего необходимо отметить, что в период ремиссии состояние больных всех групп претерпевало определенную динамику. В первые месяцы при отсутствии признаков остроты состояния больные оставались вялыми, безынициативными, малообщительными. Они были погружены в себя, отстранены от окружающих событий, стремились к уединению. Неохотно общались с окружающими, в том числе с родными. В беседе с врачом молчаливы. Кратко отвечали на вопросы. Предпочитали не обсуждать перенесенный психоз и свое настоящее состояние. На темы, не связанные с болезнью, говорили значительно охотнее. Очерченных симптомов депрессии не выявлялось. Они критично относились к «отзвучавшему» приступу, понимая болезненность своих переживаний во время него, однако недостаточно осознавали тяжесть своего настоящего состояния. Установку на прием лекарств удавалось поддержать только при помощи методов убеждения и косвенного внушения, используемых регулярно во время очередных осмотров, и контроля родных. Однако в течение последующего полугода – года состояние больных улучшалось. Этот процесс протекал крайне инертно. Постепенно больные оживлялись, становились более доступными, расположенными к общению. Они медленно возвращались к повседневному ритму жизни, расширялся круг контактов и интересов. Появлялось желание продуктивной деятельности. Повышалось доверие к врачу и родным. Одновременно изменялось отношение к заболеванию. Пациенты начинали более осмысленно оценивать болезненность перенесенного психоза и своего настоящего состояния. Стремились к сотрудничеству с врачом. Улучшалось настроение. Эти изменения постепенно приводили к восстановлению социальной адаптации больных, являющейся лакмусом их психического состояния. Описанную динамику наблюдали во всех группах, но она была более заметной у больных, принимавших клозапин.
Большой интерес вызывает квалификация психопатологических расстройств, определяющих состояние больных в первые месяцы наблюдения. Необходимо отметить первоначально возникшую трудность их разграничения и определения синдромологической принадлежности. Однако тщательное изучение психического состояния клиническим методом позволяет утверждать, что в большинстве случаев автор сталкивался с переплетением остаточной продуктивной симптоматики и вторичных негативных расстройств, являющихся следствием перенесенного психоза. Описанные симптомы были связанны между собой и с острым периодом болезни, о чем свидетельствовало их гармоничное ослабление и корреляция уменьшения их тяжести с углублением осознания болезненности перенесенных переживаний. Нельзя не упомянуть и об определенной роли в развитии этих расстройств психотравмирующих факторов. Осознание своего нездоровья и внешняя стигматизация у некоторых больных, особенно с манифестным или «вторым» психозом, выступали в качестве сильных психологических факторов, ухудшающих их состояние. Такое же значение имело появление ощущения несостоятельности у недостаточно компенсированных больных в условиях повышенных требований повседневной жизни. Поскольку точно оценить степень патопластического взаимодействия психогенно спровоцированной симптоматики с процессуальными расстройствами на начальном этапе ремиссии довольно сложно, для описания случаев, при которых их значение для состояния больного не вызывает сомнений, возможно рационально использовать термин «эндореактивная симптоматика начального периода ремиссии».
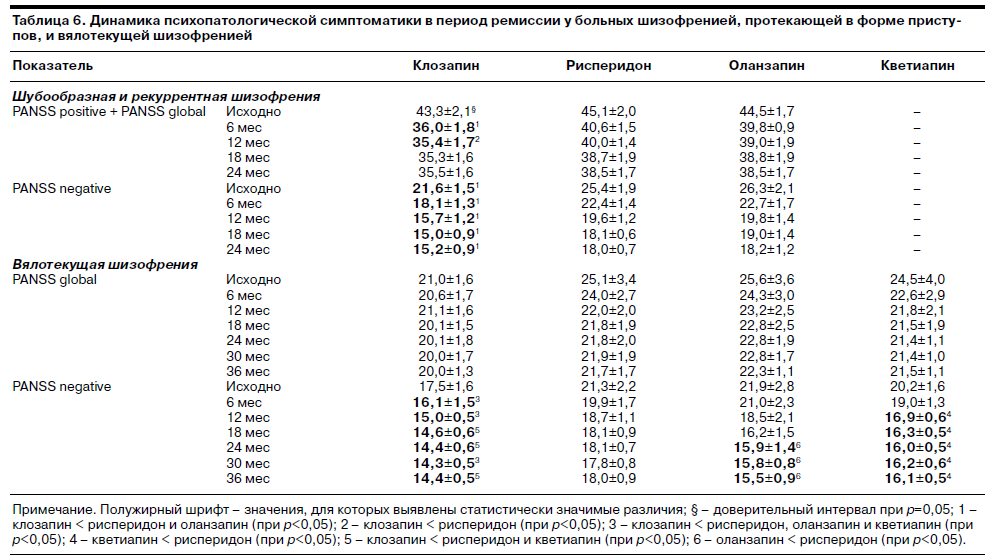
Представленные данные клинического наблюдения были подтверждены стандартизированной оценкой состояния больных. Через 6 мес наблюдения тяжесть продуктивных расстройств при приеме клозапина, рисперидона и оланзапина у больных шизофренией, протекающей приступообразно, снизилась на 7,3, 4,5 и 4,7 балла, через 12 мес – на 7,9, 5,1 и 5,5 балла по сравнению с исходным уровнем (см. табл. 6). В дальнейшем состояние пациентов оставалось относительно стабильным. Описанные изменения касались в основном лишь одного психотического симптома PANSS positive – «концептуальная дезорганизация» мышления и многих симптомов невротического регистра PANSS global – «напряженность», «манерность и поза», «депрессия», «моторная заторможенность», «отказ от сотрудничества», «нарушения внимания», «снижение критичности и осознания болезни», «нарушения воли», «активная социальная устраненность». Снижение тяжести негативных расстройств по подшкале PANSS negative при приеме клозапина, рисперидона и оланзапина составило 3,5, 3, 3,6 балла и 5,9, 5,8, 6,5 балла через 6 и 12 мес по сравнению с исходным уровнем. В дальнейшем значительных изменений не выявлено. Корреляция снижения тяжести остаточной продуктивной симптоматики и негативных расстройств в течение 1-го года ремиссии подтверждает их патогенетическое единство в этот период.
Сравнение эффективности терапии в различных группах показало, что через 6 мес прием клозапина приводил к большему ослаблению продуктивных расстройств, чем лечение другими атипичными нейролептиками (см. табл. 6). Через 12 мес статистически значимые различия выявлялись при сравнении этой группы больных только с пациентами, принимавшими рисперидон. В дальнейшем эта разница уже не достигала статистической значимости. Эффективность терапии рисперидоном и оланзапином была сопоставимой в течение всего периода наблюдения. Это свидетельствует о более быстром наступлении терапевтического эффекта при приеме клозапина при равной эффективности всех нейролептиков в целом. Учитывая длительность процесса формирования ремиссии, высокая скорость наступления положительного эффекта имеет большое практическое значение.
Терапия клозапином также была более эффективна в отношении негативных расстройств. Различия между группами выявлялись уже исходно (см. табл. 6) вследствие большей эффективности клозапина при лечении острых психозов, что приводило к меньшей выраженности вторичных негативных расстройств на момент завершения купирующей терапии. Это наблюдение отражает взаимосвязь эффективности купирующей нейролептической терапии и качества последующей ремиссии. В течение всего 2-летнего периода различия между группами сохранялись. Необходимо уточнить, что полученные в сравнительной части исследования данные об эффективности различных нейролептиков несколько условны, поскольку изначально группы не были сопоставимы по численности, а длительная непрерывная терапия оланзапином проведена лишь в 6 случаях.
Прежде чем перейти к описанию типологии ремиссий при приступообразной шизофрении, важно отметить, что их варианты определялись автором спустя длительный срок (годы) после начала их формирования. К этому времени происходила окончательная психопатологическая консолидация ремиссионного состояния и нивелировка нейролептического синдрома, который на более ранних этапах мог затруднять правильную верификацию психического статуса. Например, в период купирующей и на начальных этапах поддерживающей терапии прием нейролептиков вызывал развитие астении, заторможенности, аспонтанности. Эти расстройства были формально схожи с астеническим или апатическим симптомокомплексом в структуре соответствующих типов ремиссий, но по сути (патогенетически) ничего общего с ними не имели. Поэтому оценка структуры ремиссии в это время была бы ошибочна.
Длительное клиническое наблюдение показало, что в группе больных шизофренией, протекающей в виде приступов, формировалось 3 типа ремиссий. При лечении клозапином преобладали ремиссии простой структуры, соответствующие их апатическому (аутистическому) варианту (21 наблюдение – 77,8%). В этих случаях состояние больных определялось эмоционально-волевым обеднением, степень выраженности которого, однако, у различных больных была неодинакова и зависела от длительности болезни. Дополнительная симптоматика, которая могла присутствовать в структуре симптомокомплекса у таких больных, была настолько слаба, что не определяла их состояния. Это наблюдение доказывало высокую эффективность клозапина и свидетельствовало о хорошем «отщеплении» продуктивной симптоматики, приближении состояния больных к «чистому» дефекту. В 4 (14,8%) случаях наблюдали становление астенических ремиссий в виде повышенной утомляемости, снижения психического тонуса. Состояние 2 (7,4%) больных было расценено как ремиссии, приближающиеся к параноидным. Эти случаи относились к длительному течению шизофрении с большим количеством приступов в анамнезе. Причем в структуре таких ремиссий преобладал не бред, а нарушения ассоциативного процесса.
В группе больных, принимавших рисперидон, преобладали астенические ремиссии. Таких наблюдений было 11 (73,3%). Их структура отличалась от аналогичных ремиссий, сформированных при лечении клозапином, большей выраженностью психической истощаемости и эмоционально-волевого снижения. Также у больных, принимавших рисперидон, в структуре астенических ремиссий был более выражен депрессивно-ипохондрический компонент в виде фиксации на тяжести своего состояния и ощущения его бесперспективности. У 2 (13,3%) больных наблюдали формирование ремиссий с преобладанием нарушений мышления (параноидный тип). Апатическая и психопатоподобная ремиссии были сформированы у 2 больных (6,7 и 6,7% соответственно).
Длительный прием оланзапина приводил к формированию ремиссий, по структуре приближающихся к апатическим (100%). Возможно, такая однородность их структуры в этой группе больных была связана с малочисленностью изученной выборки.
Статистическое сравнение числа больных с различными типами ремиссий в разных группах показало, что при лечении клозапином чаще формировался их апатический тип (р=0,0000, метод Фишера), а при терапии рисперидоном – астенический вариант (р=0,0004, метод Фишера). Остальные различия между группами, выявляемые при статистическом анализе полученных данных, мы считаем недостоверными из-за небольшого количества наблюдений.
Необходимо подчеркнуть, что одновременно с выявленными различиями эффективности атипичных нейролептиков при приступообразной шизофрении полученные данные позволяют сделать вывод, который важен для понимания динамики, развития шизофренического процесса. В течение года после отзвучания острых проявлений психоза состояние больных было довольно неустойчивым. С одной стороны, наблюдали медленное, инертное ослабление остаточных продуктивных расстройств и вторичной негативной симптоматики, «консолидацию» критики. С другой стороны, очень высокой была частота развития повторных приступов болезни, связанных с нарушением режима терапии из-за еще недостаточного осознания пациентами болезненности своего настоящего состояния. Поэтому этот период, на наш взгляд, является «переходным» от психоза к ремиссии. Причем его можно рассматривать либо как завершающий этап шуба, либо как начало становления ремиссии. В наших наблюдениях наибольшая эффективность лечения в это время отмечена при продолжении интенсивной нейролептической терапии, часто той, которая использовалась в период острого состояния. Значительное снижение дозировки нейролептика в это время или его замена на средство меньшей мощности приводило к ухудшению состояния. Это наблюдение позволяет нам высказать мнение, что описанный переходный период правильнее рассматривать как завершение острого приступа болезни (шуба) с необходимостью продолжения терапии, соответствующей острому состоянию. Начало же ремиссии целесообразно относить к периоду «отзвучания» остаточных продуктивных и вторичных негативных расстройств, т.е. примерно спустя полгода – год после купирования острой психотической симптоматики. Лишь после этого можно оценивать ее качество, делать вывод о ее структуре и тяжести сформировавшегося дефекта.
Относительно невысокая частота развития обострений вялотекущей шизофрении (по сравнению с параноидной и приступообразной) позволила изучить эффективность длительной поддерживающей терапии этой формы заболевания в течение 3 лет. Количество наблюдений составило 8, 11, 12 и 11 при приеме клозапина, рисперидона, оланзапина и кветиапина соответственно.
Стандартизированную оценку продуктивной симптоматики проводили по подшкале PANSS global, поскольку именно она включает в себя симптомы, отражающие состояние больных этой формой шизофрении. В течение всего периода наблюдения значительных различий между группами в выраженности продуктивных расстройств невротического регистра не выявлено (см. табл. 6). Во всех группах в течение 1-го года терапии наблюдали слабоположительную динамику без статистически значимых различий по сравнению с исходным уровнем. Также обращает внимание постепенное сокращение границ доверительных интервалов, означающее уменьшение различий тяжести состояния больных в каждой из групп.
Различия между группами были вывлены при стандартизированной оценке негативной симптоматики по шкале PANSS negative (см. табл. 6). В течение всего периода наблюдения терапия клозапином была более эффективна, чем применение рисперидона и кветиапина, а через 6, 12 и 30 мес его прием приводил к большему ослаблению негативных расстройств, чем лечение оланзапином. Через 12 мес поддерживающей терапии и вплоть до окончания наблюдения терапия кветиапином была более эффективна, чем применение рисперидона. И наконец, прием оланзапина приводил к большему улучшению состояния больных, чем лечение рисперидоном, через 24, 30 и 36 мес наблюдения. Во всех группах состояние больных улучшалось настолько, что эта разница достигала статистической значимости по сравнению с исходным уровнем. Такое наблюдение свидетельствовало о высокой эффективности всех атипичных нейролептиков при лечении вялотекущей шизофрении.
Результаты тщательного клинического наблюдения несколько отличались от данных приведенной стандартизированной оценки. Оно показало различие эффективности атипичных нейролептиков в период ремиссии вялотекущей шизофрении в отношении продуктивных расстройств. Такое несоответствие было связано с «мягкостью» этих различий, не улавливаемых стандартизированными шкалами, но определяемых при регулярном тщательном клиническом обследовании.
Различия эффективности атипичных нейролептиков прежде всего касались симптомов эндогенного круга. При лечении клозапином, оланзапином и кветиапином реже возникали аутохтонные аффективные колебания по типу кратковременных неглубоких субдепрессий или реакций сниженного настроения и экзальтации. У больных, принимавших клозапин, реже наблюдались транзиторные обострения психопатоподобной симптоматики, астеноипохондрические и деперсонализационные расстройства. Напротив, при лечении рисперидоном больные были склонны к их развитию. При применении клозапина, оланзапина и кветиапина реже наблюдали усиление тревожной симптоматики. Клиническое наблюдение также свидетельствовало о различии эффективности терапии в отношении негативных расстройств. Терапия оланзапином и особенно клозапином была эффективной в отношении нарушений мышления по эндогенному типу, впрочем, выраженных у наших больных неярко. Напротив, применение рисперидона и кветиапина практически не влияло на эти расстройства. При лечении клозапином и кветиапином наблюдали большую активизацию больных и оживление эмоциональных реакций, чем при лечении оланзапином и особенно рисперидоном.
Особый интерес вызывает различие эффективности атипичных нейролептиков при ситуационно обусловленных психогенных расстройствах, легко развивающихся у больных вялотекущей шизофренией, особенно при небольшой давности процесса. При лечении оланзапином, кветиапином и особенно клозапином значительно реже, чем при терапии рисперидоном, наблюдали ситуационно обусловленные истероэксплозивные реакции в виде вспышек гнева, деструктивного поведения. В случае же их развития они были кратковременными и не столь выраженными, как у больных, принимавших рисперидон. Указанные различия между группами прослеживались и в отношении тревожных расстройств, развивающихся в ответ на внешние события. При лечении клозапином, оланзапином и особенно кветиапином значительно реже наблюдали неглубокие ситуационно спровоцированные аффективные расстройства в виде истеросубдепрессивных и субдепрессивных реакций. Напротив, при лечении рисперидоном наблюдали легкость возникновения эпизодов подавленного настроения. Наиболее отчетливо эти различия наблюдали в период наибольшей неустойчивости состояния больных в течение 1-го года наблюдения.
Клиническое обследование больных позволило определить типы сформированных ремиссий при вялотекущей шизофрении. При лечении клозапином наблюдали апатические (7 наблюдений – 87,5%) и астенические ремиссии (1 наблюдение – 12,5%). При лечении рисперидоном в 6 (54,5%) случаях ремиссии характеризовались преобладанием истощаемости (астенический тип). У 4 (36,4%) больных наблюдали их тимопатический вариант. В 1 (9,1%) случае преобладало эмоционально-волевое снижение (апатический тип). При лечении оланзапином у равного числа больных (по 6 наблюдений – 50%) отмечено формирование апатических и астенических ремиссий. Становление ремиссий при приеме кветиапина чаще соответствовало апатическому типу (8 больных – 72,7%) и реже астеническому (3 больных – 27,3%).
Учитывая немногочисленность наблюдений больных с различными вариантами ремиссий, нельзя с уверенностью говорить о различии групп по тому или иному варианту, но все же необходимо отметить некоторые особенности. При лечении клозапином преобладал апатический вариант ремиссии, тогда как при терапии рисперидоном – астенический тип, хотя эта разница не была статистически значимой. У больных, принимавших рисперидон, отмечены случаи тимопатических ремиссий, не выявленные в других группах, что лишний раз свидетельствует о недостаточной эффективности этой терапии в отношении аффективных расстройств. В проведенном исследовании не выявлено ни одного случая психопатоподобного или обсессивного варианта ремиссий, часто описываемых при вялотекущей шизофрении, что может быть связано с отсутствием в выборке для длительного наблюдения больных с психопатоподобной формой заболевания из-за развития у них обострений в пределах 3-летнего периода. Автор наблюдал легкие обсессии в структуре ремиссий, но они отнюдь не определяли состояния больных в такой степени, что можно было говорить об обсессивном типе ремиссионного состояния. Возможно, это было связано с тем, что сформированные ремиссии у обследованных больных были довольно качественными. Наконец, необходимо подчеркнуть, что при приеме клозапина явно прослеживалось его седативное действие. Однако оно не ухудшало качество ремиссионного состояния, а, напротив, «страховало» больных от тревоги (анксиолитический компонент) и переутомления (снотворный компонент), что и определяло редкость возникновения тревожных расстройств и астенического варианта ремиссий. Это наблюдение было справедливо и для больных приступообразной шизофренией, принимавших клозапин.
Заключение
Проведенное исследование позволяет сделать следующие выводы. Обострения шизофрении могут развиваться на любом этапе амбулаторного приема нейролептиков. Однако ухудшение состояния наиболее вероятно в течение 1 и 3-го годов лечения. В целом противорецидивная эффективность нейролептической терапии наиболее высока, особенно на ранних сроках ремиссии, при применении клозапина и значительно ниже при назначении рисперидона и оланзапина.
Применение клозапина при непрерывной параноидной шизофрении приводит к формированию ремиссий наибольшей длительности. Частота обострений, особенно в течение 1-го года лечения, значительно ниже, чем при терапии рисперидоном, оланзапином и типичными средствами. Назначение традиционных нейролептиков в период поддерживающей терапии несколько более эффективно, чем применение рисперидона. Наибольший риск обострений при лечении клозапином отмечается в течение 3-го года его приема, тогда как при терапии рисперидоном, оланзапином и типичными нейролептиками – в течение первых 12 мес.
Сходные результаты получены при изучении противорецидивной эффективности атипичных нейролептиков при поддерживающей терапии шизофрении, протекающей в форме приступов. Применение клозапина приводит к формированию ремиссий наибольшей длительности. В течение 3 лет рецидивы развиваются у всех больных, принимающих рисперидон и оланзапин, и менее чем у половины пациентов, получающих клозапин. Наибольший риск обострений при лечении клозапином отмечен в течение 3-го года его приема, тогда как при терапии рисперидоном, оланзапином и типичными нейролептиками – в течение первых 12 мес.
При вялотекущей шизофрении частота обострений при лечении клозапином, рисперидоном, оланзапином и кветиапином примерно сопоставима. Максимальный риск ухудшения состояния при приеме всех нейролептиков отмечается в течение 1-го года терапии и более высок при применении клозапина.
Представленные выше различия справедливы в случаях манифестаций различных форм шизофрении. При параноидной и приступообразной формах наиболее эффективно применение клозапина, тогда как при вялотекущей шизофрении эффективность различных нейролептиков примерно сопоставима.
После завершения купирующей терапии («отзвучание» наиболее острых проявлений психоза в рамках обострений или острых приступов шизофрении) длительный прием поддерживающей терапии приводит к дальнейшему медленному улучшению состояния больных. Такая динамика наблюдается при различных формах шизофрении. Она проявляется ослаблением «остаточных» продуктивных и вторичных негативных расстройств, а также психогенной симптоматики периода адаптации. Состояние больных максимально улучшается спустя полгода – год (и даже позже) после купирования обострения заболевания. После завершения этого периода происходит консолидация ремиссии, окончательно формируется ее структура (т.е. структура дефекта!), максимально восстанавливается социальная адаптация. Полученные данные свидетельствуют, что описанный период неустойчивого состояния (полгода – год) патогенетически более близок к этапу обострения шизофрении, чем к периоду ремиссии. Наиболее отчетливо это прослеживается при шизофрении, протекающей приступообразно.
Особенности изученной выборки больных позволили сравнить эффективность длительного приема различных атипичных нейролептиков при шизофрении, протекающей в форме приступов, и вялом течении заболевания.
При шубообразной и рекуррентной шизофрении долгосрочная эффективность клозапина, рисперидона и оланзапина в отношении продуктивных расстройств сопоставима. Однако при терапии клозапином состояние больных улучшается гораздо быстрее, что имеет большое практическое значение. Применение клозапина более эффективно, чем применение других нейролептиков, при лечении негативной симптоматики.
При вялотекущей шизофрении эффективность клозапина, рисперидона, оланзапина и кветиапина в отношении продуктивной симптоматики примерно сопоставима. Однако различия наблюдаются при сравнении динамики негативных расстройств. В этом случае эффективность терапии убывает в ряду: клозапин – оланзапин, кветиапин – рисперидон.
Эффективность клозапина при непрерывной параноидной шизофрении довольно высока и коррелирует с длительностью заболевания. При его манифестации длительный прием клозапина приводит к значительному ослаблению продуктивных расстройств, иногда вплоть до доболезненного уровня, способствует переходу течения шизофрении из непрерывного в условно приступообразное (лекарственный патоморфоз).
Психопатологическая структура лекарственных ремиссий зависит прежде всего от особенностей патологического процесса. При неблагоприятном течении шизофрении (особенно параноидная форма, некоторые случаи длительного течения шубообразной шизофрении) в структуре ремиссий наряду с негативной симптоматикой ярко выражены продуктивные расстройства (бред, нарушения стройности мышления, психопатизация). При более «мягких» вариантах течения шизофрении структура ремиссий определяется сочетанием негативной симптоматики и продуктивных расстройств невротического регистра (астенический синдром, нарушения поведения, обсессии, колебания настроения).
Терапия различными атипичными нейролептиками вносит значительные особенности в структуру лекарственных ремиссий. Применение клозапина чаще приводит к формированию ремиссий, «бедных» продуктивными расстройствами. Его длительный прием способствует хорошему «отщеплению» продуктивных расстройств, приближению структуры ремиссии к простому апатическому дефекту. Другие типы ремиссий (астенические, параноидные, психопатоподобные и др.) при такой терапии формируются реже, чем при приеме других атипичных нейролептиков. Наиболее отчетливо это прослеживается при шизофрении, протекающей приступообразно. Наиболее благоприятный вариант ремиссий при терапии рисперидоном характеризуется сочетанием симптомов простого дефицита и повышенной истощаемости (астенический вариант ремиссий). Часто в их структуре присутствуют аффективные и ипохондрические включения. Апатические ремиссии при приеме рисперидона формируются редко. Особенности изученной выборки позволили провести анализ структуры ремиссий при приеме оланзапина и кветиапина только у больных вялотекущей шизофренией. Применение этих нейролептиков приводит к формированию как апатических, так и астенических ремиссий.
В основе большинства современных стандартов лечения шизофрении лежит представление о равной эффективности всех антипсихотических средств и их различии только в спектре побочных эффектов [13, 22–25, 30]. В качестве препаратов выбора предлагается использовать атипичные нейролептики нового поколения, редко вызывающие неврологические расстройства [10, 12, 14, 20, 21, 26]. Традиционные нейролептики рассматриваются как средства второго ряда из-за частого возникновения двигательных нарушений и выраженного затормаживающего действия. Указывается, что клозапин должен использоваться в последнюю очередь (препарат резерва) в связи с возможностью развития ряда осложнений.
Несмотря на всю привлекательность идеи, лежащей в основе предложенного подхода (высокая эффективность и хорошая переносимость), представленная дифференцированная схема терапии шизофрении имеет ряд недостатков. Они связаны со «спорностью» некоторых теоретических данных, которые стали основой для ее разработки, и с определенными трудностями ее применения в клинической практике. В последнее время все чаще высказывается мнение о «предварительности» результатов исследований, свидетельствующих о высокой эффективности атипичных нейролептиков [1, 11, 15, 16, 18, 29, 31]. При их приеме часто развиваются побочные эффекты, которые могут представлять серьезную угрозу для здоровья пациентов, значительно ухудшают качество жизни, приводят к стигматизации и несоблюдению медицинских рекомендаций (метаболические и эндокринные нарушения, пируэтная тахикардия) [2, 17, 19, 24, 28, 32, 34]. До сих пор не определены профили избирательного антипсихотического эффекта атипичных нейролептиков, что связано с распространившейся недавно, но весьма спорной точкой зрения о равной эффективности всех нейролептиков и отсутствии «специфичности» их действия [13, 22, 23, 25, 27, 30, 33]. Не проведено сопоставление «специфичности» действия различных атипичных и типичных антипсихотических средств. Все это значительно затрудняет возможность дифференцированного выбора терапии. На практике его часто приходится осуществлять на основании личных предпочтений специалиста, что часто приводит к длительному «перебору» различных препаратов без достижения необходимого терапевтического эффекта.
Необходимо отметить дискутабельность вопроса об отнесении клозапина и высокопотентных традиционных средств к препаратам резерва. Недавно нами было высказано мнение о рациональности использования этих средств у ряда больных уже на ранних стадиях эндогенного процесса даже в ущерб хорошей переносимости лечения [5–8]. Оно основывается на данных сравнительных исследований эффективности различных нейролептиков при основных формах шизофрении, в которых показано, что применение клозапина намного эффективнее, чем терапия другими нейролептиками, особенно атипичными средствами нового поколения [3, 4, 7, 9].
Настоящее исследование является одним из этапов проводимой нами работы, направленной на изучение эффективности атипичных нейролептиков при лечении шизофрении. Его цель состояла в сравнении противорецидивной эффективности, качества и структуры ремиссий при проведении длительной поддерживающей терапии шизофрении клозапином, рисперидоном, оланзапином, кветиапином и высокопотентными типичными нейролептиками.
Материалы и методы
Под длительным амбулаторным наблюдением находились 267 пациентов. Их включали в исследование после завершения купирующей терапии. Из них 97 больных (36,3%) страдали непрерывной параноидной шизофренией, 85 (31,85%) – приступообразной шизофренией (шубообразная, рекуррентная), у 85 (31,85%) больных процесс протекал вяло. Их состояние соответствовало лекарственным ремиссиям различного качества, которое определялось особенностями заболевания и индивидуальной эффективностью предшествующей купирующей терапии. Наблюдались случаи как практически полного отсутствия продуктивной симптоматики, так и ее большой выраженности.
Все пациенты были разделены на 5 групп. Все группы были сопоставимы по демографическим характеристикам. Количество наблюдений в первых 3 группах составило 80, 69 и 67. Первые 3 группы были сопоставимы по числу больных с различными формами шизофрении. В 1-й группе было 27 случаев непрерывной параноидной шизофрении, 31 случай шизофрении, протекающей приступообразно, и 22 случая вялотекущей шизофрении. Во 2-й группе таких наблюдений было 20, 29 и 20 соответственно. В 3-й группе число больных с этими формами заболевания составило 20, 25 и 22. В 4-ю группу вошел 21 пациент, страдающий только вялотекущей шизофренией, а 5-я группа состояла из 30 больных параноидной шизофренией.
Всем больным назначали поддерживающую антипсихотическую терапию – клозапином (1-я группа), рисперидоном (2-я группа), оланзапином (3-я группа), кветиапином (4-я группа) или традиционными нейролептиками (5-я группа). Пациенты продолжали принимать тот нейролептик, которым проводилась предшествующая купирующая терапия. Дозы подбирали индивидуально с учетом тяжести состояния и его динамики. Дозы клозапина составляли от 25 до 500 мг/сут, рисперидона (per os) – от 0,5 до 6 мг/сут, микросфер рисперидона – от 25 до 50 мг в 2 нед, оланзапина – от 2,5 до 25 мг/сут, кветиапина – от 25 до 400 мг/сут, галоперидола (per os) – от 10 до 30 мг/сут, галоперидол-деканоата – от 50 до 150 мг в 3–4 нед, трифлуоперазина – от 15 до 25 мг/сут, флуфеназин-деканоата – от 25 до 50 мг в 2 нед. Поддерживающую терапию обычно проводили амбулаторно. В отдельных случаях допускали госпитализацию больных по социальным показаниям.
Обследование больных проводили комплексно с использованием традиционных способов оценки состояния и методов, основанных на принципах доказательной медицины. Состояние больных оценивали клиническим методом и при помощи стандартизированных шкал (PANSS). Длительность наблюдения составила 3 года. Развитие при приеме поддерживающей терапии обострения (острого приступа) болезни рассматривали в качестве критерия исключения из дальнейшего наблюдения.
Статистический анализ полученных данных проводили при помощи методов параметрической (расчет 95% доверительного интервала) и непараметрической (c2, c2 с поправкой Йетса, метод Фишера) статистики.
Результаты
Повторные обострения в обследованной группе развивались в течение всего периода наблюдения (табл. 1).

В течение 1-го года амбулаторной терапии их частота была максимальной, а именно: 21,7% через 6 мес и 23,6% через 12 мес (от общего числа больных). В течение 2-го года наблюдения частота обострений значительно снижалась. Через 18 и 24 мес ухудшение состояния наблюдали у 4,5 и 4,9% пациентов. Затем количество рецидивов вновь возрастало: 10,1 и 7,9% через 30 и 36 мес. Иными словами, через год после начала амбулаторного лечения устойчивые ремиссии сохранялись в 54,7%, через 2 года – в 45,3% и через 3 года – только в 27,3% случаев.
В табл. 1 также приведен показатель частоты обострений от числа больных, продолжавших принимать участие в исследовании. Его использование при описании полученных результатов, особенно при сравнении относительных частот в группах больных, принимавших различные нейролептики, представляется методически более правильным, чем применение показателей «% от исходного количества больных» или «накопленный % больных». Это связано с тем, что развитие обострений болезни при проведении поддерживающей терапии рассматривали в качестве одного из критериев исключения больных из исследования (неэффективность лечения). В этом случае возникала необходимость пересмотра схемы лечения с возобновлением купирующей терапии и больного исключали из дальнейшего статистического сравнения. Поэтому показатель «доля больных от их числа, продолжающих принимать участие в исследовании» часто будет использоваться при дальнейшем анализе полученных данных.
При оценке частоты обострений при приеме разных нейролептиков были выявлены значительные различия (табл. 2).

Необходимо оговориться, что представленная в табл. 2 статистически значимая разница является безоговорочной только в отношении групп больных, принимавших клозапин, рисперидон и оланзапин, поскольку они были сопоставимы по представленности основных форм заболевания (параноидная, шубообразная и рекуррентная, вялотекущая). Статистически значимая разница по сравнению с группами пациентов, которым был рекомендован прием кветиапина и типичных нейролептиков, условна, поскольку к ним относились соответственно только случаи вялотекущей и параноидной шизофрении. Это приводило к фактической несопоставимости этих групп между собой и с другими группами.
Более показательно сравнение эффективности терапии при отдельных формах заболевания. При параноидной шизофрении наибольшая длительность ремиссий достигалась при приеме клозапина, особенно на ранних сроках амбулаторного лечения (табл. 3). Эффективность рисперидона и оланзапина была примерно сопоставимой. Применение высокопотентных типичных нейролептиков чаще приводило к формированию длительных ремиссий, чем рисперидона. Статистически значимые различия между группами были выявлены в течение первых 18 мес наблюдения. Через 6 мес частота обострений при приеме клозапина была статистически значимо меньшей (7,4%), чем при лечении рисперидоном (40%), оланзапином (50%) и типичными средствами (30%). Спустя 12 мес наблюдения состояние пациентов, лечившихся клозапином, также ухудшалось значительно реже (8%), чем при терапии рисперидоном (91,7%), оланзапином (70%) и традиционными нейролептиками (47,6%). В этот период прием типичных нейролептиков был более эффективен, чем применение рисперидона (47,6% против 91,7%). Через 18 мес статистически значимые различия были выявлены при сравнении групп больных, принимавших клозапин (0%) и рисперидон (100%); клозапин (0%) и типичные нейролептики (45,5%). В дальнейшем различия между группами становились менее выраженными, что проявлялось отсутствием статистически значимой разницы между ними. Группа больных, принимавших рисперидон, через 18 мес наблюдения была полностью исключена из сравнения из-за ухудшения состояния во всех случаях. Примечательно, что наибольшее число обострений при приеме клозапина приходилось на отдаленные этапы ремиссии (3-й год наблюдения), тогда как при лечении другими нейролептиками состояние больных обычно ухудшалось в течение 1-го года. Это означает, что длительность ремиссий при приеме клозапина была значительно продолжительнее, чем при лечении рисперидоном, оланзапином и типичными средствами, что было связано с более высоким качеством ремиссий и лучшим соблюдением режима терапии. За весь период наблюдения частота обострений составила 66,7, 100, 95 и 86,7% соответственно обследованным группам. Интересно, что общее число обострений при сравнении групп больных, принимавших клозапин и типичные нейролептики, типичные нейролептики и рисперидон, было сопоставимым. Однако это не означает равную эффективность этих средств, поскольку статистически значимые различия между группами были выявлены в процессе наблюдения (6, 12 и 18 мес).
Клиническое наблюдение и статистическая обработка полученных данных свидетельствуют, что при шизофрении, протекающей в форме приступов (шубообразная и рекуррентная), наиболее длительные ремиссии также формировались при приеме клозапина (см. табл. 3).

Всего в 3,2% случаев их длительность составила менее 1 года. Через 2 года повторные приступы развились еще у 9,7% больных (от общего их числа в этой группе). В течение 3-го года состояние ухудшалось у 32,3% пациентов. При терапии рисперидоном и оланзапином ремиссии были менее устойчивыми. В течение 1-го года приема этих нейролептиков состояние ухудшалось у 41,4 и 68% пациентов. Через 2 года повторные приступы развивались еще в 6,9 и 8% случаев соответственно. В течение 3-го года повторные психозы наблюдали у 51,7 и 24% больных. За 3-летний период состояние ухудшилось у всех пациентов, принимавших рисперидон (100%) и оланзапин (100%), что значительно превышало количество повторных приступов при приеме клозапина (45,2%). В процессе наблюдения статистически значимые различия между группами были выявлены через 6 и 12, 30 и 36 мес. В течение 2-го года терапии (13–24-й месяцы) частота повторных приступов во всех группах была сопоставимой. Примечательно, что при приеме клозапина наибольшее количество рецидивов наблюдали на поздних сроках ремиссии (в течение 3-го года) обычно из-за появления у больных убежденности в выздоровлении. При приеме других нейролептиков максимальное число обострений отмечено в течение 1-го года после выписки больных из стационара. Это было связано с более низким качеством сформированных ремиссий в этих группах, а значит, с более слабым осознанием пациентами болезненности своего состояния и несоблюдением режима приема лекарств.
При вялотекущей шизофрении в отличие от других форм заболевания частота обострений в течение всего периода наблюдения во всех группах была сопоставимой (см. табл. 3). Ремиссии длительностью менее 1 года были сформированы у 54,5, 30, 27,3 и 38,1% от общего числа больных, принимавших клозапин, рисперидон, оланзапин и кветиапин. Причем в этот период частота обострений во всех группах была максимальной. В течение 2-го года наблюдения состояние ухудшалось еще в 9,1, 10, 9,1 и 4,8% случаев. В течение 3-го года повторные обострения развились у 0, 5, 9,1 и 4,8% больных. За весь период наблюдения устойчивость ремиссии нарушалась у 63,6, 45, 45,5 и 47,6% пациентов, принимавших соответственно клозапин, рисперидон, оланзапин и кветиапин. Несмотря на отсутствие статистически значимых различий между группами, обращает внимание меньшая длительность ремиссий у больных, которым рекомендовался прием клозапина, и высокая частота обострений в этой группе в течение 1-го года амбулаторной терапии. Необходимо подчеркнуть, что эта закономерность не отражала силу «истинной» противорецидивной эффективности клозапина, а была связана с субъективным отношением пациентов к такой терапии. Больные вялотекущей шизофренией, особенно при преобладании ипохондрической и психопатоподобной симптоматики, субъективно тяжело воспринимали даже легкие побочные эффекты, часто развивающиеся при приеме клозапина, нарушали режим терапии, что приводило к ухудшению их состояния. При приеме других атипичных нейролептиков субъективно тягостные побочные эффекты были менее выражены, как следствие пациенты лучше выполняли назначения врача. Это наблюдение свидетельствует о необходимости противопоставления понятий «эффективность лечебного процесса» («эффективность лечения»), которая зависит от целого комплекса факторов, и «эффективность нейролептика», которая отражает мощность антипсихотического эффекта и его спектр.
Прием клозапина при манифестации параноидной шизофрении обеспечивал формирование ремиссий длительностью более 3 лет у 83,3% больных. Напротив, за этот период обострения болезни развивались во всех случаях приема рисперидона и оланзапина. Между группами были выявлены статистически значимые различия. При приеме типичных нейролептиков состояние больных ухудшалось чаще (60%), чем при лечении клозапином (16,7%), и реже, чем при терапии рисперидоном (100%) и оланзапином (100%). Однако эти различия не достигали статистической значимости.
При шизофрении, протекающей в форме приступов, длительность ремиссий у всех больных, принимавших рисперидон и оланзапин, не превышала 3 лет. При лечении клозапином таких больных было значительно меньше – всего 28,6%. Между группами выявлены статистически значимые различия.
При вялотекущей шизофрении количество обострений в течение 3 лет было сопоставимым во всех группах и составило 42,9, 33,3, 40 и 20% соответственно.
Необходимо отметить, что эффективность поддерживающей терапии зависела не только от особенностей лечения, но, безусловно, и от особенностей патологического процесса. Это доказывалось тем, что на ранних сроках ремиссии обострения при непрерывной параноидной и вялотекущей шизофрении развивались чаще, чем при ее приступообразном течении (табл. 4).

Это было связано с более тяжелым протеканием непрерывных форм по сравнению с приступообразными (худшее качество ремиссий, меньшее осознание пациентами болезненности состояния, большая распространенность отсутствия терапевтического сотрудничества). При шубообразной и рекуррентной шизофрении большинство обострений развивалось на отдаленных этапах ремиссии (3-й год наблюдения).
Как было отмечено, в течение 1-го года наблюдения при приеме клозапина, рисперидона, оланзапина и типичных нейролептиков обострения параноидной шизофрении развились в 14,8, 95, 85 и 63,3% случаев соответственно. Это привело к утрате сопоставимости групп больных, принимавших разные нейролептики. Поэтому при этой форме заболевания сравнить качество ремиссий в различных группах не удалось. Длительная оценка динамики состояния была проведена только у больных, получавших клозапин. Качество ремиссий изучали у 20 таких пациентов, у которых в течение 2 лет не отмечено развития повторных обострений. Все эти случаи относились к среднепрогредиентному течению эндогенного процесса.
Клиническое наблюдение показало, что после «отзвучания» обострения в период последующей ремиссии непрерывно текущей параноидной шизофрении состояние больных, принимавших клозапин, продолжало улучшаться. Это проявлялось в очень медленном, постепенном ослаблении продуктивной симптоматики. Наблюдали дальнейшую дезактуализацию бредовых идей и психических автоматизмов. Во многих случаях обращало внимание ослабление нарушений стройности мышления. Примечательно, что у некоторых длительно болеющих появлялось сознание болезни, ощущение чуждости или субъективной тягостности переживаний, хотя полноценная критика у них не формировалась. В наиболее тяжелых случаях можно было говорить об «эмоциональной инкапсуляции» продуктивных расстройств, при которой сохранявшиеся переживания все в меньшей степени определяли поведение больных. Пациенты становились безучастными к ним, условно «сторонними наблюдателями».
Стандартизированная оценка доказывала результаты приведенного клинического наблюдения (табл. 5).

В течение 2 лет отмечено снижение среднего суммарного балла по подшкалам, отражающим продуктивные расстройства. Причем через 18 и 24 мес наблюдения эти различия были статистически значимыми по сравнению с исходным уровнем (р<0,05). В течение 2 лет наблюдения тяжесть продуктивных и негативных расстройств снизилась на 7,9 и 1,8 балла.
Клиническое наблюдение показало, что сформированные у больных параноидной шизофренией ремиссии относились к параноидному, психопатоподобному типу и типу Verschrobene. Таких наблюдений было 12 (60%), 2 (10%) и 6 (30%) соответственно. При параноидном варианте состояние больных определялось переплетением собственно дефицитарной симптоматики в виде эмоционально-волевого обеднения и продуктивных расстройств, проявляющихся бредовыми идеями различной степени выраженности. В легких случаях наблюдали бредовую настроенность в виде подозрительности, настороженности, недоверчивости. Затем шли случаи инкапсулированного или диссимулируемого бреда. В редких случаях при большей тяжести состояния бредовые расстройства были довольно выражены. У всех больных были заметны нарушения стройности мышления. Параноидные ремиссии формировались при активном течении шизофрении длительностью более 1 года – 2 лет и на этапе затухания активности патологического процесса (формирование дефекта). Психопатоподобный (псевдопсихопатический) тип ремиссий проявлялся сочетанием эмоционально-волевого обеднения и психопатоподобной симптоматики в виде легкого возникновения вспышек гнева, возбудимости, взрывчатости, деструктивного поведения, особенно в ответ на субъективно неприятные для больного внешние события, эгоцентризма, дурашливости. Такую картину наблюдали у больных с длительным течением патологического процесса на этапе его «выгорания». При этом симптоматика более высоких регистров (бред, нарушения стройности мышления) могла входить в структуру описываемого симптомокомплекса, но не была определяющей. Пациенты с ремиссиями типа Verschrobene будут описаны чуть ниже.
Довольно интересны данные о динамике состояния больных с манифестацией параноидной шизофрении. Несмотря на то что таких наблюдений было всего 6, полученные результаты важны для понимания закономерностей развития патологического процесса и его чувствительности к лечению. Характеризуя эту группу, необходимо отметить, что ее составили случаи болезни, начавшейся в зрелом возрасте, длительностью течения не более 1 года (на момент начала предшествующей купирующей терапии), с признаками, позволяющими прогнозировать среднюю прогредиентность течения. Длительная терапия клозапином приводила к значительному улучшению состояния таких больных. Это проявлялось в существенном ослаблении психопатологических расстройств (см. табл. 5). При суммарной оценке по подшкалам PANSS positive и PANSS global их тяжесть уменьшилась на 11 и 13,8 балла от исходного уровня через 12 и 24 мес. Терапия клозапином была эффективна в отношении не только продуктивных, но и негативных расстройств, что доказывалось статистически значимыми различиями при их оценке в процессе наблюдения по сравнению с исходным уровнем (р<0,05). Выраженность негативной симптоматики по PANSS negative через 12 и 24 мес снизилась на 7,7 и 9,7 балла. Эти различия значительно превышали средние показатели в группе больных параноидной шизофренией. Обращает внимание, что лечение клозапином манифестации непрерывной параноидной шизофрении и шизофрении, протекающей приступообразно, приводило к тому, что тяжесть психопатологической симптоматики в этих группах больных становилась сопоставимой (сравнение данных табл. 5, 6).

Ремиссии, сформированные спустя 1–2 года после начала терапии у больных с манифестацией параноидной шизофрении, характеризовались довольно высоким качеством с практически полной редукцией психотической симптоматики. Наблюдали лишь бредовую настроенность в виде подозрительности, настороженности, некоторого недоверия. Наиболее отчетливо это проявлялось в общении с окружающими. Больные были критичны к переживаниям, перенесенным во время предшествующего психоза. Выявлялись невыраженные нарушения мышления по эндогенному типу, однако они скорее входили в структуру дефекта, а не текущего процесса. В целом состояние больных можно было расценить как ремиссии типа Verschrobene с полной остановкой прогрессирования болезни на время лечения. Имеющиеся расстройства грубо не нарушали социальную адаптацию больных. Все это свидетельствует, что интенсивная терапия клозапином начального этапа параноидной шизофрении приводит к переходу ее течения из непрерывного в условно приступообразное (лекарственный патоморфоз).
Прежде всего необходимо отметить, что в период ремиссии состояние больных всех групп претерпевало определенную динамику. В первые месяцы при отсутствии признаков остроты состояния больные оставались вялыми, безынициативными, малообщительными. Они были погружены в себя, отстранены от окружающих событий, стремились к уединению. Неохотно общались с окружающими, в том числе с родными. В беседе с врачом молчаливы. Кратко отвечали на вопросы. Предпочитали не обсуждать перенесенный психоз и свое настоящее состояние. На темы, не связанные с болезнью, говорили значительно охотнее. Очерченных симптомов депрессии не выявлялось. Они критично относились к «отзвучавшему» приступу, понимая болезненность своих переживаний во время него, однако недостаточно осознавали тяжесть своего настоящего состояния. Установку на прием лекарств удавалось поддержать только при помощи методов убеждения и косвенного внушения, используемых регулярно во время очередных осмотров, и контроля родных. Однако в течение последующего полугода – года состояние больных улучшалось. Этот процесс протекал крайне инертно. Постепенно больные оживлялись, становились более доступными, расположенными к общению. Они медленно возвращались к повседневному ритму жизни, расширялся круг контактов и интересов. Появлялось желание продуктивной деятельности. Повышалось доверие к врачу и родным. Одновременно изменялось отношение к заболеванию. Пациенты начинали более осмысленно оценивать болезненность перенесенного психоза и своего настоящего состояния. Стремились к сотрудничеству с врачом. Улучшалось настроение. Эти изменения постепенно приводили к восстановлению социальной адаптации больных, являющейся лакмусом их психического состояния. Описанную динамику наблюдали во всех группах, но она была более заметной у больных, принимавших клозапин.
Большой интерес вызывает квалификация психопатологических расстройств, определяющих состояние больных в первые месяцы наблюдения. Необходимо отметить первоначально возникшую трудность их разграничения и определения синдромологической принадлежности. Однако тщательное изучение психического состояния клиническим методом позволяет утверждать, что в большинстве случаев автор сталкивался с переплетением остаточной продуктивной симптоматики и вторичных негативных расстройств, являющихся следствием перенесенного психоза. Описанные симптомы были связанны между собой и с острым периодом болезни, о чем свидетельствовало их гармоничное ослабление и корреляция уменьшения их тяжести с углублением осознания болезненности перенесенных переживаний. Нельзя не упомянуть и об определенной роли в развитии этих расстройств психотравмирующих факторов. Осознание своего нездоровья и внешняя стигматизация у некоторых больных, особенно с манифестным или «вторым» психозом, выступали в качестве сильных психологических факторов, ухудшающих их состояние. Такое же значение имело появление ощущения несостоятельности у недостаточно компенсированных больных в условиях повышенных требований повседневной жизни. Поскольку точно оценить степень патопластического взаимодействия психогенно спровоцированной симптоматики с процессуальными расстройствами на начальном этапе ремиссии довольно сложно, для описания случаев, при которых их значение для состояния больного не вызывает сомнений, возможно рационально использовать термин «эндореактивная симптоматика начального периода ремиссии».
Представленные данные клинического наблюдения были подтверждены стандартизированной оценкой состояния больных. Через 6 мес наблюдения тяжесть продуктивных расстройств при приеме клозапина, рисперидона и оланзапина у больных шизофренией, протекающей приступообразно, снизилась на 7,3, 4,5 и 4,7 балла, через 12 мес – на 7,9, 5,1 и 5,5 балла по сравнению с исходным уровнем (см. табл. 6). В дальнейшем состояние пациентов оставалось относительно стабильным. Описанные изменения касались в основном лишь одного психотического симптома PANSS positive – «концептуальная дезорганизация» мышления и многих симптомов невротического регистра PANSS global – «напряженность», «манерность и поза», «депрессия», «моторная заторможенность», «отказ от сотрудничества», «нарушения внимания», «снижение критичности и осознания болезни», «нарушения воли», «активная социальная устраненность». Снижение тяжести негативных расстройств по подшкале PANSS negative при приеме клозапина, рисперидона и оланзапина составило 3,5, 3, 3,6 балла и 5,9, 5,8, 6,5 балла через 6 и 12 мес по сравнению с исходным уровнем. В дальнейшем значительных изменений не выявлено. Корреляция снижения тяжести остаточной продуктивной симптоматики и негативных расстройств в течение 1-го года ремиссии подтверждает их патогенетическое единство в этот период.
Сравнение эффективности терапии в различных группах показало, что через 6 мес прием клозапина приводил к большему ослаблению продуктивных расстройств, чем лечение другими атипичными нейролептиками (см. табл. 6). Через 12 мес статистически значимые различия выявлялись при сравнении этой группы больных только с пациентами, принимавшими рисперидон. В дальнейшем эта разница уже не достигала статистической значимости. Эффективность терапии рисперидоном и оланзапином была сопоставимой в течение всего периода наблюдения. Это свидетельствует о более быстром наступлении терапевтического эффекта при приеме клозапина при равной эффективности всех нейролептиков в целом. Учитывая длительность процесса формирования ремиссии, высокая скорость наступления положительного эффекта имеет большое практическое значение.
Терапия клозапином также была более эффективна в отношении негативных расстройств. Различия между группами выявлялись уже исходно (см. табл. 6) вследствие большей эффективности клозапина при лечении острых психозов, что приводило к меньшей выраженности вторичных негативных расстройств на момент завершения купирующей терапии. Это наблюдение отражает взаимосвязь эффективности купирующей нейролептической терапии и качества последующей ремиссии. В течение всего 2-летнего периода различия между группами сохранялись. Необходимо уточнить, что полученные в сравнительной части исследования данные об эффективности различных нейролептиков несколько условны, поскольку изначально группы не были сопоставимы по численности, а длительная непрерывная терапия оланзапином проведена лишь в 6 случаях.
Прежде чем перейти к описанию типологии ремиссий при приступообразной шизофрении, важно отметить, что их варианты определялись автором спустя длительный срок (годы) после начала их формирования. К этому времени происходила окончательная психопатологическая консолидация ремиссионного состояния и нивелировка нейролептического синдрома, который на более ранних этапах мог затруднять правильную верификацию психического статуса. Например, в период купирующей и на начальных этапах поддерживающей терапии прием нейролептиков вызывал развитие астении, заторможенности, аспонтанности. Эти расстройства были формально схожи с астеническим или апатическим симптомокомплексом в структуре соответствующих типов ремиссий, но по сути (патогенетически) ничего общего с ними не имели. Поэтому оценка структуры ремиссии в это время была бы ошибочна.
Длительное клиническое наблюдение показало, что в группе больных шизофренией, протекающей в виде приступов, формировалось 3 типа ремиссий. При лечении клозапином преобладали ремиссии простой структуры, соответствующие их апатическому (аутистическому) варианту (21 наблюдение – 77,8%). В этих случаях состояние больных определялось эмоционально-волевым обеднением, степень выраженности которого, однако, у различных больных была неодинакова и зависела от длительности болезни. Дополнительная симптоматика, которая могла присутствовать в структуре симптомокомплекса у таких больных, была настолько слаба, что не определяла их состояния. Это наблюдение доказывало высокую эффективность клозапина и свидетельствовало о хорошем «отщеплении» продуктивной симптоматики, приближении состояния больных к «чистому» дефекту. В 4 (14,8%) случаях наблюдали становление астенических ремиссий в виде повышенной утомляемости, снижения психического тонуса. Состояние 2 (7,4%) больных было расценено как ремиссии, приближающиеся к параноидным. Эти случаи относились к длительному течению шизофрении с большим количеством приступов в анамнезе. Причем в структуре таких ремиссий преобладал не бред, а нарушения ассоциативного процесса.
В группе больных, принимавших рисперидон, преобладали астенические ремиссии. Таких наблюдений было 11 (73,3%). Их структура отличалась от аналогичных ремиссий, сформированных при лечении клозапином, большей выраженностью психической истощаемости и эмоционально-волевого снижения. Также у больных, принимавших рисперидон, в структуре астенических ремиссий был более выражен депрессивно-ипохондрический компонент в виде фиксации на тяжести своего состояния и ощущения его бесперспективности. У 2 (13,3%) больных наблюдали формирование ремиссий с преобладанием нарушений мышления (параноидный тип). Апатическая и психопатоподобная ремиссии были сформированы у 2 больных (6,7 и 6,7% соответственно).
Длительный прием оланзапина приводил к формированию ремиссий, по структуре приближающихся к апатическим (100%). Возможно, такая однородность их структуры в этой группе больных была связана с малочисленностью изученной выборки.
Статистическое сравнение числа больных с различными типами ремиссий в разных группах показало, что при лечении клозапином чаще формировался их апатический тип (р=0,0000, метод Фишера), а при терапии рисперидоном – астенический вариант (р=0,0004, метод Фишера). Остальные различия между группами, выявляемые при статистическом анализе полученных данных, мы считаем недостоверными из-за небольшого количества наблюдений.
Необходимо подчеркнуть, что одновременно с выявленными различиями эффективности атипичных нейролептиков при приступообразной шизофрении полученные данные позволяют сделать вывод, который важен для понимания динамики, развития шизофренического процесса. В течение года после отзвучания острых проявлений психоза состояние больных было довольно неустойчивым. С одной стороны, наблюдали медленное, инертное ослабление остаточных продуктивных расстройств и вторичной негативной симптоматики, «консолидацию» критики. С другой стороны, очень высокой была частота развития повторных приступов болезни, связанных с нарушением режима терапии из-за еще недостаточного осознания пациентами болезненности своего настоящего состояния. Поэтому этот период, на наш взгляд, является «переходным» от психоза к ремиссии. Причем его можно рассматривать либо как завершающий этап шуба, либо как начало становления ремиссии. В наших наблюдениях наибольшая эффективность лечения в это время отмечена при продолжении интенсивной нейролептической терапии, часто той, которая использовалась в период острого состояния. Значительное снижение дозировки нейролептика в это время или его замена на средство меньшей мощности приводило к ухудшению состояния. Это наблюдение позволяет нам высказать мнение, что описанный переходный период правильнее рассматривать как завершение острого приступа болезни (шуба) с необходимостью продолжения терапии, соответствующей острому состоянию. Начало же ремиссии целесообразно относить к периоду «отзвучания» остаточных продуктивных и вторичных негативных расстройств, т.е. примерно спустя полгода – год после купирования острой психотической симптоматики. Лишь после этого можно оценивать ее качество, делать вывод о ее структуре и тяжести сформировавшегося дефекта.
Относительно невысокая частота развития обострений вялотекущей шизофрении (по сравнению с параноидной и приступообразной) позволила изучить эффективность длительной поддерживающей терапии этой формы заболевания в течение 3 лет. Количество наблюдений составило 8, 11, 12 и 11 при приеме клозапина, рисперидона, оланзапина и кветиапина соответственно.
Стандартизированную оценку продуктивной симптоматики проводили по подшкале PANSS global, поскольку именно она включает в себя симптомы, отражающие состояние больных этой формой шизофрении. В течение всего периода наблюдения значительных различий между группами в выраженности продуктивных расстройств невротического регистра не выявлено (см. табл. 6). Во всех группах в течение 1-го года терапии наблюдали слабоположительную динамику без статистически значимых различий по сравнению с исходным уровнем. Также обращает внимание постепенное сокращение границ доверительных интервалов, означающее уменьшение различий тяжести состояния больных в каждой из групп.
Различия между группами были вывлены при стандартизированной оценке негативной симптоматики по шкале PANSS negative (см. табл. 6). В течение всего периода наблюдения терапия клозапином была более эффективна, чем применение рисперидона и кветиапина, а через 6, 12 и 30 мес его прием приводил к большему ослаблению негативных расстройств, чем лечение оланзапином. Через 12 мес поддерживающей терапии и вплоть до окончания наблюдения терапия кветиапином была более эффективна, чем применение рисперидона. И наконец, прием оланзапина приводил к большему улучшению состояния больных, чем лечение рисперидоном, через 24, 30 и 36 мес наблюдения. Во всех группах состояние больных улучшалось настолько, что эта разница достигала статистической значимости по сравнению с исходным уровнем. Такое наблюдение свидетельствовало о высокой эффективности всех атипичных нейролептиков при лечении вялотекущей шизофрении.
Результаты тщательного клинического наблюдения несколько отличались от данных приведенной стандартизированной оценки. Оно показало различие эффективности атипичных нейролептиков в период ремиссии вялотекущей шизофрении в отношении продуктивных расстройств. Такое несоответствие было связано с «мягкостью» этих различий, не улавливаемых стандартизированными шкалами, но определяемых при регулярном тщательном клиническом обследовании.
Различия эффективности атипичных нейролептиков прежде всего касались симптомов эндогенного круга. При лечении клозапином, оланзапином и кветиапином реже возникали аутохтонные аффективные колебания по типу кратковременных неглубоких субдепрессий или реакций сниженного настроения и экзальтации. У больных, принимавших клозапин, реже наблюдались транзиторные обострения психопатоподобной симптоматики, астеноипохондрические и деперсонализационные расстройства. Напротив, при лечении рисперидоном больные были склонны к их развитию. При применении клозапина, оланзапина и кветиапина реже наблюдали усиление тревожной симптоматики. Клиническое наблюдение также свидетельствовало о различии эффективности терапии в отношении негативных расстройств. Терапия оланзапином и особенно клозапином была эффективной в отношении нарушений мышления по эндогенному типу, впрочем, выраженных у наших больных неярко. Напротив, применение рисперидона и кветиапина практически не влияло на эти расстройства. При лечении клозапином и кветиапином наблюдали большую активизацию больных и оживление эмоциональных реакций, чем при лечении оланзапином и особенно рисперидоном.
Особый интерес вызывает различие эффективности атипичных нейролептиков при ситуационно обусловленных психогенных расстройствах, легко развивающихся у больных вялотекущей шизофренией, особенно при небольшой давности процесса. При лечении оланзапином, кветиапином и особенно клозапином значительно реже, чем при терапии рисперидоном, наблюдали ситуационно обусловленные истероэксплозивные реакции в виде вспышек гнева, деструктивного поведения. В случае же их развития они были кратковременными и не столь выраженными, как у больных, принимавших рисперидон. Указанные различия между группами прослеживались и в отношении тревожных расстройств, развивающихся в ответ на внешние события. При лечении клозапином, оланзапином и особенно кветиапином значительно реже наблюдали неглубокие ситуационно спровоцированные аффективные расстройства в виде истеросубдепрессивных и субдепрессивных реакций. Напротив, при лечении рисперидоном наблюдали легкость возникновения эпизодов подавленного настроения. Наиболее отчетливо эти различия наблюдали в период наибольшей неустойчивости состояния больных в течение 1-го года наблюдения.
Клиническое обследование больных позволило определить типы сформированных ремиссий при вялотекущей шизофрении. При лечении клозапином наблюдали апатические (7 наблюдений – 87,5%) и астенические ремиссии (1 наблюдение – 12,5%). При лечении рисперидоном в 6 (54,5%) случаях ремиссии характеризовались преобладанием истощаемости (астенический тип). У 4 (36,4%) больных наблюдали их тимопатический вариант. В 1 (9,1%) случае преобладало эмоционально-волевое снижение (апатический тип). При лечении оланзапином у равного числа больных (по 6 наблюдений – 50%) отмечено формирование апатических и астенических ремиссий. Становление ремиссий при приеме кветиапина чаще соответствовало апатическому типу (8 больных – 72,7%) и реже астеническому (3 больных – 27,3%).
Учитывая немногочисленность наблюдений больных с различными вариантами ремиссий, нельзя с уверенностью говорить о различии групп по тому или иному варианту, но все же необходимо отметить некоторые особенности. При лечении клозапином преобладал апатический вариант ремиссии, тогда как при терапии рисперидоном – астенический тип, хотя эта разница не была статистически значимой. У больных, принимавших рисперидон, отмечены случаи тимопатических ремиссий, не выявленные в других группах, что лишний раз свидетельствует о недостаточной эффективности этой терапии в отношении аффективных расстройств. В проведенном исследовании не выявлено ни одного случая психопатоподобного или обсессивного варианта ремиссий, часто описываемых при вялотекущей шизофрении, что может быть связано с отсутствием в выборке для длительного наблюдения больных с психопатоподобной формой заболевания из-за развития у них обострений в пределах 3-летнего периода. Автор наблюдал легкие обсессии в структуре ремиссий, но они отнюдь не определяли состояния больных в такой степени, что можно было говорить об обсессивном типе ремиссионного состояния. Возможно, это было связано с тем, что сформированные ремиссии у обследованных больных были довольно качественными. Наконец, необходимо подчеркнуть, что при приеме клозапина явно прослеживалось его седативное действие. Однако оно не ухудшало качество ремиссионного состояния, а, напротив, «страховало» больных от тревоги (анксиолитический компонент) и переутомления (снотворный компонент), что и определяло редкость возникновения тревожных расстройств и астенического варианта ремиссий. Это наблюдение было справедливо и для больных приступообразной шизофренией, принимавших клозапин.
Заключение
Проведенное исследование позволяет сделать следующие выводы. Обострения шизофрении могут развиваться на любом этапе амбулаторного приема нейролептиков. Однако ухудшение состояния наиболее вероятно в течение 1 и 3-го годов лечения. В целом противорецидивная эффективность нейролептической терапии наиболее высока, особенно на ранних сроках ремиссии, при применении клозапина и значительно ниже при назначении рисперидона и оланзапина.
Применение клозапина при непрерывной параноидной шизофрении приводит к формированию ремиссий наибольшей длительности. Частота обострений, особенно в течение 1-го года лечения, значительно ниже, чем при терапии рисперидоном, оланзапином и типичными средствами. Назначение традиционных нейролептиков в период поддерживающей терапии несколько более эффективно, чем применение рисперидона. Наибольший риск обострений при лечении клозапином отмечается в течение 3-го года его приема, тогда как при терапии рисперидоном, оланзапином и типичными нейролептиками – в течение первых 12 мес.
Сходные результаты получены при изучении противорецидивной эффективности атипичных нейролептиков при поддерживающей терапии шизофрении, протекающей в форме приступов. Применение клозапина приводит к формированию ремиссий наибольшей длительности. В течение 3 лет рецидивы развиваются у всех больных, принимающих рисперидон и оланзапин, и менее чем у половины пациентов, получающих клозапин. Наибольший риск обострений при лечении клозапином отмечен в течение 3-го года его приема, тогда как при терапии рисперидоном, оланзапином и типичными нейролептиками – в течение первых 12 мес.
При вялотекущей шизофрении частота обострений при лечении клозапином, рисперидоном, оланзапином и кветиапином примерно сопоставима. Максимальный риск ухудшения состояния при приеме всех нейролептиков отмечается в течение 1-го года терапии и более высок при применении клозапина.
Представленные выше различия справедливы в случаях манифестаций различных форм шизофрении. При параноидной и приступообразной формах наиболее эффективно применение клозапина, тогда как при вялотекущей шизофрении эффективность различных нейролептиков примерно сопоставима.
После завершения купирующей терапии («отзвучание» наиболее острых проявлений психоза в рамках обострений или острых приступов шизофрении) длительный прием поддерживающей терапии приводит к дальнейшему медленному улучшению состояния больных. Такая динамика наблюдается при различных формах шизофрении. Она проявляется ослаблением «остаточных» продуктивных и вторичных негативных расстройств, а также психогенной симптоматики периода адаптации. Состояние больных максимально улучшается спустя полгода – год (и даже позже) после купирования обострения заболевания. После завершения этого периода происходит консолидация ремиссии, окончательно формируется ее структура (т.е. структура дефекта!), максимально восстанавливается социальная адаптация. Полученные данные свидетельствуют, что описанный период неустойчивого состояния (полгода – год) патогенетически более близок к этапу обострения шизофрении, чем к периоду ремиссии. Наиболее отчетливо это прослеживается при шизофрении, протекающей приступообразно.
Особенности изученной выборки больных позволили сравнить эффективность длительного приема различных атипичных нейролептиков при шизофрении, протекающей в форме приступов, и вялом течении заболевания.
При шубообразной и рекуррентной шизофрении долгосрочная эффективность клозапина, рисперидона и оланзапина в отношении продуктивных расстройств сопоставима. Однако при терапии клозапином состояние больных улучшается гораздо быстрее, что имеет большое практическое значение. Применение клозапина более эффективно, чем применение других нейролептиков, при лечении негативной симптоматики.
При вялотекущей шизофрении эффективность клозапина, рисперидона, оланзапина и кветиапина в отношении продуктивной симптоматики примерно сопоставима. Однако различия наблюдаются при сравнении динамики негативных расстройств. В этом случае эффективность терапии убывает в ряду: клозапин – оланзапин, кветиапин – рисперидон.
Эффективность клозапина при непрерывной параноидной шизофрении довольно высока и коррелирует с длительностью заболевания. При его манифестации длительный прием клозапина приводит к значительному ослаблению продуктивных расстройств, иногда вплоть до доболезненного уровня, способствует переходу течения шизофрении из непрерывного в условно приступообразное (лекарственный патоморфоз).
Психопатологическая структура лекарственных ремиссий зависит прежде всего от особенностей патологического процесса. При неблагоприятном течении шизофрении (особенно параноидная форма, некоторые случаи длительного течения шубообразной шизофрении) в структуре ремиссий наряду с негативной симптоматикой ярко выражены продуктивные расстройства (бред, нарушения стройности мышления, психопатизация). При более «мягких» вариантах течения шизофрении структура ремиссий определяется сочетанием негативной симптоматики и продуктивных расстройств невротического регистра (астенический синдром, нарушения поведения, обсессии, колебания настроения).
Терапия различными атипичными нейролептиками вносит значительные особенности в структуру лекарственных ремиссий. Применение клозапина чаще приводит к формированию ремиссий, «бедных» продуктивными расстройствами. Его длительный прием способствует хорошему «отщеплению» продуктивных расстройств, приближению структуры ремиссии к простому апатическому дефекту. Другие типы ремиссий (астенические, параноидные, психопатоподобные и др.) при такой терапии формируются реже, чем при приеме других атипичных нейролептиков. Наиболее отчетливо это прослеживается при шизофрении, протекающей приступообразно. Наиболее благоприятный вариант ремиссий при терапии рисперидоном характеризуется сочетанием симптомов простого дефицита и повышенной истощаемости (астенический вариант ремиссий). Часто в их структуре присутствуют аффективные и ипохондрические включения. Апатические ремиссии при приеме рисперидона формируются редко. Особенности изученной выборки позволили провести анализ структуры ремиссий при приеме оланзапина и кветиапина только у больных вялотекущей шизофренией. Применение этих нейролептиков приводит к формированию как апатических, так и астенических ремиссий.
Список исп. литературыСкрыть список1. Аведисова А.С. Общие закономерности и индивидуальные различия в действии психотропных препаратов. Рос. психиат. журн. 2004; 4: 52–6.
2. Горобец Л.Н. Нейроэндокринные дисфункции у больных шизофренией и шизоаффективным расстройством в условиях современной антипсихотической терапии (клинико-биохимическое исследование). Дис. ... докт. мед. наук. М., 2007.
3. Данилов Д.С. Терапия острых состояний при шизофрении (сравнительное исследование эффективности атипичных нейролептиков клозапина, рисперидона, оланзапина и кветиапина). Труды конференции, посвященной 120-летию клиники психиатрии им. С.С.Корсакова. М., 2007; 83–97.
4. Данилов Д.С. Эффективность атипичных нейролептиков при острых приступах приступообразно-прогредиентной шизофрении. Журн. неврол. и психиат. им. С.С.Корсакова. 2007; 107 (11): 25–30.
5. Данилов Д.С. Возможность формирования ремиссии высокого качества при длительном хроническом течении шизофрении Журн. неврол. и психиат. им. С.С.Корсакова. 2008; 108 (11): 80–5.
6. Данилов Д.С. Индивидуальный выбор современной психофармакотерапии шизофрении (основные принципы, обсуждение результатов клинических исследований и некоторые практические рекомендации). Психиат. и психофармакотер. 2008; 10 (6): 50–7.
7. Данилов Д.С. Антипсихотическая терапия параноидной шизофрении с непрерывным течением (сравнительное исследование эффективности клозапина, рисперидона, оланзапина и высокопотентных традиционных нейролептиков). Рос. психиат. журн. 2009; 3: 71–80.
8. Данилов Д.С. Дифференцированное применение современных антипсихотических средств при лечении шизофрении. Журн. неврол. и психиат. им. С.С.Корсакова. 2009; 109 (4): 89–94.
9. Данилов Д.С. Купирующая терапия шубообразной шизофрении: эффективность современных антипсихотических средств и дифференциация их назначения. Психиат. и психофармакотер. 2009; 11 (1): 49–54.
10. Каледа В.Г. Терапия эндогенных приступообразных психозов юношеского возраста – основные принципы и подходы. Журн. неврол. и психиат. им. С.С.Корсакова. 2006; 106 (9): 4–11.
11. Мазаева Н.А. Риски и преимущества применения атипичных антипсихотиков в психиатрии (по данным зарубежных публикаций последних лет). Психиат. и психофармакотер. 2006; 8 (5): 4–11.
12. Мосолов С.Н. Спорные и малоизученные вопросы практического использования антипсихотической фармакотерапии у больных шизофренией (анализ интерактивного опроса врачей). Терапия психич. расстройств. 2006; 1: 41–8.
13. Попов Ю.В., Вид В.Д. Современная клиническая психиатрия. М.: Экспертное бюро, 1997.
14. Смулевич А.Б., Андрющенко А.В., Бескова Д.А. Проблема ремиссий при шизофрении: клинико-эпидемиологическое исследование. Журн. неврол. и психиат. им. С.С.Корсакова. 2007; 107 (5): 4–15.
15. Снедков Е.В. Атипичные антипсихотики: поиск решения старых и новых проблем. Психиат. и психофармакотер. 2006; 8 (4).
16. Цыганков Б.Д., Агасарян Э.Г. Анализ эффективности и безопасности современных и классических антипсихотических препаратов. Журн. неврол. и психиат. им. С.С.Корсакова. 2006; 106 (9): 64–70.
17. Чомский А.Н. Влияние побочных эффектов атипичных антипсихотиков на терапевтический процесс у больных шизофренией. Дис. ... канд. мед. наук. СПб., 2008.
18. Ahmer S, Arya P, Anderson D, Faruqui R. Conflict of interest in psychiatry. Psychiat Bull 2005; 29: 302–4.
19. Allison DB, Mentore JL, Heo M et al. Antipsychotic-induced weight gain: a comprehensive research synthesis. Am J Psychiat 1999; 156 (11): 1686–96.
20. American Psychiatric Association. Practice guideline for the treatment of patients with schizophrenia (2nd ed). Am J Psychiat 2004; 161 (2): 1–114.
21. Arana GW, Rosenbaum JF. Фармакотерапия психических расстройств. М.: Бином, 2004.
22. Baldessarini RJ, Tarazi FI. Медикаментозное лечение психозов и маний. В кн.: Клиническая фармакология по Гудману и Гилману. М.: Практика, 2006; с. 382–411.
23. Carpenter WT, Conley RR, Buchanan RW. Шизофрения. В кн.: Фармакотерапия в неврологии и психиатрии (ред. Энн С.Д., Койл Дж.Т.). М.: Мед. информ. агентство. 2007; с. 49–85.
24. Duggan L, Fenton M, Rathbone J et al. Olanzapine for schizophrenia. (Cochrane Review). In: The Cochrane Library. Oxford, Update Software. 2005; Issue 2.
25. Falkai P, Wobrock T, Lieberman J et al. WFSBP Task Force on Treatment Guidelines for Schizophrenia. World Federation of Societies of Biological Psychiatry (WFSBP) Guidelines for Biological Treatment of Schizophrenia, Part 1: Acute treatment of schizophrenia. World J Biol Psychiat 2005; 6 (3): 132–91.
26. Falkai P, Wobrock T, Lieberman J et al. WFSBP Task Force on Treatment Guidelines for Schizophrenia. World Federation of Societies of Biological Psychiatry (WFSBP) Guidelines for Biological Treatment of Schizophrenia, Part 2: Long-term treatment of schizophrenia. World J Biol Psychiat 2006; 7 (1): 5–40.
27. Geddes J, Freemantle N, Harrison P, Bebbington P. Atypical antipsychotics in the treatment of schizophrenia: systematic overview and meta-regression analysis. BMJ 2000; 321 (7273): 1371–6.
28. Haddad PM. Antipsychotics and diabetes: review of non-prospective data. Brit J Psychiat (Suppl). 2004; 47: 80–6.
29. Heres S, Davis J, Maino K et al. Why olanzapine beats risperidone, risperidone beats quetiapine and quetiapine beats olanzapine: an exploratory analysis of head-to-head comparison studies of second-generation antipsychotics. Am J Psyhiat 2006; 163 (2): 185–94.
30. Janicak PG, Davis JM, Presckorn SH, Ayd FJ. Принципы и практика психофармакотерапии. Киев: Ника-Центр, 1999.
31. Lawrie S, McIntosh A. Schizophrenia. BMJ Clinical Evidence. 2002; 8: 1019–49.
32. Leon J, Susce MT, Johnson M et al. A clinical study of the association of antipsychotics with hyperlipidemia Schizophren Res 2007; 92 (1–3): 95–102.
33. Shader R. Шизофрения. В кн.: Психиатрия (пер. с англ.). М.: Практика, 1998; с. 395–425.
34. StЪllberger C, Huber JO, Finsterer J. Antipsychotic drugs and QT prolongation. Internat Clin Psychopharmacol 2005; 20 (5): 243–51.


