Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№01 2009
Эффективность и переносимость Торина при лечении депрессий у госпитализированных больных с сердечно-сосудистой патологией №01 2009
Номера страниц в выпуске:53-56
С появлением новых антидепрессантов, существенно отличающихся по своим свойствам, а также их генерических модификаций возникает возможность подбора препарата, наиболее адекватного не только психопатологическим особенностям депрессии, но и сопутствующей соматической патологии. На первый план выдвигаются характеристики тимоаналептика, связанные с его переносимостью и безопасностью.
Введение
С появлением новых антидепрессантов, существенно отличающихся по своим свойствам, а также их генерических модификаций возникает возможность подбора препарата, наиболее адекватного не только психопатологическим особенностям депрессии, но и сопутствующей соматической патологии. На первый план выдвигаются характеристики тимоаналептика, связанные с его переносимостью и безопасностью. Однако до настоящего времени оценка таких свойств во многом основывается на обобщении данных о побочных эффектах антидепрессантов, полученных в ходе изучения препаратов у соматически благополучных пациентов. Исследования, непосредственно связанные с назначением антидепрессантов-генериков больным с актуальной патологией внутренних органов, немногочисленны [1–5]. В то же время известно, что распространенность депрессивных расстройств особенно высока в общемедицинской сети (прежде всего в кардиологической практике) [6, 7]. Частота депрессивных состояний среди этого контингента больных составляет 20–45% [6–8]. Чаще наблюдаются нозогенные тревожно-ипохондрические реакции, а также депрессии как эндогенного, так и невротического уровня.
На накопление большего объема данных об использовании тимоаналептиков-генериков у пациентов с соматической патологией направлена специальная программа, разработанная сотрудниками межклинического психосоматического отделения (зав. – акад. РАМН А.Б.Смулевич) Клиники кардиологии (руководитель – проф. А.Л.Сыркин) ММА им. И.М.Сеченова. В ходе реализации этой программы проведено исследование переносимости, безопасности и эффективности Торина (сертралина)1 – селективного ингибитора обратного захвата серотонина. У сертралина существует и ряд других психофармакологических механизмов действия [9, 10]. Активация серотонинергической системы во внутренних органах способствует снижению агрегации тромбоцитов, препятствует тромбообразованию и оказывает протективное воздействие на эндотелий сосудов. Сертралин способствует некоторому увеличению содержания в ЦНС дофамина за счет ингибирования его обратного захвата [11, 12]. Кроме того, данный моноамин способствует улучшению регуляции сердечно-сосудистой системы [8, 10, 13]. Соответственно, есть основания полагать, что Торин (сертралин) может использоваться при лечении депрессий у больных с сердечно-сосудистой патологией.
Материалы и методы
В исследование включали пациентов в возрасте от 20 до 65 лет с депрессивными эпизодами легкой или средней степени тяжести (F32.0, F32.1), биполярным аффективным расстройством (текущий эпизод легкой или умеренной депрессии – F31.3), рекуррентным депрессивным расстройством (депрессивный эпизод легкой или средней степени тяжести – F33.0, F33.1), циклотимией (F34.0), пролонгированными депрессивными реакциями в рамках расстройств адаптации (F43.2), страдающих сердечно-сосудистой патологией.
Критерием включения являлась также стабильность соматических показателей и доз соматотропной терапии, установленных как минимум за 2 нед до включения пациента в исследование.
Критерии исключения: склонность к аллергическим реакциям, включая гиперчувствительность к сертралину в анамнезе; беременность, лактация; участие в каких-либо клинических испытаниях за 4 нед до включения в настоящее исследование; признаки психической патологии, не удовлетворяющей критериям включения; зависимость от психоактивных веществ; закрытоугольная глаукома; злокачественные новообразования, неврологические заболевания; тяжелая печеночная и/или почечная недостаточность и иные тяжелые соматические заболевания в стадии декомпенсации, препятствующие участию в исследовании.
Исключали использование других антидепрессантов. При необходимости (инсомния, тревога и пр.) предусматривали назначение анксиолитиков (клоназепам, феназепам, реланиум), а также тиоксантена (хлорпротиксен, труксал).
Терапию проводили в течение 30 дней в интервале суточных доз от 50 до 250 мг. Дозу постепенно и индивидуально титровали до эффективной (в среднем 150 мг/сут). Пациенты принимали препарат во время еды.
Динамику состояния пациентов регистрировали в ходе 5 визитов. Использовали стандартные оценочные шкалы: шкалу для оценки депрессии Гамильтона (HDRS) и шкалу общего клинического впечатления (CGI).
Критерием эффективности считали: снижение на 50% и более от исходных значений среднего балла по шкале HDRS, показатели «существенное улучшение», «выраженное улучшение» и «умеренное улучшение» по шкале CGI-I, а также баллы CGI-S≤2 («нет симптомов» или «пограничное расстройство»).
При оценке переносимости и безопасности препарата учитывали следующие показатели: 1 – нежелательные явления, выявленные в результате спонтанных жалоб пациентов и целенаправленных вопросов при обследовании на каждом из предусмотренных визитов; 2 – изменения в стартовых лабораторных и инструментальных показателях соматического статуса на фоне терапии Торином. Методы обследования соответствовали стандартам курации больных в клиническом отделении, на базе которого проводили исследование: массы тела, артериальное давление (АД), частота сердечных сокращений (ЧСС), электрокардиография, суточное мониторирование по Холтеру, лабораторные показатели (общий и биохимический анализ крови, коагулограмма).
Для оценки риска лекарственных взаимодействий между Торином и препаратами соматотропного действия регистрировали случаи усиления/манифестации нежелательных эффектов Торина и соматотропных средств (назначаемых в рамках комбинированной фармакотерапии) и потенциально связанные с изменениями метаболизма одного лекарственного средства под влиянием другого. Для верификации побочных эффектов использовали шкалу побочных эффектов UKU.
Статистическая обработка данных проведена с использованием программы Statistica (компания «StatSoft», США). Достоверность различий оценивали с применением теста Колмогорова–Смирнова.
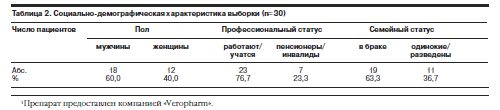
Изученную выборку составили 30 пациентов (18 женщин, 12 мужчин, средний возраст 57,4 года), из них 14 больных с депрессивными эпизодами легкой или средней степени тяжести, 11 – с пролонгированными депрессивными реакциями в рамках расстройств адаптации (нозогенные депрессии), 3 – с рекуррентным депрессивным расстройством, по 1 – с биполярным аффективным расстройством и циклотимией (табл. 1).

Синдромальная характеристика депрессивных состояний была различна и в большинстве (76,7%) наблюдений представлена тревожно-ипохондрическими депрессиями. У 16,7% больных в структуре депрессивного состояния преобладали апатоадинамические проявления, а у 6,7% – аффект тоски.
Независимо от диагностической квалификации депрессий значительное место в структуре аффективного синдрома у изученных больных занимали соматовегетативные проявления. Как правило, они выступали в виде гомономных (напоминающих симптомы сердечно-сосудистой патологии), полиморфных соматизированных и конверсионных симптомов.
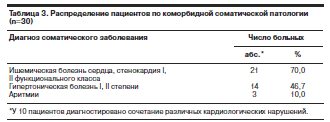
Социально-демографические характеристики изученных пациентов приведены в табл. 2. Распределение больных в соответствии с диагнозом коморбидного соматического заболевания представлено в табл. 3.
Все больные получали сопутствующую соматотропную терапию: гипотензивную, антиаритмическую, антиангинальную (ацетилсалициловая кислота, пролонгированные нитраты, b-блокаторы, антагонисты кальция, ингибиторы ангиотензинпревращающего фермента).
Из 30 больных, включенных в исследование, полностью завершили 4-недельный курс терапии 28 (93,3%) пациентов. Больные, не закончившие исследование, в соответствии с протоколом выбыли на 1–2-й неделе терапии. В обоих случаях причиной преждевременной отмены препарата явились нежелательные эффекты.
К моменту завершения исследования клинически значимое улучшение (пациенты, квалифицированные как респондеры по принятым в исследовании критериям) зафиксировано у 19 (63,3%) из 30 пациентов. Согласно шкале CGI-I «существенное улучшение» отмечено у 7 (23,3%), «выраженное улучшение» – у 12 (40%) пациентов. Сходные результаты получены при анализе динамики тяжести психопатологических расстройств по шкале CGI-S. На момент завершающей оценки исходный средний балл CGI-S (4,3) уменьшился до уровня 2 и ниже у 18 (60%) больных.
Полученные данные соответствуют приводимым в литературе результатам исследований эффективности сертралина [5, 14–19].
Отчетливую редукцию психопатологических состояний отмечали в среднем к началу 2-й недели лечения. Средняя эффективная доза Торина составила 150 мг/сут.
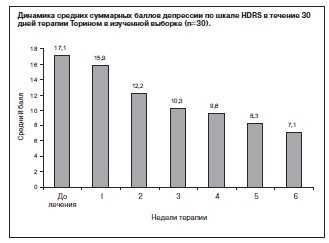
Выраженное клиническое действие Торина, установленное по критерию эффективности (шкалы CGI-I и CGI-S), подтверждается достоверной редукцией исходных баллов депрессии шкалы HDRS. Значимое обратное развитие депрессивных симптомов регистрируется на 14-й день лечения и становится более выраженным на фоне дальнейшей терапии с непрерывным улучшением показателей вплоть до 28-го дня терапии (p<0,05).
Динамика средних баллов депрессии по шкале Гамильтона (HDRS) представлена на рисунке.
К окончанию курса терапии наибольшую редукцию психопатологической симптоматики регистрировали у пациентов с тревожно-ипохондрической 69,6% (16 из 23 наблюдений) и апатоадинамической депрессией 60% (3 из 5 наблюдений). Клинически это проявлялось уменьшением выраженности гипотимии, редукцией депрессивного содержательного комплекса. Больные отмечали улучшение настроения с одновременным уменьшением вялости, подавленности, эмоциональной напряженности, чувства тревоги, раздражительности. Дезактуализировались ипохондрические идеи. Отмечая восстановление прежнего душевного равновесия, пациенты констатировали, что раньше слишком пессимистично оценивали ситуацию, «неосознанно» преувеличивали опасность сердечно-сосудистого заболевания и их социальных последствий.
Группу нонреспондеров составили 6 пациентов с психогенными депрессиями и 3 – с соматогенно провоцированными эндогенными депрессивными эпизодами. У большинства из них (7 наблюдений) в анамнезе выявлены одна депрессия и более, по поводу которых проводилось лечение различными группами антидепрессантов (полициклические, селективные). Средняя длительность актуальной депрессии среди нонреспондеров составляла 6,5 мес.
При анализе психопатологических особенностей аффективных расстройств в данной группе больных не отмечено существенного влияния Торина у больных с тоскливой депрессией, а также у 2 пациентов с апатоадинамическим и у 5 – с затяжным (более 1 года) депрессивно-ипохондрическим состоянием.
Переносимость препарата. Установлен благоприятный профиль безопасности препарата. Нежелательные явления, связанные с Торином, отмечены у 6 (20%) пациентов преимущественно в течение первых 2 нед терапии.
В соответствии с целью исследования особое внимание уделялось влиянию Торина на основные гемодинамические показатели. Ни в одном из наблюдений не зарегистрированы клинически значимые взаимодействия между Торином и средствами, направленными на коррекцию сердечно-сосудистой патологии.
На момент окончания терапии у больных изученной выборки не зафиксировано появления жизнеопасных аритмий и/или внутрисердечных блокад. В ходе исследования не отмечено клинически значимого изменения АД (включая ортостатическую гипотензию), а также значимых изменений ЧСС. Относительно результатов холтеровского мониторирования можно отметить отсутствие достоверных отличий по показателям суправентрикулярной и вентрикулярной эктопической активности, а также динамики сегмента ST. Также следует отметить отсутствие динамики интервала QT и QTc на фоне приема препарата, на что особенно обращают внимание при назначении антидепрессантов, учитывая способность трициклических антидепрессантов удлинять интервал QT и вызывать угрожающие жизни желудочковые тахикардии типа «пируэт» (torsades de роintes) [9, 20]. Не обнаружено и влияния на показатели крови.
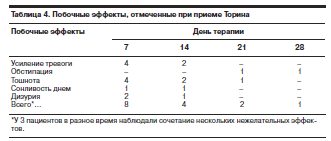
Связанные с препаратом побочные эффекты, послужившие причиной преждевременного прекращения терапии, отмечены в 2 случаях (по 1 наблюдению – тошнота и рвота, затрудненное мочеиспускание).
Другими связанными с препаратом нежелательными явлениями являлись в 4 случаях усиление чувства тревоги с соматовегетативными проявлениями, в 3 – тошнота, по 1 случаю – сонливость в дневное время, затрудненное мочеиспускание, диарея, обстипация.
Отмена Торина не сопровождалась развитием признаков, свойственных синдрому отмены (утомляемость, сонливость, головная боль, тошнота, рвота, анорексия, сухость во рту, головокружение, понос, бессонница, тревога, раздражимость, дезориентация, парестезии, потливость).
Обсуждение
В результате проведенного исследования получены достоверные доказательства эффективности Торина в терапии депрессивных расстройств легкой или средней степени тяжести у больных с сердечно-сосудистой патологией.
Препарат обеспечивает редукцию психопатологических состояний у больных с соматическими заболеваниями. Терапевтический эффект препарата реализуется быстро. Клинически значимое обратное развитие психопатологических нарушений наряду с улучшением самочувствия регистрируется у большинства больных с 14-го дня терапии.
При использовании в терапии депрессивных расстройств у соматически больных Торин обладает благоприятным профилем переносимости и безопасности.
Полученные результаты свидетельствуют о том, что Торин не оказывает отрицательного влияния на течение соматической патологии (ишемическая болезнь сердца, артериальная гипертония, аритмии) и обеспечивает высокий уровень комплаентности пациентов. Эти данные полностью согласуются с имеющимися в литературе указаниями на то, что среди побочных эффектов препарата (табл. 4) чаще всего наблюдаются тошнота и умеренный седативный эффект [5, 16, 17,19, 21].
В исследовании не отмечено признаков взаимодействия Торина в средних терапевтических дозах (150 мг/день) с современными препаратами, применяющимися для лечения сердечно-сосудистых заболеваний, что также соотносится с данными литературы о безопасности комбинированной терапии с использованием этого тимоаналептика [6, 8, 13].
Данные настоящего исследования о терапевтической эффективности Торина при лечении депрессивных расстройств легкой или средней степени тяжести, его переносимости и безопасности позволяют сделать вывод о целесообразности использования препарата при лечении депрессивных состояний у больных с сопутствующей кардиологической патологией.
С появлением новых антидепрессантов, существенно отличающихся по своим свойствам, а также их генерических модификаций возникает возможность подбора препарата, наиболее адекватного не только психопатологическим особенностям депрессии, но и сопутствующей соматической патологии. На первый план выдвигаются характеристики тимоаналептика, связанные с его переносимостью и безопасностью. Однако до настоящего времени оценка таких свойств во многом основывается на обобщении данных о побочных эффектах антидепрессантов, полученных в ходе изучения препаратов у соматически благополучных пациентов. Исследования, непосредственно связанные с назначением антидепрессантов-генериков больным с актуальной патологией внутренних органов, немногочисленны [1–5]. В то же время известно, что распространенность депрессивных расстройств особенно высока в общемедицинской сети (прежде всего в кардиологической практике) [6, 7]. Частота депрессивных состояний среди этого контингента больных составляет 20–45% [6–8]. Чаще наблюдаются нозогенные тревожно-ипохондрические реакции, а также депрессии как эндогенного, так и невротического уровня.
На накопление большего объема данных об использовании тимоаналептиков-генериков у пациентов с соматической патологией направлена специальная программа, разработанная сотрудниками межклинического психосоматического отделения (зав. – акад. РАМН А.Б.Смулевич) Клиники кардиологии (руководитель – проф. А.Л.Сыркин) ММА им. И.М.Сеченова. В ходе реализации этой программы проведено исследование переносимости, безопасности и эффективности Торина (сертралина)1 – селективного ингибитора обратного захвата серотонина. У сертралина существует и ряд других психофармакологических механизмов действия [9, 10]. Активация серотонинергической системы во внутренних органах способствует снижению агрегации тромбоцитов, препятствует тромбообразованию и оказывает протективное воздействие на эндотелий сосудов. Сертралин способствует некоторому увеличению содержания в ЦНС дофамина за счет ингибирования его обратного захвата [11, 12]. Кроме того, данный моноамин способствует улучшению регуляции сердечно-сосудистой системы [8, 10, 13]. Соответственно, есть основания полагать, что Торин (сертралин) может использоваться при лечении депрессий у больных с сердечно-сосудистой патологией.
Материалы и методы
В исследование включали пациентов в возрасте от 20 до 65 лет с депрессивными эпизодами легкой или средней степени тяжести (F32.0, F32.1), биполярным аффективным расстройством (текущий эпизод легкой или умеренной депрессии – F31.3), рекуррентным депрессивным расстройством (депрессивный эпизод легкой или средней степени тяжести – F33.0, F33.1), циклотимией (F34.0), пролонгированными депрессивными реакциями в рамках расстройств адаптации (F43.2), страдающих сердечно-сосудистой патологией.
Критерием включения являлась также стабильность соматических показателей и доз соматотропной терапии, установленных как минимум за 2 нед до включения пациента в исследование.
Критерии исключения: склонность к аллергическим реакциям, включая гиперчувствительность к сертралину в анамнезе; беременность, лактация; участие в каких-либо клинических испытаниях за 4 нед до включения в настоящее исследование; признаки психической патологии, не удовлетворяющей критериям включения; зависимость от психоактивных веществ; закрытоугольная глаукома; злокачественные новообразования, неврологические заболевания; тяжелая печеночная и/или почечная недостаточность и иные тяжелые соматические заболевания в стадии декомпенсации, препятствующие участию в исследовании.
Исключали использование других антидепрессантов. При необходимости (инсомния, тревога и пр.) предусматривали назначение анксиолитиков (клоназепам, феназепам, реланиум), а также тиоксантена (хлорпротиксен, труксал).
Терапию проводили в течение 30 дней в интервале суточных доз от 50 до 250 мг. Дозу постепенно и индивидуально титровали до эффективной (в среднем 150 мг/сут). Пациенты принимали препарат во время еды.
Динамику состояния пациентов регистрировали в ходе 5 визитов. Использовали стандартные оценочные шкалы: шкалу для оценки депрессии Гамильтона (HDRS) и шкалу общего клинического впечатления (CGI).
Критерием эффективности считали: снижение на 50% и более от исходных значений среднего балла по шкале HDRS, показатели «существенное улучшение», «выраженное улучшение» и «умеренное улучшение» по шкале CGI-I, а также баллы CGI-S≤2 («нет симптомов» или «пограничное расстройство»).
При оценке переносимости и безопасности препарата учитывали следующие показатели: 1 – нежелательные явления, выявленные в результате спонтанных жалоб пациентов и целенаправленных вопросов при обследовании на каждом из предусмотренных визитов; 2 – изменения в стартовых лабораторных и инструментальных показателях соматического статуса на фоне терапии Торином. Методы обследования соответствовали стандартам курации больных в клиническом отделении, на базе которого проводили исследование: массы тела, артериальное давление (АД), частота сердечных сокращений (ЧСС), электрокардиография, суточное мониторирование по Холтеру, лабораторные показатели (общий и биохимический анализ крови, коагулограмма).
Для оценки риска лекарственных взаимодействий между Торином и препаратами соматотропного действия регистрировали случаи усиления/манифестации нежелательных эффектов Торина и соматотропных средств (назначаемых в рамках комбинированной фармакотерапии) и потенциально связанные с изменениями метаболизма одного лекарственного средства под влиянием другого. Для верификации побочных эффектов использовали шкалу побочных эффектов UKU.
Статистическая обработка данных проведена с использованием программы Statistica (компания «StatSoft», США). Достоверность различий оценивали с применением теста Колмогорова–Смирнова.
Изученную выборку составили 30 пациентов (18 женщин, 12 мужчин, средний возраст 57,4 года), из них 14 больных с депрессивными эпизодами легкой или средней степени тяжести, 11 – с пролонгированными депрессивными реакциями в рамках расстройств адаптации (нозогенные депрессии), 3 – с рекуррентным депрессивным расстройством, по 1 – с биполярным аффективным расстройством и циклотимией (табл. 1).

Синдромальная характеристика депрессивных состояний была различна и в большинстве (76,7%) наблюдений представлена тревожно-ипохондрическими депрессиями. У 16,7% больных в структуре депрессивного состояния преобладали апатоадинамические проявления, а у 6,7% – аффект тоски.
Независимо от диагностической квалификации депрессий значительное место в структуре аффективного синдрома у изученных больных занимали соматовегетативные проявления. Как правило, они выступали в виде гомономных (напоминающих симптомы сердечно-сосудистой патологии), полиморфных соматизированных и конверсионных симптомов.
Социально-демографические характеристики изученных пациентов приведены в табл. 2. Распределение больных в соответствии с диагнозом коморбидного соматического заболевания представлено в табл. 3.


Все больные получали сопутствующую соматотропную терапию: гипотензивную, антиаритмическую, антиангинальную (ацетилсалициловая кислота, пролонгированные нитраты, b-блокаторы, антагонисты кальция, ингибиторы ангиотензинпревращающего фермента).
Из 30 больных, включенных в исследование, полностью завершили 4-недельный курс терапии 28 (93,3%) пациентов. Больные, не закончившие исследование, в соответствии с протоколом выбыли на 1–2-й неделе терапии. В обоих случаях причиной преждевременной отмены препарата явились нежелательные эффекты.
К моменту завершения исследования клинически значимое улучшение (пациенты, квалифицированные как респондеры по принятым в исследовании критериям) зафиксировано у 19 (63,3%) из 30 пациентов. Согласно шкале CGI-I «существенное улучшение» отмечено у 7 (23,3%), «выраженное улучшение» – у 12 (40%) пациентов. Сходные результаты получены при анализе динамики тяжести психопатологических расстройств по шкале CGI-S. На момент завершающей оценки исходный средний балл CGI-S (4,3) уменьшился до уровня 2 и ниже у 18 (60%) больных.
Полученные данные соответствуют приводимым в литературе результатам исследований эффективности сертралина [5, 14–19].
Отчетливую редукцию психопатологических состояний отмечали в среднем к началу 2-й недели лечения. Средняя эффективная доза Торина составила 150 мг/сут.
Выраженное клиническое действие Торина, установленное по критерию эффективности (шкалы CGI-I и CGI-S), подтверждается достоверной редукцией исходных баллов депрессии шкалы HDRS. Значимое обратное развитие депрессивных симптомов регистрируется на 14-й день лечения и становится более выраженным на фоне дальнейшей терапии с непрерывным улучшением показателей вплоть до 28-го дня терапии (p<0,05).
Динамика средних баллов депрессии по шкале Гамильтона (HDRS) представлена на рисунке.
К окончанию курса терапии наибольшую редукцию психопатологической симптоматики регистрировали у пациентов с тревожно-ипохондрической 69,6% (16 из 23 наблюдений) и апатоадинамической депрессией 60% (3 из 5 наблюдений). Клинически это проявлялось уменьшением выраженности гипотимии, редукцией депрессивного содержательного комплекса. Больные отмечали улучшение настроения с одновременным уменьшением вялости, подавленности, эмоциональной напряженности, чувства тревоги, раздражительности. Дезактуализировались ипохондрические идеи. Отмечая восстановление прежнего душевного равновесия, пациенты констатировали, что раньше слишком пессимистично оценивали ситуацию, «неосознанно» преувеличивали опасность сердечно-сосудистого заболевания и их социальных последствий.
Группу нонреспондеров составили 6 пациентов с психогенными депрессиями и 3 – с соматогенно провоцированными эндогенными депрессивными эпизодами. У большинства из них (7 наблюдений) в анамнезе выявлены одна депрессия и более, по поводу которых проводилось лечение различными группами антидепрессантов (полициклические, селективные). Средняя длительность актуальной депрессии среди нонреспондеров составляла 6,5 мес.
При анализе психопатологических особенностей аффективных расстройств в данной группе больных не отмечено существенного влияния Торина у больных с тоскливой депрессией, а также у 2 пациентов с апатоадинамическим и у 5 – с затяжным (более 1 года) депрессивно-ипохондрическим состоянием.
Переносимость препарата. Установлен благоприятный профиль безопасности препарата. Нежелательные явления, связанные с Торином, отмечены у 6 (20%) пациентов преимущественно в течение первых 2 нед терапии.
В соответствии с целью исследования особое внимание уделялось влиянию Торина на основные гемодинамические показатели. Ни в одном из наблюдений не зарегистрированы клинически значимые взаимодействия между Торином и средствами, направленными на коррекцию сердечно-сосудистой патологии.
На момент окончания терапии у больных изученной выборки не зафиксировано появления жизнеопасных аритмий и/или внутрисердечных блокад. В ходе исследования не отмечено клинически значимого изменения АД (включая ортостатическую гипотензию), а также значимых изменений ЧСС. Относительно результатов холтеровского мониторирования можно отметить отсутствие достоверных отличий по показателям суправентрикулярной и вентрикулярной эктопической активности, а также динамики сегмента ST. Также следует отметить отсутствие динамики интервала QT и QTc на фоне приема препарата, на что особенно обращают внимание при назначении антидепрессантов, учитывая способность трициклических антидепрессантов удлинять интервал QT и вызывать угрожающие жизни желудочковые тахикардии типа «пируэт» (torsades de роintes) [9, 20]. Не обнаружено и влияния на показатели крови.
Связанные с препаратом побочные эффекты, послужившие причиной преждевременного прекращения терапии, отмечены в 2 случаях (по 1 наблюдению – тошнота и рвота, затрудненное мочеиспускание).
Другими связанными с препаратом нежелательными явлениями являлись в 4 случаях усиление чувства тревоги с соматовегетативными проявлениями, в 3 – тошнота, по 1 случаю – сонливость в дневное время, затрудненное мочеиспускание, диарея, обстипация.
Отмена Торина не сопровождалась развитием признаков, свойственных синдрому отмены (утомляемость, сонливость, головная боль, тошнота, рвота, анорексия, сухость во рту, головокружение, понос, бессонница, тревога, раздражимость, дезориентация, парестезии, потливость).
Обсуждение
В результате проведенного исследования получены достоверные доказательства эффективности Торина в терапии депрессивных расстройств легкой или средней степени тяжести у больных с сердечно-сосудистой патологией.
Препарат обеспечивает редукцию психопатологических состояний у больных с соматическими заболеваниями. Терапевтический эффект препарата реализуется быстро. Клинически значимое обратное развитие психопатологических нарушений наряду с улучшением самочувствия регистрируется у большинства больных с 14-го дня терапии.
При использовании в терапии депрессивных расстройств у соматически больных Торин обладает благоприятным профилем переносимости и безопасности.
Полученные результаты свидетельствуют о том, что Торин не оказывает отрицательного влияния на течение соматической патологии (ишемическая болезнь сердца, артериальная гипертония, аритмии) и обеспечивает высокий уровень комплаентности пациентов. Эти данные полностью согласуются с имеющимися в литературе указаниями на то, что среди побочных эффектов препарата (табл. 4) чаще всего наблюдаются тошнота и умеренный седативный эффект [5, 16, 17,19, 21].


В исследовании не отмечено признаков взаимодействия Торина в средних терапевтических дозах (150 мг/день) с современными препаратами, применяющимися для лечения сердечно-сосудистых заболеваний, что также соотносится с данными литературы о безопасности комбинированной терапии с использованием этого тимоаналептика [6, 8, 13].
Данные настоящего исследования о терапевтической эффективности Торина при лечении депрессивных расстройств легкой или средней степени тяжести, его переносимости и безопасности позволяют сделать вывод о целесообразности использования препарата при лечении депрессивных состояний у больных с сопутствующей кардиологической патологией.
Список исп. литературыСкрыть список
15 января 2009
Количество просмотров: 1269
