Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№04 2013
Депрессии при сердечно-сосудистых заболеваниях №04 2013
Номера страниц в выпуске:4-9
Актуальность проблемы депрессий в кардиологии связана с широкой распространенностью, социальной значимостью рассматриваемой коморбидной патологии, а также с влиянием аффективных расстройств на лечение и прогноз сердечно-сосудистых заболеваний (ССЗ). Депрессия и ишемическая болезнь сердца (ИБС) находятся в реципрокных отношениях: каждое из этих заболеваний утяжеляет течение другого.
Резюме. В статье обобщен многолетний опыт исследования депрессий в кардиологической клинике. Рассмотрены эпидемиологические, динамические и прогностические факторы, а также психопатологические характеристики аффективных расстройств, коморбидных сердечно-сосудистой патологии. Представлена типологическая дифференциация депрессий в психокардиологии. Выделены соотношения ритмов депрессий с хронобиологическими механизмами и независимыми осцилляторами.
Ключевые слова: депрессия, кардиология, психопатология, типология.
Depression in cardiovascular diseases
A.B.Smulevich
Mental Health Research, Moscow;
First Moscow State Medical University I.M.Sechenov
Summary. The article summarizes decade’s experience of depression research in cardiology. Epidemiological, dynamical, prognostic factors and pshychopathological characteristics of affective disorders comorbid to cardio-vascular diseases are discussed. Classification of depression for psychocardiology is announced. Interrelations of depression rhythms with chronobiological mechanisms and independent oscillators are disclosed.
Key words: depression, cardiology, psychopathology, classification.
Актуальность проблемы депрессий в кардиологии связана с широкой распространенностью, социальной значимостью рассматриваемой коморбидной патологии, а также с влиянием аффективных расстройств на лечение и прогноз сердечно-сосудистых заболеваний (ССЗ). Депрессия и ишемическая болезнь сердца (ИБС) находятся в реципрокных отношениях: каждое из этих заболеваний утяжеляет течение другого.
Депрессии являются фактором, провоцирующим кардиологические заболевания (ИБС, инфаркт миокарда – ИМ, артериальную гипертензию – АГ), утяжеляющим их течение (рецидивирующие, продолжительные приступы стенокардии, нарушения сердечного ритма, высокая частота коронарных катастроф) за счет амплификации (усиления) соматических, болевых, астенических, вегетативных и других симптомокомплексов, ухудшающим прогноз телесного недуга, осложняющим терапию, повышающим риск повторных госпитализаций и их длительность.
В свою очередь ИБС может явиться причиной развития и видоизменения течения депрессии. ИМ нередко становится психотравмирующим фактором, с воздействием которого связано возникновение нозогенной депрессии. При тяжелом поражении сердца наблюдаются соматогенные – сосудистые депрессии, обусловленные нарушениями гемодинамики. Обострение ИБС может провоцировать наступление очередной депрессивной фазы эндогенной природы. Когда ИМ совпадает с уже развернутой депрессией, она обычно протрагируется, а иногда течение аффективной болезни становится хроническим (дистимия, хроническая депрессия).
В кардиологической практике пациенты с непсихотическими психическими расстройствами, как правило, являются сложной категорией длительно, с частыми обострениями, болеющих. При кардиальных проявлениях, угрожающих жизнедеятельности и/или снижающих качество жизни, часто отмечается гиподиагностика психических нарушений, обусловленная склонностью как врачей, так и пациентов рассматривать депрессивные и тревожные симптомы как психологически понятные и не требующие медицинского вмешательства. Общеизвестны факты избегания консультаций психиатров и лечения психотропными средствами из-за страха стигматизации.
По эпидемиологическим данным, уровень психических расстройств в кардиологической практике значимо выше, чем в популяции (рис. 1). При этом чаще всего встречаются депрессивные расстройства – 17–25% (в среднем 21%); рис. 2. Риск заболеть ИБС и АГ у лиц с депрессией (в том числе в анамнезе) в 2–3 раза выше, чем у лиц без аффективной патологии (J. van Melle и соавт., 2004; I.Janszky и соавт., 2010).
Клинически значимая депрессия у пациентов с ИБС может выявляться у каждого четвертого пациента, но с учетом всей совокупности расстройств аффективного спектра речь идет о еще более высокой верхней границе диапазона – до 50% и выше (K.Davidson и соавт., 2006; А.Б.Смулевич и соавт., 2005; Е.И.Чазов и соавт., 2007).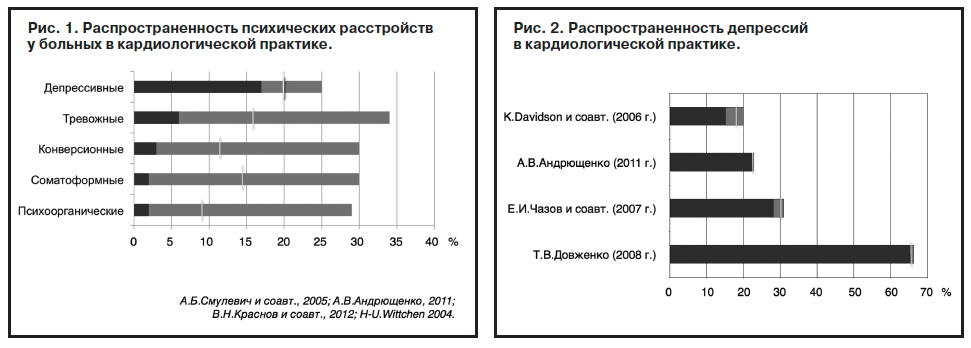
По результатам отечественного исследования КОМПАС, направленного на изучение депрессий в общесоматической практике (2002–2003 гг., 35 городов России), показатели распространенности гипотимических состояний при сердечно-сосудистой патологии (ИБС и АГ) составляют в среднем 23,8 и 46,1% соответственно, причем при АГ значение этого показателя достигает 52%, а при хронической сердечной недостаточности (ХСН) – 61%, что подтверждено результатами проспективного
(3-летнего) исследования (КООРДИНАТА, 2007).
Депрессия входит в число основных факторов риска ИМ даже в тех случаях, когда ИБС протекает без тяжелых проявлений, как и риска инсульта при АГ. У лиц, перенесших аортокоронарное шунтирование (АКШ), депрессивные и тревожные расстройства наблюдаются в 30–40% случаев (Ph.Tully, R.Baker, 2012).
При оценке факторов риска депрессий у кардиологических больных рассматривается ряд клинических, патофизиологических и социальных явлений. В числе наиболее значимых факторов выделяют униполярные или биполярные депрессии и/или тревожные расстройства в анамнезе; алкоголизм, наркомании, женский пол, наследственное предрасположение к психическим расстройствам и в первую очередь – к аффективным (T.Naqvi и соавт., 2007).
В исследованиях, интерпретирующих корреляции между аффективными расстройствами и ССЗ, приводится информация, позволяющая предполагать общность генетической предрасположенности к депрессиям и ИБС. Хотя в структуре подверженности могут участвовать различные механизмы, наиболее вероятный вклад вносят гены-кандидаты, отвечающие за процесс воспаления, а также за обмен серотонина (J.McCaffery и соавт., 2006).
В свете предиспозиции рассматривается также преморбидный конституциональный склад пациента, а именно расстройства личности аффективного круга (циклоиды, гипертимики, конституционально депрессивные). Важную роль играют конституционально обусловленные нарушения телесного самосознания по типу соматоперцептивных акцентуаций – соматопатия, соматотония, проприоцептивный диатез, сегментарная деперсонализация (А.Б.Смулевич, 2014).
К факторам, провоцирующим манифестацию психических нарушений у кардиологических больных, следует отнести также ятрогении – неблагоприятное воздействие на психическое состояние больного некоторых методов терапии, в том числе медикаментозных1. В целом риск возникновения ятрогенных психических нарушений относительно невысок, однако для пациентов с психическими расстройствами в анамнезе возрастает.
Выявлена зависимость между риском расстройств аффективного спектра у кардиологических больных и социальной дезадаптацией. По эпидемиологическим данным, эта корреляция определяется отсутствием доступной социальной поддержки, особенно при низком уровне образования и дохода. Однако клинические наблюдения свидетельствуют о том, что в ситуации жизнеугрожающего кардиологического заболевания депрессии возникают и у больных хорошо образованных, активно участвующих в трудовой деятельности.
Прогноз при ССЗ тесно связан с нейрохимическими и патофизиологическими механизмами, а также с характером психокардиологических соотношений и при наличии депрессии и/или тревожного расстройства ухудшается (Z.Khayyam-Nekoei и соавт., 2012), что достоверно связано с повышением тяжести стенокардии нестабильного течения (В.С.Собенников, Ф.И.Белялов, 2010; C.Dessotte и соавт., 2013). Так, в течение первого года число ишемических событий (повторный ИМ, опасные для жизни нарушения сердечного ритма) возрастает в 1,4–6,7 раза, фатальных событий (внезапная коронарная смерть) – в 1,4–6,0 раза (А.Б.Смулевич, А.Л.Сыркин, 2005). После первого острого ИМ (ОИМ) при наличии коморбидной депрессии повышается вероятность развития ХСН: отношение шансов 1:4 (H.May и соавт., 2009); рис. 3.
Риск смерти в течение 18 мес после ИМ при наличии депрессии повышается на 17–20% по сравнению с 3–4% при отсутствии аналогичных психических нарушений (F.Lesperance и соавт., 2002). Крайне неблагоприятный прогноз отмечается у больных с депрессией и частой желудочковой экстрасистолией. Риск развития острого коронарного синдрома или кардиоваскулярной смертности наиболее высок у мужчин старше 70 лет. Депрессия ассоциируется с повышением в 8,6 раза риска рецидива фибрилляции предсердий после успешного восстановления синусового ритма. Трехлетнее наблюдение лиц с фибрилляцией предсердий показало, что возникновение депрессий повышает риск аритмической смерти на 69% (см. рис. 2).
По показателям тяжелых осложнений и летального исхода депрессия сопоставима с такими факторами риска, как дисфункция левого желудочка, недостаточность кровообращения, предшествующие ИМ, сопутствующий сахарный диабет и хроническая обструктивная болезнь легких.
Анализ прогностической роли депрессий, по данным INTER-HEART Study, показал, что депрессия заняла 3-е место среди девяти факторов риска смерти от кардиоваскулярных событий. Депрессивные расстройства являются фактором повышенной смертности от коронарной болезни (см. рис. 3, 4). При сравнении данных о летальности после ИМ у больных, не обнаруживающих аффективных расстройств и у страдающих депрессией, оказывается, что наряду с общей характеристикой – закономерным повышением показателя смертности в течение первых 6 мес после ИМ и его стабилизацией в последующие 12 мес доля умерших при сочетании ИМ с депрессией не менее чем в 5 раз выше.
18 мес – до 3,54, превышая смертность больных, у которых ИМ не осложняется депрессией: 16,5% против 3% через 6 мес; 20% против 6% через 18 мес соответственно (N.Frasure-Smith и соавт., 1995; Ch.Nemeroff, 2003). Негативное влияние депрессии на выживаемость после ИМ и частоту госпитализаций сохраняется после поправки на другие факторы риска (возраст, функциональный класс ХСН, выброс левого желудочка, пиковое потребление кислорода).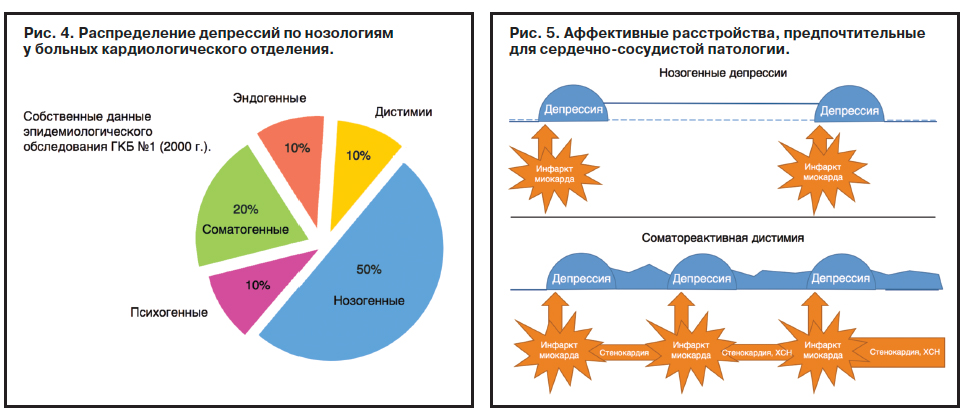
На улучшение прогноза ИБС в последние годы повлияло не только применение более эффективных современных соматотропных средств (статинов, тромболитиков, ингибиторов ангиотензинпревращающего фермента – АПФ), реваскуляризационных процедур, инструментальных методов лечения аритмий, но и адекватное лечение с присоединением к базисной терапии психотропных препаратов (прежде всего антидепрессантов группы селективных ингибиторов обратного захвата серотонина – СИОЗС). Так, по данным S.Kimmel и соавт. (2011 г.), предшествующий первому ИМ длительный (более 3 мес) прием СИОЗС (пароксетина, сертралина, флуоксетина, циталопрама) ассоциирован со статистически значимой редукцией риска ИМ (отношение шансов 0,77; 95% доверительный интервал 0,57–1,03). Эти данные подтверждаются результатами исследований, посвященных изучению СИОЗС как фактора снижения риска повторного ИМ после перенесенной сосудистой катастрофы (W.Sauer и соавт., 2001; R.Schlienger и соавт., 2004)2.
В этом контексте особое значение приобретает дискуссия, связанная с возможностью эффективной антидепрессивной терапии оптимизировать прогноз при коморбидной депрессии кардиальной патологии.
По мнению P.Shapiro (2013 г.), полная редукция депрессивных симптомов является бесспорным предиктором благоприятного прогноза ССЗ. Однако выводы рандомизированного контролируемого исследования M.Zuidersma и соавт. (2013 г.) «Лечение депрессии после ОИМ и долгосрочный прогноз риска сердечно-сосудистых осложнений и смертности» менее оптимистичны. Полученные результаты позволили авторам поставить под сомнение тот факт, что лечение коморбидных ИБС аффективных расстройств приводит к улучшению долгосрочного прогноза и снижению сердечно-сосудистой смертности. Проспективное наблюдение (длительность – 8 лет) показало, что применение тимоаналептиков не снижает риск кардиоваскулярных осложнений и смерти, но при этом повышает выживаемость при долгосрочном наблюдении. Является ли последняя корреляция прямым результатом собственно антидепрессивной терапии или зависит от ряда дополнительных факторов (отношение к болезни, комплаенс и пр.), остается проблемой, не имеющей до сих пор однозначного решения и требующей дальнейших исследований с учетом требований доказательной медицины.
При оценке негативного влияния депрессий на течение и исход ИБС нельзя рассматривать гипотимический симптомокомплекс как эпифеномен – необходима клиническая дифференциация аффективных расстройств. По данным ряда исследований (R.Carney, K.Freedland, 2012), наибольший риск в плане манифестации острого коронарного синдрома, повторных ИМ летального исхода ССЗ представляют не рекуррентные депрессии, манифестирующие задолго до соматической катастрофы, и не транзиторные гипотимии, длящиеся не более 2 нед, а первый депрессивный эпизод, дебютирующий в непосредственной связи с ОИМ. Среди аффективных расстройств, являющихся фактором высокого риска неблагоприятного течения кардиальной патологии, J.Shaffer и соавт. (2011 г.) наряду с этим фактором («индуцированная воспалением депрессия») выделяют и депрессию с ангедонией, рассматриваемую как вариант циркулярной меланхолии. Вместе с тем формирование невротической депрессии3, по мнению авторов, не оказывает существенного влияния на течение и исход ССЗ.
Типологическая структура депрессий у больных с ССЗ в оценке по Международной классификации болезней 10-го пересмотра включает расстройства адаптации, депрессивные эпизоды и рекуррентные депрессии, дистимии, органические аффективные расстройства. Однако долевое распределение этих расстройств по материалам разных публикаций варьирует в широких пределах (рис. 4).
В соответствии с данными исследований Е.А.Степановой (2011 г.), выполненных в нашей клинике на репрезентативной выборке, включающей 106 наблюдений, среди контингента больных с ИБС преобладают пациенты с расстройствами адаптации (нозогенные депрессии – 61,3%), депрессивный эпизод диагностирован у 21,7% больных, рекуррентная депрессия – у 7,5%, дистимия – менее чем у 5%, соматогенные депрессии – у 2,8%. В то же время, по материалам М.В.Семиглазовой (2008 г.), депрессивные реакции, относящиеся к расстройствам адаптации, составляют всего 13,9%. Выявленные расхождения могут быть связаны с клинической неоднородностью кардиальной патологии у обследованных больных – казуистика М.В.Семиглазовой представлена более тяжелой патологией – ОИМ, чему соответствуют и более выраженные аффективные расстройства.
Клинически значимой характеристикой депрессий, коморбидных ИБС, является их ритмологическая составляющая. При этом в качестве «задающего ритм» фактора могут выступать не только собственные осцилляторы аффективной патологии, но и триггеры, заимствованные у кардиологического заболевания. В соответствии с ритмологическими характеристиками, свойственными аффективным расстройствам, манифестирующим в общемедицинской практике, гипотимические состояния при ССЗ распределяются в пределах континуума, противоположные полюса которого принадлежат нозогенным и соматогенным депрессиям соответственно, а среди промежуточных форм выделяется соматореактивная дистимия.
Среди всего многообразия манифестирующих в пространстве сердечно-сосудистой патологии аффективных расстройств ниже будут рассмотрены два представляющих наибольшее клиническое значение в плане коморбидных соотношений с кардиальной патологией типа депрессий – нозогенные и соматореактивная дистимия (рис. 5).
Нозогенные депрессии – большая часть коморбидных ИБС аффективных расстройств – манифестируют как в инициальном периоде ССЗ (П.И.Сидоров, И.А.Новикова, 2008), так и на более поздних его этапах (после ОИМ и повторных ИМ, АКШ).
Нозогении развиваются в соответствии с заимствованным ритмом, определяющимся динамикой ССЗ как в отношении манифестации и обратного развития аффективных расстройств (совпадают с обострением и периодом стабилизации ИБС), так и суточных колебаний состояния. (Углубление подавленности во второй половине дня в связи с вечерними и ночными приступами стенокардии, улучшение настроения по утрам при нормализации основных гемодинамических показателей.)
Психопатологические проявления начальных этапов депрессий маскируются симптоматикой астенического ряда с жалобами на бессилие, утомляемость, отсутствие энергии, плохой сон (C.Rafanelli и соавт., 2007).
Развернутую картину нозогенных депрессий отличает полиморфизм психопатологических симптомокомплексов, включающих тревогу, подавленность, превалирующих над собственно аффективными, соматовегетативные проявления – нарушения сна, тахикардия, горечь во рту и др. (М.В.Семиглазова, 2008; Т.В.Довженко и др., 2011). Вместе с тем типологическая структура нозогенных депрессий в большинстве случаев достаточно однородна – чаще наблюдаются депрессии тревожные и ипохондрические.
Наряду с подавленностью и угнетенностью в структуре нозогенных депрессий выделяются тревожно-фобические расстройства – и в первую очередь трактуемые как предиктор нарастающей тяжести аффективных расстройств тревожные руминации (E.Danton и соавт., 2012). В их содержании превалируют опасения повторного приступа стенокардии, ИМ или инсульта, страх инвалидизации, повторных госпитализаций. Круг тревожных расстройств может расширяться за счет явлений невротической ипохондрии, сопровождающихся обостренным самонаблюдением и тщательной регистрацией малейших признаков телесного неблагополучия. В некоторых случаях содержанием тревожных руминаций становятся опасения социальных последствий болезни, возможности достижения поставленных ранее профессиональных целей, семейные и материальные проблемы.
При депрессиях, совпадающих с периодом реконвалесценции после ОИМ, возможен страх телесной уязвимости, снижения толерантности к нагрузкам, проявляющийся феноменом «поведенческой деактивации» (behavioral deactivation; J.Skala и соавт., 2005), сопровождающейся самощажением и как следствие – значительным снижением физической активности.
Депрессии, перекрывающиеся с ССЗ, сопряжены с высоким суицидальным риском.
Соматореактивная дистимия – категория, объединяющая группу затяжных атипичных аффективных расстройств, манифестирующих параллельно соматической (кардиальной) патологии и коррелирующих с дальнейшим течением ССЗ. По своим клиническим проявлениям соматореактивная дистимия не может с определенностью быть отнесена ни к чисто психогенным (нозогенные реакции), ни к чисто эндогенным аффективным заболеваниям, ни к ипохондрическим развитиям.
Риск развития соматореактивной дистимии увеличивается с возрастом. В исследовании B.Baune и соавт. (2006 г.) приводятся данные о значительно более высокой распространенности дистимии и униполярной депрессии у лиц пожилого возраста, страдающих ИБС и перенесших ИМ.
Соматореактивная дистимия формируется при явлениях психосоматического стресса – ОИМ или повторного ИМ (особенно с выраженными болевыми ощущениями, жизнеугрожающими нарушениями ритма), АКШ. В непосредственной временной связи с коронарной катастрофой или вслед за оперативным вмешательством возникает острое тревожно-депрессивное состояние по типу экзистенционального криза. В этот период, как показали исследования, проведенные в нашей клинике (М.А.Самушия, 2006; Б.А.Волель, 2009; Е.А.Степанова, 2011), на фоне витальной тревоги при доминирующем ощущении угрозы существованию и танатофобии формируются диссоциативные расстройства, проявляющиеся глубокими нарушениями интеграции психики и в первую очередь расстройствами идентичности личности – отчуждением сознания, прежнего «я». Психопатологические образования персонифицируются – сопровождаются становлением феномена «прозрения», «переоценки ценностей», осознания себя другим человеком, «новой несопоставимой с прежней» личностью, с кардинальным изменением приоритетов, системы ценностей и представлений о смысле жизни.
Сопоставимость расстройств самосознания при соматореактивной дистимии с перитравматической диссоциацией свидетельствует о существенных, обнаруживающихся уже в дебюте отличиях этой патологии от транзиторных нозогенных реакций с диссоциативными расстройствами истеро-невротического регистра (синдромы «прекрасного равнодушия», «множественной личности» с фрагментарным отчуждением сознания соматической болезни и др.).
Аффективные расстройства, манифестирующие в рамках соматореактивной дистимии вслед за соматической катастрофой или оперативным вмешательством, на первых этапах протекают по типу нозогенной депрессии и лишь затем принимают затяжное течение. Однако содержание депрессии с самого начала обнаруживает некоторые отличия от преходящих нозогенных реакций. Уже с момента госпитализации и установления диагноза, независимо от тяжести состояния (даже в случаях ограниченного поражения миокарда – очаговый ИМ или благоприятного исхода АКШ), формируются представления о необратимости произошедшей катастрофы, обреченности, невозможности возврата к прежнему образу жизни. Уже в это время формируется новая шкала ценностей, планируется отказ от прежней профессиональной деятельности, щадящий режим, оформление пенсии или инвалидности (феномен «новой жизни»). Доминирующей идеей становится контроль над событиями, «опасными» для больного сердца.
В дальнейшем нозогенная депрессия принимает форму дистимии, динамика которой сочетанно синхронизируется как с ритмом развития кардиальной патологии, так и с аутохтонным ритмом аффективного заболевания.
Клиническая картина соматореактивной дистимии на протяжении многих лет определяется униполярным тревожно-депрессивным расстройством с преобладанием соматовегетативных и ипохондрических симптомокомплексов.
Периодически возникающие обострения в виде двойных депрессий связаны либо с экзацербацией кардиальной патологии (повторные ИМ, приступы стенокардии и др.), либо манифестируют аутохтонно в периоды относительной компенсации ССЗ. Клинические проявления аффективных фаз, как правило, формируют картину эндоморфной депрессии – включают ряд витальных расстройств, свойственных циркулярной меланхолии (тоска с загрудинной локализацией, приобретающая физикальный характер, ощущение утраты жизненного тонуса, идеи самообвинения, подчиненность аффективных симптомокомплексов циркадианному ритму).
Дистимические расстройства, коморбидные ИБС, в отличие от эндореактивной дистимии (H.Weitbrecht, 1952) не утрачивают связи с патогенной ситуацией.
В содержании депрессии доминируют представления, отражающие неразрешимость психотравмирующего воздействия соматического страдания (H.Akiskal, 1982; K.Achte,1986; E.Murphy, 1990; M.Friedman, 1993).
Кардиологическая патология, коморбидная аффективной, чаще всего требует разграничения с кардионеврозом. Такая дифференциация особенно сложна в тех случаях, когда проявления кардионевроза также сочетаются с депрессиями.
Как показали исследования К.А.Албантовой (2010 г.), депрессии наблюдаются более чем у 1/2 (59,21%) больных кардионеврозом. В других исследованиях, выполненных на контингенте соматического стационара, приводятся еще более высокие цифры – 82,25% (Т.В.Довженко и соавт., 2011), причем преобладают гипотимии легкой и средней тяжести.
При решении дифференциально-диагностических задач необходимо учитывать различия в коморбидных соотношениях в парах: депрессия/ИБС и депрессия/ кардионевроз. Если при ИБС депрессия формируется в определенном временном интервале после манифестации сердечной катастрофы, то кардионевротический симптомокомплекс появляется чаще всего одновременно с нарушениями настроения. При этом проявления кардионевроза воспринимаются пациентами как неотъемлемая составная часть сниженного настроения, физические проявления психического неблагополучия. Перекрывание ИБС и депрессии демонстрирует полярные соотношения – гипотимия во всех случаях рассматривается в качестве вторичного по отношению к кардиальной патологии психопатологического образования.
Необходимо подчеркнуть и различия в типологической структуре депрессий, коморбидных кардионеврозу и ИБС. У больных кардионеврозом наряду с тревожными (преобладающими при ИБС) чаще наблюдаются истерические депрессии, протекающие с массивной конверсионной симптоматикой, а также гипотимии астенического типа. Тревожная составляющая депрессий при ИБС ограничена генерализованной тревогой и фобиями. Депрессии при кардионеврозе включают значительно более широкий круг анксиозных расстройств: наряду с ипохондрическими фобиями наблюдаются панические атаки, протекающие в 1/3 (33,3%) случаев, с явлениями стойкой агорафобии (К.А.Албантова, 2010), тогда как при ИБС агорафобия относится к сравнительно редким феноменам.
Примечания
1Наиболее часто в литературе отмечаются побочные эффекты при использовании a-адреноблокаторов (депрессия, сексуальная дисфункция); амиодарона и ингибиторов АПФ (мании, депрессии); сердечных гликозидов, в частности дигоксина (депрессии, зрительные галлюцинации, делирий); гиполипидемических средств, в частности холестирамина; кортикостероидов (тревога, депрессия, ажитация), нестероидных противовоспалительных препаратов (депрессия). Следует обратить внимание, что современные исследования не подтвердили депрессогенного эффекта b-адреноблокаторов у больных ИБС и АГ (Ko и соавт., 2002). В последнее время показано, что применение статинов, которое в прошлом связывалось с риском развития депрессии и тревожных расстройств, при ИБС, напротив, снижается, что предположительно связано с их противовоспалительным эффектом.
2Хотя по данным крупных исследований (ENRICHD, SADHART, MIND-IT) значимого влияния терапии депрессии на исходы ИБС не обнаружено, возникает целый ряд вопросов об адекватности проводимого антидепрессивного лечения, в частности эффективности краткосрочного применения препаратов группы СИОЗС или когнитивно-бихевиоральной терапии (L.Berkman и соавт., 2003). Возможно, решающее значение для оценки результатов имеют адекватность терапевтического вмешательства и характер ответа на лечение. В ряде исследований представлены данные о затяжных, резистентных к психотропным препаратам депрессиях как предикторе персистирования кардиальной патологии, высокой частоты повторных госпитализаций, летального исхода у больных ИБС (R.Carney, K.Freedland, 2012; K.Freedland, R.Carney, 2013; B.Foss-Neradko и соавт., 2012).
3В структуре депрессий невротического уровня могут формироваться соматизированные расстройства – чаще кардионевротические (синдром да Коста – кардиалгии, изменения ритма и сердечных сокращений, колебания артериального давления), сопряженные с тревожными опасениями, страхами ипохондрического содержания (танато-, кардиофобии), паническими атаками, ипохондрическим самонаблюдением. Подобные проявления усложняют картину ИБС, а в некоторых случаях дублируют симптомокомплексы ангинозного приступа.
Сведения об авторе
Смулевич Анатолий Болеславович – д-р мед. наук, проф., акад. РАМН, рук. отд. по изучению пограничной психической патологии и психосоматических расстройств ФГБУ НЦПЗ РАМН; зав. каф. психиатрии и психосоматики ФППОВ ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России
Ключевые слова: депрессия, кардиология, психопатология, типология.
Depression in cardiovascular diseases
A.B.Smulevich
Mental Health Research, Moscow;
First Moscow State Medical University I.M.Sechenov
Summary. The article summarizes decade’s experience of depression research in cardiology. Epidemiological, dynamical, prognostic factors and pshychopathological characteristics of affective disorders comorbid to cardio-vascular diseases are discussed. Classification of depression for psychocardiology is announced. Interrelations of depression rhythms with chronobiological mechanisms and independent oscillators are disclosed.
Key words: depression, cardiology, psychopathology, classification.
Актуальность проблемы депрессий в кардиологии связана с широкой распространенностью, социальной значимостью рассматриваемой коморбидной патологии, а также с влиянием аффективных расстройств на лечение и прогноз сердечно-сосудистых заболеваний (ССЗ). Депрессия и ишемическая болезнь сердца (ИБС) находятся в реципрокных отношениях: каждое из этих заболеваний утяжеляет течение другого.
Депрессии являются фактором, провоцирующим кардиологические заболевания (ИБС, инфаркт миокарда – ИМ, артериальную гипертензию – АГ), утяжеляющим их течение (рецидивирующие, продолжительные приступы стенокардии, нарушения сердечного ритма, высокая частота коронарных катастроф) за счет амплификации (усиления) соматических, болевых, астенических, вегетативных и других симптомокомплексов, ухудшающим прогноз телесного недуга, осложняющим терапию, повышающим риск повторных госпитализаций и их длительность.
В свою очередь ИБС может явиться причиной развития и видоизменения течения депрессии. ИМ нередко становится психотравмирующим фактором, с воздействием которого связано возникновение нозогенной депрессии. При тяжелом поражении сердца наблюдаются соматогенные – сосудистые депрессии, обусловленные нарушениями гемодинамики. Обострение ИБС может провоцировать наступление очередной депрессивной фазы эндогенной природы. Когда ИМ совпадает с уже развернутой депрессией, она обычно протрагируется, а иногда течение аффективной болезни становится хроническим (дистимия, хроническая депрессия).
В кардиологической практике пациенты с непсихотическими психическими расстройствами, как правило, являются сложной категорией длительно, с частыми обострениями, болеющих. При кардиальных проявлениях, угрожающих жизнедеятельности и/или снижающих качество жизни, часто отмечается гиподиагностика психических нарушений, обусловленная склонностью как врачей, так и пациентов рассматривать депрессивные и тревожные симптомы как психологически понятные и не требующие медицинского вмешательства. Общеизвестны факты избегания консультаций психиатров и лечения психотропными средствами из-за страха стигматизации.
По эпидемиологическим данным, уровень психических расстройств в кардиологической практике значимо выше, чем в популяции (рис. 1). При этом чаще всего встречаются депрессивные расстройства – 17–25% (в среднем 21%); рис. 2. Риск заболеть ИБС и АГ у лиц с депрессией (в том числе в анамнезе) в 2–3 раза выше, чем у лиц без аффективной патологии (J. van Melle и соавт., 2004; I.Janszky и соавт., 2010).
Клинически значимая депрессия у пациентов с ИБС может выявляться у каждого четвертого пациента, но с учетом всей совокупности расстройств аффективного спектра речь идет о еще более высокой верхней границе диапазона – до 50% и выше (K.Davidson и соавт., 2006; А.Б.Смулевич и соавт., 2005; Е.И.Чазов и соавт., 2007).

По результатам отечественного исследования КОМПАС, направленного на изучение депрессий в общесоматической практике (2002–2003 гг., 35 городов России), показатели распространенности гипотимических состояний при сердечно-сосудистой патологии (ИБС и АГ) составляют в среднем 23,8 и 46,1% соответственно, причем при АГ значение этого показателя достигает 52%, а при хронической сердечной недостаточности (ХСН) – 61%, что подтверждено результатами проспективного
(3-летнего) исследования (КООРДИНАТА, 2007).
Депрессия входит в число основных факторов риска ИМ даже в тех случаях, когда ИБС протекает без тяжелых проявлений, как и риска инсульта при АГ. У лиц, перенесших аортокоронарное шунтирование (АКШ), депрессивные и тревожные расстройства наблюдаются в 30–40% случаев (Ph.Tully, R.Baker, 2012).
При оценке факторов риска депрессий у кардиологических больных рассматривается ряд клинических, патофизиологических и социальных явлений. В числе наиболее значимых факторов выделяют униполярные или биполярные депрессии и/или тревожные расстройства в анамнезе; алкоголизм, наркомании, женский пол, наследственное предрасположение к психическим расстройствам и в первую очередь – к аффективным (T.Naqvi и соавт., 2007).
В исследованиях, интерпретирующих корреляции между аффективными расстройствами и ССЗ, приводится информация, позволяющая предполагать общность генетической предрасположенности к депрессиям и ИБС. Хотя в структуре подверженности могут участвовать различные механизмы, наиболее вероятный вклад вносят гены-кандидаты, отвечающие за процесс воспаления, а также за обмен серотонина (J.McCaffery и соавт., 2006).
В свете предиспозиции рассматривается также преморбидный конституциональный склад пациента, а именно расстройства личности аффективного круга (циклоиды, гипертимики, конституционально депрессивные). Важную роль играют конституционально обусловленные нарушения телесного самосознания по типу соматоперцептивных акцентуаций – соматопатия, соматотония, проприоцептивный диатез, сегментарная деперсонализация (А.Б.Смулевич, 2014).
К факторам, провоцирующим манифестацию психических нарушений у кардиологических больных, следует отнести также ятрогении – неблагоприятное воздействие на психическое состояние больного некоторых методов терапии, в том числе медикаментозных1. В целом риск возникновения ятрогенных психических нарушений относительно невысок, однако для пациентов с психическими расстройствами в анамнезе возрастает.
Выявлена зависимость между риском расстройств аффективного спектра у кардиологических больных и социальной дезадаптацией. По эпидемиологическим данным, эта корреляция определяется отсутствием доступной социальной поддержки, особенно при низком уровне образования и дохода. Однако клинические наблюдения свидетельствуют о том, что в ситуации жизнеугрожающего кардиологического заболевания депрессии возникают и у больных хорошо образованных, активно участвующих в трудовой деятельности.
Прогноз при ССЗ тесно связан с нейрохимическими и патофизиологическими механизмами, а также с характером психокардиологических соотношений и при наличии депрессии и/или тревожного расстройства ухудшается (Z.Khayyam-Nekoei и соавт., 2012), что достоверно связано с повышением тяжести стенокардии нестабильного течения (В.С.Собенников, Ф.И.Белялов, 2010; C.Dessotte и соавт., 2013). Так, в течение первого года число ишемических событий (повторный ИМ, опасные для жизни нарушения сердечного ритма) возрастает в 1,4–6,7 раза, фатальных событий (внезапная коронарная смерть) – в 1,4–6,0 раза (А.Б.Смулевич, А.Л.Сыркин, 2005). После первого острого ИМ (ОИМ) при наличии коморбидной депрессии повышается вероятность развития ХСН: отношение шансов 1:4 (H.May и соавт., 2009); рис. 3.

Риск смерти в течение 18 мес после ИМ при наличии депрессии повышается на 17–20% по сравнению с 3–4% при отсутствии аналогичных психических нарушений (F.Lesperance и соавт., 2002). Крайне неблагоприятный прогноз отмечается у больных с депрессией и частой желудочковой экстрасистолией. Риск развития острого коронарного синдрома или кардиоваскулярной смертности наиболее высок у мужчин старше 70 лет. Депрессия ассоциируется с повышением в 8,6 раза риска рецидива фибрилляции предсердий после успешного восстановления синусового ритма. Трехлетнее наблюдение лиц с фибрилляцией предсердий показало, что возникновение депрессий повышает риск аритмической смерти на 69% (см. рис. 2).
По показателям тяжелых осложнений и летального исхода депрессия сопоставима с такими факторами риска, как дисфункция левого желудочка, недостаточность кровообращения, предшествующие ИМ, сопутствующий сахарный диабет и хроническая обструктивная болезнь легких.
Анализ прогностической роли депрессий, по данным INTER-HEART Study, показал, что депрессия заняла 3-е место среди девяти факторов риска смерти от кардиоваскулярных событий. Депрессивные расстройства являются фактором повышенной смертности от коронарной болезни (см. рис. 3, 4). При сравнении данных о летальности после ИМ у больных, не обнаруживающих аффективных расстройств и у страдающих депрессией, оказывается, что наряду с общей характеристикой – закономерным повышением показателя смертности в течение первых 6 мес после ИМ и его стабилизацией в последующие 12 мес доля умерших при сочетании ИМ с депрессией не менее чем в 5 раз выше.
18 мес – до 3,54, превышая смертность больных, у которых ИМ не осложняется депрессией: 16,5% против 3% через 6 мес; 20% против 6% через 18 мес соответственно (N.Frasure-Smith и соавт., 1995; Ch.Nemeroff, 2003). Негативное влияние депрессии на выживаемость после ИМ и частоту госпитализаций сохраняется после поправки на другие факторы риска (возраст, функциональный класс ХСН, выброс левого желудочка, пиковое потребление кислорода).

На улучшение прогноза ИБС в последние годы повлияло не только применение более эффективных современных соматотропных средств (статинов, тромболитиков, ингибиторов ангиотензинпревращающего фермента – АПФ), реваскуляризационных процедур, инструментальных методов лечения аритмий, но и адекватное лечение с присоединением к базисной терапии психотропных препаратов (прежде всего антидепрессантов группы селективных ингибиторов обратного захвата серотонина – СИОЗС). Так, по данным S.Kimmel и соавт. (2011 г.), предшествующий первому ИМ длительный (более 3 мес) прием СИОЗС (пароксетина, сертралина, флуоксетина, циталопрама) ассоциирован со статистически значимой редукцией риска ИМ (отношение шансов 0,77; 95% доверительный интервал 0,57–1,03). Эти данные подтверждаются результатами исследований, посвященных изучению СИОЗС как фактора снижения риска повторного ИМ после перенесенной сосудистой катастрофы (W.Sauer и соавт., 2001; R.Schlienger и соавт., 2004)2.
В этом контексте особое значение приобретает дискуссия, связанная с возможностью эффективной антидепрессивной терапии оптимизировать прогноз при коморбидной депрессии кардиальной патологии.
По мнению P.Shapiro (2013 г.), полная редукция депрессивных симптомов является бесспорным предиктором благоприятного прогноза ССЗ. Однако выводы рандомизированного контролируемого исследования M.Zuidersma и соавт. (2013 г.) «Лечение депрессии после ОИМ и долгосрочный прогноз риска сердечно-сосудистых осложнений и смертности» менее оптимистичны. Полученные результаты позволили авторам поставить под сомнение тот факт, что лечение коморбидных ИБС аффективных расстройств приводит к улучшению долгосрочного прогноза и снижению сердечно-сосудистой смертности. Проспективное наблюдение (длительность – 8 лет) показало, что применение тимоаналептиков не снижает риск кардиоваскулярных осложнений и смерти, но при этом повышает выживаемость при долгосрочном наблюдении. Является ли последняя корреляция прямым результатом собственно антидепрессивной терапии или зависит от ряда дополнительных факторов (отношение к болезни, комплаенс и пр.), остается проблемой, не имеющей до сих пор однозначного решения и требующей дальнейших исследований с учетом требований доказательной медицины.
При оценке негативного влияния депрессий на течение и исход ИБС нельзя рассматривать гипотимический симптомокомплекс как эпифеномен – необходима клиническая дифференциация аффективных расстройств. По данным ряда исследований (R.Carney, K.Freedland, 2012), наибольший риск в плане манифестации острого коронарного синдрома, повторных ИМ летального исхода ССЗ представляют не рекуррентные депрессии, манифестирующие задолго до соматической катастрофы, и не транзиторные гипотимии, длящиеся не более 2 нед, а первый депрессивный эпизод, дебютирующий в непосредственной связи с ОИМ. Среди аффективных расстройств, являющихся фактором высокого риска неблагоприятного течения кардиальной патологии, J.Shaffer и соавт. (2011 г.) наряду с этим фактором («индуцированная воспалением депрессия») выделяют и депрессию с ангедонией, рассматриваемую как вариант циркулярной меланхолии. Вместе с тем формирование невротической депрессии3, по мнению авторов, не оказывает существенного влияния на течение и исход ССЗ.
Типологическая структура депрессий у больных с ССЗ в оценке по Международной классификации болезней 10-го пересмотра включает расстройства адаптации, депрессивные эпизоды и рекуррентные депрессии, дистимии, органические аффективные расстройства. Однако долевое распределение этих расстройств по материалам разных публикаций варьирует в широких пределах (рис. 4).
В соответствии с данными исследований Е.А.Степановой (2011 г.), выполненных в нашей клинике на репрезентативной выборке, включающей 106 наблюдений, среди контингента больных с ИБС преобладают пациенты с расстройствами адаптации (нозогенные депрессии – 61,3%), депрессивный эпизод диагностирован у 21,7% больных, рекуррентная депрессия – у 7,5%, дистимия – менее чем у 5%, соматогенные депрессии – у 2,8%. В то же время, по материалам М.В.Семиглазовой (2008 г.), депрессивные реакции, относящиеся к расстройствам адаптации, составляют всего 13,9%. Выявленные расхождения могут быть связаны с клинической неоднородностью кардиальной патологии у обследованных больных – казуистика М.В.Семиглазовой представлена более тяжелой патологией – ОИМ, чему соответствуют и более выраженные аффективные расстройства.
Клинически значимой характеристикой депрессий, коморбидных ИБС, является их ритмологическая составляющая. При этом в качестве «задающего ритм» фактора могут выступать не только собственные осцилляторы аффективной патологии, но и триггеры, заимствованные у кардиологического заболевания. В соответствии с ритмологическими характеристиками, свойственными аффективным расстройствам, манифестирующим в общемедицинской практике, гипотимические состояния при ССЗ распределяются в пределах континуума, противоположные полюса которого принадлежат нозогенным и соматогенным депрессиям соответственно, а среди промежуточных форм выделяется соматореактивная дистимия.
Среди всего многообразия манифестирующих в пространстве сердечно-сосудистой патологии аффективных расстройств ниже будут рассмотрены два представляющих наибольшее клиническое значение в плане коморбидных соотношений с кардиальной патологией типа депрессий – нозогенные и соматореактивная дистимия (рис. 5).
Нозогенные депрессии – большая часть коморбидных ИБС аффективных расстройств – манифестируют как в инициальном периоде ССЗ (П.И.Сидоров, И.А.Новикова, 2008), так и на более поздних его этапах (после ОИМ и повторных ИМ, АКШ).
Нозогении развиваются в соответствии с заимствованным ритмом, определяющимся динамикой ССЗ как в отношении манифестации и обратного развития аффективных расстройств (совпадают с обострением и периодом стабилизации ИБС), так и суточных колебаний состояния. (Углубление подавленности во второй половине дня в связи с вечерними и ночными приступами стенокардии, улучшение настроения по утрам при нормализации основных гемодинамических показателей.)
Психопатологические проявления начальных этапов депрессий маскируются симптоматикой астенического ряда с жалобами на бессилие, утомляемость, отсутствие энергии, плохой сон (C.Rafanelli и соавт., 2007).
Развернутую картину нозогенных депрессий отличает полиморфизм психопатологических симптомокомплексов, включающих тревогу, подавленность, превалирующих над собственно аффективными, соматовегетативные проявления – нарушения сна, тахикардия, горечь во рту и др. (М.В.Семиглазова, 2008; Т.В.Довженко и др., 2011). Вместе с тем типологическая структура нозогенных депрессий в большинстве случаев достаточно однородна – чаще наблюдаются депрессии тревожные и ипохондрические.
Наряду с подавленностью и угнетенностью в структуре нозогенных депрессий выделяются тревожно-фобические расстройства – и в первую очередь трактуемые как предиктор нарастающей тяжести аффективных расстройств тревожные руминации (E.Danton и соавт., 2012). В их содержании превалируют опасения повторного приступа стенокардии, ИМ или инсульта, страх инвалидизации, повторных госпитализаций. Круг тревожных расстройств может расширяться за счет явлений невротической ипохондрии, сопровождающихся обостренным самонаблюдением и тщательной регистрацией малейших признаков телесного неблагополучия. В некоторых случаях содержанием тревожных руминаций становятся опасения социальных последствий болезни, возможности достижения поставленных ранее профессиональных целей, семейные и материальные проблемы.
При депрессиях, совпадающих с периодом реконвалесценции после ОИМ, возможен страх телесной уязвимости, снижения толерантности к нагрузкам, проявляющийся феноменом «поведенческой деактивации» (behavioral deactivation; J.Skala и соавт., 2005), сопровождающейся самощажением и как следствие – значительным снижением физической активности.
Депрессии, перекрывающиеся с ССЗ, сопряжены с высоким суицидальным риском.
Соматореактивная дистимия – категория, объединяющая группу затяжных атипичных аффективных расстройств, манифестирующих параллельно соматической (кардиальной) патологии и коррелирующих с дальнейшим течением ССЗ. По своим клиническим проявлениям соматореактивная дистимия не может с определенностью быть отнесена ни к чисто психогенным (нозогенные реакции), ни к чисто эндогенным аффективным заболеваниям, ни к ипохондрическим развитиям.
Риск развития соматореактивной дистимии увеличивается с возрастом. В исследовании B.Baune и соавт. (2006 г.) приводятся данные о значительно более высокой распространенности дистимии и униполярной депрессии у лиц пожилого возраста, страдающих ИБС и перенесших ИМ.
Соматореактивная дистимия формируется при явлениях психосоматического стресса – ОИМ или повторного ИМ (особенно с выраженными болевыми ощущениями, жизнеугрожающими нарушениями ритма), АКШ. В непосредственной временной связи с коронарной катастрофой или вслед за оперативным вмешательством возникает острое тревожно-депрессивное состояние по типу экзистенционального криза. В этот период, как показали исследования, проведенные в нашей клинике (М.А.Самушия, 2006; Б.А.Волель, 2009; Е.А.Степанова, 2011), на фоне витальной тревоги при доминирующем ощущении угрозы существованию и танатофобии формируются диссоциативные расстройства, проявляющиеся глубокими нарушениями интеграции психики и в первую очередь расстройствами идентичности личности – отчуждением сознания, прежнего «я». Психопатологические образования персонифицируются – сопровождаются становлением феномена «прозрения», «переоценки ценностей», осознания себя другим человеком, «новой несопоставимой с прежней» личностью, с кардинальным изменением приоритетов, системы ценностей и представлений о смысле жизни.
Сопоставимость расстройств самосознания при соматореактивной дистимии с перитравматической диссоциацией свидетельствует о существенных, обнаруживающихся уже в дебюте отличиях этой патологии от транзиторных нозогенных реакций с диссоциативными расстройствами истеро-невротического регистра (синдромы «прекрасного равнодушия», «множественной личности» с фрагментарным отчуждением сознания соматической болезни и др.).
Аффективные расстройства, манифестирующие в рамках соматореактивной дистимии вслед за соматической катастрофой или оперативным вмешательством, на первых этапах протекают по типу нозогенной депрессии и лишь затем принимают затяжное течение. Однако содержание депрессии с самого начала обнаруживает некоторые отличия от преходящих нозогенных реакций. Уже с момента госпитализации и установления диагноза, независимо от тяжести состояния (даже в случаях ограниченного поражения миокарда – очаговый ИМ или благоприятного исхода АКШ), формируются представления о необратимости произошедшей катастрофы, обреченности, невозможности возврата к прежнему образу жизни. Уже в это время формируется новая шкала ценностей, планируется отказ от прежней профессиональной деятельности, щадящий режим, оформление пенсии или инвалидности (феномен «новой жизни»). Доминирующей идеей становится контроль над событиями, «опасными» для больного сердца.
В дальнейшем нозогенная депрессия принимает форму дистимии, динамика которой сочетанно синхронизируется как с ритмом развития кардиальной патологии, так и с аутохтонным ритмом аффективного заболевания.
Клиническая картина соматореактивной дистимии на протяжении многих лет определяется униполярным тревожно-депрессивным расстройством с преобладанием соматовегетативных и ипохондрических симптомокомплексов.
Периодически возникающие обострения в виде двойных депрессий связаны либо с экзацербацией кардиальной патологии (повторные ИМ, приступы стенокардии и др.), либо манифестируют аутохтонно в периоды относительной компенсации ССЗ. Клинические проявления аффективных фаз, как правило, формируют картину эндоморфной депрессии – включают ряд витальных расстройств, свойственных циркулярной меланхолии (тоска с загрудинной локализацией, приобретающая физикальный характер, ощущение утраты жизненного тонуса, идеи самообвинения, подчиненность аффективных симптомокомплексов циркадианному ритму).
Дистимические расстройства, коморбидные ИБС, в отличие от эндореактивной дистимии (H.Weitbrecht, 1952) не утрачивают связи с патогенной ситуацией.
В содержании депрессии доминируют представления, отражающие неразрешимость психотравмирующего воздействия соматического страдания (H.Akiskal, 1982; K.Achte,1986; E.Murphy, 1990; M.Friedman, 1993).
Кардиологическая патология, коморбидная аффективной, чаще всего требует разграничения с кардионеврозом. Такая дифференциация особенно сложна в тех случаях, когда проявления кардионевроза также сочетаются с депрессиями.
Как показали исследования К.А.Албантовой (2010 г.), депрессии наблюдаются более чем у 1/2 (59,21%) больных кардионеврозом. В других исследованиях, выполненных на контингенте соматического стационара, приводятся еще более высокие цифры – 82,25% (Т.В.Довженко и соавт., 2011), причем преобладают гипотимии легкой и средней тяжести.
При решении дифференциально-диагностических задач необходимо учитывать различия в коморбидных соотношениях в парах: депрессия/ИБС и депрессия/ кардионевроз. Если при ИБС депрессия формируется в определенном временном интервале после манифестации сердечной катастрофы, то кардионевротический симптомокомплекс появляется чаще всего одновременно с нарушениями настроения. При этом проявления кардионевроза воспринимаются пациентами как неотъемлемая составная часть сниженного настроения, физические проявления психического неблагополучия. Перекрывание ИБС и депрессии демонстрирует полярные соотношения – гипотимия во всех случаях рассматривается в качестве вторичного по отношению к кардиальной патологии психопатологического образования.
Необходимо подчеркнуть и различия в типологической структуре депрессий, коморбидных кардионеврозу и ИБС. У больных кардионеврозом наряду с тревожными (преобладающими при ИБС) чаще наблюдаются истерические депрессии, протекающие с массивной конверсионной симптоматикой, а также гипотимии астенического типа. Тревожная составляющая депрессий при ИБС ограничена генерализованной тревогой и фобиями. Депрессии при кардионеврозе включают значительно более широкий круг анксиозных расстройств: наряду с ипохондрическими фобиями наблюдаются панические атаки, протекающие в 1/3 (33,3%) случаев, с явлениями стойкой агорафобии (К.А.Албантова, 2010), тогда как при ИБС агорафобия относится к сравнительно редким феноменам.
Примечания
1Наиболее часто в литературе отмечаются побочные эффекты при использовании a-адреноблокаторов (депрессия, сексуальная дисфункция); амиодарона и ингибиторов АПФ (мании, депрессии); сердечных гликозидов, в частности дигоксина (депрессии, зрительные галлюцинации, делирий); гиполипидемических средств, в частности холестирамина; кортикостероидов (тревога, депрессия, ажитация), нестероидных противовоспалительных препаратов (депрессия). Следует обратить внимание, что современные исследования не подтвердили депрессогенного эффекта b-адреноблокаторов у больных ИБС и АГ (Ko и соавт., 2002). В последнее время показано, что применение статинов, которое в прошлом связывалось с риском развития депрессии и тревожных расстройств, при ИБС, напротив, снижается, что предположительно связано с их противовоспалительным эффектом.
2Хотя по данным крупных исследований (ENRICHD, SADHART, MIND-IT) значимого влияния терапии депрессии на исходы ИБС не обнаружено, возникает целый ряд вопросов об адекватности проводимого антидепрессивного лечения, в частности эффективности краткосрочного применения препаратов группы СИОЗС или когнитивно-бихевиоральной терапии (L.Berkman и соавт., 2003). Возможно, решающее значение для оценки результатов имеют адекватность терапевтического вмешательства и характер ответа на лечение. В ряде исследований представлены данные о затяжных, резистентных к психотропным препаратам депрессиях как предикторе персистирования кардиальной патологии, высокой частоты повторных госпитализаций, летального исхода у больных ИБС (R.Carney, K.Freedland, 2012; K.Freedland, R.Carney, 2013; B.Foss-Neradko и соавт., 2012).
3В структуре депрессий невротического уровня могут формироваться соматизированные расстройства – чаще кардионевротические (синдром да Коста – кардиалгии, изменения ритма и сердечных сокращений, колебания артериального давления), сопряженные с тревожными опасениями, страхами ипохондрического содержания (танато-, кардиофобии), паническими атаками, ипохондрическим самонаблюдением. Подобные проявления усложняют картину ИБС, а в некоторых случаях дублируют симптомокомплексы ангинозного приступа.
Сведения об авторе
Смулевич Анатолий Болеславович – д-р мед. наук, проф., акад. РАМН, рук. отд. по изучению пограничной психической патологии и психосоматических расстройств ФГБУ НЦПЗ РАМН; зав. каф. психиатрии и психосоматики ФППОВ ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России
Список исп. литературыСкрыть список1. Андрющенко А.В. Психические и психосоматические расстройства в учреждениях общесоматической сети (клинико-эпидемиологические аспекты, психосоматические соотношения, терапия). Автореф. дис. … д-ра мед. наук. М., 2011.
2. Довженко Т.В., Семиглазова М.В., Краснов В.Н. Расстройства тревожно-депрессивного спектра и синдром кардиальной боли при сердечно-сосудистых заболеваниях. Клинико-психопатологические аспекты. Соц. и клин. психиатрия. 2011; 21 (4): 5–13.
3. Краснов В.Н. и др. Сборник инструктивно-методических материалов для врачей первичного звена здравоохранения по оказанию помощи пациентам с непсихотическими психическими расстройствами (на основе полипрофессионального взаимодействия различных специалистов). Ч. 2. М.: Медпрактика-М, 2012.
4. Семиглазова М.В. Клинические варианты и динамика расстройств депрессивного спектра у пациентов после острого инфаркта миокарда. Автореф. дис. … канд. мед. наук. М., 2008.
5. Сидоров П.И., Новикова И.А. Концепция формирования ишемической болезни сердца с позиции синергического подхода. Психич. расстройства в общей медицине. 2008; 2: 11–7.
6. Смулевич А.Б., Сыркин А.Л. Психокардиология. М., 2005.
7. Собенников В.С., Белялов Ф.И. Соматизация и психосоматические расстройства. Иркутск, 2010.
8. Степанова Е.А. Депрессии при ишемической болезни сердца. Автореф. дис. … канд. мед. наук. М., 2011.
9. Bryant RA. Is peritraumatic dissociation always pathological? In: Dissociation and the dissociative disorders. Ed. P.Dell, J.O'Neil. Routledge: NY, 2009; pp. 185–95.
10. Carney RM, Freedland KE. Are somatic symptoms of depression better predictors of cardiac events than cognitive symptoms in coronary heart disease? Psychosom Med 2012; 74 (1): 33–8.
11. Davidson KW, Kupfer DJ, Bigger JT, Califf RM. Assessment and treatment of depression in patients with cardiovascular disease. National Heart, Lung, and Blood Institute working group report. Ann Behav Med 2006; 32 (2): 121–6.
12. Denton ED, Rieckmann N, Davidson KW et al. Psychosocial vulnerabilities to depression after acute coronary syndrome: the pivotal role of rumination in predicting and maintaining depression. Psychol Clin Settings 2012; 3: 1–9.
13. Dessotte CA, Souza e Silva F, Bolela F et al. Presence of depressive symptoms in patients with a first episode of Acute Coronary Syndrome. Rev Latino-Am Enfermagem 2013; 21 (1): 325–31.
14. Janszky I, Ahnve S, Lundberg I, Hemmingsson T. Early-onset depression, anxiety, and risk of subsequent coronary heart disease: 37-year follow-up of 49,321 young Swedish men. J Am Coll Cardiol 2010; 56 (1): 31–7.
15. Kivimäki M, Shipley MJ, Allan C et al. Vascular risk status as a predictor of later-life depressive symptoms: a cohort study. Biol Psychiat 2012; 72 (4): 324–30.
16. Lespérance F, Frasure-Smith N, Talajic M, Bourassa MG. Five-year risk of cardiac mortality in relation to initial severity and one-year changes in depression symptoms after myocardial infarction. Circulation 2002; 105: 1049–53.
17. May HT, Horne BD, Carlquist JF, Sheng X. Depression after coronary artery disease is associated with heart failure. J Am Coll Cardiol 2009; 53 (16): 1440–7.
18. McCaffery JM, Frasure-Smith N, Duben M-P et al. Common genetic vulnerability to depressive symptoms and coronary artery disease: a review and development of candidate genes related to inflammation and serotonin. Psychosom Med 2006; 68: 187–200.
19. Naqvi TZ, Rafique AM, Andreas V et al. Predictors of depressive symptoms post-acute coronary syndrome. Gend Med 2007; 14 (4): 339–51.
20. Ozer EJ, Best SR, Lipsey TL et al. Predictors of posttraumatic stress disorder and symptoms in adults: a meta-analysis. Psychol Bull 2003; 129: 52–73.
21. Rafanelli C, Roncuzzi R, Ottolini F et al. Psychological factors affecting cardiologic conditions. Ed. P.Porcelli, N.Sonino. In: Psychological factors affecting medical conditions 2007; pp. 72–108.
22. Shaffer JA, Whang W, Shimbo D et al. Do different depression phenotypes have different risks for recurrent coronary heart disease? Health Psychol Rev 2012; 6 (2): 165–79.
23. Skala JA, Freedland KE, Carney RM. Heart Disease. HOGREFE & Huber Publishers. Cambridge: USA, 2005.
24. Tully Ph, Baker R. Depression, anxiety, and cardiac morbidity outcomes after coronary artery bypass surgery: a contemporary and practical review. J Geriat Cardiol 2012; 9: 197−208.
25. Melle van JP, de Jonge P, Spijkerman TA, Tijssen JG. Prognostic association of depression following myocardial infarction with mortality and cardiovascular events: a meta-analysis. Psychosom Med 2004; 66: 814–22.
26. Wittchen H-U. Continued needs for epidemiological studies of mental disorders in the community. Psychother Psychosom 2004; 73: 197–206.
29 декабря 2013
Количество просмотров: 4375
