Yvan Vandenplas*, Elvira Levy, Roel Lemmens, Thierry Devreker
Kidz Health Castle, UZ Brussel, Vrije Universiteit Brussel, Brussels, Belgium
Цель данного обзора – суммировать все известные на сегодняшний день данные о функциональных запорах (ФЗ) у детей и понять, какие вопросы до сих пор бросают вызов врачам касательно эпидемиологии, патофизиологии, диагностики и лечения ФЗ. Несмотря на то что ФЗ – довольно часто встречающаяся проблема, их распространенность в мире неизвестна, поскольку эпидемиологические данные по некоторым регионам отсутствуют. Другая проблема заключается в том, что данные о распространенности очень разнятся, так как используются разные методы исследований и возрастные группы. Механизмы развития ФЗ до сих пор до конца не известны, однако возможно влияние многих факторов. Волевое удержание стула считается главной причиной ФЗ у детей дошкольного и школьного возраста. Генетическая предрасположенность также вероятно играет роль, поскольку у многих пациентов имеется соответствующий семейный анамнез, тем не менее генетические мутации, связанные с ФЗ, не выявлены. За последние годы было предложено несколько критериев диагностики ФЗ у детей школьного и дошкольного возраста. В 2016 г. были опубликованы Римские критерии IV. В сравнении с Римскими критериями III в последней редакции исключены 2 диагностических критерия у детей до 4 лет, у которых используются подгузники. Помимо тщательного сбора анамнеза и осмотра, другие исследования, такие как абдоминальная рентгенография, ультразвуковое исследование толстой кишки, исследование времени толстокишечного транзита, ректальная биопсия и манометрия толстой кишки, не рекомендуются в рутинной практике. Что касается лечения, руководства рекомендуют освобождение толстой кишки от каловых масс и поддерживающую терапию с применением полиэтиленгликоля (ПЭГ) с электролитами или без них. Однако практика показывает, что приемлемость, приверженность лечению и переносимость терапии ПЭГ проблематичны. Проведением консультаций родителей и детей по поводу ФЗ часто пренебрегают. Недавние исследования показывают, что коррекция поведения в сочетании с применением слабительных средств помогает избавиться от симптомов. Необходимы дальнейшие исследования, чтобы получить более определенные результаты, в том числе исследования на уровне оказания первичной медицинской помощи.
Ключевые слова: функциональный запор, дети, эпидемиология, патофизиология, диагностика, лечение.
*yvan.vandenplas@uzbrussel.be
Для цитирования: Vandenplas Y, Levy E, Lemmens R, Devreker T. Функциональный запор у детей. Педиатрия (Прил. к журн. Consilium Medicum). 2017; 1: 50–57.
Functional constipation in children
Yvan Vandenplas*, Elvira Levy, Roel Lemmens, Thierry Devreker
Kidz Health Castle, UZ Brussel, Vrije Universiteit Brussel, Brussels, Belgium
This review intends to update what is known and what is still a challenge in functional constipation (FC) in children regarding epidemiology, pathophysiology, diagnosis and management. Although FC is a common childhood problem, its global burden remains unknown as data from parts of the world are missing. Another problem is that there is a large variation in prevalence due to differences in study methods and defining age groups. The pathophysiology of FC remains unclear until now, but is probably multifactorial. Withholding behaviour is likely to be the most important factor in toddlers and young children. Genetics may also play a role since many patients have positive family history, but mutations in genes associated with FC have not been found. Over the past years, different diagnostic criteria for FC in infants and children have been proposed. This year Rome IV criteria have been released. Compared to Rome III, it eliminates two diagnostic criteria in children under the age of 4 who still wear diapers. Except taking a good medical history and physical examination, other investigations such as abdominal radiography, trans abdominal recto-ultrasonography, colonic transit time, rectal biopsies and colon manometry are not routinely recommended. Regarding treatment, guidelines recommend disimpaction and maintenance therapy with Polyethylene glycol (PEG) with or without electrolytes. But experience learns that acceptability, adherence and tolerance to PEG are still a challenge. Counselling of child and parents about causes of FC is often neglected. Recent studies suggest behaviour therapy added to laxative therapy improves relieve of symptoms. Further homogenous studies, better-defined outcomes and studies conducted in primary care are needed.
Key words: functional constipation, children, epidemiology, pathophysiology, diagnostics, treatment.
*yvan.vandenplas@uzbrussel.be
For citation: Vandenplas Y, Levy E, Lemmens R, Devreker T. Functional constipation in children. Pediatrics (Suppl. Consilium Medicum). 2017; 1: 50–57.
Вступление
Запор – это часто встречающаяся проблема во всем мире, которая ухудшает качество жизни, но часто недооценивается. Дети с запорами часто посещают врача общей практики или педиатра. Эти дети также часто госпитализируются в неотложном порядке или проходят лечение в стационаре. Следовательно, запор представляет собой значительную экономическую проблему для системы здравоохранения.
Диагностика и лечение запоров, в частности у детей, сопряжены с определенными сложностями. В статье приведены данные о том, что известно на сегодняшний день о функциональном запоре (ФЗ) и с какими трудностями мы сталкиваемся в процессе диагностики и лечения с точки зрения эпидемиологии, патофизиологии, диагностики и лечения. В этом обновленном обзоре делается акцент на эмоциональный и физический стресс, который испытывают дети с ФЗ и подчеркивается важность адекватного лечения.
Распространенность
ФЗ – это распространенная проблема среди детей с различной частотой встречаемости между регионами [1]. В Северной и Южной Америках частота встречаемости у детей, включая детей-подростков, варьирует от 10 до 23% [1–5], тогда как в Европе (только у детей дошкольного возраста) равна 0,7–12%. В Азии (включая детей-подростков) частота ФЗ находится в пределах 0,5–29,6% [1, 6–8]. Несмотря на то что ФЗ распространены на всех континентах, в настоящий момент недостаточно данных об их распространенности у детей Африки и Океании.
Распространенность ФЗ варьирует в зависимости от возрастной группы. Наиболее часто ФЗ отмечаются у детей в возрасте 2–4 лет, когда начинается приучение к горшку. Недавний систематический обзор показал, что распространенность запоров у детей в среднем составляет 12% [1]. Частота запоров у младенцев колеблется между 0,05% и 39,3%, однако в соответствии с выводами, сделанными экспертами, распространенность оценивается на уровне 15%. В этом возрасте питание является основной причиной ФЗ. В отличие от взрослых, у которых ФЗ чаще наблюдается у женщин, информация о гендерных различиях у детей и подростков не уточнена [2, 4, 6, 8, 10].
Влияние многих факторов, таких как различные трактовки ФЗ, разные возрастные группы и методы, ведет к тому, что данные по распространенности ФЗ очень вариабельны.
Патофизиология
Запор определяется как функциональный в случае отсутствия органической причины, что имеет место у большинства детей (до 95%)[12]. В 5% случаев, связанных с органической патологией, этиология заболевания варьирует от болезни Гиршпрунга, пороков развития прямой кишки, нервно-мышечных заболеваний до метаболических и эндокринных расстройств.
Патофизиологические механизмы ФЗ у детей остаются неясными, однако ясно, что они имеют мультифакториальную природу. Наиболее распространенный механизм развития ФЗ особенно у маленьких детей – осознанное удержание стула, часто начинающееся после болезненной дефекации, которая пугает ребенка [13]. Кал остается в прямой кишке, слизистая оболочка реабсорбирует из него жидкость, из-за чего эвакуация каловых масс становится еще более затруднительной. Этот порочный круг может привести к сдавлению фекальных масс, иногда недержанию кала, потере ректальной чувствительности и в конечном итоге – утрате физиологического позыва к дефекации [14].
У части детей ФЗ может возникать из-за медленного транзита. Интерстициальные клетки Кахаля играют важную роль в моторике кишечника. Эти клетки, как считается, являются водителями ритма, обусловливающими ритмичную перистальтику кишечника. Многие публикации сообщают о малом числе клеток Кахаля, выявляемом при гистологическом исследовании у детей со всеми формами запоров, хотя нормальное число интерстициальных клеток Кахаля у здоровых детей неизвестно [15]. Медленный транзит кала также связан с недостатком субстанции P и вазоактивного интестинального пептида в поперечной ободочной кишке, однако эти открытия никак не помогают найти новые способы лечения [16].
У многих пациентов с ФЗ имеется отягощенный семейный анамнез по данной патологии. Это дает основания полагать, что генетические факторы могут играть определенную роль, хотя мутации, связанные с ФЗ, до сих пор не были обнаружены. ФЗ ассоциируется с неврологическими расстройствами, например расстройствами аутического спектра (РАС). Этот патофизиологический путь остается неясным, однако предполагается, что именно с ним связано отсутствие адекватного ответного поведения на позывы к дефекации [18, 19]. Генетические факторы, включая синдромы «генных последовательностей», являющиеся результатом мутаций в нескольких соседних генах, дисбактериоз и атипичная обработка сенсорной информации были предложены как возможные объяснения связи между РАС и ФЗ.
Существует связь между методами воспитания детей и ФЗ. Наиболее высокие и наиболее низкие баллы при оценке самостоятельности поведения связываются с пониженной частотой дефекаций и учащением недержания кала. Эта закономерность особенно хорошо видна у детей старше 6 лет. Стрессовые ситуации, например насилие, в том числе сексуального характера, могут также играть свою роль в развитии ФЗ.
Критерии диагностики
В 1999 г. были утверждены Римские критерии II, однако позднее их расценили как слишком жесткие, поскольку в них разделяли некоторые патологии, такие как ФЗ и функциональная фекальная ретенция, и определяли период минимальной продолжительности симптомов в 3 мес [11].
Парижский консенсус по терминологии запора у детей (Paris Consensus on Childhood Constipation Terminology, PACCT) дал другое определение ФЗ у детей. Исследование, сравнивающее PACCT и Римские критерии II, продемонстрировало, что только у 53 детей (42,1%) из 126 был диагностирован запор согласно Римским критериям II по сравнению с PACCT. Такие различия возникли из-за того, что согласно Римским критериям II, ФЗ определялись как наличие позы удержания кала в сочетании с дефекациями менее 2 в неделю на протяжении как минимум 3 мес [11]. В Римских критериях III, опубликованных в 2006 г. и основанных на PACCT (см. таблицу), определения «энкопрез» и «каломазание» были заменены на «недержание кала» [11].
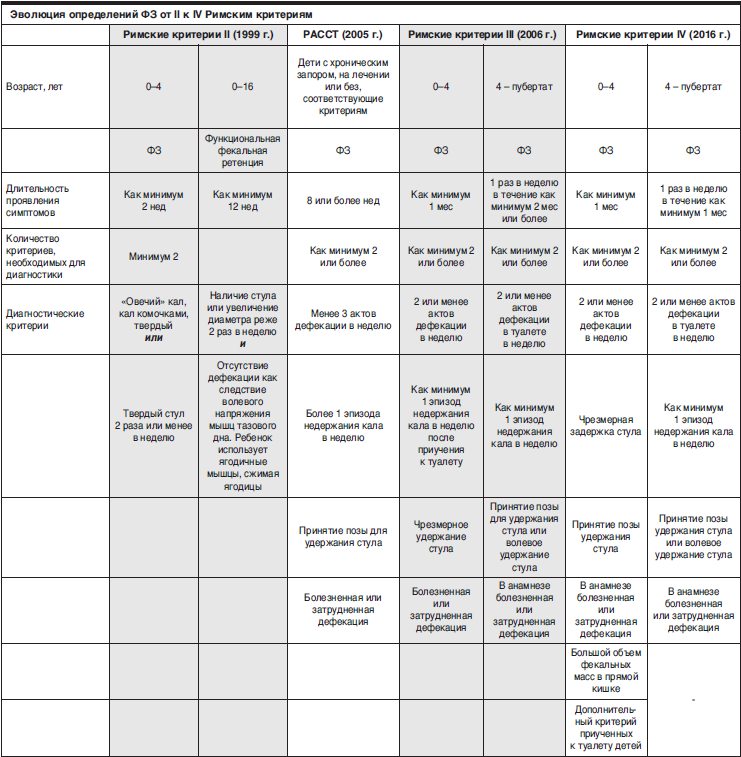
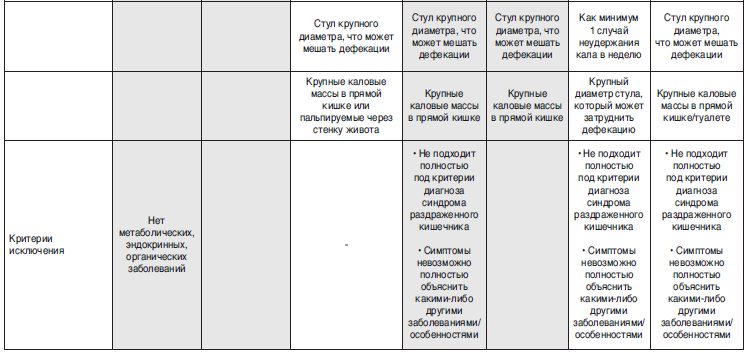
Согласно Римским критериям III для диагностики ФЗ необходимы 2 параметра из 6, а также выделены две возрастные группы. Первая – дети от 4 лет до пубертатного периода, вторая – дети в возрасте до 4 лет. Для диагностики ФЗ в младшем возрасте требуется наличие симптомов в течение 1 мес, в старшей – в течение 2 мес.
Некоторые исследования, сравнивающие Римские критерии II и III, показали противоречивые результаты. Так, ФЗ чаще диагностировался по критериям II (32,4%), чем по критериям III (18,2%) у младенцев и детей младшего возраста, посещающих педиатрические клиники в Таиланде [22]. Одной из причин такого различия было исключение детей с болезненной дефекацией по причине твердости кала из Римских критериев III. В Римских критериях III оба аспекта сгруппированы вместе, что означает необходимость присутствия еще одного критерия для диагностики ФЗ. Это может затруднить постановку диагноза. Еще один критерий, который слишком ограничивает рамки определения детских ФЗ в Римских критериях III, – это «кал большого диаметра, который может затруднять его выход». Анализ медицинских карт детей, наблюдаемых амбулаторно в центрах оказания специализированной медицинской помощи (возраст 6,3± стандартное отклонение), показал, что у детей более старшего возраста ФЗ диагностировался согласно Римским критериям III в 87% против 43% согласно Римским критериям II (p<0,001). Полученные результаты связали с такими критериями как «недержание кала по крайней мере 1 раз в неделю» и «стул большого диаметра, который может затруднить его выход». Эти симптомы чаще встречаются при тяжелых хронических запорах, наиболее часто наблюдающихся центрах оказания специализированной медицинской помощи. Эти симптомы встречаются только у 10% детей младшего возраста [22, 23].
Не так давно были выпущены новые – Римские критерии IV. Были скорректированы критерии для детей младшего возраста (группа от 0 до 4 лет умственного возраста). Дети, не приученные к горшку, не обязаны соответствовать 2 дополнительным критериям, чтобы у них был диагностирован ФЗ. Были удалены критерии «стул большого диаметра, который может препятствовать его выходу» и «недержание кала как минимум 1 эпизод в неделю». Первый критерий неприменим для этой возрастной группы. Очевидна и причина исключения второго критерия, поскольку невозможно говорить о неудержании кала, если ребенок не приучен к горшку. Кроме того, длительность симптомов, достаточная для постановки диагноза, была снижена до 1 мес для детей от 4 лет до подросткового возраста. Хотя Римские критерии IV предложены в качестве нового «золотого стандарта», их следует оценивать так же, как и другие документы. Римские критерии особенно хорошо подходят для отбора пациентов с сопоставимой степенью ФЗ для клинических исследований и могут быть куда менее полезными для диагностики ФЗ в клинической практике. Необходимы новые исследования для оценки полезности Римских критериев IV для диагностики ФЗ в повседневной практике. К настоящему моменту еще не проведены исследования для оценки этих критериев для всех возрастных групп, а лишь для определенной группы детей младшего возраста.
Анамнез заболевания
Тщательный сбор анамнеза – первый шаг в диагностике ФЗ у детей. Анамнез заболевания должен содержать информацию о многих параметрах, таких как возраст на момент возникновения симптомов, выход мекония, частота и консистенция стула, боли в животе, недержание кала, наличие волевого удержания стула, история питания, эпизоды рвоты и потери массы тела. Как уже упоминалось ранее, должны быть оценены такие параметры, как наличие стресса, нарушения/задержки нервного развития и семейный анамнез по гастроинтестинальным заболеваниям. Бристольская шкала формы кала – наиболее предпочтительный и стандартизированный метод для описания консистенции стула [24]. Однако эта шкала не адаптирована для детей, не приученных к горшку. Амстердамская шкала оценки стула была разработана для младенцев, однако сложна в использовании, так как включает в себя 18 различных изображений [25, 26]. Брюссельская шкала в настоящее время находится в разработке.
Физикальное обследование детей с ФЗ всегда должно включать в себя измерение роста, осмотр живота, осмотр перианальной области и исследование пояснично-крестцовой области.
Пальцевое исследование прямой кишки
Согласно рекомендациям European Society for Paediatric Gastroenterology Hepatology and Nutrition (ESPGHAN) и North American Society for Pediatric Gastroenterology, Hepatology and Nutrition (NASPGHAN), пальцевое исследование прямой кишки при диагностике ФЗ рекомендуется не во всех случаях для диагностики ФЗ [12]. С другой стороны, в Римских критериях III и IV наличие крупного скопления фекальных масс в прямой кишке является критерием для постановки диагноза ФЗ. Соответственно, ESPGHAN и NASPGHAN пришли к выводу, что в случае, когда присутствует только один из Римских критериев и диагноз остается неясным, рекомендуется выполнить пальцевое исследование прямой кишки. Также пальцевое исследование необходимо проводить в случае запора, не поддающегося лечению и при наличии тревожных симптомов. Осмотр анальной области необходим для выявления рубцов, геморроидальных узлов, перианального кала и трещин [27].
Лабораторное исследование
При отсутствии тревожных симптомов лабораторный скрининг на наличие гипотиреоза, целиакии, исследование уровня витамина Д, гиперкальциемии и аллергии на белок коровьего молока не рекомендуются. Тем не менее детям с постоянными жалобами на запоры может быть предложена безмолочная диета на период 2–4 нед. Несмотря на то что сам механизм остается неясным, была выдвинута гипотеза о том, что аллергическое воспаление внутреннего сфинктера может приводить к повышению анального давления покоя [28].
Рентгенологическое исследование органов брюшной полости
Руководства ESPGHAN и NASPGHAN не рекомендуют использование диагностической абдоминальной рентгенографии, являющейся легкодоступным и дешевым методом. Главный ее недостаток – облучение пациента. Было разработано несколько шкал для оценки величины калового скопления в ходе диагностики ФЗ. Тем не менее систематические обзоры показали отсутствие связи между клиническими симптомами запора и каловым скоплением, выявленном при ренгенографии органов брюшной полости [29, 30]. Также отмечена низкая воспроизводимость диагностических шкал у разных экспертов [31].
Кроме того, абдоминальная рентгенография может привести к ошибочному диагнозу. Ретроспективное когортное исследование показало, что одному из 200 детей, которым был поставлен диагноз ФЗ на основе абдоминальной рентгенографии, потребовалось хирургическое вмешательство или применение интервенционного радиологического метода в течение 7 дней. Недиагностированные патологии были потенциально опасными для жизни, включали прободной аппендицит, кишечную инвагинацию, опухоль головного мозга, лейкемию и заворот кишки [32].
В некоторых редких случаях абдоминальная рентгенография может иметь определенное преимущество, в частности при наличии некоторых психологических факторов, затрудняющих проведение пальцевого ректального исследования, например при подозрении на сексуальное насилие или у очень беспокойных детей. В случаях, когда пальпация живота затруднена, например у пациентов, страдающих ожирением, абдоминальная рентгенография также может быть полезной [27].
Трансабдоминальное ультразвуковое обследование (ТУЗИ) прямой кишки
Поскольку и пальцевое ректальное исследование, и абдоминальная рентгенография могут иметь некоторые ограничения, ультразвуковое исследование (УЗИ) считается альтернативным методом. R.Burgers и соавт. сравнили ТУЗИ и пальцевое исследование прямой кишки и обнаружили положительную корреляцию у 80% пациентов [27]. Это исследование также показало, что определить пороговое значение диаметра прямой кишки довольно сложно. Размер просвета в 30 мм часто встречается как у детей с ФЗ, так и у здоровых детей группы контроля. По всей видимости, существует логическая связь между дефекацией и изменением ректального просвета, поэтому перед проведением УЗИ у пациента необходимо спрашивать о наличии позывов к дефекации [33]. Для надежного УЗИ необходим опытный исследователь. Эти недостатки стали причиной того, что в руководствах ESPGHAN и NASPGHAN ТУЗИ прямой кишки не рекомендуется использовать рутинно для постановки диагноза ФЗ [12].
Время толстокишечного транзита (ВТТ)
ВТТ может быть использовано для оценки моторики толстой кишки. Для диагностики ФЗ не рекомендуется учитывать ВТТ. ВТТ может использоваться только в крайне неясных случаях в качестве дифференциального признака между ФЗ и функциональным недержанием кала без запора [12, 29].
Другие исследования
Если запор не поддается лечению, требуются более тщательные обследования в специализированной клинике.
Аноректальная манометрия может оказаться полезным инструментом скрининга для детей старшего возраста с не поддающимся лечению запором и подозрением на болезнь Гиршпрунга [34]. Измененный ректоанальный ингибиторный рефлекс – указывает на необходимость провести ректальную аспирационную биопсию, являющуюся «золотым стандартом» диагностики болезни Гиршпрунга.
Манометрия толстой кишки может проводиться только в тех случаях, когда лечение не приносит результатов и требуется хирургическое вмешательство. Манометрия толстой кишки может помочь дифференцировать детей с нормальной перистальтикой толстой кишки и детей с нервно-мышечными расстройствами кишечника.
Лечение
Рекомендации по терапии ФЗ включают в себя нормальное потребление пищевых волокон и жидкости, нормальную физическую активность и дополнительное фармакологическое лечение для освобождения прямой кишки от каловых масс с последующей медикаментозной поддерживающей терапией [12].
Очистка прямой кишки может быть выполнена антеградно с применением простой питьевой воды перорально или с помощью назогастрального зонда, а также ретроградно через анальное отверстие. Оральный прием полиэтиленгликоля (ПЭГ) с электролитами или без них (1–1,5 г/кг в течение 3–6 дней) является методом выбора. ПЭГ и клизма одинаково эффективны для очистки кишечника от каловых масс [12, 35, 36]. ПЭГ ассоциируется с более высокой частотой калового недержания, тогда как клизмы – с кишечными коликами и страхом [12, 35]. Таким образом, эти побочные эффекты затрудняют согласие на данные процедуры и соблюдение такого лечения детьми. В 2 исследованиях сравнивали уровень беспокойства, связанного с очисткой кишечника от каловых масс с помощью ПЭГ и с помощью клизмы. Первое из них не нашло различий между уровнями стресса [35], тогда как в другом исследовании дети, получающие клизму в отделении неотложной помощи, испытывали стресс в большей степени [36]. Также оно показало, что если у ребенка уже есть опыт лечения с помощью клизм, то их можно применять и дома [35].
Что касается поддерживающей терапии, руководства рекомендуют использование ПЭГ с электролитами или без них в меньших дозах (0,2–0,8 г/кг) [12]. Несмотря на то что детям может не нравиться вкус ПЭГ, особенно с добавлением электролитов, некоторые исследования оценивали на сколько пациенты были согласны на такое лечение и приверженность лечению ПЭГ. Только в одном исследовании проводили сравнение ПЭГ с электролитами без добавления ароматизаторов и ПЭГ без электролитов с добавлением ароматизаторов. Дети чаще соглашались принимать ПЭГ без электролитов, так как, со слов родителей, лекарство было проще давать детям (96% против 52%, р<0,001), а дети нашли ПЭГ без электролитов более приятным на вкус (42% против 2%, р<0,001). Однако спустя 4 нед не было обнаружено существенной разницы в приверженности лечению (98% против 88%, р<0,062) [37].
Систематический обзор показал, что только у 61% детей была возможность прекратить прием слабительных через 6–12 мес после начала терапии [38]. Дети с хроническими запорами, проходящими лечение в центрах оказания специализированной помощи, курировались более 10 лет, и было выявлено, что, несмотря на интенсивную тактику ведения, только 80% достигли хороших клинических результатов к 16 годам. Такой неудовлетворительный итог связывают с началом заболевания в более позднем возрасте, длительным временным промежутком между проявлением симптомов и первым посещением детской гастроэнтерологической клиники [39].
Многие родители не решаются применять препараты в течение длительного времени из-за опасений по поводу синдрома отмены или возможности привыкания [39, 40]. На основании анализа побочных эффектов, таких как тошнота, метеоризм и биохимические изменения, например уровень натрия, ПЭГ считается безопасным препаратом для применения в течение 6 мес [40–44].
Так как не все пациенты охотно принимают препарат, а также приверженность к лечению не является оптимальной, необходимо продолжать искать более эффективные стратегии терапии. Для того чтобы убедить родителей в безопасности долговременного приема ПЭГ необходимо проведение исследований с более длительным периодом наблюдения. Вместе с тем, хотя ПЭГ рекомендуется для поддерживающего лечения, проведенные исследования были неоднородные по многим параметрам (назначения, трактовка ФЗ, измерение результатов) [12]. Это было подтверждено в Кохрановском систематическом обзоре 2016 г. [41]. Оптимальная дозировка ПЭГ также нуждается в дальнейших исследованиях с более длительным периодом наблюдения. Важная, однако часто незамеченная проблема – выбор первичной конечной точки исследования. Если лечение проводится в соответствии с Римскими критериями, пациенты могут считаться вылеченными, даже если все еще сохраняется 1 из 6 критериев заболевания. Каждый врач должен стремиться к полному исчезновению всех симптомов.
Хотя руководства для лечения ФЗ рекомендуют применение осмотического слабительного, такого как ПЭГ, для поддерживающей терапии и очистки от каловых масс, ПЭГ доступен не во всех странах. Рекомендуется использование альтернативного осмотического слабительного, например лактулозы, в случае если ПЭГ недоступен. Лактулоза была лучше и больше исследована, чем гидроксид магния или минеральное масло, а также она безопасна для применения во всех возрастных группах [45].
Все исследования и метаанализы показали, что ПЭГ превосходит лактулозу по всем параметрам: частоте стула в неделю (среднее отклонение – MD 0,70, 95% доверительный интервал – ДИ 0,10–1,31), необходимости дополнительного применения слабительных препаратов (18% против 31%) и успешной очистке кишечника от каловых масс (100–80%, р=0,04). Отсутствуют статистически значимые различия между ПЭГ и лактулозой в отношении всех нежелательных явлений – метеоризма, недержания кала, болей в животе, тошноты или вздутия живота.
Лактулоза уступает не только ПЭГ, но и гидроксиду магния (MD -1,51, 95% ДИ от -2,63 до -0,39) и жидкому парафину (MD 4,94, 95% ДИ 4,28–5,61) в одном небольшом исследовании, в котором принимали участие 50 человек. Впрочем, эти данные основаны на частоте стула в неделю, а информации об успешности очистки кишечника от каловых масс нет. Лактулоза не имела существенных отличий по эффективности в сравнении с пищевыми волокнами, гликозидами сенны (слабительное, стимулирующее перистальтику), лактитолом или гидролизованной гуаровой камедью (оба – осмотические слабительные). Однако эти данные основаны только на одном исследовании каждого из перечисленных средств. Также важно упомянуть, что не проводились исследования, сравнивающие лактулозу с плацебо [41]. Учитывая тот факт, что эти исследования были крайне неоднородными и период наблюдения был очень коротким, достаточно сложно оценить лактулозу как средство для поддерживающей терапии и средство очистки кишечника. Рекомендованная доза лактулозы составляет 1–2 г/кг 1 или 2 раза в день [12, 41].
Что касается других слабительных, ПЭГ показал свое преимущество перед плацебо, магния гидроксидом, минеральным маслом (жидким парафином), смесью пищевых волокон и дескурайнией Софии (традиционное иранское лекарственное растение). Тем не менее в сравнении с гидроксидом магния не было выявлено существенных отличий в отношении успешности освобождения от каловых масс [41].
Метаанализ двух исследований жидкого парафина (число участников – 287) не выявил его преимуществ [41]. Еще в одном обзоре упоминаются такие нежелательные явления применения жидкого парафина, как маслянистые выделения из ануса, вызывающие воспаление или зуд кожи, пачкающие одежду и мебель. Также выявлен низкий уровень жирорастворимых витаминов в сыворотке крови вследствие снижения их всасывания [46].
В руководствах также упоминаются стимулирующие слабительные, например натрия пикосульфат и бисакодил. Последний Кохрановский метаанализ оценивает ведение ФЗ как с помощью осмотических, так и стимулирующих слабительных, но во включенных в метаанализ исследованиях применялись главным образом осмотические слабительные [41]. Насколько нам известно, исследования, сравнивающие бисакодил и натрия пикосульфат с ПЭГ или лактулозой, или другими слабительными в качестве поддерживающей терапии или для разового очищения от каловых масс, у детей не проводились.
Другие фармакологические методы терапии, такие как ректальные слабительные/клизмы со средствами для размягчения кала (докузат натрия или фосфат натрия), недавно открытые молекулы (любипростон, линаклотид и прукалоприд), а также пре- и пробиотики (пока) руководствами не рекомендуются.
Насколько нам известно, проведено только 1 исследование, сравнивающее эффективность клизмы с докузатом натрия и ПЭГ, и 1 исследование, сравнивающее эффективность клизмы с докузатом натрия и суппозиториями со свободными жирными кислотами для стимулирования выведения каловых масс у детей. Очистка кишечника была одинаково успешной и с помощью клизмы с докузатом натрия (80%) и при использовании ПЭГ (68%); p=0,28 [35]. Разница между эффективностью суппозиториев с высоким содержанием жирных кислот и клизмами (81% против 88%) не была выявлена, и авторы верят, что это может быть важной дополнительной лечебной опцией к уже применяемым методам [47]. Еще в 1 исследовании сравнивались эффективность и безопасность использования у детей клизм с натрия фосфатом и клизм с молоком и патокой; статистически значимой разницы между ними выявлено не было [48]. Тем временем в другом исследовании клизм с натрия фосфатом сообщалось о 35 случаях гиперфосфатемии, из которых в 80% наступило выздоровление без каких-либо осложнений. Авторы утверждают, что лучше не назначать клизмы с натрия фосфатом детям с сопутствующими заболеваниями желудочно-кишечного тракта и почек [49].
Проведено 1 исследование по применению любипростона у детей, однако оно не соответствует критериям включения в данный обзор [50]. Не проводились исследования с применением линаклотида у детей; по прукалоприду было проведено 2 исследования: 1 открытое пилотное и 1 многоцентровое рандомизированное двойное слепое [51]. Результаты пилотного исследования показали, что после 8 нед наблюдалось повышение частоты стула и снижение недержания у 55% (n=38) больных, препарат безопасен для детей. По результатам многоцентрового исследования были сделаны выводы о том, что лекарство хорошо переносится, однако отсутствует разница между прукалопридом и плацебо в отношении увеличения частоты спонтанной дефекации в неделю (60,4% против 55,1%) и возникновения нежелательных явлений (69,8% против 60,7%).
В недавнем систематическом обзоре по использованию про- и/или пребиотиков сделан вывод о том, что у большей части исследований был высок риск предвзятости. Эти исследования не показывали существенного влияния на частоту дефекаций, на недержание кала и болезненную или затрудненную дефекацию [35, 53]. Разнообразие пребиотиков и пробиотиков и вариации их дозирования практически исключают возможность сделать четкие выводы. Для проведения исследований по лечению запоров у детей необходима очень строгая стандартизация.
Допустимость отклонений – еще один важный фактор эффективной лекарственной терапии. Большая часть исследований оценивает частоту дефекаций и консистенцию стула. Однако по своей сути эти параметры очень ограничены в условиях реальной клинической практики. Между двумя группами в исследовании может наблюдаться статистически значимая разница в повышении частоты дефекаций, тем не менее неизвестно, отмечают ли улучшение дети и их родители. В одном из исследованиий поднимался вопрос о том, что прежде всего необходимо устранить противоречивость и неоднородность трактовки ФЗ и унифицировать измерение получаемых результатов. Клиницистам предлагается минимальный набор исходов, которые должны быть измерены и отрепортированы, чтобы сделать возможным сопоставление результатов разных терапевтических методов в разных исследованиях [54]. Тем временем большая часть результатов исследований не коррелирует с жалобами пациентов в рутинной практике. Необходимо разработать также минимальный объем жалоб, которые должен быть собран у пациентов и родителей.
Важный аспект, который часто игнорируется, – консультирование родителей и детей по поводу возможных причин хронического ФЗ и каломазания [21, 46, 55–57]. Методы воспитания родителями детей (высокая и низкая степень независимости от родителей, жалость к себе) ассоциируются с частотой дефекаций и вероятностью недержания кала, и поэтому решение данных вопросов является важным этапом лечения детей [20]. Недавний гайдлайн не поддерживает поведенческую психотерапию, за исключением ситуаций, при которых в поведении ребенка отмечаются отклонения [12]. Однако недавний метаанализ и Кохрановское исследование утверждают, что поведенческая терапия совместно с лечением слабительными может улучшить состояние детей с недержанием кала, связанным с запором [58, 59]. Для оптимального лечения ФЗ, особенно с фекальным недержанием, требуются хорошие взаимоотношения и глубокая эмпатия между ребенком и врачом. Привлечение постороннего человека для психотерапии может нарушить этот баланс. Назначение только лишь слабительных никогда не решает проблему ФЗ полностью. Каждый специалист должен обладать навыками и находить время на то, чтобы объяснить, обучить, мотивировать и поощрять ребенка и его родителей.
Основная часть исследований, касающихся ведения ФЗ, обычно проводится в центрах специализированной и высокоспециализированной помощи, в которых лечатся дети, страдающие продолжительными и не поддающимися лечению запорами. Однако большинство детей с запорами и их родители обращаются за медицинской помощью в центры оказания первичной медицинской помощи. Исследование, проведенное в первичном звене здравоохранения, показало, что после 2 мес лечения симптомы сохранялись примерно у 40% пациентов с запорами. Поэтому необходимы дальнейшие исследования на уровне оказания первичной медицинской помощи.
Междисциплинарный подход к лечению не включен в гайдлайны из-за отсутствия доказательств, полученных по результатам рандомизированных контролируемых исследований, демонстрирующих выгоду от такого подхода.
Тем не менее после неудач амбулаторного лечения специалисты по запорам часто прибегают к междисциплинапному подходу. На данный момент исследования, оценивающие подобный подход, не проводились.
Заключение
Хотя существуют безопасные и эффективные пути лечения ФЗ у детей, многие проблемы сохраняются. Все еще отсутствуют данные о распространенности в некоторых частях света. Остается неясным механизм развития болезни у детей. Отсутствие адекватного поведенческого ответа на позыв к дефекации – основной фактор, ведущий к запорам. Наследственность также может играть определенную роль, и этот фактор должен быть тщательнее исследован. В новых Римских критериях IV скорректированы некоторые параметры, что должно упростить диагностику ФЗ у детей младшего возраста, однако необходимы новые исследования для оценки их практической пользы в повседневной практике. Младенцы и дети, не соответствующие Римским критериям для постановки диагноза, у которых однако присутствует один из шести критериев, что доставляет им ежедневное беспокойство и поэтому требует адекватной медицинской помощи. Руководства ESPGHAN/NASPGHAN исключительно рекомендуют собирать анамнез и проводить физикальный осмотр у всех младенцев и детей с анамнестическими и клиническими данными ФЗ в отсутствие тревожных симптомов. Что касается метода очистки кишечника от каловых масс и поддерживающего лечения ФЗ, в первую очередь рекомендуется ПЭГ. Необходимы большие сходные по дизайну исследования, проводимые на случайной группе пациентов. Приемлемость терапии и приверженность лечению являются проблемой ПЭГ, поскольку детям не нравится его вкус. Исследования с более длительным периодом наблюдения необходимы для оценки приверженности лечению и безопасности ПЭГ. Как упоминалось выше, в долгосрочной перспективе следование рекомендациям является важным фактором эффективного лекарственного лечения, однако первичные исходы, используемые в исследованиях, не всегда соответствуют жалобам пациентов в повседневной практике. Минимальный набор исходов, которые должны быть измерены и отрепортированы, был предложен, чтобы унифицировать методы проведения исследований и устранить их неоднородность и противоречивость. Возможно такой же метод следует разработать для стандартизации жалоб пациентов с ФЗ и их родителей. И последний в списке, но не последний по значимости аспект лечения – консультирование родителей и детей по поводу ФЗ. Поведенческая терапия, добавленная к лекарственной терапии, улучшает результат [58, 59]. Этому подходу необходимо уделять больше внимания, он должен быть включен в руководства. Значительная часть исследований проводится в медицинских центрах специализированной и высокоспециализированной помощи, тогда как основная часть пациентов находятся и проходят лечение в центрах оказания первичной медицинской помощи.

Сведения об авторе
Vandenplas Yvan – MD, PhD, prof., Kidz health Castle, UZ Brussel, Belgium. E-mail: yvan.vandenplas@uzbrussel.be
1. Mugie SM, Benninga MA, Di Lorenzo C. Epidemiology of constipation in children and adults: a systematic review. Best Pract Res Clin Gastroenterol 2011; 25 (1): 3–18.
2. Lewis ML, Palsson OS, Whitehead WE, van Tilburg MA. Prevalence of Functional Gastrointestinal Disorders in Children and Adolescents. J Pediatr 2016; pii: S0022–3476(16)30056.
3. Saps M, Nichols-Vinueza DX, Rosen JM, Velasco-Benitez CA. Prevalence of functional gastrointestinal disorders in Colombian school children. J Pediat 2014; 164 (3): 542–5, e541.
4. Lu PL, Saps M. Gender, Age, and Prevalence of Pediatric Irritable Bowel Syndrome and Constipation in Colombia: A Population-Based Study. J Pediatr Gastroenterol Nutr 2016.
5. Lu PL, Saps M, Chanis RA, Velasco-Benitez CA. The prevalence of functional gastrointestinal disorders in children in Panama: a school-based study. Acta Paediatr 2016; 105 (5): e232–6.
6. Zhang SC, Qu RB, Su PJ et al. Epidemiologic survey on the prevalence and distribution of childhood functional constipation in the northern areas of China: a population-based study. Zhonghua Liu Xing Bing Xue Za Zhi 2010; 31 (7): 751–4.
7. Walter HA, Rajindrajith S, Devanarayana NM et al. OP-1 prevalence of functional constipation in infants and toddlers in Sri Lanka. J Pediatr Gastroenterol Nutr 2015; 61 (4): 541.
8. Bhatia V, Seth S, Kapoor A et al. Prevalence of functional gastrointestinal disorders among adolescents in Delhi based on Rome III criteria: A school-based survey. Indian J Gastroenterol 2016.
9. Vandenplas Y, Abkari A, Bellaiche M et al. Prevalence and Health Outcomes of Functional Gastrointestinal Symptoms in Infants From Birth to 12 Months of Age.
J Pediatr Gastroenterol Nutr 2015; 61 (5): 531–7.
10. Van Tilburg MA, Hyman PE, Walker L et al. Prevalence of functional gastrointestinal disorders in infants and toddlers. J Pediatr 2015; 166 (3): 684–9.
11. Boccia G, Manguso F, Coccorullo P et al. Functional defecation disorders in children: PACCT criteria versus Rome II criteria. J Pediatr 2007; 151 (4): 394–8, 398–e391.
12. Tabbers MM, DiLorenzo C, Berger MY et al. Evaluation and treatment of functional constipation in infants and children: evidence-based recommendations from ESPGHAN and NASPGHAN. J Pediatr Gastroenterol Nutr 2014; 58 (2): 258–74.
13. Mugie SM, Di Lorenzo C, Benninga MA. Constipation in childhood. Nature reviews Gastroenterol Hepatol 2011; 8 (9): 502–11.
14. Rajindrajith S, Devanarayana NM. Constipation in children: novel insight into epidemiology, pathophysiology and management. J Neurogastroenterol Motil 2011; 17 (1): 35–47.
15. Knowles CH, Farrugia G. Gastrointestinal neuromuscular pathology in chronic constipation. Best Pract Res Clin Gastroenterol 2011; 25 (1): 43–57.
16. King SK, Sutcliffe JR, Ong SY et al. Substance P and vasoactive intestinal peptide are reduced in right transverse colon in pediatric slow-transit constipation. Neurogastroenterol Motil 2010; 22 (8): 883–92, e234.
17. Peeters B, Benninga MA, Hennekam RC. Childhood constipation; an overview of genetic studies and associated syndromes. Best Pract Res Clin Gastroenterol 2011; 25 (1): 73–88.
18. Samsam M, Ahangari R, Naser SA. Pathophysiology of autism spectrum disorders: revisiting gastrointestinal involvement and immune imbalance. World J Gastroenterol 2014; 20 (29): 9942–51.
19. Mazurek MO, Vasa RA, Kalb LG et al. Anxiety, sensory over-responsivity, and gastrointestinal problems in children with autism spectrum disorders. J Abnorm Child Psychol 2013; 41 (1): 165–76.
20. Van Dijk M, de Vries GJ, Last BF. Parental child-rearing attitudes are associated with functional constipation in childhood. Arch Dis Child 2015; 100 (4): 329–33.
21. Philips EM, Peeters B, Teeuw AH et al. Stressful Life Events in Children With Functional Defecation Disorders. J Pediatr Gastroenterol Nutr 2015; 61 (4): 384–92.
22. Osatakul S, Puetpaiboon A. Use of Rome II versus Rome III criteria for diagnosis of functional constipation in young children. Pediatr Int 2014; 56 (1): 83–8.
23. Burgers R, Levin AD, Di Lorenzo C et al. Functional defecation disorders in children: comparing the Rome II with the Rome III criteria. J Pediatr 2012; 161 (4): 615–20, e611.
24. Lewis SJ, Heaton KW. Stool form scale as a useful guide to intestinal transit time. Scand J Gastroenterol 1997; 32 (9): 920–4.
25. Ghanma A, Puttemans K, Deneyer M et al. Amsterdam infant stool scale is more useful for assessing children who have not been toilet trained than Bristol stool scale. Acta Paediatr 2014; 103 (2): e91–2.
26. Bekkali N, Hamers SL, Reitsma JB. Infant stool form scale: development and results. J Pediatr 2009; 154 (4): 521–6, e521.
27. Burgers R, de Jong TP, Benninga MA. Rectal examination in children: digital versus transabdominal ultrasound. J Urol 2013; 190 (2): 667–72.
28. Miceli S, Arena R, Greco M et al Constipation and cow's milk allergy: a review of the literature. Int Arch Allergy Immunol 2014; 164 (1): 40–5.
29. Berger MY, Tabbers MM, Kurver MJ et al. Value of abdominal radiography, colonic transit time, and rectal ultrasound scanning in the diagnosis of idiopathic constipation in children: a systematic review. J Pediatr 2012; 161 (1): 44–50, e41–2.
30. Benninga MA, Tabbers MM, van Rijn RR. How to use a plain abdominal radiograph in children with functional defecation disorders. Arch Dis Childhood-E 2016; 101 (4): 187–93.
31. Pensabene L, Buonomo C, Fishman L et al. Lack of utility of abdominal x-rays in the evaluation of children with constipation: comparison of different scoring methods. J Pediatr Gastroenterol Nutr 2010; 51 (2): 155–9.
32. Freedman SB, Thull-Freedman J, Manson D et al. Pediatric abdominal radiograph use, constipation, and significant misdiagnoses. J Pediatr 2014; 164 (1): 83–8, e82.
33. Modin L, Dalby K, Walsted AM, Jakobsen M. Transabdominal ultrasound measurement of rectal diameter is dependent on time to defecation in constipated children. J Paediatr Child Health 2015; 51 (9): 875–80.
34. Rodriguez L, Sood M, Di Lorenzo C, Saps M. An ANMS-NASPGHAN consensus document on anorectal and colonic manometry in children. Neurogastroenterol Motil 2016. DOI: 10.1111/nmo.12944
35. Bekkali NL, van den Berg MM, Dijkgraaf MG et al. Rectal fecal impaction treatment in childhood constipation: enemas versus high doses oral PEG. Pediatrics 2009; 124 (6): e1108–15.
36. Miller MK, Dowd MD, Friesen CA, Walsh-Kelly CM. A randomized trial of enema versus polyethylene glycol 3350 for fecal disimpaction in children presenting to an emergency department. Pediatr Emerg Care 2012; 28 (2): 115–9.
37. Savino F, Maiullari E, Di Nardo G et al. Efficacy and tolerability of peg-only laxative on faecal impaction and chronic constipation in children. A controlled double blind randomized study vs a standard peg-electrolyte laxative. BMC Pediatrics 2012; 12.
38. Pijpers MA, Bongers ME, Benninga MA, Berger MY. Functional constipation in children: a systematic review on prognosis and predictive factors. J Pediatr Gastroenterol Nutr 2010; 50 (3) 256–68.
39. Bongers ME, van Wijk MP, Reitsma JB, Benninga MA. Long-term prognosis for childhood constipation: clinical outcomes in adulthood. Pediatrics 2010; 126 (1): e156–62.
40. Muller-Lissner SA, Kamm MA, Scarpignato C, Wald A. Myths and misconceptions about chronic constipation. Am J Gastroenterol 2005; 100 (1): 232–42.
41. Gordon MJ, Parker CE, Akobeng AK, Thomas AG. Osmotic and stimulant laxatives for the management of childhood constipation. Cochrane Database Syst Rev 2016.
42. Llerena E, Pujol MG, Hernandez HK et al. Comparison of the effectiveness and safety of polyethylene glycol with and without electrolytes in the treatment of chronic constipation. An Pediatr (Barc) 2016; 85 (1): 34–40.
43. Van Wering HM TM, Benninga MA. Are constipation drugs effective and safe to be used in children? A review of the literature. Expert Opin Drug Saf 2012; 11 (1): 71–82.
44. SH B. Long-term safety of PEG 4000 in children with chronic functional constipation: A biochemical perspective. Korean J Pediatr 2010; 53 (7): 741–4.
45. Tabbers MM, DiLorenzo C, Berger MY et al. Evaluation and treatment of functional constipation in infants and children: evidence-based recommendations from ESPGHAN and NASPGHAN. J Pediatr Gastroenterol Nutr 2014; 58 (2): 258–74.
46. Koppen IJ, Lammers LA, Benninga MA, Tabbers MM. Management of Functional Constipation in Children: Therapy in Practice. Paediatr Drugs 2015; 17 (5): 349–60.
47. Ormarsson OT, Asgrimsdottir GM, Loftsson T et al. Free fatty acid suppositories are as effective as docusate sodium and sorbitol enemas in treating constipation in children. Acta Paediatr 2016; 105 (6): 689–94.
48. Hansen SE, Whitehill JL, Goto CS et al. Safety and efficacy of milk and molasses enemas compared with sodium phosphate enemas for the treatment of constipation in a pediatric emergency department. Pediatr Emerg Care 2011; 27 (12): 1118–20.
49. Ladenhauf HN, Stundner O, Spreitzhofer F, Deluggi S. Severe hyperphosphatemia after administration of sodium-phosphate containing laxatives in children: case series and systematic review of literature. Pediatr Surg Int 2012; 28 (8): 805–14.
50. Hyman PE, Di Lorenzo C, Prestridge LL. Lubiprostone for the treatment of functional constipation in children. J Pediatr Gastroenterol Nutrit 2014; 58 (3): 283–91.
51. Winter HS, Di Lorenzo C, Benninga MA et al. Oral prucalopride in children with functional constipation. J Pediatr Gastroenterol Nutr 2013; 57 (2): 197–203.
52. Mugie SM, Korczowski B, Bodi P et al. Prucalopride is no more effective than placebo for children with functional constipation. Gastroenterology 2014; 147 (6): 1285–95, e1281.
53. Koppen IJ, Benninga MA, Tabbers MM. Is There A Role for Pre-, Pro- and Synbiotics in the Treatment of Functional Constipation in Children? A Systematic Review. J Pediatr Gastroenterol Nutr 2016; 63 (Suppl. 1): S27–35.
54. Kuizenga-Wessel S, Heckert SL, Tros W et al. Reporting on Outcome Measures of Functional Constipation in Children-A Systematic Review. J Pediatr Gastroenterol Nutr 2016; 62 (6): 840–6.
55. Van der Plas RN, Benninga MA, Taminiau JA, Buller HA. Treatment of defaecation problems in children: the role of education, demystification and toilet training. Eur J Pediatr 1997; 156 (9): 689–92.
56. Van Dijk M, Benninga MA, Grootenhuis MA, Last BF. Prevalence and associated clinical characteristics of behavior problems in constipated children. Pediatrics 2010; 125 (2): e309–17.
57. Borowitz SM, Sutphen JL, Kovatchev B. Treatment of childhood encopresis: a randomized trial comparing three treatment protocols. J Pediatr Gastroenterol Nutr 2002; 34 (4): 378–84.
58. Freeman KA, Riley A, Duke DC, Fu R. Systematic review and meta-analysis of behavioral interventions for fecal incontinence with constipation. J Pediatr Psychol 2014; 39 (8): 887–902.
59. Brazzelli M, Griffiths PV, Cody JD, Tappin D. Behavioural and cognitive interventions with or without other treatments for the management of faecal incontinence in children. Cochrane Database Syst Rev 2011 (12): CD002240.
60. Borowitz SM, Cox DJ, Kovatchev B et al. Treatment of childhood constipation by primary care physicians: efficacy and predictors of outcome. Pediatrics 2005; 115 (4): 873–7.


