Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2013
Опыт перевода с клозапина на арипипразол больных приступообразными формами шизофрении в период лекарственной ремиссии №06 2013
Номера страниц в выпуске:23-29
История антипсихотических средств прошла в своем развитии несколько этапов, каждый из которых ознаменовался значительным достижением в психофармакотерапии шизофрении. Последний из них, начало которого относится к 80-м годам XX в., заключался в появлении группы атипичных нейролептиков «нового поколения» с серотонин-дофаминовым механизмом действия. Однако уже в середине первого десятилетия нынешнего века стало очевидным, что материал для исследований в этом направлении исчерпан и его развитие вряд ли приведет к новым достижениям в лечении психических расстройств.
Резюме. Представлены результаты проспективного исследования эффективности арипипразола в период лекарственной ремиссии у больных шизофренией, протекающей в форме приступов, которые ранее лечились клозапином. Проведена оценка частоты развития повторных приступов болезни. Выявлены их клинико-психопатологические предикторы. Изучена динамика продуктивной и негативной психопатологической симптоматики. Полученные результаты свидетельствуют о высокой эффективности арипипразола на этапе устойчивой лекарственной ремиссии в случае ее изначально высокого качества у больных с небольшой длительностью заболевания.
Ключевые слова: шизофрения приступообразно-прогредиентная, шизофрения рекуррентная, лекарственная ремиссия, атипичные антипсихотические средства, арипипразол, клозапин.
Transition experience from clozapine to aripiprazole with patients having intermittent schizophrenia within the period of therapeutic remission
D.S.Danilov1,2, D.O.Magomedova3
1S.S.Korsakov Clinic of Psychiatry, the University Clinical Hospital №3, I.M.Sechenov First Moscow State Medical University, Ministry of Health of Russia
2Mental Health Research, Education and Clinical Center, I.M.Sechenov First Moscow State Medical University,
Ministry of Health of Russia
3Department of Psychiatry and Narcology, I.M.Sechenov First Moscow State Medical University, Ministry of Health
of Russia
Summary. The article presents the results of a prospective study of the effectiveness of aripiprazole during the period of therapeutic remission for patients with schizophrenia, which flows in acute attacks type of course, who have previously been treated with clozapine. Frequency estimationof the repeated bouts of illnesswas carried out. Its clinical-psychopathological predictors were identified. Dynamics of positive and negative psychopathological symptoms was investigated. The results obtained testify to the high effectiveness of aripiprazole at the stage of stable therapeutic remission in case of its original high quality for patients with a small duration of the disease, previously treated with clozapine.
Key words: intermittent schizophrenia, recurrent schizophrenia, therapeutic remission, atypical antipsychotics, aripiprazole, clozapine.
Введение
История антипсихотических средств прошла в своем развитии несколько этапов, каждый из которых ознаменовался значительным достижением в психофармакотерапии шизофрении [1]. Последний из них, начало которого относится к 80-м годам XX в., заключался в появлении группы атипичных нейролептиков «нового поколения» с серотонин-дофаминовым механизмом действия. Однако уже в середине первого десятилетия нынешнего века стало очевидным, что материал для исследований в этом направлении исчерпан и его развитие вряд ли приведет к новым достижениям в лечении психических расстройств [2–4]. В этом смысле новые надежды на успехи в лечении появились после появления в 2002 г. группы антипсихотических средств – частичных агонистов дофаминовых рецепторов1,2. В течение последних 10 лет данная группа представлена единственным нейролептиком арипипразолом, хотя предпринимаются попытки ее расширения за счет создания новых представителей. Некоторые частичные агонисты дофаминовых рецепторов (например, бифепрунокс) не прошли заключительную фазу клинических исследований. Более перспективными в этом отношении представляются другие кандидаты (например, карипразин3 [6]).
С момента появления арипипразола проведено множество исследований его эффективности при лечении шизофрении. Антипсихотическая активность арипипразола доказана результатами масштабных двойных слепых плацебо-контролируемых исследований [7]. Это нашло отражение в формулировании показаний к его применению: «лечение острых приступов шизофрении», «поддерживающая терапия шизофрении». Однако до сих пор не получено данных, позволяющих более точно дифференцировать показания к назначению арипипразола из-за неизученности клинико-психопатологических предикторов эффективности терапии. Одновременно существуют разногласия в оценке эффективности арипипразола при сравнении с другими антипсихотическими средствами. Одни исследования демонстрируют его преимущества (прежде всего в способности ослаблять негативную симптоматику) [8–10], другие оспаривают их [11, 12]. Довольно парадоксальным выглядит отсутствие исследований сравнения эффективности арипипразола и прототипа всех атипичных нейролептиков – клозапина4.
Описанная ситуация значительно затрудняет выбор терапии на практике. При назначении арипипразола специалистам часто приходится действовать методом «проб и ошибок». Поэтому весьма вероятно, что больные, у которых терапия арипипразолом была бы более эффективна, чем лечение другими нейролептиками, ее не получают. Одновременно нельзя исключить возможность применения препарата у тех больных, у которых оно не оправдано. Один из способов разрешения этой проблемы заключается в последовательном проведении серии обсервационных исследований, изучающих зависимость эффективности терапии арипипразолом от разных клинико-психопатологических факторов (в сравнении с другими антипсихотическими средствами), и формулировании дифференцированных показаний к ее назначению у разных групп больных.
Цель исследования – изучение эффективности терапии арипипразолом в период лекарственной ремиссии при шизофрении, протекающей в форме приступов, при небольшой длительности заболевания у больных, ранее лечившихся клозапином.
Материалы и методы
Было обследовано 39 больных шизофренией, протекающей в форме приступов (рекуррентная и шубообразная формы5). Все пациенты были мужчинами. Их возраст составлял от 21 до 33 лет (средний возраст – 25,9±0,86 года). Длительность заболевания во всех случаях не превышала
5 лет (средняя длительность – 2,3±0,4 года). В анамнезе наблюдалось не более 2 приступов болезни (манифестный приступ – 64,1%, 2 приступа – 35,9%). Пациенты включались в исследование в период лекарственной ремиссии.
До начала исследования длительность ремиссий (с момента отзвучания очередного острого психоза) составляла от 6 до 12 мес (средняя длительность – 9,2±0,5 мес). Состояние больных было стабильным без признаков усиления или значительного ослабления тяжести психопатологических расстройств (этап окончательной «консолидации» ремиссии [16, 17]). Качество лекарственных ремиссий у всех больных было довольно высоким. Тяжесть продуктивной симптоматики психотического и невротического уровней составляла от 24 до 45 баллов при суммарной оценке по шкале Positive and Negative Syndrome Scale (PANSS) – PANSS positive и PANSS global (средняя тяжесть – 34,9±1,8 балла). Выраженность негативной симптоматики при оценке по шкале PANSS negative составила от 8 до 25 баллов (средняя выраженность – 18,1±1,5 балла). Уровень критики и степени осознания болезни по пункту «снижение критичности и осознания болезни» шкалы PANSS регистрировался от 1 до 4 баллов (среднее значение – 2,4±0,3 балла). Состояние 7 (18%) больных соответствовало гиперстеническому варианту ремиссии, 2 (5%) – психопатоподобному, 25 (64%) – апатическому (аутистическому) и 5 (13%) – астеническому варианту ремиссии7.
До начала исследования больные принимали поддерживающую (противорецидивную) терапию клозапином в дозе от 150 до 350 мг/сут (средняя доза – 255,8±18,2 мг/сут), разделенной на 2 или 3 приема. У всех больных терапия клозапином (в более высоких дозах) была начата в период лечения острого психотического состояния и продолжена в период лекарственной ремиссии (со снижением дозы). Обязательными условиями включения больных в настоящее исследование являлись правильное соблюдение ими рекомендованной схемы приема нейролептиков8 и понимание родственниками необходимости проведения терапии. 30 (77%) больных были настроены лечиться (более
0 баллов по шкале Drug Attitudes Inventory – DAI-30). 9 (23%) пациентов принимали лекарства правильно, но неохотно (менее 0 баллов по DAI-30). Перед началом исследования больным назначался арипипразол в дозе от 10 до 15 мг/сут (средняя доза – 14,2±0,6 мг/сут) без ее титрации в виде однократного приема утром (в некоторых случаях допускался двукратный прием). Одновременно в течение 2 нед проводилась постепенная отмена клозапина. В случае развития диссомнических расстройств вечерний прием клозапина сохранялся, но в субтерапевтической (субантипсихотической) дозе (от 50 до 100 мг). Терапия арипипразолом продолжалась в течение всего периода наблюдения.
Наблюдение продолжалось 12 мес. Обследование проводилось комплексно с использованием традиционных способов оценки состояния (клинико-психопатологический метод) и методов, основанных на принципах доказательной медицины (использование стандартизированных рейтинговых шкал и опросников). В процессе исследования оценивалась частота повторных приступов заболевания. Изучалась динамика продуктивной и негативной психопатологической симптоматики по шкале PANSS. Оценка социальной адаптации проводилась по шкале Personal and Social Performance Scale (PSP). Регистрировались частота побочных эффектов терапии по шкале Udvald for Kliniske Undersogelser Scale (UKU) и частота назначения препаратов-корректоров. Отношение больных к лечению (желание лечиться) оценивалось по шкале DAI-30. Больные обследовались исходно, ежемесячно в течение первых 3 мес наблюдения, через 6, 9 и 12 мес терапии. Статистическая обработка полученных данных проводилась при помощи методов параметрической и непараметрической статистики.
Результаты проведенного исследования показали, что в течение 12 мес наблюдения у подавляющего числа больных – 32 (82,1%) человек, принимавших арипипразол, сохранялись устойчивые лекарственные ремиссии без признаков усиления тяжести продуктивной психопатологической симптоматики. Состояние 17,9% (7 наблюдений) больных ухудшалось, что проявлялось повторным развитием острых психотических состояний. Их тяжесть была разной (от симптомов, характеризующих этапы бредового настроения и восприятия, до развернутых острых психозов в виде острого параноида, острой парафрении или онейроидной кататонии) и зависела от своевременности выявления. В обследованной группе число больных с устойчивой лекарственной ремиссией значительно превышало тех, у кого развивались повторные обострения (р=0,00009) (рис. 1). Динамическая оценка частоты развития повторных приступов заболевания свидетельствует о том, что состояние больных ухудшалось в период 4–6 мес терапии. Рецидивов болезни в течение первых 3 и 6–12 мес отмечено не было.
Как было отмечено в разделе статьи «Материалы и методы», при планировании исследования допускалось, что в случае развития нарушений сна (после отмены клозапина и назначения арипипразола) вечерний прием клозапина мог быть сохранен (в дозе от 50 до 100 мг).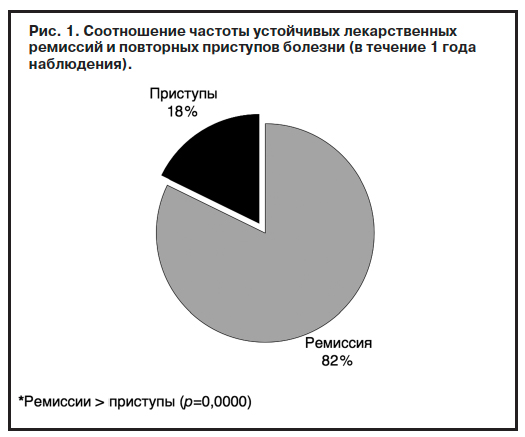 Таких наблюдений было 32 (82,1% от общего числа больных). Указанная доза клозапина сравнительно невелика и обычно рассматривается как субантипсихотическая (субпротиворецидивная). Для окончательного исключения возможности усиления антипсихотического (противорецидивного) эффекта арипипразола невысокими дозами клозапина отдельно было проведено изучение противорецидивной активности монотерапии клозапином в дозе от 50 до 100 мг/сут. Для этого была изучена выборка из 31 больного приступообразными формами шизофрении, которые вопреки рекомендациям врача принимали клозапин только однократно вечером для достижения снотворного эффекта (в дозе от 50 до 100 мг). В течение 12 мес наблюдения повторные приступы заболевания у этих больных развивались значительно чаще, чем у пациентов, принимавших комбинацию арипипразола и клозапина, – 29 (93,5%) случаев против 6 (8,8%) случаев (p=0,0000). Одновременно не было выявлено различий между группами больных с повторными рецидивами, которые принимали комбинацию арипипразола и клозапина или только арипипразол, – 6 (18,8%) случаев против 1 (14,3%) случая (p=1,0). Эти наблюдения доказывают низкую вероятность усиления антипсихотического (противорецидивного) эффекта арипипразола в случае его сочетания с невысокими дозами клозапина. Таким образом, полученные в настоящем исследовании данные о частоте повторных приступов болезни при лечении арипипразолом в сочетании с невысокими дозами клозапина можно экстраполировать на популяцию больных, принимающих монотерапию арипипразолом.
Таких наблюдений было 32 (82,1% от общего числа больных). Указанная доза клозапина сравнительно невелика и обычно рассматривается как субантипсихотическая (субпротиворецидивная). Для окончательного исключения возможности усиления антипсихотического (противорецидивного) эффекта арипипразола невысокими дозами клозапина отдельно было проведено изучение противорецидивной активности монотерапии клозапином в дозе от 50 до 100 мг/сут. Для этого была изучена выборка из 31 больного приступообразными формами шизофрении, которые вопреки рекомендациям врача принимали клозапин только однократно вечером для достижения снотворного эффекта (в дозе от 50 до 100 мг). В течение 12 мес наблюдения повторные приступы заболевания у этих больных развивались значительно чаще, чем у пациентов, принимавших комбинацию арипипразола и клозапина, – 29 (93,5%) случаев против 6 (8,8%) случаев (p=0,0000). Одновременно не было выявлено различий между группами больных с повторными рецидивами, которые принимали комбинацию арипипразола и клозапина или только арипипразол, – 6 (18,8%) случаев против 1 (14,3%) случая (p=1,0). Эти наблюдения доказывают низкую вероятность усиления антипсихотического (противорецидивного) эффекта арипипразола в случае его сочетания с невысокими дозами клозапина. Таким образом, полученные в настоящем исследовании данные о частоте повторных приступов болезни при лечении арипипразолом в сочетании с невысокими дозами клозапина можно экстраполировать на популяцию больных, принимающих монотерапию арипипразолом.
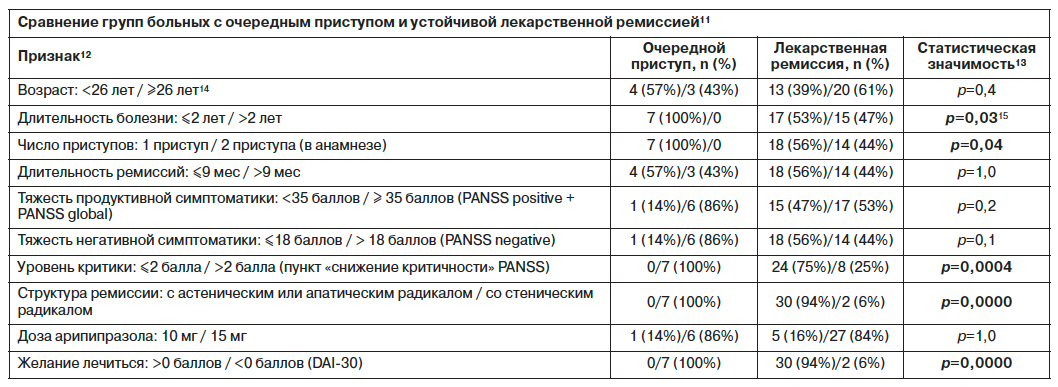
Для выявления индивидуальных предикторов эффективности терапии арипипразолом было проведено клинико-статистическое сравнение групп больных с развитием очередного приступа и с устойчивой лекарственной ремиссией10. Группы сравнивались по возрасту, клинико-психопатологическим особенностям заболевания, особенностям текущего психического состояния и терапии, по отношению больных к лекарственному лечению (см. таблицу). Полученные данные свидетельствуют, что рецидивы заболевания чаще развивались у больных, не настроенных лечиться (p=0,0000), с низким уровнем критики (более 2 баллов; p=0,0004), при длительности болезни менее 2 лет (p=0,03) и перенесших 1 манифестный психоз (p=0,04). У больных с повторными обострениями в структуре предшествующей ремиссии преобладал стенический радикал (гиперстенические и психопатоподобные ремиссии), в то время как при устойчивых лекарственных ремиссиях – простая дефицитарность (апатические и астенические ремиссии) (p=0,0000). Группы не различались по возрасту больных, длительности текущей лекарственной ремиссии, тяжести продуктивной и негативной симптоматики (при суммарной оценке каждого круга симптомов отдельно) и дозе арипипразола (p>0,05). Эти данные означают, что выраженный стенический радикал в структуре ремиссии, низкий уровень критики и отсутствие настроенности на лечение являются надежными предикторами низкой эффективности терапии, т.е. развития повторного приступа болезни. Данные, полученные от больных во время клинической беседы (в том числе post factum), опросы их родственников и учет числа неизрасходованных таблеток свидетельствовали, что большинство таких больных принимали терапию несистематически или полностью отказывались от нее в течение 1-го месяца исследования. Этим объясняется факт развития рецидивов болезни через 4–6 мес наблюдения (см. выше), поскольку для ухудшения состояния необходим период перестройки нейротрансмиттерных систем на «болезненный уровень». Интересно, что до начала исследования, несмотря на отсутствие желания лечиться, все больные придерживались рекомендованной схемы приема клозапина (обязательный критерий включения в исследование). Вероятно, при лечении клозапином противодействие больных терапии нивелировалось ее седативным эффектом. Отсутствие седативного действия при приеме арипипразола в совокупности с его активирующим эффектом приводило к усилению «негативизма» таких больных по отношению к лекарственной терапии.
Одновременно с оценкой частоты рецидивов заболевания эффективность терапии оценивалась при помощи изучения динамики психопатологической симптоматики16. Динамическая оценка выраженности продуктивных расстройств свидетельствовала о стабильности состояния больных17. Клиническое наблюдение показало, что в течение всего периода исследования устойчивые лекарственные ремиссии характеризовались высоким качеством с сохранением критики, отсутствием нарушений стройности мышления, явлений негативизма, выраженной тревоги и депрессивных реакций. При статистическом сравнении значимых различий между группами выявлено не было (средний балл PANSS positive + PANSS global составлял 33,8±1,9; 33,6±1,9; 33,3±1,7; 33,4±1,7; 33,4±1,7; 33,0±1,7 и 32,6±1,7 – исходно18, через 1, 2, 3, 6, 9 и 12 мес терапии соответственно).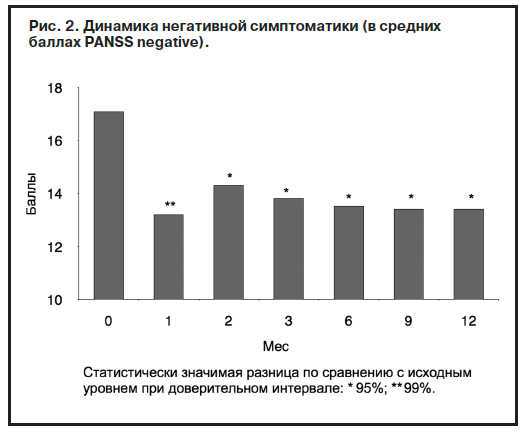
Более интересными представляются данные оценки динамики негативной симптоматики. Клиническое наблюдение свидетельствовало, что в течение 1-го месяца терапии арипипразолом состояние больных значительно улучшалось. Отмечалось эмоциональное и двигательное оживление. Расширялся круг контактов и интересов. Больные становились более расположенными к общению, стремились к нему, охотнее выполняли привычные обязанности, появлялись новые увлечения. Они описывали субъективное ощущение «четкости», «легкости» мыслей, «прояснение», «просветление в голове», «бодрости». В некоторых случаях оживление было столь отчетливым и ярким, что становилось причиной незапланированного обращения пациентов к врачу по настоянию родных. Однако ни у одного больного оно не могло быть расценено как начальный этап бредового психоза или гипомания. Через 2 мес лечения первоначальная эмоциональная и двигательная активизация несколько стихала. Однако больные оставались более оживленными, чем до начала исследования. В последующие 2 мес их состояние продолжало постепенно улучшаться, а затем стабилизировалось. Статистическое сравнение выраженности негативной симптоматики в динамике подтвердило данные клинического наблюдения (рис. 2). Выраженность негативных расстройств составила 17,1±1,5/2,019; 13,2±1,1/1,5; 14,3±1,220; 13,8±1,1; 13,5±1,2; 13,4±1,2 и 13,4±1,2 балла – исходно, через 1, 2, 3, 6, 9 и 12 мес соответственно. Клинико-статистические данные о значительном улучшении состояния больных в течение 1-го месяца наблюдения, вероятно, объясняются не только антинегативным действием арипипразола, но и устранением седативного эффекта нейролептической терапии (после отмены клозапина)21. Собственно антинегативный эффект арипипразола, по всей видимости, проявлялся начиная со 2-го месяца лечения, когда седативное действие было полностью устранено.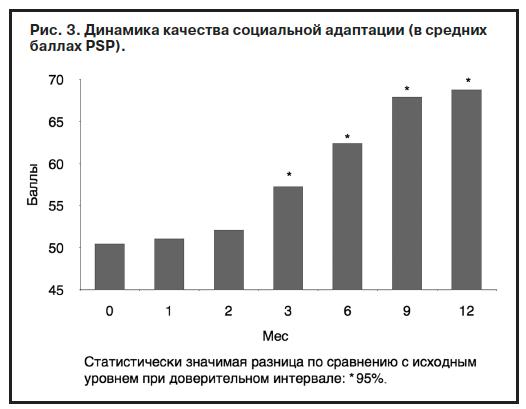
Описанная динамика негативных расстройств при приеме арипипразола проявлялась в улучшении социальной адаптации больных (рис. 3). Начиная с 3-го месяца терапии средние показатели по шкале PSP значительно превышали исходный уровень (50,5±1,7; 51,1±1,8; 52,1±1,9; 57,3±2,1; 62,4±2,5; 67,9±2,8 и 68,8±2,5 балла – исходно, через 1, 2, 3, 6, 9 и 12 мес соответственно). Наибольшее улучшение качества социальной адаптации наблюдалось через 3, 6 и 9 мес лечения. Обращает внимание «отсроченность» этого эффекта по отношению к ослаблению негативных расстройств (их выраженность ослабевала раньше – в течение первых 3 мес терапии).
В заключение необходимо остановиться на переносимости терапии арипипразолом, но лишь кратко, поскольку этот вопрос требует более тщательного анализа и достоин описания в рамках отдельной журнальной статьи. Среди побочных эффектов арипипразола в настоящем исследовании наблюдались лишь неврологические нарушения.
У 8 (20,5%) больных было отмечено развитие акатизии, тяжесть которой была невелика. Она легко корректировалась назначением тригексифенидила или биперидена в дозе от 4 до 6 мг/сут. У 1 (2,6%) больного спустя 12 мес терапии развились явления поздней дискинезии. Нарушения сна, которые отмечались в первые недели монотерапии арипипразолом (см. выше), нельзя расценивать как побочный эффект лечения. Они могли быть связаны с отменой клозапина. Других нежелательных явлений при лечении арипипразолом, которые могли бы быть выявлены во время клинических бесед или по наблюдению родственников больных, отмечено не было.
Эффективность атипичных нейролептиков при лечении шизофрении не вызывает сомнений. Однако несмотря на многочисленные исследования, до сих пор остается много разногласий в отношении зависимости терапевтического эффекта атипичных нейролептиков от клинико-психопатологических особенностей заболевания и текущего психического состояния. Одновременно противоречивы данные сравнения эффективности разных атипичных антипсихотических средств [16]. Эти вопросы в полной мере адресуются к наиболее «молодому» атипичному нейролептику – арипипразолу22. Результаты систематических Кохрановских обзоров свидетельствуют о необходимости продолжения изучения его эффективности при лечении шизофрении из-за недостаточного количества исследований [11, 12]. Отечественных исследований пока явно недостаточно, чтобы оценить эффективность терапии с позиции традиционного для российской психиатрии подхода (выделение индивидуальных предикторов эффективности и формулирование дифференцированных показаний к назначению). Немногочисленные клинические исследования [20–23], клинические наблюдения [24] и обзоры литературы [25–27] отечественных авторов пока не могут в полной мере ответить на поставленные вопросы.
Представленное исследование является попыткой выделения некоторых клинико-психопатологических предикторов эффективности арипипразола при лечении шизофрении (в сравнении с клозапином). Его результаты свидетельствуют о высокой эффективности арипипразола у больных шизофренией, протекающей в форме приступов, в период лекарственной ремиссии при условии ее изначально высокого качества и небольшой длительности болезни. Показано, что арипипразол обладает достаточным антипсихотическим (противорецидивным) эффектом для предотвращения развития повторных приступов заболевания (при условии правильного соблюдения рекомендованной схемы лечения23) и сопоставим по этому показателю с клозапином. Применение арипипразола в период лекарственной ремиссии после отмены клозапина приводит к дальнейшему улучшению состояния больных в виде их двигательной и эмоциональной активизации (снижение тяжести негативных расстройств) и последующего улучшения качества социальной адаптации. Это наблюдение представляет большой интерес, поскольку до сих пор предполагалось, что клозапин обладает максимально возможными антипсихотическим и антинегативным эффектами. Интересно, что за рубежом также предпринимаются попытки исследования эффективности арипипразола после периода лечения клозапином, но они ограничиваются резистентными случаями болезни [28]. Неоднократно отмечалось, что арипипразол обладает благоприятным (по сравнению с типичными и атипичными нейролептиками II поколения) профилем побочных эффектов, а в некоторых случаях может использоваться для их коррекции (при нейролептическом ожирении или нейролептической гиперпролактинемии) [29]. Хотя в задачи настоящего исследования не входила оценка переносимости лечения, предварительные результаты свидетельствуют, что спектр побочных эффектов у обследованных больных ограничивался лишь случаями легкой акатизии. Важно отметить, что в среднетерапевтических дозах терапия арипипразолом не приводила к развитию седативного эффекта. Это благоприятно сказывалось на состоянии части больных в период ремиссии, однако в некоторых случаях приводило к нежелательным последствиям (диссомнические расстройства, отказ от лечения в связи с усилением негативизма к лечению у больных с отсутствием критики).
Несмотря на успешное разрешение задач, поставленных в настоящем исследовании, с целью уточнения и расширения объема полученных результатов необходимо его продолжение (увеличение числа обследованных больных, более длительный период катамнеза, исследование эффективности терапии на начальных этапах ремиссии, детальная оценка переносимости терапии и т.д.). Рациональным представляется проведение подобных исследований (особенно в сравнении с другими нейролептиками) в период купирующей терапии приступообразных форм шизофрении, на разных этапах течения непрерывной параноидной и вялотекущей шизофрении.
Примечания
1Отличие этой группы от других нейролептиков заключается в том, что при избытке дофамина они блокируют дофаминовые рецепторы (ослабляя проявления психоза), а при его дефиците – стимулируют их (ослабляя негативную симптоматику). Фактически эти средства одновременно сочетают свойства низких и высоких доз дезингибирующих нейролептиков (пимозид и др.), которые в низких дозах обладают активирующим, а в высоких – антипсихотическим действием. При неизмененном уровне дофамина (в нигростриальной системе и гипофизе) частичные агонисты дофаминовых рецепторов не проявляют своей активности, поэтому в отличие от других нейролептиков риск неврологических и эндокринных расстройств при их приеме невысок. Способность частичных агонистов дофаминовых рецепторов ослаблять проявления негативной симптоматики и редкость возникновения при их приеме экстрапирамидных расстройств позволяют рассматривать их в группе атипичных антипсихотических средств. Уникальный механизм действия частичных агонистов дофаминовых рецепторов дает основание отнести их к «нейролептикам III поколения» в противовес типичным (FGAs – first-generation antipsychotics) и атипичным (SGAs – second-generation antipsychotics) антипсихотическим средствам [5].
2Термин «частичные агонисты дофаминовых рецепторов» несколько условен. Например, арипипразол одновременно с влиянием на дофаминергическую систему является сильным антагонистом 5НТ2A- и агонистом 5НТ1A-серотониновых рецепторов.
3Частичный агонист дофаминовых рецепторов, синтезированный в лаборатории фармацевтической фирмы «Gedeon Richter», известной производством одного из генериков арипипразола Амдоала.
4Справедливости ради необходимо отметить, что исследования сравнения эффективности с клозапином отсутствуют не только для арипипразола, но и для многих других атипичных нейролептиков.
5Для нозологической квалификации их состояния использовалась отечественная классификация синдромальных форм и типов течения шизофрении [13, 14]. Для «стандартизации» диагноза применялись критерии диагностики Международной классификации болезней
10-го пересмотра (состояние больных соответствовало рубрикам F20.х1, F20.x2, F20.x3, F20.x9, F25.01) [15].
6Здесь и далее в тексте представлена величина 95% доверительного интервала.
7Варианты ремиссий выделялись на основании клинической оценки состояния больных. Типы ремиссий, которые наблюдались в настоящем исследовании, были неоднократно описаны в классических работах [18, 19].
8Правильность соблюдения рекомендованной схемы лечения оценивалась на основании сопоставления данных, полученных от больных во время клинической беседы, опроса их родственников и учета числа неизрасходованных таблеток.
9На основании вычисления величины «p» при сравнении 2 пропорций. Использован двусторонний критерий статистической значимости.
10Очевидна предварительность результатов подобного клинико-статистического сравнения из-за немногочисленности больных в группе «повторный приступ». Однако полученные данные могут быть ориентиром для проведения дальнейших исследований в этом направлении.
11Сравнение проводилось только по качественным бинарным признакам. Сравнение по количественным признакам не проводилось из-за несопоставимости численности групп больных с очередным приступом и лекарственной ремиссией.
12Признак измерялся на момент начала исследования.
13Расчет производился методом Фишера.
14Для непрерывных величин в качестве критерия разделения больных на пропорции было выбрано округленное среднее значение того или иного признака (представлены в разделе «Материалы и методы»).
15Здесь и далее в этом столбце полужирным шрифтом выделены статистически значимые различия.
16Оценка проводилась в группе 32 больных, поскольку 7 человек были исключены из исследования из-за развития рецидивов болезни.
17В данном случае речь прежде всего идет об отсутствии усиления тяжести продуктивных расстройств невротического уровня, поскольку больные, у которых резко усиливались психотические симптомы (т.е. развивались рецидивы болезни), из исследования исключались.
18Представленный здесь и далее показатель исходного среднего балла отличается от показателя, представленного в разделе «Материалы и методы», поскольку он рассчитывался повторно после исключения из исследования части больных (7 человек).
19Через дробь представлены величины 95% и 99% доверительных интервалов.
20Здесь и далее представлена величина 95% доверительного интервала.
21Однако необходимо учитывать, что больные включались в исследование в среднем спустя 9 мес после отзвучания острого психотического состояния (см. раздел «Материалы и методы»), т.е. в период, когда седативное действие клозапина значительно ослабевало и значительно не влияло на состояние больных [16].
22Необходимо отметить, что почти в таком же объеме они адресуются к атипичным нейролептикам, которые используются в клинической практике уже длительное время (рисперидон, оланзапин, кветиапин, амисульприд и др.).
23Поскольку настоящее исследование проводилось в условиях университетской психиатрической клиники с традиционно индивидуальным подходом к лечению (в том числе использование психотерапевтических методов, направленных на повышение качества соблюдения больными рекомендаций врача), возможно, что в более широкой клинической практике частота рецидивов при лечении арипипразолом будет выше.
Сведения об авторах
Данилов Дмитрий Сергеевич – д-р мед. наук, зав. отд-нием Клиники психиатрии им. С.С.Корсакова Университетской клинической больницы №3 ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России; вед. науч. сотр. НОКЦ «Психическое здоровье» ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России. E-mail: clinica2001@inbox.ru
Магомедова Диана Олеговна – клин. ординатор каф. психиатрии и наркологии ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России. E-mail: clinica2001@inbox.ru:
Ключевые слова: шизофрения приступообразно-прогредиентная, шизофрения рекуррентная, лекарственная ремиссия, атипичные антипсихотические средства, арипипразол, клозапин.
Transition experience from clozapine to aripiprazole with patients having intermittent schizophrenia within the period of therapeutic remission
D.S.Danilov1,2, D.O.Magomedova3
1S.S.Korsakov Clinic of Psychiatry, the University Clinical Hospital №3, I.M.Sechenov First Moscow State Medical University, Ministry of Health of Russia
2Mental Health Research, Education and Clinical Center, I.M.Sechenov First Moscow State Medical University,
Ministry of Health of Russia
3Department of Psychiatry and Narcology, I.M.Sechenov First Moscow State Medical University, Ministry of Health
of Russia
Summary. The article presents the results of a prospective study of the effectiveness of aripiprazole during the period of therapeutic remission for patients with schizophrenia, which flows in acute attacks type of course, who have previously been treated with clozapine. Frequency estimationof the repeated bouts of illnesswas carried out. Its clinical-psychopathological predictors were identified. Dynamics of positive and negative psychopathological symptoms was investigated. The results obtained testify to the high effectiveness of aripiprazole at the stage of stable therapeutic remission in case of its original high quality for patients with a small duration of the disease, previously treated with clozapine.
Key words: intermittent schizophrenia, recurrent schizophrenia, therapeutic remission, atypical antipsychotics, aripiprazole, clozapine.
Введение
История антипсихотических средств прошла в своем развитии несколько этапов, каждый из которых ознаменовался значительным достижением в психофармакотерапии шизофрении [1]. Последний из них, начало которого относится к 80-м годам XX в., заключался в появлении группы атипичных нейролептиков «нового поколения» с серотонин-дофаминовым механизмом действия. Однако уже в середине первого десятилетия нынешнего века стало очевидным, что материал для исследований в этом направлении исчерпан и его развитие вряд ли приведет к новым достижениям в лечении психических расстройств [2–4]. В этом смысле новые надежды на успехи в лечении появились после появления в 2002 г. группы антипсихотических средств – частичных агонистов дофаминовых рецепторов1,2. В течение последних 10 лет данная группа представлена единственным нейролептиком арипипразолом, хотя предпринимаются попытки ее расширения за счет создания новых представителей. Некоторые частичные агонисты дофаминовых рецепторов (например, бифепрунокс) не прошли заключительную фазу клинических исследований. Более перспективными в этом отношении представляются другие кандидаты (например, карипразин3 [6]).
С момента появления арипипразола проведено множество исследований его эффективности при лечении шизофрении. Антипсихотическая активность арипипразола доказана результатами масштабных двойных слепых плацебо-контролируемых исследований [7]. Это нашло отражение в формулировании показаний к его применению: «лечение острых приступов шизофрении», «поддерживающая терапия шизофрении». Однако до сих пор не получено данных, позволяющих более точно дифференцировать показания к назначению арипипразола из-за неизученности клинико-психопатологических предикторов эффективности терапии. Одновременно существуют разногласия в оценке эффективности арипипразола при сравнении с другими антипсихотическими средствами. Одни исследования демонстрируют его преимущества (прежде всего в способности ослаблять негативную симптоматику) [8–10], другие оспаривают их [11, 12]. Довольно парадоксальным выглядит отсутствие исследований сравнения эффективности арипипразола и прототипа всех атипичных нейролептиков – клозапина4.
Описанная ситуация значительно затрудняет выбор терапии на практике. При назначении арипипразола специалистам часто приходится действовать методом «проб и ошибок». Поэтому весьма вероятно, что больные, у которых терапия арипипразолом была бы более эффективна, чем лечение другими нейролептиками, ее не получают. Одновременно нельзя исключить возможность применения препарата у тех больных, у которых оно не оправдано. Один из способов разрешения этой проблемы заключается в последовательном проведении серии обсервационных исследований, изучающих зависимость эффективности терапии арипипразолом от разных клинико-психопатологических факторов (в сравнении с другими антипсихотическими средствами), и формулировании дифференцированных показаний к ее назначению у разных групп больных.
Цель исследования – изучение эффективности терапии арипипразолом в период лекарственной ремиссии при шизофрении, протекающей в форме приступов, при небольшой длительности заболевания у больных, ранее лечившихся клозапином.
Материалы и методы
Было обследовано 39 больных шизофренией, протекающей в форме приступов (рекуррентная и шубообразная формы5). Все пациенты были мужчинами. Их возраст составлял от 21 до 33 лет (средний возраст – 25,9±0,86 года). Длительность заболевания во всех случаях не превышала
5 лет (средняя длительность – 2,3±0,4 года). В анамнезе наблюдалось не более 2 приступов болезни (манифестный приступ – 64,1%, 2 приступа – 35,9%). Пациенты включались в исследование в период лекарственной ремиссии.
До начала исследования длительность ремиссий (с момента отзвучания очередного острого психоза) составляла от 6 до 12 мес (средняя длительность – 9,2±0,5 мес). Состояние больных было стабильным без признаков усиления или значительного ослабления тяжести психопатологических расстройств (этап окончательной «консолидации» ремиссии [16, 17]). Качество лекарственных ремиссий у всех больных было довольно высоким. Тяжесть продуктивной симптоматики психотического и невротического уровней составляла от 24 до 45 баллов при суммарной оценке по шкале Positive and Negative Syndrome Scale (PANSS) – PANSS positive и PANSS global (средняя тяжесть – 34,9±1,8 балла). Выраженность негативной симптоматики при оценке по шкале PANSS negative составила от 8 до 25 баллов (средняя выраженность – 18,1±1,5 балла). Уровень критики и степени осознания болезни по пункту «снижение критичности и осознания болезни» шкалы PANSS регистрировался от 1 до 4 баллов (среднее значение – 2,4±0,3 балла). Состояние 7 (18%) больных соответствовало гиперстеническому варианту ремиссии, 2 (5%) – психопатоподобному, 25 (64%) – апатическому (аутистическому) и 5 (13%) – астеническому варианту ремиссии7.
До начала исследования больные принимали поддерживающую (противорецидивную) терапию клозапином в дозе от 150 до 350 мг/сут (средняя доза – 255,8±18,2 мг/сут), разделенной на 2 или 3 приема. У всех больных терапия клозапином (в более высоких дозах) была начата в период лечения острого психотического состояния и продолжена в период лекарственной ремиссии (со снижением дозы). Обязательными условиями включения больных в настоящее исследование являлись правильное соблюдение ими рекомендованной схемы приема нейролептиков8 и понимание родственниками необходимости проведения терапии. 30 (77%) больных были настроены лечиться (более
0 баллов по шкале Drug Attitudes Inventory – DAI-30). 9 (23%) пациентов принимали лекарства правильно, но неохотно (менее 0 баллов по DAI-30). Перед началом исследования больным назначался арипипразол в дозе от 10 до 15 мг/сут (средняя доза – 14,2±0,6 мг/сут) без ее титрации в виде однократного приема утром (в некоторых случаях допускался двукратный прием). Одновременно в течение 2 нед проводилась постепенная отмена клозапина. В случае развития диссомнических расстройств вечерний прием клозапина сохранялся, но в субтерапевтической (субантипсихотической) дозе (от 50 до 100 мг). Терапия арипипразолом продолжалась в течение всего периода наблюдения.
Наблюдение продолжалось 12 мес. Обследование проводилось комплексно с использованием традиционных способов оценки состояния (клинико-психопатологический метод) и методов, основанных на принципах доказательной медицины (использование стандартизированных рейтинговых шкал и опросников). В процессе исследования оценивалась частота повторных приступов заболевания. Изучалась динамика продуктивной и негативной психопатологической симптоматики по шкале PANSS. Оценка социальной адаптации проводилась по шкале Personal and Social Performance Scale (PSP). Регистрировались частота побочных эффектов терапии по шкале Udvald for Kliniske Undersogelser Scale (UKU) и частота назначения препаратов-корректоров. Отношение больных к лечению (желание лечиться) оценивалось по шкале DAI-30. Больные обследовались исходно, ежемесячно в течение первых 3 мес наблюдения, через 6, 9 и 12 мес терапии. Статистическая обработка полученных данных проводилась при помощи методов параметрической и непараметрической статистики.
Результаты проведенного исследования показали, что в течение 12 мес наблюдения у подавляющего числа больных – 32 (82,1%) человек, принимавших арипипразол, сохранялись устойчивые лекарственные ремиссии без признаков усиления тяжести продуктивной психопатологической симптоматики. Состояние 17,9% (7 наблюдений) больных ухудшалось, что проявлялось повторным развитием острых психотических состояний. Их тяжесть была разной (от симптомов, характеризующих этапы бредового настроения и восприятия, до развернутых острых психозов в виде острого параноида, острой парафрении или онейроидной кататонии) и зависела от своевременности выявления. В обследованной группе число больных с устойчивой лекарственной ремиссией значительно превышало тех, у кого развивались повторные обострения (р=0,00009) (рис. 1). Динамическая оценка частоты развития повторных приступов заболевания свидетельствует о том, что состояние больных ухудшалось в период 4–6 мес терапии. Рецидивов болезни в течение первых 3 и 6–12 мес отмечено не было.
Как было отмечено в разделе статьи «Материалы и методы», при планировании исследования допускалось, что в случае развития нарушений сна (после отмены клозапина и назначения арипипразола) вечерний прием клозапина мог быть сохранен (в дозе от 50 до 100 мг).
 Таких наблюдений было 32 (82,1% от общего числа больных). Указанная доза клозапина сравнительно невелика и обычно рассматривается как субантипсихотическая (субпротиворецидивная). Для окончательного исключения возможности усиления антипсихотического (противорецидивного) эффекта арипипразола невысокими дозами клозапина отдельно было проведено изучение противорецидивной активности монотерапии клозапином в дозе от 50 до 100 мг/сут. Для этого была изучена выборка из 31 больного приступообразными формами шизофрении, которые вопреки рекомендациям врача принимали клозапин только однократно вечером для достижения снотворного эффекта (в дозе от 50 до 100 мг). В течение 12 мес наблюдения повторные приступы заболевания у этих больных развивались значительно чаще, чем у пациентов, принимавших комбинацию арипипразола и клозапина, – 29 (93,5%) случаев против 6 (8,8%) случаев (p=0,0000). Одновременно не было выявлено различий между группами больных с повторными рецидивами, которые принимали комбинацию арипипразола и клозапина или только арипипразол, – 6 (18,8%) случаев против 1 (14,3%) случая (p=1,0). Эти наблюдения доказывают низкую вероятность усиления антипсихотического (противорецидивного) эффекта арипипразола в случае его сочетания с невысокими дозами клозапина. Таким образом, полученные в настоящем исследовании данные о частоте повторных приступов болезни при лечении арипипразолом в сочетании с невысокими дозами клозапина можно экстраполировать на популяцию больных, принимающих монотерапию арипипразолом.
Таких наблюдений было 32 (82,1% от общего числа больных). Указанная доза клозапина сравнительно невелика и обычно рассматривается как субантипсихотическая (субпротиворецидивная). Для окончательного исключения возможности усиления антипсихотического (противорецидивного) эффекта арипипразола невысокими дозами клозапина отдельно было проведено изучение противорецидивной активности монотерапии клозапином в дозе от 50 до 100 мг/сут. Для этого была изучена выборка из 31 больного приступообразными формами шизофрении, которые вопреки рекомендациям врача принимали клозапин только однократно вечером для достижения снотворного эффекта (в дозе от 50 до 100 мг). В течение 12 мес наблюдения повторные приступы заболевания у этих больных развивались значительно чаще, чем у пациентов, принимавших комбинацию арипипразола и клозапина, – 29 (93,5%) случаев против 6 (8,8%) случаев (p=0,0000). Одновременно не было выявлено различий между группами больных с повторными рецидивами, которые принимали комбинацию арипипразола и клозапина или только арипипразол, – 6 (18,8%) случаев против 1 (14,3%) случая (p=1,0). Эти наблюдения доказывают низкую вероятность усиления антипсихотического (противорецидивного) эффекта арипипразола в случае его сочетания с невысокими дозами клозапина. Таким образом, полученные в настоящем исследовании данные о частоте повторных приступов болезни при лечении арипипразолом в сочетании с невысокими дозами клозапина можно экстраполировать на популяцию больных, принимающих монотерапию арипипразолом.
Для выявления индивидуальных предикторов эффективности терапии арипипразолом было проведено клинико-статистическое сравнение групп больных с развитием очередного приступа и с устойчивой лекарственной ремиссией10. Группы сравнивались по возрасту, клинико-психопатологическим особенностям заболевания, особенностям текущего психического состояния и терапии, по отношению больных к лекарственному лечению (см. таблицу). Полученные данные свидетельствуют, что рецидивы заболевания чаще развивались у больных, не настроенных лечиться (p=0,0000), с низким уровнем критики (более 2 баллов; p=0,0004), при длительности болезни менее 2 лет (p=0,03) и перенесших 1 манифестный психоз (p=0,04). У больных с повторными обострениями в структуре предшествующей ремиссии преобладал стенический радикал (гиперстенические и психопатоподобные ремиссии), в то время как при устойчивых лекарственных ремиссиях – простая дефицитарность (апатические и астенические ремиссии) (p=0,0000). Группы не различались по возрасту больных, длительности текущей лекарственной ремиссии, тяжести продуктивной и негативной симптоматики (при суммарной оценке каждого круга симптомов отдельно) и дозе арипипразола (p>0,05). Эти данные означают, что выраженный стенический радикал в структуре ремиссии, низкий уровень критики и отсутствие настроенности на лечение являются надежными предикторами низкой эффективности терапии, т.е. развития повторного приступа болезни. Данные, полученные от больных во время клинической беседы (в том числе post factum), опросы их родственников и учет числа неизрасходованных таблеток свидетельствовали, что большинство таких больных принимали терапию несистематически или полностью отказывались от нее в течение 1-го месяца исследования. Этим объясняется факт развития рецидивов болезни через 4–6 мес наблюдения (см. выше), поскольку для ухудшения состояния необходим период перестройки нейротрансмиттерных систем на «болезненный уровень». Интересно, что до начала исследования, несмотря на отсутствие желания лечиться, все больные придерживались рекомендованной схемы приема клозапина (обязательный критерий включения в исследование). Вероятно, при лечении клозапином противодействие больных терапии нивелировалось ее седативным эффектом. Отсутствие седативного действия при приеме арипипразола в совокупности с его активирующим эффектом приводило к усилению «негативизма» таких больных по отношению к лекарственной терапии.

Одновременно с оценкой частоты рецидивов заболевания эффективность терапии оценивалась при помощи изучения динамики психопатологической симптоматики16. Динамическая оценка выраженности продуктивных расстройств свидетельствовала о стабильности состояния больных17. Клиническое наблюдение показало, что в течение всего периода исследования устойчивые лекарственные ремиссии характеризовались высоким качеством с сохранением критики, отсутствием нарушений стройности мышления, явлений негативизма, выраженной тревоги и депрессивных реакций. При статистическом сравнении значимых различий между группами выявлено не было (средний балл PANSS positive + PANSS global составлял 33,8±1,9; 33,6±1,9; 33,3±1,7; 33,4±1,7; 33,4±1,7; 33,0±1,7 и 32,6±1,7 – исходно18, через 1, 2, 3, 6, 9 и 12 мес терапии соответственно).

Более интересными представляются данные оценки динамики негативной симптоматики. Клиническое наблюдение свидетельствовало, что в течение 1-го месяца терапии арипипразолом состояние больных значительно улучшалось. Отмечалось эмоциональное и двигательное оживление. Расширялся круг контактов и интересов. Больные становились более расположенными к общению, стремились к нему, охотнее выполняли привычные обязанности, появлялись новые увлечения. Они описывали субъективное ощущение «четкости», «легкости» мыслей, «прояснение», «просветление в голове», «бодрости». В некоторых случаях оживление было столь отчетливым и ярким, что становилось причиной незапланированного обращения пациентов к врачу по настоянию родных. Однако ни у одного больного оно не могло быть расценено как начальный этап бредового психоза или гипомания. Через 2 мес лечения первоначальная эмоциональная и двигательная активизация несколько стихала. Однако больные оставались более оживленными, чем до начала исследования. В последующие 2 мес их состояние продолжало постепенно улучшаться, а затем стабилизировалось. Статистическое сравнение выраженности негативной симптоматики в динамике подтвердило данные клинического наблюдения (рис. 2). Выраженность негативных расстройств составила 17,1±1,5/2,019; 13,2±1,1/1,5; 14,3±1,220; 13,8±1,1; 13,5±1,2; 13,4±1,2 и 13,4±1,2 балла – исходно, через 1, 2, 3, 6, 9 и 12 мес соответственно. Клинико-статистические данные о значительном улучшении состояния больных в течение 1-го месяца наблюдения, вероятно, объясняются не только антинегативным действием арипипразола, но и устранением седативного эффекта нейролептической терапии (после отмены клозапина)21. Собственно антинегативный эффект арипипразола, по всей видимости, проявлялся начиная со 2-го месяца лечения, когда седативное действие было полностью устранено.

Описанная динамика негативных расстройств при приеме арипипразола проявлялась в улучшении социальной адаптации больных (рис. 3). Начиная с 3-го месяца терапии средние показатели по шкале PSP значительно превышали исходный уровень (50,5±1,7; 51,1±1,8; 52,1±1,9; 57,3±2,1; 62,4±2,5; 67,9±2,8 и 68,8±2,5 балла – исходно, через 1, 2, 3, 6, 9 и 12 мес соответственно). Наибольшее улучшение качества социальной адаптации наблюдалось через 3, 6 и 9 мес лечения. Обращает внимание «отсроченность» этого эффекта по отношению к ослаблению негативных расстройств (их выраженность ослабевала раньше – в течение первых 3 мес терапии).
В заключение необходимо остановиться на переносимости терапии арипипразолом, но лишь кратко, поскольку этот вопрос требует более тщательного анализа и достоин описания в рамках отдельной журнальной статьи. Среди побочных эффектов арипипразола в настоящем исследовании наблюдались лишь неврологические нарушения.
У 8 (20,5%) больных было отмечено развитие акатизии, тяжесть которой была невелика. Она легко корректировалась назначением тригексифенидила или биперидена в дозе от 4 до 6 мг/сут. У 1 (2,6%) больного спустя 12 мес терапии развились явления поздней дискинезии. Нарушения сна, которые отмечались в первые недели монотерапии арипипразолом (см. выше), нельзя расценивать как побочный эффект лечения. Они могли быть связаны с отменой клозапина. Других нежелательных явлений при лечении арипипразолом, которые могли бы быть выявлены во время клинических бесед или по наблюдению родственников больных, отмечено не было.
Эффективность атипичных нейролептиков при лечении шизофрении не вызывает сомнений. Однако несмотря на многочисленные исследования, до сих пор остается много разногласий в отношении зависимости терапевтического эффекта атипичных нейролептиков от клинико-психопатологических особенностей заболевания и текущего психического состояния. Одновременно противоречивы данные сравнения эффективности разных атипичных антипсихотических средств [16]. Эти вопросы в полной мере адресуются к наиболее «молодому» атипичному нейролептику – арипипразолу22. Результаты систематических Кохрановских обзоров свидетельствуют о необходимости продолжения изучения его эффективности при лечении шизофрении из-за недостаточного количества исследований [11, 12]. Отечественных исследований пока явно недостаточно, чтобы оценить эффективность терапии с позиции традиционного для российской психиатрии подхода (выделение индивидуальных предикторов эффективности и формулирование дифференцированных показаний к назначению). Немногочисленные клинические исследования [20–23], клинические наблюдения [24] и обзоры литературы [25–27] отечественных авторов пока не могут в полной мере ответить на поставленные вопросы.
Представленное исследование является попыткой выделения некоторых клинико-психопатологических предикторов эффективности арипипразола при лечении шизофрении (в сравнении с клозапином). Его результаты свидетельствуют о высокой эффективности арипипразола у больных шизофренией, протекающей в форме приступов, в период лекарственной ремиссии при условии ее изначально высокого качества и небольшой длительности болезни. Показано, что арипипразол обладает достаточным антипсихотическим (противорецидивным) эффектом для предотвращения развития повторных приступов заболевания (при условии правильного соблюдения рекомендованной схемы лечения23) и сопоставим по этому показателю с клозапином. Применение арипипразола в период лекарственной ремиссии после отмены клозапина приводит к дальнейшему улучшению состояния больных в виде их двигательной и эмоциональной активизации (снижение тяжести негативных расстройств) и последующего улучшения качества социальной адаптации. Это наблюдение представляет большой интерес, поскольку до сих пор предполагалось, что клозапин обладает максимально возможными антипсихотическим и антинегативным эффектами. Интересно, что за рубежом также предпринимаются попытки исследования эффективности арипипразола после периода лечения клозапином, но они ограничиваются резистентными случаями болезни [28]. Неоднократно отмечалось, что арипипразол обладает благоприятным (по сравнению с типичными и атипичными нейролептиками II поколения) профилем побочных эффектов, а в некоторых случаях может использоваться для их коррекции (при нейролептическом ожирении или нейролептической гиперпролактинемии) [29]. Хотя в задачи настоящего исследования не входила оценка переносимости лечения, предварительные результаты свидетельствуют, что спектр побочных эффектов у обследованных больных ограничивался лишь случаями легкой акатизии. Важно отметить, что в среднетерапевтических дозах терапия арипипразолом не приводила к развитию седативного эффекта. Это благоприятно сказывалось на состоянии части больных в период ремиссии, однако в некоторых случаях приводило к нежелательным последствиям (диссомнические расстройства, отказ от лечения в связи с усилением негативизма к лечению у больных с отсутствием критики).
Несмотря на успешное разрешение задач, поставленных в настоящем исследовании, с целью уточнения и расширения объема полученных результатов необходимо его продолжение (увеличение числа обследованных больных, более длительный период катамнеза, исследование эффективности терапии на начальных этапах ремиссии, детальная оценка переносимости терапии и т.д.). Рациональным представляется проведение подобных исследований (особенно в сравнении с другими нейролептиками) в период купирующей терапии приступообразных форм шизофрении, на разных этапах течения непрерывной параноидной и вялотекущей шизофрении.
Примечания
1Отличие этой группы от других нейролептиков заключается в том, что при избытке дофамина они блокируют дофаминовые рецепторы (ослабляя проявления психоза), а при его дефиците – стимулируют их (ослабляя негативную симптоматику). Фактически эти средства одновременно сочетают свойства низких и высоких доз дезингибирующих нейролептиков (пимозид и др.), которые в низких дозах обладают активирующим, а в высоких – антипсихотическим действием. При неизмененном уровне дофамина (в нигростриальной системе и гипофизе) частичные агонисты дофаминовых рецепторов не проявляют своей активности, поэтому в отличие от других нейролептиков риск неврологических и эндокринных расстройств при их приеме невысок. Способность частичных агонистов дофаминовых рецепторов ослаблять проявления негативной симптоматики и редкость возникновения при их приеме экстрапирамидных расстройств позволяют рассматривать их в группе атипичных антипсихотических средств. Уникальный механизм действия частичных агонистов дофаминовых рецепторов дает основание отнести их к «нейролептикам III поколения» в противовес типичным (FGAs – first-generation antipsychotics) и атипичным (SGAs – second-generation antipsychotics) антипсихотическим средствам [5].
2Термин «частичные агонисты дофаминовых рецепторов» несколько условен. Например, арипипразол одновременно с влиянием на дофаминергическую систему является сильным антагонистом 5НТ2A- и агонистом 5НТ1A-серотониновых рецепторов.
3Частичный агонист дофаминовых рецепторов, синтезированный в лаборатории фармацевтической фирмы «Gedeon Richter», известной производством одного из генериков арипипразола Амдоала.
4Справедливости ради необходимо отметить, что исследования сравнения эффективности с клозапином отсутствуют не только для арипипразола, но и для многих других атипичных нейролептиков.
5Для нозологической квалификации их состояния использовалась отечественная классификация синдромальных форм и типов течения шизофрении [13, 14]. Для «стандартизации» диагноза применялись критерии диагностики Международной классификации болезней
10-го пересмотра (состояние больных соответствовало рубрикам F20.х1, F20.x2, F20.x3, F20.x9, F25.01) [15].
6Здесь и далее в тексте представлена величина 95% доверительного интервала.
7Варианты ремиссий выделялись на основании клинической оценки состояния больных. Типы ремиссий, которые наблюдались в настоящем исследовании, были неоднократно описаны в классических работах [18, 19].
8Правильность соблюдения рекомендованной схемы лечения оценивалась на основании сопоставления данных, полученных от больных во время клинической беседы, опроса их родственников и учета числа неизрасходованных таблеток.
9На основании вычисления величины «p» при сравнении 2 пропорций. Использован двусторонний критерий статистической значимости.
10Очевидна предварительность результатов подобного клинико-статистического сравнения из-за немногочисленности больных в группе «повторный приступ». Однако полученные данные могут быть ориентиром для проведения дальнейших исследований в этом направлении.
11Сравнение проводилось только по качественным бинарным признакам. Сравнение по количественным признакам не проводилось из-за несопоставимости численности групп больных с очередным приступом и лекарственной ремиссией.
12Признак измерялся на момент начала исследования.
13Расчет производился методом Фишера.
14Для непрерывных величин в качестве критерия разделения больных на пропорции было выбрано округленное среднее значение того или иного признака (представлены в разделе «Материалы и методы»).
15Здесь и далее в этом столбце полужирным шрифтом выделены статистически значимые различия.
16Оценка проводилась в группе 32 больных, поскольку 7 человек были исключены из исследования из-за развития рецидивов болезни.
17В данном случае речь прежде всего идет об отсутствии усиления тяжести продуктивных расстройств невротического уровня, поскольку больные, у которых резко усиливались психотические симптомы (т.е. развивались рецидивы болезни), из исследования исключались.
18Представленный здесь и далее показатель исходного среднего балла отличается от показателя, представленного в разделе «Материалы и методы», поскольку он рассчитывался повторно после исключения из исследования части больных (7 человек).
19Через дробь представлены величины 95% и 99% доверительных интервалов.
20Здесь и далее представлена величина 95% доверительного интервала.
21Однако необходимо учитывать, что больные включались в исследование в среднем спустя 9 мес после отзвучания острого психотического состояния (см. раздел «Материалы и методы»), т.е. в период, когда седативное действие клозапина значительно ослабевало и значительно не влияло на состояние больных [16].
22Необходимо отметить, что почти в таком же объеме они адресуются к атипичным нейролептикам, которые используются в клинической практике уже длительное время (рисперидон, оланзапин, кветиапин, амисульприд и др.).
23Поскольку настоящее исследование проводилось в условиях университетской психиатрической клиники с традиционно индивидуальным подходом к лечению (в том числе использование психотерапевтических методов, направленных на повышение качества соблюдения больными рекомендаций врача), возможно, что в более широкой клинической практике частота рецидивов при лечении арипипразолом будет выше.
Сведения об авторах
Данилов Дмитрий Сергеевич – д-р мед. наук, зав. отд-нием Клиники психиатрии им. С.С.Корсакова Университетской клинической больницы №3 ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России; вед. науч. сотр. НОКЦ «Психическое здоровье» ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России. E-mail: clinica2001@inbox.ru
Магомедова Диана Олеговна – клин. ординатор каф. психиатрии и наркологии ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России. E-mail: clinica2001@inbox.ru:
Список исп. литературыСкрыть список1. Данилов Д.С. 60 лет антипсихотическим средствам (к вопросу об их классификации). Неврология, нейропсихиатрия и психосоматика. 2012; 4: 24–33.
2. Kane J, Malhotra A. The future of pharmacotherapy for schizophrenia. World Psychiatry 2003; 2: 81–6.
3. Stahl SM. Новые достижения в терапии шизофрении. В кн.: Шизофрения. Изучение спектра психозов. Под ред. R.J.Ancill, S.Holliday, J.Higenbottam. М.: Медицина, 2001; с. 154–70.
4. Baldessarini RJ, Tarazi FI. Медикаментозное лечение психозов и маний. В кн.: Клиническая фармакология по Гудману и Гилману. М.: Практика, 2006; с. 382–411.
5. Roth BL, Sheffler DJ, Potkin SG. Atypical antipsychotic drug actions: unitary or multiple mechanisms for «atypicality»? Clinic Neurosci Res 2003; 3: 108–17.
6. Veselinoviс T, Paulzen M, Gründer G. Cariprazine, a new, orally active dopamine D2/3 receptor partial agonist for the treatment of schizophrenia, bipolar mania and depression. Expert Review Neurotherapeutics 2013; 13 (11): 1141–59.
7. Belgamwar RB, El-Sayeh HGG. Aripiprazole versus placebo for schizophrenia. In: Cochrane Database of Systematic Reviews. 2011; 8.
8. Kasper S, Lerman MN, McQuade RD et al. Efficacy and safety of aripiprazole vs. haloperidol for long-term maintenance treatment following acute relapse of schizophrenia. Int J Neuropsychopharmacol 2003; 6 (4): 325–37.
9. Kern RS, Green MF, Cornblatt BA et al. The neurocognitive effects of aripiprazole: an open-label comparison with olanzapine. Psychopharmacology (Berl) 2006; 187 (3): 312–20.
10. Kane JM, Crandall DT, Marcus RN et al. Symptomatic remission in schizophrenia patients treated with aripiprazole or haloperidol for up to 52 weeks. Schizophr Res 2007; 95 (1–3): 143–50.
11. Bhattacharjee J, El-Sayeh HGG. Aripiprazole versus typical antipsychotic drugs for schizophrenia. In: Cochrane Database of Systematic Reviews. 2008; 3.
12. Khanna P, Komossa K, Rummel-Kluge C et al. Aripiprazole versus other atypical antipsychotics for schizophrenia. In: Cochrane Database of Systematic Reviews. 2013; 2.
13. Наджаров Р.А., Тиганов А.С., Смулевич А.Б. и др. Шизофрения.
В кн.: Руководство по психиатрии. Под ред. Г.В.Морозова. М.: Медицина, 1988; 1: с. 420–85.
14. Тиганов А.С. Классификация шизофрении. В кн.: Руководство по психиатрии. Под ред. А.С.Тиганова. М.: Медицина, 1999; 1: с. 413–8.
15. Чуркин А.А., Мартюшов А.Н. Практическое руководство по использованию МКБ-10 в психиатрии и наркологии. М.: ГНЦ СиСП им. В.П.Сербского, 2004.
16. Данилов Д.С. Эффективность терапии шизофрении атипичными нейролептиками (значение различных клинико-социальных факторов). Дис. … д-ра мед. наук. М., 2011.
17. Ханнанова А.Н. Клинико-динамические характеристики негативных расстройств и нейрокогнитивных нарушений у больных параноидной шизофренией. Автореф. дис. … канд. мед. наук. М., 2013.
18. Морозов В.М., Тарасов Ю.К. Некоторые типы спонтанных ремиссий при шизофрении. Журн. невропатологии и психиатрии им. С.С.Корсакова. 1951; 51 (4): 44–7.
19. Зеневич Г.В. Ремиссии при шизофрении. М.: Медицина, 1964.
20. Иванов М.В., Шипилин М.Ю., Банщиков Ф.Р. Опыт применения арипипразола в лечении больных шизофренией. Соц. и клин. психиатрия. 2009; 19 (2): 46–50.
21. Гурович И.Я., Любов Е.Б., Винидиктова Г.И. и др. Клинико-социальная эффективность при поддерживающем лечении больных шизофренией арипипразолом: многосторонняя оценка. Соц. и клин. психиатрия. 2009; 19 (3): 37–46.
22. Стяжкин В.Д., Тарасевич Л.А. Влияние арипипразола на качество ремиссии у больных шизофренией, находящихся на принудительном лечении. Психиатр. и психофармакотер. 2010; 12 (2): 14–9.
23. Тарасевич Л.А., Колесникова А.В. Влияние терапии арипипразолом на негативную симптоматику больных шизофренией, совершивших общественно опасные действия. Соц. и клин. психиатрия. 2010; 20 (2): 45–7.
24. Либин Л.Я., Кильдеев В.В., Иванов М.В. Эффективность, переносимость и безопасность противорецидивной терапии арипипразолом в амбулаторной психиатрической практике. Описание клинических случаев. Обозрение психиатрии и мед. психологии им. В.М.Бехтерева. 2010; 2: 38–42.
25. Морозов П.В. Арипипразол – новый атипичный антипсихотик. Психиатр. и психофармакотер. 2006; 8 (4): 14–7.
26. Любов Е.Б. Арипипразол: рациональный выбор при лечении шизофрении. Соц. и клин. психиатрия. 2008; 18 (4): 94–102.
27. Цукарзи Э.Э. Эффективность арипипразола в длительной терапии шизофрении. Журн. неврологии и психиатрии им. С.С.Корсакова. 2013; 113 (3): 94–7.
28. Assalman I, Makhoul S, Hussain K. Aripiprazole for people with schizophrenia whose illness has been partially responsive to clozapine. In: Cochrane Database of Systematic Reviews. 2012; 5.
29. Горобец Л.Н. Вопросы переносимости и безопасности терапии арипипразолом (эндокринологический аспект проблемы). Соврем. терапия психических расстройств. 2013; 1: 24–9.


