Диагностическая и интервенционная радиология 2015
№01 2015
Отдаленные результаты стентирования пациентов с многососудистым поражением коронарного русла и сопутствующим сахарным диабетом ii типа стентами с лекарственным покрытием «зотаролимус» №01 2015
Материалы и методы: были отобраны 37 пациентов с ИБС и сопутствующим сахарным диабетом II типа, которым имплантировали стенты без лекарственного покрытия («Intergrity» «Medtronic») либо стенты с лекарственным покрытием «Зотаролимус» («Resolute Integrity» «Medtronic»). Все пациенты были разделены на 2 группы: первая группа – 11 пациентов, которым имплантированы стенты без лекарственного покрытия, вторая группа – 26 пациентов, которым имплантированы стенты с лекарственным покрытием «Зотаролимус». Период наблюдения составлял 26±4 мес. Критериями эффективности стентирования служили ангиографическая оценка анатомии коронарных артерий при контрольной ангиографии после стентирования; возврат стенокардии или увеличение функционального класса, выживаемость в раннем периоде, до выписки пациентов, но не более 30 суток ( в ближайшем послеоперационном периоде до 6 мес., в средне-отдаленном периоде наблюдения – 12 мес. и в отдаленном – 24 мес).
Результаты: всем пациентам была успешно проведена эндоваскулярная реваскуляризация миокарда. Оптимальный ангиографический результат достигнут у всех пациентов. Регрессия ишемических изменений по данным ЭКГ и увеличение сократительной функции миокарда по данным ЭХОКГ отмечены также у всех пациентов. В отдаленном периоде при контрольной ангиографии у 5(45,5%) больных в группе «непокрытых» стентов отмечалось появление гемодинамически значимого рестеноза, потребовавшего выполнения повторной ангиопластики со стентированием.
Заключение: применение стентов с антипролиферативным лекарственным покрытием «Зотаролимус» возможно при лечении пациентов с ИБС и сопутствующим диагнозом сахарный диабет II типа. Применение стентов без покрытия при коронарном стентировании у пациентов с сопутствующим диагнозом сахарный диабет II типа нецелесообразно в связи с развивающимся (45% пациентов) рестенозом ранее имплантированного стента.
Цель: анализ отдаленных результатов стентирования коронарных артерий стентами с лекарственным покрытием «Зотаролимус» и стентами без лекарственного покрытия у пациентов с сопутствующим диагнозом сахарный диабет II типа.
Материалы и методы: были отобраны 37 пациентов с ИБС и сопутствующим сахарным диабетом II типа, которым имплантировали стенты без лекарственного покрытия («Intergrity» «Medtronic») либо стенты с лекарственным покрытием «Зотаролимус» («Resolute Integrity» «Medtronic»). Все пациенты были разделены на 2 группы: первая группа – 11 пациентов, которым имплантированы стенты без лекарственного покрытия, вторая группа – 26 пациентов, которым имплантированы стенты с лекарственным покрытием «Зотаролимус». Период наблюдения составлял 26±4 мес. Критериями эффективности стентирования служили ангиографическая оценка анатомии коронарных артерий при контрольной ангиографии после стентирования; возврат стенокардии или увеличение функционального класса, выживаемость в раннем периоде, до выписки пациентов, но не более 30 суток ( в ближайшем послеоперационном периоде до 6 мес., в средне-отдаленном периоде наблюдения – 12 мес. и в отдаленном – 24 мес).
Результаты: всем пациентам была успешно проведена эндоваскулярная реваскуляризация миокарда. Оптимальный ангиографический результат достигнут у всех пациентов. Регрессия ишемических изменений по данным ЭКГ и увеличение сократительной функции миокарда по данным ЭХОКГ отмечены также у всех пациентов. В отдаленном периоде при контрольной ангиографии у 5(45,5%) больных в группе «непокрытых» стентов отмечалось появление гемодинамически
 значимого рестеноза, потребовавшего выполнения повторной ангиопластики со стентированием.
значимого рестеноза, потребовавшего выполнения повторной ангиопластики со стентированием. Заключение: применение стентов с антипролиферативным лекарственным покрытием «Зотаролимус» возможно при лечении пациентов с ИБС и сопутствующим диагнозом сахарный диабет II типа. Применение стентов без покрытия при коронарном стентировании у пациентов с сопутствующим диагнозом сахарный диабет II типа нецелесообразно в связи с развивающимся (45% пациентов) рестенозом ранее имплантированного стента.
Long-term results of stenting in patients with multivessel coronary disease and concomitant diabetes mellitus type ii with drug-eluting stents «zotarolimus»
*Kichin V.V. – MD 1
Sozikin A.V. – MD, PhD, professor2
Yurishchev A.Y. – MD 1
Badikov E.F. – resident 1
Loboda A.A. – resident 1
1Main Clinical Hospital of Federal Security Service of Russian Federation
48, Petrovskoe highway, Golitsino, Odintsovskiy district, Russian Federation, 143040
2Road Clinical Hospital named after N.A.Semashko of «Russian Railways»
23, Stavropolskaya str, Moscow, Russian Federation, 109386
ABSTRACT:
Aim: was to analyze long-term results of coronary artery stenting with drug-eluting stents «Zotarolimus» and bare metal stents in patients with a concomitant diabetes mellitus type II.
Materials and methods: 37 patients with ischemic heart disease and concomitant diabetes mellitus type II were selected for analysis; they underwent implantation of stents without drug coverage («Intergrity» «Medtronic») or stents with drug-eluting «Zotarolimus» («Resolute Integrity» «Medtronic»). All patients were divided into 2 groups: first group consisted of 11 patients, who underwent implantation of bare metal stents, second group – 26 patients who underwent implantation of drug-eluting stents, «Zotarolimus». Follow-up period was 26±4 months. Сriteria of stenting efficiency were: angiographic assessment of coronary arteries anatomy in control angiography after stent implantation, reccurence of angina or functional class increase, the survival rate in the nearest post-operative period, before discharge, but not more than 30 days, and in the early post-operative period up to 6 months. In the medium-distant post-operative period – 12 months, and in the late post-operative period - 24 months.
Results: all patients underwent successfully performed endovascular revascularization. The optimal angiographic result was achieved in all patients. Regression of ischemic changes on ECG data and increase myocardial contractility by echocardiography 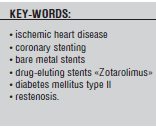 data also were marked in all patients. In long-term follow-up period, in 5 (45%) patients with bare metal stents we noted the appearence of hemodynamically significant restenosis, that needed performance of secondary angioplasty with stenting.
data also were marked in all patients. In long-term follow-up period, in 5 (45%) patients with bare metal stents we noted the appearence of hemodynamically significant restenosis, that needed performance of secondary angioplasty with stenting.
Conclusion: the use of antiproliferative drug-eluting stents «Zotarolimus» is possible in treatment of patients with coronary artery disease and comorbid diagnosis of diabetes mellitus type II. Bare metal stents in coronary stenting in patients with concomitant diagnosis of diabetes mellitus type II is impractical due to developing in-stent restenosis (45% of patients).
Введение
Ишемическая болезнь сердца (ИБС) стоит на первом месте по причинам смертности населения России средней и старшей возрастной группы. Немаловажное значение имеет различная сопутствующая патология, усугубляющая течение ИБС, и также ухудшающая планируемые результаты эндоваскулярного лечения. Одной из наиболее актуальных – сахарный диабет (СД). В настоящее время на нашей планете только по обращаемости насчитывается 366 млн больных СД (7% населения всего мира), причем около 50% всех больных диабетом приходится на наиболее активный трудоспособный возраст 40–59 лет. Численность больных СД в Российской Федерации по данным на 2005 год составляла 6–8 млн человек или 3–5% всего населения, 90% которых страдали диабетом II типа. Смертность от ИБС среди больных СД составляет 40–50%. Данный показатель среди лиц, не страдающих СД, в 2–4 раза ниже [1].За последние 5 лет возросла частота выявления СД
II типа у пациентов с ангиографически подтвержденным атеросклерозом коронарных артерий. Мнения специалистов относительно тактики и результатов эндоваскулярного лечения атеросклеротического поражения коронарных артерий у этой категории больных разделились и являются предметом постоянных дискуссий.
Актуальность данной проблемы подтверждается еще и тем, что больные СД представляют крайне неблагоприятную группу для выполнения хирургической реваскуляризации миокарда. И, хотя аортокоронарное шунтирование (АКШ) позволяет выполнить адекватную реваскуляризацию миокарда, по данным ряда авторов, в первые 1–2 года после операции наблюдается окклюзия 1–20% венозных шунтов, а в каждый последующий год дополнительно закрываются от 1% до 4% шунтов [2]. Повторная операция сопряжена с риском значительно большим, чем первичное вмешательство.
В эпоху применения голометаллических стентов неблагоприятные исходы стентирования коронарных артерий у пациентов с ИБС без сопутствующего сахарного диабета II типа и с сопутствующим сахарным диабетом II типа объяснялись избыточной пролиферацией неоинтимы.С появлением стентов с лекарственным покрытием ситуация изменилась. Через 6 и 12 месяцев после стентирования результаты оказались значительно лучше по сравнению с имплантацией голометаллических стентов [3–9]. Однако, при оценке в позднем отдаленном периоде после отмены двойной антиагрегантной терапии, достаточно часто выявлялись поздние тромбозы стентов с лекарственным покрытием. Как правило, эти случаи были зафиксированы у пациентов, страдающих ИБС с сопутствующим СД II типа. Боль-шинство специалистов, изучавших исходы лечения после стентирования коронарных артерий, пришли к выводу, что больные СД II типа, подвергшиеся эндоваскулярному лечению с помощью стентов, покрытых лекарственным веществом, имеют по сравнению с пациентами без СД более высокую частоту развития осложнений и летальность в отдаленном послеоперационном периоде [3–6]. Применение стентов с лекарственным антипролиферативным покрытием снижает вероятность развития серьезных сердечнососудистых осложнений и возобновления стенокардии в последующие 12 месяцев после вмешательства [7–10]. Однако риск возникновения неблагоприятных событий, сохраняется по истечении 2,5 лет после вмешательства.
С появлением стентов с разными видами антипролиферативного покрытия, многие специалисты в своих наблюдениях указывали на различия в эффективности стентирования коронарных артерий у пациентов с сахарным диабетом в зависимости от вида антипролиферативного покрытия у пациентов с сахарным диабетом [11].
В своих наблюдениях мы выявили аналогичную тенденцию.
Цель исследования: сопоставить отдаленные результаты применения стентов с лекарственным покрытием «Зотаролимус» (Medtronic «Resolute Integrity») со стентами без лекарственного покрытия (Medtronic «Integrity») у пациентов с сопутствующим диагнозом сахарный диабет 2-го типа (СД II типа).
Материалы и методы
Для анализа отобраны 37 пациентов с ИБС и сопутствующим СД 2-го типа, которым имплантировали стенты с лекарственным покрытием «Зотаролимус» «Resolute Integrity» или имплантировались стенты без лекарственного покрытия («Integrity»). Больные были разделены на две группы. В первую группу вошли 11 пациентов, которым имплантированы стенты без лекарственного покрытия, во вторую – 26 пациентов, которым имплантированы стенты с лекарственным покрытием «Зотаролимус». Пациентам обеих групп стентирова-ние выполнялось в 2009–2012 годах. Период наблюдения составил 26±4 мес. Максимальный период наблюдения был более 4 лет. Однососудистое поражение выявлено у 19 пациентов, двухсосудистое – у 15, а трехсосудистое – у 3 больных. Доля пациентов первой (n=11) и второй (n=26) групп составила соответственно с однососудистым поражением – 70% и 42%, с двухсосудистым – 20% и 42%, с трехсосудистым – 10% и 7%. Доля пациентов с окклюзиями коронарных артерий составила 33% (n=37), всего окклюзированных артерий – 14, диффузных поражений – 19, тубулярных – 12, дискретных – 3. В исследование не вошли пациенты со стенозом ствола левой коронарной артерии (ЛКА) и пациенты с острым инфарктом миокарда (ИМ). Средний возраст пациентов составил 40±5 лет – от 24 до 75 лет. Почти все пациенты, вошедшие в исследование, соответствовали 2–3 ФК стенокардии или ее эквиваленту.
Диагноз ишемическая болезнь и показания для проведения коронароангиографии устанавливались на основании результатов физикального, лабораторного и инструментального обследования. Стенокардия напряжения 2 ФК определена у 7 пациентов, стенокардии 3 ФК – у 7 пациентов, по данным физикального обследования, безболевая форма ишемии миокарда – у 20 пациентов с эквивалентом стенокардии по результатам нагрузочных тестов. Три пациента в возрасте 24, 27 и 52 лет соответствовали стенокардии 4 ФК. Всем без исключения пациентам перед стентированием коронарных артерий проводилось ЭХОКГ, ЭКГ. В подавляющем большинстве случаев пациентам выполнялись нагрузочные тесты и радиоизотопное исследование перфузии миокарда при безболевой форме ИБС перед коронарной ангиографией (КАГ) или для уточнения показаний к КАГ.
Ангиография и стентирование проводились на ангиографическом комплексе Allura FD 20 фирмы «Philips» (Нидерланды). Ангиография выполнялась в стандартных проекциях: для левой коронарной артерии 5 проекций, для правой – 3 проекции. При выявлении пограничных стенозов для определения операционной тактики применяли оценку фракционного резерва кровотока. Перед стентированием всем пациентам назначали клопидогрел по 75 мг/сут, при приеме данного препарата более 14 суток и по 150 мг/сут – при приеме менее 14 суток, а также аспирин по 100 мг/сут. Ангиографию и стентирование выполняли под местной инфильтрационной анестезией 0,5% р-ра новокаина гидрохлорида или 0,5% р-ра лидокаина гидрохлорида. Всем пациентам накануне вечером для премедикации назначался реланиум по 2мг/сут и перед операцией тот же препарат и тавегил. Перед стентированием вводили в/а 10 тыс. ед. р-ра гепарина. После окончания стентирования общую дозу гепарина доводили до 15 тыс. ед. После стентирования пациенты пере-водились в отделение реанимации и интенсивной терапии для мониторинга их состояния в течение 18–24 часов в раннем послеоперационном периоде. Режим двойной дезагрегантной терапии – клопидогрель по 75–150 мг/сут и аспирин по 100 мг/сут. соблюдался всеми пациентами в течение 12 мес. после вмешательства. Гиполипидемическая, сахароснижающая терапия, аспирин назначались пожизненно. С момента стентирования пациенты принимали препараты клопидогреля по схеме: в дозировке 150 мг/сут – в течение 2 мес. после стентирования и далее по 75 мг/сут – еще 12 мес. Через 6, 12 и через 24 мес. пациентам проводились неинвазивные исследования по месту жительства или в госпитале. При выявлении отрицательной динамики основного заболевания пациенты направлялись в госпиталь для выполнения контрольной КАГ. Всем пациентам через 2–3 суток после вмешательства проводилось ЭХОКГ для определения динамики изменения сократительной функции миокарда с целью подтверждения эффективности стентирования.
Всем больным (n=37) имплантировано 66 стентов. Стенты с лекарственным покрытием «Зотаролимус» были имплантированы в наиболее прогностически неблагоприятные стенозы – в зону протяженного стеноза неправильной формы, в проксимальные и средние сегменты эпикардиальных артерий, окклюзии артерий, а также в бифуркации, стенты без покрытия − в неосложненные участки поражения коронарных артерий. Пациентам первой группы всего имплантировано 24 стента, пациентам 2 группы 42 стента с лекарственным покрытием «Зотаролимус» – «Resolute Integrity». Средняя про-тяженность стентированного сегмента составила 27±4 мм. Средний диаметр артерий, стентированных указанными стентами, составил 2,6 мм. Диаметр стента подбирался на основании компьютерного измерения референсного диаметра сосуда в месте стеноза. При стентировании окклюзии и критического стеноза диаметр определялся после предварительной баллонной ангиопластики.
Динамическое наблюдение за состоянием пациентов проводили путем опроса о состоянии здоровья при помощи телефонной связи, проведения обследований на амбулаторном этапе и контрольного ангиографического исследования, в среднем, через 24 мес.
Критериями эффективности стентирования у данной категории пациентов служили ангиографическая оценка анатомии коронарных артерий при контрольной ангиографии непосредственно после стентирования, возврат стенокардии или увеличение функционального класса, выживаемость в раннем от момента стентирования периоде, до выписки пациентов, но не более 30 суток; в ближайшем послеоперационном периоде до 6 мес., в средне-отдаленном периоде наблюдения – 12 и в отдаленном периоде – 24 мес.
Критерии оценки результатов лечения:
1. При повторном обследовании по данным неинвазивных методов обследования оценивались динамика изменения функционального класса стенокардии и сократительной способности миокарда в
раннем послеоперационном, отдаленном и позднем отдаленном периодах.
2. После стентирования оценивался ангиографический результат.
3. При выполнении контрольной коронароангиографии оценивалось наличие рестеноза или тромбоза стентов у пациентов обоих групп.
4. Оценивалась необходимость в выполнении повторной ангиопластики со стентированием.
Результаты и обсуждение
Всем пациентам была успешно проведена эндоваскулярная реваскуляризация миокарда. Оптимальный ангиографический результат достигнут у всех 37 пациентов. Неполная реваскуляризация только симптом-зависимых по данным сцинтиграфии миокарда и КАГ коронарных артерий была проведена у 3 пациентов 2-й группы. Регрессия ишемических изменений по данным ЭКГ и увеличение сократительной функции миокарда по данным ЭХОКГ отмечены у всех пациентов.
При амбулаторном обследовании пациентов через 6 и 12 мес. у 30 пациентов отмечено уменьшение функционального класса стенокардии на 1–2 класса, увеличение сократительной функции миокарда по данным ЭХОКГ. У 7-ми пациентов 1-й группы при оценке сократительной функции миокарда отмечена отрицательная динамика на ЭКГ в покое и при проведении нагрузочного теста. Во время контрольной коронароангиографии у 6 пациентов выявлен рестеноз ранее имплантированного стента более 50%, который потребовал проведения баллонной ангиопластики, еще у 1 пациента через 8 мес. было выявлено прогрессирование атеросклероза с развитием стеноза de-novo, которое потребовало имплантации стента. В период наблюдения более 24 мес. после стентирования регрессия ишемических изменений по данным ЭКГ и увеличение сократительной функции миокарда по данным ЭХОКГ отмечены у 9 пациентов 1-й группы и у 26 пациентов 2-й группы по сравнению с дооперационным периодом. По данным коронароангиографии через 25 мес. после операции у 1 пациента 1-й группы был выявлен рестеноз стентированного сегмента с признаками пристеночного тромбоза. Еще у 1 пациента 1-й группы, стентированного более 4 лет назад, выявлен поздний тромбоз стента в среднем сегменте ПМЖВ. При проведении контрольной коронароангиографии у всех пациентов 2-й группы рестенозы в стентированных сегментах не превышали 10–15%, что было приемлемо для продолжения консервативного лечения. Летальность, ОИМ за все время наблюдения составили 0%.
Сравнение результатов клинической эффективности применения стентов без лекарственного покрытия и с лекарственным покрытием «Зотаролимус» у больных ИБС с сахарным диабетом II типа при наблюдении пациентов в ближайшем и среднеотдаленном периодах выявили достоверно значимые различия.
Обращает на себя внимание, что у 54% пациентов 1 группы выявлен рестеноз, потребовавший дальнейшей эндоваскулярной коррекции коронарного русла. У 100% пациентов 2-й группы были отмечены регрессия ишемических изменений по данным ЭКГ и увеличение сократительной функции миокарда по данным ЭХОКГ.
На сегодняшний день на рынке коронарных стентов с лекарственным покрытием с каждым годом появляется все больше и больше вариантов данной продукции. В данной статье мы приводим наш опыт применения относительно нового стента с лекарственным покрытием «Зотаролимус» «Resolute Integrity», разработанного и выпущенного на рынок компанией «Medtronic». Материал стента – кобальт-хромовый сплав. Толщина стенок стента – 0,0032. Лекарственное покрытие стента состоит из полимера и лекарственного препарата «Зотаролимус». Толщина полимерного покрытия − 0,007 мм. Система доставки – «монорельсовый» баллонный катетер. Номинальное давление – 8 атм. Предельное давление – 18 атм. В литературе сегодня имеется достаточно скудное количество информации о применении данной продукции у пациентов с сахарным диабетом II типа.
Клиническое наблюдение
Пациент Д., 56 лет, поступил в кардиологическое отделение госпиталя 12 октября 2010 г. с диагнозом: ишемическая болезнь сердца. Стабильная стенокардия 2ФК. Гипертоническая болезнь третьей стадии, третьей степени, риск 4. ХСН 1. Сахарный диабет II типа, компенсированный. Хронический бескаменный холецистит, ремиссия. Хронический панкреатит, ремиссия. Ухудшение состояния с мая 2010 г., когда стали возникать давящие боли и чувство дискомфорта за грудиной при привычных физических нагрузках. Боли появлялись до нескольких раз в день, впервые появилось чувство нехватки воздуха, перебои в работе сердца, существенно ухудшилась переносимость физических нагрузок. Начал пользоваться нитратами, отмечал положительный эффект от их приёма. При обследовании, на ЭКГ отмечались неспецифические нарушения процессов реполяризации по типу субэпикардиальной ишемии высоких отделов боковой стенки левого желудочка, уровень кардиоспецифических ферментов не повышался. При выполнении велоэргометрии достигнута нагрузка 50 Вт. На высоте физической нагрузки жалобы на давящие боли в области сердца, в связи с чем проба прекращена. На ЭКГ депрессия сегмента ST в отведениях V3-V6 на 1,0 мм, горизонтального типа. Боли купировались на четвертой минуте после приема нитроспрея. Проба расценена как положительная.
Выполнена диагностическая коронароангиография. При исследовании выявлено: субокклюзия среднего сегмента передней 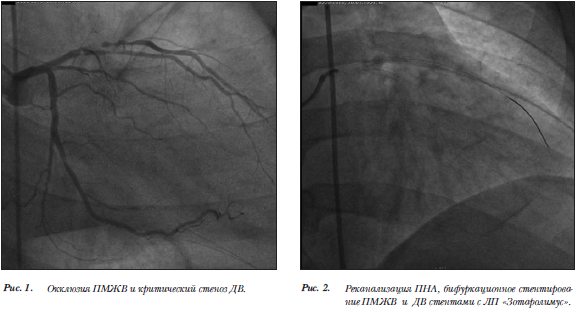 межжелудочковой ветви (ПМЖВ) левой коронарной артерии и стеноз до 80% первой диагональной ветви (ДВ) (рис.1).
межжелудочковой ветви (ПМЖВ) левой коронарной артерии и стеноз до 80% первой диагональной ветви (ДВ) (рис.1).
После предоперационной подготовки, назначения двойной дезагрегантной терапии 03 ноября 2010 г., выполнена эндоваскулярная коррекция коронарного русла. После установки проводникового катетера AL2 7F в устье левой коронарной артерии, в дистальные отделы ПМЖВ был проведен коронарный проводник 0,014˝мм и выполнена предилатация пораженного участка ПМЖВ. Далее в средний сегмент ПМЖВ давлением до 16 атм. имплантирован коронарный стент «Resolute Integrity», 2,5´22 мм, доставляющий лекарственное вещество «Зотаролимус» (рис. 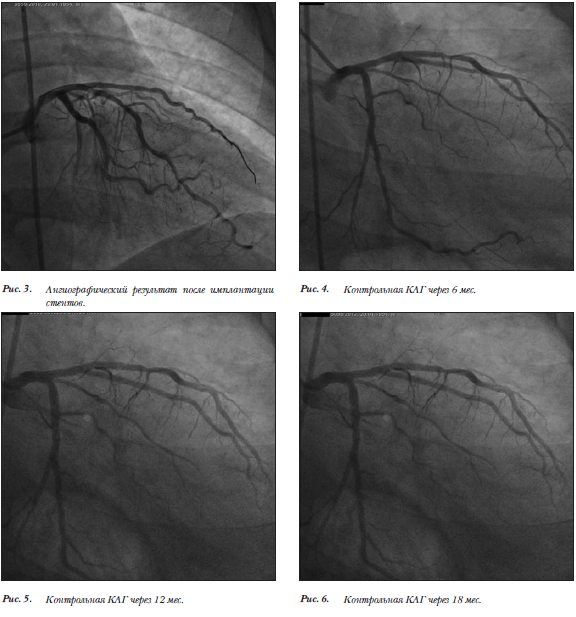 2). Получен удовлетворительный ангиографический результат, остаточный стеноз 0%. В дистальные отделы первой диагональной ветви проведен интракоронарный проводник для измерения фракционного резерва кровотока, полученные результаты измерения свидетельствовали о необходимости стентирования пораженного участка. После выполнения предилатации в проксимальный сегмент 1ДВ давлением до 16 атм. имплантирован коронарный стент «Resolute Integrity» 2,2´22 мм, доставляющий лекарственное вещество «Зотаролимус». Получен хороший ангиографический результат, остаточный стеноз 0% (рис. 3). Пациент выписан из стационара на восьмые сутки после эндоваскулярного вмешательства с рекомендациями приема клопидогреля по 150мг/сут в течение двух месяцев далее по 75мг/сут до года. Через шесть месяцев. пациент был госпитализирован для выполнения контрольной коронароангиографии. Рестеноз в местах ранее имплантированных стентов выявлен не был (рис. 4). Отмечен стеноз ПМЖВ до 35% дистальнее ранее имплантированного стента.
2). Получен удовлетворительный ангиографический результат, остаточный стеноз 0%. В дистальные отделы первой диагональной ветви проведен интракоронарный проводник для измерения фракционного резерва кровотока, полученные результаты измерения свидетельствовали о необходимости стентирования пораженного участка. После выполнения предилатации в проксимальный сегмент 1ДВ давлением до 16 атм. имплантирован коронарный стент «Resolute Integrity» 2,2´22 мм, доставляющий лекарственное вещество «Зотаролимус». Получен хороший ангиографический результат, остаточный стеноз 0% (рис. 3). Пациент выписан из стационара на восьмые сутки после эндоваскулярного вмешательства с рекомендациями приема клопидогреля по 150мг/сут в течение двух месяцев далее по 75мг/сут до года. Через шесть месяцев. пациент был госпитализирован для выполнения контрольной коронароангиографии. Рестеноз в местах ранее имплантированных стентов выявлен не был (рис. 4). Отмечен стеноз ПМЖВ до 35% дистальнее ранее имплантированного стента.
Следующее контрольное обследование через 12 месяцев после эндоваскулярного вмешательства выявило наличие поздней потери просвета стентов до 10% (рис. 5), что не потребовало коррекции. Однако был выявлен гемодинамически значимый стеноз задне-боковой ветви правой коронарной артерии до 85%.
В плановом порядке пациенту выполнена транслюминальная коронарная ангиопластика пораженного сосуда без имплантации коронарного стента ввиду малого диаметра артерии (<2 мм). При контрольной ангиографии левой коронарной артерии рестеноза ранее имплантированных стентов не выявлено (рис. 6).
Пациент выписан из стационара в удовлетворительном состоянии с рекомендациями контроля ЭКГ и выполнения коронароангиографии при нарастании симптомов стенокардии или появлении признаков ишемии миокарда.
На сроке наблюдения до 30 мес. после стентирования пациенту выполнены ЭКГ, ЭХОКГ и нагрузочный тест, по данным которых у пациента сохраняется положительный клинический эффект в стентированных клинико-зависимых артериях.
Заключение
Применение стентов с антипролиферативным лекар-ственным покрытием «Зотаролимус» возможно при лечении пациентов с ИБС и сопутствующим диагнозом сахарный диабет II типа.
Применение стентов без лекарственного покрытия у пациентов с СД II типа является нецелесообразным, в связи с высоким процентом рестеноза в отдаленном периоде.
Список исп. литературыСкрыть список1. Кereiakes D.J., Cutlip D.E., Applegate R.J., Wang J., Yaqub M., Sood P., Su X., Su G., Farhat N., Rizvi A., Simonton C.A., Sudhir K., Stone G.W. Outcomes in diabetic and nondiabetic patients treated with everolimus- or paclitaxel-eluting stents: results from the SPIRIT IV clinical trial (Clinical Evaluation of the XIENCE V Limus Eluting Coronary Stent System). J. Am. Coll. Cardiol. 2010 Dec 14; 56(25):2084–2089.
2. Петрова К.Н., Козлов С.Г., Лякишев А.А., Савченко А.П. Влияние сахарного диабета 2 типа на результаты эндоваскулярного лечения ИБС с помощью стентов с лекарственным покрытием (данные годичного наблюдения). Кардиология. 2006; 12: 22–6.
Petrova K.N., Kozlov S.G., Ljakishev A.A., Savchenko A.P. Vlijanie saharnogo diabeta 2 tipa na rezul'taty jendovaskuljarnogo lechenija IBS s pomoshh'ju stentov s lekarstvennym pokrytiem (dannye godichnogo nabljudenija) [Influence of diabetes mellitus type 2 on results of endovascular treatment of IHD with help of drug-eluting stents (data monitoring for one year)]. Kardiologija. 2006; 12: 22–6 [In Russ].
3. Abizaid A., Costa M.A., Blanchard D. et al. Sirolimus-Eluting Stents Inhibit Neointimal Hyperplasia in Diabetic Patients. Insights from the RAVEL Trial. Eur. Heart J. 2004; 25: 107–12.
4. Moussa I., Leon M.B., Baim D.S. et al. Impact of Sirolimus-Eluting Stents on Outcome in Diabetic Patients. Circulation .2004; 109: 2273–8.
5. Hermiller J.B., Raizner A., Cannon L. et al. TAXUS-IV Investigators. Outcomes With the Polymer-Based
Paclitaxel-Eluting TAXUS Stent in Patients With Diabetes Mellitus: the TAXUS-IV trial. JACC. 2005; 45: 1172–9.
6. Sabate M., Jim Оnez-Quevedo P., Angiolillo D.J. et al. Randomized Comparison of Limus-Eluting Stent Versus Standard Stent for Percutaneous Coronary Revascularization in Diabetic Patients. Circulation. 2005; 112: 2175–83.
7. Jensen J., Lagerqvist B., Aasa M., Särev T., Nilsson T., Tornvall P. Clinical and angiographic follow-up after coronary drug-eluting and bare metal stent implantation. Do drug-eluting stents hold the promise? J. Intern. Med. 2006 Aug; 260(2):118-24.
8. Jain A.K., Lotan C., Meredith I.T., Feres F., Zambahari R., Sinha N., Rothman M.T. E-Five Registry Investigators. Twelve-month outcomes in patients with diabetes implanted with a zotarolimus-eluting stent: results from the E-Five Registry. Heart. 2010 Jun; 96(11):848-53. doi: 10.1136/hrt.2009.184150.
9. Stettler C., Allemann S., Egger M. et al. Efficacy of drug eluting stents in patients with and without diabetes mellitus: indirect comparison of con-trolled trials. Heart. 2006; 92: 650–7.
10. Scheen A.J., Warzee F. Diabetes Is Still a Risk Factor for Restenosis After Drug-Eluting Stent in Coronary Arteries. Diabetes Care. 2004; 27: 1840–1.
11. Park K.W., Lee J.M., Kang S.H., Ahn H.S., Kang H.J., Koo B.K., Rhew J.Y., Hwang S.H., Lee S.Y., Kang T.S., Kwak C.H., Hong B.K., Yu C.W., Seong I.W., Ahn T., Lee H.C., Lim S.W., Kim H.S. Everolimus-eluting xience v/promus versus zotarolimus-eluting resolute stents in patients with diabetes mellitus. JACC. Cardiovasc. Interv. 2014 May;7(5):471–81. doi: 10.1016/j.jcin.2013.12.201.
