Диагностическая и интервенционная радиология 2015
№01 2015
Опыт применения бивалирудина у больных сострым коронарным синдромом с подъемом сегмента ST №01 2015
Материалы и методы: в исследование было включено 20 пациентов, которые поступили с диагнозом ОКС с подъемом сегмента ST.Среди пациентов было 3 женщины и 17 мужчин. Возраст пациентов составил от 31 до 79 лет, средний 56±10,8лет. Инфаркт миокарда нижней стенки левого желудовка (ЛЖ) был диагностирован у 9 (45%), пациентов, передней стенки ЛЖ – у 11(55%) больных. Всем пациентам в экстренном порядке была выполнена коронарография (КАГ) с последующим ЧКВ. Многососудистое поражение коронарного русла было выявлено у 35% пациентов, окклюзия одной из коронарных артерий – в 20% случаев, пора-жение на уровне бифуркации – 15% больных, ствола левой коронарной артерии – в 30% наблюдениях. Перед выполнением ЧКВ 14(70%) пациентов получили нагрузочную дозу клопидогреля (600 мг), 6(30%) пациентов– тикагрелора (180 мг) в комбинации с аспирином. Интраоперационно пациентам вводили препарат бивалирудин («Ангиокс») по схеме: 0,75 мг/кг массы тела внутривенно болюсно, в дальнейшем – внутривенная инфузия со скоростью 1,75 мг/кг/ч на протяжении всего периода проведения эндоваскулярного вмешательства.
Трем пациентам в связи с техническими особенностями во время проведения операции была выполнена интракоронарная тромболизитическая терапия. В 2 случаях потребовалась установка внутриаортального баллонного контрпульсатора.
Результаты: всего данным больным было установлено 27 стентов (в среднем 1,35 стента на человека). Непосредственный технический успех эндоваскулярного вмешательства составил 100%. В отделении реанимации в течение 4 часов после операции продолжалась инфузия бивалирудина в дозе 0,25 мг/кг/ч, после перевода в отделение кардиологии продолжалась терапия эноксапарином согласно принятым в нашей клинике стандартам в течение пяти суток. После эндоваскулярного вмешательства пациентов переводили на стандартные дозы клопидогреля (75 мг 1 раз в сутки) или тикагрелора (90 мг 2 раза в сутки) в зависимости от того, какой препарат получил пациент во время проведения ЧКВ и аспирина (100 мг); также пациенты получали адекватную медикаментозную терапию основного заболевания согласно стандартам. Представленный нами клинический опыт показал геморрагическую безопасность бивалирудина: в группе пациентов не наблюдалось ни одного геморрагического осложнения за время нахождения пациентов в условиях стационара.
Цель: изучить безопасность и эффективность использования препарата бивалирудин у пациентов с ОКС с подъемом сегмента ST.
Материалы и методы: в исследование было включено 20 пациентов, которые поступили с диагнозом ОКС с подъемом сегмента ST.Среди пациентов было 3 женщины и 17 мужчин. Возраст пациентов составил от 31 до 79 лет, средний 56±10,8лет. Инфаркт миокарда нижней стенки левого желудовка (ЛЖ) был диагностирован у 9 (45%), пациентов, передней стенки ЛЖ – у 11(55%) больных. Всем пациентам в экстренном порядке была выполнена коронарография (КАГ) с последующим ЧКВ. Многососудистое поражение коронарного русла было выявлено у 35% пациентов, окклюзия одной из коронарных артерий – в 20% случаев, пора-жение на уровне бифуркации – 15% больных, ствола левой коронарной артерии – в 30% наблюдениях. Перед выполнением ЧКВ 14(70%) пациентов получили нагрузочную дозу клопидогреля (600 мг), 6(30%) пациентов– тикагрелора (180 мг) в комбинации с аспирином. Интраоперационно пациентам вводили препарат бивалирудин («Ангиокс») по схеме: 0,75 мг/кг массы тела внутривенно болюсно, в дальнейшем – внутривенная инфузия со скоростью 1,75 мг/кг/ч на протяжении всего периода проведения эндоваскулярного вмешательства.
Трем пациентам в связи с техническими особенностями во время проведения операции была выполнена интракоронарная тромболизитическая терапия. В 2 случаях потребовалась установка внутриаортального баллонного контрпульсатора.
Результаты: всего данным больным было установлено 27 стентов (в среднем 1,35 стента на человека). Непосредственный технический успех эндоваскулярного вмешательства составил 100%. В отделении реанимации в течение 4 часов после операции продолжалась инфузия бивалирудина в дозе 0,25 мг/кг/ч, после перевода в отделение кардиологии продолжалась терапия эноксапарином согласно принятым в нашей клинике стандартам в течение пяти суток. После эндоваскулярного
 вмешательства пациентов переводили на стандартные дозы клопидогреля (75 мг 1 раз в сутки) или тикагрелора (90 мг 2 раза в сутки) в зависимости от того, какой препарат получил пациент во время проведения ЧКВ и аспирина (100 мг); также пациенты получали адекватную медикаментозную терапию основного заболевания согласно стандартам. Представленный нами клинический опыт показал геморрагическую безопасность бивалирудина: в группе пациентов не наблюдалось ни одного геморрагического осложнения за время нахождения пациентов в условиях стационара.
вмешательства пациентов переводили на стандартные дозы клопидогреля (75 мг 1 раз в сутки) или тикагрелора (90 мг 2 раза в сутки) в зависимости от того, какой препарат получил пациент во время проведения ЧКВ и аспирина (100 мг); также пациенты получали адекватную медикаментозную терапию основного заболевания согласно стандартам. Представленный нами клинический опыт показал геморрагическую безопасность бивалирудина: в группе пациентов не наблюдалось ни одного геморрагического осложнения за время нахождения пациентов в условиях стационара.
Experience in application of bivalirudin in patients with acute coronary syndrome with ST-segment elevation
* Kozhokar K.G. – MD
Urvantceva I.A. – MD, PhD
Gorkov A.I. – MD
Romashkin V.V. – MD
The state-financed institution «District cardiologic dispensary
«Centre for Diagnostics and Cardiovascular Surgery»
69/1, Lenina avenue, Surgut, Russian Federation, 628400
Аbstract:
Aim: was to study the safety and efficacy of the use of the drug bivalirudin in patients with acute coronary syndrome (ACS) with ST-segment elevation.
Materials and methods: the study included 20 patients which were admitted to hospital with a diagnosis of ACS with ST-segment elevation. Among patients - 3 women and 17 men. The age of patients ranged from 31 to 79 years, mean 56±10,8 years. Myocardial infarction of bottom wall of left ventricular (LV) was diagnosed in 9 (45%) patients, front wall – 11(55%) patients. All patients in the emergency order underwent coronary angiography (CA) with further PCI. Multivessel coronary disease was found in 35% of patients, occlusion of a coronary artery – in 20% of cases, bifurcation lesion – 15% of patients, the left main coronary artery - in 30% of cases. Before performing the PCI, 14(70%) of patients were given clopidogrel (600 mg), 6 (30%) of patients – ticagrelor (180 mg) in combination with aspirin. Intraoperative, patients received bivalirudin («Angioks») under the scheme: 0.75 mg/kg intravenous bolus, further – intravenous infusion at a rate of 1.75 mg/kg/h during the whole period of endovascular intervention.
Three patients due to technical features during the operation underwent intracoronary thrombolytic therapy. In 2 cases, situation required the installation of intra-aortic balloon counterpulsation.
Results: 20 patients underwent implanting of 27 stents (mean 1,35). Immediate technical success of endovascular intervention was 100%. In the intensive care unit for 4 hours after surgery lasted bivalirudin infusion at a dose of 0.25 mg/kg/h, after the transfer to  the Department of Cardiology continued therapy with enoxaparin within five days. After endovascular intervention patients were converted to standard doses of clopidogrel (75 mg daily) or ticagrelor (90 mg, 2 times a day), depending on drug, that patient was given during PCI and aspirin (100 mg); and patients receive adequate medical therapy of main disease according to standards of the disease. We presented clinical experience that shows safety of bivalirudin: in the group of patients was not observed any hemorrhagic complication during the time that patients were in a hospital.
the Department of Cardiology continued therapy with enoxaparin within five days. After endovascular intervention patients were converted to standard doses of clopidogrel (75 mg daily) or ticagrelor (90 mg, 2 times a day), depending on drug, that patient was given during PCI and aspirin (100 mg); and patients receive adequate medical therapy of main disease according to standards of the disease. We presented clinical experience that shows safety of bivalirudin: in the group of patients was not observed any hemorrhagic complication during the time that patients were in a hospital.
Введение
Сердечно-сосудистые заболевания будут оставаться наиболее актуальной проблемой здравоохранения большинства стран мира в XXI веке, несмотря на непрерывное совершенствование методов диагностики и лечения кардиологических больных. По данным Всемирной Организации Здравоохранения (ВОЗ), ишемическая болезнь сердца (ИБС) находится в ряду десяти ведущих причин инвалидности и смертности населения мира [1].
Согласно современным представлениям об атеросклеротическом процессе, являющемся причиной ишемической болезни сердца, течение этого заболевания может рассматриваться как смена периодов стабильности (стабильная стенокардия) и периодов обострения – острый коронарный синдром (ОКС) [2]. По определению ВНОК (2001г.): «Острый коронарный синдром – термин, обозначающий любую группу клинических признаков или симптомов, позволяющих по-дозревать острый инфаркт миокарда или нестабильную стенокардию» [3]. Подъем сегмента ST – как правило, следствие трансмуральной ишемии миокарда и возникает при наличии полной окклюзии одной из магистральных коронарных артерий. Скорейшее восстановление кровотока – наиболее действенный способ лечения острого коронарного синдрома со стойкими подъемами сегмента ST на электрокар-диограмме (ЭКГ) [4].
В настоящее время реперфузия миокарда при ОКС достигается преимущественно с помощью тромболитической терапии или чрескожного коронарного вмешательства (ЧКВ). У больных ОКС с подъемом сегмента ST на ЭКГ выполненное быстро и квалифицированно первичное ЧКВ имеет выраженные преимущества перед тромболитической терапией, включая снижение риска смерти и рецидива инфаркта миокарда [5]. «Золотым стандартом» лечения пациентов с ОКС в наши дни стало сочетанное использование возможностей рентгенэндоваскулярной хирургии и соврем-енной фармакологической поддержки как в предоперационном периоде, так и во время выполнения ЧКВ [6].
За последние годы проведено много исследований по изучению лекарственных средств и немедикаментозных вмешательств. Улучшение оказания медицинской помощи пациентам с ОКС, в том числе снижение риска развития неблагоприятных исходов, было основной целью данных работ. Среди достижений данных исследований ведущее положение занимает совершенствование антитромботического лечения в острый период заболевания. В настоящее время данная терапия включает одновременное использование двух антитромбоцитарных препаратов для приема внутрь (аспирин и блокатор P2Y12 рецепторов тромбоцитов – так называемая двойная антитромбоцитарная терапия – ДАТТ), парентеральный антикоагулянт – нефракционированный гепарин (НФГ), один из низкомолекулярных гепаринов (НМГ), фондапаринукс или бивалирудин; нередко используется третий антитромбоцитарный агент – блокатор IIb/IIIa рецепторов тромбоцитов, вводимый внутривенно в дополнение к аспирину или ДАТТ [7, 8].
В связи с внедрением агрессивных режимов антитромбоцитарной и антикоагулянтной терапии при выполнении ЧКВ у больных ОКС частота развития геморрагических осложнений, возникающих как в первые часы после операции, так и в отдаленном периоде, по-вышается от 3 до 20% (по данным различных авторов). Убедительно доказанная связь между развитием кровотечений и повышенной угрозой неблагоприятных сердечно-сосудистых осложнений (инфаркт миокарда, инсульт, смерть) привела к пересмотру отношения сочетания эффективности и безопасности современных антикоагулянтов [9, 10].
Одним из современных препаратов, позволяющих обеспечить геморрагическую безопасность и максимальную эффективность при выполнении ЧКВ у больных ОКС, является прямой ингибитор тромбина – бивалирудин.
Бивалирудин является одноцепочечным полипептидом, состоящим из 20 аминокислот и имеющим в своей основе структуру гирудина. Являясь прямым ингибитором тромбина, бивалирудин ингибирует все катализируемые и индуцируемые тромбином реакции, включая образование фибрина, активацию факторов свертывания V, VIII и XIII, активацию протеина С и агрегацию тромбоцитов. Бивалирудин обладает высокой селективностью к тромбину и не требует присутствия ко-факторов. Связывание бивалирудина с тромбином, а, следовательно, подавление активности последнего, является обратимым. Поэтому первоначально бивалирудин действует как полный неконкурентный ингибитор тромбина, но с течением времени становится конкурентным ингибитором, способным первоначально ингибировать взаимодействие молекул тромбина с другими субстратами сгустка и при необходимости ингибировать процесс коагуляции [11].
Важнейшая фармакологическая характеристика бивалирудина – отсутствие связывания с белками плазмы и 4-м тромбоцитарным фактором, обеспечивающая более предсказуемый, чем у НФГ, фармако-динамический ответ. Низкая иммуногенность делает маловероятной развитие тромбоцитопении. Важным достоинством следует признать непродолжительное время полужизни в плазме (25 минут). Кроме того, устраняя из кровотока активный тромбин, бивалирудин ослабляет его влияние на тромбоцитарные рецепторы, активированные протеазой, ограничивая активацию тромбоцитов [6–8].
Цель работы: на основе собственного клинического опыта изучить безопасность и эффективность использования препарата бивалирудин у пациентов с ОКС с подъемом сегмента ST.
Материалы и методы
В исследование было включено 20 пациентов, которые поступили с диагнозом ОКС с подъемом сегмента ST в БУ ХМАО-Югры «ОКД «ЦД и ССХ» г. Сургута за период с декабря 2011 г. по январь 2014 г. У данных пациентов во время выполнения ЧКВ применялся препарат бивалирудин («Ангиокс»). Среди пациентов было 3 женщины и 17 мужчин. Возраст пациентов составил от 31 до 79 лет, средний 56±10,8 лет. Клинико-демографическая характеристика пациентов представлена в таблице 1.
Диагноз инфаркт миокарда был установлен в соответствии с Европейскими рекомендациями: учитывалась клиническая картина, измения на электрокардио-грамме (ЭКГ), повышение сердечного тропонина (Т). Инфаркт миокарда нижней стенки левого желудовка (ЛЖ) был диагностирован у 9(45%) пациентов, передней стенки ЛЖ – у 11 (55%) больных.
Всем пациентам в экстренном порядке была выполнена коронарография (КАГ) трансфеморальным доступом с последующим ЧКВ. По заключению коронарографии, многососудистое поражение коронарного русла было выявлено у 35% пациентов, окклюзия одной из коронарных артерий – в 20% случаев, поражение на уровне бифуркации – 15% пациентов, 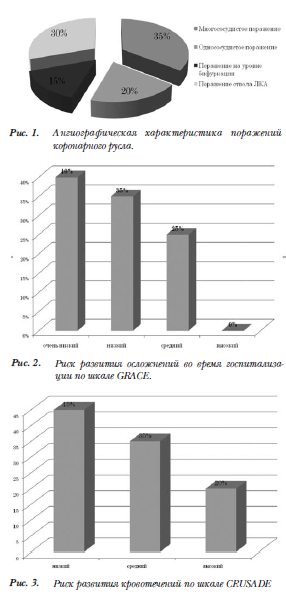 ствола левой коронарной артерии – 30% (рис. 1).
ствола левой коронарной артерии – 30% (рис. 1).
Следует отметить, что тромболитическая терапия данным пациентам на догоспитальном этапе не проводилась в связи с имеющейся возможностью быстрой транспортировки больных в стационар для выполнения реперфузии миокарда посредством ЧКВ.
У всех пациентов перед операцией проводилась оценка риска развития осложнений во время госпитализации по шкале GRACE (рис. 2) и риска развития кровотечений по шкале CRUSADE (рис. 3).
Перед выполнением ЧКВ 14(70%) пациентов получили нагрузочную дозу клопидогреля (600 мг), 6(30%) пациентов – тикагрелора (180 мг) в комбинации с аспирином. Интраоперационно пациентам вводили препарат бивалирудин («Ангиокс») по схеме: 0,75 мг/кг массы тела внутривенно болюсно, в дальнейшем – внутривенная инфузия со скоростью 1,75 мг/кг/ч на протяжении всего периода проведения эндоваскулярного вмешательства.
Трем пациентам в связи с техническими особенностями во время проведения операции была выполнена интракоронарная тромболитическая терапия. В 2 случаях потребовалась установка внутриаортального баллонного контрпульсатора.
Всего данным больным было установлено 27 стентов (в среднем 1,35 стента на человека). Непосредственный технический успех эндоваскулярного вмешательства составил 100%.
Оценка эффективности антикоагулянтной терапии осуществлялась посредством контроля показателей коагулограммы: активированного частичного тромбинового времени (АЧТВ), активированного времени свертывания (АВС), агрегации тромбоцитов. В частности, величина АВС через 5 мин. после введения препарата составляла более 300 с., что являлось свидетельством высокой антикоагулянтной активности препарата.
В отделении реанимации в течение 4 часов после операции продолжалась инфузия бивалирудина в дозе 0,25 мг/кг/ч, после перевода в отделение кардиологии продолжалась терапия эноксапарином согласно принятым в нашей клинике стандартам в течение пяти суток. После эндоваскулярного вмешательства пациентов переводили на стандартные дозы клопидогреля (75 мг 1 раз в сутки) или тикагрелора (90 мг 2 раза в сутки) в зависимости от того, какой препарат получил пациент во время проведения ЧКВ и аспирина (100 мг); также пациенты получали адекватную медикаментозную терапию основного заболевания согласно стандартам.
Средний койко-день нахождения пациентов в стационаре составил 9,5 (от 6 до 14 койко-дней). Максимальное количество койко-дней провел один из пациентов в связи с развитием у него в раннем послеоперационном периоде клиники дисциркуляторной энцефалопатии.
Кровотечений любой локализации во время нахождения в стационаре у пациентов не было зарегистрировано.
Все пациенты в течение года после выполнения оперативного вмешательства наблюдались у врача-кардиолога поликлиники ОКД «ЦД и ССХ». В отдаленном периоде мы получили следующие результаты: три пациента в течение года после перенесенного инфаркта миокарда были госпитализированы в кардиохирургическое отделение ОКД «ЦД и ССХ» для выполнения планового оперативного вмешательства в объеме аортокоронарного/маммарокоронарного шунтиро-вания в связи с наличием у них многососудистого поражения коронарного русла. Один пациент через 4 месяца после первой госпитализации был доставлен в приемное отделение с клиникой острого инфаркта миокарда, однако причиной госпитализации послужило прогрессирование атеросклеротического процесса в другой, ранее не стентированной коронарной артерии. Этот же больной еще через 3,5 месяца после повторной госпитализации обратился к врачу-кардиологу в связи с развитием рецидива клиники стенокардии; при детальном же изучении анамнеза выяснилось, что пациент назначенные препараты принимал нерегулярно или вовсе не принимал. Остальные пациенты отмечали субъективное улучшение самочувствия на фоне приема назначенной терапии, отсутствие рецидивов ангинозных болей. Повторных госпитализаций в связи с ухудшением состояния в течение года зарегистрировано не было.
Обсуждение
Нефракционированный гепарин (НФГ) долгое время был единственным ингибитором тромбина, применяемым при ОКС в большинстве клиник России. Несмотря на кажущуюся экономическую выгоду использования данного препарата, НФГ имеет ряд недостатков: необходимость частого контроля показателей коагулограммы, способность вызывать гепарининдуцированную тромбоцитопению с угрожающими жизни последствиями [12].
Использование низкомолекулярных гепаринов (НМГ) позволило снизить частоту развития побочных эффектов, однако при сравнении частоты встречаемости крупных геморрагических осложнений, группы НФГ и НМГ были сопоставимы [13].
Ингибитор фактора Xа, фондапаринукс, считается эффективным препаратом при ЧКВ, особенно у больных ОКС без подъема сегмента ST в связи отсутствием возможности взаимодействия с тромбином и ослабления свертывания крови на начальных этапах каскада коагуляции [8].
История клинического применения препарата бивалирудин в зарубежных странах насчитывает более 20 лет. В России данный препарат был зарегистрирован в 2010 г. Доказательная база эффективности бивалирудина включает 9 крупных рандомизированных исследований, в которых приняли участие более 40 000 больных.
Первым рандомизированным сравнительным исследованием, показавшим эффективность использова-ния бивалирудина в сравнении с НФГ при выполнении ЧКВ, стало HAS/BAT (Hirulog Angioplasty Study/Bivalirudin Angioplasty Trial). В группу исследуемых входило 4312 больных с постинфарктной стенокардией. Повторный анализ данных (BAT), подтвердил: бивалирудин не уступал НФГ в предотвращении смерти, инфаркта миокарда или необходимости выполне-ния повторной реваскуляризации миокарда; также достоверно реже (р<0,001) развивались крупные кровотечения – 3,5% в группе бивалирудина и 9,3% в группе гепарина [10].
Возможность использования бивалирудина у больных ОКС с подъемом сегмента ST, в отношении которых была выбрана интервенционная стратегия реперфузии с помощью ЧКВ, была доказана в проспективном рандомизированном открытом многоцентровом исследовании HORIZONS-AMI (the Harmonizing Outcomes with Revascularization and Stents in Acute Myocardial Infarction). Больные были рандомизированы в две группы: НФГ + блокатор IIb/IIIa рецепторов тромбоцитов (n=1802) и монотерапия бивалирудином (без блокаторов IIb/IIIa рецепторов тромбоцитов, n=1800). В ходе исследования были получены следующие результаты: по сравнению с гепарином в сочетании с ингибиторами GP IIb/IIIa, бивалирудин в монотерапии снижал риск наступления большого сердечно-сосудистого события на 24% лучше; сердечно-сосудистая смертность и летальность от любых причин на 30-й день среди пациентов, получавших бивалирудин в монотерапии, была соответственно на 38% и 34% достоверно ниже; риск развития большого кровотечения в группе бивалирудина был на 40% ниже. Таким образом, замена сочетания гепарина и блокатора IIb/IIIa рецепторов тромбоцитов на бивалирудин привела не только к снижению частоты кровотечений, но и к снижению смертности [14,15].
Представленный нами клинический опыт показал геморрагическую безопасность бивалирудина: в группе пациентов не наблюдалось ни одного геморрагического осложнения за время нахождения пациентов в условиях стационара.
Опираясь на анализ крупных рандомизированных исследований прямого ингибитора тромбина – бивалирудина и наш собственный опыт применения данного препарата, можно сделать следующие выводы: препарат отличается высокой эффективностью и безопасностью, позволяет значительно улучшить прогноз больных ОКС.
Cогласно Европейским рекомендациям ESC/EACT 2010 года по реваскуляризации миокарда, ESC 2012 года по лечению пациентов с подъемом сегмента ST, а также Американским рекомендациям ACC/AHA 2009 года по лечению больных ОКС с подъемом сегмента ST, препарат бивалирудин включен в самый высший I класс рекомендаций, уровень доказательности В и является обязательным к использованию у больных ОКС [6,16,7].
Список исп. литературыСкрыть списокСписок литературы/References
1. Болезни сердца: Руководство для врачей. (Под ред. Р.Г. Оганова, И.Г. Фоминой) М.: Литера. 2006; 1328.
Bolezni serdca: Rukovodstvo dlja vrachej [Cardiac diseases: guide-book for doctors]. (pod red. R.G. Oganova, I.G. Fominoj) M.: Litera. 2006; 1328 [In Russ].
2. Byrne C.E., Fitzgerald A., Cannon C.P., Fitzgerald D. J., Shields D. C. Elevated white cell count in acute coronary syndromes: relationship to variants in inflammatory and thrombotic genes Text. BMC Med. Genet. 2004; 5: 13.
3. Национальные клинические рекомендации (под ред. Р.Г. Оганова, М.Н. Мамедова) М.: МЕДИ-Экспо, 2009; 390.
Nacional'nye klinicheskie rekomendacii [National clinical recommendations] (pod red. R.G. Oganova, M.N. Mamedova) M.: MEDI-Jekspo, 2009; 390 [In Russ].
4. Довгалевский П.Я. Острый коронарный синдром: патогенез, клиническая картина, аспекты лечения. Что мы знаем и что надо делать? Сердце. 2002; 1(1): 1315.
Dovgalevskij P.Ja. Ostryj koronarnyj sindrom: patogenez, klinicheskaja kartina, aspekty lechenija. Chto my znaem i chto nado delat'? [Acute coronary syndrome: pathogenesis, clinical picture, aspects of treatment. What we know and what to do?] Serdce. 2002; 1(1): 1315 [In Russ].
5. Keeley E.C., Boura J.A., Grines C.L. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomized trials. Lancet. 2003; 361: 13–20.
6. Steg G., Stefan K. James, Atar D. et al. ESC Guidelines for the management of acute myocardial infarction in patients with ST-segment elevation. Eur. Heart J. 2012; 33: 2569–2619.
7. Wright R.S., Anderson J.L., Adams C.D. et al. 2011 ACCF/AHA focused update of the guidelines for the management of patients with unstable angina/non-ST-elevation myocardial infarction (updating the 2007 guideline): a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J. Am. Coll. Cardiol. 2011; 57: 1920–59.
8. Аверков О.В. Теоретическое обоснование и практические аспекты ис-пользования бивалирудина при чреcкожных внутрикоронарных вмешательствах у больных с острым коронарным синдромом. Российский кардиологический журнал. 2012; 3 (95): 102–112.
Averkov O.V. Teoreticheskoe obosnovanie i prakticheskie as-pekty ispol'zovanija bivalirudina pri chrezkozhnyh vnutrikoronarnyh vmeshatel'stvah u bol'nyh s ostrym koronarnym sindromom [Theoretical basis and practical aspects of the use of bivalirudin during PCI in patients with acute coronary syndrome.]. Rossijskij kardiologicheskij zhurnal. 2012; 3 (95): 102–112 [In Russ].
9. Mehran R., Pocock S.J., Stone G.W. et al. Associations of major bleeding and myocardial infarction with the incidence and timing of mortality in patients presenting with non-ST-elevation acute coronary syndromes: a risk model from the ACUITY trial. Eur. Heart J. 2009; 30: 655–661.
10. Bittle J.A., Chaitman B.R., Feit F. et al. Bivalirudin versus heparin during coronary angioplasty for unstable or postinfarction angina: Final report reanalysis of the Bivalirudin Angioplasty Study. Am. Heart J. 2001; 142(6): 952–959.
11. Nicolas W. Shammas. Bivalirudin: Pharmacology and Clinical Applications. Cardiovascular Drug Reviews. 2005; 23( 4): 345–360.
12. Kelton J.G., Warkentin T.E. Heparin-induced thrombocytopenia: a historical perspective. Blood. 2008; 112 (7): 2607–16.
13. Montalescot G., Collet G.P., Lison L. et al. Effects of various anticoagulant treatments on von Willebrand factor release in unstable angina. J. Am. Coll. Cardiol. 2000; 36: 100–114.
14. Stone G.W., Witzenbichler B., Guagliumi G. et al. for the HORIZONS-AMI Trial Investigators. Bivalirudin during primary PCI in acute myocardial infarction. N. Engl. J. Med. 2008 May 22; 358 (21): 2218–30.
15. Stone G.W., Witzenbichler B., Guagliumi G. et al. Heparin plus a glycoprotein IIb/IIIa inhibitors versus bivalirudin monotherapy and paclitaxel-eluting stents versus bare-metal stents in acute myocardial infarction (HORIZONS-AMI): final 3-years results from a multicenter, randomized controlled trial. Lancet. 2011; 377 (9784): 2193–2204.
16. Guidelines on myocardial revascularization, Eur. Heart J. 2010; doi 10.1093/eurheartj/ehj277.
17. Kushner F.G., Hand M., Smith S.C., et al. 2009 Focused updates: ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction (updating the 2004 guidline and 2007 focused update) and ACC/AHA/SCAI guidelines on percutaneous coronary intervention (updating the 2005 guideline and 2007 focused update): A report of the American College of Cardiology Foundation/ American Heart Assotiation Task Force on practice guidelines. J. Am. Coll. Cardiol. 2009; 54: 2205–2241.
