Диагностическая и интервенционная радиология 2015
№02 2015
Эндоваскулярная реваскуляризация миокарда у пациента в условиях частичного искусственного кровообращения (клиническое наблюдение) №02 2015
Ключевые слова:
• чрескожное коронарное вмешательство
• коронарное шунтирование
• искусственное кровообращение
• фракция выброса левого желудочка
• инфаркт миокарда
Приведено клиническое наблюдение, когда превентивное подключение вспомогательного искусственного кровообращения (ИК) позволило выполнить полную эндоваскулярную реваскуляризацию пациенту с инфарктом миокарда, многососудистым анатомически сложным поражением коронарных артерий и резко сниженной фракцией выброса левого желудочка.
Ключевые слова:
• чрескожное коронарное вмешательство
• коронарное шунтирование
• искусственное кровообращение
• фракция выброса левого желудочка
• инфаркт миокарда
Endovascular myocardial revascularization in patient during partial extracorporeal circulatian (case report)
Shmatkov M.G. – MD
*Morozova E.V. – MD
Morozov Z.A. – MD
Pantuhina M.A. – MD
Karpuhin V.G. – MD
Ministry of Health and Development of the Russain
Federation National Center of Cardiovascular Surgery
6, Stasova str., Penza, Russian Federation, 440071
ABSTRACT:
We present report of successful full revascularization of heart during additional adjuvant extracorporeal revascularization (EcR) in case of difficult anatomy of anatomically difficult, multivessel lesions of coronary arteries and reduced ejection fraction (EF) of left ventricular (LV).
Key-words:
• percutaneous intervention
• coronary bypass
• extracorporeal circulation
• ejection fraction of left ventricular
• myocardial infarction
Введение
Пациенты высокого хирургического риска с тяжелым поражением коронарных артерий, с инфарктом миокарда и низкой фракцией выброса (ФВ) левого желудочка (ЛЖ) все чаще подвергаются чрескожным коронарным вмешательствам (ЧКВ), как методу реваскуляризации. Коронарное шунтирование (КШ) до сих пор считается стандартом лечения у таких пациентов. Однако превосходства хирургической реваскуляризации в значительной степени нивелируются возможным периоперационным риском [1].
Одними из основных ограничивающих факторов для проведения КШ являются ИМ и резко сниженная ФВ ЛЖ. По действующим рекомендациям ACC / AHA КШ у пациентов с ФВ ЛЖ 35–50% имеет класс рекомендаций IIa и уровень доказательности В; а также IIb класс и уровень доказательности B для пациентов с ФВ ЛЖ менее 35% [2].
Чрескожное коронарное вмешательство у пациентов с ФВ <35% как с преобладанием клиники стенокардии, так и с превалированием недостаточности кровообращения возможно при наличии соответствующей анатомии коронарных артерий и жизнеспособного миокарда (класс рекомендаций IIb, уровень доказательности C [2].
На практике, если пациенту требуется реваскуляризация миокарда при наличии факторов риска для КШ предпочтение отдается ЧКВ. Однако само эндоваскулярное вмешательство при многососудистом поражении и низкой ФВ ЛЖ связано с высоким риском. Летальность может достигать 10%. Ряд авторов в подобных тактически сложных ситуациях рекомендует использовать экстракорпоральную поддержку кровообращения при ЧКВ [3–5].
Применение средств вспомогательного кровообращения, по некоторым данным, позволяет снизить этот показатель до 2,5–5,5% [6].
Клинический пример
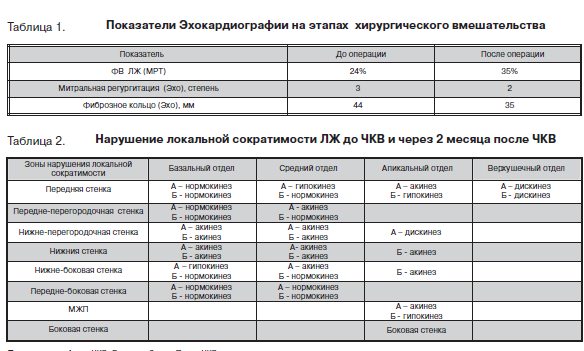
 Пациент С., 53 года, поступил 14.07.2014 г. в ФГБУ «ФЦССХ» Минздрава России (г. Пенза) на КШ с пластикой митрального клапана (МК). По данным эхокардиографии сердца (ЭХО-КГ) и магнитно-резонансной томографии (МРТ) сердца: ФВ ЛЖ составила 24%, регургитация на митральном клапане (МК) 3 степени с дилатацией фиброзного кольца (ФК) до 44 мм, легочная гипертензия 2 ст.
Пациент С., 53 года, поступил 14.07.2014 г. в ФГБУ «ФЦССХ» Минздрава России (г. Пенза) на КШ с пластикой митрального клапана (МК). По данным эхокардиографии сердца (ЭХО-КГ) и магнитно-резонансной томографии (МРТ) сердца: ФВ ЛЖ составила 24%, регургитация на митральном клапане (МК) 3 степени с дилатацией фиброзного кольца (ФК) до 44 мм, легочная гипертензия 2 ст.
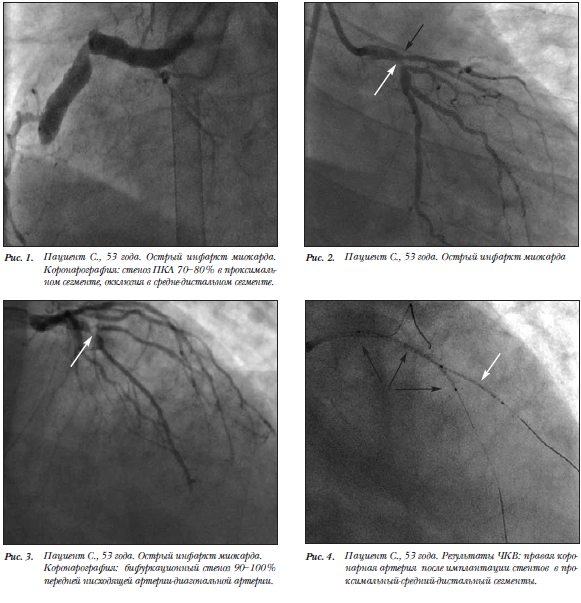
На коронарографии: стеноз ствола левой коронарной артерии (ЛКА), окклюзия правой коронарной артерии (рис.1), значимые устьевые поражения ПНА и ОА (рис. 2), критический бифуркационный стеноз ПНА-ДВ1 (рис. 3). Значение Syntax Score составило 52 балла.
Отмечает ухудшение в состоянии за последние несколько дней (давящие боли в области сердца при малейшей физической нагрузке, купирующиеся приемом нитратов). Принимая во внимание клиническую картину, данные электрокардиографического обследования (ЭКГ): патологический зубец Q во 2, 3 и avF, депрессия сегмента ST в avL, V4-6); тропонин Т: 321,4 нг/л (при норме 0–100) был выставлен диагноз инфаркта миокарда. (EuroSCORE – 12; 35,48%).
Учитывая сложность поражения коронарного русла, резко сниженную насосную функцию ЛЖ и инфаркт миокарда (ИМ) решено выполнить эндоваскулярную реваскуляризацию миокарда в условиях частичного искусственного кровообращения (ИК).
 Под эндотрахеальным наркозом секционно канюлированы бедренные артерия и вена слева. После болюсного введения гепарина в дозе 3 мкг/кг начато ИК с использованием центрифужного насоса, стандартного оксигенатора и модифицированного мини-контура, при котором из циркуляции исключается кардиотомный резервуар.
Под эндотрахеальным наркозом секционно канюлированы бедренные артерия и вена слева. После болюсного введения гепарина в дозе 3 мкг/кг начато ИК с использованием центрифужного насоса, стандартного оксигенатора и модифицированного мини-контура, при котором из циркуляции исключается кардиотомный резервуар.
Чрескожное коронарное вмешательство (ЧКВ) проводили по стандартной методике чрезбедренным доступом с имплантацией голометаллических стентов, так как предполагалось, что через 3 месяца пациенту будет выполнено КШ с пластикой МК.
Первым этапом выполнена реканализация правой коронарной артерии (ПКА) с имплантацией стентов размерами: 3,5´32 мм, 4,0´24 мм и 3,5´32 мм (рис.4).
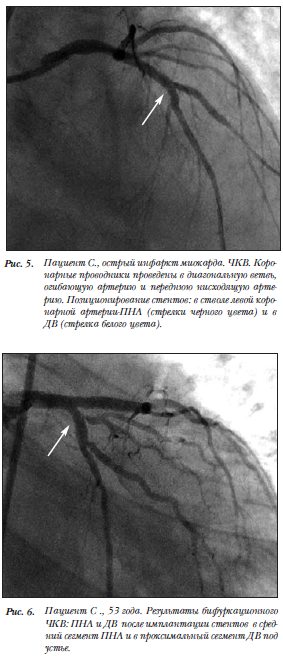
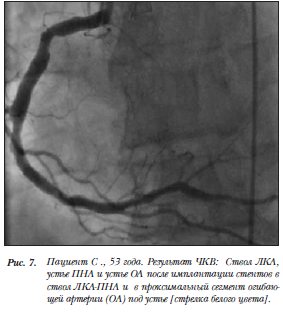
Затем выполнена реканализация дистального сегмента ПНА и бифуркационное: стентирование ствола левой коронарной артерии (ЛКА)-ПНА и ПНА-ДВ с имплантацией стентов размерами: 3,0´19 мм в ДВ и 3,5´32 мм в позицию ствол ЛКА-ПНА (проксимальный-средний сегменты); имплантация стента размерами 3,5´8 мм в устье ОА (рис.5–7). Необходимо отметить, что во время имплантации стентов в ПНА и ОА неоднократно возникали эпизоды фибрилляции желудочков.
Основной этап операции проводили в условиях частичного ИК на разгруженном сердце. Длительность ИК составила 32 мин. Артериотомный разрез общей бедренной артерии слева послойно ушит. Пациент экстубирован через 1 час. На следующие сутки после операции пациент был переведен в профильное отделение. Пациент был выписан домой на 7 сутки в удовлетворительном состоянии.
Антитромбоцитарная терапия осуществлялась клопидогрелем в нагрузочной дозе 600 мг и 75 мг в сутки в последующем, и аспирином в нагрузочной дозе 320 мг (затем 75 мг в сутки).
Через 2 месяца при контрольном обследовании отмечает улучшение состояния. Стенокардия на уровне
2-го функционального класса. По данным инструментальных методов обследования (ЭХОКГ и МРТ сердца): ФВ ЛЖ возросла с исходных 24% до 35%; регургитация на МК снизилась с 3 до 2 степени, фиброзное кольцо митрального клапана уменьшилось до 35 мм (табл.1).
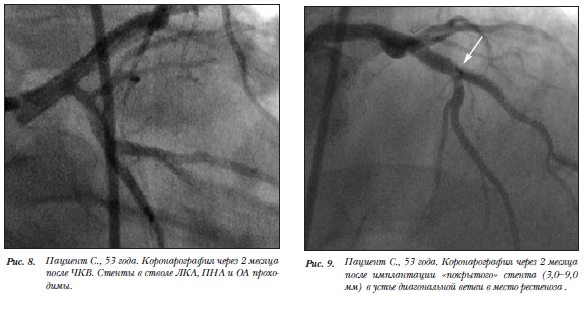
Отмечается улучшение сократимости передней, передне-перегородочной, нижнебоковой, боковой стенок и МЖП (рис.8). Индекс локальной сократимости снизился с 2,44 до 1,88 (табл.2).
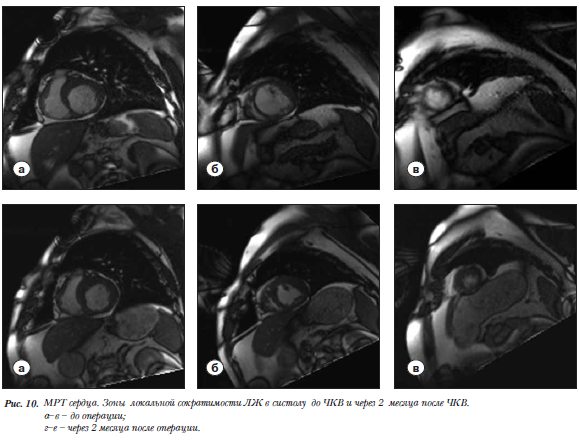 На контрольной коронарографии стенты в ПКА, ПНА, ОА проходимы, отмечается рестеноз стента в ДВ, по поводу чего проведена имплантация стента с лекарственным покрытием (рис. 9,10).
На контрольной коронарографии стенты в ПКА, ПНА, ОА проходимы, отмечается рестеноз стента в ДВ, по поводу чего проведена имплантация стента с лекарственным покрытием (рис. 9,10).
Обсуждение
Большинство исследований, сравнивающих ЧКВ с КШ, включает не более 20% пациентов с нарушением функции ЛЖ. У пациентов с дисфункцией ЛЖ предпочтение отдается КШ, так как доказано улучшение выживаемости по сравнению с ЧКВ. У хирургической реваскуляризации имеются очевидные преимущества при мягкой и умеренной дисфункции ЛЖ, и менее выраженные при тяжелом нарушении сократимости ЛЖ. Основная причина связана с высоким риском периоперационных осложнений у пациентов с ФВ <30 [7,8].
Пациенты с ИМ, высокими значениями Syntax Score (более 32) и ФВ<30% входят в группу высокого риска, как для КШ, так и для ЧКВ. Методом выбора у пациентов высокого риска до настоящего времени остается КШ, потому что может обеспечить более полную реваскуляризацию с хорошими отдаленными результатами. Тем не менее, некоторые такие пациенты отказываются от КШ или имеют сопутствующие заболевания, которые ставят их в непомерно высокий хирургический риск, достигающий по некоторым данным 30–50% [9]. В таких ситуациях ЧКВ при поддержке частичного ИК предоставляет альтернативное лечение КШ. Смертность у пациентов с ИБС и ФВ ЛЖ <25% существенно снижается при выполнении ЧКВ в условиях вспомогательного ИК и составляет 2,5–5,5%. Частота успеха ЧКВ составляет около 100% при отсутствии операционной летальности. Смертность в течение одного года не превышает 2,0% –2,5% [11,12]. Первые сообщения о применении частичного ИК во время ЧКВ у пациента высокого риска были датированы еще 80-ми годами [9]. Однако до сих пор не отражены в рекомендациях. Чрескожное коронарное вмешательство у пациентов с высоким риском связано с несколькими этапами временного прекращения кровотока, а также возможностью появления новых зон ишемии миокарда. Это может спровоцировать возникновение жизнеугрожающих аритмий и остановку сердечной деятельности. У больных с низким коронарным резервом данная цепь событий может стать фатальной. Частичное ИК позволяет поддерживать перфузионное артериальное давление в аорте даже при критических значениях сердечного выброса, а жизнеугрожающие аритмии носят обратимый характер [10].
Смертность при ЧКВ с ИК по сравнению с КШ у пациентов с ИМ при многососудистом поражении и резко сниженной ФВ ЛЖ, составляет 4,8% и 18,8% соответственно [4, 11]. При развитии кардиогенного шока летальность достигает 50–70% [13].
Заключение
Использование экстракорпоральной поддержки позволяет специалисту по рентгеноэндоваскулярной диагностике и лечению комфортно работать, не делая поправок на фактор времени и возможную необходимость проведения реанимационных мероприятий. Наш опыт показывает, что превентивное подключение частичного ИК у больных с планируемым ЧКВ высокого риска, может сыграть ключевую роль в успехе ЧКВ. Поддержка частичным ИК является более безопасным и менее инвазивным методом лечения, имеет более низкий процедурный риск и острую смертность, чем АКШ для пациентов с высоким хирургическим риском.
Список исп. литературыСкрыть список1. Serruys P.W., Morice M.C., Kappetein A.P., Colombo A., et al. Percutaneous coronary intervention versus coronary-artery bypass grafting for severe coronary artery disease. Engl. J. Med. 2009; 360: 961–972.
2. Levine G., Bates E., Blankenship J., et al. 2011 ACCF/AHA/SCAI guideline for percutaneous coronary intervention: a report of the American College of Cardio-logy Foundation/ American Heart Association Task Force on Practice Guidelines and the Society for Cardiovascular Angiography and Interventions. J Am. Coll.Cardiol. 2011.
3. Shawl F.A., Bajaj S., Hoff S.B., Dougherty K.G. Percutaneous cardiopulmonary bypass-supported coronary angioplasty in patients Levine G., with unstable angina pectoris or myocardial infarction and a left ventricular ejection fraction ≤25%. Am. J. Cardiol. 1996;77: 14–9.
4. Teirstein P., Vogel R., Dorros G., et al. Prophylactic versus standby cardiopulmonary support for high risk percutaneous transluminal coronary angioplasty. J. Am. Coll. Cardiol. 1993;21:590–6.
5. Cho S., Oh C., Jang J., Yu H. et al. Percutaneous Cardiopulmonary Support-Supported Percutaneous Coronary Intervention: A Single Center Experience. Korean Circ. J. 2011 Jun; 41(6): 299–303.
6. William W., O'Neill. What is High-risk PCI, and How Do You Safely Perform It? J. Invasive. Cardiol. 2011; 23(10): 425–426.
7. Passamani E. A randomized trial of coronary artery bypass surgery. Survival of patients with a low ejection fraction. Engl. J. Med. 1985; 312(26): 1665–71.
8. Scott S.M. VA Study of Unstable Angina. 10-year results show duration of surgical advantage for patients with impaired ejection fraction. Circulation. 1994. 90(5 Pt 2): p.II120–3.
9. Chin-Hu Lai, Yi-Shian Chu, Wen-Ling Li еt al. Percutaneous Coronary Intervention under Extracorporeal Membrane Oxygenation Support for High-Risk Acute Myocardial Infarction with Cardiogenic Shock. J. Med. Sci. 2008; 28(1):039–044.
10. Sung Soo Cho, Chang-Myung Oh, Ji-Yong Jang еt al. Percutaneous Cardiopulmonary Support-Supported Percutaneous Coronary Intervention: A Single Center Experience Sung. original article doi 10.4070/kcj. 2011.41.6.299.
11. Wong P., Wong V., Tse K.K., еt al. A prospective study of elective stenting in unprotected left main coronary disease. Cathet. Cardiovas. Intervent. 1999;46:153–159.
12. Silvestri M., Barragan P., Sainsous J., et al. Unprotected left main coronary artery stenting: Immediate and medium-term outcomes of 140 elective procedures. J. Am. Coll. Cardiol. 2000; 35: 1543–1550.
13. Zeymer U., Vogt A., Zahn R., еt al. Predictors of in-hospital mortality in 1333 patients with acute myocardial infarction complicated by cardiogenic shock treated with primary percutaneous coronary intervention (PCI). Eur. Heart J. 2004; 25: 322–328.
