Психиатрия Дневник психиатра (психиатрическая газета)
Психиатрия Дневник психиатра (психиатрическая газета)
№04 2012
Большое депрессивное расстройство, ангедония и Вальдоксан: открытое исследование №04 2012
Номера страниц в выпуске:15-16
Депрессия относится к числу главных причин дезадаптации в соответствии с показателями YLD (Years Lost due to disability) и заняла третье место среди основных факторов бремени болезни DALY (Disability Adjusted Life Years) в 2004 г. В соответствии с текущими прогнозами к 2020 г. депрессия выйдет на второе место по показателям DALYs для всех возрастных групп и обоих полов. Кроме того, последствия депрессивных симптомов распространяются далеко за пределы психиатрии и часто определяют различные формы патологии, включая иммунологические и эндокринные расстройства, болезни сердца. Ангедония, т.е. утрата интересов и реакций на положительные стимулы, рассматривается как ядерный симптом депрессии и входит в число диагностических критериев большого депрессивного расстройства (БДР). Ангедония является предиктором неблагоприятного прогноза через 12 мес и относится к типичным резидуальным симптомам после терапии. Современный арсенал средств терапии депрессии включает множество эффективных антидепрессантов. Однако эффект терапии часто оказывается недостаточным. Примерно 30% пациентов с диагнозом БДР не отвечают на терапию антидепрессантами и менее 60% достигают ремиссии. Основные проблемы, связанные с применением современных антидепрессантов, включают в себя нежелательные эффекты при кратковременном и длительном применении, такие как гастроинтестинальные расстройства, тошнота, расстройства сна, прибавка массы тела, половые дисфункции, недостаточная эффективность, задержка эффекта, взаимодействие с другими медикаментами и в некоторых случаях потребность в полифармакотерапии. Эти недостатки определяют необходимость разработки альтернативных средств с высокой эффективностью, хорошей переносимостью, улучшенной безопасностью и быстрым развитием эффекта. Вальдоксан открывает новую стратегию в терапии депрессии. В отличие от других антидепрессантов Вальдоксан обладает инновационным нейрохимическим механизмом. Вальдоксан действует как агонист мелатонинергических MT1- и MT2-рецепторов и селективный антагонист 5HT2C-рецепторов. Вальдоксан легко проникает через гематоэнцефалический барьер и синхронизирует циркадианный ритм. Основная гипотеза, объясняющая механизм антидепрессивного эффекта Вальдоксана, предполагает синергическое взаимодействие с мелатонинергическими и 5HT2C-рецепторами. Этот синергизм может реализоваться на уровне циркадианных ритмов с преобладанием мелатонинергического компонента действия в ночное время и серотонинергического в дневное время. Данные преклинических и клинических исследований свидетельствуют, что Вальдоксан обладает свойствами антидепрессанта, редуцирует симптомы тревоги, связанные с депрессией, и обеспечивает быструю редукцию симптомов в сравнении с плацебо. Кроме того, профиль переносимости и безопасности Вальдоксана характеризуется минимальным влиянием на половую функцию, отсутствием симптомов отмены после завершения терапии и улучшением качества сна у пациентов с депрессией. Для подтверждения клинической эффективности и переносимости Вальдоксана в терапии рекуррентного депрессивного расстройства в Италии нами выполнено открытое 8-недельное исследование Вальдоксана у 30 амбулаторных пациентов с диагнозом БДР по DSM-IV. Дополнительно изучался эффект Вальдоксана на ангедонию.
Выборку исследования составили 30 амбулаторных пациентов мужского и женского пола в возрасте от 18 до 60 лет с диагнозом БДР по критериям DSM-IV (American Psychiatry Association, 1994), по результатам Структурированного диагностического интервью для DSM-IV (SCID-P). Критерии включения также предусматривали способность пациента понять и подписать информированное согласие. Были приняты следующие критерии исключения: клинически значимое заболевание, препятствующее оценке терапии или влияющее на безопасность субъектов исследования (например, цирроз печени, почечная недостаточность, нестабильная артериальная гипертензия, артериальная гипотензия, сахарный диабет, судороги); биполярное расстройство, шизофрения, шизоаффективное расстройство, расстройство пищевого поведения, обсессивно-компульсивное расстройство, зависимость от психоактивных веществ, сопутствующее применение других антидепрессантов (в этом случае требовался период отмывки 7 дней), печеночная недостаточность. В исследовании не могли участвовать пациенты женского пола во время беременности, кормления грудью или не использующие адекватных средств контрацепции. Исследование было одобрено этическим комитетом и проводилось в соответствии с принципами качественной клинической практики. От всех пациентов было получено письменное информированное согласие до их включения в исследование.
Открытое 8-недельное исследование проводилось на базе двух учреждений: Университет G.d’Annunzio в г. Киети (Chieti) и Клиника нейропсихиатрии (Casa di cura neuropsichiatrica) Villa Maria Pia в Риме. Исследование продолжалось 4 мес в 2 этапа: 8 нед – отбор пациентов, и еще 8 нед – терапия включенных пациентов. Пациенты, соответствовавшие критериям включения и исключения, участвовали в исследовании после подписания информированного согласия. У всех пациентов собирали медицинский и семейный анамнез, данные фиксировались в специальных ИРК. Для пациентов, принимавших антидепрессанты (трициклики, ИМАО, СИОЗС и другие антидепрессанты новых поколений), предусматривался 7-дневный период фармакологической отмывки. После подтверждения соответствия критериям участия в исследовании в скрининговом периоде пациенты начинали терапию Вальдоксаном в стартовой дозе 25 мг/сут, внутрь, однократно, перед сном. В отсутствие клинического эффекта и с последующего одобрения исследователя допускалось повышение дозы до 50 мг/сут однократно. Медицинское обследование выполнялось квалифицированным врачом изначально (T0), далее на 7 (T1), 14 (T2), 30 (T3) и 60-й (T4) дни и включало оценку витальных показателей, регистрацию медикаментов сопутствующей терапии и оценку тяжести всех нежелательных явлений. На стартовом визите (T0) оценивались личностные характеристики пациентов с помощью шкалы темперамента и характера (Temperament и Character Inventory, TCI) и структурированного интервью для расстройств по оси II в DSM-IV (SCID II). На визитах T1, T2, T3 и T4 оценивался эффект терапии по степени редукции депрессивных и тревожных симптомов (шкала депрессии Гамильтона, HAM-D, шкала тревоги Гамильтона, HAM-A) и ангедонии (шкала Снайта–Гамильтона, SHAPS). Вопросник Leeds для оценки сна (LSEQ), 10-пунктовая визуальная аналоговая шкала использовались для измерения эффекта Вальдоксана на сон. Общая клиническая оценка (шкала общего клинического впечатления, CGI) и оценка качества жизни – КЖ (индекс КЖ – Quality of Life Index) выполнялись исследователем в начале и по завершении терапии.
В соответствии с задачами исследования главным параметром эффективности была степень редукции баллов депрессивных и тревожных симптомов по шкалам HAM-D и HAM-A. В первую очередь оценивалась разница между показателями в начале (Т0) и по завершении (60 дней, T4) терапии. Дополнительным параметром была редукция ангедонии и инсомнии по шкалам SHAPS и LSEQ соответственно, а также улучшение КЖ и клинического состояния (CGI) на T4, в абсолютных и процентных изменениях стартовых значений (T0). Дополнительным параметром также была оценка переносимости Вальдоксана.
Сведения о нежелательных явлениях собирались у пациентов на протяжении всего периода исследования. Витальные показатели, масса тела и рост оценивались во время скрининга, на стартовом и каждом последующем визитах. Анализы крови (клеточная формула с дифференцированным подсчетом, билирубин, АСТ, АЛТ, щелочная фосфатаза, g-глутамилтрансфераза, натрий, хлор, азот мочевины крови, креатинин, глюкоза) и мочи выполнялись на стартовом (T0) и финальном (T4) визитах.
Главный и дополнительные анализы эффективности проводились в общей выборке терапии (intent-to-treat), в которую включались все пациенты, получившие минимум одну дозу препарата исследования. Психометрические данные пациентов анализировались методом вариационного анализа (ANOVA) для повторных измерений с помощью метода замещения недостающего значения предыдущим (LOCF). Post-hoc анализы проводились для сравнения психометрических показателей при стартовых измерениях с показателями через 1 нед терапии (T1) и по завершении исследования (T4). Тесты были двусторонними с уровнем статистической достоверности p<0,05.
 После скрининга 43 пациентов в исследование были включены 30 пациентов. Скрининг не прошли 5 пациентов, отозвавшие информированное согласие, 3 пациента, не соответствовавшие психиатрическим критериям включения, 2 пациента, не соответствовавшие медицинским критериям включения, и 3 пациента, не соответствовавшие критериям участия в исследовании по другим причинам. Средний возраст, пол, социодемографические характеристики и длительность текущего депрессивного эпизода 30 включенных в исследование пациентов представлены в табл. 1.
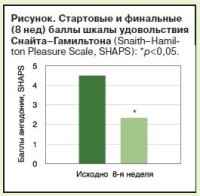
После скрининга 43 пациентов в исследование были включены 30 пациентов. Скрининг не прошли 5 пациентов, отозвавшие информированное согласие, 3 пациента, не соответствовавшие психиатрическим критериям включения, 2 пациента, не соответствовавшие медицинским критериям включения, и 3 пациента, не соответствовавшие критериям участия в исследовании по другим причинам. Средний возраст, пол, социодемографические характеристики и длительность текущего депрессивного эпизода 30 включенных в исследование пациентов представлены в табл. 1.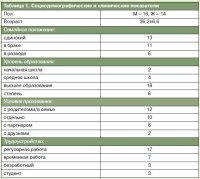 24 (80%) пациента полностью завершили 8 нед терапии. Преждевременно выбыли 6 пациентов по следующим причинам: решение пациента (n=1), невозможность катамнестической оценки из-за утраты связи с пациентом (n=4) и недостаточная эффективность (n=1). Не было ни одного случая преждевременного исключения из-за побочных эффектов. Также не было пациентов с ухудшением аффективных симптомов или госпитализированных в результате терапии исследования. По завершении исследования значительное улучшение отмечалось по всем показателям (табл. 2). Значимое улучшение наблюдалось на всех визитах в показателях HAM-D (p<05), HAM-A (p<0,01), SHAPS (p<05) (см. рисунок), LSEQ (p<0,05). Также отмечалось достоверное улучшение баллов CGI и КЖ (p<0,05). На 1-й неделе 9 (30%) пациентов были респондерами (95% ДИ 13–46%) и 5 (17%) пациентов достигли ремиссии. По завершении исследования в ремиссии были 18 (60%) пациентов (95% ДИ 42–77%). У 3 пациентов редукция баллов депрессии отмечалась после повышения дозы Вальдоксана до 50 мг/сут. Серьезных нежелательных явлений не отмечалось.
24 (80%) пациента полностью завершили 8 нед терапии. Преждевременно выбыли 6 пациентов по следующим причинам: решение пациента (n=1), невозможность катамнестической оценки из-за утраты связи с пациентом (n=4) и недостаточная эффективность (n=1). Не было ни одного случая преждевременного исключения из-за побочных эффектов. Также не было пациентов с ухудшением аффективных симптомов или госпитализированных в результате терапии исследования. По завершении исследования значительное улучшение отмечалось по всем показателям (табл. 2). Значимое улучшение наблюдалось на всех визитах в показателях HAM-D (p<05), HAM-A (p<0,01), SHAPS (p<05) (см. рисунок), LSEQ (p<0,05). Также отмечалось достоверное улучшение баллов CGI и КЖ (p<0,05). На 1-й неделе 9 (30%) пациентов были респондерами (95% ДИ 13–46%) и 5 (17%) пациентов достигли ремиссии. По завершении исследования в ремиссии были 18 (60%) пациентов (95% ДИ 42–77%). У 3 пациентов редукция баллов депрессии отмечалась после повышения дозы Вальдоксана до 50 мг/сут. Серьезных нежелательных явлений не отмечалось. 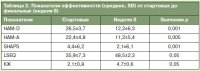 Наиболее типичными нежелательными явлениями, связанными с терапией исследования, были головокружение (6,6%; n=2), тошнота (3,3%; n=1) и слабость (3,3%; n=1). Повышения аминотрансфераз не выявлено. Не было ни одного случая развития мании.
Наиболее типичными нежелательными явлениями, связанными с терапией исследования, были головокружение (6,6%; n=2), тошнота (3,3%; n=1) и слабость (3,3%; n=1). Повышения аминотрансфераз не выявлено. Не было ни одного случая развития мании.
Материалы и методы
ПациентыВыборку исследования составили 30 амбулаторных пациентов мужского и женского пола в возрасте от 18 до 60 лет с диагнозом БДР по критериям DSM-IV (American Psychiatry Association, 1994), по результатам Структурированного диагностического интервью для DSM-IV (SCID-P). Критерии включения также предусматривали способность пациента понять и подписать информированное согласие. Были приняты следующие критерии исключения: клинически значимое заболевание, препятствующее оценке терапии или влияющее на безопасность субъектов исследования (например, цирроз печени, почечная недостаточность, нестабильная артериальная гипертензия, артериальная гипотензия, сахарный диабет, судороги); биполярное расстройство, шизофрения, шизоаффективное расстройство, расстройство пищевого поведения, обсессивно-компульсивное расстройство, зависимость от психоактивных веществ, сопутствующее применение других антидепрессантов (в этом случае требовался период отмывки 7 дней), печеночная недостаточность. В исследовании не могли участвовать пациенты женского пола во время беременности, кормления грудью или не использующие адекватных средств контрацепции. Исследование было одобрено этическим комитетом и проводилось в соответствии с принципами качественной клинической практики. От всех пациентов было получено письменное информированное согласие до их включения в исследование.
Дизайн исследования
Оценка эффективности
Оценка переносимости и безопасности
Статистический анализ
Результаты
 После скрининга 43 пациентов в исследование были включены 30 пациентов. Скрининг не прошли 5 пациентов, отозвавшие информированное согласие, 3 пациента, не соответствовавшие психиатрическим критериям включения, 2 пациента, не соответствовавшие медицинским критериям включения, и 3 пациента, не соответствовавшие критериям участия в исследовании по другим причинам. Средний возраст, пол, социодемографические характеристики и длительность текущего депрессивного эпизода 30 включенных в исследование пациентов представлены в табл. 1.
После скрининга 43 пациентов в исследование были включены 30 пациентов. Скрининг не прошли 5 пациентов, отозвавшие информированное согласие, 3 пациента, не соответствовавшие психиатрическим критериям включения, 2 пациента, не соответствовавшие медицинским критериям включения, и 3 пациента, не соответствовавшие критериям участия в исследовании по другим причинам. Средний возраст, пол, социодемографические характеристики и длительность текущего депрессивного эпизода 30 включенных в исследование пациентов представлены в табл. 1. 24 (80%) пациента полностью завершили 8 нед терапии. Преждевременно выбыли 6 пациентов по следующим причинам: решение пациента (n=1), невозможность катамнестической оценки из-за утраты связи с пациентом (n=4) и недостаточная эффективность (n=1). Не было ни одного случая преждевременного исключения из-за побочных эффектов. Также не было пациентов с ухудшением аффективных симптомов или госпитализированных в результате терапии исследования. По завершении исследования значительное улучшение отмечалось по всем показателям (табл. 2). Значимое улучшение наблюдалось на всех визитах в показателях HAM-D (p<05), HAM-A (p<0,01), SHAPS (p<05) (см. рисунок), LSEQ (p<0,05). Также отмечалось достоверное улучшение баллов CGI и КЖ (p<0,05). На 1-й неделе 9 (30%) пациентов были респондерами (95% ДИ 13–46%) и 5 (17%) пациентов достигли ремиссии. По завершении исследования в ремиссии были 18 (60%) пациентов (95% ДИ 42–77%). У 3 пациентов редукция баллов депрессии отмечалась после повышения дозы Вальдоксана до 50 мг/сут. Серьезных нежелательных явлений не отмечалось.
24 (80%) пациента полностью завершили 8 нед терапии. Преждевременно выбыли 6 пациентов по следующим причинам: решение пациента (n=1), невозможность катамнестической оценки из-за утраты связи с пациентом (n=4) и недостаточная эффективность (n=1). Не было ни одного случая преждевременного исключения из-за побочных эффектов. Также не было пациентов с ухудшением аффективных симптомов или госпитализированных в результате терапии исследования. По завершении исследования значительное улучшение отмечалось по всем показателям (табл. 2). Значимое улучшение наблюдалось на всех визитах в показателях HAM-D (p<05), HAM-A (p<0,01), SHAPS (p<05) (см. рисунок), LSEQ (p<0,05). Также отмечалось достоверное улучшение баллов CGI и КЖ (p<0,05). На 1-й неделе 9 (30%) пациентов были респондерами (95% ДИ 13–46%) и 5 (17%) пациентов достигли ремиссии. По завершении исследования в ремиссии были 18 (60%) пациентов (95% ДИ 42–77%). У 3 пациентов редукция баллов депрессии отмечалась после повышения дозы Вальдоксана до 50 мг/сут. Серьезных нежелательных явлений не отмечалось.  Наиболее типичными нежелательными явлениями, связанными с терапией исследования, были головокружение (6,6%; n=2), тошнота (3,3%; n=1) и слабость (3,3%; n=1). Повышения аминотрансфераз не выявлено. Не было ни одного случая развития мании.
Наиболее типичными нежелательными явлениями, связанными с терапией исследования, были головокружение (6,6%; n=2), тошнота (3,3%; n=1) и слабость (3,3%; n=1). Повышения аминотрансфераз не выявлено. Не было ни одного случая развития мании.
Обсуждение
Насколько нам известно, это первое исследование Вальдоксана как средства ресинхронизации циркадианных ритмов у пациентов южного побережья Средиземного моря – региона, в котором продолжительность светового дня, климатические условия и распространенность сезонного аффективного расстройства отличаются от таковых в Северной Европе. В результате 8-недельного открытого исследования Вальдоксана с гибким режимом дозирования в пределах 25–50 мг/сут у 30 амбулаторных пациентов с БДР выявлено достоверное улучшение баллов HAM-D, HAM-A, SHAPS и LSEQ, начиная со 2-й недели терапии и далее вплоть до конца исследования (p<0,001). Установленный антидепрессивный эффект Вальдоксана согласуется с результатами предыдущих исследований. В этом исследовании Вальдоксан редуцировал симптомы тревоги. Анксиолитический эффект препарата также был показан в предыдущем исследовании, в котором Вальдоксан 25–50 мг/сут обеспечивал редукцию баллов шкалы тревоги Гамильтона у пациентов с генерализованным тревожным расстройством. Полученные нами данные о положительном влиянии Вальдоксана на сон согласуются с результатами предыдущих исследований, в которых Вальдоксан в дозах 25–50 мг/сут обеспечивал более выраженное улучшение субъективных параметров сна в сравнении с венлафаксином и был сопоставим по эффективности с ребоксетином. Вальдоксан представляется эффективным средством монотерапии БДР у пациентов, участвовавших в данном исследовании. Это подтверждается оценками самих пациентов и исследователей. Более того, отмечалось достоверное улучшение индекса КЖ на протяжении всего исследования (p<0,001). Как и в предыдущих исследованиях, нами зафиксировано раннее развитие эффекта и нарастание редукции баллов депрессии после увеличения дозы Вальдоксана. Такая стратегия терапии представляется клинически ценной для пациентов с недостаточным ранним эффектом терапии, а результаты ее применения подчеркивают важность гибкого режима дозирования. Кроме того, в нашем исследовании показано, что Вальдоксан обладает благоприятным профилем переносимости и безопасен в применении. Более того, Вальдоксан обеспечивает значимую редукцию ангедонии. Это первое исследование, в котором изучалась эффективность Вальдоксана в этой симптоматической категории. Термин «ангедония», впервые предложенный Ribot (1896 г.), определяет неспособность испытывать удовольствие. Ангедония соотносится с симптомами различных психических расстройств и личностными чертами. Ангедония имеет ключевое значение для диагностики депрессии и считается потенциальным маркером личностного индивидуального предрасположения к депрессии, злоупотреблению алкоголем и психоактивными веществами. Эта гипотеза подтверждается данными ряда исследований, в которых показано, что ангедония может предшествовать развитию депрессии, коррелирует с неудовлетворительным прогнозом через 12 мес, относится к типичным резидуальным симптомам после терапии и связана с дисфункцией системы подкрепления в головном мозге. Таким образом, эффективность Вальдоксана в отношении ангедонии может иметь особое значение для терапии пациентов с явлениями ангедонии. Новейший антидепрессант Вальдоксан, агонист мелатонинергических MT1/MT2-рецепторов и антагонист 5HT2C-рецепторов, обнаруживает антидепрессивный эффект и обладает благоприятным профилем переносимости, обеспечивающим высокую приверженность пациентов терапии. Однако следует соблюдать осторожность в сопоставлении наших данных с результатами предыдущих исследований в связи со значительными методологическими различиями. Основными недостатками данного исследования являются малый объем выборки и, что более важно, отсутствие контрольной группы и открытый (не двойной слепой) метод терапии. Для уточнения места Вальдоксана в современной фармакотерапии депрессивных расстройств требуются дополнительные сравнительные исследования с более длительными периодами терапии.21 декабря 2012
Количество просмотров: 2383



