Психиатрия Дневник психиатра (психиатрическая газета)

Психиатрия Дневник психиатра (психиатрическая газета)
№03 2013
Экстрапирамидные побочные эффекты нейролептиков: классификация и современные способы коррекции №03 2013
Номера страниц в выпуске:16-19

Нейролептики, или антипсихотические средства, составляют одну из главных групп современных психотропных средств и занимают центральное место в клинической психофармакологии. К нейролептическим средствам относятся препараты различных химических групп, обладающие рядом общих психофармакологических свойств. Эти свойства были наиболее полно сформулированы J.Delay и P.Deniker (1961 г.):
1) психолептическое действие без снотворного эффекта;
2) купирующее действие в отношении разных видов возбуждения, включая и маниакальное;
3) редуцирующее влияние на некоторые острые, хронические и экспериментальные психозы;
4) способность вызывать характерные неврологические и вегетативные нарушения;
5) преобладающее воздействие на подкорковые структуры центральной нервной системы (ЦНС).
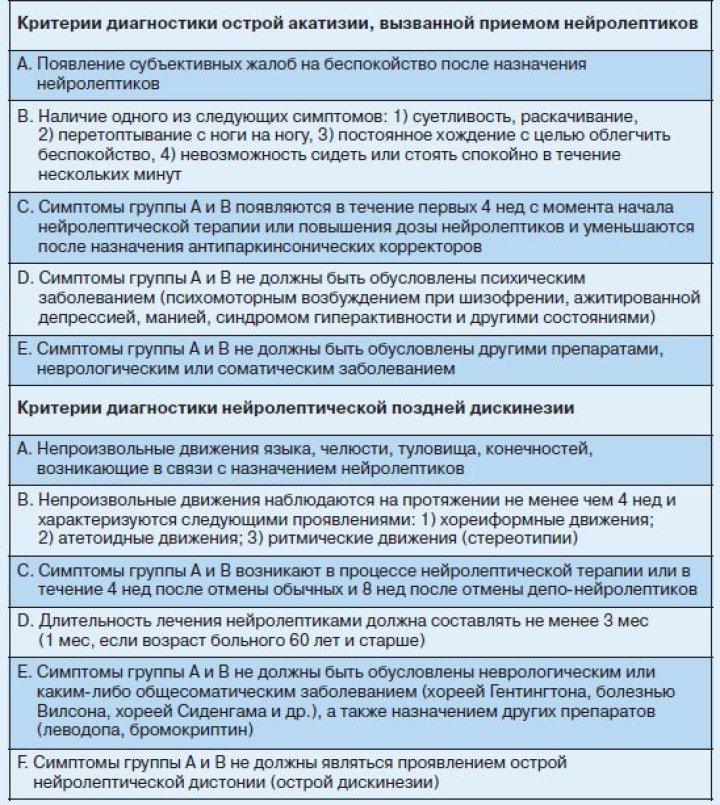
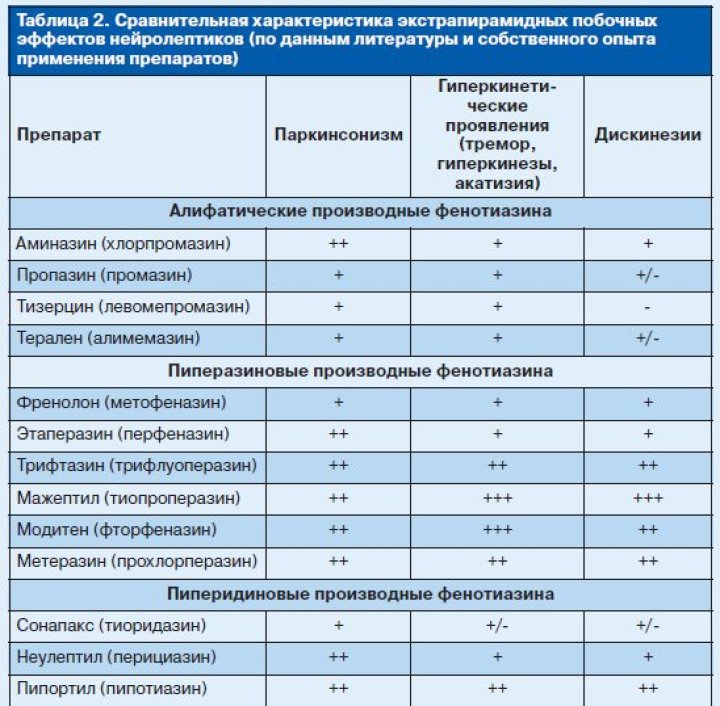
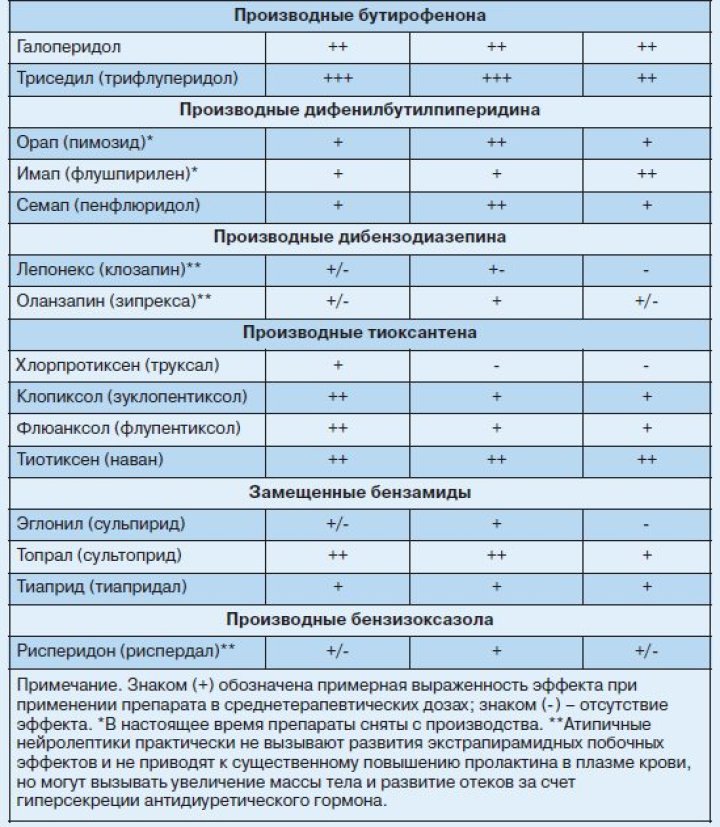
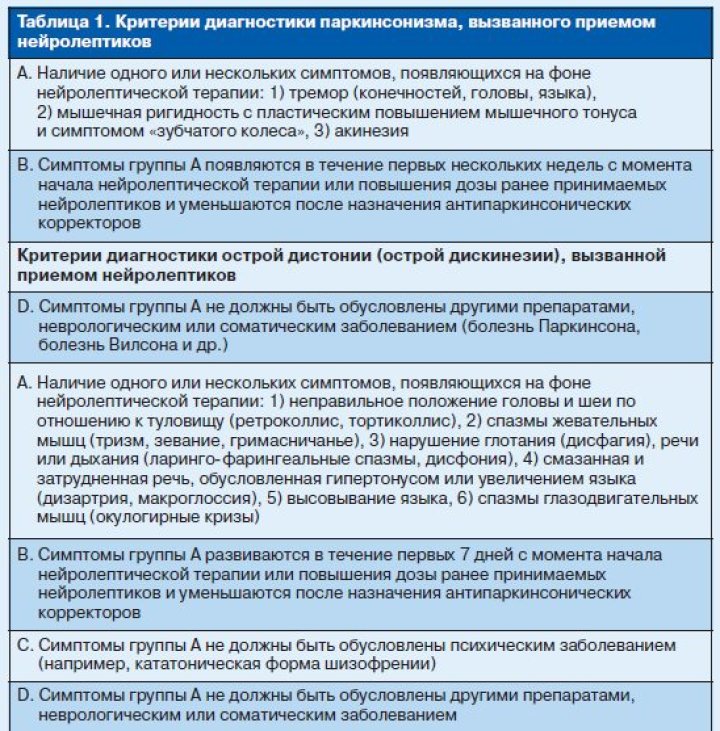
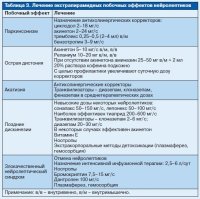
Позднее А.Carlsson и соавт. (1963–1987) показали, что особенности клинического действия нейролептиков обусловлены их общими нейрохимическими свойствами, заключающимися в способности избирательно блокировать дофаминовые D2-рецепторы различных отделов мозга (стриатум, прилежащее ядро, кора мозга) с подавлением центральной дофаминергической передачи и развивающимся компенсаторно увеличением скорости биосинтеза и метаболизма дофамина в соответствующих структурах мозга. Развитие побочных неврологических эффектов классических нейролептиков связано с блокадой дофаминовых D2-рецепторов в нигростриальной системе мозга. Главным отличием нейролептиков нового поколения (рисполепт, зипрекса и др.) является то, что они не вызывают (или почти не вызывают) экстрапирамидных побочных эффектов. Это свойство определяется спектром их нейрохимической активности. Атипичные нейролептики обладают избирательностью действия по отношению к мезолимбической и мезокортикальной дофаминергической системе мозга и менее выраженным влиянием на нигростриальную систему. Кроме того, атипичные нейролептики помимо блокады дофаминовых рецепторов одновременно блокируют 5НТ2-серотониновые рецепторы. Взаимоотношениям между блокадой дофаминовых и серотониновых рецепторов отводится важная роль в механизме действия атипичных нейролептиков. Установлено, что блокада 5НТ2-серотониновых рецепторов приводит к компенсаторному повышению концентрации дофамина в нигростриальной системе и тем самым уменьшает выраженность экстрапирамидных побочных эффектов, обусловленных дофаминблокирующей активностью этих нейролептиков. В соответствии с классификацией DSM-IV все экстрапирамидные двигательные расстройства, связанные с приемом нейролептиков, можно разделить на паркинсонизм, острую дистонию, острую акатизию и поздние дискинезии. Критерии диагностики экстрапирамидных нейролептических расстройств по DSM-IV представлены в табл. 1. Разные нейролептики обладают разной экстрапирамидной активностью. Установлено, что способность классических нейролептиков вызывать экстрапирамидные расстройства возрастает с известной закономерностью от алифатических к пиперазиновым производным фенотиазина и к бутирофенонам. При этом изменяется характер побочных экстрапирамидных эффектов – от преобладающего акинеторигидного синдрома к гиперкинетическому и дискинетическому синдрому. Атипичные нейролептики обладают дозозависимым эффектом в плане влияния на развитие экстрапирамидных расстройств. В среднетерапевтических дозах рисполепт и зипрекса вызывают появление экстрапирамидных симптомов с той же частотой, что и плацебо. По мере увеличения дозировок (рисполепт более 6 мг/сут и зипрекса более 10 мг/сут) частота развития экстрапирамидных побочных эффектов превышает плацебо, но значительно уступает галоперидолу. Исключение, по нашим данным, могут представлять больные шизофренией с явлениями резидуальной церебральной органической недостаточности, у которых даже невысокие дозы препаратов могут вызывать появление экстрапирамидных расстройств. Сравнительная характеристика экстрапирамидных побочных эффектов нейролептиков представлена в табл. 2. Нейролептический паркинсонизм возникает более чем в 50% случаев при лечении классическими нейролептиками в течение первых недель с момента начала нейролептической терапии или повышения дозы ранее принимаемых нейролептиков и характеризуется появлением общей скованности с характерной позой с согнутыми в локтях и приведенными к туловищу руками, тремором конечностей, акатизией и сопровождающими их вегетативными нарушениями (сальностью лица, потливостью, себореей). Мышечный тонус повышен по пластическому типу с симптомом «зубчатого колеса». Могут наблюдаться различные гиперкинезы, которые не являются стойкими. Лечение. Как правило, экстрапирамидная симптоматика редуцируется после назначения антипаркинсонических корректоров – циклодола, акинетона и др. (табл. 3). У больных с резидуальной церебральной органической недостаточностью экстрапирамидная симптоматика может приобретать затяжное течение – «затяжной экстрапирамидный синдром» по И.Я.Гуровичу. В этих случаях назначают высокие дозы антипаркинсонических корректоров в сочетании с ноотропами, уменьшают дозу принимаемых нейролептиков, назначают препараты с минимальной экстрапирамидной активностью (см. табл. 2). Наши исследования показали, что при тяжелом, затяжном течении экстрапирамидного нейролептического синдрома эффективным является проведение экстракорпоральных методов детоксикации – плазмафереза и гемосорбции.


Острые дистонии (или ранние дискинезии) возникают в 25–75% случаев в первые 7–10 дней с момента начала терапии классическими нейролептиками или повышения дозы ранее принимаемых препаратов и характеризуются внезапным появлением двигательных нарушений спастического тетаноформного характера. Моторные нарушения могут быть локальными и возникать в типичных областях, затрагивая изолированную группу мышц, или генерализованными, сопровождающимися общим моторным возбуждением с аффектами страха, тревоги, сужением сознания и вегетативными расстройствами (профузный пот, гиперсаливация, слезотечение, вазомоторные реакции и др.). При локальных дистониях возникают судороги языка, тризм, гиперкинезы мимической мускулатуры, спазмы взора (окулогирные кризы), кривошея, опистотонус, диспноэ и др. Описан также оральный синдром (Kulenkampff–Tarnow), который проявляется неожиданным тоническим сокращением мышц шеи, рта, высовыванием языка, нарушением фонации и дыхания. В некоторых случаях эти симптомы могут быть расценены как проявления эпилепсии или инфекционных заболеваний ЦНС (менингита, энцефалита и др.). Лечение. При развитии локальных дистоний наиболее эффективным является внутримышечное или внутривенное введение акинетона в дозе 5 мг. При отсутствии препарата дистонические реакции можно купировать аминазином в дозе 25–50 мг внутримышечно и 2 мл 20% раствора кофеина подкожно. При генерализованных дистониях показано одновременное назначение аминазина или тизерцина в дозе до 50 мг внутримышечно и антипаркинсонических корректоров (акинетона 5 мг внутримышечно). Острые дистонии можно купировать назначением диазепама (реланиума) в дозе 20 мг внутривенно медленно или внутримышечно. Для предупреждения повторного развития дискинезий назначают антипаркинсонические корректоры или увеличивают их дозу. Акатизия возникает в течение первых 4 нед с момента начала нейролептической терапии или повышения дозы нейролептиков и характеризуется появлением жалоб на беспокойство, неусидчивость, потребность двигаться, менять положение тела. Больные становятся суетливыми, перетоптываются с ноги на ногу, вынуждены постоянно ходить, для того чтобы облегчить беспокойство, не могут сидеть или стоять на месте в течение нескольких минут. Акатизия может сочетаться с нейролептическим паркинсонизмом. Описаны также редкие «поздние» случаи акатизии, при которых не наблюдается быстрой реакции на назначение антипаркинсонических корректоров и уменьшение дозы нейролептиков. Эти случаи трудно отличить от поздних дискинезий. Лечение. Антипаркинсонические корректоры циклодол, акинетон и др. Эффективно также назначение транквилизаторов – диазепама, клоназепама, феназепама в среднетерапевтических дозах.
Поздние дискинезии являются одними из наиболее тяжелых неврологических осложнений нейролептической терапии и развиваются у 20–30% больных, постоянно принимающих классические нейролептики. Частота развития поздних дискинезий у лиц молодого возраста, принимающих нейролептическую терапию в течение года, составляет 5%, у пожилых – 25–30%. При лечении атипичными нейролептиками (рисполепт, зипрекса) поздние дискинезии развиваются значительно реже. Так, согласно некоторым исследованиям, при лечении рисполептом в течение года поздние дискинезии были отмечены у 0,23% больных. Двигательные нарушения при поздних дискинезиях должны сохраняться на протяжении более чем 4 нед после отмены нейролептической терапии. Они могут возникать на фоне длительного приема нейролептических средств или появляться в течение первых 4 нед после отмены обычных нейролептиков и 8 нед после отмены нейролептиков пролонгированного действия. Клиническая картина этого осложнения характеризуется постепенным развитием разнообразных гиперкинезов (оральных, атетоидных, хореиформных, торсионно-дистонических) с тенденцией к их генерализации. В других случаях гиперкинезы могут появляться после внезапного прекращения приема нейролептиков. Часто гиперкинезы усиливаются в перерывах между курсами терапии, в то время как другие экстрапирамидные расстройства подвергаются обратному развитию. Одновременно с неврологическими стойкие изменения возникают и в психической сфере. Их совокупность описана как проявления психофармакотоксической энцефалопатии. Они характеризуются пассивностью больных, повышенной психофизической истощаемостью, аффективной неустойчивостью, замедлением интеллектуальных процессов, назойливостью, а также явлениями «истеризации» психики с тенденцией к демонстративному усилению имеющихся дискинезий.
Лечение. При появлении первых признаков развития поздних дискинезий необходима отмена нейролептиков (при условии, что это позволяет сделать психическое состояние больного). В тех случаях, когда терапию прекратить нельзя, предпочтение следует отдавать атипичным нейролептикам (азалептину, рисполепту, зипрексе), при которых риск развития осложнения существенно ниже. Установлено, что в 1/2 случаев поздние дискинезии проходят после прекращения приема препаратов. При этом после отмены нейролептиков дискинезии могут обостриться, а улучшение состояния во многих случаях наступает в течение нескольких месяцев. Для уменьшения дискинезий эффективным является применение антиоксиданта a-токоферола (витамина Е). В связи с наличием у многих больных церебральной органической недостаточности в схему терапии должны включаться препараты нейрометаболического действия (ноотропил, пикамилон, пантогам, фенибут и др.), методы общеукрепляющей и физиотерапии. Рекомендуется также баклофен 15–30 мг/сут, вальпроат натрия 400–600 мг/сут. Если дискинезии не исчезают, то больным назначают нейролептики в невысоких дозах – сонапакс 50–150 мг/сут, лепонекс 50–100 мг/сут. Наиболее эффективным является применение тиапридала 200–600 мг/сут. Рекомендуется также прием бензодиазепинов – диазепама 10–30 мг/сут, клоназепама 2–6 мг/сут. Применение антипаркинсонических корректоров с центральной холинолитической активностью при хроническом экстрапирамидном нейролептическом синдроме оказывается малоэффективным. Некоторое уменьшение выраженности дискинезий можно добиться при применении акинетона, который, по нашему мнению, по сравнению с другими антипаркинсоническими препаратами более эффективно действует на гиперкинетические проявления. Кроме того, наличие ампулированной формы позволяет использовать акинетон для парентерального – внутримышечного и внутривенного капельного введения, что усиливает терапевтический эффект. Некоторые авторы отмечают возможность усиления дискинезий при применении антихолинергических корректоров. Наши исследования показали, что антихолинергические корректоры оказывают положительный эффект, если одновременно с дискинезиями наблюдаются явления паркинсонизма в виде амиостатического симптомокомплекса с пластическим повышением мышечного тонуса. Предполагается, что развитие дискинезий связано с гиперчувствительностью дофаминовых рецепторов. Не исключено, что в этот процесс могут вовлекаться аутоиммунные механизмы. В последнее время было установлено, что аутоиммунный процесс может затрагивать непосредственно структуры дофаминовой системы на уровне дофаминовых рецепторов с образованием антирецепторных антител со стимулирующим и блокирующим действием. С этих позиций теоретически оправданным может быть применение методов экстракорпоральной детоксикации, оказывающих детоксикационное и иммунокорригирующее действие. Результаты собственных исследований показали, что после проведения плазмафереза и гемосорбции одновременно с уменьшением двигательных нарушений наблюдается улучшение психического и общего физического состояния – уменьшение вялости, апатии, повышение активности, улучшение сна, аппетита. Таким образом, вместе с экстрапирамидной симптоматикой редукции подвергаются и проявления психоорганического синдрома. Профилактика осложнения должна строиться на основе учета факторов риска. Установлено, что поздние дискинезии возникают наиболее часто при следующих предрасполагающих факторах:
• Наличие церебральной органической недостаточности.
• Пожилой возраст.
• Длительность применения высоких доз нейролептиков, особенно пиперазиновых производных фенотиазина и бутирофенонов.
• Склонность к развитию массивной экстрапирамидной симптоматики с преобладанием затяжных гиперкинезов. При наличии указанных факторов, особенно при их сочетании, терапию следует проводить с особой осторожностью, учитывая возможности возникновения осложнения.