Психиатрия Дневник психиатра (психиатрическая газета)
 Удивительный и неожиданный синергизм антагонистического действия на серотонинергические 5HT2C-рецепторы и агонистического действия на мелатонинергические рецепторы Вальдоксана (действующее вещество – агомелатин), препар
Удивительный и неожиданный синергизм антагонистического действия на серотонинергические 5HT2C-рецепторы и агонистического действия на мелатонинергические рецепторы Вальдоксана (действующее вещество – агомелатин), препар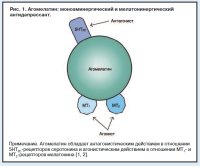 ата, обладающего обоими этими свойствами.
ата, обладающего обоими этими свойствами.
коре.
2. Стимуляция мелатонинергических MT1- и MT2-рецепторов вызывает синхронизацию циркадианных ритмов.
3. Комбинация 5HT2C-антагонизма с MT1- и MT2-агонизмом проявляется в неожиданном синергическом действии, включающем большее высвобождение дофамина и норэпинефрина в префронтальной коре, чем в случае только 5HT2C-антагонизма, а также несколько действий, не отмечаемых при воздействии на эти рецепторы по отдельности, включающих увеличение количества нейротрофического фактора головного мозга (BDNF) в префронтальной коре и редукцию вызванного стрессом высвобождения глутамата в миндалевидном
теле.
4. Теоретически этот синергизм может объяснять антидепрессивное действие моноаминергического/мелатонинергического препарата Вальдоксан и лежать в основе его уникального клинического профиля.Новый антидепрессант Вальдоксан («Лаборатории Сервье», Франция), представленный на рынке многих стран, обладает отличным от других антидепрессантов механизмом действия [1, 2]. В нем сочетается антагонистическое действие на серотонинергические 5HT2C-рецепторы и агонистическое действие на мелатонинергические MT1- и MT2- (рис. 1). Отсутствуют данные об эффективности при депрессии каждого из этих механизмов в отдельности, но доказано антидепрессивное действие их комбинации в одной молекуле Вальдоксана [1–4]. инефрина в префронтальной коре (рис. 2, a) [1]. При блокаде 5HT2C-рецепторов в префронтальной коре растормаживается высвобождение дофамина и норэпинефрина, что приводит к повышению их уровня (рис. 2, б). 5HT2C-антагонистическое действие является одним из множественных фармакологических свойств многих антидепрессантов и других психо-тропных препаратов и таким образом может вносить вклад в антидепрессивное действие кветиапина, оланзапина, миртазапина и, возможно, азенапина, некоторых трициклических антидепрессантов и других известных антидепрессантов [1].Обычно стимуляция мелатонинергических рецепторов приводит к развитию «ресинхронизирующего» действия на циркадианные ритмы [1, 2] без нарушения уровней моноаминов. Однако при комбинации MT1/MT2-стимуляции и 5HT2C-антагонизма в префронтальной коре отмечается поразительное и внезапное потенцирование высвобождения дофамина и норэпинефрина (рис. 3) [5]. Это не единственный пример синергизма между этими двумя механизмами. Случайное обнаружение синергизма между 5HT2C-антагонизмом и MT1/MT2-агонизмом продемонстрировано как для увеличения уровня нейротрофического фактора головного мозга – BDNF (рис. 4) [6], так и для блокирования вызванного стрессом высвобождения глутамата (рис. 5) [7].
инефрина в префронтальной коре (рис. 2, a) [1]. При блокаде 5HT2C-рецепторов в префронтальной коре растормаживается высвобождение дофамина и норэпинефрина, что приводит к повышению их уровня (рис. 2, б). 5HT2C-антагонистическое действие является одним из множественных фармакологических свойств многих антидепрессантов и других психо-тропных препаратов и таким образом может вносить вклад в антидепрессивное действие кветиапина, оланзапина, миртазапина и, возможно, азенапина, некоторых трициклических антидепрессантов и других известных антидепрессантов [1].Обычно стимуляция мелатонинергических рецепторов приводит к развитию «ресинхронизирующего» действия на циркадианные ритмы [1, 2] без нарушения уровней моноаминов. Однако при комбинации MT1/MT2-стимуляции и 5HT2C-антагонизма в префронтальной коре отмечается поразительное и внезапное потенцирование высвобождения дофамина и норэпинефрина (рис. 3) [5]. Это не единственный пример синергизма между этими двумя механизмами. Случайное обнаружение синергизма между 5HT2C-антагонизмом и MT1/MT2-агонизмом продемонстрировано как для увеличения уровня нейротрофического фактора головного мозга – BDNF (рис. 4) [6], так и для блокирования вызванного стрессом высвобождения глутамата (рис. 5) [7].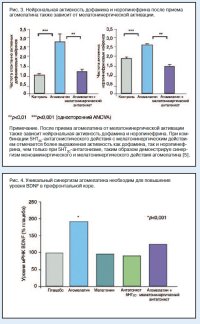
Как действует такой синергизм и каковы функциональные последствия комбинирования 5HT2C-антагонизма с MT1/MT2-агонизмом у пациентов с депрессией? Возможно, действие Вальдоксана специфическим образом нацелено на область супрахиазматического ядра, пейсмекера головного мозга, в котором происходит регуляция циркадианных ритмов и где представлены в большом количестве как 5HT2C-, так и MT1/MT2-рецепторы [1, 2].
Возможно, что раздельные действия в различных областях головного мозга также могут лежать в основе некоторых наблюдаемых видов фармакологического синергизма. Там, где эти различные рецепторы находятся в близком физическом контакте, существует даже возможность взаимодействия рецепторов в результате гетеродимеризации [2]. На сегодняшний день точный механизм синергизма одновременного действия на 5HT2C- и MT1/MT2-рецепторы остается в фазе активного исследования.
[1, 8]. Этот же факт теоретически может лежать в основе мощного действия Вальдоксана при лечении ангедонии [9], притупления эмоций [10], сонливости в течение дня [11], нарушения когнитивных функций, внимания и психомоторной заторможенности [12], которое не сопровождается развитием сексуальной дисфункции [13].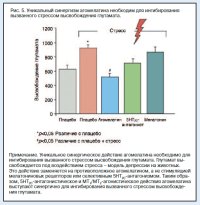
Такие клинические действия Вальдоксана при депрессии соотносятся с его известными фармакологическими действиями на дофамин и норэпинефрин (а не на серотонин), так как недостаток дофамина и норэпинефрина теоретически связан со «сниженным позитивным аффектом» [1, 8], а именно подавленным настроением, потерей ощущения счастья/веселья, удовольствия/интересов, энергии/энтузиазма, сниженной готовностью/когнитивным функционированием/вниманием/концентрацией и уверенностью в себе [8].
Клинические исследования действия Вальдоксана выявили улучшение позитивного аффекта [9–13], что отличает Вальдоксан от серотонинергических антидепрессантов, таких как селективные ингибиторы обратного захвата серотонина (СИОЗС) и ингибиторы обратного захвата серотонина и норэпинефрина (ИОЗСН), которые, в частности, не обладают мощным действием по восстановлению сниженного позитивного аффекта, но являются более стойкими в своем терапевтическом действии по снижению увеличенного негативного аффекта, наблюдаемого у некоторых пациентов с депрессией [1, 8], и включают вину/недовольство, страх/тревогу, враждебность, раздражительность и чувство одиночества [8].
Уникаьное синергическое действие агомелатина необходимо для увеличения уровня BDNF в префронтальной коре. Агомелатин повышает уровень нейротрофического фактора головного мозга (BDNF) в префронтальной коре. Этот уникальный результат достигается работой двух фармакологических механизмов агомелатина, так как уровень BDNF не повышается ни вследствие действия 5HT2C-антагониста, ни мелатонина, а влияние агомелатина на BDNF аннулируется действием антагониста мелатонина. Таким образом, 5HT2C-антагонистическое и МТ1/МТ2-агонистическое действия агомелатина являются синергическими для повышения BDNF в префронтальной коре.
Психиатрия Дневник психиатра (психиатрическая газета)
№03 2014
У наших друзей: Механизм действия Вальдоксана: инновационный антидепрессант, использующий синергизм между моноаминергическими и мелатонинергическими свойствами №03 2014
Номера страниц в выпуске:7-9
Удивительный и неожиданный синергизм антагонистического действия на серотонинергические 5HT2C-рецепторы и агонистического действия на мелатонинергические рецепторы Вальдоксана (действующее вещество – агомелатин), препарата, обладающего обоими этими свойствами.
 Удивительный и неожиданный синергизм антагонистического действия на серотонинергические 5HT2C-рецепторы и агонистического действия на мелатонинергические рецепторы Вальдоксана (действующее вещество – агомелатин), препар
Удивительный и неожиданный синергизм антагонистического действия на серотонинергические 5HT2C-рецепторы и агонистического действия на мелатонинергические рецепторы Вальдоксана (действующее вещество – агомелатин), препар ата, обладающего обоими этими свойствами.
ата, обладающего обоими этими свойствами.
Особенности синергизма:
1. Блокада серотонинергических 5HT2C-рецепторов приводит к повышенному высвобождению как дофамина, так и норэпинефрина в префронтальнойкоре.
2. Стимуляция мелатонинергических MT1- и MT2-рецепторов вызывает синхронизацию циркадианных ритмов.
3. Комбинация 5HT2C-антагонизма с MT1- и MT2-агонизмом проявляется в неожиданном синергическом действии, включающем большее высвобождение дофамина и норэпинефрина в префронтальной коре, чем в случае только 5HT2C-антагонизма, а также несколько действий, не отмечаемых при воздействии на эти рецепторы по отдельности, включающих увеличение количества нейротрофического фактора головного мозга (BDNF) в префронтальной коре и редукцию вызванного стрессом высвобождения глутамата в миндалевидном
теле.
4. Теоретически этот синергизм может объяснять антидепрессивное действие моноаминергического/мелатонинергического препарата Вальдоксан и лежать в основе его уникального клинического профиля.Новый антидепрессант Вальдоксан («Лаборатории Сервье», Франция), представленный на рынке многих стран, обладает отличным от других антидепрессантов механизмом действия [1, 2]. В нем сочетается антагонистическое действие на серотонинергические 5HT2C-рецепторы и агонистическое действие на мелатонинергические MT1- и MT2- (рис. 1). Отсутствуют данные об эффективности при депрессии каждого из этих механизмов в отдельности, но доказано антидепрессивное действие их комбинации в одной молекуле Вальдоксана [1–4].
Фармакологический синергизм Вальдоксана
В норме 5HT2C-рецепторы ингибируют нисходящее высвобождение дофамина и норэп инефрина в префронтальной коре (рис. 2, a) [1]. При блокаде 5HT2C-рецепторов в префронтальной коре растормаживается высвобождение дофамина и норэпинефрина, что приводит к повышению их уровня (рис. 2, б). 5HT2C-антагонистическое действие является одним из множественных фармакологических свойств многих антидепрессантов и других психо-тропных препаратов и таким образом может вносить вклад в антидепрессивное действие кветиапина, оланзапина, миртазапина и, возможно, азенапина, некоторых трициклических антидепрессантов и других известных антидепрессантов [1].Обычно стимуляция мелатонинергических рецепторов приводит к развитию «ресинхронизирующего» действия на циркадианные ритмы [1, 2] без нарушения уровней моноаминов. Однако при комбинации MT1/MT2-стимуляции и 5HT2C-антагонизма в префронтальной коре отмечается поразительное и внезапное потенцирование высвобождения дофамина и норэпинефрина (рис. 3) [5]. Это не единственный пример синергизма между этими двумя механизмами. Случайное обнаружение синергизма между 5HT2C-антагонизмом и MT1/MT2-агонизмом продемонстрировано как для увеличения уровня нейротрофического фактора головного мозга – BDNF (рис. 4) [6], так и для блокирования вызванного стрессом высвобождения глутамата (рис. 5) [7].
инефрина в префронтальной коре (рис. 2, a) [1]. При блокаде 5HT2C-рецепторов в префронтальной коре растормаживается высвобождение дофамина и норэпинефрина, что приводит к повышению их уровня (рис. 2, б). 5HT2C-антагонистическое действие является одним из множественных фармакологических свойств многих антидепрессантов и других психо-тропных препаратов и таким образом может вносить вклад в антидепрессивное действие кветиапина, оланзапина, миртазапина и, возможно, азенапина, некоторых трициклических антидепрессантов и других известных антидепрессантов [1].Обычно стимуляция мелатонинергических рецепторов приводит к развитию «ресинхронизирующего» действия на циркадианные ритмы [1, 2] без нарушения уровней моноаминов. Однако при комбинации MT1/MT2-стимуляции и 5HT2C-антагонизма в префронтальной коре отмечается поразительное и внезапное потенцирование высвобождения дофамина и норэпинефрина (рис. 3) [5]. Это не единственный пример синергизма между этими двумя механизмами. Случайное обнаружение синергизма между 5HT2C-антагонизмом и MT1/MT2-агонизмом продемонстрировано как для увеличения уровня нейротрофического фактора головного мозга – BDNF (рис. 4) [6], так и для блокирования вызванного стрессом высвобождения глутамата (рис. 5) [7].
Как действует такой синергизм и каковы функциональные последствия комбинирования 5HT2C-антагонизма с MT1/MT2-агонизмом у пациентов с депрессией? Возможно, действие Вальдоксана специфическим образом нацелено на область супрахиазматического ядра, пейсмекера головного мозга, в котором происходит регуляция циркадианных ритмов и где представлены в большом количестве как 5HT2C-, так и MT1/MT2-рецепторы [1, 2].
Возможно, что раздельные действия в различных областях головного мозга также могут лежать в основе некоторых наблюдаемых видов фармакологического синергизма. Там, где эти различные рецепторы находятся в близком физическом контакте, существует даже возможность взаимодействия рецепторов в результате гетеродимеризации [2]. На сегодняшний день точный механизм синергизма одновременного действия на 5HT2C- и MT1/MT2-рецепторы остается в фазе активного исследования.
Моноаминергический/мелатонинергический синергизм и клинический профиль Вальдоксана
Поскольку восстановление нейротрансмиссии дофамина и норэпинефрина выражается в антидепрессивном действии, этот факт может отчасти объяснять механизм антидепрессивного действия Вальдоксана, которое комбинирует 5HT2C-антагонизм с MT1/MT2-агонизмом (см. рис. 1)[1, 8]. Этот же факт теоретически может лежать в основе мощного действия Вальдоксана при лечении ангедонии [9], притупления эмоций [10], сонливости в течение дня [11], нарушения когнитивных функций, внимания и психомоторной заторможенности [12], которое не сопровождается развитием сексуальной дисфункции [13].

Такие клинические действия Вальдоксана при депрессии соотносятся с его известными фармакологическими действиями на дофамин и норэпинефрин (а не на серотонин), так как недостаток дофамина и норэпинефрина теоретически связан со «сниженным позитивным аффектом» [1, 8], а именно подавленным настроением, потерей ощущения счастья/веселья, удовольствия/интересов, энергии/энтузиазма, сниженной готовностью/когнитивным функционированием/вниманием/концентрацией и уверенностью в себе [8].
Клинические исследования действия Вальдоксана выявили улучшение позитивного аффекта [9–13], что отличает Вальдоксан от серотонинергических антидепрессантов, таких как селективные ингибиторы обратного захвата серотонина (СИОЗС) и ингибиторы обратного захвата серотонина и норэпинефрина (ИОЗСН), которые, в частности, не обладают мощным действием по восстановлению сниженного позитивного аффекта, но являются более стойкими в своем терапевтическом действии по снижению увеличенного негативного аффекта, наблюдаемого у некоторых пациентов с депрессией [1, 8], и включают вину/недовольство, страх/тревогу, враждебность, раздражительность и чувство одиночества [8].
Уникаьное синергическое действие агомелатина необходимо для увеличения уровня BDNF в префронтальной коре. Агомелатин повышает уровень нейротрофического фактора головного мозга (BDNF) в префронтальной коре. Этот уникальный результат достигается работой двух фармакологических механизмов агомелатина, так как уровень BDNF не повышается ни вследствие действия 5HT2C-антагониста, ни мелатонина, а влияние агомелатина на BDNF аннулируется действием антагониста мелатонина. Таким образом, 5HT2C-антагонистическое и МТ1/МТ2-агонистическое действия агомелатина являются синергическими для повышения BDNF в префронтальной коре.
Список исп. литературыСкрыть список1. Stahl SM. Stahl’s Essential Psychopharmacology. 4th ed. NY: Cambridge University Press, 2013.
2. De Bodinat C, Guardiola-Lemaitre B, Mocaer E. Agomelatine, the first melatonergic antidepressant: discovery, characterization and development. Nat Rev Drug Dis 2010; 9 (8): 928–42.
3. Zajecka J, Schatzberg A, Stahl S et al. Efficacy and safety of agomelatine in the treatment of major depressive disorder: a multicenter, randomized, double-blind, placebo-controlled trial. J Clin Psychopharmacol 2010; 30 (2): 135–44.
4. Stahl SM, Fava M, Trivedi M et al. Agomelatine in the treatment of major depressive disorder: an 8 week, multicenter, randomized, placebo-controlled trial. J Clin Psychiat 2010; 71 (5): 616–26.
5. Chenu F, El Mansari M, Blier P. Electrophysiological effects of repeated administration of agomelatine on the dopamine, norepinephrine and serotonin systems in the rat brain. Neuropsychopharmacol 2013; 38 (2): 275–84.
6. Molteni R, Calabrese F, Pisoni S et al. Synergistic mechanisms in the modulation of the neurotrophin BDNF in the rat prefrontal cortex following acute agomelatine. World
J Biol Psychiat 2010; 11 (2): 148–53.
7. Tardito D, Milanese M, Bonifacino T et al. Blockade of stress-induced increase of glutamate release in the rat prefrontal/frontal cortex by agomelatine involves synergy between melatonergic and 5-HT2C-receptordependent pathways. BMC Neurosci 2010; 11: 68.
8. Nutt D, Demyttenaere K, Janka Z et al. The other face of depression, reduced positive affect: the role of catecholamine’s in causation and cure. J Psychopharmacol 2007; 21 (5): 461–71.
9. Martinotti G, Sepede G, Gambi F et al. Agomelatine vs. venlafaxine XR in the treatment of anhedonia in major depressive disorder: a pilot study. J Clin Psychopharmacol 2012; 32 (4): 487–91.
10. Corruble E, de Bodinat C, Belaidi C, Goodwin GM. Agomelatine Study Group. Efficacy of agomelatine and escitalopram on depression, subjective sleep and emotional experiences in patients with major depressive disorder: a 24-week randomized, controlled, double-blind trial. Int J Neuropsychopharmacol 2013; 16 (10): 2219–34.
11. Lemoine P, Guilleminault C, Alvarez E. Improvement in subjective sleep in major depressive disorder with a novel antidepressant, agomelatine: randomized, double-blind comparison with venlafaxine.
J Clin Psychiat 2007; 68 (11): 1723–32.
12. Quera-Salva MA, Hajak G, Philip P et al. Comparison of agomelatine and escitalopram on nighttime sleep and daytime condition and efficacy in major depressive disorder patients. Int Clin Psychopharmacol 2011; 26 (5): 252–62.
13. Kennedy SH, Rizvi S, Fulton K, Rasmussen J. A double-blind comparison of sexual functioning, antidepressant efficacy and tolerability between agomelatine and venlafaxine XR. J Clin Psychopharmacol 2008; 28 (3): 329–33.
9 октября 2014
Количество просмотров: 3512


