Клинический разбор в акушерстве, гинекологии и репродуктологии №02 2021
Cervical intraepithelial neoplasia associated with human papillomavirus (clinical analysis)
Tatiana V. Klinyshkova
Omsk State Medical University, Omsk, Russia
klin_tatyana@mail.ru
Abstract
Cervical intraepithelial neoplasia (CIN) is the most relevant topic in cervicology due to the risk of progression to cervical cancer and its rejuvenation. The relationship of precancer with human papillomavirus (HPV) expands the range of examination in CIN. A clinical example of the management of a patient with CIN I is given. The significance of HPV infection risk factors and the possibility of CIN I progression, which led to a change in the planned management plan, is presented. Modern approaches to the diagnosis and management of patients with CIN I, including the possibilities of immunomorphology, are considered.
Key words: cervical intraepithelial neoplasia, human papillomavirus, liquid cytology, immunocytological examination, p16/Ki-67.
For citation: Klinyshkova Т.V. Cervical intraepithelial neoplasia associated with human papillomavirus (clinical analysis). Clinical case discussion in obstetrics, gynecology and reproductive medicine. 2021; 2: 33–36. DOI: 10.47407/kragr2021.1.2.00014
Цервикальная интраэпителиальная неоплазия (cervical intraepithelial neoplasia, CIN) является наиболее актуальной темой в цервикологии ввиду риска прогрессирования в рак шейки матки (РШМ) и его омоложением в последние годы. Последнее десятилетие характеризуется ежегодным увеличением числа пациенток, страдающих РШМ [1]. Заболеваемость РШМ на протяжении нескольких лет находится на 2-й позиции после рака тела матки в структуре раков гениталий в стране [2].
CIN этиологически взаимосвязана с папилломавирусной инфекцией или вирусом папилломы человека высокого риска (ВПЧ ВР). В связи с этим актуальным является как совершенствование методов диагностики цервикальной папилломавирусной инфекции, так и своевременное лечение пациенток с ВПЧ-ассоциированным предраком.
Клинический пример
Пациентка 26 лет обратилась на прием с профилактической целью.
Из анамнеза: менструальная функция не нарушена; половая жизнь с 15 лет, курит; имела хламидийную инфекцию, лечение с выздоровлением; дважды бактериальный вагиноз на протяжении последних 2 лет. В репродуктивном анамнезе один медицинский аборт без осложнений в 19 лет. Не в браке. Репродуктивных планов в ближайшее время не имеет.
По данным осмотра наружных гениталий и перианальной области патология не выявлена. В зеркалах слизистая влагалища обычной окраски, выявлена гиперемия шейки матки, тело матки и придатки не увеличены, безболезненны. Выделения светлые, умеренные.
Лабораторная диагностика: микроскопия мазков влагалищного отделяемого, цервикального канала и уретры в пределах нормы; жидкостная цитология шейки матки – LSIL (низкая степень плоскоклеточного интраэпителиального поражения); ВПЧ-тест на 14 типов Hybrid Capture – ВПЧ тип 58 (вирусная нагрузка 4,2×103 копий/100 тыс. клеток).
С учетом результата аномального цитологического мазка на фоне ВПЧ ВР выполнена расширенная кольпоскопия. Заключение: зона трансформации 1-го типа, аномальная кольпоскопическая картина 1-й степени (тонкий ацетобелый эпителий – АБЭ, очаги мозаики); рис. 1. Выполнена прицельная биопсия шейки матки. Результат гистологического исследования – CIN I.
Клинический диагноз: CIN I, ассоциированная с ВПЧ (тип 58).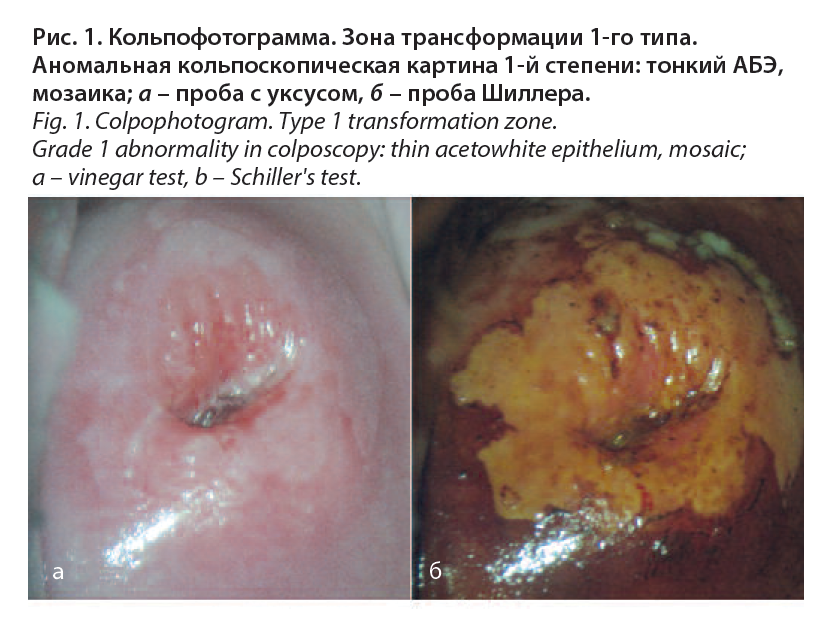
В соответствии с полученными данными была запланирована выжидательная тактика c динамическим наблюдением за состоянием шейки матки до 18 мес. Последующее обследование выполнялось каждые
6 мес. При первом цитологическом контроле (через 6 мес) – ASCUS (атипические клетки плоского эпителия неясного значения). Через 6 мес обратилась с жалобами на обильные выделения из половых путей с неприятным запахом. В зеркалах – обильные гомогенные светлые выделения, шейка матки гиперемирована вокруг зева. Тело матки и придатки не увеличены, безболезненны. В мазке на микроскопию – лейкоциты 2–3 (U), 10–15 (C), 15–20 в поле зрения (V); ключевые клетки. рН=6,0.
Клинический диагноз: рецидивирующий бактериальный вагиноз. CIN I, ассоциированная с ВПЧ ВР (тип 58).
Назначено местное двухэтапное лечение: клиндамицин 2% по 5,0 вагинально ежедневно 7 дней, Лактожиналь по 1 капсуле в день 14 дней. После клинического выздоровления по поводу бактериального вагиноза, подтвержденного отсутствием критериев Amsel, проведен второй цитологический контроль, результат – LSIL, койлоциты. Рекомендовано провести ВПЧ-тест, который был выполнен спустя 4 мес. Результат: ВПЧ 16 (вирусная нагрузка 3,9×102 копий/100 тыс. клеток) и ВПЧ 58 (вирусная нагрузка 6,2×103 копий/100 тыс. клеток).
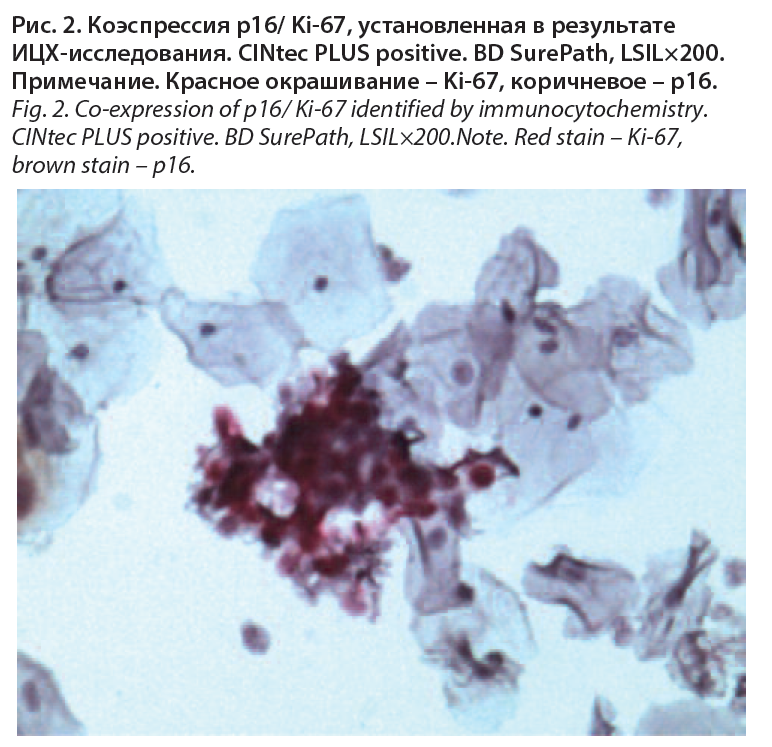
С учетом изменившейся картины по ВПЧ ВР, отсутствия регрессии LSIL при длительности наблюдения более 17 мес проведено иммуноцитохимическое (ИЦХ) исследование цервикального мазка (рис. 2). Результат ИЦХ-исследования – коэкспрессия р16/Ki-67. Повторная кольпоскопия – тонкий АБЭ с очагами плотного, мозаика. Выполнена биопсия, результат патологоанатомического исследования – СIN II.
Клинический диагноз: персистирующая форма сочетанной папилломавирусной инфекции. Прогрессирование CIN I. CIN II, ассоциированная с ВПЧ ВР (типы 16, 58).
Учитывая расхождение данных цитологии, кольпоскопии и гистологического исследования выбрана активная тактика в объеме радиоволновой эксцизии шейки матки в сочетании с противовирусным лечением: изопринозин внутрь по 1000 мг 3 раз в день в течение 10 дней, после отторжения струпа – Панавир вагинально №10. Результат гистологического исследования цервикального фрагмента CIN II совпал с данными биопсии. Через 6 мес после лечения получены следующие результаты обследования: жидкостная цитология – NILM (негативный в отношении интраэпителиального поражения и злокачественности), ВПЧ-тест – отрицательно.
Обсуждение
 Пациентка исходно имела факторы риска CIN: раннее начало половой жизни, инфекции, передаваемые половым путем (хламидийная инфекция), бактериальный вагиноз, курение, промискуитет. Обращает внимание отсутствие цитологического скрининга шейки матки до момента обращения. Цервикальный цитологический скрининг показан начиная с 21 года до 65 лет. В то же время проведение цитологического исследования микропрепарата шейки матки рекомендуется при обращении пациентки менее 21 года при половой жизни более 3 лет. В возрасте 21–29 лет цитологическое исследование микропрепарата шейки матки проводится не реже 1 раза в 3 года. В возрасте 30–65 лет цитологическое исследование рекомендовано не реже
Пациентка исходно имела факторы риска CIN: раннее начало половой жизни, инфекции, передаваемые половым путем (хламидийная инфекция), бактериальный вагиноз, курение, промискуитет. Обращает внимание отсутствие цитологического скрининга шейки матки до момента обращения. Цервикальный цитологический скрининг показан начиная с 21 года до 65 лет. В то же время проведение цитологического исследования микропрепарата шейки матки рекомендуется при обращении пациентки менее 21 года при половой жизни более 3 лет. В возрасте 21–29 лет цитологическое исследование микропрепарата шейки матки проводится не реже 1 раза в 3 года. В возрасте 30–65 лет цитологическое исследование рекомендовано не реже
1 раза в 5 лет.
Результаты цитологического исследования атипии многослойного плоского эпителия:
NILM – негативный в отношении интраэпителиального поражения и злокачественности;
ASCUS – атипические клетки плоского эпителия неясного значения;
ASC-Н – атипические клетки плоского эпителия, не позволяющие исключить НSIL;
LSIL – низкая степень плоскоклеточного интраэпителиального поражения;
НSIL – высокая степень плоскоклеточного интраэпителиального поражения.
Выявление аномального цитологического мазка (LSIL в данном случае) – основание для ВПЧ-теста. ВПЧ-тестирование рекомендуется при атипических результатах цитологических мазков, включая ASCUS, ASC-H, LSIL, AGC, AIS (по классификации Bethesda, 2015 г.), в то время как при HSIL необходимо провести срочную кольпоскопию. ВПЧ-тестирование целесообразно проводить всем женщинам в качестве скринингового метода с 30 лет в сочетании с цитологическим исследованием цервикального образца (co-test).
В соответствии с полученными данными у 26-летней нерожавшей c CIN I, была запланирована выжидательная тактика c динамическим наблюдением за состоянием шейки матки в течение 18–24 мес в виде цитологического контроля 1 раз в 6 мес и ВПЧ-тестирования 1 раз в 12 мес. Данный подход регламентирован действующими клиническими рекомендациями. В основе разработанной тактики лежит вероятность спонтанной элиминации ВПЧ при CIN I и регресс заболевания. Результаты регрессии описаны даже при CIN II: 44,1% поражений регрессировали без лечения в течение 12 мес наблюдения [3]. Вероятность спонтанной регрессии CIN II зависит от возраста. У женщин до 25 лет она наблюдается чаще – до 62% случаев за 8 мес [4].
Важно соблюдать последовательность алгоритма обследования при выборе выжидательной тактики.
В данном примере контрольный ВПЧ-тест проведен через 16 мес вместо 12 мес. С учетом выявленной коинфекции ВПЧ ВР (типы 16, 58) на фоне LSIL без регрессии и длительности наблюдения 17,5 мес выполнено ИЦХ-исследование, установившее коэкспрессию р16/Ki-67, что побудило заподозрить прогрессирование процесса. Данный результат согласуется с данными последующего гистологического исследования (CIN II), несмотря на цитологическое заключение LSIL, соответствующее CIN I. К факторам, ускоряющим прогрессирование CIN, можно отнести бактериальный вагиноз на фоне ВПЧ, который рецидивировал у пациентки через 1 год от начала наблюдения. Один из последних метаанализов подтверждает взаимосвязь ВПЧ-инфекции с бактериальным вагинозом (относительный риск – ОР 2,57, 95% доверительный интервал – ДИ 1,78–3,71, p<0,05), Chlamydia trachomatis (ОР 3,16, 95% ДИ 2,55–3,90, p<0,05) и Ureaplasma urealyticum (ОР 1,35, 95% ДИ 1,20–1,51, p<0,05). Наряду с этим, статистически значимо подтверждена связь бактериального вагиноза не только с ВПЧ-инфекцией, но и с CIN (ОР 1,56, 95% ДИ 1,21–2,00, p<0,05) [5].
ИЦХ-исследование является дополнительным морфологическим методом. Положительная экспрессия р16 и Ki67 при ASCUS, ASC-H и LSIL предполагает большую вероятность наличия HSIL, что нашло отражение в клинических рекомендациях. В настоящее время ИЦХ-исследование рекомендуется для выбора тактики при ASCUS и LSIL. Клиническая интерпретация теста двойного окрашивания р16/Ki-67 (белок контроля клеточного цикла и белок клеточной пролиферации соответственно) имеет следующее значение. При персистирующем течении инфекции, вызванной ВПЧ ВР, уровень экспрессии р16 возрастает, способствуя усилению пролиферации цервикального эпителия. Оценка уровня пролиферативного потенциала эпителия шейки матки на основании одновременного изучения экспрессии двух маркеров р16/Ki-67 позволяет прогнозировать течение папилломавирусной инфекции. При отсутствии экспрессии вероятность прогрессирования CIN I низкая, при положительном тесте – риск возрастает. По нашим данным, при CIN I частота коэкспрессии р16/Ki-67 в эпителиальных клетках в сравнении с женщинами без цервикальной патологии не имеет различий, однако случаи позитивного теста двойного окрашивания встречаются в каждом десятом случае (Клинышкова Т.В., 2021 в печати). Соответственно и тактика ведения таких пациенток должна быть скорректирована, поскольку выжидательная тактика на протяжении 24 мес представляет риск трансформации CIN I в CIN II еще до отведенного срока обследования в соответствие с алгоритмом.
По мнению С. Areán-Cuns и соавт., двойное окрашивание для p16/Ki-67 является более специфичным тестом, чем цитология для сортировки ВПЧ-позитивных женщин. Тест на p16/Ki67 обнаруживал двукратное преимущество в подтверждении CIN и рака в сравнении с цитологией по результатам исследования
ВПЧ-позитивных пациенток [6]. Появились также доказательства преимущества оценки p16/Ki-67 для детекции CIN II+/CINIII+ в сравнении с ВПЧ ВР – тестом среди пациенток с начальными признаками аномальных цитологических мазков, таких как ASC-US или LSIL [7].
ИЦХ-исследование целесообразно было сделать ранее, при повторном выявлении LSIL (2-й цитологический контроль). Наличие позитивного теста двойного окрашивания диктует целесообразность активной тактики ведения, учитывая риск прогрессирования CIN I. Объем хирургического лечения у нерожавшей выбран правильно, поскольку аблативные методы приемлемы только при CIN I. В действующих клинических рекомендациях 2020 г. и Национальном руководстве «Гинекология» отмечено, что хирургическое лечение показано при CIN II p16 позитивных. Динамическое наблюдение допустимо у женщин до 25 лет с диагнозом CIN II в биоптате при р16 – негативном результате иммуногистохимии с использованием цитологии,
ВПЧ-теста и кольпоскопии 1 раз в 6 мес в течение 2 лет.
В случае отсутствия регресса – активная тактика (эксцизия шейки матки). Медикаментозное лечение иммунотропными препаратами ВПЧ-инфекции, инициирующей и поддерживающей прогрессию CIN, патогенетически оправдано в качестве дополнения к эксцизионному лечению. В качестве медикаментозного компонента лечения возможно применение препаратов изопринозин, гроприносин, аллокин, панавир и др. [8–11]. Опыт применения изопринозина при CIN II свидетельствует о повышении эффективности лечения в 1,4 раза и элиминации ВПЧ (86,7%) в сравнении с традиционным лечением (без противовирусного компонента) (p<0,05) [9].
Заключение
Лечение CIN, ассоциированной с ВПЧ-инфекцией, требует индивидуального подхода с учетом стадии заболевания и факторов риска. На клиническом примере показана значимость факторов риска ВПЧ-инфекции и возможность прогрессирования в CIN II, что привело к изменению намеченного плана ведения. Наряду с традиционными методами диагностики внедрение в клиническую практику иммуноморфологических методов исследования позволяет своевременно разрабатывать наиболее рациональную тактику ведения при CIN. Отсутствие маркеров пролиферативной активности эпителия шейки матки при CIN I допускает возможность консервативного подхода, в то же время наличие экспрессии маркеров (р16-позитивный результат иммуногистохимии, p16/Ki-67-позитивный результат иммуноцитохимии) диктует целесообразность активной тактики ведения, учитывая риск прогрессирования CIN I. Ведение пациентов с CIN, включая объем, кратность обследования и вариант лечения, должно соответствовать клиническим рекомендациям, утвержденным Минздравом России.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Клинышкова Татьяна Владимировна – проф., д-р мед. наук, проф. каф. акушерства и гинекологии №1, ФГБОУ ВО ОмГМУ.
E-mail: klin_tatyana@mail.ru; ORCID: 0000-0002-0544-8184; Scopus Author ID: 55377219600
Tatiana V. Klinyshkova – D. Sci. (Med.), Full Prof., Omsk State Medical University. E-mail: klin_tatyana@mail.ru;
ORCID: 0000-0002-0544-8184; Scopus Author ID: 55377219600
Статья поступила в редакцию / The article received: 18.07.2021
Статья принята к печати / The article approved for publication: 05.08.2021
Клинический разбор в акушерстве, гинекологии и репродуктологии №02 2021
Цервикальная интраэпителиальная неоплазия, ассоциированная с вирусом папилломы человека (клинический разбор)
Аннотация
Цервикальная интраэпителиальная неоплазия (CIN) является наиболее актуальной темой в цервикологии ввиду риска прогрессирования в рак шейки матки и его омоложением в последние годы. Взаимосвязь предрака с вирусом папилломы человека расширяет диапазон обследования при CIN. Приведен клинический пример ведения пациентки с CIN I. Представлена значимость факторов риска
ВПЧ-инфекции и возможность прогрессирования CIN I, что привело к изменению намеченного плана ведения. Рассматриваются современные подходы к диагностике и ведению пациенток с CIN I, включая возможности иммуноморфологии.
Ключевые слова: цервикальная интраэпителиальная неоплазия, вирус папилломы человека, жидкостная цитология, иммуноцитохимическое исследование, p16/Ki-67.
Для цитирования: Клинышкова Т.В. Цервикальная интраэпителиальная неоплазия, ассоциированная с вирусом папилломы человека (клинический разбор). Клинический разбор в акушерстве, гинекологии и репродуктологии. 2021; 2: 33–36. DOI: 10.47407/kragr2021.1.2.00014
Цервикальная интраэпителиальная неоплазия (CIN) является наиболее актуальной темой в цервикологии ввиду риска прогрессирования в рак шейки матки и его омоложением в последние годы. Взаимосвязь предрака с вирусом папилломы человека расширяет диапазон обследования при CIN. Приведен клинический пример ведения пациентки с CIN I. Представлена значимость факторов риска
ВПЧ-инфекции и возможность прогрессирования CIN I, что привело к изменению намеченного плана ведения. Рассматриваются современные подходы к диагностике и ведению пациенток с CIN I, включая возможности иммуноморфологии.
Ключевые слова: цервикальная интраэпителиальная неоплазия, вирус папилломы человека, жидкостная цитология, иммуноцитохимическое исследование, p16/Ki-67.
Для цитирования: Клинышкова Т.В. Цервикальная интраэпителиальная неоплазия, ассоциированная с вирусом папилломы человека (клинический разбор). Клинический разбор в акушерстве, гинекологии и репродуктологии. 2021; 2: 33–36. DOI: 10.47407/kragr2021.1.2.00014
Cervical intraepithelial neoplasia associated with human papillomavirus (clinical analysis)
Tatiana V. Klinyshkova
Omsk State Medical University, Omsk, Russia
klin_tatyana@mail.ru
Abstract
Cervical intraepithelial neoplasia (CIN) is the most relevant topic in cervicology due to the risk of progression to cervical cancer and its rejuvenation. The relationship of precancer with human papillomavirus (HPV) expands the range of examination in CIN. A clinical example of the management of a patient with CIN I is given. The significance of HPV infection risk factors and the possibility of CIN I progression, which led to a change in the planned management plan, is presented. Modern approaches to the diagnosis and management of patients with CIN I, including the possibilities of immunomorphology, are considered.
Key words: cervical intraepithelial neoplasia, human papillomavirus, liquid cytology, immunocytological examination, p16/Ki-67.
For citation: Klinyshkova Т.V. Cervical intraepithelial neoplasia associated with human papillomavirus (clinical analysis). Clinical case discussion in obstetrics, gynecology and reproductive medicine. 2021; 2: 33–36. DOI: 10.47407/kragr2021.1.2.00014
Цервикальная интраэпителиальная неоплазия (cervical intraepithelial neoplasia, CIN) является наиболее актуальной темой в цервикологии ввиду риска прогрессирования в рак шейки матки (РШМ) и его омоложением в последние годы. Последнее десятилетие характеризуется ежегодным увеличением числа пациенток, страдающих РШМ [1]. Заболеваемость РШМ на протяжении нескольких лет находится на 2-й позиции после рака тела матки в структуре раков гениталий в стране [2].
CIN этиологически взаимосвязана с папилломавирусной инфекцией или вирусом папилломы человека высокого риска (ВПЧ ВР). В связи с этим актуальным является как совершенствование методов диагностики цервикальной папилломавирусной инфекции, так и своевременное лечение пациенток с ВПЧ-ассоциированным предраком.
Клинический пример
Пациентка 26 лет обратилась на прием с профилактической целью.
Из анамнеза: менструальная функция не нарушена; половая жизнь с 15 лет, курит; имела хламидийную инфекцию, лечение с выздоровлением; дважды бактериальный вагиноз на протяжении последних 2 лет. В репродуктивном анамнезе один медицинский аборт без осложнений в 19 лет. Не в браке. Репродуктивных планов в ближайшее время не имеет.
По данным осмотра наружных гениталий и перианальной области патология не выявлена. В зеркалах слизистая влагалища обычной окраски, выявлена гиперемия шейки матки, тело матки и придатки не увеличены, безболезненны. Выделения светлые, умеренные.
Лабораторная диагностика: микроскопия мазков влагалищного отделяемого, цервикального канала и уретры в пределах нормы; жидкостная цитология шейки матки – LSIL (низкая степень плоскоклеточного интраэпителиального поражения); ВПЧ-тест на 14 типов Hybrid Capture – ВПЧ тип 58 (вирусная нагрузка 4,2×103 копий/100 тыс. клеток).
С учетом результата аномального цитологического мазка на фоне ВПЧ ВР выполнена расширенная кольпоскопия. Заключение: зона трансформации 1-го типа, аномальная кольпоскопическая картина 1-й степени (тонкий ацетобелый эпителий – АБЭ, очаги мозаики); рис. 1. Выполнена прицельная биопсия шейки матки. Результат гистологического исследования – CIN I.
Клинический диагноз: CIN I, ассоциированная с ВПЧ (тип 58).
В соответствии с полученными данными была запланирована выжидательная тактика c динамическим наблюдением за состоянием шейки матки до 18 мес. Последующее обследование выполнялось каждые
6 мес. При первом цитологическом контроле (через 6 мес) – ASCUS (атипические клетки плоского эпителия неясного значения). Через 6 мес обратилась с жалобами на обильные выделения из половых путей с неприятным запахом. В зеркалах – обильные гомогенные светлые выделения, шейка матки гиперемирована вокруг зева. Тело матки и придатки не увеличены, безболезненны. В мазке на микроскопию – лейкоциты 2–3 (U), 10–15 (C), 15–20 в поле зрения (V); ключевые клетки. рН=6,0.
Клинический диагноз: рецидивирующий бактериальный вагиноз. CIN I, ассоциированная с ВПЧ ВР (тип 58).
Назначено местное двухэтапное лечение: клиндамицин 2% по 5,0 вагинально ежедневно 7 дней, Лактожиналь по 1 капсуле в день 14 дней. После клинического выздоровления по поводу бактериального вагиноза, подтвержденного отсутствием критериев Amsel, проведен второй цитологический контроль, результат – LSIL, койлоциты. Рекомендовано провести ВПЧ-тест, который был выполнен спустя 4 мес. Результат: ВПЧ 16 (вирусная нагрузка 3,9×102 копий/100 тыс. клеток) и ВПЧ 58 (вирусная нагрузка 6,2×103 копий/100 тыс. клеток).
С учетом изменившейся картины по ВПЧ ВР, отсутствия регрессии LSIL при длительности наблюдения более 17 мес проведено иммуноцитохимическое (ИЦХ) исследование цервикального мазка (рис. 2). Результат ИЦХ-исследования – коэкспрессия р16/Ki-67. Повторная кольпоскопия – тонкий АБЭ с очагами плотного, мозаика. Выполнена биопсия, результат патологоанатомического исследования – СIN II.
Клинический диагноз: персистирующая форма сочетанной папилломавирусной инфекции. Прогрессирование CIN I. CIN II, ассоциированная с ВПЧ ВР (типы 16, 58).
Учитывая расхождение данных цитологии, кольпоскопии и гистологического исследования выбрана активная тактика в объеме радиоволновой эксцизии шейки матки в сочетании с противовирусным лечением: изопринозин внутрь по 1000 мг 3 раз в день в течение 10 дней, после отторжения струпа – Панавир вагинально №10. Результат гистологического исследования цервикального фрагмента CIN II совпал с данными биопсии. Через 6 мес после лечения получены следующие результаты обследования: жидкостная цитология – NILM (негативный в отношении интраэпителиального поражения и злокачественности), ВПЧ-тест – отрицательно.
Обсуждение
1 раза в 5 лет.
Результаты цитологического исследования атипии многослойного плоского эпителия:
NILM – негативный в отношении интраэпителиального поражения и злокачественности;
ASCUS – атипические клетки плоского эпителия неясного значения;
ASC-Н – атипические клетки плоского эпителия, не позволяющие исключить НSIL;
LSIL – низкая степень плоскоклеточного интраэпителиального поражения;
НSIL – высокая степень плоскоклеточного интраэпителиального поражения.
Выявление аномального цитологического мазка (LSIL в данном случае) – основание для ВПЧ-теста. ВПЧ-тестирование рекомендуется при атипических результатах цитологических мазков, включая ASCUS, ASC-H, LSIL, AGC, AIS (по классификации Bethesda, 2015 г.), в то время как при HSIL необходимо провести срочную кольпоскопию. ВПЧ-тестирование целесообразно проводить всем женщинам в качестве скринингового метода с 30 лет в сочетании с цитологическим исследованием цервикального образца (co-test).
В соответствии с полученными данными у 26-летней нерожавшей c CIN I, была запланирована выжидательная тактика c динамическим наблюдением за состоянием шейки матки в течение 18–24 мес в виде цитологического контроля 1 раз в 6 мес и ВПЧ-тестирования 1 раз в 12 мес. Данный подход регламентирован действующими клиническими рекомендациями. В основе разработанной тактики лежит вероятность спонтанной элиминации ВПЧ при CIN I и регресс заболевания. Результаты регрессии описаны даже при CIN II: 44,1% поражений регрессировали без лечения в течение 12 мес наблюдения [3]. Вероятность спонтанной регрессии CIN II зависит от возраста. У женщин до 25 лет она наблюдается чаще – до 62% случаев за 8 мес [4].
Важно соблюдать последовательность алгоритма обследования при выборе выжидательной тактики.
В данном примере контрольный ВПЧ-тест проведен через 16 мес вместо 12 мес. С учетом выявленной коинфекции ВПЧ ВР (типы 16, 58) на фоне LSIL без регрессии и длительности наблюдения 17,5 мес выполнено ИЦХ-исследование, установившее коэкспрессию р16/Ki-67, что побудило заподозрить прогрессирование процесса. Данный результат согласуется с данными последующего гистологического исследования (CIN II), несмотря на цитологическое заключение LSIL, соответствующее CIN I. К факторам, ускоряющим прогрессирование CIN, можно отнести бактериальный вагиноз на фоне ВПЧ, который рецидивировал у пациентки через 1 год от начала наблюдения. Один из последних метаанализов подтверждает взаимосвязь ВПЧ-инфекции с бактериальным вагинозом (относительный риск – ОР 2,57, 95% доверительный интервал – ДИ 1,78–3,71, p<0,05), Chlamydia trachomatis (ОР 3,16, 95% ДИ 2,55–3,90, p<0,05) и Ureaplasma urealyticum (ОР 1,35, 95% ДИ 1,20–1,51, p<0,05). Наряду с этим, статистически значимо подтверждена связь бактериального вагиноза не только с ВПЧ-инфекцией, но и с CIN (ОР 1,56, 95% ДИ 1,21–2,00, p<0,05) [5].
ИЦХ-исследование является дополнительным морфологическим методом. Положительная экспрессия р16 и Ki67 при ASCUS, ASC-H и LSIL предполагает большую вероятность наличия HSIL, что нашло отражение в клинических рекомендациях. В настоящее время ИЦХ-исследование рекомендуется для выбора тактики при ASCUS и LSIL. Клиническая интерпретация теста двойного окрашивания р16/Ki-67 (белок контроля клеточного цикла и белок клеточной пролиферации соответственно) имеет следующее значение. При персистирующем течении инфекции, вызванной ВПЧ ВР, уровень экспрессии р16 возрастает, способствуя усилению пролиферации цервикального эпителия. Оценка уровня пролиферативного потенциала эпителия шейки матки на основании одновременного изучения экспрессии двух маркеров р16/Ki-67 позволяет прогнозировать течение папилломавирусной инфекции. При отсутствии экспрессии вероятность прогрессирования CIN I низкая, при положительном тесте – риск возрастает. По нашим данным, при CIN I частота коэкспрессии р16/Ki-67 в эпителиальных клетках в сравнении с женщинами без цервикальной патологии не имеет различий, однако случаи позитивного теста двойного окрашивания встречаются в каждом десятом случае (Клинышкова Т.В., 2021 в печати). Соответственно и тактика ведения таких пациенток должна быть скорректирована, поскольку выжидательная тактика на протяжении 24 мес представляет риск трансформации CIN I в CIN II еще до отведенного срока обследования в соответствие с алгоритмом.
По мнению С. Areán-Cuns и соавт., двойное окрашивание для p16/Ki-67 является более специфичным тестом, чем цитология для сортировки ВПЧ-позитивных женщин. Тест на p16/Ki67 обнаруживал двукратное преимущество в подтверждении CIN и рака в сравнении с цитологией по результатам исследования
ВПЧ-позитивных пациенток [6]. Появились также доказательства преимущества оценки p16/Ki-67 для детекции CIN II+/CINIII+ в сравнении с ВПЧ ВР – тестом среди пациенток с начальными признаками аномальных цитологических мазков, таких как ASC-US или LSIL [7].
ИЦХ-исследование целесообразно было сделать ранее, при повторном выявлении LSIL (2-й цитологический контроль). Наличие позитивного теста двойного окрашивания диктует целесообразность активной тактики ведения, учитывая риск прогрессирования CIN I. Объем хирургического лечения у нерожавшей выбран правильно, поскольку аблативные методы приемлемы только при CIN I. В действующих клинических рекомендациях 2020 г. и Национальном руководстве «Гинекология» отмечено, что хирургическое лечение показано при CIN II p16 позитивных. Динамическое наблюдение допустимо у женщин до 25 лет с диагнозом CIN II в биоптате при р16 – негативном результате иммуногистохимии с использованием цитологии,
ВПЧ-теста и кольпоскопии 1 раз в 6 мес в течение 2 лет.
В случае отсутствия регресса – активная тактика (эксцизия шейки матки). Медикаментозное лечение иммунотропными препаратами ВПЧ-инфекции, инициирующей и поддерживающей прогрессию CIN, патогенетически оправдано в качестве дополнения к эксцизионному лечению. В качестве медикаментозного компонента лечения возможно применение препаратов изопринозин, гроприносин, аллокин, панавир и др. [8–11]. Опыт применения изопринозина при CIN II свидетельствует о повышении эффективности лечения в 1,4 раза и элиминации ВПЧ (86,7%) в сравнении с традиционным лечением (без противовирусного компонента) (p<0,05) [9].
Заключение
Лечение CIN, ассоциированной с ВПЧ-инфекцией, требует индивидуального подхода с учетом стадии заболевания и факторов риска. На клиническом примере показана значимость факторов риска ВПЧ-инфекции и возможность прогрессирования в CIN II, что привело к изменению намеченного плана ведения. Наряду с традиционными методами диагностики внедрение в клиническую практику иммуноморфологических методов исследования позволяет своевременно разрабатывать наиболее рациональную тактику ведения при CIN. Отсутствие маркеров пролиферативной активности эпителия шейки матки при CIN I допускает возможность консервативного подхода, в то же время наличие экспрессии маркеров (р16-позитивный результат иммуногистохимии, p16/Ki-67-позитивный результат иммуноцитохимии) диктует целесообразность активной тактики ведения, учитывая риск прогрессирования CIN I. Ведение пациентов с CIN, включая объем, кратность обследования и вариант лечения, должно соответствовать клиническим рекомендациям, утвержденным Минздравом России.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Клинышкова Татьяна Владимировна – проф., д-р мед. наук, проф. каф. акушерства и гинекологии №1, ФГБОУ ВО ОмГМУ.
E-mail: klin_tatyana@mail.ru; ORCID: 0000-0002-0544-8184; Scopus Author ID: 55377219600
Tatiana V. Klinyshkova – D. Sci. (Med.), Full Prof., Omsk State Medical University. E-mail: klin_tatyana@mail.ru;
ORCID: 0000-0002-0544-8184; Scopus Author ID: 55377219600
Статья поступила в редакцию / The article received: 18.07.2021
Статья принята к печати / The article approved for publication: 05.08.2021