Клинический разбор в общей медицине №03 2021
Oksana V. Fesenko
Russian Medical Academy of Continuous Professional Education, Moscow, Russia
ofessenko@mail.ru
Abstract
Continuously increasing resistance of infectious agents together with rapid decrease in the number of novel antibacterial drugs makes the rational antibiotic selection one of the important challenges facing modern medicine. The urgency of the issue is also growing because of strategic and tactical mistakes in treatment of respiratory tract infections significantly affecting the disease outcome. The paper reports principles of respiratory tract infection antibiotic therapy based on contemporary federal guidelines on management of infectious respiratory tract diseases. Clinical example of rational antibiotic therapy selection in patient with community-acquired pneumonia is provided.
Key words: respiratory tract infections, community-acquired pneumonia, antibiotic therapy, resistance, rational antibiotic use.
For citation: Fesenko O.V. Principles of respiratory tract infection rational antibiotic therapy Clinical review for general practice. 2021; 3: 39–44. DOI: 10.47407/kr2021.2.3.00048
Клинический пример
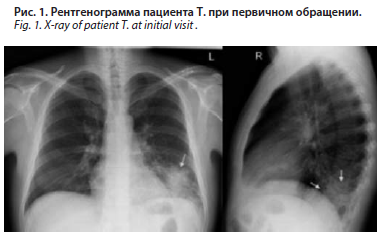 Пациент Т., 59 лет, обратился к терапевту с жалобами на кашель с желтой мокротой, повышение температуры тела до 37,8 °C, слабость.
Пациент Т., 59 лет, обратился к терапевту с жалобами на кашель с желтой мокротой, повышение температуры тела до 37,8 °C, слабость.
Из анамнеза известно, что заболел остро 4 дня назад, когда отметил повышение температуры тела до 37,5 °C. Самостоятельно принимал жаропонижающие препараты, однако температура не снижалась. Через 2 дня присоединились кашель и боль в грудной клетке слева при глубоком дыхании.
Пациент не курит, алкоголем не злоупотребляет. Профессиональных вредностей нет. Аллергоанамнез без особенностей.
В анамнезе: артериальная гипертензия и сахарный диабет 2-го типа (постоянно принимает глибенкламид).
При осмотре: состояние средней тяжести, температура тела 37,5° С. Частота дыхания 20 в минуту. При перкуссии – незначительное притуплении перкуторного звука в нижних отделах левого легкого. Дыхание везикулярное, слева в нижних отделах несколько ослаблено, там же выслушивается крепитация. Sat – 96%.
Тоны сердца приглушены, ритмичные. Пульс – 78 в минуту, артериальное давление – 130/80 мм рт. ст.
Клинический анализ крови: лейкоциты – 10,7×109/л, нейтрофилы сегментоядерные – 70%, нейтрофилы палочкоядерные – 4%, СОЭ – 28 мм/ч.
Биохимический анализ крови: глюкоза – 4,5 ммоль/л, С-реактивный белок – 115 мг/л, общий белок – 76 мг/л, креатинин – 81 мкмоль/л.
Анализ мочи – без особенностей.
При рентгенографии органов грудной клетки на фоне нормального легочного рисунка в нижних отделах левого легкого выявлено затенение (инфильтрация) легочной ткани (рис. 1).
Данные анамнеза, осмотра и выполненного обследования позволили установить диагноз: внебольничная пневмония нижней доли левого легкого нетяжелого течения неуточненной этиологии.
• установление точного диагноза;
• знание этиологии заболеваний;
• учет клинико-эпидемиологической ситуации в регионе (устойчивость возбудителя);
• учет роли индивидуальных факторов риска инфицирования резистентным возбудителем;
• оценка эффективности антибактериальной терапии;
• продолжительность антибактериальной терапии;
• соответствие проводимой антибактериальной терапии клиническим рекомендациям.

Ошибки могут быть обусловлены как неправильной трактовкой симптоматики, когда острая респираторная инфекция (ОРВИ) принимается за бактериальную инфекцию, так и стремлением не допустить бактериальное осложнение вирусной инфекции. Антибиотики не предотвращают бактериальную суперинфекцию, более того они способствуют селекции более агрессивных патогенов и развитию нежелательных побочных явлений. Следует всегда помнить, что нерациональное использование антибактериальной терапии имеет серьезные последствия [3].
Спектр антимикробной активности препарата в этом случае должен включать большинство вероятных бактериальных возбудителей инфекции данной локализации. В случае бактериальной инфекции дыхательных путей препарат должен проявлять активность в отношении наиболее частых возбудителей: Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Streptococcus pyogenes (табл. 1).
Учет клинико-эпидемиологической ситуации в регионе (устойчивость возбудителя)
Основным ограничением эффективности антимикробных препаратов является способность патогенных микроорганизмов формировать резистентность к их действию, что является серьезной проблемой [10, 11]. Этот процесс многократно ускоряется при необоснованном и избыточном применении антибиотиков в качестве средств профилактики, в том числе в последний год, с учетом возросшей частоты самолечения антибактериальными препаратами симптомов, свойственных новой вирусной инфекции COVID-19.
Важной проблемой является устойчивая тенденция увеличения доли резистентных штаммов пневмококков к β-лактамам и макролидам. Так, чувствительность пневмококков к пенициллину в последние годы снизилась до 96,3%, к цефтриаксону – до 91,9%. Согласно информации, полученной с помощью открытой онлайн-платформы анализа данных по резистентности к антибиотикам (AMRmap), в настоящее время в России при внебольничных инфекциях устойчивость пневмококков к современным макролидам уже превышает 30% [12].
Уровень устойчивости среди клинических штаммов H. influenzae к аминопенициллинам также возрастает, и, как показывают последние исследования, в России составляет 19% [13].
В настоящее время подавляющее большинство клинических изолятов M. catarrhalis продуцируют β-лактамазы, которые ингибируются клавулановой кислотой [14].
Факторы риска инфицирования лекарственно-устойчивыми возбудителями [15]:
• прием антибиотиков в течение предшествующих 3 мес;
• госпитализация в течение предшествующих 3 мес;
• пребывание в домах длительного ухода;
• лечение в дневных стационарах поликлиник;
• контакт с детьми, посещающими дошкольные учреждения;
• иммунодепрессивные заболевания/состояния;
• множественная коморбидность;
• хронические заболевания органов дыхания: бронхиальная астма, хроническая обструктивная болезнь легких (ХОБЛ);
• сахарный диабет;
• алкоголизм;
• лечение гемодиализом;
• недавние путешествия.
Ключевыми параметрами стратификации выступают: прием антибиотиков в течение последних трех месяцев и наличие сопутствующей патологии. Такой подход позволяет изначально сделать выбор в пользу препаратов, способных преодолеть возможные механизмы резистентности возбудителей [15].
Сохранение отдельных клинических, лабораторных или рентгенологических признаков пневмонии не является абсолютным показанием к продолжению антибактериальной терапии или ее модификации. В подавляющем большинстве случаев их разрешение происходит самостоятельно или под влиянием симптоматической терапии. Длительно сохраняющийся субфебрилитет не является признаком бактериальной инфекции. Рентгенологические проявления при пневмонии разрешаются медленнее клинических симптомов, поэтому контрольная рентгенография грудной клетки не может служить критерием для определения длительности антибактериальной терапии [17].
Во всем мире отмечается неуклонный рост резистентности бактериальных возбудителей к незащищенным аминопенициллинам. К настоящему времени эти препараты утратили свое значение в лечении многих инфекций, в этиологической структуре которых преобладают бактерии с высоким уровнем вторичной резистентности, прежде всего за счет продукции β-лактамаз. Это объясняется тем, что аминопенициллины, как и природные пенициллины, подвержены гидролизу всеми известными β-лактамазами. Незащищенные аминопенициллины могут рассматриваться в качестве препаратов стартовой терапии только у пациентов без факторов риска инфицирования лекарственно-устойчивыми возбудителями [19–24].
В клинических рекомендациях по лечению пневмонии у взрослых и детей отсутствуют некоторые пероральные цефалоспорины III поколения (Цефиксим, Цефтибутен). Всемирная организация здравоохранения не рекомендует использовать эти препараты для лечения респираторных инфекций, в связи с низкой активностью указанных препаратов в отношении пневмококка. Согласно заключению Европейского комитета по тестированию антимикробной чувствительности все штаммы пневмококка могут оцениваться как резистентные к цефиксиму без предварительного тестирования, поэтому определение чувствительности пневмококка к цефиксиму не рекомендуется [25, 26].
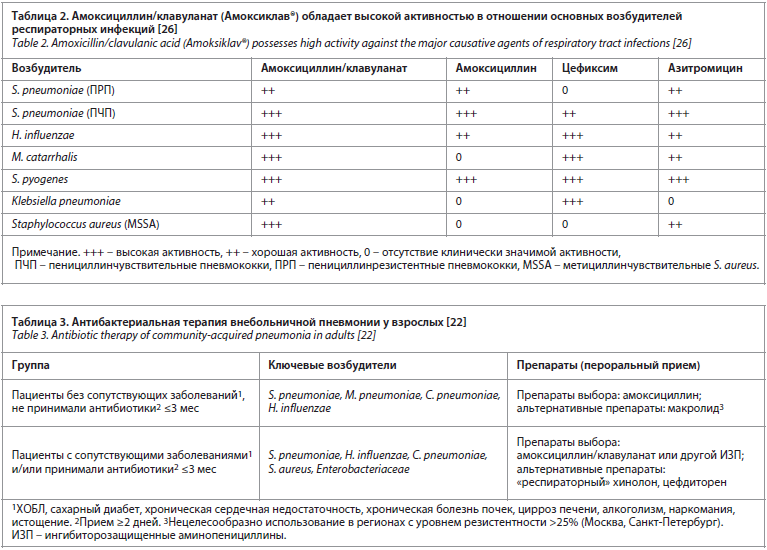
 В рекомендациях по лечению респираторных инфекций важное место занимает амоксициллин/клавуланат. Препарат обладает высокой стабильной активностью в отношении основных бактериальных возбудителей инфекций респираторной системы и ЛОР-органов: S. pneumoniae, S. aureus, H. influenzae, M. catarrhalis, анаэробов (табл. 2). Амоксициллин/клавуланат – препарат выбора у больных с фактором риска инфицирования лекарственно-устойчивыми возбудителями и/или высокой вероятностью участия β-лактамазпродуцирующих возбудителей [19–24].
В рекомендациях по лечению респираторных инфекций важное место занимает амоксициллин/клавуланат. Препарат обладает высокой стабильной активностью в отношении основных бактериальных возбудителей инфекций респираторной системы и ЛОР-органов: S. pneumoniae, S. aureus, H. influenzae, M. catarrhalis, анаэробов (табл. 2). Амоксициллин/клавуланат – препарат выбора у больных с фактором риска инфицирования лекарственно-устойчивыми возбудителями и/или высокой вероятностью участия β-лактамазпродуцирующих возбудителей [19–24].
Выбор антибактериальной терапии у пациента Т.
Основываясь на рекомендациях по ведению внебольничной пневмонии и учитывая наличие у больного сахарного диабета, являющегося фактором риска инфицирования лекарственно устойчивым возбудителем пневмонии, пациенту был назначен амоксициллин/клавуланат (Амоксиклав®) в дозе 1000 мг 2 раза в день (табл. 3) [22].
При осмотре через 3 дня отмечено улучшение состояния больного. Нормализовалась температура тела, исчезли слабость и боль в грудной клетке при дыхании, прекратился кашель. При аускультации – некоторое ослабление дыхания слева в нижних отделах.
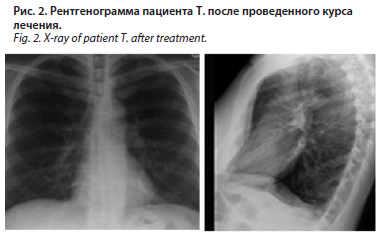
При рентгенографии органов грудной клетки, выполненной через 14 дней, отмечено отсутствие инфильтрации на фоне некоторого усиления легочного рисунка, корни легких структурны, синусы свободны (рис. 2).
Пациенту рекомендовано наблюдение участковым терапевтом, эндокринологом, пульмонологом в течение года, вакцинация против гриппа, пневмококка.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Информация об авторах / Information about the authors
Фесенко Оксана Вадимовна – д-р мед. наук, проф. каф. пульмонологии, ФГБОУ ДПО РМАНПО. Е-mail: ofessenko@mail.ru
Oksana V. Fesenko – D. Sci. (Med.), Prof., Russian Medical Academy of Continuous Professional Education. Е-mail: ofessenko@mail.ru
Статья поступила в редакцию / The article received: 27.04.2021
Статья принята к печати / The article approved for publication: 29.04.2021
Клинический разбор в общей медицине №03 2021
Принципы рациональной антибактериальной терапии респираторных инфекций
Номера страниц в выпуске:39-44
Аннотация
Продолжающийся рост устойчивости возбудителей инфекционных заболеваний и резкое уменьшение количества новых антибактериальных препаратов делает выбор рациональной антибиотикотерапии одной из актуальных проблем современной медицины. Актуальность данной проблемы возрастает и потому, что стратегические и тактические ошибки при лечении респираторных инфекций оказывают существенное влияние на его исход. В статье рассматриваются принципы антибактериальной терапии респираторных инфекций, основанные на современных федеральных рекомендациях по ведению инфекционных заболеваний дыхательных путей. Приведен клинический пример рационального выбора антибиотикотерапии у пациента с внебольничной пневмонией.
Ключевые слова: респираторные инфекции, внебольничная пневмония, антибактериальная терапия, резистентность, рациональное применение антибиотиков.
Для цитирования: Фесенко О.В. Принципы рациональной антибактериальной терапии респираторных инфекций. Клинический разбор в общей медицине. 2021; 3: 39–44. DOI: 10.47407/kr2021.2.3.00048
Продолжающийся рост устойчивости возбудителей инфекционных заболеваний и резкое уменьшение количества новых антибактериальных препаратов делает выбор рациональной антибиотикотерапии одной из актуальных проблем современной медицины. Актуальность данной проблемы возрастает и потому, что стратегические и тактические ошибки при лечении респираторных инфекций оказывают существенное влияние на его исход. В статье рассматриваются принципы антибактериальной терапии респираторных инфекций, основанные на современных федеральных рекомендациях по ведению инфекционных заболеваний дыхательных путей. Приведен клинический пример рационального выбора антибиотикотерапии у пациента с внебольничной пневмонией.
Ключевые слова: респираторные инфекции, внебольничная пневмония, антибактериальная терапия, резистентность, рациональное применение антибиотиков.
Для цитирования: Фесенко О.В. Принципы рациональной антибактериальной терапии респираторных инфекций. Клинический разбор в общей медицине. 2021; 3: 39–44. DOI: 10.47407/kr2021.2.3.00048
Principles of respiratory tract infection rational antibiotic therapy
Oksana V. Fesenko
Russian Medical Academy of Continuous Professional Education, Moscow, Russia
ofessenko@mail.ru
Abstract
Continuously increasing resistance of infectious agents together with rapid decrease in the number of novel antibacterial drugs makes the rational antibiotic selection one of the important challenges facing modern medicine. The urgency of the issue is also growing because of strategic and tactical mistakes in treatment of respiratory tract infections significantly affecting the disease outcome. The paper reports principles of respiratory tract infection antibiotic therapy based on contemporary federal guidelines on management of infectious respiratory tract diseases. Clinical example of rational antibiotic therapy selection in patient with community-acquired pneumonia is provided.
Key words: respiratory tract infections, community-acquired pneumonia, antibiotic therapy, resistance, rational antibiotic use.
For citation: Fesenko O.V. Principles of respiratory tract infection rational antibiotic therapy Clinical review for general practice. 2021; 3: 39–44. DOI: 10.47407/kr2021.2.3.00048
Введение
Современную терапию респираторных инфекций уже невозможно представить без назначения антибактериальных препаратов. Однако выбор антимикробного препарата в конкретной клинической ситуации нередко вызывает у врача много вопросов. Это связано с невозможностью в большинстве случаев этиологической расшифровки инфекционного процесса, меняющимися представлениями об этиологии инфекционно-воспалительных заболеваний дыхательных путей, ростом резистентности микроорганизмов. Затрудняют выбор антибиотика в ряде случаев и недостаточные знания практикующих врачей об особенностях фармакокинетики, спектрах антимикробной активности и токсичности современных антибактериальных препаратов. Согласно некоторым международным исследованиям более 60% назначений антибиотиков выполнено необоснованно или нерационально [1, 2], а стратегические и тактические ошибки при лечении респираторных инфекций оказывают существенное влияние на его исход.Клинический пример
 Пациент Т., 59 лет, обратился к терапевту с жалобами на кашель с желтой мокротой, повышение температуры тела до 37,8 °C, слабость.
Пациент Т., 59 лет, обратился к терапевту с жалобами на кашель с желтой мокротой, повышение температуры тела до 37,8 °C, слабость. Из анамнеза известно, что заболел остро 4 дня назад, когда отметил повышение температуры тела до 37,5 °C. Самостоятельно принимал жаропонижающие препараты, однако температура не снижалась. Через 2 дня присоединились кашель и боль в грудной клетке слева при глубоком дыхании.
Пациент не курит, алкоголем не злоупотребляет. Профессиональных вредностей нет. Аллергоанамнез без особенностей.
В анамнезе: артериальная гипертензия и сахарный диабет 2-го типа (постоянно принимает глибенкламид).
При осмотре: состояние средней тяжести, температура тела 37,5° С. Частота дыхания 20 в минуту. При перкуссии – незначительное притуплении перкуторного звука в нижних отделах левого легкого. Дыхание везикулярное, слева в нижних отделах несколько ослаблено, там же выслушивается крепитация. Sat – 96%.
Тоны сердца приглушены, ритмичные. Пульс – 78 в минуту, артериальное давление – 130/80 мм рт. ст.
Клинический анализ крови: лейкоциты – 10,7×109/л, нейтрофилы сегментоядерные – 70%, нейтрофилы палочкоядерные – 4%, СОЭ – 28 мм/ч.
Биохимический анализ крови: глюкоза – 4,5 ммоль/л, С-реактивный белок – 115 мг/л, общий белок – 76 мг/л, креатинин – 81 мкмоль/л.
Анализ мочи – без особенностей.
При рентгенографии органов грудной клетки на фоне нормального легочного рисунка в нижних отделах левого легкого выявлено затенение (инфильтрация) легочной ткани (рис. 1).
Данные анамнеза, осмотра и выполненного обследования позволили установить диагноз: внебольничная пневмония нижней доли левого легкого нетяжелого течения неуточненной этиологии.
Принципы выбора и проведения эффективной антибактериальной терапии
Для эффективной антибактериальной терапии врачу следует придерживаться основных принципов:• установление точного диагноза;
• знание этиологии заболеваний;
• учет клинико-эпидемиологической ситуации в регионе (устойчивость возбудителя);
• учет роли индивидуальных факторов риска инфицирования резистентным возбудителем;
• оценка эффективности антибактериальной терапии;
• продолжительность антибактериальной терапии;
• соответствие проводимой антибактериальной терапии клиническим рекомендациям.

Установление точного диагноза
Серьезной проблемой терапии инфекций верхних и нижних дыхательных путей является неоправданно частое назначение антимикробных препаратов без соответствующих показаний и, в первую очередь, их применение при вирусных инфекциях.Ошибки могут быть обусловлены как неправильной трактовкой симптоматики, когда острая респираторная инфекция (ОРВИ) принимается за бактериальную инфекцию, так и стремлением не допустить бактериальное осложнение вирусной инфекции. Антибиотики не предотвращают бактериальную суперинфекцию, более того они способствуют селекции более агрессивных патогенов и развитию нежелательных побочных явлений. Следует всегда помнить, что нерациональное использование антибактериальной терапии имеет серьезные последствия [3].
Знание этиологии заболеваний
Если бактериальная этиология заболевания высоковероятна, то следующим шагом является выбор препарата, активного в отношении потенциального возбудителя инфекционного заболевания. В подавляющем большинстве случаев антимикробная терапия назначается эмпирически, т.е. возбудитель и его чувствительность к антибиотикам не устанавливаются.Спектр антимикробной активности препарата в этом случае должен включать большинство вероятных бактериальных возбудителей инфекции данной локализации. В случае бактериальной инфекции дыхательных путей препарат должен проявлять активность в отношении наиболее частых возбудителей: Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Streptococcus pyogenes (табл. 1).
Учет клинико-эпидемиологической ситуации в регионе (устойчивость возбудителя)
Основным ограничением эффективности антимикробных препаратов является способность патогенных микроорганизмов формировать резистентность к их действию, что является серьезной проблемой [10, 11]. Этот процесс многократно ускоряется при необоснованном и избыточном применении антибиотиков в качестве средств профилактики, в том числе в последний год, с учетом возросшей частоты самолечения антибактериальными препаратами симптомов, свойственных новой вирусной инфекции COVID-19.
Важной проблемой является устойчивая тенденция увеличения доли резистентных штаммов пневмококков к β-лактамам и макролидам. Так, чувствительность пневмококков к пенициллину в последние годы снизилась до 96,3%, к цефтриаксону – до 91,9%. Согласно информации, полученной с помощью открытой онлайн-платформы анализа данных по резистентности к антибиотикам (AMRmap), в настоящее время в России при внебольничных инфекциях устойчивость пневмококков к современным макролидам уже превышает 30% [12].
Уровень устойчивости среди клинических штаммов H. influenzae к аминопенициллинам также возрастает, и, как показывают последние исследования, в России составляет 19% [13].
В настоящее время подавляющее большинство клинических изолятов M. catarrhalis продуцируют β-лактамазы, которые ингибируются клавулановой кислотой [14].
Роль индивидуальных факторов риска инфицирования резистентным возбудителем
Микробный пейзаж внебольничных инфекций может включать индивидуальные устойчивые штаммы микроорганизмов. Именно поэтому при выборе того или иного антибиотика необходимо прогнозировать риски наличия резистентных патогенов. Методология такого прогнозирования заключается в стратификации пациентов по факторам риска.Факторы риска инфицирования лекарственно-устойчивыми возбудителями [15]:
• прием антибиотиков в течение предшествующих 3 мес;
• госпитализация в течение предшествующих 3 мес;
• пребывание в домах длительного ухода;
• лечение в дневных стационарах поликлиник;
• контакт с детьми, посещающими дошкольные учреждения;
• иммунодепрессивные заболевания/состояния;
• множественная коморбидность;
• хронические заболевания органов дыхания: бронхиальная астма, хроническая обструктивная болезнь легких (ХОБЛ);
• сахарный диабет;
• алкоголизм;
• лечение гемодиализом;
• недавние путешествия.
Ключевыми параметрами стратификации выступают: прием антибиотиков в течение последних трех месяцев и наличие сопутствующей патологии. Такой подход позволяет изначально сделать выбор в пользу препаратов, способных преодолеть возможные механизмы резистентности возбудителей [15].
Оценка эффективности антибактериальной терапии
Первоначальная оценка эффективности терапии должна проводиться через 48–72 ч после начала лечения. Критериями эффективности в эти сроки являются снижение температуры, уменьшение симптомов интоксикации и других проявлений (например, одышки). Если у пациента сохраняются высокая лихорадка и интоксикация или симптоматика прогрессирует, лечение следует признать неэффективным. В этом случае необходимо пересмотреть тактику антибактериальной терапии и повторно оценить целесообразность госпитализации пациента [16].Продолжительность антибактериальной терапии
Оптимальная длительность лечения пациентов с респираторными инфекциями остается предметом обсуждения. Например, при нетяжелой внебольничной пневмонии ключевым критерием отмены антибактериальной терапии является стойкая нормализация температуры тела на протяжении 48–72 ч при положительной динамике других симптомов и отсутствии признаков клинической нестабильности. При таком подходе длительность лечения обычно не превышает 7 дней. К критериям адекватности антибактериальной терапии эксперты относят: стойкое снижение температуры тела ≤37,2 °C, отсутствие симптомов интоксикации, дыхательной недостаточности (частота дыхания менее 20 в минуту), гнойной мокроты, положительную динамику показателей периферической крови (количество лейкоцитов в крови <10×109/л, нейтрофилов <80%, юных форм <6%), а также отсутствие отрицательной динамики на рентгенограмме.Сохранение отдельных клинических, лабораторных или рентгенологических признаков пневмонии не является абсолютным показанием к продолжению антибактериальной терапии или ее модификации. В подавляющем большинстве случаев их разрешение происходит самостоятельно или под влиянием симптоматической терапии. Длительно сохраняющийся субфебрилитет не является признаком бактериальной инфекции. Рентгенологические проявления при пневмонии разрешаются медленнее клинических симптомов, поэтому контрольная рентгенография грудной клетки не может служить критерием для определения длительности антибактериальной терапии [17].
Соответствие проводимой антибактериальной терапии клиническим рекомендациям
Согласно федеральному закону №489-ФЗ от 25.12.2018, клинические рекомендации, утвержденные Минздравом России, являются обязательными при оказании медицинской помощи населению [18]. Качество лечения напрямую зависит от степени выполнения клинических рекомендаций.Во всем мире отмечается неуклонный рост резистентности бактериальных возбудителей к незащищенным аминопенициллинам. К настоящему времени эти препараты утратили свое значение в лечении многих инфекций, в этиологической структуре которых преобладают бактерии с высоким уровнем вторичной резистентности, прежде всего за счет продукции β-лактамаз. Это объясняется тем, что аминопенициллины, как и природные пенициллины, подвержены гидролизу всеми известными β-лактамазами. Незащищенные аминопенициллины могут рассматриваться в качестве препаратов стартовой терапии только у пациентов без факторов риска инфицирования лекарственно-устойчивыми возбудителями [19–24].
В клинических рекомендациях по лечению пневмонии у взрослых и детей отсутствуют некоторые пероральные цефалоспорины III поколения (Цефиксим, Цефтибутен). Всемирная организация здравоохранения не рекомендует использовать эти препараты для лечения респираторных инфекций, в связи с низкой активностью указанных препаратов в отношении пневмококка. Согласно заключению Европейского комитета по тестированию антимикробной чувствительности все штаммы пневмококка могут оцениваться как резистентные к цефиксиму без предварительного тестирования, поэтому определение чувствительности пневмококка к цефиксиму не рекомендуется [25, 26].

 В рекомендациях по лечению респираторных инфекций важное место занимает амоксициллин/клавуланат. Препарат обладает высокой стабильной активностью в отношении основных бактериальных возбудителей инфекций респираторной системы и ЛОР-органов: S. pneumoniae, S. aureus, H. influenzae, M. catarrhalis, анаэробов (табл. 2). Амоксициллин/клавуланат – препарат выбора у больных с фактором риска инфицирования лекарственно-устойчивыми возбудителями и/или высокой вероятностью участия β-лактамазпродуцирующих возбудителей [19–24].
В рекомендациях по лечению респираторных инфекций важное место занимает амоксициллин/клавуланат. Препарат обладает высокой стабильной активностью в отношении основных бактериальных возбудителей инфекций респираторной системы и ЛОР-органов: S. pneumoniae, S. aureus, H. influenzae, M. catarrhalis, анаэробов (табл. 2). Амоксициллин/клавуланат – препарат выбора у больных с фактором риска инфицирования лекарственно-устойчивыми возбудителями и/или высокой вероятностью участия β-лактамазпродуцирующих возбудителей [19–24].Выбор антибактериальной терапии у пациента Т.
Основываясь на рекомендациях по ведению внебольничной пневмонии и учитывая наличие у больного сахарного диабета, являющегося фактором риска инфицирования лекарственно устойчивым возбудителем пневмонии, пациенту был назначен амоксициллин/клавуланат (Амоксиклав®) в дозе 1000 мг 2 раза в день (табл. 3) [22].
При осмотре через 3 дня отмечено улучшение состояния больного. Нормализовалась температура тела, исчезли слабость и боль в грудной клетке при дыхании, прекратился кашель. При аускультации – некоторое ослабление дыхания слева в нижних отделах.
При рентгенографии органов грудной клетки, выполненной через 14 дней, отмечено отсутствие инфильтрации на фоне некоторого усиления легочного рисунка, корни легких структурны, синусы свободны (рис. 2).
Пациенту рекомендовано наблюдение участковым терапевтом, эндокринологом, пульмонологом в течение года, вакцинация против гриппа, пневмококка.
Заключение
Серьезными проблемами терапии инфекций верхних и нижних дыхательных путей является неоправданно частое назначение антимикробных препаратов без соответствующих показаний, что приводит к увеличению резистентности патогенных микроорганизмов. В связи с этим основными принципами рациональной антибактериальной терапии являются: точное установление диагноза, выбор стартового антибиотика с учетом возбудителя, учет уровня резистентности в стране и регионе, а также индивидуальных факторов риска инфицирования резистентными возбудителями. На эффективность антибактериальной терапии, несомненно, влияют соблюдение точной дозировки препарата, корректная оценка эффективности и продолжительности антимикробной терапии. Ведение пациентов с внебольничными инфекциями дыхательных путей должно соответствовать клиническим рекомендациям, утвержденным Минздравом России.Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Информация об авторах / Information about the authors
Фесенко Оксана Вадимовна – д-р мед. наук, проф. каф. пульмонологии, ФГБОУ ДПО РМАНПО. Е-mail: ofessenko@mail.ru
Oksana V. Fesenko – D. Sci. (Med.), Prof., Russian Medical Academy of Continuous Professional Education. Е-mail: ofessenko@mail.ru
Статья поступила в редакцию / The article received: 27.04.2021
Статья принята к печати / The article approved for publication: 29.04.2021
Список исп. литературыСкрыть список1. WHO Model List of Essential Medicines, 20th List (March 2017). The selection and use of essential medicines. Report of the WHO Expert Committee on Selection and Use of Essential Medicines, 2017 (including the 20th WHO Model List of Essential Medicines and the 6th WHO Model List of Essential Medicines for Children). www.who.int/medicines/publications/essentialmedicines/en
2. Fendrick AM, Monto AS, Nightengale B, Sarnes M. The economic burden of non-influenzarelated viral respiratory tract infection in the United States. Arch Intern Med 2003; 163 (4): 487–94.
3. Козлов Р.С., Голуб А.В. Остановить темпы роста антибиотикорезистентности микроорганизмов сегодня – дать шанс на выживание человечества завтра. Клиническая микробиология и антимикробная химиотерапия. 2019; 4: 310–3.
[Kozlov R.S., Golub A.V. To stop the progress of antimicrobial resistance today means to give a chance of mankind surviving tomorrow. Klinicheskaja mikrobiologija i antimikrobnaja himioterapija. 2019; 4: 310–3 (in Russian).]
4. O’Brien KL, Wolfson LJ, Watt JP et al. Burden of disease caused by Streptococcus pneumoniae in children younger than 5 years: global estimates. Lancet 2009; 374 (9693): 893–902. DOI: 10.1016/S0140- 6736(09)61204-6
5. Kolditz M, Tesch F, Mocke L et al. Burden and risk factors of ambulatory or hospitalized CAP: a population based cohort study. Respir Med 2016; 121: 32–8. DOI: 10.1016/j.rmed.2016.10.015
6. Zhang Z, Chen M, Yu Y et al. Antimicrobial susceptibility among Streptococcus pneumoniae and Haemophilus influenzae collected globally between 2015 and 2017 as part of the Tigecycline Evaluation and Surveillance Trial (TEST). Infect Drug Resist 2019; 12: 1209–20. DOI: 10.2147/IDR.S203121
7. Giufrè M, Fabiani M, Cardines R et al. Increasing trend in invasive non-typeable Haemophilus influenzae disease and molecular characterization of the isolates, Italy, 2012–2016. Vaccine 2018; 36 (45): 6615–22. DOI: 10.1016/j.vaccine.2018.09.060
8. Liapikou A, Torres A. The clinical management of lower respiratory tract infections. Expert Rev Respir Med 2016; 10: 441–52. DOI: 10.1586/17476348.2016.1156537
9. Handbook of microbiological media. Roland M. Atlas. 2nd ed. CRS Press, 1997.
10. One world, one fight! Antimicrob Resist Infect Control 2015; 4: 49. DOI: 10.1186/s13756-015-0091-2
11. Zumla A, Memish ZA, Maeurer M et al. Emerging novel and antimicrobial-resistant respiratory tract infections: new drug development and therapeutic options. Lancet Infect Dis 2014; 14: 1136–49. DOI: 10.1016/S1473-3099(14)70828-X
12. Кузьменков А.Ю., Трушин И.В., Авраменко А.А. и др. AMRmap: Интернет-платформа мониторинга антибиотикорезистентности. Клиническая микробиология и антимикробная химиотерапия. 2017; 19 (2): 84–90.
[Kuzmenkov A.Yu., Trushin I.V, Avramenko A.A. et al. AMRmap: an online platform for monitoring antibiotic resistance. Klinicheskaja mikrobiologija i antimikrobnaja himioterapija. 2017; 19 (2): 84–90 (in Russian).]
13. Torumkuney D et al. Results from the Survey of Antibiotic Resistance (SOAR) 2014–16 in Russia. J Antimicrob Chemother 2018; 73 (Suppl. 5): v14–v21.
14. Dabernat H, Delmas C. Epidemiology and evolution of antibiotic resistance of Heamophilus influenzae in children 5 years of age or less in France, 2001–2008: a retrospective database analysis. Eur J clin Microb Infect Dis 2012; 31 (10): 2745–53.
15. Эмпирическая антибактериальная терапия инфекций дыхательных путей с учетом факторов риска резистентной флоры. Резолюция совета экспертов. Справочник поликлинического врача. 2018; 1: 6–10.
[Empiricheskaia antibakterial'naia terapiia infektsii dykhatel'nykh putei s uchetom faktorov riska rezistentnoi flory. Rezoliutsiia soveta ekspertov. Spravochnik poliklinicheskogo vracha. 2018; 1: 6–10 (in Russian).]
16. Harris AM, Hicks LA, Qaseem A. Appropriate antibiotic use for acute respiratory tract infection in adults: advice for high-value care from the American College of Physicians and the Centers for Disease Control and Prevention. Ann Intern Med 2016; 164: 425–34. DOI: 10.7326/M15-1840
17. Респираторная медицина: руководство: в 3 т. Т. 2. Под ред.
А.Г. Чучалина. 2-е изд., перераб. и доп. М.: Литтерра, 2017.
[Respiratornaia meditsina: rukovodstvo: v 3 t. T. 2. Ed. A.G. Chuchalin. 2-e izd., pererab. i dop. Moscow: Litterra, 2017 (in Russian).]
18. Федеральный закон от 25 декабря 2018 г. №489-ФЗ «О внесении изменений в статью 40 Федерального закона «Об обязательном медицинском страховании в Российской Федерации» и Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» по вопросам клинических рекомендаций» Минздрава России. http://cr.rosminzdrav.ru/
[Federal'nyi zakon ot 25 dekabria 2018 g. №489-FZ "O vnesenii izmenenii v stat'iu 40 Federal'nogo zakona "Ob obiazatel'nom meditsinskom strakhovanii v Rossiiskoi Federatsii' i Federal'nyi zakon "Ob osnovakh okhrany zdorov'ia grazhdan v Rossiiskoi Federatsii' po voprosam klinicheskikh rekomendatsii' Minzdrava Rossii. http://cr.rosminzdrav.ru/ (in Russian).]
19. Клинические рекомендации. Отит средний острый. Минздрав России. Национальная медицинская ассоциация оториноларингологов. М., 2016.
[Klinicheskie rekomendatsii. Otit srednii ostryi. Minzdrav Rossii. Natsional'naia meditsinskaia assotsiatsiia otorinolaringologov. Moscow, 2016 (in Russian).]
20. Клинические рекомендации. Острый синусит. Минздрав России. Национальная медицинская ассоциация оториноларингологов. М., 2016.
[Klinicheskie rekomendatsii. Ostryi sinusit. Minzdrav Rossii. Natsional'naia meditsinskaia assotsiatsiia otorinolaringologov. Moscow, 2016. (in Russian).]
21. Клинические рекомендации. Острый тонзиллофаринит. Минздрав России. Национальная медицинская ассоциация оториноларингологов. М., 2016.
[Klinicheskie rekomendatsii. Ostryi tonzillofarinit. Minzdrav Rossii. Natsional'naia meditsinskaia assotsiatsiia otorinolaringologov. Moscow, 2016 (in Russian).]
22. Федеральные клинические рекомендации. Внебольничная пневмония. Минздрав России. РРО. МАКМАХ. М., 2018.
[Federal'nye klinicheskie rekomendatsii. Vnebol'nichnaia pnevmoniia. Minzdrav Rossii. RRO. MAKMAKh. Moscow, 2018 (in Russian).]
23. Эмпирическая антибактериальная терапия инфекций дыхательных путей с учетом факторов риска резистентной флоры. Резолюция совета экспертов. Справочник поликлинического врача. 2018; 1: 6–10.
[Empiricheskaia antibakterial'naia terapiia infektsii dykhatel'nykh putei s uchetom faktorov riska rezistentnoi flory. Rezoliutsiia soveta ekspertov. Spravochnik poliklinicheskogo vracha. 2018; 1: 6–10 (in Russian).]
24. Федеральные клинические рекомендации. Хроническая обструктивная болезнь легких. Минздрав России. РРО. М., 2016.
[Federal'nye klinicheskie rekomendatsii. Khronicheskaia obstruktivnaia bolezn' legkikh. Minzdrav Rossii. RRO. Moscow, 2016 (in Russian).]
25. WHO Model List of Essential Medicines for Children. 6th List [updated 2017 March; cited 2017 Oct 9]. http://www.who.int/medicines/ publications/essentialmedicines/ 6th_EMLc2017.pdf
26. Справочник по антимикробной терапии. Выпуск 2. Под ред.
Р.С. Козлова, А.В. Дехнича. Смоленск: МАКМАХ, 2010.
[Spravochnik po antimikrobnoi terapii. Vypusk 2. Ed. R.S. Kozlov, A.V. Dekhnich. Smolensk: MAKMAKh, 2010 (in Russian).]
27. Веселов А.В. Амоксициллин/клавуланат: особенности фармакокинетики и фармакодинамики при терапии респираторных инфекций. Практическая пульмонология. 2008; 4: 33–6.
[Veselov A.V. Amoksitsillin/klavulanat: osobennosti farmakokinetiki i farmakodinamiki pri terapii respiratornykh infektsii. Prakticheskaia pul'monologiia. 2008; 4: 33–6 (in Russian).]


