Клинический разбор в общей медицине №06 2021
Burdenko national medical research centre for neurosurgery, Moscow, Russia
likhterman@nsi.ru
Abstract
Clinical and morphological forms of traumatic brain injury effects are reported, distinguished based on the results, obtained during years of research in the National Medical Research Center for Neurosurgery. Basic criteria are proposed for the diagnosis of those based on the neurological and instrumental examination data, mostly on the neuroimaging data (CT, MRI, angiography).
Key words: traumatic brain injury effects, clinical and morphological forms, neuroimaging diagnosis.
For citation: Likhterman L.B., Kravchuk A.D., Okhlopkov V.A. Theory about traumatic brain injury effects. Part II. Clinical and morphological forms of traumatic brain injury effects. Clinical review for general practice. 2021; 6: 23–34. DOI: 10.47407/kr2021.2.6.00077
Исходя из классификации последствий черепно-мозговой травмы (ЧМТ), изложенной в части I этой статьи, представляем конкретные их клинико-морфологические формы.
Атрофия мозга есть запущенный ЧМТ процесс уменьшения объема мозгового вещества (как серого, так и белого). В ее основе лежат, наряду с первичной гибелью клеток, последующие дегенеративно-деструктивно-дистрофические изменения: демиелинизация аксонов, ишемия, глиоз, уменьшение числа функционирующих капилляров, запустевание периваскулярных пространств и др. Различают диффузную и локальную посттравматическую атрофию. Ее развитие, характер и степень выраженности определяются биомеханикой и тяжестью ЧМТ, возрастом пострадавшего, его анамнезом, в частности дотравматической патологией, качеством лечения и другими факторами.
При диффузном аксональном повреждении обычно развивается диффузная атрофия вещества мозга. При очаговых повреждениях на фоне диффузной атрофии часто доминирует локальная атрофия (в зоне бывших очагов размозжения, внутримозговых гематом и др.). При посттравматической атрофии происходит расширение желудочков мозга и субарахноидальных пространств с заполнением их цереброспинальной жидкостью (ЦСЖ).
Первые признаки посттравматической атрофии могут обнаруживаться уже спустя 2–4 нед после ЧМТ.
В дальнейшем этот процесс либо останавливается, либо прогрессирует на протяжении длительного времени. Различают легкую, среднюю и тяжелую степени очаговой и диффузной посттравматической атрофии.
Следует отметить, что между морфологической выраженностью атрофии и ее клиническим выражением часто нет параллелизма. Симптоматика посттравматической диффузной атрофии мозга характеризуется нарастающим вплоть до деменции оскудением психической деятельности. Неврологически в далеко зашедших
стадиях доминирует двусторонняя мозжечковая и подкорковая симптоматика, включая псевдобульбарные парезы.
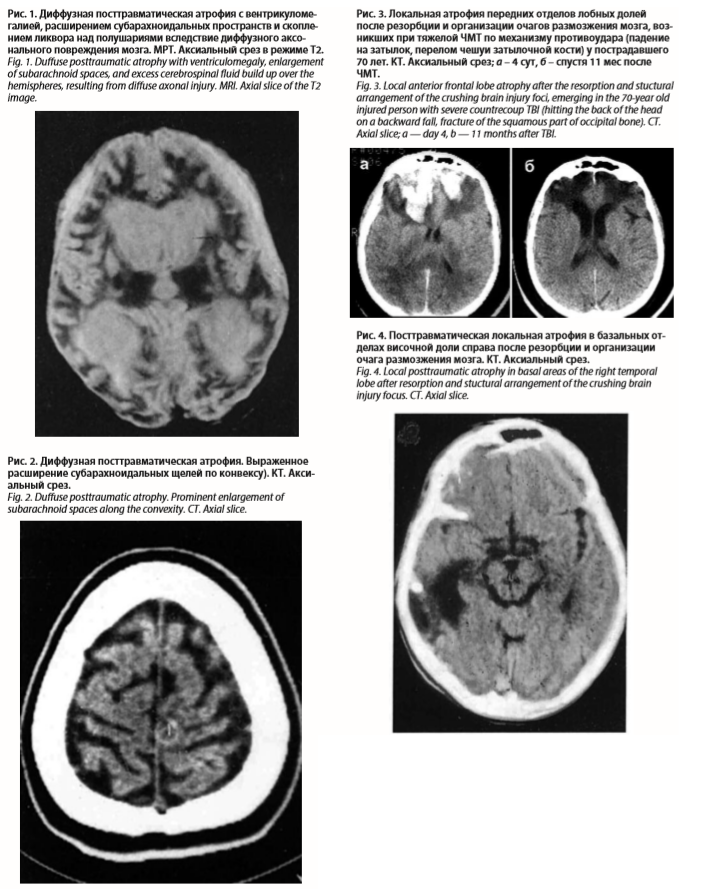
Сочетание на компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) одновременного и симметричного увеличения желудочков мозга и субарахноидальных пространств (по конвексу, межполушарных и боковых щелей), а также отсутствие перивентрикулярного отека однозначно свидетельствуют в пользу диффузной атрофии (рис. 1, 2).
Локальная посттравматическая атрофия мозга характеризуется разнообразием клинического проявления в зависимости от топики процесса. Вместе с тем, очевидная по данным КТ и МРТ локальная атрофия мозга (рис. 3, 4), может давать лишь минимальную симптоматику либо, нередко, в функциональном отношении быть полностью компенсированной.
Большую роль в патогенезе арахноидита, особенно при повторных ЧМТ или несостоятельности (по разным причинам) клеточных и гуморальных механизмов защиты, играют иммунные процессы и, прежде всего, аутосенсибилизация организма к мозгу за счет выработки антител к антигенам поврежденной мозговой ткани.
Паутинная оболочка из-за фиброза утолщается и уплотняется, из прозрачной становится серовато-белесоватой. Между ней и мягкой мозговой оболочкой возникают спайки и сращения. Нарушается циркуляция ЦСЖ с образованием различных по размерам кистеобразных расширений, увеличиваются размеры желудочков мозга.
В зависимости от соотношения спаечных и кистозных изменений выделяют слипчивый, кистозный и слипчиво-кистозный посттравматический арахноидит. Характерно ремиттирующее течение, когда экзацербация заболевания сменяется ремиссией различной продолжительности. На первый план в клинической картине выступают общемозговые симптомы: головная боль, имеющая оболочечно-сосудистую окраску, головокружение, тошнота, непереносимость резких раздражителей, общая слабость, быстрая утомляемость, физическая и психическая истощаемость и др. Обычно выражены астенические, эмоциональные и вегетативные расстройства.
Ведущими очаговыми признаками конвекситального арахноидита являются нарушения функций лобной, теменной или височной долей, часто в виде сочетания мягких симптомов выпадения и раздражения, эпилептические припадки.
Ведущими очаговыми признаками базального арахноидита являются нарушения функций черепных нервов, чаще зрительных, отводящих, тройничных и др. Посттравматический оптохиазмальный арахноидит характеризуется снижением остроты и изменением полей зрения. Отмечаются парацентральные и центральные скотомы, первичная и вторичная атрофия сосков зрительных нервов.
Ведущими очаговыми признаками арахноидита задней черепной ямки являются нарушения функций слухового нерва, особенно его вестибулярной порции, тройничного, отводящего и ряда других черепных нервов, а также мозжечковые симптомы. При окклюзирующих формах арахноидита задней черепной ямки на фоне гипертензионно-гидроцефальной симптоматики становятся грубыми нарушения статики и походки.
Клинический диагноз посттравматического арахноидита подтверждается характерными данными КТ или МРТ, обнаруживающими неравномерность субарахноидальных щелей по конвексу с кистозными расширениями либо их отсутствие обычно на фоне того или иного увеличения желудочков мозга.
Различают наружный (эпидуральный), внутренний (субдуральный) и смешанный (эпи-субдуральный) посттравматический пахименингит.
Характерным симптомом посттравматического пахименингита является локальная головная боль. При парабазальной его локализации отмечаются краниобазальные или орбитальные боли. Наблюдаются тошнота, рвота, брадикардия, что обусловлено раздражением окончаний тройничного нерва в ТМО. Могут проявляться: гиперемия и гипергидроз лица, асимметрия артериального давления, болезненность шейных точек вследствие ирритации вегетативных волокон в ТМО. Порой развиваются эпилептические припадки; судороги имеют очаговый или генерализованный характер. КТ или МРТ уточняют локализацию и распространенность посттравматического пахименингита, выявляя характерную протяженную зону повышенной плотности, прилежащую к внутренней поверхности костей черепа.
Оболочечно-мозговые рубцы формируются в месте повреждений костей черепа, оболочек и вещества мозга. Процесс организации оболочечно-мозговых рубцов начинается в остром, продолжается в промежуточном и завершается в отдаленном периодах ЧМТ.
В клинической картине при оболочечно-мозговых рубцах доминируют цефалгический и эпилептический синдромы (судорожные и бессудорожные пароксизмы), возможна психопатизация личности, метеопатизация, а также при дефектах костей – местные изменения часто с втянутостью мягких покровов головы.
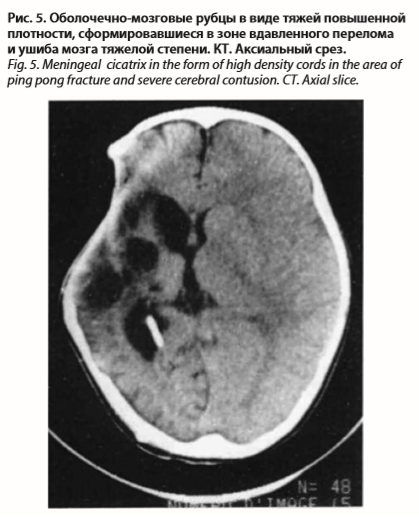
Диагноз оболочечно-мозгового рубца объективизируют КТ (рис. 5) и МРТ, выявляющие соответственно его локализации и размер мозаичных по плотности участков с преобладанием гиперденсивного компонента.
Клинически существенны (вплоть до главной причины инвалидизации пострадавших) одно- или двусторонние посттравматические парезы глазодвигательных нервов (III, IV, VI), которые возникают при переломах основания черепа (чаще на уровне средней черепной ямки).
Одно- или двусторонняя аносмия часто сопутствует очаговым повреждениям лобных долей и переломам решетчатой кости.
При переломах пирамиды височной кости наблюдаются периферические парезы лицевого, слухового и вкусового нервов. При переломах основания черепа, верхней и нижней челюсти нередко отмечаются поражение чувствительной и двигательной порции тройничного нерва. Непосредственное поражение корешков IX, X, XI, XII пар черепных нервов встречается редко. Поражение языкоглоточного и блуждающего нервов проявляется нарушениями глотания, голоса, речи.
Костные дефекты обусловлены ЧМТ с оскольчато-вдавленными и вдавленными переломами черепа, его повреждениями холодным оружием (топор, сабля и др.), огнестрельными ранениями. Все же чаще они являются следствием резекционной или декомпрессивной трепанации при вдавленных переломах, удалении внутричерепных гематом и др.
Размеры посттравматических дефектов черепа варьируют от малых (3–20 см2) до больших (60–80 см2 и более), захватывающих 2–3 соседние кости свода черепа.
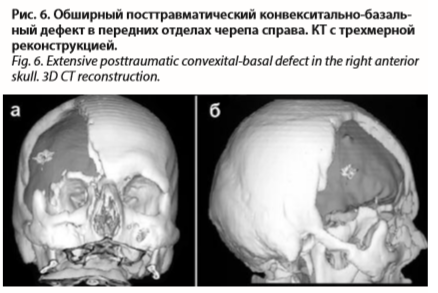
Клинически костные дефекты нередко проявляются синдромом трепанированного черепа: общие головные боли и местные боли в области дефекта, возникающие и/или усиливающиеся при изменении атмосферного давления, температуры окружающей среды; выпячивание содержимого черепа в дефект при кашле, чихании, наклоне головы, физическом напряжении и т.п. Характерны жалобы на боязнь повреждения мозга через дефект, чувство неполноценности, а также на косметические неудобства. Особенно тягостны для пострадавших обезображивающие их обширные кранио-орбито-базальные дефекты. Диагностика посттравматических дефектов черепа уточняется краниографически и КТ, в том числе с использованием трехмерной реконструкции (рис. 6).
Инородные тела, прежде всего, опасны как потенциальные очаги инфекции. Особого внимания заслуживают костные отломки, представляющие благоприятную среду для развития инфекции (менингита, энцефалита, абсцесса, гранулемы и др.). Кроме того, костные отломки поддерживают дегенеративные и рубцово-спаечные процессы в мозговой ткани.
В отдаленном периоде ЧМТ инородные тела могут клинически себя ничем не проявлять. Однако чаще обнаруживается разнообразная симптоматика в зависимости от локализации, размеров, количества инородных тел и других факторов.
При присоединении инфекции либо миграции инородных тел неврологическая картина усугубляется, симптомы раздражения часто сменяют симптомы выпадения мозговых функций.
Решающая роль в распознавании инородных тел принадлежит краниографии и КТ (рис. 8–10).
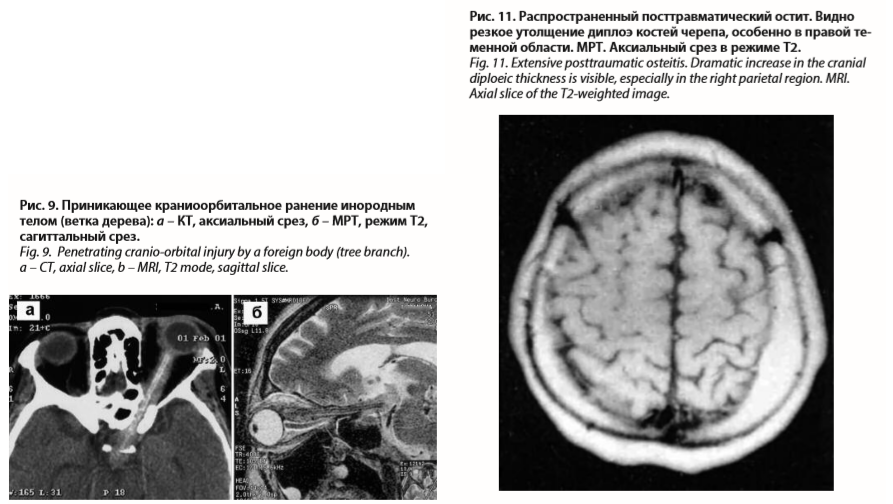
Наиболее информативные методы его диагностики – краниография и МРТ (рис. 11).
Посттравматическая гидроцефалия
Гидроцефалия – прогрессирующий процесс избыточного накопления жидкости в ликворных пространствах и веществе головного мозга вследствие ЧМТ, обусловленный нарушениями циркуляции и резорбции ЦСЖ и характеризующийся: морфологически – увеличением желудочковой системы, перивентрикулярным отеком и облитерацией субарахноидальных щелей; клинически – развитием определенного симптомокомплекса с доминированием психических (интеллектуально-мнестических) и атаксических расстройств. Следует дифференцировать активную посттравматическую гидроцефалию от совершенно различного по механизму пассивного процесса – увеличения размеров желудочков мозга и субарахноидальных пространств, заполняемых ЦСЖ вследствие посттравматической атрофии мозга.
Сроки развития посттравматической гидроцефалии широко варьируют – от одного месяца до года и больше. После тяжелой ЧМТ с очаговыми поражениями мозга развиваются различные формы гидроцефалии: нормотензивная, гипертензионная и окклюзионная; после диффузного аксонального повреждения мозга – нормотензивная гидроцефалия.
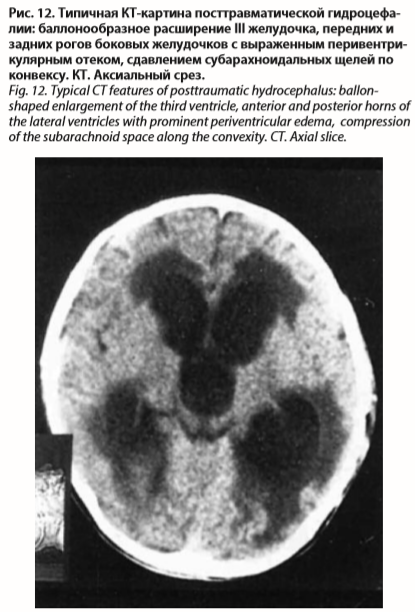
Характерным КТ-признаком посттравматической гидроцефалии является расширение боковых (преимущественно передних рогов) и III желудочков (рис. 12). Они приобретают «баллонообразную» форму за счет давления ЦСЖ изнутри. При этом обычно не визуализируются конвекситальные субарахнодальные щели, а также сужены базальные цистерны. К типичным симптомам посттравматической гидроцефалии относятся перивентрикулярный отек, возникающий вначале вокруг передних рогов и затем распространяющийся вдоль других отделов боковых желудочков. В зонах повреждения мозговой ткани возникают дивертикулы, порэнцефалические ходы и кистозные полости. Степень увеличения размеров желудочковой системы не всегда соответствует уровню инвалидизации больных, определяемому и другими последствиями перенесенной тяжелой ЧМТ. Одинаковая выраженность водянки мозга может наблюдаться у больных с умеренной и с грубой инвалидизацией, а также находящихся в вегетативном статусе.
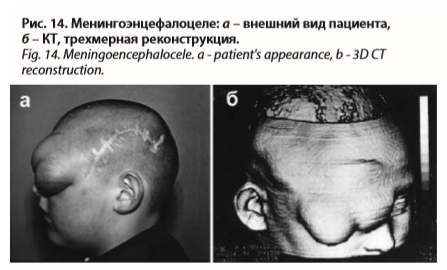
Если в посттравматический дефект черепа и ТМО выпячивается заполненный ЦСЖ грыжевой мешок, состоящий из измененных паутинной и мягкой мозговых оболочек, покрытых кожей, то речь идет о менингоцеле; при наличии в содержимом грыжевого выпячивания поврежденной мозговой ткани – речь идет о посттравматическом менингоэнцефалоцеле. Менингоэнцефалоцеле и менингоцеле часто наблюдаются у детей в зоне растущих переломов.
Клиническая картина определяется неврологическими последствиями перенесенной ЧМТ в сочетании с различной степенью выраженности ликвородинамических нарушений, а также локальными изменениями мягких тканей в области грыжевого выпячивания.
КТ и МРТ уточняют диагноз данной патологии (рис. 14).
В клинической картине хронических субдуральных гигром сочетаются общемозговые (гипертензионные) и очаговые (раздражения и выпадения) симптомы; типично ремиттирующее течение.
 КТ (рис. 15) и МРТ способны обеспечить точный диагноз хронической субдуральной гигромы, а также уточнить их источник с характерной дорожкой от места разрыва базальных цистерн, обеспечивающей непосредственную связь конвекситального скопления жидкости с основанием мозга через боковую цистерну.
КТ (рис. 15) и МРТ способны обеспечить точный диагноз хронической субдуральной гигромы, а также уточнить их источник с характерной дорожкой от места разрыва базальных цистерн, обеспечивающей непосредственную связь конвекситального скопления жидкости с основанием мозга через боковую цистерну.
Клинически посттравматичские кисты характеризуются длительным ремиттирующим течением. Одним из основных симптомов являются эпилептические припадки, различные по структуре и частоте.
При субарахноидальных посттравматических кистах у детей наблюдается отставание в психическом развитии, а также выпячивание и истончение прилежащей кости при отсутствии изменений и болезненности мягких тканей, непостоянный односторонний экзофтальм и др. Различают посттравматические кисты несообщающиеся и сообщающиеся с базальными цистернами или желудочками мозга.
Диагностика посттравматических кист основывается на данных анамнеза, клинической картины и инструментальных методов исследования, ведущими среди которых являются КТ (рис. 16) и МРТ (кистозная полость), а также краниография (локальное истончение, выпячивание кости).
Переломы костей основания черепа и разрывы мозговых оболочек могут обусловливать ликворею, которая приводит, в конечном итоге, к формированию фистулы. Частота ликворей у взрослых и детей соотносится как 10:1.
Наиболее часто посттравматическая фистула локализуется в области ситовидной пластинки, реже – в области лобной, решетчатой и основной пазух. Переломы каменистой части пирамиды височной кости и области ячеек сосцевидного отростка могут обусловить оторею. Парадоксальная ринорея может возникнуть при переломе каменистой части пирамиды в области среднего уха при интактной барабанной перепонке, при этом ликвор сначала будет поступать в слуховую трубу, а затем изливаться наружу через нос. «Скрытая» ликворея может быть заподозрена при возникновении или рецидивах менингита без видимой причины.
Наиболее очевидным признаком является истечение ЦСЖ из носа, уха или раны. Произвольное вызывание ринореи изменением положения головы указывает на возможность наличия резервуара, например скопление жидкости в синусе. Аносмия указывает на повреждение костных структур в области передней черепной ямки, глухота – в области средней черепной ямки.
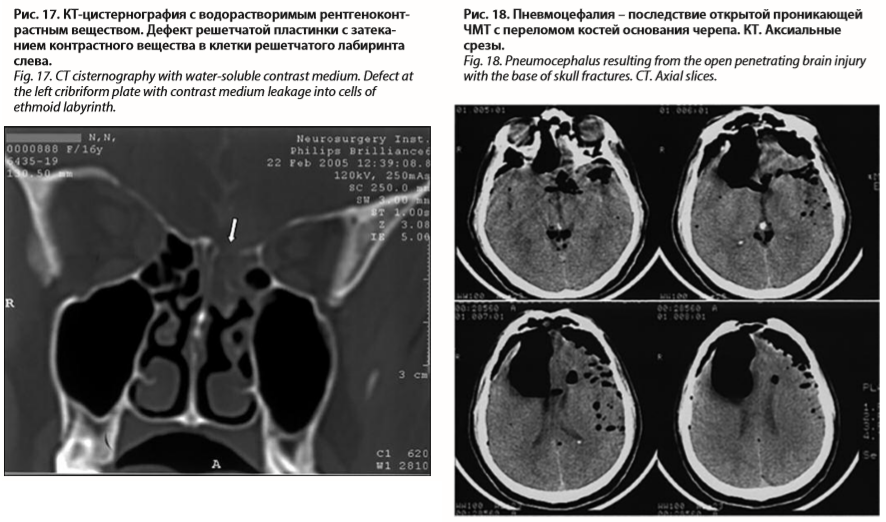
Для выявления ликворной фистулы наиболее информативна компьютерная цистернография при использовании фронтальных срезов с водорастворимыми контрастными веществами (рис. 17).
Воздух в полости черепа может скапливаться экстрадурально, субдурально, субарахноидально, а также в желудочках мозга (чему способствует порэнцефалия). Пневмоцефалия нередко сочетается с ликвореей.
Пневмоцефалия может выявляться как в ранние, так и поздние сроки после травмы и стойко держаться.
У детей она обнаруживается редко вследствие слабой пневматизации костей черепа.
Пневмоцефалия, особенно при вентрикулярном скоплении воздуха, вызывает ощущение «переливания», «плеска» при перемене положения головы.
В клинической картине проявляются различной выраженности общемозговые и оболочечные симптомы. При значительном субдуральном скоплении воздуха его можно выявить перкуссией черепа (характерный локальный тимпанит). Основными методами диагностики являются краниография и КТ, однозначно определяющие наличие воздуха в полости черепа (рис. 18).
Ишемия мозга может возникать в любом периоде ЧМТ, являясь наиболее частой причиной вторичного повреждения центральной нервной системы.
Посттравматическую ишемию обусловливают как интракраниальные (внутричерепная гипертензия, отек мозга, нарушение метаболизма и кровотока), так и экстракраниальные (гипоксемия, артериальная гипотензия и др.) факторы. Наиболее часто ишемическое поражение, вплоть до инсульта, наблюдается в зонах смежного кровоснабжения крупных церебральных артерий, что объясняется снижением мозгового перфузионного давления.
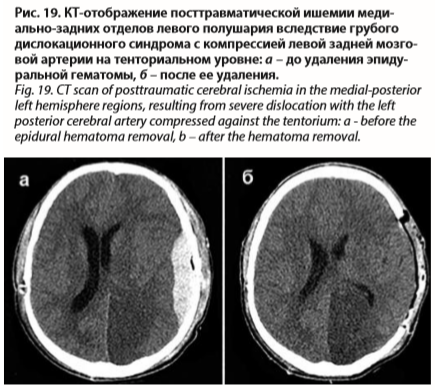
При ущемлении среднего мозга в отверстии мозжечкового намета могут возникать значительные по объему очаги ишемического поражения мозга в затылочно-теменных отделах полушарий за счет сдавления и спазма задних мозговых артерий. Клинически посттравматическая ишемия проявляется ухудшением состояния, нарастанием очаговой и общемозговой неврологической симптоматики. КТ легко визуализирует ишемические очаги, выявляя в месте их расположения гиподенсивные зоны (рис. 19). МРТ также обеспечивает точную диагностику.
 Посттравматические хронические субдуральные гематомы (ПХСГ) отличаются от острых и подострых наличием отграничительной капсулы, определяющей все дальнейшие особенности их пато- и саногенеза, клинического течения и тактики лечения. Капсула ПХСГ обычно различима и начинает функционировать уже спустя 2 нед после ЧМТ. Этот срок и принят большинством авторов для разграничения хронических гематом от острых и подострых. Вместе с тем развитие и организация капсулы ПХСГ – процесс, продолжающийся месяцы и годы.
Посттравматические хронические субдуральные гематомы (ПХСГ) отличаются от острых и подострых наличием отграничительной капсулы, определяющей все дальнейшие особенности их пато- и саногенеза, клинического течения и тактики лечения. Капсула ПХСГ обычно различима и начинает функционировать уже спустя 2 нед после ЧМТ. Этот срок и принят большинством авторов для разграничения хронических гематом от острых и подострых. Вместе с тем развитие и организация капсулы ПХСГ – процесс, продолжающийся месяцы и годы.
Если раньше ПХСГ выявлялись почти исключительно у лиц пожилого и старческого возраста, то в настоящее время они значительно «помолодели», наблюдаясь достаточно часто у лиц молодого и среднего возраста, а также у детей. Главной причиной учащения ХСГ является распространенность ЧМТ. Существенное значение приобретает постарение населения, что в связи с возрастной атрофией мозга, изменениями сосудистой системы, реологических свойств крови создает дополнительные предпосылки для формирования ПХСГ даже при легкой ЧМТ. У детей в образовании ПХСГ играют роль врожденные и приобретенные краниоцеребральные диспропорции. Определенное место в учащении хронических субдуральных гематом занимает алкоголизм, а также ряд других неблагоприятных воздействий на головной мозг и другие органы.
Капсула ПХСГ состоит из соединительно-тканных волокон и новообразованных тонкостенных сосудов. Содержимое полости ПХСГ обычно представляет собой измененную кровь – жидкость темно-коричневого либо коричневато-зеленого цвета с мелкими свертками фибрина. Замыкая содержимое ПХСГ, капсула формирует сравнительно автономное образование, сосуществующее с другими слагаемыми внутричерепного пространства. Динамическое равновесие внутричерепных объемов легко нарушается под влиянием самых различных обстоятельств и факторов.
Размеры ПХСГ наиболее часто увеличиваются вследствие повторных микро- или макроизлияний из неполноценных сосудов капсулы под влиянием гиперфибринолиза, возникающего в содержимом гематомы за счет продуктов деградации фибрина.
Для ПХСГ характерно конвекситально-парасагиттальное распространение с захватом 2–3 долей или всего полушария. Примерно 1/10 часть ПХСГ имеет двустороннее расположение. Объем ХСГ колеблется от 60 до 250 мл, чаще составляет 100–200 мл.
Светлый промежуток при ПХСГ может длиться неделями, месяцами и даже годами. Клиническая манифестация ПХСГ исключительно полиморфна. Наблюдается как постепенное развитие компрессионного синдрома, так и внезапное резкое ухудшение состояния больного до сопора и комы спонтанно или под влиянием разных факторов (легкая повторная травма головы, перегревание на солнце, употребление алкоголя, простудные заболевания и др.).
Клиническая картина при этом может напоминать различные заболевания центральной нервной системы: доброкачественные и злокачественные опухоли мозга, инсульт, спонтанное субарахноидальное кровоизлияние, церебральный атеросклероз, энцефалит, эпилепсию, и даже психозы разной структуры и др.
В период развернутой клинической картины ПХСГ часты изменения сознания в виде оглушения или аментивной спутанности с нарушениями памяти, ориентировки.
Головная боль имеет оболочечный оттенок. Может отмечаться притупление перкуторного звука над зоной расположения гематомы. Среди очаговых признаков ПХСГ ведущая роль принадлежит пирамидному гемисиндрому, а также негрубым речевым нарушениям и др. Большой удельный вес в клинике ПХСГ имеет экстрапирамидная симптоматика (гипомимия, брадикинезия, общая скованность, повышение мышечного тонуса по пластическому типу, подкорковый тремор и др.); нередко выявляются хоботковый и хватательный рефлексы, а также нарушения статики и походки.
В фазах клинической декомпенсации может проявляться вторичная дислокационная среднемозговая симптоматика (парез взора вверх, двусторонние стопные знаки, анизокория, спонтанный нистагм и др.).
При повозрастном анализе клиники ПХСГ установлены следующие основные закономерности: 1) обычное преобладание общемозговой симптоматики над очаговой во всех возрастных группах; 2) изменение структуры общемозговых симптомов по мере увеличения возраста больных: от гипертензионных – в детском, молодом и среднем возрасте до гипотензионных – в пожилом и старческом возрасте, что связано с преобладанием в младших возрастных группах отека мозга и внутричерепной гипертензии, а в старших возрастных группах – его коллапса и внутричерепной гипотензии; 3) повышение (с возрастом больных) роли сосудистых факторов в генезе симптомов при ПХСГ, что вместе с инволюционными изменениями обусловливает большую частоту нарушений психики у лиц пожилого и старческого возраста по сравнению с младшими возрастными группами; 4) преобладание двигательных нарушений среди очаговых симптомов, степень их выраженности и устойчивости обычно усугубляется с возрастом больного.
Распознавание ПХСГ основывается на тщательном анализе анамнеза (факт ЧМТ, даже легкой, внезапные ухудшения и выраженные ремиссии) и клинической картины.
Среди инструментальных методов диагностики ПХСГ значимы эхоэнцефалография (выраженное смещение срединного эха) и каротидная ангиография (характерная линзообразная аваскулярная зона, отделяющая по конвексу сосудистый рисунок пораженного полушария от внутренней поверхности костей свода черепа). Наиболее адекватными методами распознавания ПХСГ являются КТ и МРТ.
КТ-синдром характеризуется зоной измененной плотности (гиподенсивной, гиперденсивной либо гетероденсивной) между костями черепа и веществом мозга, имеющей серповидную форму и многодолевое или плащевое распространение. Типично отсутствие субарахноидальных щелей на стороне расположения гематомы, что особенно важно для диагностики изоденсивных ПХСГ. При двусторонних гематомах конвекситальные субарахноидальные пространства не дифференцируются с обеих сторон, отмечается сближение передних рогов боковых желудочков, а также изменение их талии и сближение задних рогов. КТ-синдром ПХСГ порой может дополняться другими прямыми их признаками: феноменом седиментации, визуализацией капсулы гематомы, многокамерностью ее строения, наличием интрагематомных трабекул. КТ позволят судить о реакциях мозга на ПХСГ (отек, коллапс, дисгемия), о краниоцеребральных соотношениях, а также преморбидных изменениях вещества мозга и ликворных пространств.
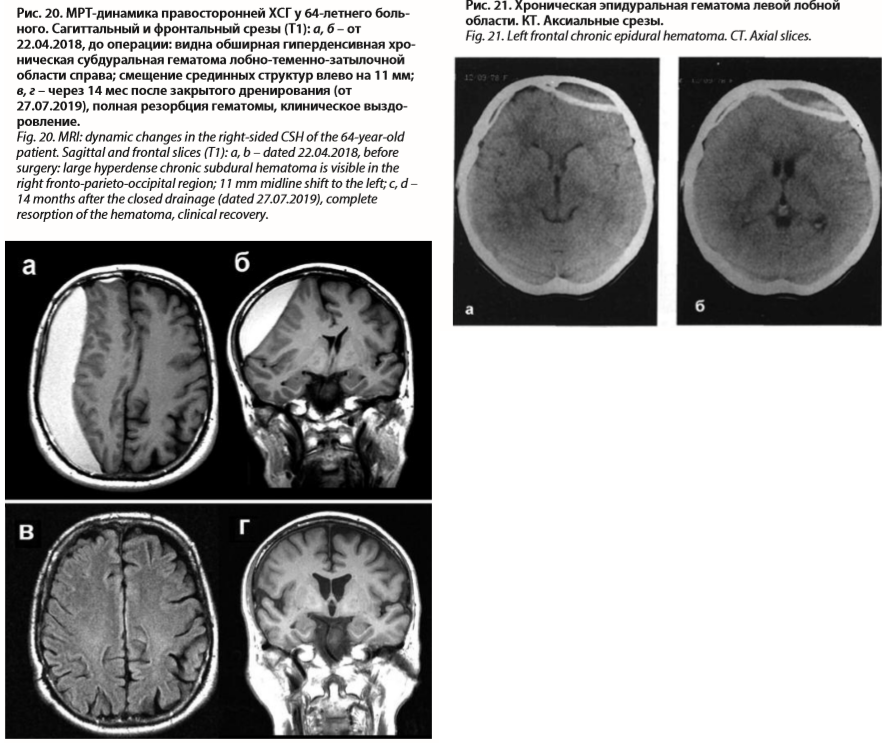
МРТ-синдром ПХСГ характеризуется: а) наличием гомогенной зоны сигнала повышенной интенсивности (вне зависимости от давности ПХСГ и ее консистенции) над веществом головного мозга; б) значительным преобладанием площади патологической зоны над ее толщиной при серповидной форме на аксиальных срезах и линзообразной – на фронтальных срезах (рис. 20). МРТ имеет особые преимущества перед КТ в диагностике изоденсивных и плоскостных ПХСГ.
Гораздо реже, чем хронические субдуральные гематомы, встречаются хронические эпидуральные гематомы (рис. 21), которые склонны к обызвествлению. Как казуистика могут наблюдаться и хронические внутримозговые гематомы.
 В механизме развития посттравматических аневризм (истинных и ложных) чаще всего лежит разрыв или надрыв одного из слоев стенки кровеносного сосуда; возможно также перерастяжение сосуда, превышающее предел его эластичности, и сквозное повреждение стенки сосуда. В последнем случае образуется ложная артериальная аневризма, т.е. полость аневризмы ограничивают уже не сохранившиеся оболочки сосудистой стенки, как при истинной аневризме, а окружающие ткани. По форме аневризмы делят на мешотчатые и веретенообразные (фузиформные). Частым вариантом последних бывают расслаивающие аневризмы, когда кровь, иногда на значительном участке артерии, проникает между слоями ее стенки и растягивает их, одновременно суживая просвет сосуда, чем затрудняет ангиографическую диагностику повреждения.
В механизме развития посттравматических аневризм (истинных и ложных) чаще всего лежит разрыв или надрыв одного из слоев стенки кровеносного сосуда; возможно также перерастяжение сосуда, превышающее предел его эластичности, и сквозное повреждение стенки сосуда. В последнем случае образуется ложная артериальная аневризма, т.е. полость аневризмы ограничивают уже не сохранившиеся оболочки сосудистой стенки, как при истинной аневризме, а окружающие ткани. По форме аневризмы делят на мешотчатые и веретенообразные (фузиформные). Частым вариантом последних бывают расслаивающие аневризмы, когда кровь, иногда на значительном участке артерии, проникает между слоями ее стенки и растягивает их, одновременно суживая просвет сосуда, чем затрудняет ангиографическую диагностику повреждения.
Посттравматические аневризмы образуются обычно при переломах основания черепа, в том числе на участках прохождения магистральных артерий через его костные каналы.
Клиническая симптоматика зависит в первую очередь от локализации и величины аневризмы. Например, наиболее частые аневризмы внутренней сонной артерии в области кавернозного синуса вызывают экзофтальм, застойные изменения в области глазницы, нарушение функции II, III, IV, V, VI черепных нервов. Характерным признаком является локальный болевой синдром, причем боль носит иногда пульсирующий
характер. Если аневризма прилежит к слизистой оболочке основной пазухи, она может превратиться в ложную и проявляться повторными профузными носовыми кровотечениями. Интракраниальные кровоизлияния при аневризмах бывают редко. Аневризмы могут служить причиной ишемических нарушений в бассейне несущего их сосуда. Тогда развивается соответствующий церебральный синдром. Интракавернозные аневризмы сонной артерии часто разрываются и превращаются в каротидно-кавернозные соустья.
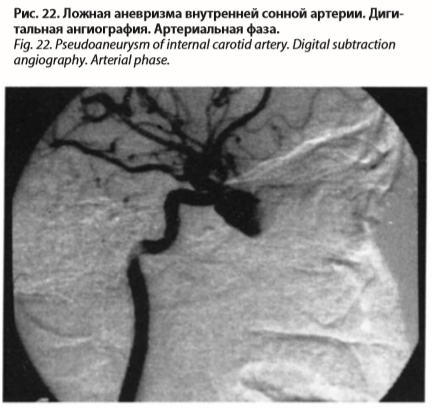
Основным методом диагностики является ангиография (рис. 22). Определенную роль играют КТ и МРТ.
Клиническая картина каротидно-кавернозного соустья включает: первичные симптомы, непосредственно связанные с образованием патологического перетока крови, и вторичные симптомы, вызванные длительно существующими застойными явлениями. К первичным симптомам относятся: пульсирующий, синхронный с пульсом шум, экзофтальм, пульсация глазного яблока, расширение и пульсация вен лица, шеи, свода черепа, отек конъюнктивы, расширение ее вен, застой крови в сосудах радужки и сетчатки, повышение внутриглазного давления, нарушение подвижности глазного яблока, диплопия, опущение верхнего века, нарушения иннервации зрачка, трофические и чувствительные изменения роговицы, застой крови в венах носовой полости, перераспределение мозгового кровообращения. Ко вторичным симптомам относятся: атрофия ретробульбарной клетчатки и кровоизлияния в нее, помутнение прозрачных сред глаза, язвы роговицы, тромбофлебит вен глазницы и острая глаукома, атрофия соска зрительного нерва, понижение зрения и слепота, кровотечение из сосудов глазного яблока, из носа, атрофия прилежащих участков, кости, осложнения, зависящие от нарушения мозгового кровообращения (психозы, деменция и др.). Диагностика основывается на характерных клинических данных. Важную роль играет аускультация головы, выявляющая шум, синхронный с пульсом. Шум, как правило, исчезает при пережатии поврежденной сонной артерии на шее. Решающее значение в определении размеров, локализации каротидно-кавернозного соустья, состояния церебральной гемодинамики, венозного оттока имеет ангиографическое исследование (рис. 23, 24).
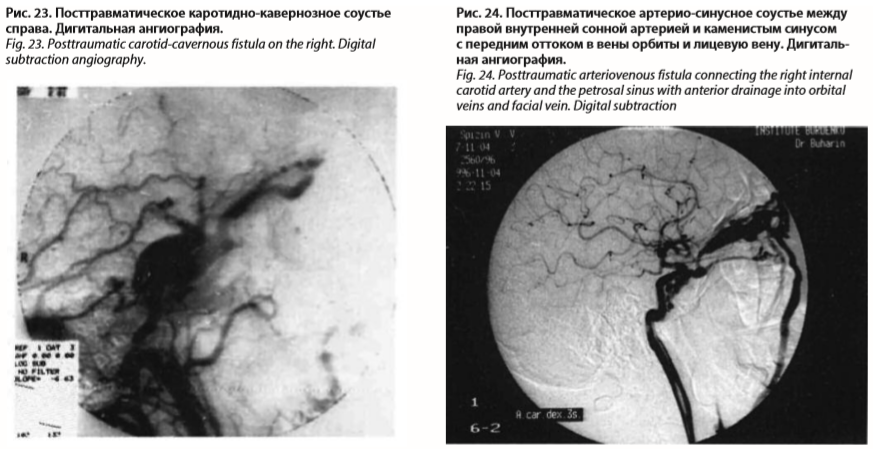
Ангиография обнаруживает нарушение дренажной функции церебральных вен и незаполнение верхнего стреловидного, либо другого синуса. На КТ определяются расширение желудочков мозга и усиление контрастирования в области мозжечкового намета. МРТ способна обеспечить прямую диагностику тромбоза синусов головного мозга.
Информация об авторах / Information about the authors
Лихтерман Леонид Болеславович – д-р мед. наук, проф., невролог, гл. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Leonid B. Likhterman – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Кравчук Александр Дмитриевич – д-р мед. наук, проф., нейрохирург, зав. 9-м нейрохирургическим отделением, ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». ORCID: 0000-0002-3112-8256
Aleksandr D. Kravchuk – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0002-3112-8256
Охлопков Владимир Александрович – канд. мед. наук, доцент, нейрохирург, ст. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». ORCID: 0000-0001-8911-2372
Vladimir A. Okhlopkov – Cand. Sci. (Med.), Assoc. Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0001-8911-2372
Статья поступила в редакцию / The article received: 10.09.2021
Статья принята к печати / The article approved for publication: 16.09.2021
Клинический разбор в общей медицине №06 2021
Учение о последствиях черепно-мозговой травмы Часть II. Клинико-морфологические формы последствий черепно-мозговой травмы
Номера страниц в выпуске:23-34
Аннотация
Описаны клинико-морфологические формы последствий черепно-мозговой травмы, выделенные на основании многолетних исследований в НМИЦ нейрохирургии им. акад. Н.Н. Бурденко. Предложены основные критерии их диагностики по неврологическим и инструментальным данным, главным образом нейровизуализационным (компьютерная томография, магнитно-резонансная томография, ангиография).
Ключевые слова: последствия черепно-мозговой травмы, клинико-морфологические формы, нейровизуализационная диагностика.
Для цитирования: Лихтерман Л.Б., Кравчук А.Д., Охлопков В.А. Учение о последствиях черепно-мозговой травмы. Часть II. Клинико-морфологические формы последствий черепно-мозговой травмы. Клинический разбор в общей медицине. 2021; 6: 23–34. DOI: 10.47407/kr2021.2.6.00077
Описаны клинико-морфологические формы последствий черепно-мозговой травмы, выделенные на основании многолетних исследований в НМИЦ нейрохирургии им. акад. Н.Н. Бурденко. Предложены основные критерии их диагностики по неврологическим и инструментальным данным, главным образом нейровизуализационным (компьютерная томография, магнитно-резонансная томография, ангиография).
Ключевые слова: последствия черепно-мозговой травмы, клинико-морфологические формы, нейровизуализационная диагностика.
Для цитирования: Лихтерман Л.Б., Кравчук А.Д., Охлопков В.А. Учение о последствиях черепно-мозговой травмы. Часть II. Клинико-морфологические формы последствий черепно-мозговой травмы. Клинический разбор в общей медицине. 2021; 6: 23–34. DOI: 10.47407/kr2021.2.6.00077
Theory about traumatic brain injury effects. Part II. Clinical and morphological forms of traumatic brain injury effects
Leonid B. Likhterman, Aleksandr D. Kravchuk, Vladimir A. OkhlopkovBurdenko national medical research centre for neurosurgery, Moscow, Russia
likhterman@nsi.ru
Abstract
Clinical and morphological forms of traumatic brain injury effects are reported, distinguished based on the results, obtained during years of research in the National Medical Research Center for Neurosurgery. Basic criteria are proposed for the diagnosis of those based on the neurological and instrumental examination data, mostly on the neuroimaging data (CT, MRI, angiography).
Key words: traumatic brain injury effects, clinical and morphological forms, neuroimaging diagnosis.
For citation: Likhterman L.B., Kravchuk A.D., Okhlopkov V.A. Theory about traumatic brain injury effects. Part II. Clinical and morphological forms of traumatic brain injury effects. Clinical review for general practice. 2021; 6: 23–34. DOI: 10.47407/kr2021.2.6.00077
Исходя из классификации последствий черепно-мозговой травмы (ЧМТ), изложенной в части I этой статьи, представляем конкретные их клинико-морфологические формы.
1. Клинико-морфологические формы тканевых последствий черепно-мозговой травмы
Посттравматическая атрофия мозгаАтрофия мозга есть запущенный ЧМТ процесс уменьшения объема мозгового вещества (как серого, так и белого). В ее основе лежат, наряду с первичной гибелью клеток, последующие дегенеративно-деструктивно-дистрофические изменения: демиелинизация аксонов, ишемия, глиоз, уменьшение числа функционирующих капилляров, запустевание периваскулярных пространств и др. Различают диффузную и локальную посттравматическую атрофию. Ее развитие, характер и степень выраженности определяются биомеханикой и тяжестью ЧМТ, возрастом пострадавшего, его анамнезом, в частности дотравматической патологией, качеством лечения и другими факторами.
При диффузном аксональном повреждении обычно развивается диффузная атрофия вещества мозга. При очаговых повреждениях на фоне диффузной атрофии часто доминирует локальная атрофия (в зоне бывших очагов размозжения, внутримозговых гематом и др.). При посттравматической атрофии происходит расширение желудочков мозга и субарахноидальных пространств с заполнением их цереброспинальной жидкостью (ЦСЖ).
Первые признаки посттравматической атрофии могут обнаруживаться уже спустя 2–4 нед после ЧМТ.
В дальнейшем этот процесс либо останавливается, либо прогрессирует на протяжении длительного времени. Различают легкую, среднюю и тяжелую степени очаговой и диффузной посттравматической атрофии.
Следует отметить, что между морфологической выраженностью атрофии и ее клиническим выражением часто нет параллелизма. Симптоматика посттравматической диффузной атрофии мозга характеризуется нарастающим вплоть до деменции оскудением психической деятельности. Неврологически в далеко зашедших
стадиях доминирует двусторонняя мозжечковая и подкорковая симптоматика, включая псевдобульбарные парезы.
Сочетание на компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) одновременного и симметричного увеличения желудочков мозга и субарахноидальных пространств (по конвексу, межполушарных и боковых щелей), а также отсутствие перивентрикулярного отека однозначно свидетельствуют в пользу диффузной атрофии (рис. 1, 2).
Локальная посттравматическая атрофия мозга характеризуется разнообразием клинического проявления в зависимости от топики процесса. Вместе с тем, очевидная по данным КТ и МРТ локальная атрофия мозга (рис. 3, 4), может давать лишь минимальную симптоматику либо, нередко, в функциональном отношении быть полностью компенсированной.

Посттравматический арахноидит
В основе арахноидита лежит запущенный ЧМТ хронический продуктивный процесс, преимущественно распространяющийся на паутинную и мягкие оболочки мозга, также эпендимарную выстилку желудочковой системы.Большую роль в патогенезе арахноидита, особенно при повторных ЧМТ или несостоятельности (по разным причинам) клеточных и гуморальных механизмов защиты, играют иммунные процессы и, прежде всего, аутосенсибилизация организма к мозгу за счет выработки антител к антигенам поврежденной мозговой ткани.
Паутинная оболочка из-за фиброза утолщается и уплотняется, из прозрачной становится серовато-белесоватой. Между ней и мягкой мозговой оболочкой возникают спайки и сращения. Нарушается циркуляция ЦСЖ с образованием различных по размерам кистеобразных расширений, увеличиваются размеры желудочков мозга.
В зависимости от соотношения спаечных и кистозных изменений выделяют слипчивый, кистозный и слипчиво-кистозный посттравматический арахноидит. Характерно ремиттирующее течение, когда экзацербация заболевания сменяется ремиссией различной продолжительности. На первый план в клинической картине выступают общемозговые симптомы: головная боль, имеющая оболочечно-сосудистую окраску, головокружение, тошнота, непереносимость резких раздражителей, общая слабость, быстрая утомляемость, физическая и психическая истощаемость и др. Обычно выражены астенические, эмоциональные и вегетативные расстройства.
Ведущими очаговыми признаками конвекситального арахноидита являются нарушения функций лобной, теменной или височной долей, часто в виде сочетания мягких симптомов выпадения и раздражения, эпилептические припадки.
Ведущими очаговыми признаками базального арахноидита являются нарушения функций черепных нервов, чаще зрительных, отводящих, тройничных и др. Посттравматический оптохиазмальный арахноидит характеризуется снижением остроты и изменением полей зрения. Отмечаются парацентральные и центральные скотомы, первичная и вторичная атрофия сосков зрительных нервов.
Ведущими очаговыми признаками арахноидита задней черепной ямки являются нарушения функций слухового нерва, особенно его вестибулярной порции, тройничного, отводящего и ряда других черепных нервов, а также мозжечковые симптомы. При окклюзирующих формах арахноидита задней черепной ямки на фоне гипертензионно-гидроцефальной симптоматики становятся грубыми нарушения статики и походки.
Клинический диагноз посттравматического арахноидита подтверждается характерными данными КТ или МРТ, обнаруживающими неравномерность субарахноидальных щелей по конвексу с кистозными расширениями либо их отсутствие обычно на фоне того или иного увеличения желудочков мозга.
Посттравматический пахименингит
Пахименингит представляет реактивное асептическое воспаление твердой мозговой оболочки (ТМО) вследствие ее механического раздражения или повреждения.Различают наружный (эпидуральный), внутренний (субдуральный) и смешанный (эпи-субдуральный) посттравматический пахименингит.
Характерным симптомом посттравматического пахименингита является локальная головная боль. При парабазальной его локализации отмечаются краниобазальные или орбитальные боли. Наблюдаются тошнота, рвота, брадикардия, что обусловлено раздражением окончаний тройничного нерва в ТМО. Могут проявляться: гиперемия и гипергидроз лица, асимметрия артериального давления, болезненность шейных точек вследствие ирритации вегетативных волокон в ТМО. Порой развиваются эпилептические припадки; судороги имеют очаговый или генерализованный характер. КТ или МРТ уточняют локализацию и распространенность посттравматического пахименингита, выявляя характерную протяженную зону повышенной плотности, прилежащую к внутренней поверхности костей черепа.
 Посттравматические оболочечно-мозговые рубцы
Посттравматические оболочечно-мозговые рубцы
Оболочечно-мозговые рубцы формируются в месте повреждений костей черепа, оболочек и вещества мозга. Процесс организации оболочечно-мозговых рубцов начинается в остром, продолжается в промежуточном и завершается в отдаленном периодах ЧМТ. В клинической картине при оболочечно-мозговых рубцах доминируют цефалгический и эпилептический синдромы (судорожные и бессудорожные пароксизмы), возможна психопатизация личности, метеопатизация, а также при дефектах костей – местные изменения часто с втянутостью мягких покровов головы.
Диагноз оболочечно-мозгового рубца объективизируют КТ (рис. 5) и МРТ, выявляющие соответственно его локализации и размер мозаичных по плотности участков с преобладанием гиперденсивного компонента.
Посттравматические поражения черепных нервов
Посттравматические поражения черепных нервов могут играть важную, а порой и доминирующую роль в клинике последствий ЧМТ. Среди них особенно значимо поражение зрительных нервов, что обусловливает снижение зрения (до слепоты) и различные нарушения полей зрения. Причины: повреждения орбиты и основной кости (перелом, гематома, разрывы зрительных нервов, кровоизлияния), краниобазальные ушибы, особенно височной локализации, рубцово-спаечные процессы и др.Клинически существенны (вплоть до главной причины инвалидизации пострадавших) одно- или двусторонние посттравматические парезы глазодвигательных нервов (III, IV, VI), которые возникают при переломах основания черепа (чаще на уровне средней черепной ямки).
Одно- или двусторонняя аносмия часто сопутствует очаговым повреждениям лобных долей и переломам решетчатой кости.
При переломах пирамиды височной кости наблюдаются периферические парезы лицевого, слухового и вкусового нервов. При переломах основания черепа, верхней и нижней челюсти нередко отмечаются поражение чувствительной и двигательной порции тройничного нерва. Непосредственное поражение корешков IX, X, XI, XII пар черепных нервов встречается редко. Поражение языкоглоточного и блуждающего нервов проявляется нарушениями глотания, голоса, речи.
 Посттравматические дефекты черепа
Посттравматические дефекты черепа
Костные дефекты обусловлены ЧМТ с оскольчато-вдавленными и вдавленными переломами черепа, его повреждениями холодным оружием (топор, сабля и др.), огнестрельными ранениями. Все же чаще они являются следствием резекционной или декомпрессивной трепанации при вдавленных переломах, удалении внутричерепных гематом и др.Размеры посттравматических дефектов черепа варьируют от малых (3–20 см2) до больших (60–80 см2 и более), захватывающих 2–3 соседние кости свода черепа.
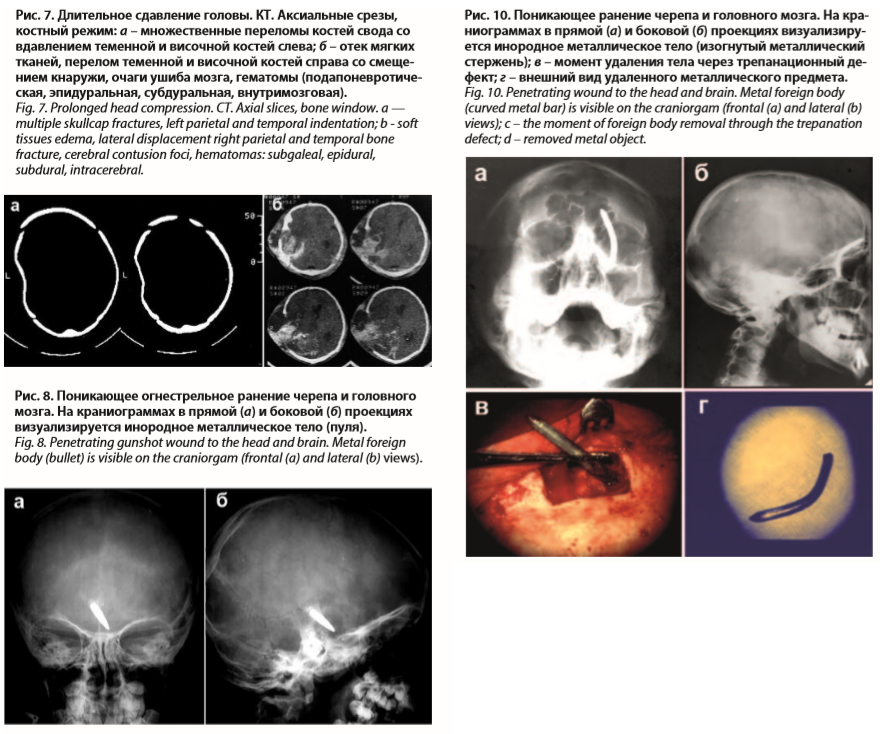
Клинически костные дефекты нередко проявляются синдромом трепанированного черепа: общие головные боли и местные боли в области дефекта, возникающие и/или усиливающиеся при изменении атмосферного давления, температуры окружающей среды; выпячивание содержимого черепа в дефект при кашле, чихании, наклоне головы, физическом напряжении и т.п. Характерны жалобы на боязнь повреждения мозга через дефект, чувство неполноценности, а также на косметические неудобства. Особенно тягостны для пострадавших обезображивающие их обширные кранио-орбито-базальные дефекты. Диагностика посттравматических дефектов черепа уточняется краниографически и КТ, в том числе с использованием трехмерной реконструкции (рис. 6).
Посттравматическая деформация черепа
Деформация черепа нередко возникает при длительном сдавлении головы, а также при родовой травме. Неврологическое ее проявление зависит от локализации повреждений мозга. Диагностика основывается на краниографии, КТ (рис. 7), особенно наглядна трехмерная КТ-реконструкция.

Внутричерепные инородные тела
Обычно инородные тела являются следствием открытой проникающей ЧМТ. В мирное время чаще обнаруживаются костные отломки, металлические предметы (дробь, осколки, пули), реже – кусочки стекла, пластмасс, дерева, тканей и др.Инородные тела, прежде всего, опасны как потенциальные очаги инфекции. Особого внимания заслуживают костные отломки, представляющие благоприятную среду для развития инфекции (менингита, энцефалита, абсцесса, гранулемы и др.). Кроме того, костные отломки поддерживают дегенеративные и рубцово-спаечные процессы в мозговой ткани.
В отдаленном периоде ЧМТ инородные тела могут клинически себя ничем не проявлять. Однако чаще обнаруживается разнообразная симптоматика в зависимости от локализации, размеров, количества инородных тел и других факторов.
При присоединении инфекции либо миграции инородных тел неврологическая картина усугубляется, симптомы раздражения часто сменяют симптомы выпадения мозговых функций.
Решающая роль в распознавании инородных тел принадлежит краниографии и КТ (рис. 8–10).
Посттравматический остит
Представляет собой хронический продуктивный процесс, распространяющийся на кости черепа. Посттравматический остит встречается редко.Наиболее информативные методы его диагностики – краниография и МРТ (рис. 11).
 2. Клинико-морфологические формы ликвородинамических последствий черепно-мозговой травмы
2. Клинико-морфологические формы ликвородинамических последствий черепно-мозговой травмы
Посттравматическая гидроцефалияГидроцефалия – прогрессирующий процесс избыточного накопления жидкости в ликворных пространствах и веществе головного мозга вследствие ЧМТ, обусловленный нарушениями циркуляции и резорбции ЦСЖ и характеризующийся: морфологически – увеличением желудочковой системы, перивентрикулярным отеком и облитерацией субарахноидальных щелей; клинически – развитием определенного симптомокомплекса с доминированием психических (интеллектуально-мнестических) и атаксических расстройств. Следует дифференцировать активную посттравматическую гидроцефалию от совершенно различного по механизму пассивного процесса – увеличения размеров желудочков мозга и субарахноидальных пространств, заполняемых ЦСЖ вследствие посттравматической атрофии мозга.
Сроки развития посттравматической гидроцефалии широко варьируют – от одного месяца до года и больше. После тяжелой ЧМТ с очаговыми поражениями мозга развиваются различные формы гидроцефалии: нормотензивная, гипертензионная и окклюзионная; после диффузного аксонального повреждения мозга – нормотензивная гидроцефалия.
Характерным КТ-признаком посттравматической гидроцефалии является расширение боковых (преимущественно передних рогов) и III желудочков (рис. 12). Они приобретают «баллонообразную» форму за счет давления ЦСЖ изнутри. При этом обычно не визуализируются конвекситальные субарахнодальные щели, а также сужены базальные цистерны. К типичным симптомам посттравматической гидроцефалии относятся перивентрикулярный отек, возникающий вначале вокруг передних рогов и затем распространяющийся вдоль других отделов боковых желудочков. В зонах повреждения мозговой ткани возникают дивертикулы, порэнцефалические ходы и кистозные полости. Степень увеличения размеров желудочковой системы не всегда соответствует уровню инвалидизации больных, определяемому и другими последствиями перенесенной тяжелой ЧМТ. Одинаковая выраженность водянки мозга может наблюдаться у больных с умеренной и с грубой инвалидизацией, а также находящихся в вегетативном статусе.
Посттравматическая порэнцефалия
Порэнцефалия – наличие каналов, ходов в мозговой ткани, возникающих вследствие тяжелой ЧМТ и соединяющих желудочки мозга или образовавшиеся в нем полости с подпаутинным пространством, либо с оболочечным и внутримозговыми кистами. Клиническая картина полиморфна, часто включает цефальгический и эпилептичский синдромы. Диагноз уточняется с помощью КТ (рис. 13) или МРТ.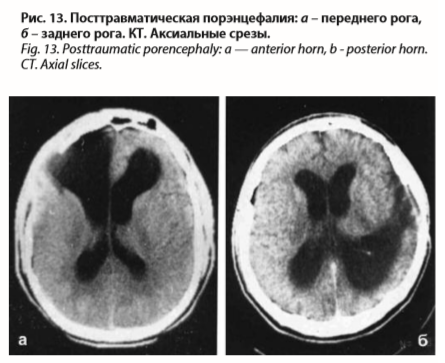 Посттравматическое менингоэнцефалоцеле
Посттравматическое менингоэнцефалоцеле
Если в посттравматический дефект черепа и ТМО выпячивается заполненный ЦСЖ грыжевой мешок, состоящий из измененных паутинной и мягкой мозговых оболочек, покрытых кожей, то речь идет о менингоцеле; при наличии в содержимом грыжевого выпячивания поврежденной мозговой ткани – речь идет о посттравматическом менингоэнцефалоцеле. Менингоэнцефалоцеле и менингоцеле часто наблюдаются у детей в зоне растущих переломов.Клиническая картина определяется неврологическими последствиями перенесенной ЧМТ в сочетании с различной степенью выраженности ликвородинамических нарушений, а также локальными изменениями мягких тканей в области грыжевого выпячивания.
КТ и МРТ уточняют диагноз данной патологии (рис. 14).
Посттравматическая хроническая субдуральная гигрома
К гигромам относят возникшее в результате ЧМТ отграниченное капсулой скопление ЦСЖ в субдуральном пространстве, вызывающее сдавление головного мозга. Хронические субдуральные гигромы образуются вследствие разрыва субарахнодальных цистерн, чаще на основании мозга (супраселлярной, боковой и др.), откуда ЦСЖ распространяется конвекситально.В клинической картине хронических субдуральных гигром сочетаются общемозговые (гипертензионные) и очаговые (раздражения и выпадения) симптомы; типично ремиттирующее течение.
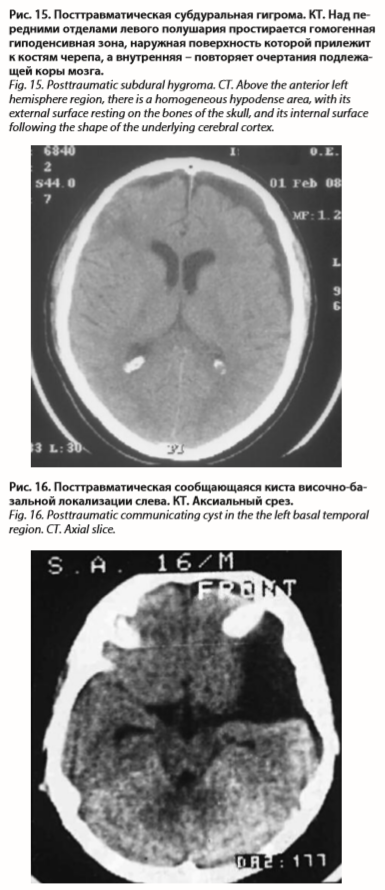
 КТ (рис. 15) и МРТ способны обеспечить точный диагноз хронической субдуральной гигромы, а также уточнить их источник с характерной дорожкой от места разрыва базальных цистерн, обеспечивающей непосредственную связь конвекситального скопления жидкости с основанием мозга через боковую цистерну.
КТ (рис. 15) и МРТ способны обеспечить точный диагноз хронической субдуральной гигромы, а также уточнить их источник с характерной дорожкой от места разрыва базальных цистерн, обеспечивающей непосредственную связь конвекситального скопления жидкости с основанием мозга через боковую цистерну.Посттравматическая ликворная киста
Различают субарахноидальные и внутримозговые ликворные кисты. Первые чаще наблюдаются у детей, вторые – у взрослых. Субарахноидальные кисты являются следствием субарахноидальных кровоизлияний и реактивного слипчивого лептоменингита. Внутримозговые кисты образуются при резорбции интрацеребральных кровоизлияний, очагов ушиба и размозжения мозга, в зоне посттравматического ишемического размягчения.Клинически посттравматичские кисты характеризуются длительным ремиттирующим течением. Одним из основных симптомов являются эпилептические припадки, различные по структуре и частоте.
При субарахноидальных посттравматических кистах у детей наблюдается отставание в психическом развитии, а также выпячивание и истончение прилежащей кости при отсутствии изменений и болезненности мягких тканей, непостоянный односторонний экзофтальм и др. Различают посттравматические кисты несообщающиеся и сообщающиеся с базальными цистернами или желудочками мозга.
Диагностика посттравматических кист основывается на данных анамнеза, клинической картины и инструментальных методов исследования, ведущими среди которых являются КТ (рис. 16) и МРТ (кистозная полость), а также краниография (локальное истончение, выпячивание кости).
 Посттравматическая ликворная фистула
Посттравматическая ликворная фистула
Переломы костей основания черепа и разрывы мозговых оболочек могут обусловливать ликворею, которая приводит, в конечном итоге, к формированию фистулы. Частота ликворей у взрослых и детей соотносится как 10:1.Наиболее часто посттравматическая фистула локализуется в области ситовидной пластинки, реже – в области лобной, решетчатой и основной пазух. Переломы каменистой части пирамиды височной кости и области ячеек сосцевидного отростка могут обусловить оторею. Парадоксальная ринорея может возникнуть при переломе каменистой части пирамиды в области среднего уха при интактной барабанной перепонке, при этом ликвор сначала будет поступать в слуховую трубу, а затем изливаться наружу через нос. «Скрытая» ликворея может быть заподозрена при возникновении или рецидивах менингита без видимой причины.
Наиболее очевидным признаком является истечение ЦСЖ из носа, уха или раны. Произвольное вызывание ринореи изменением положения головы указывает на возможность наличия резервуара, например скопление жидкости в синусе. Аносмия указывает на повреждение костных структур в области передней черепной ямки, глухота – в области средней черепной ямки.
Для выявления ликворной фистулы наиболее информативна компьютерная цистернография при использовании фронтальных срезов с водорастворимыми контрастными веществами (рис. 17).
Посттравматическая пневмоцефалия
Пневмоцефалия – проникновение воздуха в полость черепа вследствие его дегерметизации. При этом отмечаются повреждения костей черепа, мозговых оболочек, а часто и вещества мозга.Воздух в полости черепа может скапливаться экстрадурально, субдурально, субарахноидально, а также в желудочках мозга (чему способствует порэнцефалия). Пневмоцефалия нередко сочетается с ликвореей.
Пневмоцефалия может выявляться как в ранние, так и поздние сроки после травмы и стойко держаться.
У детей она обнаруживается редко вследствие слабой пневматизации костей черепа.
Пневмоцефалия, особенно при вентрикулярном скоплении воздуха, вызывает ощущение «переливания», «плеска» при перемене положения головы.
В клинической картине проявляются различной выраженности общемозговые и оболочечные симптомы. При значительном субдуральном скоплении воздуха его можно выявить перкуссией черепа (характерный локальный тимпанит). Основными методами диагностики являются краниография и КТ, однозначно определяющие наличие воздуха в полости черепа (рис. 18).
3. Клинико-морфологические формы сосудистых последствий черепно-мозговой травмы
Посттравматическая ишемия головного мозгаИшемия мозга может возникать в любом периоде ЧМТ, являясь наиболее частой причиной вторичного повреждения центральной нервной системы.
Посттравматическую ишемию обусловливают как интракраниальные (внутричерепная гипертензия, отек мозга, нарушение метаболизма и кровотока), так и экстракраниальные (гипоксемия, артериальная гипотензия и др.) факторы. Наиболее часто ишемическое поражение, вплоть до инсульта, наблюдается в зонах смежного кровоснабжения крупных церебральных артерий, что объясняется снижением мозгового перфузионного давления.
При ущемлении среднего мозга в отверстии мозжечкового намета могут возникать значительные по объему очаги ишемического поражения мозга в затылочно-теменных отделах полушарий за счет сдавления и спазма задних мозговых артерий. Клинически посттравматическая ишемия проявляется ухудшением состояния, нарастанием очаговой и общемозговой неврологической симптоматики. КТ легко визуализирует ишемические очаги, выявляя в месте их расположения гиподенсивные зоны (рис. 19). МРТ также обеспечивает точную диагностику.

Посттравматические хронические субдуральные гематомы
 Посттравматические хронические субдуральные гематомы (ПХСГ) отличаются от острых и подострых наличием отграничительной капсулы, определяющей все дальнейшие особенности их пато- и саногенеза, клинического течения и тактики лечения. Капсула ПХСГ обычно различима и начинает функционировать уже спустя 2 нед после ЧМТ. Этот срок и принят большинством авторов для разграничения хронических гематом от острых и подострых. Вместе с тем развитие и организация капсулы ПХСГ – процесс, продолжающийся месяцы и годы.
Посттравматические хронические субдуральные гематомы (ПХСГ) отличаются от острых и подострых наличием отграничительной капсулы, определяющей все дальнейшие особенности их пато- и саногенеза, клинического течения и тактики лечения. Капсула ПХСГ обычно различима и начинает функционировать уже спустя 2 нед после ЧМТ. Этот срок и принят большинством авторов для разграничения хронических гематом от острых и подострых. Вместе с тем развитие и организация капсулы ПХСГ – процесс, продолжающийся месяцы и годы.Если раньше ПХСГ выявлялись почти исключительно у лиц пожилого и старческого возраста, то в настоящее время они значительно «помолодели», наблюдаясь достаточно часто у лиц молодого и среднего возраста, а также у детей. Главной причиной учащения ХСГ является распространенность ЧМТ. Существенное значение приобретает постарение населения, что в связи с возрастной атрофией мозга, изменениями сосудистой системы, реологических свойств крови создает дополнительные предпосылки для формирования ПХСГ даже при легкой ЧМТ. У детей в образовании ПХСГ играют роль врожденные и приобретенные краниоцеребральные диспропорции. Определенное место в учащении хронических субдуральных гематом занимает алкоголизм, а также ряд других неблагоприятных воздействий на головной мозг и другие органы.
Капсула ПХСГ состоит из соединительно-тканных волокон и новообразованных тонкостенных сосудов. Содержимое полости ПХСГ обычно представляет собой измененную кровь – жидкость темно-коричневого либо коричневато-зеленого цвета с мелкими свертками фибрина. Замыкая содержимое ПХСГ, капсула формирует сравнительно автономное образование, сосуществующее с другими слагаемыми внутричерепного пространства. Динамическое равновесие внутричерепных объемов легко нарушается под влиянием самых различных обстоятельств и факторов.
Размеры ПХСГ наиболее часто увеличиваются вследствие повторных микро- или макроизлияний из неполноценных сосудов капсулы под влиянием гиперфибринолиза, возникающего в содержимом гематомы за счет продуктов деградации фибрина.
Для ПХСГ характерно конвекситально-парасагиттальное распространение с захватом 2–3 долей или всего полушария. Примерно 1/10 часть ПХСГ имеет двустороннее расположение. Объем ХСГ колеблется от 60 до 250 мл, чаще составляет 100–200 мл.
Светлый промежуток при ПХСГ может длиться неделями, месяцами и даже годами. Клиническая манифестация ПХСГ исключительно полиморфна. Наблюдается как постепенное развитие компрессионного синдрома, так и внезапное резкое ухудшение состояния больного до сопора и комы спонтанно или под влиянием разных факторов (легкая повторная травма головы, перегревание на солнце, употребление алкоголя, простудные заболевания и др.).
Клиническая картина при этом может напоминать различные заболевания центральной нервной системы: доброкачественные и злокачественные опухоли мозга, инсульт, спонтанное субарахноидальное кровоизлияние, церебральный атеросклероз, энцефалит, эпилепсию, и даже психозы разной структуры и др.
В период развернутой клинической картины ПХСГ часты изменения сознания в виде оглушения или аментивной спутанности с нарушениями памяти, ориентировки.
Головная боль имеет оболочечный оттенок. Может отмечаться притупление перкуторного звука над зоной расположения гематомы. Среди очаговых признаков ПХСГ ведущая роль принадлежит пирамидному гемисиндрому, а также негрубым речевым нарушениям и др. Большой удельный вес в клинике ПХСГ имеет экстрапирамидная симптоматика (гипомимия, брадикинезия, общая скованность, повышение мышечного тонуса по пластическому типу, подкорковый тремор и др.); нередко выявляются хоботковый и хватательный рефлексы, а также нарушения статики и походки.
В фазах клинической декомпенсации может проявляться вторичная дислокационная среднемозговая симптоматика (парез взора вверх, двусторонние стопные знаки, анизокория, спонтанный нистагм и др.).
При повозрастном анализе клиники ПХСГ установлены следующие основные закономерности: 1) обычное преобладание общемозговой симптоматики над очаговой во всех возрастных группах; 2) изменение структуры общемозговых симптомов по мере увеличения возраста больных: от гипертензионных – в детском, молодом и среднем возрасте до гипотензионных – в пожилом и старческом возрасте, что связано с преобладанием в младших возрастных группах отека мозга и внутричерепной гипертензии, а в старших возрастных группах – его коллапса и внутричерепной гипотензии; 3) повышение (с возрастом больных) роли сосудистых факторов в генезе симптомов при ПХСГ, что вместе с инволюционными изменениями обусловливает большую частоту нарушений психики у лиц пожилого и старческого возраста по сравнению с младшими возрастными группами; 4) преобладание двигательных нарушений среди очаговых симптомов, степень их выраженности и устойчивости обычно усугубляется с возрастом больного.
Распознавание ПХСГ основывается на тщательном анализе анамнеза (факт ЧМТ, даже легкой, внезапные ухудшения и выраженные ремиссии) и клинической картины.
Среди инструментальных методов диагностики ПХСГ значимы эхоэнцефалография (выраженное смещение срединного эха) и каротидная ангиография (характерная линзообразная аваскулярная зона, отделяющая по конвексу сосудистый рисунок пораженного полушария от внутренней поверхности костей свода черепа). Наиболее адекватными методами распознавания ПХСГ являются КТ и МРТ.
КТ-синдром характеризуется зоной измененной плотности (гиподенсивной, гиперденсивной либо гетероденсивной) между костями черепа и веществом мозга, имеющей серповидную форму и многодолевое или плащевое распространение. Типично отсутствие субарахноидальных щелей на стороне расположения гематомы, что особенно важно для диагностики изоденсивных ПХСГ. При двусторонних гематомах конвекситальные субарахноидальные пространства не дифференцируются с обеих сторон, отмечается сближение передних рогов боковых желудочков, а также изменение их талии и сближение задних рогов. КТ-синдром ПХСГ порой может дополняться другими прямыми их признаками: феноменом седиментации, визуализацией капсулы гематомы, многокамерностью ее строения, наличием интрагематомных трабекул. КТ позволят судить о реакциях мозга на ПХСГ (отек, коллапс, дисгемия), о краниоцеребральных соотношениях, а также преморбидных изменениях вещества мозга и ликворных пространств.
МРТ-синдром ПХСГ характеризуется: а) наличием гомогенной зоны сигнала повышенной интенсивности (вне зависимости от давности ПХСГ и ее консистенции) над веществом головного мозга; б) значительным преобладанием площади патологической зоны над ее толщиной при серповидной форме на аксиальных срезах и линзообразной – на фронтальных срезах (рис. 20). МРТ имеет особые преимущества перед КТ в диагностике изоденсивных и плоскостных ПХСГ.
Гораздо реже, чем хронические субдуральные гематомы, встречаются хронические эпидуральные гематомы (рис. 21), которые склонны к обызвествлению. Как казуистика могут наблюдаться и хронические внутримозговые гематомы.

Посттравматические внутричерепные артериальные аневризмы
 В механизме развития посттравматических аневризм (истинных и ложных) чаще всего лежит разрыв или надрыв одного из слоев стенки кровеносного сосуда; возможно также перерастяжение сосуда, превышающее предел его эластичности, и сквозное повреждение стенки сосуда. В последнем случае образуется ложная артериальная аневризма, т.е. полость аневризмы ограничивают уже не сохранившиеся оболочки сосудистой стенки, как при истинной аневризме, а окружающие ткани. По форме аневризмы делят на мешотчатые и веретенообразные (фузиформные). Частым вариантом последних бывают расслаивающие аневризмы, когда кровь, иногда на значительном участке артерии, проникает между слоями ее стенки и растягивает их, одновременно суживая просвет сосуда, чем затрудняет ангиографическую диагностику повреждения.
В механизме развития посттравматических аневризм (истинных и ложных) чаще всего лежит разрыв или надрыв одного из слоев стенки кровеносного сосуда; возможно также перерастяжение сосуда, превышающее предел его эластичности, и сквозное повреждение стенки сосуда. В последнем случае образуется ложная артериальная аневризма, т.е. полость аневризмы ограничивают уже не сохранившиеся оболочки сосудистой стенки, как при истинной аневризме, а окружающие ткани. По форме аневризмы делят на мешотчатые и веретенообразные (фузиформные). Частым вариантом последних бывают расслаивающие аневризмы, когда кровь, иногда на значительном участке артерии, проникает между слоями ее стенки и растягивает их, одновременно суживая просвет сосуда, чем затрудняет ангиографическую диагностику повреждения.Посттравматические аневризмы образуются обычно при переломах основания черепа, в том числе на участках прохождения магистральных артерий через его костные каналы.
Клиническая симптоматика зависит в первую очередь от локализации и величины аневризмы. Например, наиболее частые аневризмы внутренней сонной артерии в области кавернозного синуса вызывают экзофтальм, застойные изменения в области глазницы, нарушение функции II, III, IV, V, VI черепных нервов. Характерным признаком является локальный болевой синдром, причем боль носит иногда пульсирующий
характер. Если аневризма прилежит к слизистой оболочке основной пазухи, она может превратиться в ложную и проявляться повторными профузными носовыми кровотечениями. Интракраниальные кровоизлияния при аневризмах бывают редко. Аневризмы могут служить причиной ишемических нарушений в бассейне несущего их сосуда. Тогда развивается соответствующий церебральный синдром. Интракавернозные аневризмы сонной артерии часто разрываются и превращаются в каротидно-кавернозные соустья.
Основным методом диагностики является ангиография (рис. 22). Определенную роль играют КТ и МРТ.
Посттравматическое каротидно-кавернозное соустье
Соустье может возникать как после открытой, так и закрытой ЧМТ. Повреждение внутренней сонной артерии в кавернозном синусе при открытой травме обусловлено костными отломками или инородными телами, а при закрытой – чаще всего в результате гидравлического удара. Слабое развитие среднего мышечного и эластического слоя, резкие изгибы артерии в пещеристой пазухе, дотравматические инфекционные и атеросклеротические поражения создают условия для ее разрыва при ЧМТ. В результате заброса артериальной крови резко повышается давление в кавернозном синусе (от 14–16 до 80–100 мм рт. ст.). Он увеличивается до 3–4 см в диаметре, происходит сдавление черепных нервов, проходящих в его растянутой стенке, резко расширяется верхняя глазничная вена. Это приводит к нарушению оттока и застою в головном мозгу, ретроградному току артериальной крови по дренирующей синус венозной системе, а, в конечном итоге, к церебральной гипоксии, снижению зрения, атрофическим процессам в мозгу и орбите.Клиническая картина каротидно-кавернозного соустья включает: первичные симптомы, непосредственно связанные с образованием патологического перетока крови, и вторичные симптомы, вызванные длительно существующими застойными явлениями. К первичным симптомам относятся: пульсирующий, синхронный с пульсом шум, экзофтальм, пульсация глазного яблока, расширение и пульсация вен лица, шеи, свода черепа, отек конъюнктивы, расширение ее вен, застой крови в сосудах радужки и сетчатки, повышение внутриглазного давления, нарушение подвижности глазного яблока, диплопия, опущение верхнего века, нарушения иннервации зрачка, трофические и чувствительные изменения роговицы, застой крови в венах носовой полости, перераспределение мозгового кровообращения. Ко вторичным симптомам относятся: атрофия ретробульбарной клетчатки и кровоизлияния в нее, помутнение прозрачных сред глаза, язвы роговицы, тромбофлебит вен глазницы и острая глаукома, атрофия соска зрительного нерва, понижение зрения и слепота, кровотечение из сосудов глазного яблока, из носа, атрофия прилежащих участков, кости, осложнения, зависящие от нарушения мозгового кровообращения (психозы, деменция и др.). Диагностика основывается на характерных клинических данных. Важную роль играет аускультация головы, выявляющая шум, синхронный с пульсом. Шум, как правило, исчезает при пережатии поврежденной сонной артерии на шее. Решающее значение в определении размеров, локализации каротидно-кавернозного соустья, состояния церебральной гемодинамики, венозного оттока имеет ангиографическое исследование (рис. 23, 24).

Посттравматический тромбоз внутричерепных синусов
Тромбоз внутричерепных синусов редко наблюдается при открытой проникающей ЧМТ. При закрытых повреждениях он является казуистикой. Наиболее частые признаки тромбоза синусов – повышение внутричерепного давления и нарушение резорбции ЦСЖ. Отмечаются головная боль, рвота, отек сосков зрительных нервов, а также нарушения походки. Очаговые симптомы выпадения (парезы конечностей и др.) обычно возникают при распространении тромбоза на кортикальные вены.Ангиография обнаруживает нарушение дренажной функции церебральных вен и незаполнение верхнего стреловидного, либо другого синуса. На КТ определяются расширение желудочков мозга и усиление контрастирования в области мозжечкового намета. МРТ способна обеспечить прямую диагностику тромбоза синусов головного мозга.
Заключение
Понятно, что наряду с описанными основными клинико-морфологическим формами последствий ЧМТ существуют и другие их варианты, и различные сочетания. Кроме того, нередко встречаются и такие формы последствий ЧМТ, которые не имеют четкого морфологического отражения, по крайней мере, при существующих разрешающих возможностях рутинной аппаратуры для нейровизуализации (такие, например, как стойкая посттравматическая астения). Однако знание основных клинико-морфологических последствий ЧМТ дает достаточную ориентацию для адекватной диагностики и дифференцированного лечения.Информация об авторах / Information about the authors
Лихтерман Леонид Болеславович – д-р мед. наук, проф., невролог, гл. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Leonid B. Likhterman – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Кравчук Александр Дмитриевич – д-р мед. наук, проф., нейрохирург, зав. 9-м нейрохирургическим отделением, ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». ORCID: 0000-0002-3112-8256
Aleksandr D. Kravchuk – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0002-3112-8256
Охлопков Владимир Александрович – канд. мед. наук, доцент, нейрохирург, ст. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». ORCID: 0000-0001-8911-2372
Vladimir A. Okhlopkov – Cand. Sci. (Med.), Assoc. Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0001-8911-2372
Статья поступила в редакцию / The article received: 10.09.2021
Статья принята к печати / The article approved for publication: 16.09.2021


