Клинический разбор в общей медицине №6 2022
Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University, Pyatigorsk, Russia
larsky.mikhail@gmail.com
Abstract
Aim. Biopharmaceutical assessment of various solid dosage forms (capsules and coated tablets) of febuxostat formulations including comparison of excipients used in these dosage forms, disintegration pathways under static conditions, and dissolution kinetic profiles.
Methods. The Azurix® coated tablets and Podagrel hard gelatin capsules containing 80 mg of febuxostat were the object of the study. The model of disintegration under static conditions was used to assess disintegration of the dosage forms. Quantification of febuxostat in the samples diring the comparative study of dissolution kinetics was performed by high-performance liquid chromatography.
Results. When assessing morphological changes of dosage forms in the static model developed to simulate gastric environment, various desintegration patterns and rates confirmed by the differences in the qualitative composition of the excipients used were defined for these dosage forms. The comparative kinetics study showed different rates of febuxostat release from the studied dosage forms.
Conclusion. The findings demonstrate a significant impact of the excipient composition on the behavior of dosage forms in the body environment, particularly on the dosage form desintegration, which in turn defines the rate and degree of the active ingredient release. Thus, the test shows pronounced differences in biopharmaceutical parameters, capable of affecting the studied drugs bioavailability, between two febuxostat dosage forms.
Key words: febuxostat, coated tablets, capsules, in vitro release, disintegration under static conditions, high-performance liquid chromatography.
For citation: For citation: Larsky M.V., Zolotykh D.S., Chiriapkin A.S., Vernikovsky V.V. The comparative biopharmaceutical study of febuxostat solid dosage forms. Clinical review for general practice. 2022; 6: 78–95. DOI: 10.47407/kr2022.3.4.0012090p
Фебуксостат представляет собой 2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксильную кислоту и является селективным непуриновым ингибитором ксантиноксиредуктазы (КОР) – фермента, участвующего в обмене пуринов, пиримидинов, птерина и альдегидных субстратов. Стойко и длительно подавляя активность КОР, фебуксостат блокирует превращение ксантина в мочевую кислоту, что приводит к снижению концентрации уратов в сыворотке крови [4].
Фармакокинетика фебуксостата изучена в основном с точки зрения его биодоступности (относительной), а также вопросов скорости и путей выведения из организма человека [1, 4, 5]. В то же время вопросы абсорбции фебуксостата освещены в литературе недостаточно, однако имеются сведения о том, что скорость достижения и величина максимальной концентрации в плазме крови прямо пропорциональна дозе фебуксостата в диапазоне от 10 до 240 мг [6]. Исходя из этого, на скорость всасывания фебуксостата может оказывать влияние скорость и степень его высвобождения из лекарственной формы.
В настоящее время при изучении биодоступности лекарственных препаратов внимание привлекают процессы, протекающие непосредственно после приема лекарственной формы, т.е. ее поведение в момент контакта с жидкостями пищеварительной системы. При этом отмечается, что характер и кинетика распадаемости имеют решающее значение для качества и эффективности пероральных твердых лекарственных форм.
Распад таблеток или капсул приводит к образованию твердых фрагментов и частиц в водной среде и предшествует растворению и высвобождению действующего компонента. Таким образом, процесс распадаемости твердой лекарственной формы предваряет дальнейшее поведение лекарственного средства в организме, описываемого классической схемой LADME(R). Вместе с тем констатируется, что закрепленные в нормативной документации методы оценки распадаемости и растворения не позволяют оценить протекающие при этом микропроцессы, например смачивание, проникновение влаги в лекарственную форму, а также набухание, что особенно важно при оценке эффективности введения в состав лекарственных форм супердезинтегрантов [7].
Для оценки способности таблеток высвобождать заключенный в них действующий компонент в Государственную фармакопею Российской Федерации XIV издания (ГФ) включен тест «Распадаемость» на модели так называемой «качающейся корзинки». Колебательные движения, создаваемые в емкости прибора для определения распадаемости, происходят в вертикальной плоскости при частоте 28–32 цикла в 1 мин (т.е. примерно 1 колебание каждые 2 с) и призваны моделировать перистальтику желудочно-кишечного тракта (ЖКТ). Однако, как и любая другая модель, «качающаяся корзинка» достаточно условна, а интенсивное механическое воздействие динамических потоков жидкости мешает в полной мере оценить процесс распада таблетки и влияние на него используемых вспомогательных веществ и технологических приемов.
В литературе описана модель изучения процесса распадаемости (дезинтеграции) твердых лекарственных форм в статичных условиях, в которых исключается искусственное движение жидкости, не позволяющее фиксировать отличия протекающих изменений для разных объектов исследования [8, 9].
Согласно данным литературы, величина pH среды в желудке составляет от 1,0 до 3,0, а время прохождения этого отдела ЖКТ лекарственным препаратом составляет 30–40 мин [10, 11]. Согласно рекомендациям ГФ таблетки, покрытые оболочкой, и капсулы должны распадаться в течение 30 мин. Исходя из этого, можно заключить, что процесс распада лекарственных форм (за исключением кишечнорастворимых) происходит именно в желудке человека. Таким образом, модель распадаемости в статичных условиях в среде 0,1 М раствора кислоты хлористоводородной описывает типичную ситуацию приема лекарственного препарата в виде твердой лекарственной формы (таблетки или капсулы), которая после проглатывания находится в состоянии относительного покоя в желудочном соке [12].
Целью настоящего исследования является сравнительная биофармацевтическая оценка лекарственных препаратов фебуксостата в виде различных твердых лекарственных форм (капсул и таблеток, покрытых оболочкой), включающая сравнение используемых вспомогательных веществ, процессов распадаемости лекарственных форм в статических условиях и профилей кинетики растворения.
В качестве среды распадаемости был выбран 0,1 М раствор кислоты хлористоводородной (рН 1,2), имитирующий желудочный сок. Растворы с рН 4,5 и рН 6,8, моделирующие среду отделов кишечника, не использовались, поскольку распадаемость твердых лекарственных форм немедленного высвобождения происходит в среде желудка [10].
Для изучения кинетики растворения использовали тестер растворения РС-1 типа «Лопастная мешалка». Испытание проводили в соответствии с требованиями ОФС.1.4.2.0014.15 «Растворение для твердых дозированных лекарственных форм» [13]. Объем среды растворения – 900 мл, скорость вращения мешалки – 75 об/мин.
В качестве сред растворения выбраны фосфатные буферные растворы с рН 6,0 (среда контроля качества) и рН 6,8 (имитирует среду в среднем отделе тонкой кишки). Использование кислых сред с рН 4,5 и рН 1,2, также рекомендуемых для проведения теста сравнительной кинетики растворения, не является репрезентативным в отношении изучения высвобождения фебуксостата из его лекарственных форм в связи с его низкой растворимостью при данных значениях pH [14].
Перед использованием среды растворения деаэрировали нагреванием до температуры 41 °С при осторожном перемешивании и фильтрованием под вакуумом через нейлоновый мембранный фильтр с размером пор 0,45 мкм при энергичном перемешивании. После фильтрования продолжали воздействие вакуумом в течение 5 мин.
Для испытания в сосуд для растворения помещали единицу лекарственной формы (таблетку или капсулу). Для предупреждения всплывания таблеток и капсул на поверхность среды растворения использовали грузило из инертного материала, удерживающее лекарственную форму на дне сосуда. Через 5, 10, 15, 30 и 45 мин отбирали аликвоту раствора объемом 10,0 мл и фильтровали через нейлоновый фильтр с размером пор 0,45 мкм, отбрасывая первую порцию фильтрата. Объем среды сразу после отбора каждой пробы восполняли внесением по 10,0 мл свежей среды растворения и продолжали перемешивание.
Количественное определение фебуксостата в пробах проводили методом высокоэффективной жидкостной хроматографии на жидкостном хроматографе Dionex Ultimate 3000 с УФ-детектором VWD-3000 (Thermo Scientific, США) с колонкой Luna C18(2) размером 250×4,6 мм, зернение сорбента 5 мкм (Phenomenex, США). Подвижная фаза А – 0,1 М водный раствор аммония ацетата с рН 4,0, подвижная фаза B – ацетонитрил. Режим элюирования изократический, объемное соотношение подвижных фаз А и В 1:1.
Количество действующего вещества (фебуксостата), высвободившегося в среду растворения относительно заявленного содержания, в процентах (Х), рассчитывали по формуле (1):
X = S×α0×900×1×P = S×α0×P×9,
S0×L×10×10 S×L
где S – площадь пика фебуксостата на хроматограмме испытуемого раствора;
S0 – площадь пика фебуксостата на хроматограмме стандартного раствора;
α0 – навеска стандартного образца (СО) фебуксостата в миллиграммах;
P – содержание основного вещества в СО фебуксостата в процентах;
L – заявленное содержание фебуксостата в таблетке (капсуле) в миллиграммах.
Как следует из данных, представленных в табл. 1, композиции изучаемых лекарственных препаратов в основных аспектах схожи, что объясняется близостью используемых лекарственных форм. При некотором упрощении обе исследуемые лекарственные формы можно рассматривать как варианты «твердой лекарственной формы, заключенной в оболочку». С этой точки зрения становятся заметны аналогичные подходы в создании обеих композиций: использование микрокристаллической целлюлозы в качестве наполнителя, кроскармеллозы натрия в качестве разрыхлителя и сочетания кремния диоксида коллоидного и магния стеарата как веществ, способствующих скольжению. Вместе с тем в составах имеются и существенные различия.
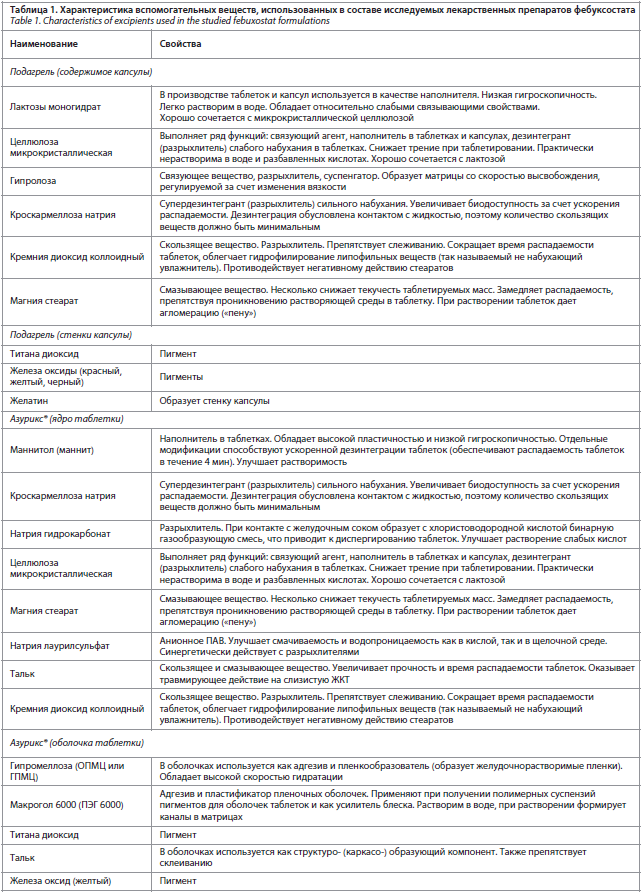
В связи с тем, что в доступных открытых источниках не удалось обнаружить количественные составы изучаемых лекарственных препаратов, было проведено только качественное сравнение составов. При этом в случае, если вспомогательное вещество выполняет несколько функций, то, в соответствии с рекомендациями «Правил проведения исследований биоэквивалентности лекарственных средств Евразийского экономического союза», его относили к той группе вспомогательных веществ, отличия в содержании для которой указаны как наиболее критичные [15]. Результаты представлены в табл. 2.
Качественное сопоставление составов изучаемых препаратов (см. табл. 2) позволяет выявить ряд отличий, которые могут оказывать значительное влияние на процессы распадаемости и растворения. Так, в качестве наполнителя в лекарственном препарате Подагрель использован лактозы моногидрат – «стандартный» наполнитель, основными технологическими преимуществами которого является хорошая сыпучесть и низкая гигроскопичность. В качестве наполнителя в лекарственном препарате Азурикс® используется маннитол, более характерный для жевательных таблеток из-за приятного вкуса. Однако для ряда модификаций маннитола указывается способность обеспечивать ускоренную распадаемость таблеток [10, 11].
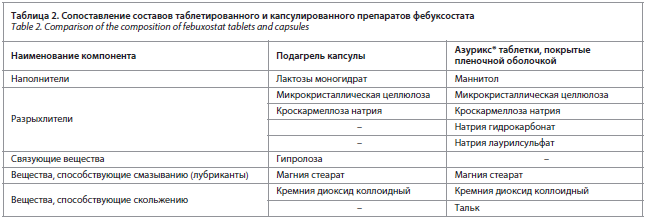
В качестве разрыхлителя в состав таблеток Азурикс® включен натрия гидрокарбонат, который при контакте с хлористоводородной кислотой желудочного сока образует бинарную газообразующую смесь «кислота – гидрокарбонат», вызывающую быструю распадаемость таблетки [16]. Кроме того, в составе лекарственного препарата Азурикс® используется смачивающее поверхностно активное вещество – натрия лаурилсульфат, также способствующее распадаемости. Таким образом, следует отметить, что Подагрель содержит только разрыхлители набухающего действия со слабым (микрокристаллическая целлюлоза) и сильным (кроскармеллоза натрия) набуханием. Лекарственный препарат Азурикс® дополнительно к указанным двум разрыхлителям содержит газообразующее вещество (натрия гидрокарбонат) и смачивающее вещество (натрия лаурилсульфат), что позволяет сделать предположение о более высокой скорости распадаемости данного лекарственного препарата, а значит прогнозировать более высокую биодоступность.
Вспомогательным веществом, для которого известно препятствование процессу смачивания, и, следовательно, растворению и распадаемости, является магния стеарат, представленный в композициях обоих лекарственных препаратов. Для снижения адгезии порошков и гранул к поверхностям оборудования магния стеарат в настоящее время наносят опудриванием поверхности частиц. Образующийся тонкий слой способствует скольжению частиц при контакте, однако одновременно препятствует смачиванию и проникновению воды.
Для нейтрализации негативного эффекта магния стеарата применяется другое известное скользящее вспомогательное вещество – коллоидный диоксид кремния, или аэросил. Для аэросила описано гидрофилирующее действие в отношении липофильных поверхностей, благодаря чему улучшается смачиваемость, что, в свою очередь, ведет к ускорению процессов распадаемости и растворения.
Оболочки, используемые в изучаемых лекарственных препаратах, также значительно отличаются. Лекарственный препарат Подагрель представляет собой твердые капсулы с крышечкой, оболочка которых образована желатином. Желатин растворяется в воде, проходя через стадию предварительного набухания. Оптимальной температурой для его растворения является температура выше 40 °C [16], что выходит за пределы физиологической нормы. В лекарственном препарате Азурикс® таблетки-ядра покрыты комбинированной оболочкой из гипромеллозы и макрогола 6000. Оба эти полимера достаточно быстро растворяются в воде, при этом для гипромеллозы указывается способность к быстрой гидратации, а для макрогола 6000 известна способность формировать в матрице, в которой он распределен, каналы, по которым может проникать вода [10]. Таким образом, качественные составы оболочек позволяют предположить более быстрое растворение пленочной оболочки таблеток Азурикс® по сравнению с желатиновой оболочкой капсул Подагрель.
В фармакологии этапы взаимодействия ЛС с организмом характеризуются аббревиатурой LADME, т.е. «высвобождение, всасывание, распределение, метаболизм и выведение». Все эти критерии влияют на кинетику воздействия ЛС на ткани и, следовательно, влияют на действие и фармакологическую активность соединения как ЛС. Однако критерий «высвобождение» в случае использования твердых ЛФ обусловлен двумя процессами – распадаемостью и растворением. Эти процессы тесно связаны, протекают в основном одновременно, однако имеют различный характер.
Распадаемость подразумевает механическое нарушение целостности твердой ЛФ (таблетки, капсулы и т.д.) и обусловлено технологическими особенностями получения конкретной ЛФ (способ и параметры получения, используемые ингредиенты).
Растворение, т.е. переход действующего вещества в форму отдельных молекул или ионов, является процессом физико-химическим и обусловлено свойствами и состоянием растворяемого вещества (кристалличность частиц, их размеры, объем распределения и др.) и условиями растворения (температуры, состава растворителя, pH и др.).
Для подтверждения гипотезы о различиях в скорости и характере распадаемости исследуемых лекарственных препаратов было проведено изучение распадаемости в статических условиях. Для фиксации процесса распадаемости использовалась фото- и видеосъемка на цифровую камеру с макрообъективом, позволяющая оценить происходящие морфологические изменения лекарственных форм при распаде в статических условиях (pH 1,2; 37,0±0,1 °C) и обеспечить визуализацию процесса распада изучаемых лекарственных препаратов.
При изучении лекарственного препарата Азурикс® (таблетки, покрытые оболочкой) были получены следующие результаты.
Таблетки, как объекты, обладающие высокой плотностью, полностью погружаются в среду, моделирующую желудочный сок.
В течение первых десяти с небольшим секунд (рис. 1) визуально не отмечается каких-либо изменений, однако в это время протекает процесс гидратации и частичного растворения оболочки.
На 15-й секунде (рис. 2, а) на поверхности оболочки начинают появляться пузырьки газа. С высокой долей вероятности это объясняется возникновением в пленочной оболочке таблетки микроканалов, через которые жидкая среда вступает в контакт с ядром таблетки. Формирование микроканалов в пленке, образованной гипромеллозой, может протекать благодаря наличию в ее составе молекул макрогола 6000, которые быстро гидратируются и служат своеобразным «проводником» жидкой фазы. Поступившая по микроканалу среда контактирует с корпусом таблетки, в результате чего одновременно запускается ряд процессов. Ключевую роль в дальнейшем распаде таблетки, по-видимому, играет процесс химического взаимодействия натрия гидрокарбоната с хлористоводородной кислотой, в результате чего и начинается газообразование.
На 20-й секунде (рис. 2, б) количество пузырьков газа на поверхности таблетки увеличивается, что свидетельствует об увеличении количества микроканалов в пленочной оболочке. Можно заметить, что пузырьки газа сосредоточены преимущественно на боковых гранях таблетки. Возможно, причина этого явления состоит в меньшей толщине оболочки на боковых поверхностях по сравнению с верхней и нижней плоскостями таблетки.
На 25-й секунде (рис. 3, а) газообразование усиливается настолько, что начинается отрыв пузырьков газа от поверхности таблетки. Кроме того, становится заметным процесс растворения оболочки, его можно зафиксировать визуально по окрашенным микропотокам жидкости.

На 30-й секунде (рис. 3, б) процессы газообразования и растворения приводят к нарушению целостности оболочки, которое происходит на боковых поверхностях таблетки.
На 35-й секунде (рис. 4, а) можно зафиксировать практически полный разрыв между нижней пленкой оболочки и ее боковыми частями из-за интенсивного газообразования. Отдельные фрагменты пленки при этом захватываются восходящим газо-жидкостным потоком и уносятся от таблетки.
На 40-й секунде (рис. 4, б) боковые поверхности таблетки обнажаются наполовину, газообразование протекает чрезвычайно активно, становится заметным начинающийся процесс деформации ядра таблетки в местах непосредственного контакта с жидкой средой.
На 45-й секунде (рис. 5, а) на боковой поверхности оболочки формируется второй разрыв – с пленкой верхней поверхности. Процесс газообразования протекает бурно с продолжающейся деформацией боковых стенок таблетки и уносом образующихся частиц восходящим газо-жидкостным потоком.
На 50-й секунде (рис. 5, б) процесс газообразования захватывает боковые поверхности практически полностью. Не растворившиеся остатки пленочной оболочки отрываются пузырьками газа и отслаиваются от поверхности таблетки. Следует отметить, что пленка нижней поверхности таблетки, контакт с жидкостью которой ограничен, формирует под таблеткой «подложку» со складчатым краем.
На 55-й секунде (рис. 6, а) боковые поверхности таблетки полностью лишены оболочки. Процесс распада таблетки идет быстро, благодаря активному газообразованию.
К концу 1-й минуты (рис. 6, б) корпус таблетки заметно деградировал и лежит на нижней пленке. Пленка верхней плоскости таблетки сильно деформирована за счет активного газообразования.

Через 1 мин 10 с (рис. 7, а) становится заметно разрушение остатков пленки на верхней плоскости таблетки. Модельная среда начинает насыщаться частичками таблетки, ранее унесенными газо-жидкостным потоком, а теперь оседающими. При этом активизируется процесс растворения образовавшихся изолированных частиц, из-за чего начинает нарастать мутность приемного раствора.
Через 1 мин 20 с (рис. 7, б) газо-жидкостный поток, формирующийся при взаимодействии натрия гидрокарбоната с хлористоводородной кислотой модельной среды, механически разрушает остатки пленочной оболочки на верхней плоскости таблетки. Процесс сопровождается отрывом фрагментов пленки и их уносом от таблетки.
Через 1,5 мин после внесения таблетки в модельную среду (рис. 8, а) происходит окончательное освобождение верхней поверхности таблетки от остатков пленочной оболочки (часть уносимого фрагмента можно заметить в верхней части фото).
Через 1 мин 40 с (рис. 8, б) таблетка практически полностью освобождена от пленочной оболочки (за исключением прилегающей к нижней части). Процесс распада сопровождается газообразованием, из-за чего в модельной среде формируются конвективные потоки, распределяющие отделяющиеся от таблетки частицы по всему объему. Мутность системы повышается, что обусловлено параллельно протекающим процессом распределения в среде высокомолекулярных компонентов таблетки.
В течение последующих 20 с вплоть до конца 2-й минуты (рис. 9, а и б) процесс распада таблетки протекает без изменений, сопровождается интенсивным газообразованием и отрывом от корпуса таблетки мелких частиц. Силуэт таблетки сохраняет контур в виде прямоугольника с закругленными краями.

После 2-й минуты (рис. 10) модельная среда приобретает вид тонкой суспензии с характерной опалесценцией, серьезно затрудняющей визуальное наблюдение за процессом распадаемости таблетки.
Через 2,5 мин (рис. 11, а) процесс распада таблетки продолжался совместно с газообразованием. Корпус таблетки заметно деформировался. Из-за восходящего тока жидкости, образуемого поднимающимися пузырьками газа, процесс разрушения не сопровождался «рассыпанием», так как отделяющиеся частицы захватывались и уносились от таблетки. Однако нарастающая мутность среды сделала невозможной дальнейшую фотосъемку (рис. 11, б).
Визуальное наблюдение позволило установить, что разрушение корпуса таблетки на отдельные фрагменты происходило после 4 мин выдерживания в модельной смеси, однако при этом сохранялось очаговое газообразование. Газообразование в модельных условиях прекращалось после 10 мин, что свидетельствовало о полном расходовании натрия гидрокарбоната в ходе реакции с хлористоводородной кислотой.
Таким образом, изучение распадаемости таблеток Азурикс® в статических условиях позволило установить, что ведущую роль в этом процессе играет газообразование, начинающееся с 10-й секунды попадания таблетки в среду, моделирующую желудочный сок, и протекающее в течение всего времени распада таблетки (примерно 4 мин) и далее, до полной нейтрализации натрия гидрокарбоната.
Из полученных данных можно сделать вывод, что после приема внутрь таблетки Азурикс® полностью распадаются в желудке по типу шипучих таблеток, и дальнейшее высвобождение (растворение) действующего компонента происходит уже из диспергированного состояния.
Изучение распадаемости лекарственного препарата Подагрель показало иную кинетику этого процесса. При попадании капсул в желудок они ведут себя идентично пищевым комкам, плавая в слое желудочного сока и на его поверхности. Идентичное поведение капсул Подагрель было зафиксировано в ходе эксперимента. При внесении в модельную среду капсулы плавали на поверхности, при этом постепенно набухала желатиновая оболочка.
Через 30 с (рис. 12, а) становится заметной набухание части капсулы, погруженной в модельную среду. На корпусе капсулы появляются небольшие деформации.
Через 1 мин (рис. 12, б) по окрашенным потокам жидкости можно зафиксировать начало процесса растворения оболочки и усилившуюся деформацию корпуса капсулы.

Через 1,5 мин (рис. 13, а) продолжающегося растворения и деформации оболочки в стенке капсулы появляется отверстие (белое пятно в левой нижней части капсулы на фото). Буквально через 1 с (рис. 13, б) сквозь образовавшееся отверстие начинает выходить воздух из капсулы, захватывая часть порошкообразного содержимого.
Через 2 мин (рис. 14, а) в сформировавшееся отверстие в левой части капсулы продолжает поступать среда. Становится заметным набухание видимой части содержимого капсулы. Внутренняя газовая среда смещается в правую часть капсулы, о чем свидетельствует небольшой перекос.
Через 2 мин 10 с (рис. 14, б) в оболочке капсулы формируется второе отверстие, в правой части.
Через 2,5 мин (рис. 15, а) из отверстия в правой части капсулы с пузырьками газовой среды выдавливается содержимое, которое в виде отдельных частиц оседает.
К 3-й минуте (рис. 15, б) отверстия формируют разрывы в капсуле. Отходят полукруглые части корпуса капсулы и ее крышечки. Через оба разрыва начинается эвакуация содержимого капсулы в виде отдельных крупинок, причем через правый, находящийся выше, содержимое выдавливается пневматически, за счет выхода газовой фазы.

Особенно хорошо пневматический характер выталкивания содержимого капсулы становится виден в ходе 4-й минуты (рис. 16), в конце которой заметен газовый пузырек, освободившийся от частиц порошка и удерживаемый частью крышечки капсулы. Через нижнее отверстие в капсуле видно, что ее содержимое набухло при контакте с жидкостью (рис. 16, б).
Дальнейший процесс распадаемости капсулы происходит за счет постепенного растворения желатиновой оболочки с увеличивающейся при этом поверхностью контакта между содержимым капсулы и окружающей жидкостью.
Через 6 мин (рис. 17, а) сохраняющая плавучесть капсула растворилась еще сильнее. Содержимое капсулы сильно набухло, скорее всего, за счет входящих в состав разрыхлителей. Высвобождение содержимого происходит в виде отдельных частиц, оседающих на дно емкости с формированием характерных «горок».
Через 7 мин (рис. 17, б) процесс продолжается без изменений. Оболочка капсулы продолжает постепенно растворяться, в результате чего в ней формируется новое отверстие в области края прилегания крышечки к корпусу. Содержимое продолжает высвобождаться из внутренней полости в виде отдельных частиц, часть из которых всплывает на поверхность, однако основная масса оседает.
Через 8 мин (рис. 18, а) основная масса содержимого нижней части капсулы вместе с не растворившимся фрагментом оболочки падает на дно в виде единого агломерата, по-видимому, за счет адгезии частиц содержимого между собой.
Через 9 мин (рис. 18, б) менее крупный агломерат отделяется и от верхней части капсулы. Становится заметным, что остатки содержимого располагаются в части, где толщина оболочки была наибольшей за счет наложения стенок крышечки и корпуса капсулы.

В течение следующих 3 мин (рис. 19, а) процесс распада капсулы развивается по сложившимся направлениям. Оболочка капсулы продолжает растворяться и за счет этого деформироваться. Этот процесс ускоряется за счет оставшейся части содержимого капсулы, своим весом оказывающего дополнительное воздействие на размягчившуюся оболочку. На 12-й минуте деформация кольцевидного остатка капсулы под механическим воздействием набухшего порошка хорошо заметна.
Через 14 мин (рис. 19, б) деформация кольцевидной части капсулы принимает такую форму, что за счет внутреннего откоса содержимое начинает соскальзывать и высыпаться.
Еще через 0,5 мин (общее время 14 мин 30 с) деформация оставшейся части капсулы приобретает характер разрыва, кольцевидный фрагмент раскрывается, полностью высвобождая остатки содержимого (рис. 20, а).
Через 19 мин от начала эксперимента (рис. 20, б) капсула разрушилась практически полностью, нижняя часть погружается, одновременно растворяясь, а верхний фрагмент с небольшой частью содержимого сохраняет плавучесть за счет удерживаемых пузырьков газовой фазы. При этом продолжается процесс медленного оседания порошка в виде отдельных частиц.
Следует отметить, что основная масса высвободившегося из капсул содержимого осела на дно модельной емкости и только незначительная часть была распределена в объеме в виде суспензионных частиц либо находилась на поверхности.

При сравнении кинетики распадаемости изучаемых лекарственных препаратов в статических условиях сразу становится видна значительная разница в характере и скорости протекания этих процессов. Согласно требованиям ГФ и таблетки, покрытые оболочкой, и капсулы должны распадаться в течение 30 мин. Однако таблетки Азурикс® за счет включения в их состав газообразующего натрия гидрокарбоната распадаются очень быстро, в течение 4 мин, при этом образуя взвесь частиц, распределенных во всем объеме модельной жидкости. Высокая мутность образующейся системы указывает на образование тонкодисперсных частиц и, возможно, активно протекающий процесс растворения компонентов таблетированной смеси.
Капсулы Подагрель распадаются значительно медленнее, проходя через стадию набухания и постепенного растворения желатиновой оболочки, за счет чего в ней формируются отверстия, через которые и начинает высвобождаться содержимое. Процесс эвакуации содержимого из капсулы при этом обеспечивается несколькими механизмами: разрушением оболочки капсулы в процессе ее растворения; взаимного выталкивания частиц из полости капсулы за счет увеличения их объема при набухании; выдавливания и уноса части содержимого при выходе из внутреннего объема капсулы газовой фазы. Высвобождающиеся при этом частицы преимущественно оседают, сохраняя достаточно плотное агломерированное состояние, в объеме приемной жидкости распределена незначительная их часть.
Исходя из результатов проверки распадаемости в статических условиях, можно выдвинуть гипотезу о более высоких биофармацевтических качествах лекарственного препарата Азурикс® в части времени наступления фармакотерапевтического эффекта за счет более высокой скорости распадаемости лекарственной формы и, как следствие, потенциально более быстрого растворения фебуксостата, т.е. высвобождения действующего компонента.
Кинетика процесса высвобождения in vitro фебуксостата из таблеток Азурикс® и капсул Подагрель в фосфатный буферный раствор с рН 6,0 графически отражена на рис. 21.
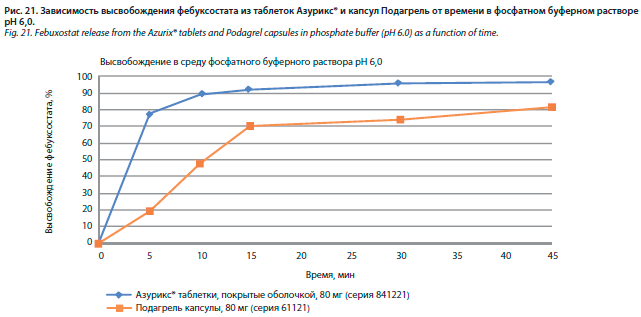
Как видно из представленных на рис. 21 кривых, отражающих кинетику процесса растворения (т.е. высвобождения) фебуксостата из изучаемых лекарственных препаратов, она значительно различается для таблеток и капсул. Кривая таблеток Азурикс® имеет значительный угол роста, что отражает высвобождение более 77% от дозы действующего вещества уже через 5 мин после помещения лекарственной формы в приемную среду. Во второй контрольной точке (10 мин) количество высвободившегося фебуксостата достигает величины 89% от дозы, а в третьей (15 мин) – превышает 90%, плавно нарастая в дальнейшем и достигая к 45 мин величины около 97% от дозы.
Иной характер имеет высвобождение фебуксостата из капсул. Первые 15 мин, в течение которых происходит распадаемость лекарственной формы, концентрация действующего вещества в приемной среде растет с равномерной скоростью, обеспечивая к 15-й мин высвобождение около 70% от дозы. Далее кривая выходит на «плато»: к 45-й минуте эксперимента степень высвобождения лишь немного превышает 80%.
Таким образом, следует отметить, что вид кинетических кривых высвобождения для таблеток Азурикс® и капсул Подагрель отличается значительно: точки «перелома» кривых разнесены по времени (5 мин для таблеток Азурикс® и 15 мин для капсул Подагрель), уровни «плато» также не совпадают (около 89–97% для таблеток Азурикс® и примерно 70–80% для капсул Подагрель).
Статистическую обработку результатов тестов сравнительной кинетики растворения осуществляли путем расчета среднего значения процента высвобождения фебуксостата и величин стандартного отклонения (S) и относительного стандартного отклонения (RSD). Все полученные данные были валидированы в соответствии с установленными требованиями. Для оценки эквивалентности кинетики высвобождения исследуемых лекарственных препаратов использовались следующие стандартные критерии [15, 17]:
1. Значение критерия f2 должно находиться в пределах от 50 до 100.
Фактор сходимости (коэффициент подобия) f2 рассчитывают по формуле (2):
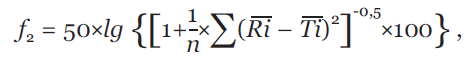
где n – число временных точек,
Ri – количество лекарственного средства, перешедшего в раствор из препарата сравнения (референтного препарата) в i-той временной точке, %;
Ti– количество лекарственного средства, перешедшего в раствор из испытуемого препарата в i-той временной точке,%.
Если в течение 15 мин в раствор высвободилось более 85% действующего вещества, то кинетика растворения признается сопоставимой без дальнейшего математического анализа данных.
2. Величина стандартного отклонения результатов, полученных для первой временной точки, не должна превышать 20%; для последующих точек не должна превышать 10%.
В результате было установлено, что при использовании в качестве среды растворения фосфатного буферного раствора рН 6,0 рассчитанное значение величины фактора сходимости f2 для лекарственного препарата Азурикс® и лекарственного препарата Подагрель составило 21,5, что находится вне диапазона от 50 до 100. Таким образом, полученные результаты свидетельствовали о неэквивалентности кинетики перехода действующего вещества в данную среду, что подтверждает превосходство таблетированной формы фебуксостата по данному показателю.
Величина RSD, рассчитанная по значениям процента высвобождения фебуксостата для лекарственных препаратов Азурикс® и Подагрель, составляла 2,4% и 19,6% соответственно, для первой временной точки, и 1,9% и 4,5% для остальных точек, что соответствует требованиям.
Данные исследования свидетельствуют о том, что высвобождение фебуксостата из лекарственного препарата Азурикс® и лекарственного препарата Подагрель в среду, моделирующую содержимое среднего отдела тонкого кишечника, происходило схожим образом. Так как значение степени высвобождения фебуксостата в раствор при использовании фосфатного буферного раствора с рН 6,8 превышало 85% через 15 мин во всех 12 использованных образцах, то кинетика перехода действующего вещества может быть признана эквивалентной без расчета фактора сходимости f2. При этом в случае лекарственного препарата Азурикс® за указанный промежуток времени полностью высвобождалась вся доза фебуксостата, в то время как для лекарственного препарата Подагрель – только около 90%.
Величина RSD, рассчитанная по значениям процента высвобождения фебуксостата для лекарственных препаратов Азурикс® и Подагрель, составляла 1,6% и 19,2% соответственно, для первой временной точки, и 1,0% и 5,3% для остальных точек, что соответствует требованиям.
Как следует из результатов сравнительного изучения кинетики растворения лекарственных препаратов Азурикс® (таблетки, покрытые оболочкой) и Подагрель (твердые желатиновые капсулы), показатели высвобождения фебуксостата из таблетированного препарата превосходили аналогичные показатели для капсул. Объяснение может заключаться в используемых композициях вспомогательных веществ, оказывающих значительное влияние на предшествующий растворению действующего компонента (т.е. собственно «высвобождение») процесс распадаемости лекарственной формы.
В результате изучения распадаемости исследуемых препаратов было установлено, что в таблетированном препарате пленочная оболочка, благодаря использованным вспомогательным веществам (гипромеллоза и макрогол 6000), быстро гидратируется, обеспечивая доступ жидкой среды к ядру таблетки. Контакт жидкой среды с ядром, в свою очередь, запускает химическую реакцию с одним из использованных в составе разрыхлителей – натрия гидрокарбонатом. Вступая во взаимодействие с компонентами модельных сред (кислотой хлористоводородной или гидрофосфатом) во всех поверхностях контакта, натрия гидрокарбонат выделяет углекислый газ. Именно газообразование с высокой долей вероятности обусловливает быструю распадаемость таблетки, что наряду с эффектом других использованных вспомогательных веществ (например, быстро растворимого наполнителя маннитола) обеспечивает переход применяемой лекарственной формы из твердого состояния в высокодисперсное. Находясь в форме микросуспензии, фебуксостат быстрее растворяется в приемной среде, что и фиксируется при дальнейшем химическом анализе.
При распадаемости капсулированного препарата процесс идет значительно медленнее. Это связано как с вспомогательным веществом, образующим стенки капсулы (желатин относится к высокомолекулярным веществам с ограниченной набухаемостью), так и собственно со строением капсулы. Так, при визуальном наблюдении за морфологией капсулы в ходе изучения распадаемости в статических условиях было установлено, что капсула распадается не равномерно, а на начальных этапах «раскрывается» по торцевым граням, где, по-видимому, толщина слоя желатина минимальна. При этом формируется «трубка», из которой содержимое капсулы высвобождается за счет нескольких механизмов: пневматически выталкивается выходящей газовой фазой при проникновении во внутренний объем капсулы жидкости; выталкивается за счет набухания и увеличения собственного объема; «высыпается» под действием силы тяжести за счет большего по сравнению с окружающей жидкостью удельного веса. Содержимое эвакуируется из капсулы в виде относительно компактных агломератов, формирующихся во внутренней полости капсулы при набухании разрыхляющих вспомогательных веществ в механически ограниченном стенками пространстве. Таким образом, после высвобождения из оболочки содержимое капсулы обладает относительно низкой удельной поверхностью, что и сказывается на скорости процесса растворения фебуксостата.
В случае рассматриваемых в статье ЛП следует учитывать два фактора:
1. Фебуксостат является веществом, растворимым в водной среде при pH 6 и выше.
2. ЛФ, в которых выпускается фебуксостат, относятся к пероральным формам «немедленного высвобождения», т.е. начинают распадаться и растворяться сразу после контакта с водными средами организма.
После приёма внутрь обе ЛФ начинают распадаться уже в желудке, а полученные экспериментальные результаты позволяют сделать вывод о полном механическом разрушении ЛФ за время нахождения в этом участке ЖКТ. Однако из физико-химических свойств фебуксостата следует, что его растворения при этом практически не происходит, т.к. растворимость фебуксостата при данных значениях pH (кислая среда) пренебрежимо мала.
Растворение фебуксостата происходит при pH 6 и выше, что соответствует условиям среднего отдела тонкого кишечника, куда ЛФ попадает уже в распавшемся состоянии. В этом случае на скорость растворения (а, следовательно, и всасывания растворённого вещества) будет оказывать влияние физическое состояние распавшейся ЛФ (размер частиц, наличие их агломератов и т.д.). Растворение фебуксостата из мелкодисперсного состояния будет протекать быстрее, чем из частиц крупного размера, объединённых в агломераты (комки), что подтверждалось тестами растворения.
Таким образом, можно заключить, что:
• с точки зрения реальной кинетики в ЖКТ поведение исследуемых ЛФ может быть описано следующим образом: желудок (распадаемость ЛФ) -> тонкий кишечник (растворение и всасывание фебуксостата);
• за время нахождения в среде желудка оба ЛП переходят в диспергированное состояние, однако растворимость фебуксостата в данных условиях пренебрежимо мала;
• в кишечник (место всасывания фебуксостата) оба препарата поступают в диспергированном состоянии, однако на кинетику растворения будет влиять характер образующихся в результате распадаемости частиц.
Благодаря композиции вспомогательных веществ таблетки Азурикс® полностью распадались в течение примерно 4 мин с образованием высокодисперсной системы (микросуспензии), обеспечивая, таким образом, в дальнейшем более высокую скорость перехода фебуксостата в раствор, что может рассматриваться как фактор, повышающий биодоступность действующего компонента. Капсулы Подагрель распадались значительно медленнее (около 14 мин) с образованием относительно плотных агломератов частиц. Кинетика растворения (in vitro) лекарственного препарата Азурикс® и лекарственного препарата Подагрель при использовании в качестве среды растворения фосфатного буферного раствора рН 6,0 (среда контроля качества) не являлась эквивалентной (фактор подобия составлял 21,5), при этом значения RSD, рассчитанные для первой и последующих точек, не превышали предельно допустимых значений.
При использовании в качестве среды растворения фосфатного буферного раствора рН 6,8 (имитирует среду среднего отдела тонкой кишки) кинетика растворения (in vitro) исследуемых лекарственных препаратов могла быть признана эквивалентной без расчета фактора сходимости f2 по факту высвобождения более 85% действующего вещества в течение 15 мин, однако в случае лекарственного препарата Азурикс® за указанный промежуток времени полностью высвобождалась вся доза фебуксостата, в то время как для лекарственного препарата Подагрель – только около 90%. Значения RSD, рассчитанные для первой и последующих точек, также не превышали предельно допустимых значений.
Как показало исследование процесса распадаемости, таблетированная форма в среде, моделирующей желудочный сок, образует тонкодисперсную систему, обеспечивая высокую удельную поверхность растворения и всасывания фебуксостата, что приводит к быстрому и полному переходу действующего компонента в раствор. Капсулированный препарат, в свою очередь, высвобождает композицию вспомогательных веществ и действующего компонента в виде крупнозернистых агломератов, обладающих относительно низкой удельной поверхностью, что может негативно влиять на параметры биодоступности.
Высокая скорость высвобождения действующего компонента лекарственного препарата является одним из факторов, обеспечивающих быстрое достижение уровня биодоступности, позволяющего врачу своевременно получать отклик на медикаментозную терапию в клинической практике.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах / Information about the authors
Ларский Михаил Владимирович – канд. фарм. наук, доц. каф. фармацевтической химии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: larsky.mikhail@gmail.com;
ORCID: 0000-0002-4406-7165
Mikhail V. Larsky – Cand. Sci. (Farm.), Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: larsky.mikhail@gmail.com;
ORCID: 0000-0002-4406-7165
Золотых Денис Сергеевич – канд. фарм. наук, доц. каф. токсикологической и аналитической химии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: metronidazol@mail.ru;
ORCID: 0000-0001-6186-1611
Denis S. Zolotykh – Cand. Sci. (Farm.), Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: metronidazol@mail.ru;
ORCID: 0000-0001-6186-1611
Чиряпкин Алексей Сергеевич – аспирант каф. органической химии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: alexey.chiriapkin@yandex.ru;
ORCID: 0000-0001-8207-2953
Aleksei S. Chiriapkin – Graduate Student, Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: alexey.chiriapkin@yandex.ru;
ORCID: 0000-0001-8207-2953
Верниковский Владислав Владиславович – канд. биол. наук, доц. каф. фармацевтической технологии с курсом медицинской биотехнологии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: v.v.vernikovsky@mail.ru;
ORCID: 0000-0002-0324-1999
Vladislav V. Vernikovsky – Cand. Sci. (Biol.), Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: v.v.vernikovsky@mail.ru;
ORCID: 0000-0002-0324-1999
Статья поступила в редакцию / The article received: 29.09.2022
Статья принята к печати / The article approved for publication: 27.10.2022
Клинический разбор в общей медицине №6 2022
Сравнительное биофармацевтическое исследование твердых лекарственных форм фебуксостата
Номера страниц в выпуске:78-95
Аннотация
Цель. Биофармацевтическая оценка лекарственных препаратов фебуксостата в виде различных твердых лекарственных форм (капсул и таблеток, покрытых оболочкой), включающая сравнение используемых в их составе вспомогательных веществ, процессов распадаемости в статических условиях и профилей кинетики растворения.
Материалы и методы. Объектом исследования стали покрытые оболочкой таблетки Азурикс® и твердые желатиновые капсулы Подагрель, содержащие фебуксостат в дозировке 80 мг. Для оценки процесса распадаемости лекарственных форм использовалась модель распадаемости в статических условиях. Количественное определение фебуксостата в пробах при исследовании сравнительной кинетики растворения проводили методом высокоэффективной жидкостной хроматографии.
Результаты. При оценке морфологических изменений лекарственных форм в статических условиях, моделирующих среду желудка, установлены различные характеры и скорости их распадаемости, подкрепленные отличиями в качественном составе использованных вспомогательных веществ. Изучение сравнительной кинетики растворения также показало разную скорость высвобождения фебуксостата из исследуемых лекарственных форм.
Выводы. Полученные результаты свидетельствуют о значимом влиянии композиции вспомогательных веществ на поведение лекарственных форм в средах организма и, в частности, на их распадаемость, что, в свою очередь, определяет скорость и степень высвобождения действующего компонента. Таким образом, тест демонстрирует выраженные отличия в биофармацевтических параметрах двух лекарственных форм фебуксостата, которые могут влиять на биодоступность изучаемых препаратов.
Ключевые слова: фебуксостат, таблетки, покрытые оболочкой, капсулы, высвобождение in vitro, распадаемость в статических условиях, высокоэффективная жидкостная хроматография.
Для цитирования: Ларский М.В., Золотых Д.С., Чиряпкин А.С., Верниковский В.В. Сравнительное биофармацевтическое исследование твердых лекарственных форм фебуксостата. Клинический разбор в общей медицине. 2022; 6: 78–95. DOI: 10.47407/kr2022.3.4.0012090p
Цель. Биофармацевтическая оценка лекарственных препаратов фебуксостата в виде различных твердых лекарственных форм (капсул и таблеток, покрытых оболочкой), включающая сравнение используемых в их составе вспомогательных веществ, процессов распадаемости в статических условиях и профилей кинетики растворения.
Материалы и методы. Объектом исследования стали покрытые оболочкой таблетки Азурикс® и твердые желатиновые капсулы Подагрель, содержащие фебуксостат в дозировке 80 мг. Для оценки процесса распадаемости лекарственных форм использовалась модель распадаемости в статических условиях. Количественное определение фебуксостата в пробах при исследовании сравнительной кинетики растворения проводили методом высокоэффективной жидкостной хроматографии.
Результаты. При оценке морфологических изменений лекарственных форм в статических условиях, моделирующих среду желудка, установлены различные характеры и скорости их распадаемости, подкрепленные отличиями в качественном составе использованных вспомогательных веществ. Изучение сравнительной кинетики растворения также показало разную скорость высвобождения фебуксостата из исследуемых лекарственных форм.
Выводы. Полученные результаты свидетельствуют о значимом влиянии композиции вспомогательных веществ на поведение лекарственных форм в средах организма и, в частности, на их распадаемость, что, в свою очередь, определяет скорость и степень высвобождения действующего компонента. Таким образом, тест демонстрирует выраженные отличия в биофармацевтических параметрах двух лекарственных форм фебуксостата, которые могут влиять на биодоступность изучаемых препаратов.
Ключевые слова: фебуксостат, таблетки, покрытые оболочкой, капсулы, высвобождение in vitro, распадаемость в статических условиях, высокоэффективная жидкостная хроматография.
Для цитирования: Ларский М.В., Золотых Д.С., Чиряпкин А.С., Верниковский В.В. Сравнительное биофармацевтическое исследование твердых лекарственных форм фебуксостата. Клинический разбор в общей медицине. 2022; 6: 78–95. DOI: 10.47407/kr2022.3.4.0012090p
The comparative biopharmaceutical study of febuxostat solid dosage forms
Mikhail V. Larsky, Denis S. Zolotykh, Aleksei S. Chiriapkin, Vladislav V. VernikovskyPyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University, Pyatigorsk, Russia
larsky.mikhail@gmail.com
Abstract
Aim. Biopharmaceutical assessment of various solid dosage forms (capsules and coated tablets) of febuxostat formulations including comparison of excipients used in these dosage forms, disintegration pathways under static conditions, and dissolution kinetic profiles.
Methods. The Azurix® coated tablets and Podagrel hard gelatin capsules containing 80 mg of febuxostat were the object of the study. The model of disintegration under static conditions was used to assess disintegration of the dosage forms. Quantification of febuxostat in the samples diring the comparative study of dissolution kinetics was performed by high-performance liquid chromatography.
Results. When assessing morphological changes of dosage forms in the static model developed to simulate gastric environment, various desintegration patterns and rates confirmed by the differences in the qualitative composition of the excipients used were defined for these dosage forms. The comparative kinetics study showed different rates of febuxostat release from the studied dosage forms.
Conclusion. The findings demonstrate a significant impact of the excipient composition on the behavior of dosage forms in the body environment, particularly on the dosage form desintegration, which in turn defines the rate and degree of the active ingredient release. Thus, the test shows pronounced differences in biopharmaceutical parameters, capable of affecting the studied drugs bioavailability, between two febuxostat dosage forms.
Key words: febuxostat, coated tablets, capsules, in vitro release, disintegration under static conditions, high-performance liquid chromatography.
For citation: For citation: Larsky M.V., Zolotykh D.S., Chiriapkin A.S., Vernikovsky V.V. The comparative biopharmaceutical study of febuxostat solid dosage forms. Clinical review for general practice. 2022; 6: 78–95. DOI: 10.47407/kr2022.3.4.0012090p
Введение
Повышенное содержание мочевой кислоты в сыворотке крови (гиперурикемия), вызванное рядом факторов, как алиментарных, так и генетических, может приводить к отложению кристаллов мочевой кислоты в суставах и околосуставных тканях и внутренних органах – подагре, которая является в настоящее время распространенным заболеванием [1]. Длительный повышенный уровень мочевой кислоты в крови связывается также с увеличением риска развития сердечно-сосудистых заболеваний (ишемическая болезнь сердца, сердечная недостаточность, фибрилляция предсердий) и уровня смертности от всех причин [2]. Результаты многолетних исследований указывают также на то, что высокий уровень мочевой кислоты является независимым фактором риска развития артериальной гипертензии [3]. Все это показывает на необходимость контроля и управления концентрацией мочевой кислоты в плазме крови человека.Фебуксостат представляет собой 2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксильную кислоту и является селективным непуриновым ингибитором ксантиноксиредуктазы (КОР) – фермента, участвующего в обмене пуринов, пиримидинов, птерина и альдегидных субстратов. Стойко и длительно подавляя активность КОР, фебуксостат блокирует превращение ксантина в мочевую кислоту, что приводит к снижению концентрации уратов в сыворотке крови [4].
Фармакокинетика фебуксостата изучена в основном с точки зрения его биодоступности (относительной), а также вопросов скорости и путей выведения из организма человека [1, 4, 5]. В то же время вопросы абсорбции фебуксостата освещены в литературе недостаточно, однако имеются сведения о том, что скорость достижения и величина максимальной концентрации в плазме крови прямо пропорциональна дозе фебуксостата в диапазоне от 10 до 240 мг [6]. Исходя из этого, на скорость всасывания фебуксостата может оказывать влияние скорость и степень его высвобождения из лекарственной формы.
В настоящее время при изучении биодоступности лекарственных препаратов внимание привлекают процессы, протекающие непосредственно после приема лекарственной формы, т.е. ее поведение в момент контакта с жидкостями пищеварительной системы. При этом отмечается, что характер и кинетика распадаемости имеют решающее значение для качества и эффективности пероральных твердых лекарственных форм.
Распад таблеток или капсул приводит к образованию твердых фрагментов и частиц в водной среде и предшествует растворению и высвобождению действующего компонента. Таким образом, процесс распадаемости твердой лекарственной формы предваряет дальнейшее поведение лекарственного средства в организме, описываемого классической схемой LADME(R). Вместе с тем констатируется, что закрепленные в нормативной документации методы оценки распадаемости и растворения не позволяют оценить протекающие при этом микропроцессы, например смачивание, проникновение влаги в лекарственную форму, а также набухание, что особенно важно при оценке эффективности введения в состав лекарственных форм супердезинтегрантов [7].
Для оценки способности таблеток высвобождать заключенный в них действующий компонент в Государственную фармакопею Российской Федерации XIV издания (ГФ) включен тест «Распадаемость» на модели так называемой «качающейся корзинки». Колебательные движения, создаваемые в емкости прибора для определения распадаемости, происходят в вертикальной плоскости при частоте 28–32 цикла в 1 мин (т.е. примерно 1 колебание каждые 2 с) и призваны моделировать перистальтику желудочно-кишечного тракта (ЖКТ). Однако, как и любая другая модель, «качающаяся корзинка» достаточно условна, а интенсивное механическое воздействие динамических потоков жидкости мешает в полной мере оценить процесс распада таблетки и влияние на него используемых вспомогательных веществ и технологических приемов.
В литературе описана модель изучения процесса распадаемости (дезинтеграции) твердых лекарственных форм в статичных условиях, в которых исключается искусственное движение жидкости, не позволяющее фиксировать отличия протекающих изменений для разных объектов исследования [8, 9].
Согласно данным литературы, величина pH среды в желудке составляет от 1,0 до 3,0, а время прохождения этого отдела ЖКТ лекарственным препаратом составляет 30–40 мин [10, 11]. Согласно рекомендациям ГФ таблетки, покрытые оболочкой, и капсулы должны распадаться в течение 30 мин. Исходя из этого, можно заключить, что процесс распада лекарственных форм (за исключением кишечнорастворимых) происходит именно в желудке человека. Таким образом, модель распадаемости в статичных условиях в среде 0,1 М раствора кислоты хлористоводородной описывает типичную ситуацию приема лекарственного препарата в виде твердой лекарственной формы (таблетки или капсулы), которая после проглатывания находится в состоянии относительного покоя в желудочном соке [12].
Целью настоящего исследования является сравнительная биофармацевтическая оценка лекарственных препаратов фебуксостата в виде различных твердых лекарственных форм (капсул и таблеток, покрытых оболочкой), включающая сравнение используемых вспомогательных веществ, процессов распадаемости лекарственных форм в статических условиях и профилей кинетики растворения.
Материалы и методы исследования
Процесс распадаемости твердых лекарственных форм в статических условиях изучали в соответствии с методиками, описанными в литературе [8, 9]. Для этого в стеклянную емкость объемом 1000 мл наливали модельную среду. Систему термостатировали при 37,0±0,1 °C в течение 30 мин, затем в среду помещали изучаемую твердую лекарственную форму (таблетку, капсулу) и визуально контролировали процесс распадаемости. Фиксацию результатов вели с помощью цифровой зеркальной фотокамеры Nikon D5100 с объективом для макросъемки.В качестве среды распадаемости был выбран 0,1 М раствор кислоты хлористоводородной (рН 1,2), имитирующий желудочный сок. Растворы с рН 4,5 и рН 6,8, моделирующие среду отделов кишечника, не использовались, поскольку распадаемость твердых лекарственных форм немедленного высвобождения происходит в среде желудка [10].
Для изучения кинетики растворения использовали тестер растворения РС-1 типа «Лопастная мешалка». Испытание проводили в соответствии с требованиями ОФС.1.4.2.0014.15 «Растворение для твердых дозированных лекарственных форм» [13]. Объем среды растворения – 900 мл, скорость вращения мешалки – 75 об/мин.
В качестве сред растворения выбраны фосфатные буферные растворы с рН 6,0 (среда контроля качества) и рН 6,8 (имитирует среду в среднем отделе тонкой кишки). Использование кислых сред с рН 4,5 и рН 1,2, также рекомендуемых для проведения теста сравнительной кинетики растворения, не является репрезентативным в отношении изучения высвобождения фебуксостата из его лекарственных форм в связи с его низкой растворимостью при данных значениях pH [14].
Перед использованием среды растворения деаэрировали нагреванием до температуры 41 °С при осторожном перемешивании и фильтрованием под вакуумом через нейлоновый мембранный фильтр с размером пор 0,45 мкм при энергичном перемешивании. После фильтрования продолжали воздействие вакуумом в течение 5 мин.
Для испытания в сосуд для растворения помещали единицу лекарственной формы (таблетку или капсулу). Для предупреждения всплывания таблеток и капсул на поверхность среды растворения использовали грузило из инертного материала, удерживающее лекарственную форму на дне сосуда. Через 5, 10, 15, 30 и 45 мин отбирали аликвоту раствора объемом 10,0 мл и фильтровали через нейлоновый фильтр с размером пор 0,45 мкм, отбрасывая первую порцию фильтрата. Объем среды сразу после отбора каждой пробы восполняли внесением по 10,0 мл свежей среды растворения и продолжали перемешивание.
Количественное определение фебуксостата в пробах проводили методом высокоэффективной жидкостной хроматографии на жидкостном хроматографе Dionex Ultimate 3000 с УФ-детектором VWD-3000 (Thermo Scientific, США) с колонкой Luna C18(2) размером 250×4,6 мм, зернение сорбента 5 мкм (Phenomenex, США). Подвижная фаза А – 0,1 М водный раствор аммония ацетата с рН 4,0, подвижная фаза B – ацетонитрил. Режим элюирования изократический, объемное соотношение подвижных фаз А и В 1:1.
Количество действующего вещества (фебуксостата), высвободившегося в среду растворения относительно заявленного содержания, в процентах (Х), рассчитывали по формуле (1):
X = S×α0×900×1×P = S×α0×P×9,
S0×L×10×10 S×L
где S – площадь пика фебуксостата на хроматограмме испытуемого раствора;
S0 – площадь пика фебуксостата на хроматограмме стандартного раствора;
α0 – навеска стандартного образца (СО) фебуксостата в миллиграммах;
P – содержание основного вещества в СО фебуксостата в процентах;
L – заявленное содержание фебуксостата в таблетке (капсуле) в миллиграммах.
Результаты и их обсуждение
При оценке биоэквивалентности лекарственных препаратов значительное внимание уделяется различиям по качественному и сопоставимости по количественному составу используемых вспомогательных веществ [15]. Для проведения данной оценки было проведено изучение свойств вспомогательных веществ, использованных в изучаемых лекарственных препаратах. Результаты, полученные при использовании литературных источников [10, 11, 16], представлены в табл. 1.Как следует из данных, представленных в табл. 1, композиции изучаемых лекарственных препаратов в основных аспектах схожи, что объясняется близостью используемых лекарственных форм. При некотором упрощении обе исследуемые лекарственные формы можно рассматривать как варианты «твердой лекарственной формы, заключенной в оболочку». С этой точки зрения становятся заметны аналогичные подходы в создании обеих композиций: использование микрокристаллической целлюлозы в качестве наполнителя, кроскармеллозы натрия в качестве разрыхлителя и сочетания кремния диоксида коллоидного и магния стеарата как веществ, способствующих скольжению. Вместе с тем в составах имеются и существенные различия.

В связи с тем, что в доступных открытых источниках не удалось обнаружить количественные составы изучаемых лекарственных препаратов, было проведено только качественное сравнение составов. При этом в случае, если вспомогательное вещество выполняет несколько функций, то, в соответствии с рекомендациями «Правил проведения исследований биоэквивалентности лекарственных средств Евразийского экономического союза», его относили к той группе вспомогательных веществ, отличия в содержании для которой указаны как наиболее критичные [15]. Результаты представлены в табл. 2.
Качественное сопоставление составов изучаемых препаратов (см. табл. 2) позволяет выявить ряд отличий, которые могут оказывать значительное влияние на процессы распадаемости и растворения. Так, в качестве наполнителя в лекарственном препарате Подагрель использован лактозы моногидрат – «стандартный» наполнитель, основными технологическими преимуществами которого является хорошая сыпучесть и низкая гигроскопичность. В качестве наполнителя в лекарственном препарате Азурикс® используется маннитол, более характерный для жевательных таблеток из-за приятного вкуса. Однако для ряда модификаций маннитола указывается способность обеспечивать ускоренную распадаемость таблеток [10, 11].

В качестве разрыхлителя в состав таблеток Азурикс® включен натрия гидрокарбонат, который при контакте с хлористоводородной кислотой желудочного сока образует бинарную газообразующую смесь «кислота – гидрокарбонат», вызывающую быструю распадаемость таблетки [16]. Кроме того, в составе лекарственного препарата Азурикс® используется смачивающее поверхностно активное вещество – натрия лаурилсульфат, также способствующее распадаемости. Таким образом, следует отметить, что Подагрель содержит только разрыхлители набухающего действия со слабым (микрокристаллическая целлюлоза) и сильным (кроскармеллоза натрия) набуханием. Лекарственный препарат Азурикс® дополнительно к указанным двум разрыхлителям содержит газообразующее вещество (натрия гидрокарбонат) и смачивающее вещество (натрия лаурилсульфат), что позволяет сделать предположение о более высокой скорости распадаемости данного лекарственного препарата, а значит прогнозировать более высокую биодоступность.
Вспомогательным веществом, для которого известно препятствование процессу смачивания, и, следовательно, растворению и распадаемости, является магния стеарат, представленный в композициях обоих лекарственных препаратов. Для снижения адгезии порошков и гранул к поверхностям оборудования магния стеарат в настоящее время наносят опудриванием поверхности частиц. Образующийся тонкий слой способствует скольжению частиц при контакте, однако одновременно препятствует смачиванию и проникновению воды.
Для нейтрализации негативного эффекта магния стеарата применяется другое известное скользящее вспомогательное вещество – коллоидный диоксид кремния, или аэросил. Для аэросила описано гидрофилирующее действие в отношении липофильных поверхностей, благодаря чему улучшается смачиваемость, что, в свою очередь, ведет к ускорению процессов распадаемости и растворения.
Оболочки, используемые в изучаемых лекарственных препаратах, также значительно отличаются. Лекарственный препарат Подагрель представляет собой твердые капсулы с крышечкой, оболочка которых образована желатином. Желатин растворяется в воде, проходя через стадию предварительного набухания. Оптимальной температурой для его растворения является температура выше 40 °C [16], что выходит за пределы физиологической нормы. В лекарственном препарате Азурикс® таблетки-ядра покрыты комбинированной оболочкой из гипромеллозы и макрогола 6000. Оба эти полимера достаточно быстро растворяются в воде, при этом для гипромеллозы указывается способность к быстрой гидратации, а для макрогола 6000 известна способность формировать в матрице, в которой он распределен, каналы, по которым может проникать вода [10]. Таким образом, качественные составы оболочек позволяют предположить более быстрое растворение пленочной оболочки таблеток Азурикс® по сравнению с желатиновой оболочкой капсул Подагрель.
В фармакологии этапы взаимодействия ЛС с организмом характеризуются аббревиатурой LADME, т.е. «высвобождение, всасывание, распределение, метаболизм и выведение». Все эти критерии влияют на кинетику воздействия ЛС на ткани и, следовательно, влияют на действие и фармакологическую активность соединения как ЛС. Однако критерий «высвобождение» в случае использования твердых ЛФ обусловлен двумя процессами – распадаемостью и растворением. Эти процессы тесно связаны, протекают в основном одновременно, однако имеют различный характер.
Распадаемость подразумевает механическое нарушение целостности твердой ЛФ (таблетки, капсулы и т.д.) и обусловлено технологическими особенностями получения конкретной ЛФ (способ и параметры получения, используемые ингредиенты).
Растворение, т.е. переход действующего вещества в форму отдельных молекул или ионов, является процессом физико-химическим и обусловлено свойствами и состоянием растворяемого вещества (кристалличность частиц, их размеры, объем распределения и др.) и условиями растворения (температуры, состава растворителя, pH и др.).
Для подтверждения гипотезы о различиях в скорости и характере распадаемости исследуемых лекарственных препаратов было проведено изучение распадаемости в статических условиях. Для фиксации процесса распадаемости использовалась фото- и видеосъемка на цифровую камеру с макрообъективом, позволяющая оценить происходящие морфологические изменения лекарственных форм при распаде в статических условиях (pH 1,2; 37,0±0,1 °C) и обеспечить визуализацию процесса распада изучаемых лекарственных препаратов.
При изучении лекарственного препарата Азурикс® (таблетки, покрытые оболочкой) были получены следующие результаты.
Таблетки, как объекты, обладающие высокой плотностью, полностью погружаются в среду, моделирующую желудочный сок.
В течение первых десяти с небольшим секунд (рис. 1) визуально не отмечается каких-либо изменений, однако в это время протекает процесс гидратации и частичного растворения оболочки.
На 15-й секунде (рис. 2, а) на поверхности оболочки начинают появляться пузырьки газа. С высокой долей вероятности это объясняется возникновением в пленочной оболочке таблетки микроканалов, через которые жидкая среда вступает в контакт с ядром таблетки. Формирование микроканалов в пленке, образованной гипромеллозой, может протекать благодаря наличию в ее составе молекул макрогола 6000, которые быстро гидратируются и служат своеобразным «проводником» жидкой фазы. Поступившая по микроканалу среда контактирует с корпусом таблетки, в результате чего одновременно запускается ряд процессов. Ключевую роль в дальнейшем распаде таблетки, по-видимому, играет процесс химического взаимодействия натрия гидрокарбоната с хлористоводородной кислотой, в результате чего и начинается газообразование.
На 20-й секунде (рис. 2, б) количество пузырьков газа на поверхности таблетки увеличивается, что свидетельствует об увеличении количества микроканалов в пленочной оболочке. Можно заметить, что пузырьки газа сосредоточены преимущественно на боковых гранях таблетки. Возможно, причина этого явления состоит в меньшей толщине оболочки на боковых поверхностях по сравнению с верхней и нижней плоскостями таблетки.
На 25-й секунде (рис. 3, а) газообразование усиливается настолько, что начинается отрыв пузырьков газа от поверхности таблетки. Кроме того, становится заметным процесс растворения оболочки, его можно зафиксировать визуально по окрашенным микропотокам жидкости.

На 30-й секунде (рис. 3, б) процессы газообразования и растворения приводят к нарушению целостности оболочки, которое происходит на боковых поверхностях таблетки.
На 35-й секунде (рис. 4, а) можно зафиксировать практически полный разрыв между нижней пленкой оболочки и ее боковыми частями из-за интенсивного газообразования. Отдельные фрагменты пленки при этом захватываются восходящим газо-жидкостным потоком и уносятся от таблетки.
На 40-й секунде (рис. 4, б) боковые поверхности таблетки обнажаются наполовину, газообразование протекает чрезвычайно активно, становится заметным начинающийся процесс деформации ядра таблетки в местах непосредственного контакта с жидкой средой.
На 45-й секунде (рис. 5, а) на боковой поверхности оболочки формируется второй разрыв – с пленкой верхней поверхности. Процесс газообразования протекает бурно с продолжающейся деформацией боковых стенок таблетки и уносом образующихся частиц восходящим газо-жидкостным потоком.
На 50-й секунде (рис. 5, б) процесс газообразования захватывает боковые поверхности практически полностью. Не растворившиеся остатки пленочной оболочки отрываются пузырьками газа и отслаиваются от поверхности таблетки. Следует отметить, что пленка нижней поверхности таблетки, контакт с жидкостью которой ограничен, формирует под таблеткой «подложку» со складчатым краем.
На 55-й секунде (рис. 6, а) боковые поверхности таблетки полностью лишены оболочки. Процесс распада таблетки идет быстро, благодаря активному газообразованию.
К концу 1-й минуты (рис. 6, б) корпус таблетки заметно деградировал и лежит на нижней пленке. Пленка верхней плоскости таблетки сильно деформирована за счет активного газообразования.

Через 1 мин 10 с (рис. 7, а) становится заметно разрушение остатков пленки на верхней плоскости таблетки. Модельная среда начинает насыщаться частичками таблетки, ранее унесенными газо-жидкостным потоком, а теперь оседающими. При этом активизируется процесс растворения образовавшихся изолированных частиц, из-за чего начинает нарастать мутность приемного раствора.
Через 1 мин 20 с (рис. 7, б) газо-жидкостный поток, формирующийся при взаимодействии натрия гидрокарбоната с хлористоводородной кислотой модельной среды, механически разрушает остатки пленочной оболочки на верхней плоскости таблетки. Процесс сопровождается отрывом фрагментов пленки и их уносом от таблетки.
Через 1,5 мин после внесения таблетки в модельную среду (рис. 8, а) происходит окончательное освобождение верхней поверхности таблетки от остатков пленочной оболочки (часть уносимого фрагмента можно заметить в верхней части фото).
Через 1 мин 40 с (рис. 8, б) таблетка практически полностью освобождена от пленочной оболочки (за исключением прилегающей к нижней части). Процесс распада сопровождается газообразованием, из-за чего в модельной среде формируются конвективные потоки, распределяющие отделяющиеся от таблетки частицы по всему объему. Мутность системы повышается, что обусловлено параллельно протекающим процессом распределения в среде высокомолекулярных компонентов таблетки.
В течение последующих 20 с вплоть до конца 2-й минуты (рис. 9, а и б) процесс распада таблетки протекает без изменений, сопровождается интенсивным газообразованием и отрывом от корпуса таблетки мелких частиц. Силуэт таблетки сохраняет контур в виде прямоугольника с закругленными краями.

После 2-й минуты (рис. 10) модельная среда приобретает вид тонкой суспензии с характерной опалесценцией, серьезно затрудняющей визуальное наблюдение за процессом распадаемости таблетки.
Через 2,5 мин (рис. 11, а) процесс распада таблетки продолжался совместно с газообразованием. Корпус таблетки заметно деформировался. Из-за восходящего тока жидкости, образуемого поднимающимися пузырьками газа, процесс разрушения не сопровождался «рассыпанием», так как отделяющиеся частицы захватывались и уносились от таблетки. Однако нарастающая мутность среды сделала невозможной дальнейшую фотосъемку (рис. 11, б).
Визуальное наблюдение позволило установить, что разрушение корпуса таблетки на отдельные фрагменты происходило после 4 мин выдерживания в модельной смеси, однако при этом сохранялось очаговое газообразование. Газообразование в модельных условиях прекращалось после 10 мин, что свидетельствовало о полном расходовании натрия гидрокарбоната в ходе реакции с хлористоводородной кислотой.
Таким образом, изучение распадаемости таблеток Азурикс® в статических условиях позволило установить, что ведущую роль в этом процессе играет газообразование, начинающееся с 10-й секунды попадания таблетки в среду, моделирующую желудочный сок, и протекающее в течение всего времени распада таблетки (примерно 4 мин) и далее, до полной нейтрализации натрия гидрокарбоната.
Из полученных данных можно сделать вывод, что после приема внутрь таблетки Азурикс® полностью распадаются в желудке по типу шипучих таблеток, и дальнейшее высвобождение (растворение) действующего компонента происходит уже из диспергированного состояния.
Изучение распадаемости лекарственного препарата Подагрель показало иную кинетику этого процесса. При попадании капсул в желудок они ведут себя идентично пищевым комкам, плавая в слое желудочного сока и на его поверхности. Идентичное поведение капсул Подагрель было зафиксировано в ходе эксперимента. При внесении в модельную среду капсулы плавали на поверхности, при этом постепенно набухала желатиновая оболочка.
Через 30 с (рис. 12, а) становится заметной набухание части капсулы, погруженной в модельную среду. На корпусе капсулы появляются небольшие деформации.
Через 1 мин (рис. 12, б) по окрашенным потокам жидкости можно зафиксировать начало процесса растворения оболочки и усилившуюся деформацию корпуса капсулы.

Через 1,5 мин (рис. 13, а) продолжающегося растворения и деформации оболочки в стенке капсулы появляется отверстие (белое пятно в левой нижней части капсулы на фото). Буквально через 1 с (рис. 13, б) сквозь образовавшееся отверстие начинает выходить воздух из капсулы, захватывая часть порошкообразного содержимого.
Через 2 мин (рис. 14, а) в сформировавшееся отверстие в левой части капсулы продолжает поступать среда. Становится заметным набухание видимой части содержимого капсулы. Внутренняя газовая среда смещается в правую часть капсулы, о чем свидетельствует небольшой перекос.
Через 2 мин 10 с (рис. 14, б) в оболочке капсулы формируется второе отверстие, в правой части.
Через 2,5 мин (рис. 15, а) из отверстия в правой части капсулы с пузырьками газовой среды выдавливается содержимое, которое в виде отдельных частиц оседает.
К 3-й минуте (рис. 15, б) отверстия формируют разрывы в капсуле. Отходят полукруглые части корпуса капсулы и ее крышечки. Через оба разрыва начинается эвакуация содержимого капсулы в виде отдельных крупинок, причем через правый, находящийся выше, содержимое выдавливается пневматически, за счет выхода газовой фазы.

Особенно хорошо пневматический характер выталкивания содержимого капсулы становится виден в ходе 4-й минуты (рис. 16), в конце которой заметен газовый пузырек, освободившийся от частиц порошка и удерживаемый частью крышечки капсулы. Через нижнее отверстие в капсуле видно, что ее содержимое набухло при контакте с жидкостью (рис. 16, б).
Дальнейший процесс распадаемости капсулы происходит за счет постепенного растворения желатиновой оболочки с увеличивающейся при этом поверхностью контакта между содержимым капсулы и окружающей жидкостью.
Через 6 мин (рис. 17, а) сохраняющая плавучесть капсула растворилась еще сильнее. Содержимое капсулы сильно набухло, скорее всего, за счет входящих в состав разрыхлителей. Высвобождение содержимого происходит в виде отдельных частиц, оседающих на дно емкости с формированием характерных «горок».
Через 7 мин (рис. 17, б) процесс продолжается без изменений. Оболочка капсулы продолжает постепенно растворяться, в результате чего в ней формируется новое отверстие в области края прилегания крышечки к корпусу. Содержимое продолжает высвобождаться из внутренней полости в виде отдельных частиц, часть из которых всплывает на поверхность, однако основная масса оседает.
Через 8 мин (рис. 18, а) основная масса содержимого нижней части капсулы вместе с не растворившимся фрагментом оболочки падает на дно в виде единого агломерата, по-видимому, за счет адгезии частиц содержимого между собой.
Через 9 мин (рис. 18, б) менее крупный агломерат отделяется и от верхней части капсулы. Становится заметным, что остатки содержимого располагаются в части, где толщина оболочки была наибольшей за счет наложения стенок крышечки и корпуса капсулы.

В течение следующих 3 мин (рис. 19, а) процесс распада капсулы развивается по сложившимся направлениям. Оболочка капсулы продолжает растворяться и за счет этого деформироваться. Этот процесс ускоряется за счет оставшейся части содержимого капсулы, своим весом оказывающего дополнительное воздействие на размягчившуюся оболочку. На 12-й минуте деформация кольцевидного остатка капсулы под механическим воздействием набухшего порошка хорошо заметна.
Через 14 мин (рис. 19, б) деформация кольцевидной части капсулы принимает такую форму, что за счет внутреннего откоса содержимое начинает соскальзывать и высыпаться.
Еще через 0,5 мин (общее время 14 мин 30 с) деформация оставшейся части капсулы приобретает характер разрыва, кольцевидный фрагмент раскрывается, полностью высвобождая остатки содержимого (рис. 20, а).
Через 19 мин от начала эксперимента (рис. 20, б) капсула разрушилась практически полностью, нижняя часть погружается, одновременно растворяясь, а верхний фрагмент с небольшой частью содержимого сохраняет плавучесть за счет удерживаемых пузырьков газовой фазы. При этом продолжается процесс медленного оседания порошка в виде отдельных частиц.
Следует отметить, что основная масса высвободившегося из капсул содержимого осела на дно модельной емкости и только незначительная часть была распределена в объеме в виде суспензионных частиц либо находилась на поверхности.

При сравнении кинетики распадаемости изучаемых лекарственных препаратов в статических условиях сразу становится видна значительная разница в характере и скорости протекания этих процессов. Согласно требованиям ГФ и таблетки, покрытые оболочкой, и капсулы должны распадаться в течение 30 мин. Однако таблетки Азурикс® за счет включения в их состав газообразующего натрия гидрокарбоната распадаются очень быстро, в течение 4 мин, при этом образуя взвесь частиц, распределенных во всем объеме модельной жидкости. Высокая мутность образующейся системы указывает на образование тонкодисперсных частиц и, возможно, активно протекающий процесс растворения компонентов таблетированной смеси.
Капсулы Подагрель распадаются значительно медленнее, проходя через стадию набухания и постепенного растворения желатиновой оболочки, за счет чего в ней формируются отверстия, через которые и начинает высвобождаться содержимое. Процесс эвакуации содержимого из капсулы при этом обеспечивается несколькими механизмами: разрушением оболочки капсулы в процессе ее растворения; взаимного выталкивания частиц из полости капсулы за счет увеличения их объема при набухании; выдавливания и уноса части содержимого при выходе из внутреннего объема капсулы газовой фазы. Высвобождающиеся при этом частицы преимущественно оседают, сохраняя достаточно плотное агломерированное состояние, в объеме приемной жидкости распределена незначительная их часть.
Исходя из результатов проверки распадаемости в статических условиях, можно выдвинуть гипотезу о более высоких биофармацевтических качествах лекарственного препарата Азурикс® в части времени наступления фармакотерапевтического эффекта за счет более высокой скорости распадаемости лекарственной формы и, как следствие, потенциально более быстрого растворения фебуксостата, т.е. высвобождения действующего компонента.
Кинетика процесса высвобождения in vitro фебуксостата из таблеток Азурикс® и капсул Подагрель в фосфатный буферный раствор с рН 6,0 графически отражена на рис. 21.

Как видно из представленных на рис. 21 кривых, отражающих кинетику процесса растворения (т.е. высвобождения) фебуксостата из изучаемых лекарственных препаратов, она значительно различается для таблеток и капсул. Кривая таблеток Азурикс® имеет значительный угол роста, что отражает высвобождение более 77% от дозы действующего вещества уже через 5 мин после помещения лекарственной формы в приемную среду. Во второй контрольной точке (10 мин) количество высвободившегося фебуксостата достигает величины 89% от дозы, а в третьей (15 мин) – превышает 90%, плавно нарастая в дальнейшем и достигая к 45 мин величины около 97% от дозы.
Иной характер имеет высвобождение фебуксостата из капсул. Первые 15 мин, в течение которых происходит распадаемость лекарственной формы, концентрация действующего вещества в приемной среде растет с равномерной скоростью, обеспечивая к 15-й мин высвобождение около 70% от дозы. Далее кривая выходит на «плато»: к 45-й минуте эксперимента степень высвобождения лишь немного превышает 80%.
Таким образом, следует отметить, что вид кинетических кривых высвобождения для таблеток Азурикс® и капсул Подагрель отличается значительно: точки «перелома» кривых разнесены по времени (5 мин для таблеток Азурикс® и 15 мин для капсул Подагрель), уровни «плато» также не совпадают (около 89–97% для таблеток Азурикс® и примерно 70–80% для капсул Подагрель).
Статистическую обработку результатов тестов сравнительной кинетики растворения осуществляли путем расчета среднего значения процента высвобождения фебуксостата и величин стандартного отклонения (S) и относительного стандартного отклонения (RSD). Все полученные данные были валидированы в соответствии с установленными требованиями. Для оценки эквивалентности кинетики высвобождения исследуемых лекарственных препаратов использовались следующие стандартные критерии [15, 17]:
1. Значение критерия f2 должно находиться в пределах от 50 до 100.
Фактор сходимости (коэффициент подобия) f2 рассчитывают по формуле (2):
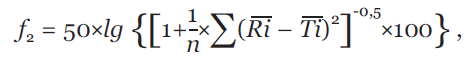
где n – число временных точек,
Ri – количество лекарственного средства, перешедшего в раствор из препарата сравнения (референтного препарата) в i-той временной точке, %;
Ti– количество лекарственного средства, перешедшего в раствор из испытуемого препарата в i-той временной точке,%.
Если в течение 15 мин в раствор высвободилось более 85% действующего вещества, то кинетика растворения признается сопоставимой без дальнейшего математического анализа данных.
2. Величина стандартного отклонения результатов, полученных для первой временной точки, не должна превышать 20%; для последующих точек не должна превышать 10%.
В результате было установлено, что при использовании в качестве среды растворения фосфатного буферного раствора рН 6,0 рассчитанное значение величины фактора сходимости f2 для лекарственного препарата Азурикс® и лекарственного препарата Подагрель составило 21,5, что находится вне диапазона от 50 до 100. Таким образом, полученные результаты свидетельствовали о неэквивалентности кинетики перехода действующего вещества в данную среду, что подтверждает превосходство таблетированной формы фебуксостата по данному показателю.
Величина RSD, рассчитанная по значениям процента высвобождения фебуксостата для лекарственных препаратов Азурикс® и Подагрель, составляла 2,4% и 19,6% соответственно, для первой временной точки, и 1,9% и 4,5% для остальных точек, что соответствует требованиям.
Данные исследования свидетельствуют о том, что высвобождение фебуксостата из лекарственного препарата Азурикс® и лекарственного препарата Подагрель в среду, моделирующую содержимое среднего отдела тонкого кишечника, происходило схожим образом. Так как значение степени высвобождения фебуксостата в раствор при использовании фосфатного буферного раствора с рН 6,8 превышало 85% через 15 мин во всех 12 использованных образцах, то кинетика перехода действующего вещества может быть признана эквивалентной без расчета фактора сходимости f2. При этом в случае лекарственного препарата Азурикс® за указанный промежуток времени полностью высвобождалась вся доза фебуксостата, в то время как для лекарственного препарата Подагрель – только около 90%.
Величина RSD, рассчитанная по значениям процента высвобождения фебуксостата для лекарственных препаратов Азурикс® и Подагрель, составляла 1,6% и 19,2% соответственно, для первой временной точки, и 1,0% и 5,3% для остальных точек, что соответствует требованиям.
Как следует из результатов сравнительного изучения кинетики растворения лекарственных препаратов Азурикс® (таблетки, покрытые оболочкой) и Подагрель (твердые желатиновые капсулы), показатели высвобождения фебуксостата из таблетированного препарата превосходили аналогичные показатели для капсул. Объяснение может заключаться в используемых композициях вспомогательных веществ, оказывающих значительное влияние на предшествующий растворению действующего компонента (т.е. собственно «высвобождение») процесс распадаемости лекарственной формы.
В результате изучения распадаемости исследуемых препаратов было установлено, что в таблетированном препарате пленочная оболочка, благодаря использованным вспомогательным веществам (гипромеллоза и макрогол 6000), быстро гидратируется, обеспечивая доступ жидкой среды к ядру таблетки. Контакт жидкой среды с ядром, в свою очередь, запускает химическую реакцию с одним из использованных в составе разрыхлителей – натрия гидрокарбонатом. Вступая во взаимодействие с компонентами модельных сред (кислотой хлористоводородной или гидрофосфатом) во всех поверхностях контакта, натрия гидрокарбонат выделяет углекислый газ. Именно газообразование с высокой долей вероятности обусловливает быструю распадаемость таблетки, что наряду с эффектом других использованных вспомогательных веществ (например, быстро растворимого наполнителя маннитола) обеспечивает переход применяемой лекарственной формы из твердого состояния в высокодисперсное. Находясь в форме микросуспензии, фебуксостат быстрее растворяется в приемной среде, что и фиксируется при дальнейшем химическом анализе.
При распадаемости капсулированного препарата процесс идет значительно медленнее. Это связано как с вспомогательным веществом, образующим стенки капсулы (желатин относится к высокомолекулярным веществам с ограниченной набухаемостью), так и собственно со строением капсулы. Так, при визуальном наблюдении за морфологией капсулы в ходе изучения распадаемости в статических условиях было установлено, что капсула распадается не равномерно, а на начальных этапах «раскрывается» по торцевым граням, где, по-видимому, толщина слоя желатина минимальна. При этом формируется «трубка», из которой содержимое капсулы высвобождается за счет нескольких механизмов: пневматически выталкивается выходящей газовой фазой при проникновении во внутренний объем капсулы жидкости; выталкивается за счет набухания и увеличения собственного объема; «высыпается» под действием силы тяжести за счет большего по сравнению с окружающей жидкостью удельного веса. Содержимое эвакуируется из капсулы в виде относительно компактных агломератов, формирующихся во внутренней полости капсулы при набухании разрыхляющих вспомогательных веществ в механически ограниченном стенками пространстве. Таким образом, после высвобождения из оболочки содержимое капсулы обладает относительно низкой удельной поверхностью, что и сказывается на скорости процесса растворения фебуксостата.
В случае рассматриваемых в статье ЛП следует учитывать два фактора:
1. Фебуксостат является веществом, растворимым в водной среде при pH 6 и выше.
2. ЛФ, в которых выпускается фебуксостат, относятся к пероральным формам «немедленного высвобождения», т.е. начинают распадаться и растворяться сразу после контакта с водными средами организма.
После приёма внутрь обе ЛФ начинают распадаться уже в желудке, а полученные экспериментальные результаты позволяют сделать вывод о полном механическом разрушении ЛФ за время нахождения в этом участке ЖКТ. Однако из физико-химических свойств фебуксостата следует, что его растворения при этом практически не происходит, т.к. растворимость фебуксостата при данных значениях pH (кислая среда) пренебрежимо мала.
Растворение фебуксостата происходит при pH 6 и выше, что соответствует условиям среднего отдела тонкого кишечника, куда ЛФ попадает уже в распавшемся состоянии. В этом случае на скорость растворения (а, следовательно, и всасывания растворённого вещества) будет оказывать влияние физическое состояние распавшейся ЛФ (размер частиц, наличие их агломератов и т.д.). Растворение фебуксостата из мелкодисперсного состояния будет протекать быстрее, чем из частиц крупного размера, объединённых в агломераты (комки), что подтверждалось тестами растворения.
Таким образом, можно заключить, что:
• с точки зрения реальной кинетики в ЖКТ поведение исследуемых ЛФ может быть описано следующим образом: желудок (распадаемость ЛФ) -> тонкий кишечник (растворение и всасывание фебуксостата);
• за время нахождения в среде желудка оба ЛП переходят в диспергированное состояние, однако растворимость фебуксостата в данных условиях пренебрежимо мала;
• в кишечник (место всасывания фебуксостата) оба препарата поступают в диспергированном состоянии, однако на кинетику растворения будет влиять характер образующихся в результате распадаемости частиц.
Заключение
В результате проведенных исследований было установлено, что кинетика распадаемости в статических условиях (in vitro) лекарственного препарата Азурикс® (таблетки, покрытые оболочкой) и лекарственного препарата Подагрель (твердые желатиновые капсулы) при использовании в качестве модельной среды 0,1 М раствора кислоты хлористоводородной (аналогична желудочному соку) значительно различалась.Благодаря композиции вспомогательных веществ таблетки Азурикс® полностью распадались в течение примерно 4 мин с образованием высокодисперсной системы (микросуспензии), обеспечивая, таким образом, в дальнейшем более высокую скорость перехода фебуксостата в раствор, что может рассматриваться как фактор, повышающий биодоступность действующего компонента. Капсулы Подагрель распадались значительно медленнее (около 14 мин) с образованием относительно плотных агломератов частиц. Кинетика растворения (in vitro) лекарственного препарата Азурикс® и лекарственного препарата Подагрель при использовании в качестве среды растворения фосфатного буферного раствора рН 6,0 (среда контроля качества) не являлась эквивалентной (фактор подобия составлял 21,5), при этом значения RSD, рассчитанные для первой и последующих точек, не превышали предельно допустимых значений.
При использовании в качестве среды растворения фосфатного буферного раствора рН 6,8 (имитирует среду среднего отдела тонкой кишки) кинетика растворения (in vitro) исследуемых лекарственных препаратов могла быть признана эквивалентной без расчета фактора сходимости f2 по факту высвобождения более 85% действующего вещества в течение 15 мин, однако в случае лекарственного препарата Азурикс® за указанный промежуток времени полностью высвобождалась вся доза фебуксостата, в то время как для лекарственного препарата Подагрель – только около 90%. Значения RSD, рассчитанные для первой и последующих точек, также не превышали предельно допустимых значений.
Выводы
Различные лекарственные средства, содержащие в качестве главного действующего вещества фебуксостат, демонстрируют отличные биофармацевтические параметры, в частности общее количество действующего вещества, высвобождаемого в течение периода распадаемости лекарственной формы. Так, таблетка препарата Азурикс® показывает равномерный процесс распадаемости за более короткое время, а также большее количество действующего вещества, высвобождаемого из нее за все время проводимого теста растворения. Сочетание этих факторов позволяет прогнозировать более высокий уровень биодоступности действующего компонента у таблетированного препарата по сравнению с лекарственным препаратом в виде капсул и более быстрое время наступления фармакологического эффекта.Как показало исследование процесса распадаемости, таблетированная форма в среде, моделирующей желудочный сок, образует тонкодисперсную систему, обеспечивая высокую удельную поверхность растворения и всасывания фебуксостата, что приводит к быстрому и полному переходу действующего компонента в раствор. Капсулированный препарат, в свою очередь, высвобождает композицию вспомогательных веществ и действующего компонента в виде крупнозернистых агломератов, обладающих относительно низкой удельной поверхностью, что может негативно влиять на параметры биодоступности.
Высокая скорость высвобождения действующего компонента лекарственного препарата является одним из факторов, обеспечивающих быстрое достижение уровня биодоступности, позволяющего врачу своевременно получать отклик на медикаментозную терапию в клинической практике.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах / Information about the authors
Ларский Михаил Владимирович – канд. фарм. наук, доц. каф. фармацевтической химии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: larsky.mikhail@gmail.com;
ORCID: 0000-0002-4406-7165
Mikhail V. Larsky – Cand. Sci. (Farm.), Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: larsky.mikhail@gmail.com;
ORCID: 0000-0002-4406-7165
Золотых Денис Сергеевич – канд. фарм. наук, доц. каф. токсикологической и аналитической химии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: metronidazol@mail.ru;
ORCID: 0000-0001-6186-1611
Denis S. Zolotykh – Cand. Sci. (Farm.), Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: metronidazol@mail.ru;
ORCID: 0000-0001-6186-1611
Чиряпкин Алексей Сергеевич – аспирант каф. органической химии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: alexey.chiriapkin@yandex.ru;
ORCID: 0000-0001-8207-2953
Aleksei S. Chiriapkin – Graduate Student, Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: alexey.chiriapkin@yandex.ru;
ORCID: 0000-0001-8207-2953
Верниковский Владислав Владиславович – канд. биол. наук, доц. каф. фармацевтической технологии с курсом медицинской биотехнологии Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ. E-mail: v.v.vernikovsky@mail.ru;
ORCID: 0000-0002-0324-1999
Vladislav V. Vernikovsky – Cand. Sci. (Biol.), Pyatigorsk Medical and Pharmaceutical Institute – branch of Volgograd Medical State University. E-mail: v.v.vernikovsky@mail.ru;
ORCID: 0000-0002-0324-1999
Статья поступила в редакцию / The article received: 29.09.2022
Статья принята к печати / The article approved for publication: 27.10.2022
Список исп. литературыСкрыть список1. Петрова М.С., Мазуров В.И., Инамова О.В. Фебуксостат для лечения хронической гиперурикемии у пациентов, страдающих подагрой. Медицинский Совет. 2017; 17: 114–22. DOI: 10.21518/2079-701X-2017-17-114-122
[Petrova M.S., Mazurov V.I., Inamova O.V. Febuksostat dlia lecheniia khronicheskoi giperurikemii u patsientov, stradaiushchikh podagroi. Meditsinskii Sovet. 2017; 17: 114–22. DOI: 10.21518/2079-701X-2017-17-114-122 (in Russian).]
2. Молчанова О.В., Бритов А.Н., Платонова Е.В. Значение повышенного уровня мочевой кислоты в развитии и профилактике хронических неинфекционных заболеваний. Профилактическая медицина. 2020; 23 (2): 102–8. DOI: 10.17116/profmed20202 3021102
[Molchanova O.V., Britov A.N., Platonova E.V. Znachenie povyshennogo urovnia mochevoi kisloty v razvitii i profilaktike khronicheskikh neinfektsionnykh zabolevanii. Profilakticheskaia meditsina. 2020; 23 (2): 102–8. DOI: 10.17116/profmed20202 3021102 (in Russian).]
3. Подпалова О.В., Деев А.Д., Журова О.Н. и др. Повышенный уровень мочевой кислоты как независимый фактор риска развития артериальной гипертензии (по данным 5-летнего проспективного исследования). Кардиология в Беларуси. 2019: 11 (4): 567–75.
[Podpalova O.V., Deev A.D., Zhurova O.N. et al. Povyshennyi uroven' mochevoi kisloty kak nezavisimyi faktor riska razvitiia arterial'noi gipertenzii (po dannym 5-letnego prospektivnogo issledovaniia). Kardiologiia v Belarusi. 2019: 11 (4): 567–75 (in Russian).]
4. Ильиных Е.В., Владимиров С.А., Елисеев М.С. Фебуксостат в терапии подагры: от теории к практике. Современная ревматология. 2017; 11 (4): 83–8. DOI: 10.14412/1996-7012-2017-4-83-88
[Il'inykh E.V., Vladimirov S.A., Eliseev M.S. Febuksostat v terapii podagry: ot teorii k praktike. Sovremennaia revmatologiia. 2017; 11 (4): 83–8. DOI: 10.14412/1996-7012-2017-4-83-88 (in Russian).]
5. Kamel B, Graham GG, Stocker SL et al. A pharmacokinetic-pharmacodynamic study of a single dose of febuxostat in healthy subjects. Br J Clin Pharmacol 2020; 86: 2486–96. DOI: 10.1111/bcp.14357
6. Kamel B, Graham GG, Williams KM et al. Clinical pharmacokinetics and pharmacodynamics of febuxostat. Clin Pharmacokinet 2017; 56: 459–75. DOI: 10.1007/s40262-016-0466-4
7. Berardi A, Bisharat L, Quodbach J et al. Advancing the understanding of the tablet disintegration phenomenon – An update on recent studies. International Journal of Pharmaceutics 2021; 598. DOI: 10.1016/j.ijpharm.2021.120390
8. Deng L, Fu Y. Seeing Is Believing: Time-Lapse Macro-Imaging of Morphological Changes of Solid Dosages as a Teaching and Research Tool. Pharmaceutical Research 2022; 39: 1019–24. DOI: 10.1007/ s11095-022-03271-5
9. Malallah O, Rashid Z, Li CL et al. Digital Image Disintegration Analysis: A Novel Quality Control Method for Fast Disintegrating Tablets. AAPS PharmSciTech 2021; 22 (219). DOI: 10.1208/s12249-021-02080-0
10. Алексеев К.В., Кедик С.А., Блынская Е.В. и др. Фармацевтическая технология. Твердые лекарственные формы. Под ред. С.А. Кедика. М.: Изд-во ЗАО «Институт фармацевтических технологий», 2011.
[Alekseev K.V., Kedik S.A., Blynskaia E.V. et al. Farmatsevticheskaia tekhnologiia. Tverdye lekarstvennye formy. Pod red. S.A. Kedika. Moscow: Izd-vo ZAO "Institut farmatsevticheskikh tekhnologii', 2011 (in Russian).]
11. Алексеев К.В., Кедик С.А., Блынская Е.В. и др. Фармацевтическая технология. Таблетки. Под ред. С.А. Кедика. М.: ЗАО ИФТ, 2015.
[Alekseev K.V., Kedik S.A., Blynskaia E.V. et al. Farmatsevticheskaia tekhnologiia. Tabletki. Pod red. S.A. Kedika. Moscow: ZAO IFT, 2015 (in Russian).]
12. Ураков А.Л., Николенко В.Н., Решетников А.П. и др. Физико-химические характеристики таблеток: факторы местного раздражающего действия. Фармация. 2019; 68 (8): 52–6. DOI: 10.29296/25419218-2019-08-09
[Urakov A.L., Nikolenko V.N., Reshetnikov A.P. et al. Fiziko-khimicheskie kharakteristiki tabletok: faktory mestnogo razdrazhaiushchego deistviia. Farmatsiia. 2019; 68 (8): 52–6. DOI: 10.29296/25419218-2019-08-09 (in Russian).]
13. Растворение для твердых дозированных лекарственных форм. Т. 2. Государственная фармакопея Российской Федерации XIV изд. ОФС.1.4.2.0014.15. М., 2018. С. 2164–82. URL: https://femb.ru/ record/pharmacopea14
[Rastvorenie dlia tverdykh dozirovannykh lekarstvennykh form. T. 2. Gosudarstvennaia farmakopeia Rossiiskoi Federatsii XIV izd. OFS.1.4.2.0014.15. Moscow, 2018. P. 2164–82. URL: https://femb.ru/ record/pharmacopea14 (in Russian).]
14. ФС «Фебуксостат, таблетки» (проект). URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/053/199/original/ФС_Фебуксостат__таблетки_08.12.2020.docx?1607683123
[FS "Febuksostat, tabletki" (proekt). URL: https://static-0.minzdrav. gov.ru/system/attachments/attaches/000/053/199/original/FS_Febuksostat__tabletki_08.12.2020.docx?1607683123 (in Russian).]
15. Правила проведения исследований биоэквивалентности лекарственных средств Евразийского экономического союза (утв. Решением Совета Евразийской экономической комиссии от 03.11.2016 №85; в ред. Решения Совета Евразийской экономической комиссии от 04.09.2020 №67). URL: https://www.alta.ru/tamdoc/16sr0085/
[Pravila provedeniia issledovanii bioekvivalentnosti lekarstvennykh sredstv Evraziiskogo ekonomicheskogo soiuza (utv. Resheniem Soveta Evraziiskoi ekonomicheskoi komissii ot 03.11.2016 №85; v red. Resheniia Soveta Evraziiskoi ekonomicheskoi komissii ot 04.09.2020 №67). URL: https://www.alta.ru/tamdoc/16sr0085/ (in Russian).]
16. Sheskey PJ, Cook WG, Cable CG. Handbook of pharmaceutical excipients. Eighth edition. London: Pharmaceutical Press, 2017.
17. Руководство по экспертизе лекарственных средств. Том III. М.: Полиграф-Плюс, 2014. С. 217–24.
[Rukovodstvo po ekspertize lekarstvennykh sredstv. Tom III. Moscow: Poligraf-Plius, 2014. P. 217–24 (in Russian).]
29 декабря 2022
Количество просмотров: 1174


