Клинический разбор в общей медицине №8 2023
Julia G. Patraman2, Marianna R. Mazra1, Alexander A. Kopelev1, Tamara O. Myshlyaeva1
1 Pirogov Russian National Research Medical University, Moscow, Russia;
2 Bauman City Clinical Hospital No29, Moscow, Russia
mazra.marianna@yandex.ru
Abstract
Waldenström macroglobulinemia (WM) is a type of plasma cell disease that is a malignant B-cell lymphoplasmacytic lymphoma. In patients with WM, immunological blood tests may remain unchanged for a while without pathological changes, but then tumor infiltration of the bone marrow gradually leads to anemia and thrombocytopenia. This patient has anemic syndrome according to clinical and laboratory examination, in which a number of diseases were diagnosed. An early diagnostic method, electrophoresis allows the consideration of immunoproliferative disorders with monoclonal IgM. Immunotyping is widely used with the eye chart of gammopathies using antisera to light (G, A, M) and light (kappa, lambda) chains of immunoglobulins. An increase in blood vessels IgM > 30 g/l, when identified with neurological symptoms of the source, associate these manifestations with hyperviscosity syndrome in WM.
Key words: macroglobulinemia, plasma cell diseases, hyperviscosity syndrome, monoclonal IgM, immunoproliferative disorders.
For citation: Khokhlova S.M., Pasyuta O.N., Chervyakova Ju.B. et al. Macroglobulinemia: hidden by anemia (clinical case report). Clinical review for general practice. 2023; 4 (8): 101–105 (In Russ.). DOI: 10.47407/kr2023.4.8.00337
В настоящий момент МВ встречается крайне редко с ежегодной заболеваемостью от 3 до 4 случаев на миллион человек, что составляет примерно 2% от всех гематологических злокачественных новообразований. Данная патология распространена среди пожилых людей в возрасте 65–80 лет, преимущественно у лиц мужского пола, при соотношении мужчин и женщин 2,3 : 1 [3, 4].
Этиология МВ до конца не изучена, однако существует несколько факторов ее развития, к которым относятся генетическая предрасположенность (дефект Т-клеточной супрессорной функции, мутация в генах MYD8, CXCR4), влияние радиационных воздействий, химических мутагенов и вирусов (вирус иммунодефицита человека, гепатита С), риккетсий [5–7].
Ключевую роль в патогенезе МВ играет соматическая гипермутация вариабельного района тяжелой цепи генов ИГ, а именно 3 семейство (VH3-гены ИГ), в результате чего возникает диспропорциональная пролиферация одного клона БК и ПК с продукцией только IgM. БК памяти в стадии постфолликулярной дифференцировки с преимущественной экспрессией CD27+ считается структурной единицей опухоли при данном процессе. Однако эта теория подвергается критике, так как у некоторых больных МВ опухоль состоит из наивных БК, экспрессирующих не только CD27+ рецептор, но и CD5+, СD19+, CD20+, CD22+, CD25+ и др. [5, 8].
В клинической картине МВ преобладают симптомы, присущие ЛПЗ (B-симптомы): лихорадка, ночная потливость, слабость, снижение массы тела, лимфаденопатия и гепатоспленомегалия (которых может и не отмечаться), также часто наблюдается артралгия. Отдельную группу составляют симптомы, связанные с отложением IgМ в тканях, а именно клубочках почек, кишечнике, коже, что может проявляться протеинурией, диареей, появлением кожных папул или узлов. В редких случаях у пациента можно обнаружить холодовые гемагглютинины, которые при взаимодействии с антигенами эритроцитов при низкой температуре вызывают гемолитическую анемию или положительную пробу Кумбса, синдром Рейно, холодовую крапивницу [9, 10].
Более того, определяется характерная лимфоидная инфильтрация костного мозга, лимфатических узлов, печени, селезенки, а также наличие в сыворотке крови избыточного количества IgM. При повышении уровня IgM>30 г/л возникает синдром гипервязкости, характеризующийся в основном неврологической симптоматикой (слабость, снижение памяти, ухудшение зрения, парезы и другие нейропатии), повышенной кровоточивостью кожи и слизистых оболочек. Возможно развитие сердечной недостаточности вследствие увеличения объема плазмы крови [2, 3, 10–12].
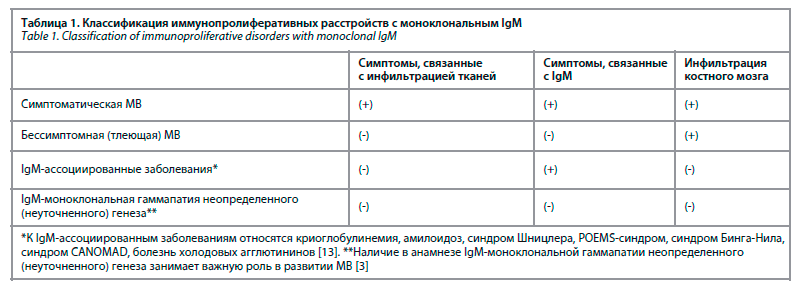
Для подтверждения диагноза МВ, необходимо выявить в крови моноклональный IgM и инфильтрацию костного мозга малыми лимфоцитами, плазмоцитоидными и ПК. Важно отметить, что гиперпродукция IgM не всегда указывает на МВ, так как есть ряд других иммунопролиферативных расстройств (табл. 1), связанных с IgM [3, 10, 13].
При постановке диагноза МВ рекомендуется назначение лечения врачом-онкогематологом. Основными подходами являются плазмаферез при синдроме гипервязкости, поддержка глюкокортикоидами для снижения опухолевой нагрузки и индивидуальный подбор химиотерапии. В настоящее время наиболее широко применяется ритуксимаб как в монорежиме, так и комбинациях [3–5].

Учитывая вялотекущее развитие МВ, большая часть пациентов не нуждается в немедленной терапии после постановки диагноза. По современным данным, не рекомендуется начинать медикаментозное лечение только на основании уровня IgM, поскольку его повышение не всегда коррелирует с клиническими проявлениями. Однако начало терапии целесообразно у пациентов, у которых наблюдается повышение концентрации IgM наряду с признаками или симптомами, связанными с прогрессированием заболевания (табл. 2).
Лечение противоопухолевыми препаратами с глюкокортикоидами должно проводиться как можно скорее, так как при терапии только плазмаферезом уровни IgM повысятся и вернутся к исходному уровню в течение 4 нед [14].
При анализе описанных ранее случаев МВ (А.Т. Фиясь и соавт., А.К. Ильющенко и соавт., Н.Я. Дзеранова и соавт., N. Kolikkat и соавт.), где авторами также проводилось сопоставление с литературными данными, лишь в одном (зарубежном) источнике приведен сходный с нашим случай, но там для постановки диагноза, так как отмечался клинико-гематологически только анемический синдром, потребовалось больше времени и анализ результатов миелограммы с иммуногистохимическим исследованием. В отечественных наблюдениях присутствовали органные поражения, диагностическая концепция МВ фигурировала, зачастую, в качестве основной, затруднение же представляло дифференцировать ее от миело- (МПЗ) и/или ЛПЗ [8, 12, 15]. Приводим собственный клинический случай МВ у пожилого пациента с клинической манифестацией под маской анемии.
При осмотре: состояние средней степени тяжести. Рост – 172 см, масса – 62 кг (индекс Кетле 20,9 кг/м2). Температура тела – 36,8 °С. Кожа и видимые слизистые чистые, бледные, обычной влажности. Лимфаденопатии, отеков нет. В легких дыхание везикулярное, проводится равномерно по всем отделам, хрипы не выслушиваются, частота дыхательных движений (ЧДД) – 18 в 1 минуту, сатурация 96%. Тоны сердца приглушены, ритм правильный, шумы не определяются, частота сердечных сокращений – 66 в мин, АД – 130/80 мм рт. ст. Живот мягкий, безболезненный. Печень и селезенка физикально не изменены. Стул и мочеиспускание без особенностей. Очаговой и менингеальной симптоматики, а также признаков поражения черепных нервов и компрессии спинного мозга и нервных корешков не выявлено.
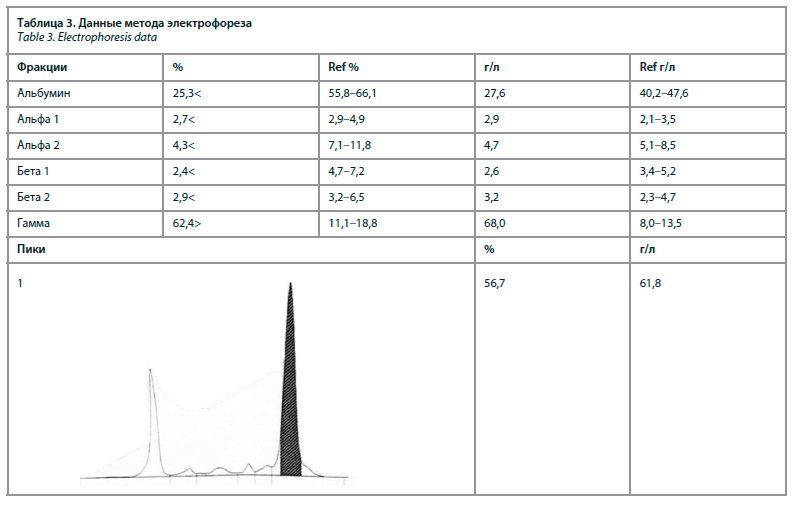
Проведено дообследование. Клинический анализ крови: сохранение гипохромной нормоцитарной анемии Hb 80→82 г/л, тромбоцитопении 99→57×109/л, СОЭ – 90 мм/ч. Биохимический анализ крови: общий белок 108,4→109 г/л, трансферрин 1,65→1,41 г/л, общая железосвязывающая способность – 43,8 мкмоль/л, железо – 12,2 мкмоль/л, прямая проба Кумбса положительная, прочие показатели крови без патологических изменений. Проведен электрофорез (табл. 3), по данным которого была подтверждена диспротеинемия с увеличением доли гамма-глобулинов до 62,4% (68,0 г/л) от общего белка, т.е. подтверждено наличие МП. В результате иммунотипирования МП был идентифицирован как полноразмерный моноклональный IgM lambda.
По данным рентгенографии плоских костей черепа и таза от 14.09.2023, эндоскопии: эзофагогастродуоденоскопии от 13.09.2023 и колоноскопии от 17.09.2023 – патологии не выявлено, что позволило исключить ММ; МПЗ и ЛПЗ результаты обследования также не соответствовали. Был выставлен диагноз МВ, пациент консультирован гематологом и переведен в онкогематологическое отделение, где на момент написания статьи проводится подбор химиотерапии, сеансы плазмафереза с положительным эффектом в виде уменьшения выраженности болевого синдрома.
Направление на исключение анемии хронических заболеваний (которая в типичном своем проявлении нормоцитарная и нормохромная) позволило выявить значимую гиперпротеинемию, приведшую к смене диагностической концепции: протеинограмма позволила обнаружить МП, а иммунотипирование установило, что он является моноклональным IgM. Это, а также отсутствие по результатам дополнительного обследования признаков ММ, МПЗ и ЛПЗ, дало основания установить диагноз МВ, а боль, послужившую причиной обращения, связать с синдромом гипервязкости.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Хохлова Светлана Михайловна – студентка 6-го курса, каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: cxoxlova@inbox.ru; ORCID: 0009-0003-1110-0971
Svetlana M. Khokhlova – Student, Pirogov Russian National Research Medical University. E-mail: cxoxlova@inbox.ru; ORCID: 0009-0003-1110-0971
Пасюта Ольга Николаевна – студентка 6-го курса, каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: olechkapasuta@gmail.com; ORCID: 0009-0000-2839-5970
Olga N. Pasyuta – Student, Pirogov Russian National Research Medical University. E-mail: olechkapasuta@gmail.com; ORCID: 0009-0000-2839-5970
Червякова Юлия Борисовна – канд. мед. наук, доц., каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: chervyakova_j@mail.ru; ORCID: 0000-0003-0069-4260
Julia B. Chervyakova – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: chervyakova_j@mail.ru; ORCID: 0000-0003-0069-4260
Громова Маргарита Александровна – канд. мед. наук, доц. каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: margarita-gromov@mail.ru; ORCID: 0000-0002-3757-058X
Margarita A. Gromova – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: margarita-gromov@mail.ru; ORCID: 0000-0002-3757-058X
Патраман Юлия Георгиевна – врач-терапевт, 4-е терапевтическое отделение, ГБУЗ «ГКБ №29 им. Н.Э. Баумана». E- mail: iuliya_02_07@mail.ru; ORCID: 0009-0009-5136-4860
Julia G. Patraman – The general practitioner, Bauman Clinical City Hospital No29. E- mail: iuliya_02_07@mail.ru; ORCID: 0009-0009-5136-4860
Мазра Марианна Рамазиевна – студентка 6-го курса, каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: mazra.marianna@yandex.ru; ORCID: 0000-0001-8064-2406
Marianna R. Mazra – Student, Pirogov Russian National Research Medical University. E-mail: mazra.marianna@yandex.ru; ORCID: 0000-0001-8064-2406
Копелев Александр Александрович – канд. мед. наук, доц. каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: akopelev@mail.ru; ORCID: 0000-0002-4328-3384
Alexander A. Kopelev – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: akopelev@mail.ru; ORCID: 0000-0002-4328-3384
Мышляева Тамара Олеговна – канд. мед. наук, ассистент каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: tlixa@mail.ru; ORCID: 0009-0005-8437-7482
Tamara O. Myshlyaeva – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: tlixa@mail.ru; ORCID: 0009-0005-8437-7482
Поступила в редакцию: 07.11.2023
Поступила после рецензирования: 14.11.2023
Принята к публикации: 16.11.2023
Received: 07.11.2023
Revised: 14.11.2023
Accepted: 16.11.2023
Клинический разбор в общей медицине №8 2023
Атипичное течение макроглобулинемии «под маской» анемии (клиническое наблюдение)
Номера страниц в выпуске:101-105
Аннотация
Макроглобулинемия Вальденстрема (МВ) – это один из вариантов плазмоклеточных заболеваний, представляющий собой злокачественную В-клеточную лимфоплазмоцитарную лимфому. У пациентов с МВ клинический анализ крови длительное время может оставаться без патологических изменений, однако затем опухолевая инфильтрация костного мозга постепенно приводит к развитию анемии и тромбоцитопении. У данного пациента анемический синдром, по данным клинико-лабораторного обследования, расширил диагностический ряд заболеваний. Ранняя диагностика методом электрофореза с иммунотипированием позволила своевременно предположить иммунопролиферативное расстройство с моноклональным иммуноглобулином M (IgM). Иммунотипирование широко применяется с целью диагностики гаммапатий при помощи антисывороток к тяжелым (G, A, M) и легким (kappa, lambda) цепям иммуноглобулинов. Увеличение концентрации в крови IgM>30 г/л в совокупности с неврологической симптоматикой позволило связать данные проявления с синдромом гипервязкости при МВ.
Ключевые слова: макроглобулинемия, плазмоклеточные заболевания, синдром гипервязкости, моноклональный IgM, иммунопролиферативные расстройства.
Для цитирования: Хохлова С.М., Пасюта О.Н., Червякова Ю.Б. и др. Атипичное течение макроглобулинемии «под маской» анемии (клиническое наблюдение). Клинический разбор в общей медицине. 2023; 4 (8): 101–105. DOI: 10.47407/kr2023.4.8.00337
Макроглобулинемия Вальденстрема (МВ) – это один из вариантов плазмоклеточных заболеваний, представляющий собой злокачественную В-клеточную лимфоплазмоцитарную лимфому. У пациентов с МВ клинический анализ крови длительное время может оставаться без патологических изменений, однако затем опухолевая инфильтрация костного мозга постепенно приводит к развитию анемии и тромбоцитопении. У данного пациента анемический синдром, по данным клинико-лабораторного обследования, расширил диагностический ряд заболеваний. Ранняя диагностика методом электрофореза с иммунотипированием позволила своевременно предположить иммунопролиферативное расстройство с моноклональным иммуноглобулином M (IgM). Иммунотипирование широко применяется с целью диагностики гаммапатий при помощи антисывороток к тяжелым (G, A, M) и легким (kappa, lambda) цепям иммуноглобулинов. Увеличение концентрации в крови IgM>30 г/л в совокупности с неврологической симптоматикой позволило связать данные проявления с синдромом гипервязкости при МВ.
Ключевые слова: макроглобулинемия, плазмоклеточные заболевания, синдром гипервязкости, моноклональный IgM, иммунопролиферативные расстройства.
Для цитирования: Хохлова С.М., Пасюта О.Н., Червякова Ю.Б. и др. Атипичное течение макроглобулинемии «под маской» анемии (клиническое наблюдение). Клинический разбор в общей медицине. 2023; 4 (8): 101–105. DOI: 10.47407/kr2023.4.8.00337
Macroglobulinemia: hidden by anemia (clinical case report)
Svetlana M. Khokhlova1, Olga N. Pasyuta1, Julia B. Chervyakova1, Margarita A. Gromova1,Julia G. Patraman2, Marianna R. Mazra1, Alexander A. Kopelev1, Tamara O. Myshlyaeva1
1 Pirogov Russian National Research Medical University, Moscow, Russia;
2 Bauman City Clinical Hospital No29, Moscow, Russia
mazra.marianna@yandex.ru
Abstract
Waldenström macroglobulinemia (WM) is a type of plasma cell disease that is a malignant B-cell lymphoplasmacytic lymphoma. In patients with WM, immunological blood tests may remain unchanged for a while without pathological changes, but then tumor infiltration of the bone marrow gradually leads to anemia and thrombocytopenia. This patient has anemic syndrome according to clinical and laboratory examination, in which a number of diseases were diagnosed. An early diagnostic method, electrophoresis allows the consideration of immunoproliferative disorders with monoclonal IgM. Immunotyping is widely used with the eye chart of gammopathies using antisera to light (G, A, M) and light (kappa, lambda) chains of immunoglobulins. An increase in blood vessels IgM > 30 g/l, when identified with neurological symptoms of the source, associate these manifestations with hyperviscosity syndrome in WM.
Key words: macroglobulinemia, plasma cell diseases, hyperviscosity syndrome, monoclonal IgM, immunoproliferative disorders.
For citation: Khokhlova S.M., Pasyuta O.N., Chervyakova Ju.B. et al. Macroglobulinemia: hidden by anemia (clinical case report). Clinical review for general practice. 2023; 4 (8): 101–105 (In Russ.). DOI: 10.47407/kr2023.4.8.00337
Введение
Макроглобулинемия, названная ранее в честь описавшего ее Я.Г. Вальденстрема (МВ) – один из вариантов плазмоклеточных заболеваний (ПЗ), характеризующийся гиперпродукцией иммуноглобулина (ИГ) класса М (IgM). В целом данной группе присуща диспропорциональная пролиферация одного из клонов В-лимфоцитов (БК) и, соответственно, плазматических клеток (ПК) с преобладанием ИГ, синтезируемого данным клоном, именуемого М-протеином (МП). Повреждение органов и тканей происходит за счет как ПК (остеопороз, цитопения), так и МП. По мнению исследователей, МВ больше напоминает лимфопролиферативные заболевания (ЛПЗ), нежели другие ПЗ, включая миеломную болезнь (ММ). Возможно, это обусловлено особенностями МП при ней, так как сочетание накопления IgM и сходных клинических проявлений описано у 5% больных неходжкинскими лимфомами и, реже, хроническим лимфолейкозом [1–3].В настоящий момент МВ встречается крайне редко с ежегодной заболеваемостью от 3 до 4 случаев на миллион человек, что составляет примерно 2% от всех гематологических злокачественных новообразований. Данная патология распространена среди пожилых людей в возрасте 65–80 лет, преимущественно у лиц мужского пола, при соотношении мужчин и женщин 2,3 : 1 [3, 4].
Этиология МВ до конца не изучена, однако существует несколько факторов ее развития, к которым относятся генетическая предрасположенность (дефект Т-клеточной супрессорной функции, мутация в генах MYD8, CXCR4), влияние радиационных воздействий, химических мутагенов и вирусов (вирус иммунодефицита человека, гепатита С), риккетсий [5–7].
Ключевую роль в патогенезе МВ играет соматическая гипермутация вариабельного района тяжелой цепи генов ИГ, а именно 3 семейство (VH3-гены ИГ), в результате чего возникает диспропорциональная пролиферация одного клона БК и ПК с продукцией только IgM. БК памяти в стадии постфолликулярной дифференцировки с преимущественной экспрессией CD27+ считается структурной единицей опухоли при данном процессе. Однако эта теория подвергается критике, так как у некоторых больных МВ опухоль состоит из наивных БК, экспрессирующих не только CD27+ рецептор, но и CD5+, СD19+, CD20+, CD22+, CD25+ и др. [5, 8].
В клинической картине МВ преобладают симптомы, присущие ЛПЗ (B-симптомы): лихорадка, ночная потливость, слабость, снижение массы тела, лимфаденопатия и гепатоспленомегалия (которых может и не отмечаться), также часто наблюдается артралгия. Отдельную группу составляют симптомы, связанные с отложением IgМ в тканях, а именно клубочках почек, кишечнике, коже, что может проявляться протеинурией, диареей, появлением кожных папул или узлов. В редких случаях у пациента можно обнаружить холодовые гемагглютинины, которые при взаимодействии с антигенами эритроцитов при низкой температуре вызывают гемолитическую анемию или положительную пробу Кумбса, синдром Рейно, холодовую крапивницу [9, 10].
Более того, определяется характерная лимфоидная инфильтрация костного мозга, лимфатических узлов, печени, селезенки, а также наличие в сыворотке крови избыточного количества IgM. При повышении уровня IgM>30 г/л возникает синдром гипервязкости, характеризующийся в основном неврологической симптоматикой (слабость, снижение памяти, ухудшение зрения, парезы и другие нейропатии), повышенной кровоточивостью кожи и слизистых оболочек. Возможно развитие сердечной недостаточности вследствие увеличения объема плазмы крови [2, 3, 10–12].
Для подтверждения диагноза МВ, необходимо выявить в крови моноклональный IgM и инфильтрацию костного мозга малыми лимфоцитами, плазмоцитоидными и ПК. Важно отметить, что гиперпродукция IgM не всегда указывает на МВ, так как есть ряд других иммунопролиферативных расстройств (табл. 1), связанных с IgM [3, 10, 13].

При постановке диагноза МВ рекомендуется назначение лечения врачом-онкогематологом. Основными подходами являются плазмаферез при синдроме гипервязкости, поддержка глюкокортикоидами для снижения опухолевой нагрузки и индивидуальный подбор химиотерапии. В настоящее время наиболее широко применяется ритуксимаб как в монорежиме, так и комбинациях [3–5].

Учитывая вялотекущее развитие МВ, большая часть пациентов не нуждается в немедленной терапии после постановки диагноза. По современным данным, не рекомендуется начинать медикаментозное лечение только на основании уровня IgM, поскольку его повышение не всегда коррелирует с клиническими проявлениями. Однако начало терапии целесообразно у пациентов, у которых наблюдается повышение концентрации IgM наряду с признаками или симптомами, связанными с прогрессированием заболевания (табл. 2).
Лечение противоопухолевыми препаратами с глюкокортикоидами должно проводиться как можно скорее, так как при терапии только плазмаферезом уровни IgM повысятся и вернутся к исходному уровню в течение 4 нед [14].
При анализе описанных ранее случаев МВ (А.Т. Фиясь и соавт., А.К. Ильющенко и соавт., Н.Я. Дзеранова и соавт., N. Kolikkat и соавт.), где авторами также проводилось сопоставление с литературными данными, лишь в одном (зарубежном) источнике приведен сходный с нашим случай, но там для постановки диагноза, так как отмечался клинико-гематологически только анемический синдром, потребовалось больше времени и анализ результатов миелограммы с иммуногистохимическим исследованием. В отечественных наблюдениях присутствовали органные поражения, диагностическая концепция МВ фигурировала, зачастую, в качестве основной, затруднение же представляло дифференцировать ее от миело- (МПЗ) и/или ЛПЗ [8, 12, 15]. Приводим собственный клинический случай МВ у пожилого пациента с клинической манифестацией под маской анемии.
Клиническое наблюдение
Больной К, 68 лет, поступил 12.09.2023 в ГБУЗ «Городская клиническая больница №29 им. Н.Э. Баумана» (ГКБ №29) с жалобами на ноющую боль «по всему позвоночнику» преимущественно в шейном и поясничном отделах, нижних конечностях, головокружение, слабость. Из анамнеза известно, что с декабря 2022 г., без видимой причины, постепенно нарастала боль в позвоночнике, нижних конечностях. В середине августа 2023 г. начали беспокоить головокружение, слабость. Самостоятельно не лечился. Обратился в поликлинику по месту жительства 07.09.2023, где была выявлена гипохромная нормоцитарная анемия средней степени тяжести (гемоглобин 81 г/л), тромбоцитопения 51×109/л. Из перенесенных заболеваний, травм, операций: эпизоды повышения артериального давления (АД) до 140/100 мм рт. ст. (препараты не помнит), эссенциальный тремор, язвенная болезнь двенадцатиперстной кишки, закрытая черепно-мозговая травма и пластика паховой грыжи слева «в молодости».При осмотре: состояние средней степени тяжести. Рост – 172 см, масса – 62 кг (индекс Кетле 20,9 кг/м2). Температура тела – 36,8 °С. Кожа и видимые слизистые чистые, бледные, обычной влажности. Лимфаденопатии, отеков нет. В легких дыхание везикулярное, проводится равномерно по всем отделам, хрипы не выслушиваются, частота дыхательных движений (ЧДД) – 18 в 1 минуту, сатурация 96%. Тоны сердца приглушены, ритм правильный, шумы не определяются, частота сердечных сокращений – 66 в мин, АД – 130/80 мм рт. ст. Живот мягкий, безболезненный. Печень и селезенка физикально не изменены. Стул и мочеиспускание без особенностей. Очаговой и менингеальной симптоматики, а также признаков поражения черепных нервов и компрессии спинного мозга и нервных корешков не выявлено.
Проведено дообследование. Клинический анализ крови: сохранение гипохромной нормоцитарной анемии Hb 80→82 г/л, тромбоцитопении 99→57×109/л, СОЭ – 90 мм/ч. Биохимический анализ крови: общий белок 108,4→109 г/л, трансферрин 1,65→1,41 г/л, общая железосвязывающая способность – 43,8 мкмоль/л, железо – 12,2 мкмоль/л, прямая проба Кумбса положительная, прочие показатели крови без патологических изменений. Проведен электрофорез (табл. 3), по данным которого была подтверждена диспротеинемия с увеличением доли гамма-глобулинов до 62,4% (68,0 г/л) от общего белка, т.е. подтверждено наличие МП. В результате иммунотипирования МП был идентифицирован как полноразмерный моноклональный IgM lambda.

По данным рентгенографии плоских костей черепа и таза от 14.09.2023, эндоскопии: эзофагогастродуоденоскопии от 13.09.2023 и колоноскопии от 17.09.2023 – патологии не выявлено, что позволило исключить ММ; МПЗ и ЛПЗ результаты обследования также не соответствовали. Был выставлен диагноз МВ, пациент консультирован гематологом и переведен в онкогематологическое отделение, где на момент написания статьи проводится подбор химиотерапии, сеансы плазмафереза с положительным эффектом в виде уменьшения выраженности болевого синдрома.
Обсуждение
Преобладание у данного больного в клиническом анализе крови анемии и тромбоцитопении при отсутствии лимфаденопатии и гепатоспленомегалии в начале указывало иное направление диагностического поиска. Однако сочетание нормоцитоза и гипохромии не соответствовало мегалобластическим анемиям, для которых типично угнетение и других ростков кроветворения, но необходимо наличие макроцитоза и гиперхромии, отсутствовала и типичная картина фуникулярного миелоза, ожидаемого в случае дефицита витамина B12. Гипохромия возможна при железодефицитной, но в ее случае практически обязателен микроцитоз, а тромбоцитопения, напротив, не присуща. Основания подозревать гемолитический генез, без характерных изменений эритроцитов и билирубина, отсутствовали. Гипохромной нормоцитарной может быть сидеробластная анемия, но сочетание ее с тромбоцитопенией ожидаемо только в структуре миелодиспластического синдрома, диагностировать который, учитывая сохранность лейкоцитов (снижение уровня коих необходимо и для апластической анемии, да и мегалобластических), оснований также не было.Направление на исключение анемии хронических заболеваний (которая в типичном своем проявлении нормоцитарная и нормохромная) позволило выявить значимую гиперпротеинемию, приведшую к смене диагностической концепции: протеинограмма позволила обнаружить МП, а иммунотипирование установило, что он является моноклональным IgM. Это, а также отсутствие по результатам дополнительного обследования признаков ММ, МПЗ и ЛПЗ, дало основания установить диагноз МВ, а боль, послужившую причиной обращения, связать с синдромом гипервязкости.
Заключение
Приведенное клиническое наблюдение представляет интерес тем, что на начальном этапе обследования обращали на себя внимание вторичные изменения в виде болевого синдрома и анемии, но их атипичные характеристики потребовали отступления от стандартных протоколов диагностического поиска. Кроме того, описанный случай диктует необходимость включения МВ в дифференциальный диагноз у пожилых мужчин, особенно с симптоматикой, причиной которой может служить синдром гипервязкости, поскольку МВ, при своей редкости в общей популяции, достаточно распространена именно в данной группе.Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Хохлова Светлана Михайловна – студентка 6-го курса, каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: cxoxlova@inbox.ru; ORCID: 0009-0003-1110-0971
Svetlana M. Khokhlova – Student, Pirogov Russian National Research Medical University. E-mail: cxoxlova@inbox.ru; ORCID: 0009-0003-1110-0971
Пасюта Ольга Николаевна – студентка 6-го курса, каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: olechkapasuta@gmail.com; ORCID: 0009-0000-2839-5970
Olga N. Pasyuta – Student, Pirogov Russian National Research Medical University. E-mail: olechkapasuta@gmail.com; ORCID: 0009-0000-2839-5970
Червякова Юлия Борисовна – канд. мед. наук, доц., каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: chervyakova_j@mail.ru; ORCID: 0000-0003-0069-4260
Julia B. Chervyakova – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: chervyakova_j@mail.ru; ORCID: 0000-0003-0069-4260
Громова Маргарита Александровна – канд. мед. наук, доц. каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: margarita-gromov@mail.ru; ORCID: 0000-0002-3757-058X
Margarita A. Gromova – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: margarita-gromov@mail.ru; ORCID: 0000-0002-3757-058X
Патраман Юлия Георгиевна – врач-терапевт, 4-е терапевтическое отделение, ГБУЗ «ГКБ №29 им. Н.Э. Баумана». E- mail: iuliya_02_07@mail.ru; ORCID: 0009-0009-5136-4860
Julia G. Patraman – The general practitioner, Bauman Clinical City Hospital No29. E- mail: iuliya_02_07@mail.ru; ORCID: 0009-0009-5136-4860
Мазра Марианна Рамазиевна – студентка 6-го курса, каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: mazra.marianna@yandex.ru; ORCID: 0000-0001-8064-2406
Marianna R. Mazra – Student, Pirogov Russian National Research Medical University. E-mail: mazra.marianna@yandex.ru; ORCID: 0000-0001-8064-2406
Копелев Александр Александрович – канд. мед. наук, доц. каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: akopelev@mail.ru; ORCID: 0000-0002-4328-3384
Alexander A. Kopelev – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: akopelev@mail.ru; ORCID: 0000-0002-4328-3384
Мышляева Тамара Олеговна – канд. мед. наук, ассистент каф. факультетской терапии ЛФ, ФГАОУ ВО «РНИМУ им. Н.И. Пирогова». E-mail: tlixa@mail.ru; ORCID: 0009-0005-8437-7482
Tamara O. Myshlyaeva – Cand. Sci. (Med.), Pirogov Russian National Research Medical University. E-mail: tlixa@mail.ru; ORCID: 0009-0005-8437-7482
Поступила в редакцию: 07.11.2023
Поступила после рецензирования: 14.11.2023
Принята к публикации: 16.11.2023
Received: 07.11.2023
Revised: 14.11.2023
Accepted: 16.11.2023
Список исп. литературыСкрыть список1. Gertz MA. Waldenstrom macroglobulinemia: 2023 update on diagnosis, risk stratification, and management. Am J Hematol. 2023; 98 (2): 348–58. DOI: 10.1002/ajh.26796
2. Sanchez E, Tanenbaum EJ, Patil S et al. The clinical significance of B-cell maturation antigen as a therapeutic target and biomarker. Expert Rev Mol Diagn. 2018; 18 (4): 319–29. DOI: 10.1080/14737159.2018.1448269
3. Макроглобулинемия Вальденстрема. Клинические рекомендации. Национальное гематологическое общество совместно с Ассоциацией онкологов России. М., 2023. Ссылка активна на 05.11.2023. URL: https: //npngo.ru/uploads/media_document/733/54fd2ceb-240c-4577-af6d-7752f0e10c06.docx
Waldenström macroglobulinemia. Clinical guidelines. The National Hematology Society together with the Association of Oncologists of Russia. URL: https: //npngo.ru/uploads/media_document/733/ 54fd2ceb-240c-4577-af6d-7752f0e10c06.docx (in Russian).
4. Kaseb H, Gonzalez-Mosquera LF, Parsi M, Mewawalla P. Lymphoplasmacytic lymphoma. Treasure Island (FL): StatPearls Publishing; 2023.
5. Балакирева Т.В., Андреева Н.Е. Макроглобулинемия Вальденстрема. Клиническая онкогематология. Фундаментальные исследования и клиническая практика. 2009; 2 (2): 121–36. Ссылка активна на 05.11.2023. URL: https: //cyberleninka.ru/article/n/makroglobulinemiya-valdenstrema/viewer
Balakireva TV, Andreeva NE. Waldenström's macroglobulinemia. Clinical oncohematology. Basic Research and Clinical Practice. 2009; 2 (2): 121–36. URL: https: //cyberleninka.ru/article/n/makroglobulinemiya-valdenstrema/viewer (in Russian).
6. Hunter ZR, Xu L, Yang G et al. The genomic landscape of Waldenstrom macroglobulinemia is characterized by highly recurring MYD88 and WHIM-like CXCR4 mutations, and small somatic deletions associated with B-cell lymphomagenesis. Blood. 2014; 123 (11): 1637–46. DOI: 10.1182/blood-2013-09-525808
7. Monge J, Braggio E, Ansell SM. Genetic factors and pathogenesis of Waldenström's macroglobulinemia. Curr Oncol Rep. 2013; 15 (5): 450–6. DOI: 10.1007/s11912-013-0331-7
8. Фиясь А.Т., Чайковская О.П., Пищик Е.О., Френкель Б.И. К вопросу о макроглобулинемии Вальденстрема. Журнал ГрГМУ. 2010; (3): 95–7. Ссылка активна на 05.11.2023. URL: http: //journal-grsmu.by/index.php/ojs/article/view/607/538
Fiyas AT, Chaikovskaya OP, Pishchik EO, Frenkel BI. On the issue of Waldenström's macroglobulinemia. Journal GrSMU. 2010; (3): 95–7. URL: http: //journal-grsmu.by/index.php/ojs/article/view/607/538 (in Russian).
9. Vos JM, Gustine J, Rennke HG et al. Renal disease related to Waldenstrom macroglobulinacmia: incidence. pathology and clinical outcomes. Br J Haematol. 2016; 175 (4): 623–30. DOI: 10.1111/bjh.
14279
10. Askari E, Rodriguez S, Garcia-Sanz R. Waldenström’s Macroglobulinemia: An Exploration into the Pathology and Diagnosis of a Complex B-Cell Malignancy. J Blood Med. 2021; 12: 795–807. DOI: 10.2147/JBM.S267938
11. Nobile-Orazio E. Antigenic determinants in IgM paraprotein-related neuropathies. Clin. Lymph. Myeloma 2009; 9 (1): 107–9. DOI: 10.3816/CLM.2009.n.02
12. Дзеранова Н.Я., Кудряшова Е.Ю., Никитина А.В., Исаков В.А. Макроглобулинемия Вальденстрема: диагностика в клинической практике. Медицина: теория и практика. 2018; 3 (3): 10–5. Ссылка активна на 05.11.2023. URL: https: //ojs3.gpmu.org/index.php/med-theory-and-practice/article/view/495
Dzeranova NYa, Kudryashova EYu, Nikitina AV, Isakov VA. Waldenström macroglobulinemia: diagnostics in clinical practice. Medicine: theor and practice. 2018; 3 (3): 10–5. URL: https: //ojs3.gpmu.org/ index.php/med-theory-and-practice/article/view/495 (in Russian).
13. Khwaja J, D’Sa S, Minnema MC et al. IgM monoclonal gammopathies of clinical significance: diagnosis and management. Haematologica. 2022; 107 (9): 2037–50; DOI: 10.3324/haematol.2022.280953
14. Castillo JJ, Ghobrial IM, Treon SP. Biology, prognosis, and therapy of Waldenström Macroglobulinemia. Cancer Treat Res. 2015; 165: 177–95. DOI: 10.1007/978-3-319-13150-4_7
15. Kolikkat N, Moideen S, Khader A et al. Waldenstrom's Macroglobulinemia: A case report. J Family Med Prim Care. 2020; 9 (3): 1768–71. DOI: 10.4103/jfmpc.jfmpc_972_19
12 декабря 2023
Количество просмотров: 2084


