Клинический разбор в общей медицине №2 2024
Клинический разбор в общей медицине №2 2024
Терапевтические возможности и перспективы самоконтроля гликемии – неотъемлемого компонента управления сахарным диабетом
Номера страниц в выпуске:82-88
Аннотация
Сахарный диабет (СД) − одна из глобальных проблем мирового здравоохранения. Опасными последствиями заболевания являются системные сосудистые осложнения, ведущий фактор развития – хроническая гипергликемия. Контроль гликемии остается эффективной стратегией профилактики диабетических осложнений, что требует достижения и поддержания целевых метаболических показателей в течение всей жизни пациента. Обсуждаются современные рекомендации по индивидуализированному выбору целей терапии по уровню гликированного гемоглобина и методы контроля гликемии. Подчеркивается роль самоконтроля гликемии (СКГ) – одного из важных факторов эффективности проводимой сахароснижающей терапии и профилактики гипогликемии. Осуществление грамотного СКГ невозможно без терапевтического обучения больных СД. Современное понимание СКГ подразумевает определенную кратность систематических измерений уровней глюкозы крови в зависимости от типа СД, вида сахароснижающей терапии. Для измерения сахара крови в домашних условиях доступны разнообразные глюкометры. Критериями для выбора глюкометра являются соответствие действующим стандартам точности, простота и удобство использования, легкость получения результата пациентами, что позволяет легко осуществлять процедуру измерения глюкозы в крови пациентам любого возраста. С развитием современных технологий появились глюкометры, которые благодаря интеграции с бесплатным мобильным приложением значительно расширяют возможности управления СД.
Ключевые слова: сахарный диабет, гипергликемия, целевой контроль, гликированный гемоглобин, самоконтроль гликемии, постпрандиальная гликемия, глюкометры.
Для цитирования: Бирюкова Е.В. Терапевтические возможности и перспективы самоконтроля гликемии – неотъемлемого компонента управления сахарным диабетом. Клинический разбор в общей медицине. 2024; 5 (2): 82–88. DOI: 10.47407/kr2023.5.2.00392
Сахарный диабет (СД) − одна из глобальных проблем мирового здравоохранения. Опасными последствиями заболевания являются системные сосудистые осложнения, ведущий фактор развития – хроническая гипергликемия. Контроль гликемии остается эффективной стратегией профилактики диабетических осложнений, что требует достижения и поддержания целевых метаболических показателей в течение всей жизни пациента. Обсуждаются современные рекомендации по индивидуализированному выбору целей терапии по уровню гликированного гемоглобина и методы контроля гликемии. Подчеркивается роль самоконтроля гликемии (СКГ) – одного из важных факторов эффективности проводимой сахароснижающей терапии и профилактики гипогликемии. Осуществление грамотного СКГ невозможно без терапевтического обучения больных СД. Современное понимание СКГ подразумевает определенную кратность систематических измерений уровней глюкозы крови в зависимости от типа СД, вида сахароснижающей терапии. Для измерения сахара крови в домашних условиях доступны разнообразные глюкометры. Критериями для выбора глюкометра являются соответствие действующим стандартам точности, простота и удобство использования, легкость получения результата пациентами, что позволяет легко осуществлять процедуру измерения глюкозы в крови пациентам любого возраста. С развитием современных технологий появились глюкометры, которые благодаря интеграции с бесплатным мобильным приложением значительно расширяют возможности управления СД.
Ключевые слова: сахарный диабет, гипергликемия, целевой контроль, гликированный гемоглобин, самоконтроль гликемии, постпрандиальная гликемия, глюкометры.
Для цитирования: Бирюкова Е.В. Терапевтические возможности и перспективы самоконтроля гликемии – неотъемлемого компонента управления сахарным диабетом. Клинический разбор в общей медицине. 2024; 5 (2): 82–88. DOI: 10.47407/kr2023.5.2.00392
Review
Russian University of Medicine, Moscow, Russia
lena@obsudim.ru
Abstract. Diabetes mellitus (DM) is one of the global problems of world’s healthcare. Systemic vascular complications are the dangerous sequelae of the disease, and chronic hyperglycemia is the leading factor contributing to the disease development. Glycemic control remains an effective strategy to prevent diabetes complications that requires achieving and maintaining metabolic targets throughout the life of the patient. The current guidelines on the selection of personalized treatment goals based on the glycated hemoglobin (HbA1c) levels and the glycemic control methods are discussed. The emphasis is placed on self-monitoring of blood glucose (SMBG), one of the important factors contributing to the efficacy of the ongoing glucose-lowering therapy and hypoglycemia prevention. Proper SMBG is impossible without therapeutic training of DM patients. The current understanding of SMBG implies a certain frequency of the systematic measurement of blood glucose levels depending on the DM type and the type of glucose-lowering therapy. Various glucose meters for measurement of blood glucose levels at home are available. The criteria for choosing the glucose meter include compliance with the relevant accuracy standards, simplicity and ease of use, ease of getting the results by patients, which allow patients of any age to easily measure blood glucose levels. With all the advancements in modern technology, the glucose meters have appeared that significantly expand the possibilities of DM control due to integration with the free mobile application.
Keywords: diabetes mellitus, hyperglycemia, target range, glycated hemoglobin, self-monitoring of blood glucose, postprandial blood glucose levels, glucose meters.
For citation: Biryukova E.V. Therapeutic avenues and prospects of blood glucose self-monitoring, the essential component of diabetes mellitus management. Clinical analysis in general medicine. 2024; 5 (2): 82–88 (In Russ.). DOI: 10.47407/kr2023.5.2.00392
Сахарный диабет (СД) − одна из глобальных проблем мирового здравоохранения, поэтому актуально обсуждение вопросов лечения заболевания и эффективного гликемического контроля. В Российской Федерации (на 01.01.2023) число только зарегистрированных больных составило 4 962 762 [1]. Опасными последствиями СД являются системные сосудистые осложнения – нефропатия, ретинопатия, поражение магистральных сосудов сердца, головного мозга, артерий нижних конечностей, которые приводят к ранней инвалидизации и влияют на прогноз жизни пациентов. В связи с развитием системных сосудистых осложнений, преждевременной инвалидизацией, необходимостью пожизненной фармакотерапии, высокой смертностью СД представляет тяжелое бремя для системы здравоохранения и бюджета государства [1–3].
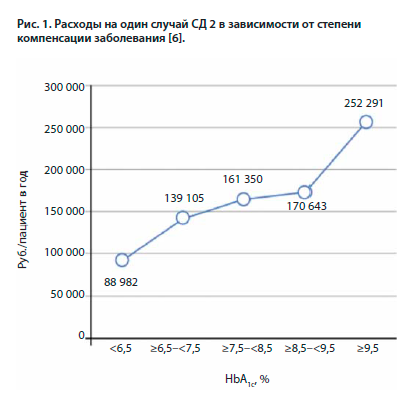 Значимость достижения гликемического контроля имеет широкие научные доказательства, вместе с тем еще не решены насущные проблемы, связанные с достижением оптимального метаболического контроля и профилактикой хронических осложнений СД [3, 4]. Согласно крупному метаанализу 24 исследований только 42,8% пациентов с СД 2-го типа – СД 2 (95% доверительный интервал 38,1–47,5%) имели целевой контроль гликемии [5]. В экономическом анализе, целью которого было определение затрат системы отечественного здравоохранения и потерь в экономике, связанных с СД 2 и его сердечно-сосудистыми осложнениями, результаты подсчетов затрат показали, что на некомпенсированных больных СД 2 тратится больше средств, чем на пациентов с контролируемым заболеванием (рис. 1) [6]. Усредненный экономический ущерб на 1 пациента с СД 2 нарастает с декомпенсацией заболевания, согласно эпидемиологическим данным, приемлемые показатели гликированного гемоглобина HbA1c (менее 6,5%, до 7,5%) наблюдались в 47,9% случаев, а 52,1% больных имели некомпенсированный СД 2, причем половина из них – HbA1c>8,5%, что представляется весьма опасным с точки зрения развития и прогрессирования сердечно-сосудистых осложнений. Одним из механизмов потенциального снижения экономического бремени СД является предотвращение его осложнений, что может быть реализовано через улучшение гликемического контроля [2, 6].
Значимость достижения гликемического контроля имеет широкие научные доказательства, вместе с тем еще не решены насущные проблемы, связанные с достижением оптимального метаболического контроля и профилактикой хронических осложнений СД [3, 4]. Согласно крупному метаанализу 24 исследований только 42,8% пациентов с СД 2-го типа – СД 2 (95% доверительный интервал 38,1–47,5%) имели целевой контроль гликемии [5]. В экономическом анализе, целью которого было определение затрат системы отечественного здравоохранения и потерь в экономике, связанных с СД 2 и его сердечно-сосудистыми осложнениями, результаты подсчетов затрат показали, что на некомпенсированных больных СД 2 тратится больше средств, чем на пациентов с контролируемым заболеванием (рис. 1) [6]. Усредненный экономический ущерб на 1 пациента с СД 2 нарастает с декомпенсацией заболевания, согласно эпидемиологическим данным, приемлемые показатели гликированного гемоглобина HbA1c (менее 6,5%, до 7,5%) наблюдались в 47,9% случаев, а 52,1% больных имели некомпенсированный СД 2, причем половина из них – HbA1c>8,5%, что представляется весьма опасным с точки зрения развития и прогрессирования сердечно-сосудистых осложнений. Одним из механизмов потенциального снижения экономического бремени СД является предотвращение его осложнений, что может быть реализовано через улучшение гликемического контроля [2, 6].
Пациенты с СД должны как можно раньше получать лечение в полном объеме в соответствии с национальными и международными рекомендациями, краеугольным камнем которых является концепция персонализированной медицины. Изменение образа жизни (рациональное питание и повышение физической активности), обучение принципам управления заболеванием являются неотъемлемой частью лечения и должны осуществляться на всем протяжении заболевания [7, 8]. Современное эффективное управление СД – это комплексный процесс, который включает многие взаимосвязанные компоненты и предполагает тесное взаимодействие врача и пациента для достижения гликемического контроля.
Улучшение прогноза пациентов с СД определяется оптимальным контролем основных показателей углеводного обмена, которые включают HbA1c, гликемию натощак, постпрандиальную гликемию (ППГ) [7–9]. HbA1c имеет неоценимое значение для диагностики СД, а также выбора терапии (моно- или комбинированная терапия) и интенсификации сахароснижающей терапии (ССТ), а также для контроля ее эффективности; однако этот показатель не несет информации касательно ежедневного уровня глюкозы в крови, эпизодов гипогликемии и вариабельности уровня глюкозы [9]. Целевые уровни HbA1c – уровни показателя, при которых риск диабетических осложнений существенно снижается [10].
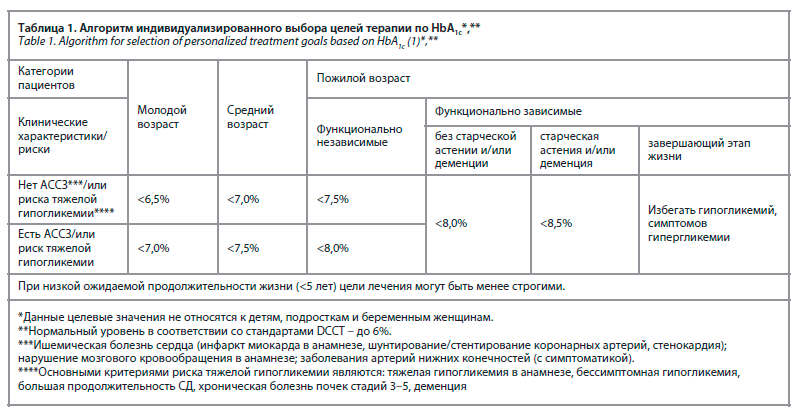
Клинические рекомендации по стандартизации и оптимизации оказания медицинской помощи больным СД во всех регионах России предлагают подход для индивидуализированного выбора целей терапии по HbA1c, основанный на возрасте пациента, ожидаемой продолжительности жизни, наличии атеросклеротических сердечно-сосудистых заболеваний (АССЗ) и риска тяжелой гипогликемии (табл. 1).
Для успешного результата лечения СД также необходимы данные оперативного контроля уровня гликемии в разные временные периоды (натощак, до приема пищи, через 2 ч после приема пищи, перед сном). Это помогает выявить не только показатели глюкозы в крови, выходящие за пределы целевых значений, но и индивидуальные закономерности изменения гликемии в разное время суток, а также оценить влияние на показатели глюкозы в крови факторов питания, физической нагрузки и эффективность и безопасность назначенной терапии СД [11–13].
Оптимальным инструментом контроля гликемии является суточное мониторирование глюкозы, отражающее все суточные колебания гликемии. Однако этот метод исследования глюкозы в повседневной жизни пока невыполним для большинства пациентов с СД. Самоконтроль гликемии (СКГ) с помощью глюкометра – самый простой и, возможно, наиболее практичный инструмент для контроля гликемии. Он дополняет тестирование HbA1c при оценке гликемического профиля и играет ключевую роль в ежедневном мониторинге уровня глюкозы в плазме у пациентов с СД [12–14].
СКГ – ключевой компонент повышения эффективности немедикаментозных и медикаментозых методов управления гликемией [15]. В настоящее время модификация образа жизни рекомендуется в качестве первой линии лечения СД 2. Важной терапевтической задачей наряду с эффективным контролем гликемии является снижение массы тела, что достигается повышением физической активности и ограничением калорийности рациона [7, 16, 17]. Физическая активность является важным компонентом здорового образа жизни, повышает качество жизни, но не является методом ССТ при СД 1-го типа (СД 1) и может повышать риски гипогликемий во время и после нагрузки. Пациенты с СД должны иметь информацию о возможных колебаниях уровня глюкозы в крови во время любой физической активности и занятий спортом. СКГ позволяет дать оценку индивидуальной реакции со стороны уровня глюкозы в крови у пациента в ответ на различные виды физической нагрузки и повысить мотивацию пациентов к регулярной физической активности [7, 18].
Выполнение физических упражнений должно быть безопасно, поэтому всем пациентам следует контролировать гликемию, а особенно получающим препараты инсулина или пероральные препараты, стимулирующие секрецию инсулина. Мониторинг гликемии необходим перед физическими нагрузками, временным противопоказанием для которых является уровень глюкозы плазмы более 13,0 ммоль/л в сочетании с кетонурией или 16 ммоль/л (даже без кетонурии). Больным СД 1, проводящим СКГ и владеющим методами профилактики гипогликемий, можно заниматься любыми видами физической активности [7].
Регулярная физическая активность у больных СД 2 способствует достижению целевых уровней гликемии, похудению, помогает уменьшить инсулинорезистентность. Применение многокомпонентных программ модификации образа жизни способствует улучшению клинических показателей [19]. Показано, что СКГ повышает результат подобных программ по коррекции образа жизни. В ретроспективный анализ S. Tomah и соавт. были включены результаты программы модификации образа жизни (Why WAIT, продолжительность 12 нед); наряду с изменением образа жизни участникам (средний возраст 57±9 лет, длительность СД 2 10±8 лет, индекс массы тела 36±6 кг/м², HbA1c 7,8±1,4%, 45% пациентов получали инсулин) было предложено самостоятельно контролировать уровень глюкозы в крови с помощью глюкометра ежедневно. Гликемию необходимо было измерять перед каждым приемом пищи, перед сном, до и после тренировки, периодически через 2 ч после еды, а также при подозрении, что уровень глюкозы в их крови низкий или высокий [16]. С учетом частоты СКГ, осуществляемого пациентами с СД 2 за период наблюдения, участников разделили на 3 группы (в зависимости от тертиля СКГ): средний диапазон частоты СКГ составил 2,3 (1,1–2,9) раза в сутки в группе нижнего тертиля, 3,4 (3–3,9) раза в сутки и 5 (4–7,7) раз в сутки в группах среднего и высокого тертиля частоты СКГ соответственно. Исходно средняя масса тела пациентов составляла 107,6±20,3 кг в группе нижнего тертиля частоты СКГ, 107,4±19,2 кг – в группе среднего тертиля и 107,4±24 кг – высшего тертиля; HbA1c – 7,5±1,0%, 8,0±1,5% и 8,0±1,6% соответственно. Группы были сопоставимы по возрасту, полу, расе, продолжительности диабета, использованию инсулина, уровню HbA1c, индексу массы тела.
Через 12 нед участники группы с высокой частотой СКГ достигли значительно большей потери массы тела по сравнению с группами более низкой частоты тестирования уровня глюкозы. Участники из группы самого высокого тертиля частоты СКГ достигли среднего снижения массы тела на 10,4 кг (от -7,6 до -14,4 кг) по сравнению с 8,3 кг (от -5,2 до -12,2 кг) и -6,9 кг (от -4,2 до -8,9 кг) в группах среднего и нижнего тертиля соответственно (p=0,018). Динамика индекса массы тела в зависимости от тертилей частоты СКГ у пациентов составила -3,9 кг/м² (от -2,8 до -4,9 кг/м²), -2,7 кг/м² (от -1,6 до -3,9 кг/м²) и -2,5 кг/м² (от -1,5 до 3,3 кг/м²); p=0,012. Более высокая частота тестирования уровня глюкозы была связана со значительно лучшей динамикой HbA1c, отмеченной в конце исследования. Так, снижение HbA1c составило -1,25% (от -0,6 до -3,1%) в группе с высокой частотой СКГ по сравнению с -0,8% (от -0,3 до -2%) и -0,5% (от -0,2 до -1,2%) в группах среднего и нижнего тертилей частоты СКГ соответственно (p=0,048).
Различные исследования демонстрируют, что уровень HbA1c начинает значимо улучшаться, как только пациент увеличивает частоту СКГ независимо от типа СД или вида ССТ [13, 20, 21]. В то же время пациенты не всегда выполняют врачебные рекомендации, что касается и регулярности осуществления СКГ [22, 23]. В частности, по данным исследования M. Hansen и соавт., лишь 39% больных СД проводят СКГ ежедневно, 20% – несколько раз в неделю, 17% – 1–2 раза в неделю и 24% – реже одного раза в неделю [23]. К причинам, мешающим адекватному проведению регулярного СКГ, относят разные факторы, включая длительный стаж СД, хроническую боль, злоупотребление алкоголем, полипрагмазию, плохую информированность о своем состоянии, непрохождение обучения в школе СД и, как следствие, непонимание, каким образом нужно реагировать на полученные цифры измерения глюкозы крови, депрессию, высокую обеспокоенность собственным диабетом, отсутствием поддержки со стороны близких, нехватку льготных расходных материалов для самоконтроля и их высокую стоимость в аптечных сетях, отсутствие медицинской страховки, плохой контакт между пациентом и врачом и, наконец, незаинтересованность врача в данных самоконтроля [24].
Регулярный и грамотный СКГ невозможен без терапевтического обучения больных СД с помощью специально разработанных структурированных программ.
В процессе обучения происходят выработка обоснованных положительных мотиваций, формирование и отработка практических навыков, необходимых для самостоятельного правильного измерения гликемии и интерпретации полученных результатов, изменения поведения пациента в отношении питания и физической активности (структурированный СКГ) [11, 12, 14]. К сожалению, некоторые пациенты оставляют без внимания результаты СКГ, даже видя значительные отклонения гликемии от целевых значений, и, соответственно, не вносят необходимых изменений в питание, режим физических нагрузок, лечение. Поэтому, несмотря на проведение пациентом СКГ, не реализуются его значимые преимущества для лечения СД. Это происходит только в случае, когда обученный пациент активно использует результаты самоконтроля как отправную точку для принятия самостоятельных решений в различных жизненных ситуациях [12, 14, 18]. В том числе СКГ может предотвратить отклонения глик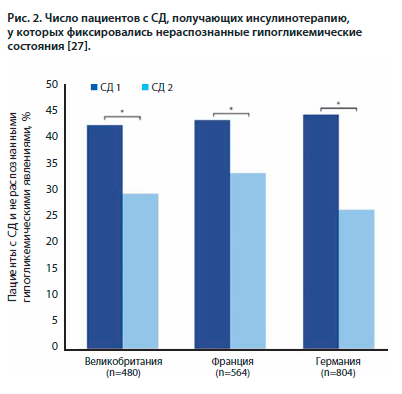 емии, которые могут быть опасными при определенных видах занятости (например, посменная работа, работа в ночное время, работа, связанная с выраженной физической нагрузкой, вождение автомобиля).
емии, которые могут быть опасными при определенных видах занятости (например, посменная работа, работа в ночное время, работа, связанная с выраженной физической нагрузкой, вождение автомобиля).
В процессе терапевтического обучения необходимо обсудить с пациентом индивидуальные целевые значения основных показателей гликемического контроля и частоту проведения СКГ, время измерения гликемии [7, 8, 14]. К сожалению, в реальности многие пациенты с СД контролируют гликемию нерегулярно и в основном измеряют уровень глюкозы натощак: в исследовании S. Farhan и соавт. только 20% пациентов выполняли СКГ через 2 ч после основного приема пищи, при этом 16% – проводили СКГ при плохом самочувствии, а 14% – при симптомах гипогликемии [22]. Наиболее выраженные колебания глюкозы крови у больных СД наблюдаются после приема пищи; ППГ – это достаточно частый лабораторный сдвиг, наблюдаемый даже у пациентов с целевым уровнем HbA1c. Доказано, что ППГ ассоциируется с сердечно-сосудистыми осложнениями и смертностью [25]. Поэтому СКГ обязательно должен включать измерение глюкозы не только натощак, но и через 2 ч после приема пищи [7]. Измерение гликемии через 2 ч после приема пищи позволяет выявить повышение ППГ, оценить влияние факторов питания, эффективности ССТ.
Гипогликемия может ограничить проведение интенсивного контроля гликемии, который является основой предотвращения осложнений СД [26]. Особого внимания заслуживают гипогликемические состояния, не сопровождающиеся характерной клинической симптоматикой, т.е. бессимптомные, которые наблюдаются у пациентов с нарушением способности распознавать приближающуюся гипогликемию (нарушение автономного ответа на гипогликемию). В исследовании J. Diago-Cabezudo по результатам онлайн-опроса 1848 пациентов с СД, получающих инсулинотерапию (из них 50% с СД 2), были получены интересные данные [27]: каждый третий пациент не всегда мог распознать симптомы гипогликемии, около четверти опрошенных не ощущали характерных симптомов при снижении уровня глюкозы крови ниже нормы (рис. 2). Кроме того, 37% участников сообщили, что стараются поддерживать уровень гликемии выше рекомендованных врачом значений из-за опасения возникновения гипогликемических состояний. 80% респондентов высказали заинтересованность в глюкометрах, способных информировать об отклонениях глюкозы от нормы как в сторону низких, так и в сторону высоких значений.
СКГ позволяет своевременно выявить гипогликемию и осуществить мероприятия, направленные на ее купирование; это особенно важно для пациентов на инсулинотерапии. Кроме того, риски гипогликемий могут увеличивать и другие сахароснижающие препараты (табл. 2) [7].
Структурированный СКГ является основой эффективности проводимой ССТ и профилактики гипогликемии, позволяя помочь в принятии решений по коррекции лечения [12, 14]. Значимые для практики результаты были получены в исследовании N. Lalić и соавт. с участием пациентов с СД на инсулинотерапии (СД 1 – 57 человек, СД 2 – 289 человек), в котором в течение 10 дней проводилось групповое структурированное обучение; психологическое состояние пациентов оценивали по шкале дистресса (Diabetes Distress Scale – DDS) [28]. Спустя 24 нед существенно увеличилась частота СКГ (14,6 раза в неделю по сравнению с 4,3 раза в неделю, р<0,001), отмечено значимое снижение уровня HbA1c на 0,94%; индивидуальные показатели гликемии также значительно улучшились по сравнению с исходными значениями. Важным итогом этой работы стало снижение среднего количества госпитализаций за период наблюдения по сравнению с шестимесячным периодом до включения в исследование (0,14±0,04 по сравнению с 0,59±0,09), также улучшились показатели психологического состояния пациентов по шкале DDS (39,6±13,9 по сравнению с 33,9±14,5, р<0,01), несмотря на увеличение частоты СКГ.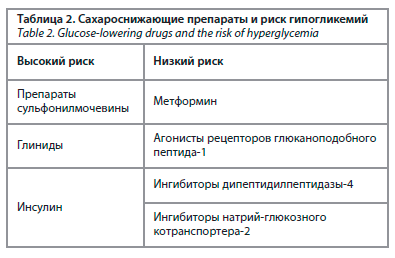 Использование самостоятельного измерения уровня гликемии крови в сочетании со структурированным обучением пациентов напрямую связано с клинически значимым снижением уровня HbA1c, улучшением индивидуальных показателей гликемии крови и качества жизни пациентов с СД.
Использование самостоятельного измерения уровня гликемии крови в сочетании со структурированным обучением пациентов напрямую связано с клинически значимым снижением уровня HbA1c, улучшением индивидуальных показателей гликемии крови и качества жизни пациентов с СД.
Метаанализ Y. Hou и соавт. подтверил, что систематический СКГ дополнительно снижает уровень HbA1c, однако большее преимущество СКГ выявлено в группе пациентов, которые не только регулярно контролировали уровень глюкозы в крови, но и корректировали свой план лечения СД на основе его результатов, что подчеркивает важность именно структурированного СКГ [29].
Рекомендуемая частота СКГ в зависимости от типа СД, вида ССТ отражена в национальных и международных руководствах по лечению СД [7, 8]. В соответствии с Российскими клиническими рекомендациями больным СД 1, а также СД 2 в дебюте заболевания и при недостижении целевых уровней гликемического контроля необходимо определять гликемию ежедневно не менее 4 раз (до еды, через 2 ч после еды, на ночь, периодически ночью) [7]. Далее частота СКГ при СД 2 определяется видом ССТ:
• на интенсифицированной инсулинотерапии – не менее 4 раз ежедневно (до еды, через 2 ч после еды, на ночь, периодически ночью);
• на пероральной ССТ и/или агонистах рецепторов глюканоподобного пептида-1 и/или базальном инсулине – не менее 1 раза в сутки в разное время с одним дополнительным гликемическим профилем (не менее 4 раз в сутки) в неделю (возможно уменьшение частоты при использовании только препаратов с низким риском гипогликемии);
• на готовых смесях инсулина – не менее 2 раз в сутки в разное время + 1 гликемический профиль (не менее 4 раз в сутки) в неделю;
• на диетотерапии – 1 раз в неделю в разное время суток.
При наличии признаков хронических осложнений СД, присоединении сопутствующих заболеваний, появлении дополнительных факторов риска вопрос о частоте обследований решается индивидуально.
Самостоятельный мониторинг гликемии дополнительно необходим перед физическими нагрузками и после них, при подозрении на гипогликемию и после ее лечения, при сопутствующих заболеваниях, если предстоят какие-то действия, потенциально опасные для пациента и окружающих (например, вождение транспортного средства или управление сложными механизмами) [7].
В настоящее время для самостоятельного мониторинга уровня глюкозы в крови рекомендуется применять персональные глюкометры, включая приборы с настройкой индивидуального целевого диапазона гликемии [7]. Внедрение новых технологий в современные системы измерения гликемии делает процесс СКГ значительно проще, и все больше пациентов используют их в повседневной жизни. «Умная» система Contour™ Plus One (Контур Плюс Уан) включает не только сам глюкометр, но и мобильное приложение (рис. 3), что значительно расширяет возможности управления СД со стороны пациента и взаимодействия с врачом.
Важным критерием для выбора глюкометра является соответствие стандартам точности. Глюкометр Контур Плюс Уан продемонстрировал высокую точность, превосходящую требования к точности стандарта ISO 15197:2013 [30, 31]. Высокая точность измерений уровня глюкозы в крови, наряду с удобством применения и наличием расширенных функций, в том числе и в мобильном приложении, помогают пациентам улучшить эффективность СКГ, избежать неправильных решений (например, ошибок в дозировке инсулин) по лечению и достичь лучших результатов.

Технология «Второй шанс» дает возможность повторного нанесения крови на тест-полоску в случае ее недостаточного заполнения, что удобно для каждого пациента с СД, но особенно для лиц старшего возраста. К удобству использования данного глюкометра можно отнести короткое время измерения глюкозы в крови – 5 с, что важно для пациентов в случае развития гипогликемического состояния. Прибор оснащен световым индикатором, расположенным в порте для тест-полосок, – функция «Умная подсветка», которая показывает, что уровень глюкозы в крови находится в пределах диапазона целевого значения (зеленый цвет), выше диапазона целевого значения или ниже диапазона целевого значения (желтый и красный цвета соответственно).
Система Контур Плюс Уан обеспечивает широкие возможности для достижения оптимального и безопасного уровня глюкозы в крови у пациентов с СД. Прибор может автоматически синхронизироваться с мобильным приложением Контур Диабитис (Contour Diabetes), являющимся, по сути, многофункциональным электронным вариантом дневника самоконтроля. Все данные, необходимые для адекватного СКГ, отражаются в электронной версии дневника самоконтроля, что наделяет глюкометр важными информативными функциями и позволяет пациентам более активно использовать СКГ (отмечать количество хлебных единиц, ССТ, оставлять примечания, подробные записи о съеденной пище, прикреплять фото блюд, фиксировать изменения в образе жизни и др.). Функция «Мои тенденции» помогает выявлять тенденции в результатах измерения уровня глюкозы в крови, отправляет уведомления, в том числе о возможных причинах отклонений. Стоит добавить, что наблюдение за положительным влиянием правильного стиля питания и регулярных физических нагрузок на уровень глюкозы в крови может стать мощным мотиватором для улучшения приверженности пациента, помогая укрепить успешное изменение образа и повысить качество жизни [32, 33].
С помощью функции отчетов на основе всех данных, которые поступают в мобильное приложение Контур Диабитис, реализуются современные информационно-коммуникационные технологии в процессе взаимодействия пациента и лечащего врача с целью оптимизации оказания медицинской помощи. Пациенты могут предоставлять врачу в электронном виде подробную информацию о мониторинге гликемии, что позволяет совместно выяснить причины отклонения уровня глюкозы крови и выявить ситуации, требующие обращения к врачу.
Таким образом, для достижения и поддержания целевых показателей гликемического контроля существенное значение имеет систематический самоконтроль гликемии пациентом с СД. Современные технологии методов СКГ направлены на повышение эффективности ССТ, приверженности лечению и улучшение качества жизни пациентов. Высокая точность, упрощение процедуры измерений глюкозы крови, информационно-коммуникационные технологии взаимодействия пациента и лечащего врача, широкий выбор дополнительных функций системы Контур Плюс Уан позволяют реализовать все преимущества СКГ на практике.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Информация об авторе
Information about the author
Бирюкова Елена Валерьевна – д-р мед. наук, проф. каф. эндокринологии и диабетологии, ФГБОУ ВО РосУниМед.
E-mail: lena@obsudim.ru ORCID: 0000-0001-9007-4123
Elena V. Biryukova – Dr. Sci. (Med.), Professor, Russian University of Medicine. E-mail: lena@obsudim.ru
ORCID: 0000-0001-9007-4123
Поступила в редакцию: 02.03.2024
Поступила после рецензирования: 15.03.2024
Принята к публикации: 21.03.2024
Received: 02.03.2024
Revised: 15.03.2024
Accepted: 21.03.2024
Therapeutic avenues and prospects of blood glucose self-monitoring, the essential component of diabetes mellitus management
Elena V. BiryukovaRussian University of Medicine, Moscow, Russia
lena@obsudim.ru
Abstract. Diabetes mellitus (DM) is one of the global problems of world’s healthcare. Systemic vascular complications are the dangerous sequelae of the disease, and chronic hyperglycemia is the leading factor contributing to the disease development. Glycemic control remains an effective strategy to prevent diabetes complications that requires achieving and maintaining metabolic targets throughout the life of the patient. The current guidelines on the selection of personalized treatment goals based on the glycated hemoglobin (HbA1c) levels and the glycemic control methods are discussed. The emphasis is placed on self-monitoring of blood glucose (SMBG), one of the important factors contributing to the efficacy of the ongoing glucose-lowering therapy and hypoglycemia prevention. Proper SMBG is impossible without therapeutic training of DM patients. The current understanding of SMBG implies a certain frequency of the systematic measurement of blood glucose levels depending on the DM type and the type of glucose-lowering therapy. Various glucose meters for measurement of blood glucose levels at home are available. The criteria for choosing the glucose meter include compliance with the relevant accuracy standards, simplicity and ease of use, ease of getting the results by patients, which allow patients of any age to easily measure blood glucose levels. With all the advancements in modern technology, the glucose meters have appeared that significantly expand the possibilities of DM control due to integration with the free mobile application.
Keywords: diabetes mellitus, hyperglycemia, target range, glycated hemoglobin, self-monitoring of blood glucose, postprandial blood glucose levels, glucose meters.
For citation: Biryukova E.V. Therapeutic avenues and prospects of blood glucose self-monitoring, the essential component of diabetes mellitus management. Clinical analysis in general medicine. 2024; 5 (2): 82–88 (In Russ.). DOI: 10.47407/kr2023.5.2.00392
Сахарный диабет (СД) − одна из глобальных проблем мирового здравоохранения, поэтому актуально обсуждение вопросов лечения заболевания и эффективного гликемического контроля. В Российской Федерации (на 01.01.2023) число только зарегистрированных больных составило 4 962 762 [1]. Опасными последствиями СД являются системные сосудистые осложнения – нефропатия, ретинопатия, поражение магистральных сосудов сердца, головного мозга, артерий нижних конечностей, которые приводят к ранней инвалидизации и влияют на прогноз жизни пациентов. В связи с развитием системных сосудистых осложнений, преждевременной инвалидизацией, необходимостью пожизненной фармакотерапии, высокой смертностью СД представляет тяжелое бремя для системы здравоохранения и бюджета государства [1–3].
 Значимость достижения гликемического контроля имеет широкие научные доказательства, вместе с тем еще не решены насущные проблемы, связанные с достижением оптимального метаболического контроля и профилактикой хронических осложнений СД [3, 4]. Согласно крупному метаанализу 24 исследований только 42,8% пациентов с СД 2-го типа – СД 2 (95% доверительный интервал 38,1–47,5%) имели целевой контроль гликемии [5]. В экономическом анализе, целью которого было определение затрат системы отечественного здравоохранения и потерь в экономике, связанных с СД 2 и его сердечно-сосудистыми осложнениями, результаты подсчетов затрат показали, что на некомпенсированных больных СД 2 тратится больше средств, чем на пациентов с контролируемым заболеванием (рис. 1) [6]. Усредненный экономический ущерб на 1 пациента с СД 2 нарастает с декомпенсацией заболевания, согласно эпидемиологическим данным, приемлемые показатели гликированного гемоглобина HbA1c (менее 6,5%, до 7,5%) наблюдались в 47,9% случаев, а 52,1% больных имели некомпенсированный СД 2, причем половина из них – HbA1c>8,5%, что представляется весьма опасным с точки зрения развития и прогрессирования сердечно-сосудистых осложнений. Одним из механизмов потенциального снижения экономического бремени СД является предотвращение его осложнений, что может быть реализовано через улучшение гликемического контроля [2, 6].
Значимость достижения гликемического контроля имеет широкие научные доказательства, вместе с тем еще не решены насущные проблемы, связанные с достижением оптимального метаболического контроля и профилактикой хронических осложнений СД [3, 4]. Согласно крупному метаанализу 24 исследований только 42,8% пациентов с СД 2-го типа – СД 2 (95% доверительный интервал 38,1–47,5%) имели целевой контроль гликемии [5]. В экономическом анализе, целью которого было определение затрат системы отечественного здравоохранения и потерь в экономике, связанных с СД 2 и его сердечно-сосудистыми осложнениями, результаты подсчетов затрат показали, что на некомпенсированных больных СД 2 тратится больше средств, чем на пациентов с контролируемым заболеванием (рис. 1) [6]. Усредненный экономический ущерб на 1 пациента с СД 2 нарастает с декомпенсацией заболевания, согласно эпидемиологическим данным, приемлемые показатели гликированного гемоглобина HbA1c (менее 6,5%, до 7,5%) наблюдались в 47,9% случаев, а 52,1% больных имели некомпенсированный СД 2, причем половина из них – HbA1c>8,5%, что представляется весьма опасным с точки зрения развития и прогрессирования сердечно-сосудистых осложнений. Одним из механизмов потенциального снижения экономического бремени СД является предотвращение его осложнений, что может быть реализовано через улучшение гликемического контроля [2, 6].Пациенты с СД должны как можно раньше получать лечение в полном объеме в соответствии с национальными и международными рекомендациями, краеугольным камнем которых является концепция персонализированной медицины. Изменение образа жизни (рациональное питание и повышение физической активности), обучение принципам управления заболеванием являются неотъемлемой частью лечения и должны осуществляться на всем протяжении заболевания [7, 8]. Современное эффективное управление СД – это комплексный процесс, который включает многие взаимосвязанные компоненты и предполагает тесное взаимодействие врача и пациента для достижения гликемического контроля.
Улучшение прогноза пациентов с СД определяется оптимальным контролем основных показателей углеводного обмена, которые включают HbA1c, гликемию натощак, постпрандиальную гликемию (ППГ) [7–9]. HbA1c имеет неоценимое значение для диагностики СД, а также выбора терапии (моно- или комбинированная терапия) и интенсификации сахароснижающей терапии (ССТ), а также для контроля ее эффективности; однако этот показатель не несет информации касательно ежедневного уровня глюкозы в крови, эпизодов гипогликемии и вариабельности уровня глюкозы [9]. Целевые уровни HbA1c – уровни показателя, при которых риск диабетических осложнений существенно снижается [10].
Клинические рекомендации по стандартизации и оптимизации оказания медицинской помощи больным СД во всех регионах России предлагают подход для индивидуализированного выбора целей терапии по HbA1c, основанный на возрасте пациента, ожидаемой продолжительности жизни, наличии атеросклеротических сердечно-сосудистых заболеваний (АССЗ) и риска тяжелой гипогликемии (табл. 1).

Для успешного результата лечения СД также необходимы данные оперативного контроля уровня гликемии в разные временные периоды (натощак, до приема пищи, через 2 ч после приема пищи, перед сном). Это помогает выявить не только показатели глюкозы в крови, выходящие за пределы целевых значений, но и индивидуальные закономерности изменения гликемии в разное время суток, а также оценить влияние на показатели глюкозы в крови факторов питания, физической нагрузки и эффективность и безопасность назначенной терапии СД [11–13].
Оптимальным инструментом контроля гликемии является суточное мониторирование глюкозы, отражающее все суточные колебания гликемии. Однако этот метод исследования глюкозы в повседневной жизни пока невыполним для большинства пациентов с СД. Самоконтроль гликемии (СКГ) с помощью глюкометра – самый простой и, возможно, наиболее практичный инструмент для контроля гликемии. Он дополняет тестирование HbA1c при оценке гликемического профиля и играет ключевую роль в ежедневном мониторинге уровня глюкозы в плазме у пациентов с СД [12–14].
СКГ – ключевой компонент повышения эффективности немедикаментозных и медикаментозых методов управления гликемией [15]. В настоящее время модификация образа жизни рекомендуется в качестве первой линии лечения СД 2. Важной терапевтической задачей наряду с эффективным контролем гликемии является снижение массы тела, что достигается повышением физической активности и ограничением калорийности рациона [7, 16, 17]. Физическая активность является важным компонентом здорового образа жизни, повышает качество жизни, но не является методом ССТ при СД 1-го типа (СД 1) и может повышать риски гипогликемий во время и после нагрузки. Пациенты с СД должны иметь информацию о возможных колебаниях уровня глюкозы в крови во время любой физической активности и занятий спортом. СКГ позволяет дать оценку индивидуальной реакции со стороны уровня глюкозы в крови у пациента в ответ на различные виды физической нагрузки и повысить мотивацию пациентов к регулярной физической активности [7, 18].
Выполнение физических упражнений должно быть безопасно, поэтому всем пациентам следует контролировать гликемию, а особенно получающим препараты инсулина или пероральные препараты, стимулирующие секрецию инсулина. Мониторинг гликемии необходим перед физическими нагрузками, временным противопоказанием для которых является уровень глюкозы плазмы более 13,0 ммоль/л в сочетании с кетонурией или 16 ммоль/л (даже без кетонурии). Больным СД 1, проводящим СКГ и владеющим методами профилактики гипогликемий, можно заниматься любыми видами физической активности [7].
Регулярная физическая активность у больных СД 2 способствует достижению целевых уровней гликемии, похудению, помогает уменьшить инсулинорезистентность. Применение многокомпонентных программ модификации образа жизни способствует улучшению клинических показателей [19]. Показано, что СКГ повышает результат подобных программ по коррекции образа жизни. В ретроспективный анализ S. Tomah и соавт. были включены результаты программы модификации образа жизни (Why WAIT, продолжительность 12 нед); наряду с изменением образа жизни участникам (средний возраст 57±9 лет, длительность СД 2 10±8 лет, индекс массы тела 36±6 кг/м², HbA1c 7,8±1,4%, 45% пациентов получали инсулин) было предложено самостоятельно контролировать уровень глюкозы в крови с помощью глюкометра ежедневно. Гликемию необходимо было измерять перед каждым приемом пищи, перед сном, до и после тренировки, периодически через 2 ч после еды, а также при подозрении, что уровень глюкозы в их крови низкий или высокий [16]. С учетом частоты СКГ, осуществляемого пациентами с СД 2 за период наблюдения, участников разделили на 3 группы (в зависимости от тертиля СКГ): средний диапазон частоты СКГ составил 2,3 (1,1–2,9) раза в сутки в группе нижнего тертиля, 3,4 (3–3,9) раза в сутки и 5 (4–7,7) раз в сутки в группах среднего и высокого тертиля частоты СКГ соответственно. Исходно средняя масса тела пациентов составляла 107,6±20,3 кг в группе нижнего тертиля частоты СКГ, 107,4±19,2 кг – в группе среднего тертиля и 107,4±24 кг – высшего тертиля; HbA1c – 7,5±1,0%, 8,0±1,5% и 8,0±1,6% соответственно. Группы были сопоставимы по возрасту, полу, расе, продолжительности диабета, использованию инсулина, уровню HbA1c, индексу массы тела.
Через 12 нед участники группы с высокой частотой СКГ достигли значительно большей потери массы тела по сравнению с группами более низкой частоты тестирования уровня глюкозы. Участники из группы самого высокого тертиля частоты СКГ достигли среднего снижения массы тела на 10,4 кг (от -7,6 до -14,4 кг) по сравнению с 8,3 кг (от -5,2 до -12,2 кг) и -6,9 кг (от -4,2 до -8,9 кг) в группах среднего и нижнего тертиля соответственно (p=0,018). Динамика индекса массы тела в зависимости от тертилей частоты СКГ у пациентов составила -3,9 кг/м² (от -2,8 до -4,9 кг/м²), -2,7 кг/м² (от -1,6 до -3,9 кг/м²) и -2,5 кг/м² (от -1,5 до 3,3 кг/м²); p=0,012. Более высокая частота тестирования уровня глюкозы была связана со значительно лучшей динамикой HbA1c, отмеченной в конце исследования. Так, снижение HbA1c составило -1,25% (от -0,6 до -3,1%) в группе с высокой частотой СКГ по сравнению с -0,8% (от -0,3 до -2%) и -0,5% (от -0,2 до -1,2%) в группах среднего и нижнего тертилей частоты СКГ соответственно (p=0,048).
Различные исследования демонстрируют, что уровень HbA1c начинает значимо улучшаться, как только пациент увеличивает частоту СКГ независимо от типа СД или вида ССТ [13, 20, 21]. В то же время пациенты не всегда выполняют врачебные рекомендации, что касается и регулярности осуществления СКГ [22, 23]. В частности, по данным исследования M. Hansen и соавт., лишь 39% больных СД проводят СКГ ежедневно, 20% – несколько раз в неделю, 17% – 1–2 раза в неделю и 24% – реже одного раза в неделю [23]. К причинам, мешающим адекватному проведению регулярного СКГ, относят разные факторы, включая длительный стаж СД, хроническую боль, злоупотребление алкоголем, полипрагмазию, плохую информированность о своем состоянии, непрохождение обучения в школе СД и, как следствие, непонимание, каким образом нужно реагировать на полученные цифры измерения глюкозы крови, депрессию, высокую обеспокоенность собственным диабетом, отсутствием поддержки со стороны близких, нехватку льготных расходных материалов для самоконтроля и их высокую стоимость в аптечных сетях, отсутствие медицинской страховки, плохой контакт между пациентом и врачом и, наконец, незаинтересованность врача в данных самоконтроля [24].
Регулярный и грамотный СКГ невозможен без терапевтического обучения больных СД с помощью специально разработанных структурированных программ.
В процессе обучения происходят выработка обоснованных положительных мотиваций, формирование и отработка практических навыков, необходимых для самостоятельного правильного измерения гликемии и интерпретации полученных результатов, изменения поведения пациента в отношении питания и физической активности (структурированный СКГ) [11, 12, 14]. К сожалению, некоторые пациенты оставляют без внимания результаты СКГ, даже видя значительные отклонения гликемии от целевых значений, и, соответственно, не вносят необходимых изменений в питание, режим физических нагрузок, лечение. Поэтому, несмотря на проведение пациентом СКГ, не реализуются его значимые преимущества для лечения СД. Это происходит только в случае, когда обученный пациент активно использует результаты самоконтроля как отправную точку для принятия самостоятельных решений в различных жизненных ситуациях [12, 14, 18]. В том числе СКГ может предотвратить отклонения глик
 емии, которые могут быть опасными при определенных видах занятости (например, посменная работа, работа в ночное время, работа, связанная с выраженной физической нагрузкой, вождение автомобиля).
емии, которые могут быть опасными при определенных видах занятости (например, посменная работа, работа в ночное время, работа, связанная с выраженной физической нагрузкой, вождение автомобиля).В процессе терапевтического обучения необходимо обсудить с пациентом индивидуальные целевые значения основных показателей гликемического контроля и частоту проведения СКГ, время измерения гликемии [7, 8, 14]. К сожалению, в реальности многие пациенты с СД контролируют гликемию нерегулярно и в основном измеряют уровень глюкозы натощак: в исследовании S. Farhan и соавт. только 20% пациентов выполняли СКГ через 2 ч после основного приема пищи, при этом 16% – проводили СКГ при плохом самочувствии, а 14% – при симптомах гипогликемии [22]. Наиболее выраженные колебания глюкозы крови у больных СД наблюдаются после приема пищи; ППГ – это достаточно частый лабораторный сдвиг, наблюдаемый даже у пациентов с целевым уровнем HbA1c. Доказано, что ППГ ассоциируется с сердечно-сосудистыми осложнениями и смертностью [25]. Поэтому СКГ обязательно должен включать измерение глюкозы не только натощак, но и через 2 ч после приема пищи [7]. Измерение гликемии через 2 ч после приема пищи позволяет выявить повышение ППГ, оценить влияние факторов питания, эффективности ССТ.
Гипогликемия может ограничить проведение интенсивного контроля гликемии, который является основой предотвращения осложнений СД [26]. Особого внимания заслуживают гипогликемические состояния, не сопровождающиеся характерной клинической симптоматикой, т.е. бессимптомные, которые наблюдаются у пациентов с нарушением способности распознавать приближающуюся гипогликемию (нарушение автономного ответа на гипогликемию). В исследовании J. Diago-Cabezudo по результатам онлайн-опроса 1848 пациентов с СД, получающих инсулинотерапию (из них 50% с СД 2), были получены интересные данные [27]: каждый третий пациент не всегда мог распознать симптомы гипогликемии, около четверти опрошенных не ощущали характерных симптомов при снижении уровня глюкозы крови ниже нормы (рис. 2). Кроме того, 37% участников сообщили, что стараются поддерживать уровень гликемии выше рекомендованных врачом значений из-за опасения возникновения гипогликемических состояний. 80% респондентов высказали заинтересованность в глюкометрах, способных информировать об отклонениях глюкозы от нормы как в сторону низких, так и в сторону высоких значений.
СКГ позволяет своевременно выявить гипогликемию и осуществить мероприятия, направленные на ее купирование; это особенно важно для пациентов на инсулинотерапии. Кроме того, риски гипогликемий могут увеличивать и другие сахароснижающие препараты (табл. 2) [7].
Структурированный СКГ является основой эффективности проводимой ССТ и профилактики гипогликемии, позволяя помочь в принятии решений по коррекции лечения [12, 14]. Значимые для практики результаты были получены в исследовании N. Lalić и соавт. с участием пациентов с СД на инсулинотерапии (СД 1 – 57 человек, СД 2 – 289 человек), в котором в течение 10 дней проводилось групповое структурированное обучение; психологическое состояние пациентов оценивали по шкале дистресса (Diabetes Distress Scale – DDS) [28]. Спустя 24 нед существенно увеличилась частота СКГ (14,6 раза в неделю по сравнению с 4,3 раза в неделю, р<0,001), отмечено значимое снижение уровня HbA1c на 0,94%; индивидуальные показатели гликемии также значительно улучшились по сравнению с исходными значениями. Важным итогом этой работы стало снижение среднего количества госпитализаций за период наблюдения по сравнению с шестимесячным периодом до включения в исследование (0,14±0,04 по сравнению с 0,59±0,09), также улучшились показатели психологического состояния пациентов по шкале DDS (39,6±13,9 по сравнению с 33,9±14,5, р<0,01), несмотря на увеличение частоты СКГ.
 Использование самостоятельного измерения уровня гликемии крови в сочетании со структурированным обучением пациентов напрямую связано с клинически значимым снижением уровня HbA1c, улучшением индивидуальных показателей гликемии крови и качества жизни пациентов с СД.
Использование самостоятельного измерения уровня гликемии крови в сочетании со структурированным обучением пациентов напрямую связано с клинически значимым снижением уровня HbA1c, улучшением индивидуальных показателей гликемии крови и качества жизни пациентов с СД.Метаанализ Y. Hou и соавт. подтверил, что систематический СКГ дополнительно снижает уровень HbA1c, однако большее преимущество СКГ выявлено в группе пациентов, которые не только регулярно контролировали уровень глюкозы в крови, но и корректировали свой план лечения СД на основе его результатов, что подчеркивает важность именно структурированного СКГ [29].
Рекомендуемая частота СКГ в зависимости от типа СД, вида ССТ отражена в национальных и международных руководствах по лечению СД [7, 8]. В соответствии с Российскими клиническими рекомендациями больным СД 1, а также СД 2 в дебюте заболевания и при недостижении целевых уровней гликемического контроля необходимо определять гликемию ежедневно не менее 4 раз (до еды, через 2 ч после еды, на ночь, периодически ночью) [7]. Далее частота СКГ при СД 2 определяется видом ССТ:
• на интенсифицированной инсулинотерапии – не менее 4 раз ежедневно (до еды, через 2 ч после еды, на ночь, периодически ночью);
• на пероральной ССТ и/или агонистах рецепторов глюканоподобного пептида-1 и/или базальном инсулине – не менее 1 раза в сутки в разное время с одним дополнительным гликемическим профилем (не менее 4 раз в сутки) в неделю (возможно уменьшение частоты при использовании только препаратов с низким риском гипогликемии);
• на готовых смесях инсулина – не менее 2 раз в сутки в разное время + 1 гликемический профиль (не менее 4 раз в сутки) в неделю;
• на диетотерапии – 1 раз в неделю в разное время суток.
При наличии признаков хронических осложнений СД, присоединении сопутствующих заболеваний, появлении дополнительных факторов риска вопрос о частоте обследований решается индивидуально.
Самостоятельный мониторинг гликемии дополнительно необходим перед физическими нагрузками и после них, при подозрении на гипогликемию и после ее лечения, при сопутствующих заболеваниях, если предстоят какие-то действия, потенциально опасные для пациента и окружающих (например, вождение транспортного средства или управление сложными механизмами) [7].
В настоящее время для самостоятельного мониторинга уровня глюкозы в крови рекомендуется применять персональные глюкометры, включая приборы с настройкой индивидуального целевого диапазона гликемии [7]. Внедрение новых технологий в современные системы измерения гликемии делает процесс СКГ значительно проще, и все больше пациентов используют их в повседневной жизни. «Умная» система Contour™ Plus One (Контур Плюс Уан) включает не только сам глюкометр, но и мобильное приложение (рис. 3), что значительно расширяет возможности управления СД со стороны пациента и взаимодействия с врачом.
Важным критерием для выбора глюкометра является соответствие стандартам точности. Глюкометр Контур Плюс Уан продемонстрировал высокую точность, превосходящую требования к точности стандарта ISO 15197:2013 [30, 31]. Высокая точность измерений уровня глюкозы в крови, наряду с удобством применения и наличием расширенных функций, в том числе и в мобильном приложении, помогают пациентам улучшить эффективность СКГ, избежать неправильных решений (например, ошибок в дозировке инсулин) по лечению и достичь лучших результатов.

Технология «Второй шанс» дает возможность повторного нанесения крови на тест-полоску в случае ее недостаточного заполнения, что удобно для каждого пациента с СД, но особенно для лиц старшего возраста. К удобству использования данного глюкометра можно отнести короткое время измерения глюкозы в крови – 5 с, что важно для пациентов в случае развития гипогликемического состояния. Прибор оснащен световым индикатором, расположенным в порте для тест-полосок, – функция «Умная подсветка», которая показывает, что уровень глюкозы в крови находится в пределах диапазона целевого значения (зеленый цвет), выше диапазона целевого значения или ниже диапазона целевого значения (желтый и красный цвета соответственно).
Система Контур Плюс Уан обеспечивает широкие возможности для достижения оптимального и безопасного уровня глюкозы в крови у пациентов с СД. Прибор может автоматически синхронизироваться с мобильным приложением Контур Диабитис (Contour Diabetes), являющимся, по сути, многофункциональным электронным вариантом дневника самоконтроля. Все данные, необходимые для адекватного СКГ, отражаются в электронной версии дневника самоконтроля, что наделяет глюкометр важными информативными функциями и позволяет пациентам более активно использовать СКГ (отмечать количество хлебных единиц, ССТ, оставлять примечания, подробные записи о съеденной пище, прикреплять фото блюд, фиксировать изменения в образе жизни и др.). Функция «Мои тенденции» помогает выявлять тенденции в результатах измерения уровня глюкозы в крови, отправляет уведомления, в том числе о возможных причинах отклонений. Стоит добавить, что наблюдение за положительным влиянием правильного стиля питания и регулярных физических нагрузок на уровень глюкозы в крови может стать мощным мотиватором для улучшения приверженности пациента, помогая укрепить успешное изменение образа и повысить качество жизни [32, 33].
С помощью функции отчетов на основе всех данных, которые поступают в мобильное приложение Контур Диабитис, реализуются современные информационно-коммуникационные технологии в процессе взаимодействия пациента и лечащего врача с целью оптимизации оказания медицинской помощи. Пациенты могут предоставлять врачу в электронном виде подробную информацию о мониторинге гликемии, что позволяет совместно выяснить причины отклонения уровня глюкозы крови и выявить ситуации, требующие обращения к врачу.
Таким образом, для достижения и поддержания целевых показателей гликемического контроля существенное значение имеет систематический самоконтроль гликемии пациентом с СД. Современные технологии методов СКГ направлены на повышение эффективности ССТ, приверженности лечению и улучшение качества жизни пациентов. Высокая точность, упрощение процедуры измерений глюкозы крови, информационно-коммуникационные технологии взаимодействия пациента и лечащего врача, широкий выбор дополнительных функций системы Контур Плюс Уан позволяют реализовать все преимущества СКГ на практике.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Информация об авторе
Information about the author
Бирюкова Елена Валерьевна – д-р мед. наук, проф. каф. эндокринологии и диабетологии, ФГБОУ ВО РосУниМед.
E-mail: lena@obsudim.ru ORCID: 0000-0001-9007-4123
Elena V. Biryukova – Dr. Sci. (Med.), Professor, Russian University of Medicine. E-mail: lena@obsudim.ru
ORCID: 0000-0001-9007-4123
Поступила в редакцию: 02.03.2024
Поступила после рецензирования: 15.03.2024
Принята к публикации: 21.03.2024
Received: 02.03.2024
Revised: 15.03.2024
Accepted: 21.03.2024
Список исп. литературыСкрыть список1. Дедов И.И., Шестакова М.В., Викулова О.К. и др. Сахарный диабет в Российской Федерации: динамика эпидемиологических показателей по данным Федерального регистра сахарного диабета за период 2010–2022 гг. Сахарный диабет. 2023;26(2):104-23.
Dedov I.I., Shestakova M.V., Vikulova O.K. et al. Diabetes mellitus in the Russian Federation: dynamics of epidemiological indicators according to the Federal Register of Diabetes Mellitus for the period 2010–2022. Diabetes. 2023;26(2):104-23 (in Russian).
2. Harding JL, Pavkov ME, Magliano DJ et al. Global trends in diabetes complications: a review of current evidence. Diabetologia 2019; 62(1):3-16. DOI: 10.1007/s00125-018-4711-2
3. Giugliano J, Maiorino MI, Bellastella G et al. Glycemic control, preexisting cardiovascular disease, and risk of major cardiovascular events in patients with type 2 diabetes mellitus: systematic review with meta-Aanalysis of cardiovascular outcome trials and intensive glucose control trials. Am Heart Assoc 2019;8(12):e012356. DOI: 10.1161/JAHA.119.012356
4. Ceriello A, Ihnat MA, Thorpe JE. The metabolic memory: is more than just tight glucose control nessesary to prevent diabetic complications? J Clin Metab 2009;94(2):410-5. DOI: 10.1210/jc.2008-1824
5. Khunti K, Ceriello A, Cos X, De Block C. Achievement of guideline targets for blood pressure, lipid, and glycaemic control in type 2 diabetes: A meta-analysis. Diabetes Res Clin Pract 2018;137:137-48. DOI: 10.1016/j.diabres.2017.12.004. Epub 2018 Jan 8. PMID: 29325774
6. Дедов И.И., Концевая А.В., Шестакова М.В. и др. Экономические затраты на сахарный диабет 2 типа и его основные сердечно-сосудистые осложнения в Российской Федерации. Сахарный диабет. 2016;19(6):518-27. DOI: 10.14341/DM8153
Dedov I.I., Kontsevaya A.V., Shestakova M.V. et al. Economic costs of type 2 diabetes mellitus and its main cardiovascular complications in the Russian Federation. Diabetes. 2016;19(6):518-27. DOI: 10.14341/DM8153 (in Russian).
7. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. Под ред. И.И. Дедова, М.В. Шестаковой,
А.Ю. Майорова. 11-й выпуск. М., 2023.
Algorithms for specialized medical care for patients with diabetes. Ed. I.I. Dedova, M.V. Shestakova, A.Yu. Mayorova. 11th issue. Moscow, 2023 (in Russian).
8. ElSayed NA, Aleppo G, Aroda VR et al. Diabetes Technology: Standards of Care in Diabetes-2023. Diabetes Care 2023;46(Suppl. 1):S111-S127. DOI: 10.2337/dc23-S007
9. Selvin E. Hemoglobin A1c-Using Epidemiology to Guide Medical Practice: Kelly West Award Lecture 2020. Diabetes Care 2021;44(10):2197-204. DOI: 10.2337/dci21-0035
10. Diabetes Prevention Program Research Group. HbA1c as a predictor of diabetes and as an outcome in the Diabetes Prevention Program: a randomized clinical trial. Diabetes Care 2015;38(1):51-8. DOI: 10.2337/dc14-0886
11. Chrvala CA, Sherr D, Lipman RD. Diabetes self-management education for adults with type 2 diabetes mellitus: A systematic review of the effect on glycemic control. Patient Educ Couns 2016;99(6):926-43. DOI: 10.1016/j.pec.2015.11.003
12. Майоров А.Ю., Мельникова О.Г., Филиппов Ю.И. Вопросы самоконтроля гликемии в практике лечения сахарного диабета. Справочник поликлинического врача. 2012;12:32-6.
Mayorov A.Yu., Melnikova O.G., Filippov Yu.I. Issues of glycemic self-control in the practice of treating diabetes mellitus. Directory of a polyclinic doctor. 2012;12:32-6 (in Russian).
13. Schnell O, Hanefeld M, Monnier L. Self-monitoring of blood glucose: a prerequisite for diabetes management in outcome trials. J Diabetes Sci Technol 2014;8(3):609-14. DOI: 10.1177/1932296814528134
14. Benjamin EV. Self-monitoring of blood glucose: The basics. Clin Diabetes 2002;20(1):45-7. DOI: 10.2337/diaclin.20.1.45
15. Shah SZA, Karam JA, Zeb A et al. Movement is improvement: the therapeutic effects of exercise and general physical activity on glycemic control in patients with type 2 diabetes mellitus: a systematic review and meta-analysis of randomized controlled trials. Diabetes Therapy 2021;12(3):707-32. DOI: 10.1007/s13300-021-01005-1
16. Tomah S, Mahmoud N, Mottalib A et al. Frequency of self-monitoring of blood glucose in relation to weight loss and A1C during intensive multidisciplinary weight management in patients with type 2 diabetes and obesity. BMJ Open Diabetes Res Care 2019;7(1):e000659. Published online 2019 Jul 29. DOI: 10.1136/bmjdrc-2019-000659
17. Colberg SR, Sigal RJ, Yardley JE et al. Physical Activity/Exercise and Diabetes: A Position Statement of the American Diabetes Association. Diabetes Care 2016;39(11):2065-79.
18. Biankin SA, Jenkins AB, Campbell LV et al. Target-seeking behavior of plasma glucose with exercise in type 1 diabetes. Diabetes Care 2003;26:297-301.
19. Chen L, Pei J-H, Kuang J et al. Effect of lifestyle intervention in patients with type 2 diabetes: a meta-analysis. Metabolism 2015;64(2):338-47.
20. Sia HK, Kor CT, Tu ST et al. Self-monitoring of blood glucose in association with glycemic control in newly diagnosed non-insulin-treated diabetes patients: a retrospective cohort study. Sci Rep 2021;11(1):1176. DOI: 10.1038/s41598-021-81024-x
21. Zou Y, Zhao S, Li G et al. The Efficacy and Frequency of Self-monitoring of Blood Glucose in Non-insulin-Treated T2D Patients: a Systematic Review and Meta-analysis. J Gen Intern Med 2023;38(3):755-64. DOI: 10.1007/s11606-022-07864-z
22. Farhan SA, Shaikh AT, Zia M et al. Prevalence and Predictors of Home Use of Glucometers in Diabetic Patients. Cureus 2017;9(6):e1330. DOI: 10.7759/cureus.1330
23. Hansen MV, Pedersen-Bjergaard U, Heller SR et al. Frequency and motives of blood glucose self-monitoring in type 1 diabetes. Diabetes Res Clin Pract 2009;85:183-8.
24. Марченкова Л.А., Макарова Е.В. Мотивация пациентов в достижении эффективности самоконтроля гликемии при сахарном диабете: проблемы и их решения. Consilium Medicum. 2017;19(4):
32-5.
Marchenkova L.A., Makarova E.V. Motivation of patients to achieve effective glycemic self-control in diabetes mellitus: problems and their solutions. Consilium Medicum. 2017;19(4):32-5 (in Russian).
25. Levitan EB, Song Y, Ford ES et al. Is nondiabetic hyperglycemia a risk factor for cardiovascular disease? A meta-analysis of prospective studies. Arch Intern Med 2004;164(19):2147-55. DOI: 10.1001/archinte.164.19.2147
26. Seaquist ER, Anderson J, Childs B et al. Hypoglycemia and diabetes: a report of a workgroup of the American Diabetes Association and the Endocrine Society. Diabetes Care 2013;36(5):1384-95. DOI: 10.2337/dc12-2480
27. Diago-Cabezudo JI, Madec-Hily A, Aftab Aslam A. Perceptions of hypoglycemia and self-monitoring of blood glucose in insulin-treated diabetes patients: results from a European online survey. Diabetes Manage 2013;3(1):15-23. DOI:10.2217/dmt.12.66
28. Lalić NM, Lalić K, Jotić A et al. The Impact of Structured Self-Monitoring of Blood Glucose Combined With Intensive Education on HbA1c Levels, Hospitalizations, and Quality-of-Life Parameters in Insulin-Treated Patients With Diabetes at Primary Care in Serbia: The Multicenter SPA-EDU Study. J Diabetes Sci Technol 2017;11(4):746-52. DOI: 10.1177/1932296816681323
29. Hou YY, Li W, Qiu JB, Wang XH. Efficacy of blood glucose self-monitoring on glycemic control in patients with non-insulin-treated type 2 diabetes: a meta-analysis. Int J Nurs Sci 2014;1(2):191-5. DOI: 10.1016/j.ijnss.2014.05.003
30. Freckmann G, Jendrike N, Baumstark A et al. User Performance Evaluation of Four Blood Glucose Monitoring Systems Applying ISO 15197:2013 Accuracy Criteria and Calculation of Insulin Dosing Errors. Diabetes Ther 2018;9(2):683-97. DOI: 10.1007/s13300-018-0392-6
31. Bailey TS, Wallace JF, Pardo S et al. Accuracy and User Performance Evaluation of a New, Wireless-enabled Blood Glucose Monitoring System That Links to a Smart Mobile Device. J Diabetes Sci Technol 2017;11(4):736-43. DOI: 10.1177/1932296816680829
32. Parkin CG, Davidson JA. Value of self-monitoring blood glucose pattern analysis in improving diabetes outcomes. J Diabetes Sci Technol 2009;3(3):500-8. DOI: 10.1177/193229680900300314
33. Li Z, Hu Y, Yan R et al. Twenty Minute Moderate-Intensity Post-Dinner Exercise Reduces the Postprandial Glucose Response in Chinese Patients with Type 2 Diabetes. Med Sci Monit 2018;24:7170-7. DOI: 10.12659/MSM.910827


