Клинический разбор в общей медицине №5 2024
Клинический разбор в общей медицине №5 2024
Динамика течения головной боли после окончания курса лечения эренумабом у пациентов с эпизодической и хронической мигренью
Номера страниц в выпуске:6-12
Аннотация
Введение. Мигрень находится на втором месте среди заболеваний по степени влияния на трудоспособность и сопровождается множественными коморбидными состояниями, частота которых увеличивается при хронической форме. Лечение мигрени и улучшение качества жизни пациентов представляют важную клиническую задачу. Моноклональные антитела к кальцитонин-ген родственному пептиду (CGRP) являются первой таргетной терапией мигрени. До настоящего момента нет опубликованных данных об определении продолжительности стойкого эффекта после использования моноклональных антител.
Цель. Определение продолжительности сохранения положительного эффекта после применения эренумаба у пациентов с мигренью.
Материал и методы. В исследовании приняли участие 64 пациента с мигренью, которым было произведено как минимум трехкратное введение эренумаба с прекращением лечения при достижении урежения частоты головной боли как минимум на 30%. Оценивалась частота головной боли и мигрени через 1, 3 и 6 мес после окончания терапии.
Результаты. Отмечается значимое нарастание частоты боли по сравнению с показателями при окончании лечения, однако в сравнении с исходной частотой показатели остаются значимо ниже. У определенного числа пациентов отмечается отсутствие учащения после отмены лечения.
Ключевые слова: мигрень, терапия, моноклональные антитела, эренумаб, качество жизни.
Для цитирования: Гарманова А.А., Бердникова А.В., Латышева Н.В. Динамика течения головной боли после окончания курса лечения эренумабом у пациентов с эпизодической и хронической мигренью. Клинический разбор в общей медицине. 2024; 5 (5): 6–12. DOI: 10.47407/kr2024.5.5.00398
Введение. Мигрень находится на втором месте среди заболеваний по степени влияния на трудоспособность и сопровождается множественными коморбидными состояниями, частота которых увеличивается при хронической форме. Лечение мигрени и улучшение качества жизни пациентов представляют важную клиническую задачу. Моноклональные антитела к кальцитонин-ген родственному пептиду (CGRP) являются первой таргетной терапией мигрени. До настоящего момента нет опубликованных данных об определении продолжительности стойкого эффекта после использования моноклональных антител.
Цель. Определение продолжительности сохранения положительного эффекта после применения эренумаба у пациентов с мигренью.
Материал и методы. В исследовании приняли участие 64 пациента с мигренью, которым было произведено как минимум трехкратное введение эренумаба с прекращением лечения при достижении урежения частоты головной боли как минимум на 30%. Оценивалась частота головной боли и мигрени через 1, 3 и 6 мес после окончания терапии.
Результаты. Отмечается значимое нарастание частоты боли по сравнению с показателями при окончании лечения, однако в сравнении с исходной частотой показатели остаются значимо ниже. У определенного числа пациентов отмечается отсутствие учащения после отмены лечения.
Ключевые слова: мигрень, терапия, моноклональные антитела, эренумаб, качество жизни.
Для цитирования: Гарманова А.А., Бердникова А.В., Латышева Н.В. Динамика течения головной боли после окончания курса лечения эренумабом у пациентов с эпизодической и хронической мигренью. Клинический разбор в общей медицине. 2024; 5 (5): 6–12. DOI: 10.47407/kr2024.5.5.00398
Original article
1 Polyclinic No. 1, Department of the President of the Russian Federation Moscow, Russia;
2 Alexander Vein Headache Clinic, Moscow, Russia;
3 I.M. Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia
garmanova_aa@bk.ru
Abstract
Background. Migraine is the second most incapacitating disease and is accompanied by multiple comorbidities, especially in chronic migraines. Migraine treatment and improvement of the patients’ quality of life are an important clinical issue. The calcitonin gene-related peptide (CGRP) monoclonal antibodies (mAbs) are the first target therapy for migraine. To date, there are no published data on the duration of effect after using mAbs.
Aim. To determine the effect duration after cessation of erenumab treatment in patients with migraine.
Methods. The study included 64 patients with migraine, who received at least three doses of erenumab; treatment was stopped when reduction of the headache frequency by at least 30% was achieved. The frequency of headache and migraine were assessed 1, 3 and 6 months after the end of treatment.
Results. There was a significant increase in the frequency of headache compared to the values reported at the end of treatment, however, the rates were still significantly lower compared to the baseline values. In some patients, no increase in headache frequency following discontinuation of treatment was observed.
Keywords: migraine, therapy, monoclonal antibodies, erenumab, quality of life.
For citation: Garmanova A.A., Berdnikova A.V., Latysheva N.V. The course of headache after the end of treatment with erenumab in patients with episodic and chronic migraine. Clinical review for general practice. 2024; 5 (5): 6–12. (In Russ.). DOI: 10.47407/ kr2023.5.5.00398
В последние 5 лет возможности помощи пациентам с мигренью расширились в связи с появлением нового класса препаратов, что представляет собой серьезный терапевтический прорыв [5]. Моноклональные антитела (мАТ) к основному болевому медиатору мигрени CGRP (Calcitonin Gene-Related Peptide – кальцитонин-ген родственный пептид) или его рецептору стали одними из препаратов первого выбора для лечения как ЭМ, так и ХМ [6]. Терапия данными препаратами является таргетной, так как направлена непосредственно на CGRP как на ключевую молекулу патогенеза приступа мигрени. Данные рандомизированных контролируемых исследований убедительно подтверждают эффективность и безопасность этих препаратов [7].
В последнее время во всем мире уделяется огромное внимание изучению коморбидности мигрени с депрессией, тревогой, астенией, диссомнией, паническим расстройством. Данные исследований указывают, что у людей, страдающих мигренью, вероятность развития психических расстройств в 2–4 раза выше в сравнении со здоровыми людьми, при этом преобладают аффективные и тревожные расстройства [8–13]. При ХМ, по сравнению с ЭМ, депрессия, тревога и хронические болевые расстройства выявляются чаще и выражены в большей степени [14–16]. В связи с этим пациентам с мигренью необходимо проведение профилактического лечения с целью предотвращения трансформации мигрени из эпизодической формы в хроническую, а также скрининг на наличие депрессии и иных коморбидных расстройств с целью повышения качества жизни пациента [17].
До настоящего момента нет опубликованных данных об определении продолжительности стойкого эффекта после использования мАТ в целом и эренумаба в частности. В связи с этим целью нашего исследования являлось определение продолжительности сохранения положительного эффекта после применения эренумаба у пациентов с мигренью
Материалы и методы. В исследование вошли
64 пациента с установленным диагнозом ЭМ или ХМ. Все участники являлись пациентами Клиники головной боли и вегетативных расстройств им. акад. Александра Вейна, ФГБУ «Поликлиника №1» УД Президента РФ и клиники Фомина.
Были приняты следующие критерии включения в исследование:
• диагноз ЭМ или ХМ в соответствии с критериями Международной классификации ГБ третьего пересмотра [2];
• возраст старше 18 лет;
• как минимум трехкратное введение эренумаба в дозировке 70 мг один раз в месяц с прекращением лечения при достижении урежения частоты ГБ как минимум на 30%;
• информированное добровольное согласие на участие в исследовании.
Пациенты не включались в исследование при наличии тяжелых соматических, неврологических или психических заболеваний, также критериями невключения являлись возраст младше 18 лет, беременность и лактация.
Исходно проводился сбор жалоб и анамнеза, общий клинический и неврологический осмотр, оценка сопутствующих заболеваний. Далее ежемесячно в течение
6 мес оценивался дневник ГБ, клиническое интервью и контролировалось общее состояние пациента.
Статистический анализ полученных данных проводился посредством онлайн-ресурса Statistics Kingdom и программы Microsoft Excel 2016. Для обозначения статистически значимых различий (p<0,05) был принят символ «*».
 В исследовании приняли участие 64 пациента, из них 63 (98,4%) женщины и 1 (1,6%) мужчина. Средний возраст пациентов составил 41,8±11,9 года. Из них исходно до терапии мАТ 23 (35,9%) пациента имели диагноз ЭМ, а 41 пациент (64,1%) – диагноз ХМ. Терапию в течение 3 мес получали 23 (35,9%) пациента, от 4 до 6 мес – 31 (48,3%) пациент, от 7 до 9 мес – 4 (6,25%) пациента, от 10 до 12 мес – 6 (9,75%) пациентов. В среднем, пациенты получили 5,5±2,5 инъекции эренумаба.
В исследовании приняли участие 64 пациента, из них 63 (98,4%) женщины и 1 (1,6%) мужчина. Средний возраст пациентов составил 41,8±11,9 года. Из них исходно до терапии мАТ 23 (35,9%) пациента имели диагноз ЭМ, а 41 пациент (64,1%) – диагноз ХМ. Терапию в течение 3 мес получали 23 (35,9%) пациента, от 4 до 6 мес – 31 (48,3%) пациент, от 7 до 9 мес – 4 (6,25%) пациента, от 10 до 12 мес – 6 (9,75%) пациентов. В среднем, пациенты получили 5,5±2,5 инъекции эренумаба.
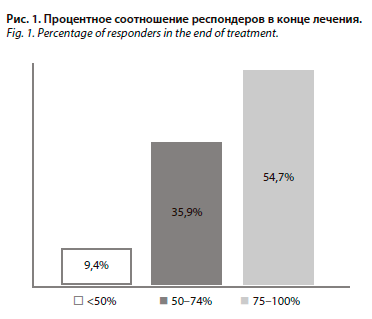
Отмечалось статистически значимое снижение частоты ГБ, частоты мигрени и распространенности избыточного употребления анальгетиков в течение курса лечения. У 6 (9,4%) пациентов снижение частоты ГБ составило <50% от исходного уровня, у 58 (90,6%) пациентов – 50% и более (рис. 1). Клинические данные представлены в табл. 1.

В связи с недостаточно высокой комплаентностью пациентов в течение периода наблюдения число участников уменьшилось, и к 6-му месяцу исследования составило 33 человека. Схема исследования представлена на рис. 2.
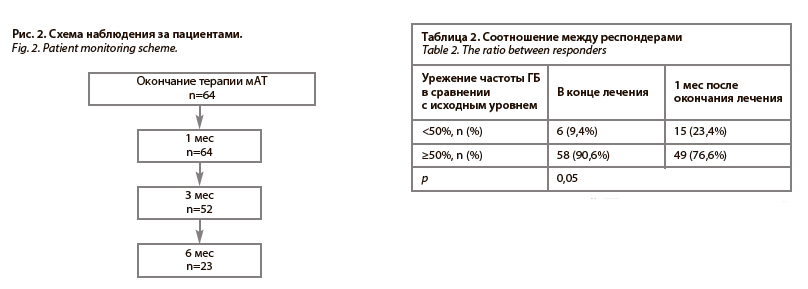
Динамика показателей частоты ГБ и частоты мигрени 1 мес после окончания терапии. По прошествии 1 мес после введения последней инъекции мАТ отмечалось статистически значимое увеличение частоты ГБ по сравнению с последним месяцем лечения – от 4 (2, 7,3) до 5 (3, 9), p<0,00001*, однако частота ГБ осталась значимо ниже показателей ГБ перед началом лечения, p<0,00001* (рис. 3).
Медиана количества дней, на которое увеличилась частота ГБ, составила 1 (0, 3). Не отмечается значимого уменьшения числа ≥50% респондеров относительно исходной частоты боли (табл. 2).
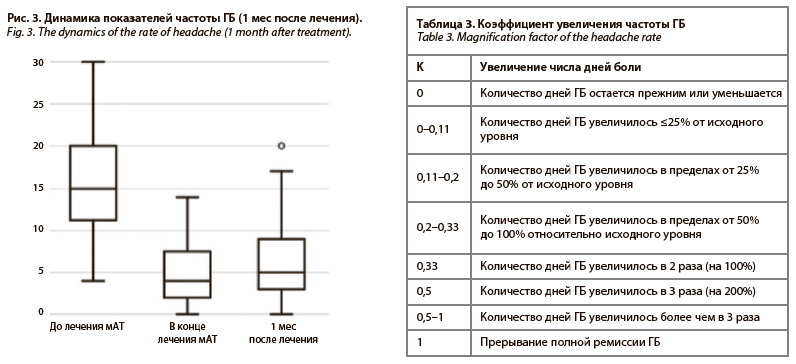
Частота мигрени также значимо возросла по сравнению с последним месяцем лечения – от 3 (2, 5, 3)
до 4 (2, 6), p<0,001*, но осталась значимо ниже относительно показателей перед началом лечения, p<0,001*.
Для оценки процентного изменения частоты ГБ между показателями в конце лечения и показателями в месяц отслеживания после окончания лечения (1, 3,
6 мес) был принят коэффициент (k), равный отношению разности количества дней боли на сумму количества дней боли в конце лечения и количества дней боли в месяц отслеживания:
разность количества дней боли между месяцами
k = количество дней боли в месяц в конце лечения +
количество дней боли в месяц в момент отслеживания
При оценке коэффициента увеличения числа дней ГБ между последним месяцем терапии и через месяц после ее окончания показатель k составил 0,14 (0, 0,3), что соответствует увеличению дней ГБ в пределах от 25% до 50%. У 28 (35%) пациентов наблюдалось отсутствие учащения ГБ (k=0), у 6 (7,5%) пациентов учащение составило <25% (0<k<0,11) у 11 (13,75%) пациентов число дней ГБ увеличилось в пределах от 25% до 50% (0,11≤k<0,2), у 15 (18,75%) пациентов – более 50% (0,2≤k<0,33), у 13 (16,25%) пациентов частота увеличилась в два раза и более (0,33≤k<1), и у 7 (8,75%) пациентов прервалась ремиссия ГБ (k=1). Данные представлены в графическом виде на рис. 4.
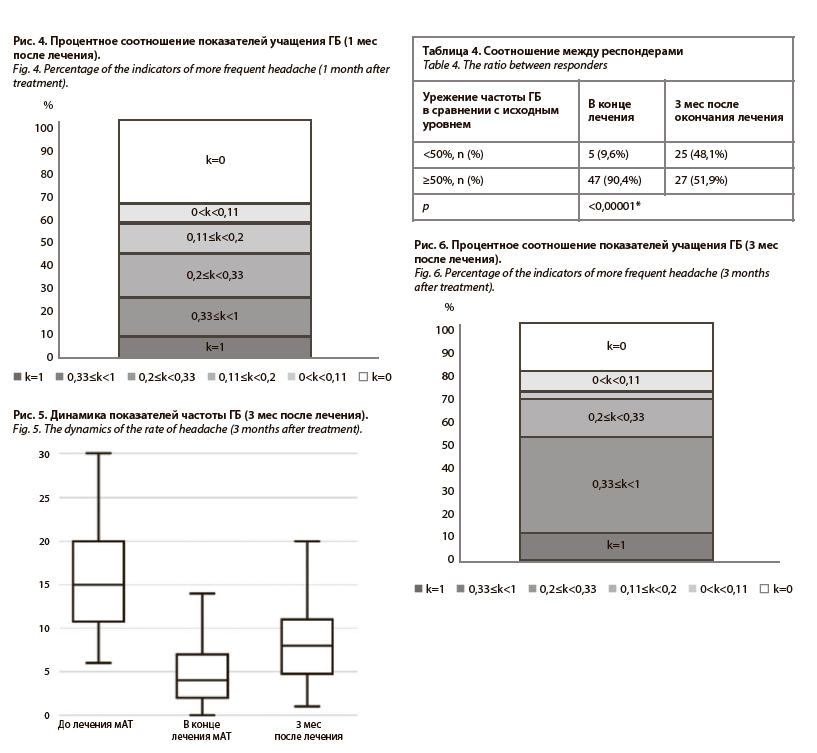
При сравнении показателей учащения ГБ (менее чем на 50% или на 50% и более) после отмены терапии у пациентов с ЭМ и ХМ не отмечалось статистически значимой разницы, p=0,1.3 мес после окончания терапии. Через 3 мес после окончания терапии мАТ также наблюдалось значимое учащение частоты ГБ по сравнению с показателями при окончании лечения, от 4 (2, 7) до 8 (5, 11), p<0,00001*, но при этом частота ГБ оставалась значимо меньше в сравнении с исходным уровнем до лечения, p<0,00001*. Данные графически представлены на рис. 5.
Медиана количества дней увеличения частоты ГБ составила 3 (1, 6). Доля ≥50% респондеров по сравнению с периодом активной терапии значимо снизилась. Данные представлены в табл. 4.
Что касается частоты мигрени, отмечается статистически значимое увеличение по сравнению с частотой при окончании терапии, от 3 (1, 5) до 7 (4, 10), p<0,00001*. В сравнении с частотой мигрени до начала лечения, количество дней мигрени через 3 мес после окончания лечения было статистически значимо ниже, p<0,00001*.
Медиана коэффициента увеличения количества дней ГБ между окончанием терапии и 3 мес наблюдения после окончания составила 0,33 (0,07, 0,54), что соответствует увеличению частоты ГБ в два раза (см. табл. 3). Отсутствие учащения ГБ (k=0) наблюдалось у 13 (20%) пациентов, у 6 (9,2%) пациентов учащение составило <25% (0<k<0,11) у 1 (1,5%) пациента учащение наблюдалось в пределах от 25% до 50% (0,11≤k<0,2), у 11 (16,9%) пациентов учащение составило более 50% (0,2≤k<0,33), у 26 (40%) пациентов частота увеличилась в два раза и более (0,33≤k<1), и у 8 (12,3%) пациентов прервалась ремиссия ГБ (k=1). Данные представлены в графическом виде на рис. 6.
При сравнении показателей учащения ГБ (менее чем на 50% или на 50% и более) у пациентов с ЭМ и ХМ не отмечалось статистически значимой разницы, p=0,6.
Через 2 мес после прекращения терапии эренумабом частота ГБ увеличилась клинически значимо (более чем на одно стандартное отклонение – 4 дня в месяц) у 32% пациентов, через 3 мес – у 45% пациентов.
6 мес после окончания терапии. Отмечалось значимое увеличение количества дней ГБ по сравнению с моментом окончания лечения – от 3 (2, 6) до 6 (3, 10), p=0,005*. Медиана увеличения дней ГБ составила 2 (1, 6), что не отличается статистически от медианы увеличения дней ГБ через 3 мес после окончания терапии, p=0,5. В сравнении с исходной частотой ГБ до лечения, частота ГБ через 6 мес после окончания терапии статистически значимо ниже, p<0,00001* (рис. 7).
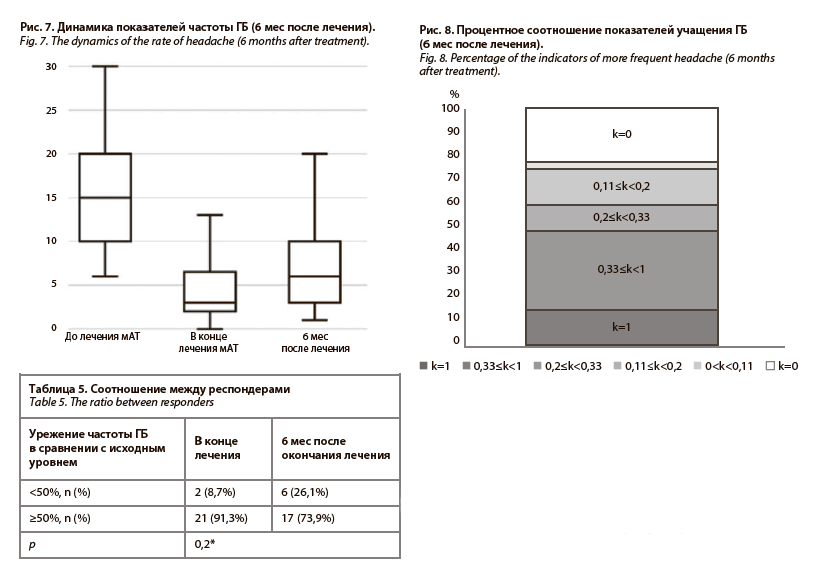
Соотношение числа пациентов с урежением частоты ГБ относительно исходного уровня в конце лечения и через 6 мес статистически значимо не различается (n=23) (табл. 5), дальнейшего учащение ГБ по сравнению с 3 мес после окончания терапии не наблюдается.
Частота мигрени значимо увеличилась по сравнению с моментом окончания лечения, от 3 (1, 5) до 5 (3, 9), p=0,002*, однако по сравнению с исходной частотой осталась статистически значимо низкой, p<0,00001*.
Медиана коэффициента увеличения количества дней ГБ между окончанием терапии и 6-м месяцем наблюдения после окончания составила 0,25 (0,05, 0,67), что соответствует увеличению частоты ГБ более чем на 50%, но менее чем в 2 раза. У 7 (21,2%) пациентов наблюдалось отсутствие увеличения частоты ГБ (k=0), у 1 (3%) пациента увеличение частоты составило <25% (0<k<0,11), у 5 (15,2%) пациентов – в пределах от 25% до 50% (0,11≤k<0,2), у 3 (9,1%) пациентов – более 50% (0,2≤k<0,33), у 11 (33,3%) пациентов частота увеличилась в 2 раза и более (0,33≤k<1) и у 5 (15,2%) пациентов вновь появились ГБ после полной ремиссии (k=1). Данные представлены в графическом виде на рис. 8.
При сравнении показателей учащения ГБ (менее чем на 50% или на 50% и более) у пациентов с ЭМ и ХМ не отмечалось статистически значимой разницы, p=1.
Однако вопрос долгосрочного сохранения эффекта после отмены препарата и скорость обратного возрастания частоты ГБ остаются малоизученными. В исследовании de Matteis и соавт. [20] оценивалось возрастание количества дней боли через 1 мес после окончания терапии. Авторами было показано, что у пациентов, снижение частоты боли у которых в момент окончания лечения по сравнению с исходным уровнем составило 50% и более, через 1 мес после окончания терапии отмечается значимое возрастание количества дней ГБ в сравнении с моментом окончания терапии, тогда как количество дней ГБ через 1 мес после окончания значимо ниже, чем количество дней ГБ перед началом лечения. Эти данные сопоставимы с нашими результатами, при этом стоит отметить, что в исследовании de Matteis пациенты (n=32) получали терапию в течение 12 мес, тогда как среди наших пациентов только 6 (7,5%) человек получили 12 инъекций препаратов мАТ, а большая часть проходила терапию в течение
4–6 мес (44 пациента – 55%). В исследовании M. Nsaka и соавт. [21] изучалось состояние пациентов с ЭМ (n=14) и ХМ (n=32) во время двухмесячного перерыва после годового курса анти-CGRP мАТ. 64% пациентов с ЭМ и 56% пациентов с ХМ сообщали об ухудшении ГБ более чем на 50%. По результатам нашего исследования подобное ухудшение через 1 мес после окончания терапии отмечали 35 (43,8%) пациентов.
В нашем исследовании изучен бóльший промежуток времени после окончания терапии в сравнении с данными мировой литературы – до 6 мес, и расчеты проведены на бóльшей выборке пациентов (n=64). Интерпретация показателей учащения частоты боли представляет сложный научный и клинический вопрос. Нами предложен коэффициент, который отражает связь разницы дней между рассматриваемыми временны́ми точками с количеством дней боли в рассматриваемые интервалы и показывает выраженность увеличения частоты ГБ для каждого конкретного пациента, позволяя сравнивать показатели и оценивать структуру выборки.
Представляют интерес данные, свидетельствующие о том, что как через 1 мес, так и через 3 и 6 мес после прекращения лечения частота ГБ значимо увеличивается, однако при этом частота ГБ в каждый рассматриваемый месяц после окончания лечения остается значимо ниже, чем показатели, отмечавшиеся до начала лечения. Что касается количества дней мигрени, результаты являются аналогичными. При этом у определенного процента пациентов не отмечалось нарастания частоты ГБ (сохранение эффекта) – 35% среди обследованных – через 1 мес, 20% среди обследованных – через 3 мес, 21,2% среди обследованных – через 6 мес. Для дальнейшей интерпретации полученных результатов и возможности сделать заключение о стойкости полученного эффекта как минимум у 1/5 пациентов (≈20%), необходимо проведение исследований на больших выборках пациентов.
Обращает на себя внимание не описанная ранее в литературе стабилизация частоты ГБ через 3 мес после отмены эренумаба и отсутствие значимого дальнейшего нарастания частоты ГБ и частоты мигрени.
Количество пациентов, частота ГБ у которых увеличилась менее чем на 50% в группе, обследованной через 1 мес после окончания терапии, составило 56,3%, через 3 мес – 30,8%, через 6 мес – 39,4%, что позволяет выразить осторожный оптимизм относительно возможности дальнейшего определения предикторов удержания эффектов проведенной терапии. Это также свидетельствует о необходимости длительной терапии эренумабом в лечении как ЭМ, так и ХМ.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Гарманова Анна Александровна – врач-невролог, исполняющая обязанности зав. отделением неврологии, мануальной терапии и рефлексотерапии, ФГБУ «Поликлиника №1»
УД Президента РФ. E-mail: garmanova_aa@bk.ru;
ORCID: 0000-0002-1248-0545
Anna A. Garmanova – Neurologist, Polyclinic No. 1 Department of the President of the Russian Federation.
E-mail: garmanova_aa@bk.ru; ORCID: 0000-0002-1248-0545
Бердникова Анна Владимировна – ассистент каф. нервных болезней Института профессионального образования, ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет), Клиника головной боли и вегетативных расстройств им. акад. Александра Вейна. E-mail: asimcin@mail.ru;
ORCID: 0000-0002-4447-2152
Anna V. Berdnikova – Аssistant, Sechenov First Moscow State Medical University (Sechenov University), Clinic
of headache and autonomic disorders named after Alexander Vane. E-mail: asimcin@mail.ru;
ORCID: 0000-0002-4447-2152
Латышева Нина Владимировна – д-р мед. наук, доц., проф. каф. нервных болезней Института профессионального образования, ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет), Клиника головной боли и вегетативных расстройств им. акад. Александра Вейна. E-mail: ninalat@gmail.com;
ORCID: 0000-0001-9600-5540
Nina V. Latysheva – Dr. Sci. (Med.), Assoc. Prof., Sechenov First Moscow State Medical University (Sechenov University), Clinic of headache and autonomic disorders named after Alexander Vane. E-mail: ninalat@gmail.com;
ORCID: 0000-0001-9600-5540
Поступила в редакцию: 15.05.2024
Поступила после рецензирования: 23.05.2024
Принята к публикации: 23.05.2024
Received: 15.05.2024
Revised: 23.05.2024
Accepted: 23.05.2024
The course of headache after the end of treatment with erenumab in patients with episodic and chronic migraine
Anna A. Garmanova1, Anna V. Berdnikova2,3, Nina V. Latysheva2,31 Polyclinic No. 1, Department of the President of the Russian Federation Moscow, Russia;
2 Alexander Vein Headache Clinic, Moscow, Russia;
3 I.M. Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia
garmanova_aa@bk.ru
Abstract
Background. Migraine is the second most incapacitating disease and is accompanied by multiple comorbidities, especially in chronic migraines. Migraine treatment and improvement of the patients’ quality of life are an important clinical issue. The calcitonin gene-related peptide (CGRP) monoclonal antibodies (mAbs) are the first target therapy for migraine. To date, there are no published data on the duration of effect after using mAbs.
Aim. To determine the effect duration after cessation of erenumab treatment in patients with migraine.
Methods. The study included 64 patients with migraine, who received at least three doses of erenumab; treatment was stopped when reduction of the headache frequency by at least 30% was achieved. The frequency of headache and migraine were assessed 1, 3 and 6 months after the end of treatment.
Results. There was a significant increase in the frequency of headache compared to the values reported at the end of treatment, however, the rates were still significantly lower compared to the baseline values. In some patients, no increase in headache frequency following discontinuation of treatment was observed.
Keywords: migraine, therapy, monoclonal antibodies, erenumab, quality of life.
For citation: Garmanova A.A., Berdnikova A.V., Latysheva N.V. The course of headache after the end of treatment with erenumab in patients with episodic and chronic migraine. Clinical review for general practice. 2024; 5 (5): 6–12. (In Russ.). DOI: 10.47407/ kr2023.5.5.00398
Введение
Мигрень – наиболее распространенное неврологическое расстройство из группы первичных головных болей (ГБ), нарушающее привычный жизненный стереотип [1, 2]. Мигрень находится на втором месте по степени влияния на трудоспособность по индексу YLD (Years Lived With Disability – годы жизни, прожитые с нетрудоспособностью), а среди женщин от 15 до 49 лет – на первом [3]. В российской популяции распространенность эпизодической мигрени (ЭМ) в среднем составляет 20,8%, хронической мигрени (ХМ) – 6,8% [4].В последние 5 лет возможности помощи пациентам с мигренью расширились в связи с появлением нового класса препаратов, что представляет собой серьезный терапевтический прорыв [5]. Моноклональные антитела (мАТ) к основному болевому медиатору мигрени CGRP (Calcitonin Gene-Related Peptide – кальцитонин-ген родственный пептид) или его рецептору стали одними из препаратов первого выбора для лечения как ЭМ, так и ХМ [6]. Терапия данными препаратами является таргетной, так как направлена непосредственно на CGRP как на ключевую молекулу патогенеза приступа мигрени. Данные рандомизированных контролируемых исследований убедительно подтверждают эффективность и безопасность этих препаратов [7].
В последнее время во всем мире уделяется огромное внимание изучению коморбидности мигрени с депрессией, тревогой, астенией, диссомнией, паническим расстройством. Данные исследований указывают, что у людей, страдающих мигренью, вероятность развития психических расстройств в 2–4 раза выше в сравнении со здоровыми людьми, при этом преобладают аффективные и тревожные расстройства [8–13]. При ХМ, по сравнению с ЭМ, депрессия, тревога и хронические болевые расстройства выявляются чаще и выражены в большей степени [14–16]. В связи с этим пациентам с мигренью необходимо проведение профилактического лечения с целью предотвращения трансформации мигрени из эпизодической формы в хроническую, а также скрининг на наличие депрессии и иных коморбидных расстройств с целью повышения качества жизни пациента [17].
До настоящего момента нет опубликованных данных об определении продолжительности стойкого эффекта после использования мАТ в целом и эренумаба в частности. В связи с этим целью нашего исследования являлось определение продолжительности сохранения положительного эффекта после применения эренумаба у пациентов с мигренью
Материалы и методы. В исследование вошли
64 пациента с установленным диагнозом ЭМ или ХМ. Все участники являлись пациентами Клиники головной боли и вегетативных расстройств им. акад. Александра Вейна, ФГБУ «Поликлиника №1» УД Президента РФ и клиники Фомина.
Были приняты следующие критерии включения в исследование:
• диагноз ЭМ или ХМ в соответствии с критериями Международной классификации ГБ третьего пересмотра [2];
• возраст старше 18 лет;
• как минимум трехкратное введение эренумаба в дозировке 70 мг один раз в месяц с прекращением лечения при достижении урежения частоты ГБ как минимум на 30%;
• информированное добровольное согласие на участие в исследовании.
Пациенты не включались в исследование при наличии тяжелых соматических, неврологических или психических заболеваний, также критериями невключения являлись возраст младше 18 лет, беременность и лактация.
Исходно проводился сбор жалоб и анамнеза, общий клинический и неврологический осмотр, оценка сопутствующих заболеваний. Далее ежемесячно в течение
6 мес оценивался дневник ГБ, клиническое интервью и контролировалось общее состояние пациента.
Статистический анализ полученных данных проводился посредством онлайн-ресурса Statistics Kingdom и программы Microsoft Excel 2016. Для обозначения статистически значимых различий (p<0,05) был принят символ «*».
Результаты
Характеристика пациентов и исходные показатели В исследовании приняли участие 64 пациента, из них 63 (98,4%) женщины и 1 (1,6%) мужчина. Средний возраст пациентов составил 41,8±11,9 года. Из них исходно до терапии мАТ 23 (35,9%) пациента имели диагноз ЭМ, а 41 пациент (64,1%) – диагноз ХМ. Терапию в течение 3 мес получали 23 (35,9%) пациента, от 4 до 6 мес – 31 (48,3%) пациент, от 7 до 9 мес – 4 (6,25%) пациента, от 10 до 12 мес – 6 (9,75%) пациентов. В среднем, пациенты получили 5,5±2,5 инъекции эренумаба.
В исследовании приняли участие 64 пациента, из них 63 (98,4%) женщины и 1 (1,6%) мужчина. Средний возраст пациентов составил 41,8±11,9 года. Из них исходно до терапии мАТ 23 (35,9%) пациента имели диагноз ЭМ, а 41 пациент (64,1%) – диагноз ХМ. Терапию в течение 3 мес получали 23 (35,9%) пациента, от 4 до 6 мес – 31 (48,3%) пациент, от 7 до 9 мес – 4 (6,25%) пациента, от 10 до 12 мес – 6 (9,75%) пациентов. В среднем, пациенты получили 5,5±2,5 инъекции эренумаба. Отмечалось статистически значимое снижение частоты ГБ, частоты мигрени и распространенности избыточного употребления анальгетиков в течение курса лечения. У 6 (9,4%) пациентов снижение частоты ГБ составило <50% от исходного уровня, у 58 (90,6%) пациентов – 50% и более (рис. 1). Клинические данные представлены в табл. 1.

В связи с недостаточно высокой комплаентностью пациентов в течение периода наблюдения число участников уменьшилось, и к 6-му месяцу исследования составило 33 человека. Схема исследования представлена на рис. 2.

Динамика показателей частоты ГБ и частоты мигрени 1 мес после окончания терапии. По прошествии 1 мес после введения последней инъекции мАТ отмечалось статистически значимое увеличение частоты ГБ по сравнению с последним месяцем лечения – от 4 (2, 7,3) до 5 (3, 9), p<0,00001*, однако частота ГБ осталась значимо ниже показателей ГБ перед началом лечения, p<0,00001* (рис. 3).
Медиана количества дней, на которое увеличилась частота ГБ, составила 1 (0, 3). Не отмечается значимого уменьшения числа ≥50% респондеров относительно исходной частоты боли (табл. 2).

Частота мигрени также значимо возросла по сравнению с последним месяцем лечения – от 3 (2, 5, 3)
до 4 (2, 6), p<0,001*, но осталась значимо ниже относительно показателей перед началом лечения, p<0,001*.
Для оценки процентного изменения частоты ГБ между показателями в конце лечения и показателями в месяц отслеживания после окончания лечения (1, 3,
6 мес) был принят коэффициент (k), равный отношению разности количества дней боли на сумму количества дней боли в конце лечения и количества дней боли в месяц отслеживания:
разность количества дней боли между месяцами
k = количество дней боли в месяц в конце лечения +
количество дней боли в месяц в момент отслеживания
Если у пациента отмечалась ремиссия мигрени
(0 дней боли), то появление дней с болью соответствует коэффициенту 1, что является самым неблагоприятным исходом, так как свидетельствует о выходе из ремиссии. Чем меньше процентно изменилось количество дней боли, тем k ближе к нулю. При отсутствии ухудшения (количество дней ГБ остается прежним) k равен нулю. Для упрощения интерпретации при уменьшении количества дней ГБ k также принимался равным нулю. Интерпретация значений k представлена в табл. 3.При оценке коэффициента увеличения числа дней ГБ между последним месяцем терапии и через месяц после ее окончания показатель k составил 0,14 (0, 0,3), что соответствует увеличению дней ГБ в пределах от 25% до 50%. У 28 (35%) пациентов наблюдалось отсутствие учащения ГБ (k=0), у 6 (7,5%) пациентов учащение составило <25% (0<k<0,11) у 11 (13,75%) пациентов число дней ГБ увеличилось в пределах от 25% до 50% (0,11≤k<0,2), у 15 (18,75%) пациентов – более 50% (0,2≤k<0,33), у 13 (16,25%) пациентов частота увеличилась в два раза и более (0,33≤k<1), и у 7 (8,75%) пациентов прервалась ремиссия ГБ (k=1). Данные представлены в графическом виде на рис. 4.

При сравнении показателей учащения ГБ (менее чем на 50% или на 50% и более) после отмены терапии у пациентов с ЭМ и ХМ не отмечалось статистически значимой разницы, p=0,1.3 мес после окончания терапии. Через 3 мес после окончания терапии мАТ также наблюдалось значимое учащение частоты ГБ по сравнению с показателями при окончании лечения, от 4 (2, 7) до 8 (5, 11), p<0,00001*, но при этом частота ГБ оставалась значимо меньше в сравнении с исходным уровнем до лечения, p<0,00001*. Данные графически представлены на рис. 5.
Медиана количества дней увеличения частоты ГБ составила 3 (1, 6). Доля ≥50% респондеров по сравнению с периодом активной терапии значимо снизилась. Данные представлены в табл. 4.
Что касается частоты мигрени, отмечается статистически значимое увеличение по сравнению с частотой при окончании терапии, от 3 (1, 5) до 7 (4, 10), p<0,00001*. В сравнении с частотой мигрени до начала лечения, количество дней мигрени через 3 мес после окончания лечения было статистически значимо ниже, p<0,00001*.
Медиана коэффициента увеличения количества дней ГБ между окончанием терапии и 3 мес наблюдения после окончания составила 0,33 (0,07, 0,54), что соответствует увеличению частоты ГБ в два раза (см. табл. 3). Отсутствие учащения ГБ (k=0) наблюдалось у 13 (20%) пациентов, у 6 (9,2%) пациентов учащение составило <25% (0<k<0,11) у 1 (1,5%) пациента учащение наблюдалось в пределах от 25% до 50% (0,11≤k<0,2), у 11 (16,9%) пациентов учащение составило более 50% (0,2≤k<0,33), у 26 (40%) пациентов частота увеличилась в два раза и более (0,33≤k<1), и у 8 (12,3%) пациентов прервалась ремиссия ГБ (k=1). Данные представлены в графическом виде на рис. 6.
При сравнении показателей учащения ГБ (менее чем на 50% или на 50% и более) у пациентов с ЭМ и ХМ не отмечалось статистически значимой разницы, p=0,6.
Через 2 мес после прекращения терапии эренумабом частота ГБ увеличилась клинически значимо (более чем на одно стандартное отклонение – 4 дня в месяц) у 32% пациентов, через 3 мес – у 45% пациентов.
6 мес после окончания терапии. Отмечалось значимое увеличение количества дней ГБ по сравнению с моментом окончания лечения – от 3 (2, 6) до 6 (3, 10), p=0,005*. Медиана увеличения дней ГБ составила 2 (1, 6), что не отличается статистически от медианы увеличения дней ГБ через 3 мес после окончания терапии, p=0,5. В сравнении с исходной частотой ГБ до лечения, частота ГБ через 6 мес после окончания терапии статистически значимо ниже, p<0,00001* (рис. 7).

Соотношение числа пациентов с урежением частоты ГБ относительно исходного уровня в конце лечения и через 6 мес статистически значимо не различается (n=23) (табл. 5), дальнейшего учащение ГБ по сравнению с 3 мес после окончания терапии не наблюдается.
Частота мигрени значимо увеличилась по сравнению с моментом окончания лечения, от 3 (1, 5) до 5 (3, 9), p=0,002*, однако по сравнению с исходной частотой осталась статистически значимо низкой, p<0,00001*.
Медиана коэффициента увеличения количества дней ГБ между окончанием терапии и 6-м месяцем наблюдения после окончания составила 0,25 (0,05, 0,67), что соответствует увеличению частоты ГБ более чем на 50%, но менее чем в 2 раза. У 7 (21,2%) пациентов наблюдалось отсутствие увеличения частоты ГБ (k=0), у 1 (3%) пациента увеличение частоты составило <25% (0<k<0,11), у 5 (15,2%) пациентов – в пределах от 25% до 50% (0,11≤k<0,2), у 3 (9,1%) пациентов – более 50% (0,2≤k<0,33), у 11 (33,3%) пациентов частота увеличилась в 2 раза и более (0,33≤k<1) и у 5 (15,2%) пациентов вновь появились ГБ после полной ремиссии (k=1). Данные представлены в графическом виде на рис. 8.
При сравнении показателей учащения ГБ (менее чем на 50% или на 50% и более) у пациентов с ЭМ и ХМ не отмечалось статистически значимой разницы, p=1.
Обсуждение
Действие препаратов мАТ направлено на блокаду периферических эффектов CGRP путем связывания самой молекулы или воздействия на ее рецептор. Период полувыведения препаратов составляет 28–30 дней, после чего требуется повторное введение, и возможно снижение эффективности при отсутствии своевременной инъекции. Согласно рекомендациям российских экспертов, основанных на данных исследований и клиническом опыте, рекомендуемый курс лечения мАТ составляет 6–12 мес при редкой ЭМ, 12–18 мес – при частой ЭМ и ХМ и при необходимости может быть продолжен [18]. Исследование M. Ashina и соавт. [19] показали эффективность и безопасность лечения эренумабом при 5-летнем применении препарата у пациентов с мигренью.Однако вопрос долгосрочного сохранения эффекта после отмены препарата и скорость обратного возрастания частоты ГБ остаются малоизученными. В исследовании de Matteis и соавт. [20] оценивалось возрастание количества дней боли через 1 мес после окончания терапии. Авторами было показано, что у пациентов, снижение частоты боли у которых в момент окончания лечения по сравнению с исходным уровнем составило 50% и более, через 1 мес после окончания терапии отмечается значимое возрастание количества дней ГБ в сравнении с моментом окончания терапии, тогда как количество дней ГБ через 1 мес после окончания значимо ниже, чем количество дней ГБ перед началом лечения. Эти данные сопоставимы с нашими результатами, при этом стоит отметить, что в исследовании de Matteis пациенты (n=32) получали терапию в течение 12 мес, тогда как среди наших пациентов только 6 (7,5%) человек получили 12 инъекций препаратов мАТ, а большая часть проходила терапию в течение
4–6 мес (44 пациента – 55%). В исследовании M. Nsaka и соавт. [21] изучалось состояние пациентов с ЭМ (n=14) и ХМ (n=32) во время двухмесячного перерыва после годового курса анти-CGRP мАТ. 64% пациентов с ЭМ и 56% пациентов с ХМ сообщали об ухудшении ГБ более чем на 50%. По результатам нашего исследования подобное ухудшение через 1 мес после окончания терапии отмечали 35 (43,8%) пациентов.
В нашем исследовании изучен бóльший промежуток времени после окончания терапии в сравнении с данными мировой литературы – до 6 мес, и расчеты проведены на бóльшей выборке пациентов (n=64). Интерпретация показателей учащения частоты боли представляет сложный научный и клинический вопрос. Нами предложен коэффициент, который отражает связь разницы дней между рассматриваемыми временны́ми точками с количеством дней боли в рассматриваемые интервалы и показывает выраженность увеличения частоты ГБ для каждого конкретного пациента, позволяя сравнивать показатели и оценивать структуру выборки.
Представляют интерес данные, свидетельствующие о том, что как через 1 мес, так и через 3 и 6 мес после прекращения лечения частота ГБ значимо увеличивается, однако при этом частота ГБ в каждый рассматриваемый месяц после окончания лечения остается значимо ниже, чем показатели, отмечавшиеся до начала лечения. Что касается количества дней мигрени, результаты являются аналогичными. При этом у определенного процента пациентов не отмечалось нарастания частоты ГБ (сохранение эффекта) – 35% среди обследованных – через 1 мес, 20% среди обследованных – через 3 мес, 21,2% среди обследованных – через 6 мес. Для дальнейшей интерпретации полученных результатов и возможности сделать заключение о стойкости полученного эффекта как минимум у 1/5 пациентов (≈20%), необходимо проведение исследований на больших выборках пациентов.
Обращает на себя внимание не описанная ранее в литературе стабилизация частоты ГБ через 3 мес после отмены эренумаба и отсутствие значимого дальнейшего нарастания частоты ГБ и частоты мигрени.
Количество пациентов, частота ГБ у которых увеличилась менее чем на 50% в группе, обследованной через 1 мес после окончания терапии, составило 56,3%, через 3 мес – 30,8%, через 6 мес – 39,4%, что позволяет выразить осторожный оптимизм относительно возможности дальнейшего определения предикторов удержания эффектов проведенной терапии. Это также свидетельствует о необходимости длительной терапии эренумабом в лечении как ЭМ, так и ХМ.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Гарманова Анна Александровна – врач-невролог, исполняющая обязанности зав. отделением неврологии, мануальной терапии и рефлексотерапии, ФГБУ «Поликлиника №1»
УД Президента РФ. E-mail: garmanova_aa@bk.ru;
ORCID: 0000-0002-1248-0545
Anna A. Garmanova – Neurologist, Polyclinic No. 1 Department of the President of the Russian Federation.
E-mail: garmanova_aa@bk.ru; ORCID: 0000-0002-1248-0545
Бердникова Анна Владимировна – ассистент каф. нервных болезней Института профессионального образования, ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет), Клиника головной боли и вегетативных расстройств им. акад. Александра Вейна. E-mail: asimcin@mail.ru;
ORCID: 0000-0002-4447-2152
Anna V. Berdnikova – Аssistant, Sechenov First Moscow State Medical University (Sechenov University), Clinic
of headache and autonomic disorders named after Alexander Vane. E-mail: asimcin@mail.ru;
ORCID: 0000-0002-4447-2152
Латышева Нина Владимировна – д-р мед. наук, доц., проф. каф. нервных болезней Института профессионального образования, ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет), Клиника головной боли и вегетативных расстройств им. акад. Александра Вейна. E-mail: ninalat@gmail.com;
ORCID: 0000-0001-9600-5540
Nina V. Latysheva – Dr. Sci. (Med.), Assoc. Prof., Sechenov First Moscow State Medical University (Sechenov University), Clinic of headache and autonomic disorders named after Alexander Vane. E-mail: ninalat@gmail.com;
ORCID: 0000-0001-9600-5540
Поступила в редакцию: 15.05.2024
Поступила после рецензирования: 23.05.2024
Принята к публикации: 23.05.2024
Received: 15.05.2024
Revised: 23.05.2024
Accepted: 23.05.2024
Список исп. литературыСкрыть список1. GBD 2013 Mortality and Causes of Death Collaborators. Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet. 2015;385(9963):117-71.
2. Headache Classification Committee of the International Headache Society (IHS) The International Classification of Headache Disorders, 3rd edition. Cephalalgia. 2018;38(1):1-21.
3. Steiner TJ, Stovner LJ, Jensen R et al. Migraine remains second among the world’s causes of disability, and first among young women: findings from GBD2019. J Headache Pain. 2020;21(1):137.
4. Ayzenberg I, Katsarava Z, Sborowski A et al. The prevalence of primary headache disorders in Russia: a countrywide survey. Cephalalgia. 2012;32(5):373-81.
5. Sacco S, Bendtsen L, Ashina M, Reuter U et al. European headache federation guideline on the use of monoclonal antibodies acting on the calcitonin gene related peptide or its receptor for migraine prevention. J Headache Pain. 2019;20(1):
6. Филатова Е.Г., Осипова В.В., Табеева Г.Р. и др. Диагностика и лечение мигрени: рекомендации российских экспертов. Неврология, нейропсихиатрия, психосоматика. 2020;12(4):4-14.
Filatova E.G., Osipova V.V., Tabeeva G.R. et al. Diagnosis and treatment of migraine: recommendations of Russian experts. Neurology, neuropsychiatry, psychosomatics. 2020;12(4):4-14 (in Russian).
7. Амелин А.В., Соколов А.Ю., Ваганова Ю.С. Пятилетний опыт применения нового класса препаратов для таргетной профилактической терапии мигрени. Российский неврологический журнал. 2021;26(3):4-14.
Amelin A.V., Sokolov A.Yu., Vaganova Yu.S. Five-year experience in the use of a new class of drugs for targeted preventive therapy of migraine. Russian Neurological Journal. 2021;26(3):4-14 (in Russian).
8. Zhang Q, Shao A, Jiang Z et al. The exploration of mechanisms of comorbidity between migraine and depression. J Cell Mol Med. 2019;23(7):42505-4513.
9. Ashina S, Serrano D, Lipton RB et al. Depression and risk of transformation of episodic to chronic migraine. J Headache Pain. 2012;13(8):615-24.
10. Peres MFP, Mercante JPP et al. Anxiety and depression symptoms and migraine: a symptom-based approach research. J Headache Pain. 2017;18(1):37.
11. Smitherman TA, Kolivas ED, Bailey JR. Panic disorder and migraine: comorbidity, mechanisms, and clinical implications. Headache. 2013;53(1):23-45.
12. Hamelsky SW, Lipton RB. Psychiatric comorbidity of migraine. Headache. 2006;46(9):1327-33.
13. Jette N, Patten S, Williams J et al. Comorbidity of migraine and psychiatric disorders—a national population-based study. Headache. 2008;48(4):501-16.
14. Buse DC, Manack A, Serrano D et al. Sociodemographic and comorbidity profiles of chronic migraine and episodic migraine sufferers. J Neurol Neurosurg Psychiatry. 2010;81(4):428-32.
15. Blumenfeld AM, Varon SF, Wilcox TK et al. Disability, HRQoL and resource use among chronic and episodic migraineurs: results from the International Burden of Migraine Study (IBMS). Cephalalgia. 2011;31(3):301-15.
16. Артеменко А.Р., Куренков А.Л., Антипова О.С. Диагностика и лечение хронической мигрени. М.: Горячая линия – Телеком, 2014.
Artemenko A.R., Kurenkov A.L., Antipova O.S. Diagnostics and treatment of chronic migraine. Moscow: Goryachaya liniya – Telekom, 2014 (in Russian).
17. Frediani F, Villani V. Migraine and depression. Neurol Sci. 2007;28 (Suppl. 2):S161-5.
18. Сергеев А.В., Табеева Г.Р., Филатова Е.Г. и др. Применение новой биологической патогенетической терапии мигрени в клинической практике: консенсус экспертов Российского общества по изучению головной боли. Неврология, нейропсихиатрия, психосоматика. 2022;14(5):109-16.
Sergeev A.V., Tabeeva G.R., Filatova E.G. et al. Application of a new biological pathogenetic therapy of migraine in clinical practice: consensus of experts of the Russian Society for the Study of Headache. Neurology, neuropsychiatry, psychosomatics. 2022;14(5):109-16 (in Russian).
19. Ashina M, Goadsby PJ, Reuter U et al. Long-term efficacy and safety of erenumab in migraine prevention: Results from a 5-year, open-label treatment phase of a randomized clinical trial. Eur J Neurol. 2021;28(5):1716-25.
20. De Matteis E, Affaitati G, Frattale I, Caponnetto V, Pistoia F, Giamberardino MA, Sacco S, Ornello R. Early outcomes of migraine after erenumab discontinuation: data from a real-life setting. Neurol Sci. 2021;42(8):3297-303.
21. Nsaka M, Scheffler A, Wurthmann S et al. Real-world evidence following a mandatory treatment break after a 1-year prophylactic treatment with calcitonin gene-related peptide (pathway) monoclonal antibodies. Brain Behav. 2022;12(7):e2662.
18 июня 2024
Количество просмотров: 12336


