Клинический разбор в общей медицине №5 2024
Kazan State Medical University, Kazan, Russia
khayros.kzn@gmail.com
Abstract
Relevance. The phenomenon of central sensitization occurs when physiological activity in nociceptive pathways increases and leads to abnormal sensitivity; it is defined as “increased sensitivity of nociceptive neurons of the central nervous system to their normal or subthreshold afferent input,” according to the definition provided by the International Association for the Study of Pain (IASP). The excitability of spinal cord neurons significantly modifies the gain of the somatosensory system. Chronic pain syndromes, anxiety-depressive disorder, sleep disorders are currently very common in the population, significantly reducing the quality of life of the population; the pathogenesis of these nosologies lies in central sensitization.
Objective. To study the clinical manifestations of central sensitization in patients with episodic migraine associated with neck pain or cervicogenic headache.
Materials and methods. The longitudinal prospective study included 180 patients, divided into 3 groups: 1) patients with a combination of migraine and cervicogenic headache – 60 people (study group); 2) patients with a combination of migraine and cervicalgia diagnoses – 60 people (control group); 3) patients diagnosed with migraine without complaints of pain and limitation of movements in the cervical spine – 60 people (additional group).
Results. In patients with migraine and comorbid cervical headache, more pronounced central sensitization was revealed when compared with comorbid cervicalgia. Myofascial pain syndrome involving the trapezius and temporal muscles can resolve on its own with specific migraine therapy with monoclonal antibodies, however, to relieve tension and soreness in the masseter and inferior oblique muscles, the addition of therapeutic exercises and gentle manual techniques is more effective. Taking into account the identified direct relationships of moderate strength between the number of painful points of exit of the trigeminal nerve, the muscles of the pericranial region involved, as well as the effect of treatment of migraine attacks with monoclonal antibodies, it can be concluded that central sensitization is more pronounced when the masseter and inferior oblique muscles are involved.
Conclusions. During examination of patients with migraine with comorbid active cervicalgic factor or even if it is absence, it is necessary to make a thorough examination of the facial and cranioverebral region muscles, even in the absence of patient complaints of pain in the face or neck, and also prescribe specific therapeutic exercises to increase the effectiveness of treatment. In all patients with migraine, regardless of chronicity, it is necessary to assess the intensity of central sensitization for timely and more complete provision of medical care.
Keywords: central sensitization, cervicogenic headache, migraine, cervicalgia, monoclonal antibodies, physical exercises for migraine.
For citation: Khairutdinova O.S., Bogdanov E.I. Cervicalgia in patients with migraine – a comorbid nosology or a clinical aspect of central sensitization? Clinical review for general practice. 2024; 5 (5): 13–20. (In Russ.). DOI: 10.47407/kr2024.5.5.00399
Центральная сенситизация (ЦС) – это патофизиологический феномен формирования усиленного, гипертрофированного ответа структур центральной нервной системы на сенсорные и периферические ноцицептивные стимулы, характеризующийся гипервозбудимостью нейронов дорсальных рогов спинного мозга, восходящих по спиноталамическому тракту [1–3]. ЦС характеризуется тем, что после прекращения действия периферических болевых стимулов остается определенный уровень возбуждения в центральных сенсорных нейронах заднего рога, и это состояние сохраняется автономно или поддерживается слабой ноцицептивной стимуляцией. Сенситизация ноцицепторов возникает вследствие действия алгогенов, поступающих из плазмы крови и выделяющихся из поврежденной ткани, а также из периферических терминалей С-ноцицепторов. Эктопической спонтанной активностью можно объяснить боли в зонах гипестезии, когда волокна большого диаметра повреждены, а боль воспринимается через импульсы, генерируемые в ноцицепторных С-волокнах меньшего диаметра [4].
Кроме того, ЦС включает механизмы, воздействующие на пороги возбудимости болевых и А-бета механорецепторов, таким образом, неболевые стимулы воспринимаются как боль. Так, формируются аллодиния, гипералгезия и следовые реакции. При этом происходят усиленное выделение глутамата и активация N-метил-d-аспартат (NMDA)-рецепторов, дисбаланс и угнетение тормозящих ГАМК-эргических систем.
В научной литературе показано, что ЦС играет роль в патогенезе фибромиалгии, мигрени, головной боли напряжения, синдроме раздраженного кишечника и синдроме беспокойных ног, также данный феномен может лежать в основе процесса хронизации болевых синдромов.
Важнейшим аспектом формирования ЦС является коморбидность психоэмоциональных нарушений, тревожно-депрессивных расстройств у пациентов с болевыми синдромами. Депрессивные расстройства наблюдаются более чем у 1/2 пациентов с хронической болью. Многие авторы приходят к заключению о комплексной модели депрессии и хронической боли. Преимущественная роль отводится недостаточности нисходящих противоболевых систем, дефициту норадреналина и серотонина в синаптической щели, что приводит к увеличению количества и сенсибилизации рецепторов постсинаптической мембраны [5].
Кроме того, хронический стресс и боль индуцируют активность гипоталамо-гипофизарно-надпочечниковой и тиреоидной систем, вследствие чего снижается синтез мозгового нейротрофического фактора (BDNF), нарушается метаболизм фосфолипидов, субстанции Р и других нейрокининов. Также изменяется чувствительность NMDA-рецепторов, усиливается цитотоксическое действие глутамата, нарушается кальциевый гомеостаз, повышается выработка свободных радикалов. Психологический компонент с точки зрения эмоционального стресса следует учитывать в процессе диагностики, чтобы лучше справляться с хроническими болевыми состояниями [6]. Тревога и депрессия могут способствовать развитию, сохранению и
обострению боли.
Другим дисфункциональным компонентом является вызванный болевым раздражением спинальный сенсомоторный рефлекс в соответствующем сегменте спинного мозга, сопровождающийся активацией мотонейронов, что, в свою очередь, приводит к спазму мышц, иннервируемых этими нейронами, мышечный спазм приводит к усилению стимуляции болевых рецепторов мышцы. Предположительно в сформированных триггерных точках содержатся множественные локусы сенситизации, состоящие из одного или нескольких сенситизированных нервных окончаний.
ЦС у пациентов с цервикогенной головной болью (ЦГБ) – основа формирования и поддержания персистирующей головной боли при повреждениях в области шеи. В сравнительном нейрофизиологическом исследовании, включавшем пациентов с ЦГБ и пациентов с дисфункцией в области шеи, но без ЦГБ, у первых обнаружен феномен ЦС. Цервикалгия при этом является одним из наиболее часто представленных сопутствующих болевых синдромов у пациентов с мигренью. По данным различных исследований (Lampl и соавт., Н.В. Латышева) ее распространенность у пациентов с мигренью составляет до 58–71% [7].
Данный аспект является основополагающим в формировании цели нашего исследования: изучить клинические аспекты ЦС у пациентов с мигренью, коморбидной цервикалгией и ЦГБ.
1) пациенты с сочетанием мигрени и ЦГБ – 60 человек (исследуемая группа);
2) пациенты с сочетанием диагнозов мигрень и цервикалгия – 60 человек (контрольная группа);
3) пациенты с диагнозом мигрень без жалоб на боль и ограничение движений в шейном отделе позвоночника – 60 человек (дополнительная группа).
Всем пациентам проведен тщательный сбор анамнеза, неврологический осмотр, верификация ранее установленных диагнозов «эпизодическая мигрень с аурой», «эпизодическая мигрень без ауры», в соответствии с критериями Международной классификации головной боли 3-го пересмотра Международного общества головной боли.
В связи с неоднозначностью критериев диагностики ЦГБ выставлялась пациентам при полном соответствии Международной классификации головной боли 3-го пересмотра Международного общества головной боли, диагностическим критериям O. Sjaastad [8] и определению N. Bogduk, а также при полном купировании головной боли после выполнения новокаиновой блокады латеральных атлантоаксиальных суставов, дугоотросчатых суставов С2-С3, С3-С4, медиальных ветвей С3 и С4 [9].
Интенсивность болевого синдрома оценивалась путем применения трехступенчатой шкалы оценки боли Всемирной организации здравоохранения и шкалы социальной и бытовой дисфункции из-за болевого синдрома MIDAS. Все пациенты регулярно заполняли дневник головной боли, оформленный в виде таблицы, аналогичной форме Дневника головной боли Российского общества изучения головной боли, рассчитанной на 90 дней заполнения. Психоэмоциональное состояние исследуемых оценивалось путем применения Госпитальной шкалы тревоги и депрессии (HADS).
Наличие клинических проявлений ЦС и их интенсивности оценивалось при помощи Шкалы оценки центральной сенситизации (CSI) в адаптированной версии под редакцией О.Р. Есина. Пациентам были проведены инструментальные обследования, результаты которых были отображены в анкете:
• магнитно-резонанасная томография (МРТ) головного мозга – для оценки морфологических характеристик головного мозга, а также с целью исключения новообразований и жизнеугрожающих состояний, приводящих к формированию вторичной головной боли у пациентов;
• МРТ шейного отдела позвоночника – с целью оценки дегенеративно-дистрофических изменений шейного отдела позвоночника и его особенностей.
МРТ пациентам была выполнена на томографе Siemens Avanto 1,5T в режимах Т1, Т2, FLAIR и DWI.
Интенсивность вегетативных проявлений, сопутствующих приступу мигрени – в связи с отсутствием верифицированной шкалы оценки вегетативных реакций для пациентов в приступе мигрени для числового анализа в данном исследовании была принята градация:
• 0 баллов – отсутствие тошноты, рвоты;
• 1 балл – легкая тошнота, не усугубляющая тяжесть приступа мигрени, и отсутствие рвоты, отсутствие необходимости приема противорвотных препаратов;
• 2 балла – наличие умеренной тошноты, влияющей на тяжесть приступа или/и однократная рвота, наличие необходимости приема противорвотных препаратов;
• 3 балла – выраженная тошнота, значительно влияющая на страдание во время приступа мигрени и неоднократная рвота, наличие необходимости приема противорвотных препаратов.
Указанные баллы пациент присваивал каждому приступу в дневнике головной боли, среднее арифметическое этих баллов до лечения и после лечения были приняты к анализу.
Распределение пациентов в группах было следующим:
1) с сочетанием мигрени и ЦГБ: мужчин – 10 (16,7 %), женщин – 50 (83,3 %);
2) с сочетанием мигрени и цервикалгии: мужчин – 11 (18,3 %), женщин 49 – (81,7 %);
3) с мигренью без жалоб на боль и ограничение объема движений в шейном отделе позвоночника: мужчин – 16 (26 %), женщин – 44 (74%).
Средний возраст пациентов:
• с сочетанием мигрени и ЦГБ составил 44,4 года [33; 55] – группа 1 является наиболее гомогенная в возрастных характеристиках пациентов;
• сочетанием мигрени и цервикалгии 41,2 года [22; 54] – группа 2;
• мигренью без жалоб на боль и ограничение объема движений в шейном отделе позвоночника: 35 лет [18; 53] – группа 3.
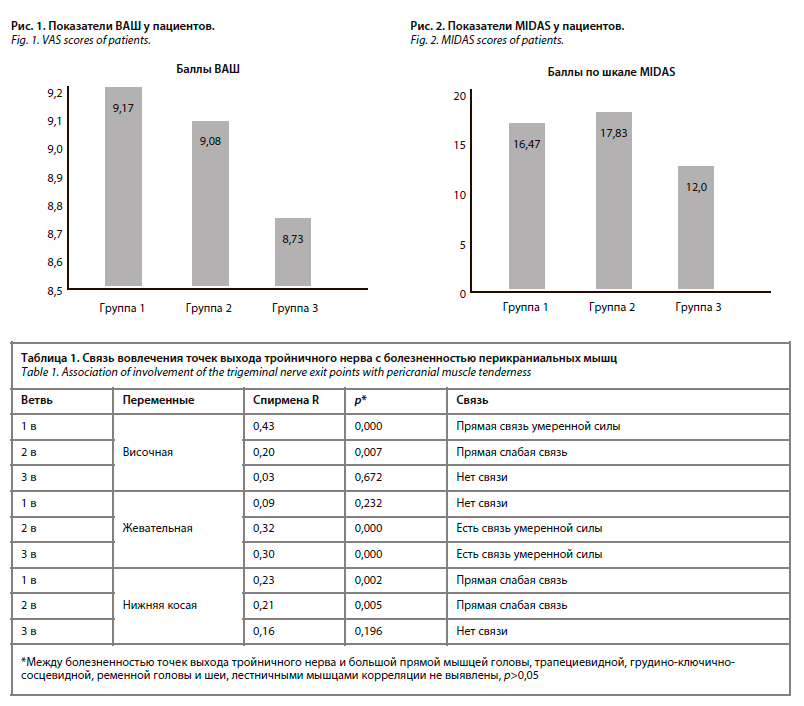
Исходные показатели шкалы MIDAS в трех группах достоверно не различались (критерий Краскела–Уоллиса р=0,6326, >0,05). Баллы 1-й группы: 16,4±1,98, 2-й группы: 15,82±2,27, 3-й группы: 15,33±1,8 (рис. 2).
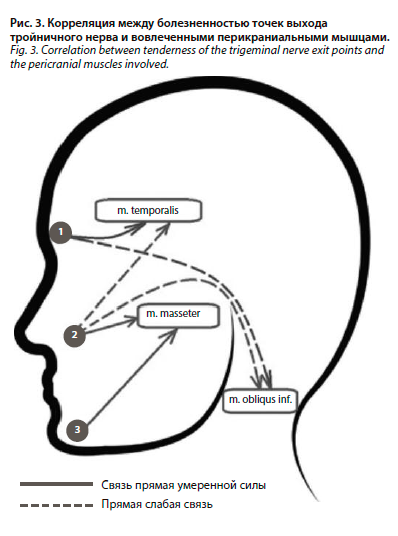 Пальпация точек выхода тройничного нерва является неотъемлемой частью неврологического осмотра, их болезненность часто встречается у пациентов с лицевыми и головными болями. В рамках данного исследования был проведен анализ частоты вовлечения 1, 2, 3 точек выхода у всех 180 пациентов (выявляемость болезненности точки выхода 1-й ветви тройничного нерва равна 77%, 2-й – 58%, 3-й – 22%) и исследована связь данного вовлечения с болезненностью перикраниальных мышц (табл. 1).
Пальпация точек выхода тройничного нерва является неотъемлемой частью неврологического осмотра, их болезненность часто встречается у пациентов с лицевыми и головными болями. В рамках данного исследования был проведен анализ частоты вовлечения 1, 2, 3 точек выхода у всех 180 пациентов (выявляемость болезненности точки выхода 1-й ветви тройничного нерва равна 77%, 2-й – 58%, 3-й – 22%) и исследована связь данного вовлечения с болезненностью перикраниальных мышц (табл. 1).
В результате чего была выявлена прямая связь умеренной силы между болезненностью точки выхода 1-й тригеминальной ветви и височной мышцы, а также слабая прямая связь со 2-й, при этом 1-ая точка выхода наиболее часто была болезненной при пальпации у всех пациентов.
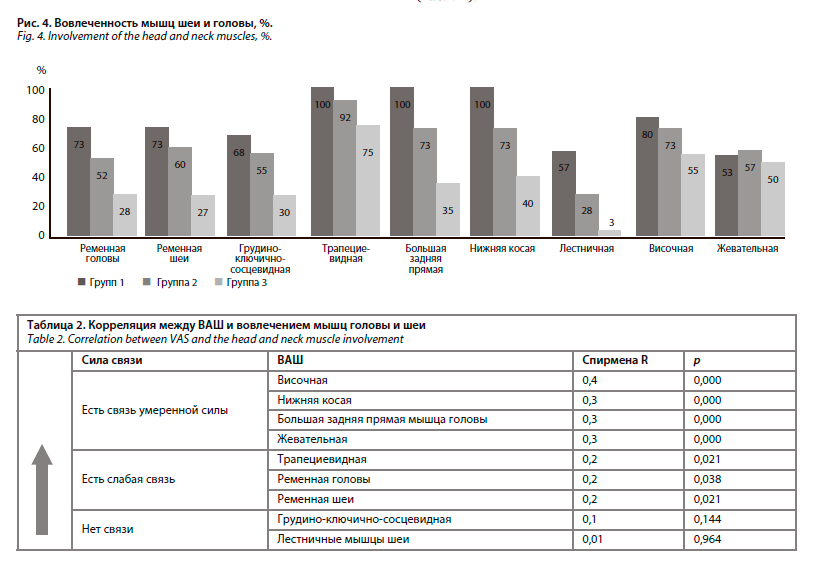
Наиболее интересной находкой является обнаружение связи умеренной силы между болезненностью 1-й и 2-й точек выхода тройничного нерва и жевательной мышцей. Таким образом, триггерные точки в жевательной мышце соответствовали болезненности сразу обеих – 1-й и 2-й точек выхода, такое же сочетание находилось в слабой прямой связи лишь с одной мышцей со стороны цервикокраниальной области – нижней косой мышцы головы (рис. 3).
Данный факт можно рассмотреть в качестве практической рекомендации: при выявлении болезненности при пальпации 1-й и 2-й точек выхода тройничного нерва стоит уделить внимание исследованию болезненности как височной, жевательной мышц, так и группы коротких разгибателей затылка.
У пациентов 1-й группы с мигренью и ЦГБ при сравнении с пациентами 2-й и 3-й групп достоверно чаще выявлялась болезненность при пальпации трапециевидной, задней прямой, нижней косой, лестничных мышц.
Основополагающим фактором включения пациентов в группу 3 было наличие мигрени в сочетании с отсутствием жалоб на боль в шее и значимых дегенеративно-дистрофических изменений шейного отдела позвоночника, однако при пальпации мышц головы и шеи у данных исследуемых болезненность некоторых зон все же была выявлена.
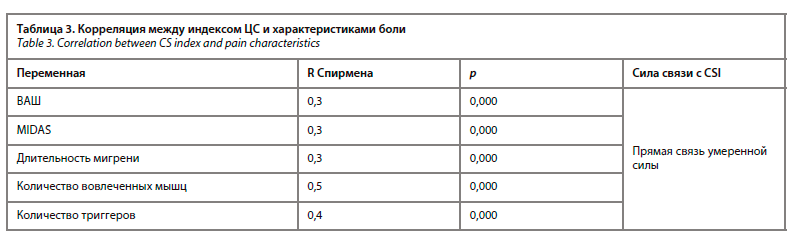
В отличие от первых двух групп у пациентов группы 3 реже отмечалась болезненность трапециевидной и грудино-ключично-сосцевидной мышц, но частота выявления триггеров в височной и жевательной мышцах была сопоставимо высокой (критерий Краскела–Уоллиса для височной мышцы: р=0,368, >0,05; критерий Краскела–Уоллиса для жевательной мышцы: р=0,632, >0,05); рис. 4. Данное наблюдение показывает определенную специфичность m. temporalis по отношению к мигренозной головной боли, что было замечено некоторыми исследователями ранее. Также были определены мышцы, достоверно чаще детерминирующие ЦГБ от цервикалгии – нижняя косая, задняя прямая мышцы головы, данные локации активных триггеров были выявлены у 100% пациентов 1-й группы, тогда как во 2-й группе – у 73% (для обеих мышц), в 3-й группе – у 40% и 35% соответственно, р>0,05.
Обратила на себя внимание обнаруженная связь умеренной силы между ВАШ и некоторыми мышцами перикраниальной области, а именно: в височной, нижней косой, большой задней прямой, жевательной мышцах (табл. 2).
Стоит отметить соответствие интенсивности ЦС у пациентов с эпизодической мигренью и ЦГБ аналогичным результатам у пациентов с хронической мигренью [7].
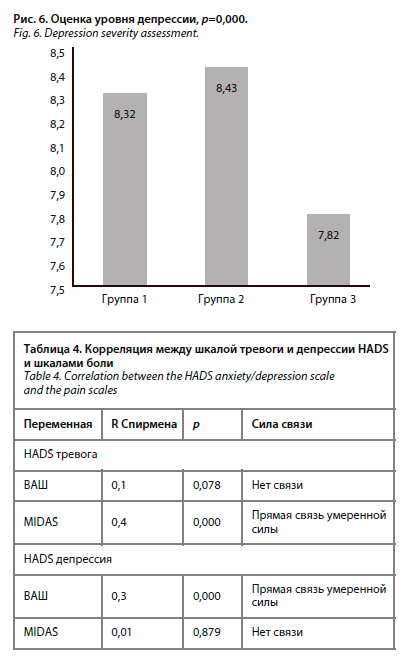 Клинически важными аспектами ЦС являются тревожно-депрессивные расстройства. Средний балл среди всех пациентов по HADS: тревога = 9,172, стандартное отклонение 2,197; HADS депрессия = 8,189, стандартное отклонение 2,353. При расчете значений и распределении их по группам было выявлено статистически значимое различие показателей 1-й и 2-й групп, относительно группы 3 ( р<0,05); рис. 5, 6.
Клинически важными аспектами ЦС являются тревожно-депрессивные расстройства. Средний балл среди всех пациентов по HADS: тревога = 9,172, стандартное отклонение 2,197; HADS депрессия = 8,189, стандартное отклонение 2,353. При расчете значений и распределении их по группам было выявлено статистически значимое различие показателей 1-й и 2-й групп, относительно группы 3 ( р<0,05); рис. 5, 6.
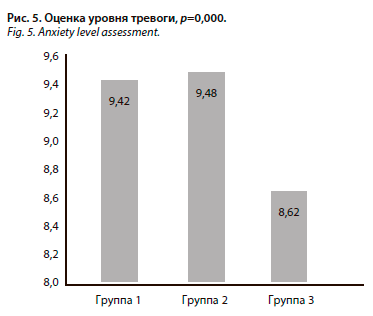
Интересным наблюдением явилась прямая связь умеренной силы между показателями тревоги HADS и баллами по MIDAS, а также между показателями депрессии по HADS и баллами ВАШ (табл. 4).
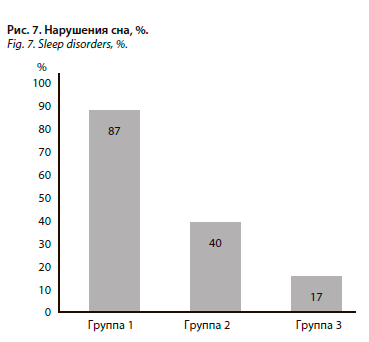
При анализе данных также было отмечено статистически значимое преобладание жалоб нарушения сна у пациентов 1-й группы, р<0,00001 (рис. 7).
Влияние МАТ-терапии на течение цервикалгического миофасциального болевого синдрома у пациентов с хронической мигренью
После анализа данных возник вопрос – является ли цервикалгия проявлением ЦС и может ли она быть купирована лишь терапией ЦС.
В качестве дополнения к исследованию были отобраны 10 пациентов с диагнозом «хроническая мигрень» и «миофасциальный цервикалгический болевой синдром», соответствовавших критериям включения, они были разделены на две дополнительных группы. Данным пациентам была назначена терапия мигрени специфическими моноклональными антителами (МАТ) Фреманезумаб, подкожно 1 раз в месяц в дозировке 225 мг, никаких препаратов данные пациенты более не принимали:
• 1-ая дополнительная группа (5 пациентов) дополнили лечение физическими упражнениями, окципитальным релизом и постизометрической релаксацией;
• 2-ая дополнительная группа (5 пациентов) отказались от выполнения каких-либо физических упражнений.
Анализ клинических проявлений цервикалгии проводился до введения первой инъекции Фреманезумаба и через 6 мес после начала терапии.
В качестве исследуемых мышц были выбраны трапециевидная, жевательная, височная и нижняя косая, с учетом ранее предоставленных данных о более частом вовлечении у пациентов с мигренью. Интенсивность болезненности при пальпации оценивалась по шкале ВАШ (0–10 баллов).
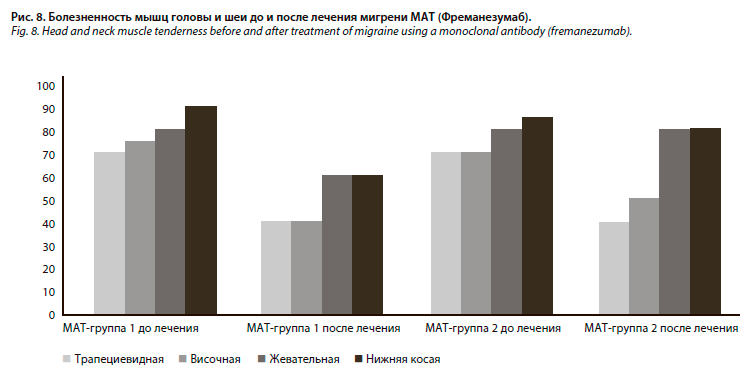
В результате исследования было обнаружено достоверное снижение болезненности трапециевидной и височной мышц в обеих группах, вне зависимости от выполнения физических упражнений, в отличие от жевательной и нижней косой мышц – в данном случае показатели достоверно снизились лишь при сочетании МАТ-терапии и физических упражнений.
2. Миофасциальный болевой синдром с вовлечением трапециевидной и височной мышц может самостоятельно разрешиться при специфической терапии мигрени моноклональными антителами, однако для купирования напряжения и болезненности в жевательной и нижней косой мышцах более эффективным является дополнение в виде лечебной гимнастики и мягких мануальных техник.
3. С учетом выявленных прямых связей умеренной силы между числом болезненных точек выхода тройничного нерва, вовлеченными мышцами перикраниальной области, а также эффектом от терапии приступов мигрени моноклональными антителами, можно сделать вывод о более выраженной ЦС при вовлечении жевательной и нижней косой мышц.
4. При осмотре пациентов с мигренью и активным цервикалгическим фактором либо при его отсутствии необходимо проводить тщательный осмотр мышц лицевой и краниовертебральной области, даже при отсутствии жалоб пациента на боль в лице или шее, а также назначать специфичную лечебную гимнастику для повышения эффективности лечения.
5. У всех пациентов с мигренью, вне зависимости от хронизации, необходимо проводить оценку интенсивности ЦС для своевременного и более полного оказания лечебной помощи.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Хайрутдинова Ольга Сергеевна – ассистент каф. реабилитации и спортивной медицины, ФГБОУ ВО «Казанский ГМУ».
E-mail: khayros.kzn@gmail.com; ORCID: 0000-0003-0442-4954
Olga S. Khairutdinova – Аssistant, Kazan State Medical University. E-mail: khayros.kzn@gmail.com;
ORCID: 0000-0003-0442-4954
Богданов Энвер Ибрагимович – д-р мед. наук, проф., зав. каф. неврологии, ФГБОУ ВО «Казанский ГМУ».
E-mail: enver_bogdanov@mail.com; ORCID: 0000-0001-9332-8053
Enver I. Bogdanov – Dr. Sci. (Med.), Prof., Kazan State Medical University. E-mail: enver_bogdanov@mail.com; ORCID: 0000-0001-9332-8053
Поступила в редакцию: 15.05.2024
Поступила после рецензирования: 22.05.2024
Принята к публикации: 23.05.2024
Received: 15.05.2024
Revised: 22.05.2024
Accepted: 23.05.2024
Клинический разбор в общей медицине №5 2024
Цервикалгия у пациентов с мигренью – коморбидная нозология или клинический аспект центральной сенситизации?
Номера страниц в выпуске:13-20
Аннотация
Актуальность. Феномен центральной сенситизации возникает, когда физиологическая активность в ноцицептивных путях усиливается и приводит к аномальной чувствительности; она определяется как «повышенная чувствительность ноцицептивных нейронов центральной нервной системы к их нормальному или подпороговому афферентному импульсу», согласно определению, представленному Международной ассоциацией изучения боли (IASP). Возбудимость нейронов спинного мозга существенно модифицирует усиление соматосенсорной системы. Хронические болевые синдромы, тревожно-депрессивное расстройство, нарушения сна в настоящее время встречаются в популяции очень часто, значительно снижая качество жизни населения, в патогенезе данных нозологий лежит центральная сенситизация.
Цель. Изучить клинические проявления центральной сенситизации у пациентов с эпизодической мигренью при сочетании с болью в шее или цервикогенной головной болью.
Материалы и методы. В продольное проспективное исследование включены 180 пациентов, разделенные на 3 группы: 1) пациенты с сочетанием мигрени и цервикогенной головной боли – 60 человек (исследуемая группа); 2) пациенты с сочетанием диагнозов мигрень и цервикалгия – 60 человек (контрольная группа); 3) пациенты с диагнозом мигрень без жалоб на боль и ограничение движений в шейном отделе позвоночника – 60 человек (дополнительная группа).
Результаты. У пациентов с мигренью и коморбидной цервикогенной головной болью выявлена более выраженная центральная сенситизация при сравнении с коморбидной цервикалгией. Миофасциальный болевой синдром с вовлечением трапециевидной и височной мышц может самостоятельно разрешиться при специфической терапии мигрени моноклональными антителами, однако для купирования напряжения и болезненности в жевательной и нижней косой мышцах более эффективным является дополнение в виде лечебной гимнастики и мягких мануальных техник. С учетом выявленных прямых связей умеренной силы между числом болезненных точек выхода тройничного нерва, вовлеченными мышцами перикраниальной области, а также эффектом от терапии приступов мигрени моноклональными антителами, можно сделать вывод о более выраженной центральной сенситизации при вовлечении жевательной и нижней косой мышц.
Выводы. При осмотре пациентов с мигренью и активным цервикалгическим фактором либо при его отсутствии необходимо проводить тщательный осмотр мышц лицевой и краниовертебральной области, даже при отсутствии жалоб пациента на боль в лице или шее, а также назначать специфичную лечебную гимнастику для повышения эффективности лечения. У всех пациентов с мигренью, вне зависимости от хронизации, необходимо проводить оценку интенсивности центральной сенситизации для своевременного и более полного оказания лечебной помощи.
Ключевые слова: центральная сенситизация, цервикогенная головная боль, мигрень, цервикалгия, моноклональные антитела, лечебная гимнастика при мигрени.
Для цитирования: Хайрутдинова О.С., Богданов Э.И. Цервикалгия у пациентов с мигренью – коморбидная нозология или клинический аспект центральной сенситизации? Клинический разбор в общей медицине. 2024; 5 (5): 13–20. DOI: 10.47407/kr2024.5.5.00399
Актуальность. Феномен центральной сенситизации возникает, когда физиологическая активность в ноцицептивных путях усиливается и приводит к аномальной чувствительности; она определяется как «повышенная чувствительность ноцицептивных нейронов центральной нервной системы к их нормальному или подпороговому афферентному импульсу», согласно определению, представленному Международной ассоциацией изучения боли (IASP). Возбудимость нейронов спинного мозга существенно модифицирует усиление соматосенсорной системы. Хронические болевые синдромы, тревожно-депрессивное расстройство, нарушения сна в настоящее время встречаются в популяции очень часто, значительно снижая качество жизни населения, в патогенезе данных нозологий лежит центральная сенситизация.
Цель. Изучить клинические проявления центральной сенситизации у пациентов с эпизодической мигренью при сочетании с болью в шее или цервикогенной головной болью.
Материалы и методы. В продольное проспективное исследование включены 180 пациентов, разделенные на 3 группы: 1) пациенты с сочетанием мигрени и цервикогенной головной боли – 60 человек (исследуемая группа); 2) пациенты с сочетанием диагнозов мигрень и цервикалгия – 60 человек (контрольная группа); 3) пациенты с диагнозом мигрень без жалоб на боль и ограничение движений в шейном отделе позвоночника – 60 человек (дополнительная группа).
Результаты. У пациентов с мигренью и коморбидной цервикогенной головной болью выявлена более выраженная центральная сенситизация при сравнении с коморбидной цервикалгией. Миофасциальный болевой синдром с вовлечением трапециевидной и височной мышц может самостоятельно разрешиться при специфической терапии мигрени моноклональными антителами, однако для купирования напряжения и болезненности в жевательной и нижней косой мышцах более эффективным является дополнение в виде лечебной гимнастики и мягких мануальных техник. С учетом выявленных прямых связей умеренной силы между числом болезненных точек выхода тройничного нерва, вовлеченными мышцами перикраниальной области, а также эффектом от терапии приступов мигрени моноклональными антителами, можно сделать вывод о более выраженной центральной сенситизации при вовлечении жевательной и нижней косой мышц.
Выводы. При осмотре пациентов с мигренью и активным цервикалгическим фактором либо при его отсутствии необходимо проводить тщательный осмотр мышц лицевой и краниовертебральной области, даже при отсутствии жалоб пациента на боль в лице или шее, а также назначать специфичную лечебную гимнастику для повышения эффективности лечения. У всех пациентов с мигренью, вне зависимости от хронизации, необходимо проводить оценку интенсивности центральной сенситизации для своевременного и более полного оказания лечебной помощи.
Ключевые слова: центральная сенситизация, цервикогенная головная боль, мигрень, цервикалгия, моноклональные антитела, лечебная гимнастика при мигрени.
Для цитирования: Хайрутдинова О.С., Богданов Э.И. Цервикалгия у пациентов с мигренью – коморбидная нозология или клинический аспект центральной сенситизации? Клинический разбор в общей медицине. 2024; 5 (5): 13–20. DOI: 10.47407/kr2024.5.5.00399
Cervicalgia in patients with migraine – a comorbid nosology or a clinical aspect of central sensitization?
Olga S. Khairutdinova, Enver I. BogdanovKazan State Medical University, Kazan, Russia
khayros.kzn@gmail.com
Abstract
Relevance. The phenomenon of central sensitization occurs when physiological activity in nociceptive pathways increases and leads to abnormal sensitivity; it is defined as “increased sensitivity of nociceptive neurons of the central nervous system to their normal or subthreshold afferent input,” according to the definition provided by the International Association for the Study of Pain (IASP). The excitability of spinal cord neurons significantly modifies the gain of the somatosensory system. Chronic pain syndromes, anxiety-depressive disorder, sleep disorders are currently very common in the population, significantly reducing the quality of life of the population; the pathogenesis of these nosologies lies in central sensitization.
Objective. To study the clinical manifestations of central sensitization in patients with episodic migraine associated with neck pain or cervicogenic headache.
Materials and methods. The longitudinal prospective study included 180 patients, divided into 3 groups: 1) patients with a combination of migraine and cervicogenic headache – 60 people (study group); 2) patients with a combination of migraine and cervicalgia diagnoses – 60 people (control group); 3) patients diagnosed with migraine without complaints of pain and limitation of movements in the cervical spine – 60 people (additional group).
Results. In patients with migraine and comorbid cervical headache, more pronounced central sensitization was revealed when compared with comorbid cervicalgia. Myofascial pain syndrome involving the trapezius and temporal muscles can resolve on its own with specific migraine therapy with monoclonal antibodies, however, to relieve tension and soreness in the masseter and inferior oblique muscles, the addition of therapeutic exercises and gentle manual techniques is more effective. Taking into account the identified direct relationships of moderate strength between the number of painful points of exit of the trigeminal nerve, the muscles of the pericranial region involved, as well as the effect of treatment of migraine attacks with monoclonal antibodies, it can be concluded that central sensitization is more pronounced when the masseter and inferior oblique muscles are involved.
Conclusions. During examination of patients with migraine with comorbid active cervicalgic factor or even if it is absence, it is necessary to make a thorough examination of the facial and cranioverebral region muscles, even in the absence of patient complaints of pain in the face or neck, and also prescribe specific therapeutic exercises to increase the effectiveness of treatment. In all patients with migraine, regardless of chronicity, it is necessary to assess the intensity of central sensitization for timely and more complete provision of medical care.
Keywords: central sensitization, cervicogenic headache, migraine, cervicalgia, monoclonal antibodies, physical exercises for migraine.
For citation: Khairutdinova O.S., Bogdanov E.I. Cervicalgia in patients with migraine – a comorbid nosology or a clinical aspect of central sensitization? Clinical review for general practice. 2024; 5 (5): 13–20. (In Russ.). DOI: 10.47407/kr2024.5.5.00399
Центральная сенситизация (ЦС) – это патофизиологический феномен формирования усиленного, гипертрофированного ответа структур центральной нервной системы на сенсорные и периферические ноцицептивные стимулы, характеризующийся гипервозбудимостью нейронов дорсальных рогов спинного мозга, восходящих по спиноталамическому тракту [1–3]. ЦС характеризуется тем, что после прекращения действия периферических болевых стимулов остается определенный уровень возбуждения в центральных сенсорных нейронах заднего рога, и это состояние сохраняется автономно или поддерживается слабой ноцицептивной стимуляцией. Сенситизация ноцицепторов возникает вследствие действия алгогенов, поступающих из плазмы крови и выделяющихся из поврежденной ткани, а также из периферических терминалей С-ноцицепторов. Эктопической спонтанной активностью можно объяснить боли в зонах гипестезии, когда волокна большого диаметра повреждены, а боль воспринимается через импульсы, генерируемые в ноцицепторных С-волокнах меньшего диаметра [4].
Кроме того, ЦС включает механизмы, воздействующие на пороги возбудимости болевых и А-бета механорецепторов, таким образом, неболевые стимулы воспринимаются как боль. Так, формируются аллодиния, гипералгезия и следовые реакции. При этом происходят усиленное выделение глутамата и активация N-метил-d-аспартат (NMDA)-рецепторов, дисбаланс и угнетение тормозящих ГАМК-эргических систем.
В научной литературе показано, что ЦС играет роль в патогенезе фибромиалгии, мигрени, головной боли напряжения, синдроме раздраженного кишечника и синдроме беспокойных ног, также данный феномен может лежать в основе процесса хронизации болевых синдромов.
Важнейшим аспектом формирования ЦС является коморбидность психоэмоциональных нарушений, тревожно-депрессивных расстройств у пациентов с болевыми синдромами. Депрессивные расстройства наблюдаются более чем у 1/2 пациентов с хронической болью. Многие авторы приходят к заключению о комплексной модели депрессии и хронической боли. Преимущественная роль отводится недостаточности нисходящих противоболевых систем, дефициту норадреналина и серотонина в синаптической щели, что приводит к увеличению количества и сенсибилизации рецепторов постсинаптической мембраны [5].
Кроме того, хронический стресс и боль индуцируют активность гипоталамо-гипофизарно-надпочечниковой и тиреоидной систем, вследствие чего снижается синтез мозгового нейротрофического фактора (BDNF), нарушается метаболизм фосфолипидов, субстанции Р и других нейрокининов. Также изменяется чувствительность NMDA-рецепторов, усиливается цитотоксическое действие глутамата, нарушается кальциевый гомеостаз, повышается выработка свободных радикалов. Психологический компонент с точки зрения эмоционального стресса следует учитывать в процессе диагностики, чтобы лучше справляться с хроническими болевыми состояниями [6]. Тревога и депрессия могут способствовать развитию, сохранению и
обострению боли.
Другим дисфункциональным компонентом является вызванный болевым раздражением спинальный сенсомоторный рефлекс в соответствующем сегменте спинного мозга, сопровождающийся активацией мотонейронов, что, в свою очередь, приводит к спазму мышц, иннервируемых этими нейронами, мышечный спазм приводит к усилению стимуляции болевых рецепторов мышцы. Предположительно в сформированных триггерных точках содержатся множественные локусы сенситизации, состоящие из одного или нескольких сенситизированных нервных окончаний.
ЦС у пациентов с цервикогенной головной болью (ЦГБ) – основа формирования и поддержания персистирующей головной боли при повреждениях в области шеи. В сравнительном нейрофизиологическом исследовании, включавшем пациентов с ЦГБ и пациентов с дисфункцией в области шеи, но без ЦГБ, у первых обнаружен феномен ЦС. Цервикалгия при этом является одним из наиболее часто представленных сопутствующих болевых синдромов у пациентов с мигренью. По данным различных исследований (Lampl и соавт., Н.В. Латышева) ее распространенность у пациентов с мигренью составляет до 58–71% [7].
Данный аспект является основополагающим в формировании цели нашего исследования: изучить клинические аспекты ЦС у пациентов с мигренью, коморбидной цервикалгией и ЦГБ.
Материалы и методы
В продольное проспективное исследование были включены 180 пациентов, разделенные на 3 группы:1) пациенты с сочетанием мигрени и ЦГБ – 60 человек (исследуемая группа);
2) пациенты с сочетанием диагнозов мигрень и цервикалгия – 60 человек (контрольная группа);
3) пациенты с диагнозом мигрень без жалоб на боль и ограничение движений в шейном отделе позвоночника – 60 человек (дополнительная группа).
Всем пациентам проведен тщательный сбор анамнеза, неврологический осмотр, верификация ранее установленных диагнозов «эпизодическая мигрень с аурой», «эпизодическая мигрень без ауры», в соответствии с критериями Международной классификации головной боли 3-го пересмотра Международного общества головной боли.
В связи с неоднозначностью критериев диагностики ЦГБ выставлялась пациентам при полном соответствии Международной классификации головной боли 3-го пересмотра Международного общества головной боли, диагностическим критериям O. Sjaastad [8] и определению N. Bogduk, а также при полном купировании головной боли после выполнения новокаиновой блокады латеральных атлантоаксиальных суставов, дугоотросчатых суставов С2-С3, С3-С4, медиальных ветвей С3 и С4 [9].
Интенсивность болевого синдрома оценивалась путем применения трехступенчатой шкалы оценки боли Всемирной организации здравоохранения и шкалы социальной и бытовой дисфункции из-за болевого синдрома MIDAS. Все пациенты регулярно заполняли дневник головной боли, оформленный в виде таблицы, аналогичной форме Дневника головной боли Российского общества изучения головной боли, рассчитанной на 90 дней заполнения. Психоэмоциональное состояние исследуемых оценивалось путем применения Госпитальной шкалы тревоги и депрессии (HADS).
Наличие клинических проявлений ЦС и их интенсивности оценивалось при помощи Шкалы оценки центральной сенситизации (CSI) в адаптированной версии под редакцией О.Р. Есина. Пациентам были проведены инструментальные обследования, результаты которых были отображены в анкете:
• магнитно-резонанасная томография (МРТ) головного мозга – для оценки морфологических характеристик головного мозга, а также с целью исключения новообразований и жизнеугрожающих состояний, приводящих к формированию вторичной головной боли у пациентов;
• МРТ шейного отдела позвоночника – с целью оценки дегенеративно-дистрофических изменений шейного отдела позвоночника и его особенностей.
МРТ пациентам была выполнена на томографе Siemens Avanto 1,5T в режимах Т1, Т2, FLAIR и DWI.
Интенсивность вегетативных проявлений, сопутствующих приступу мигрени – в связи с отсутствием верифицированной шкалы оценки вегетативных реакций для пациентов в приступе мигрени для числового анализа в данном исследовании была принята градация:
• 0 баллов – отсутствие тошноты, рвоты;
• 1 балл – легкая тошнота, не усугубляющая тяжесть приступа мигрени, и отсутствие рвоты, отсутствие необходимости приема противорвотных препаратов;
• 2 балла – наличие умеренной тошноты, влияющей на тяжесть приступа или/и однократная рвота, наличие необходимости приема противорвотных препаратов;
• 3 балла – выраженная тошнота, значительно влияющая на страдание во время приступа мигрени и неоднократная рвота, наличие необходимости приема противорвотных препаратов.
Указанные баллы пациент присваивал каждому приступу в дневнике головной боли, среднее арифметическое этих баллов до лечения и после лечения были приняты к анализу.
Результаты
При анализе гендерного распределения среди обследованных было выявлено преобладание женщин над мужчинами, что соответствует межнациональным эпидемиологическим данным.Распределение пациентов в группах было следующим:
1) с сочетанием мигрени и ЦГБ: мужчин – 10 (16,7 %), женщин – 50 (83,3 %);
2) с сочетанием мигрени и цервикалгии: мужчин – 11 (18,3 %), женщин 49 – (81,7 %);
3) с мигренью без жалоб на боль и ограничение объема движений в шейном отделе позвоночника: мужчин – 16 (26 %), женщин – 44 (74%).
Средний возраст пациентов:
• с сочетанием мигрени и ЦГБ составил 44,4 года [33; 55] – группа 1 является наиболее гомогенная в возрастных характеристиках пациентов;
• сочетанием мигрени и цервикалгии 41,2 года [22; 54] – группа 2;
• мигренью без жалоб на боль и ограничение объема движений в шейном отделе позвоночника: 35 лет [18; 53] – группа 3.
Анализ характеристик болевого синдрома у пациентов
Исходные баллы визуально-аналоговой шкалы (ВАШ) в трех группах: средний балл имели пациенты 1-й группы (М±δ) – 9,17±0,65; минимальный – у пациентов 3-й группы – 8,73±0,64. Достоверных различий среди показателей трех групп не выявлено (критерий Краскела–Уоллиса р=0,05937, >0,05); рис 1. Средний балл по ВАШ пациентов с мигренью и цервикалгией (группа 2) равен 9,08±0,68.Исходные показатели шкалы MIDAS в трех группах достоверно не различались (критерий Краскела–Уоллиса р=0,6326, >0,05). Баллы 1-й группы: 16,4±1,98, 2-й группы: 15,82±2,27, 3-й группы: 15,33±1,8 (рис. 2).

Болезненность при пальпации ветвей тройничного нерва
 Пальпация точек выхода тройничного нерва является неотъемлемой частью неврологического осмотра, их болезненность часто встречается у пациентов с лицевыми и головными болями. В рамках данного исследования был проведен анализ частоты вовлечения 1, 2, 3 точек выхода у всех 180 пациентов (выявляемость болезненности точки выхода 1-й ветви тройничного нерва равна 77%, 2-й – 58%, 3-й – 22%) и исследована связь данного вовлечения с болезненностью перикраниальных мышц (табл. 1).
Пальпация точек выхода тройничного нерва является неотъемлемой частью неврологического осмотра, их болезненность часто встречается у пациентов с лицевыми и головными болями. В рамках данного исследования был проведен анализ частоты вовлечения 1, 2, 3 точек выхода у всех 180 пациентов (выявляемость болезненности точки выхода 1-й ветви тройничного нерва равна 77%, 2-й – 58%, 3-й – 22%) и исследована связь данного вовлечения с болезненностью перикраниальных мышц (табл. 1).В результате чего была выявлена прямая связь умеренной силы между болезненностью точки выхода 1-й тригеминальной ветви и височной мышцы, а также слабая прямая связь со 2-й, при этом 1-ая точка выхода наиболее часто была болезненной при пальпации у всех пациентов.
Наиболее интересной находкой является обнаружение связи умеренной силы между болезненностью 1-й и 2-й точек выхода тройничного нерва и жевательной мышцей. Таким образом, триггерные точки в жевательной мышце соответствовали болезненности сразу обеих – 1-й и 2-й точек выхода, такое же сочетание находилось в слабой прямой связи лишь с одной мышцей со стороны цервикокраниальной области – нижней косой мышцы головы (рис. 3).
Данный факт можно рассмотреть в качестве практической рекомендации: при выявлении болезненности при пальпации 1-й и 2-й точек выхода тройничного нерва стоит уделить внимание исследованию болезненности как височной, жевательной мышц, так и группы коротких разгибателей затылка.
Вовлеченность мышц головы и шеи
Во время первичного осмотра у всех пациентов были исследованы на предмет болезненности доступные пальпации мышцы головы и шеи.У пациентов 1-й группы с мигренью и ЦГБ при сравнении с пациентами 2-й и 3-й групп достоверно чаще выявлялась болезненность при пальпации трапециевидной, задней прямой, нижней косой, лестничных мышц.
Основополагающим фактором включения пациентов в группу 3 было наличие мигрени в сочетании с отсутствием жалоб на боль в шее и значимых дегенеративно-дистрофических изменений шейного отдела позвоночника, однако при пальпации мышц головы и шеи у данных исследуемых болезненность некоторых зон все же была выявлена.
В отличие от первых двух групп у пациентов группы 3 реже отмечалась болезненность трапециевидной и грудино-ключично-сосцевидной мышц, но частота выявления триггеров в височной и жевательной мышцах была сопоставимо высокой (критерий Краскела–Уоллиса для височной мышцы: р=0,368, >0,05; критерий Краскела–Уоллиса для жевательной мышцы: р=0,632, >0,05); рис. 4. Данное наблюдение показывает определенную специфичность m. temporalis по отношению к мигренозной головной боли, что было замечено некоторыми исследователями ранее. Также были определены мышцы, достоверно чаще детерминирующие ЦГБ от цервикалгии – нижняя косая, задняя прямая мышцы головы, данные локации активных триггеров были выявлены у 100% пациентов 1-й группы, тогда как во 2-й группе – у 73% (для обеих мышц), в 3-й группе – у 40% и 35% соответственно, р>0,05.

Обратила на себя внимание обнаруженная связь умеренной силы между ВАШ и некоторыми мышцами перикраниальной области, а именно: в височной, нижней косой, большой задней прямой, жевательной мышцах (табл. 2).
Центральная сенситизация у пациентов с мигренью при сочетании с цервикогенной головной болью или/и цервикалгией
При оценке результатов опроса по шкале CSI у пациентов 3-й группы выявлена субклиническая ЦС (29 баллов). У всех остальных пациентов наблюдался клинически выраженный феномен ЦС: у пациентов 1-й группы средний балл составляет 44,7, 2-й группы – 41,23, что соответствует умеренной степени ЦС (критерий Краскела–Уоллиса: р<0,00001, разница статистически значима). Таким образом, у 66,7% пациентов продемонстрирована умеренная степень выраженности феномена ЦС (среднее значение индекса CSI=38,317, стандартное отклонение = 8,43), а количество вовлеченных мышц прямо коррелировало с интенсивностью феномена ЦС (табл. 3).
Стоит отметить соответствие интенсивности ЦС у пациентов с эпизодической мигренью и ЦГБ аналогичным результатам у пациентов с хронической мигренью [7].
Оценка тревожно-депрессивного компонента и расстройств сна
 Клинически важными аспектами ЦС являются тревожно-депрессивные расстройства. Средний балл среди всех пациентов по HADS: тревога = 9,172, стандартное отклонение 2,197; HADS депрессия = 8,189, стандартное отклонение 2,353. При расчете значений и распределении их по группам было выявлено статистически значимое различие показателей 1-й и 2-й групп, относительно группы 3 ( р<0,05); рис. 5, 6.
Клинически важными аспектами ЦС являются тревожно-депрессивные расстройства. Средний балл среди всех пациентов по HADS: тревога = 9,172, стандартное отклонение 2,197; HADS депрессия = 8,189, стандартное отклонение 2,353. При расчете значений и распределении их по группам было выявлено статистически значимое различие показателей 1-й и 2-й групп, относительно группы 3 ( р<0,05); рис. 5, 6. 
Интересным наблюдением явилась прямая связь умеренной силы между показателями тревоги HADS и баллами по MIDAS, а также между показателями депрессии по HADS и баллами ВАШ (табл. 4).
При анализе данных также было отмечено статистически значимое преобладание жалоб нарушения сна у пациентов 1-й группы, р<0,00001 (рис. 7).

Влияние МАТ-терапии на течение цервикалгического миофасциального болевого синдрома у пациентов с хронической мигренью
После анализа данных возник вопрос – является ли цервикалгия проявлением ЦС и может ли она быть купирована лишь терапией ЦС.
В качестве дополнения к исследованию были отобраны 10 пациентов с диагнозом «хроническая мигрень» и «миофасциальный цервикалгический болевой синдром», соответствовавших критериям включения, они были разделены на две дополнительных группы. Данным пациентам была назначена терапия мигрени специфическими моноклональными антителами (МАТ) Фреманезумаб, подкожно 1 раз в месяц в дозировке 225 мг, никаких препаратов данные пациенты более не принимали:
• 1-ая дополнительная группа (5 пациентов) дополнили лечение физическими упражнениями, окципитальным релизом и постизометрической релаксацией;
• 2-ая дополнительная группа (5 пациентов) отказались от выполнения каких-либо физических упражнений.
Анализ клинических проявлений цервикалгии проводился до введения первой инъекции Фреманезумаба и через 6 мес после начала терапии.
В качестве исследуемых мышц были выбраны трапециевидная, жевательная, височная и нижняя косая, с учетом ранее предоставленных данных о более частом вовлечении у пациентов с мигренью. Интенсивность болезненности при пальпации оценивалась по шкале ВАШ (0–10 баллов).
В результате исследования было обнаружено достоверное снижение болезненности трапециевидной и височной мышц в обеих группах, вне зависимости от выполнения физических упражнений, в отличие от жевательной и нижней косой мышц – в данном случае показатели достоверно снизились лишь при сочетании МАТ-терапии и физических упражнений.

Выводы
1. У пациентов с мигренью и коморбидной ЦГБ выявлена более выраженная ЦС при сравнении с коморбидной цервикалгией, в связи с чем при подборе терапии необходимо уделять внимание не только купированию ЦГБ, но и профилактике мигренозных приступов, коррекции психоэмоциональных расстройств и нарушений сна.2. Миофасциальный болевой синдром с вовлечением трапециевидной и височной мышц может самостоятельно разрешиться при специфической терапии мигрени моноклональными антителами, однако для купирования напряжения и болезненности в жевательной и нижней косой мышцах более эффективным является дополнение в виде лечебной гимнастики и мягких мануальных техник.
3. С учетом выявленных прямых связей умеренной силы между числом болезненных точек выхода тройничного нерва, вовлеченными мышцами перикраниальной области, а также эффектом от терапии приступов мигрени моноклональными антителами, можно сделать вывод о более выраженной ЦС при вовлечении жевательной и нижней косой мышц.
4. При осмотре пациентов с мигренью и активным цервикалгическим фактором либо при его отсутствии необходимо проводить тщательный осмотр мышц лицевой и краниовертебральной области, даже при отсутствии жалоб пациента на боль в лице или шее, а также назначать специфичную лечебную гимнастику для повышения эффективности лечения.
5. У всех пациентов с мигренью, вне зависимости от хронизации, необходимо проводить оценку интенсивности ЦС для своевременного и более полного оказания лечебной помощи.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Хайрутдинова Ольга Сергеевна – ассистент каф. реабилитации и спортивной медицины, ФГБОУ ВО «Казанский ГМУ».
E-mail: khayros.kzn@gmail.com; ORCID: 0000-0003-0442-4954
Olga S. Khairutdinova – Аssistant, Kazan State Medical University. E-mail: khayros.kzn@gmail.com;
ORCID: 0000-0003-0442-4954
Богданов Энвер Ибрагимович – д-р мед. наук, проф., зав. каф. неврологии, ФГБОУ ВО «Казанский ГМУ».
E-mail: enver_bogdanov@mail.com; ORCID: 0000-0001-9332-8053
Enver I. Bogdanov – Dr. Sci. (Med.), Prof., Kazan State Medical University. E-mail: enver_bogdanov@mail.com; ORCID: 0000-0001-9332-8053
Поступила в редакцию: 15.05.2024
Поступила после рецензирования: 22.05.2024
Принята к публикации: 23.05.2024
Received: 15.05.2024
Revised: 22.05.2024
Accepted: 23.05.2024
Список исп. литературыСкрыть список1. Ji RR, Nackley A, Huh Y et al. Neuroinflammation and Central Sensitization in Chronic and Widespread Pain. Anesthesiology. 2018;129(2):343-66. DOI: 10.1097/ALN.0000000000002130
2. URL: https://www.iasp-pain.org/resources/terminology/
3. Volcheck MM, Graham SM, Fleming KC et al. Central sensitization, chronic pain, and other symptoms: Better understanding, better management. Cleve Clin J Med. 2023;90(4):245-54. DOI: 10.3949/ccjm.90a.22019;
4. Suzuki K, Suzuki S, Shiina T et al. Central Sensitization in Migraine: A Narrative Review. J Pain Res. 2022;15:2673-82. DOI: 10.2147/JPR.S329280
5. Woolf CJ. Pain amplification- A perspective on the how, why, when, and where of central sensitization. J Appl Biobehav Res. 2018;23(2):e12124. DOI:10.1111/jabr.12124
6. Ji RR, Nackley A, Huh Y et al. Neuroinflammation and Central Sensitization in Chronic and Widespread Pain. Anesthesiology. 2018;129(2):343-66. DOI: 10.1097/ALN.0000000000002130
7. Латышева Н.В. Коморбидные заболевания у пациентов с хронической мигренью. Автореферат. М., 2020.
Latysheva N.V. Comorbid diseases in patients with chronic migraine. The abstract. Moscow, 2020 (in Russian).
8. Sjaastad O. Fredriksen TA, Pfaffenrath V. Cervicogenic headache: diagnostic criteria. Headache. 1998;38:442-5.
9. Govind J, Bogduk N. Sources of Cervicogenic Headache Among the Upper Cervical Synovial Joints. Pain Med. 2022;23(6):1059-65. DOI: 10.1093/pm/pnaa469
18 июня 2024
Количество просмотров: 10868


