Клинический разбор в общей медицине №11 2024
Клинический разбор в общей медицине №11 2024
Клиническая эффективность геля Холисал в составе комлексного консервативного лечения пациентов с воспалительными заболеваниями пародонта
Номера страниц в выпуске:125-134
Аннотация
Цель. Изучить обезболивающие, противовоспалительные и антимикробные свойства геля Холисал при его применении для консервативного лечения пациентов с гингивитом и пародонтитом.
Материал и методы. Проведено комплексное стоматологическое обследование и лечение 40 пациентов в возрасте от 25 до 54 лет без тяжелой соматической патологии. В 1-ю группу вошли 20 человек с диагнозом «хронический гингивит», во 2-ю – 20 пациентов с пародонтитом легкой степени тяжести. В составе комплексного консервативного лечения в обеих группах применяли стоматологический гель Холисал. Для оценки обезболивающего эффекта геля Холисал проводили опрос пациентов до и после его однократного применения на стоматологическом приеме. Боль оценивали по вербальной шкале. Для оценки эффективности курса лечения проводили стоматологическое обследование пациентов с индексной оценкой состояния тканей пародонта и ПЦР-исследование поддесневой микрофлоры, сравнивая показатели до лечения и через 10 дней от начала лечения.
Результаты. Опрос пациентов показал, что через 10 мин после однократного применения геля Холисал стоматологом после проведения профессиональной гигиены полости рта отмечался выраженный обезболивающий эффект: на отсутствие боли указывали 17 (85,0%) пациентов 1-й группы и 15 (75,0%) – 2-й группы. При проведении курса лечения с применением геля Холисал через 10 дней от начала лечения у пациентов с гингивитом наблюдалось статистически значимое снижение индекса гигиены Green–Vermillion на 72,0% (<0,001), а индекса кровоточивости Muhlemann–Cowell – на 67,3% (р<0,001). У пациентов с пародонтитом индекс гигиены снизился на 64,6% (р<0,001), индекс кровоточивости Muhlemann–Cowell – на 67,8% (р<0,001), а также наблюдалось статистически значимое снижение глубины пародонтальных карманов (с 2,1±0,2 мм до 1,3±0,2 мм, р<0,05). ПЦР-исследование поддесневой микрофлоры показало, что применение геля Холисал в составе комплексной терапии способствовало полной элиминации пародонтопатогенной микрофлоры у пациентов с гингивитом. У пациентов с пародонтитом после завершения курса лечения произошло значительное снижение частоты выявления таких представителей анаэробной микрофлоры, как Aggregatibacter actinomycetemcomitans и Porphyromonas gingivalis, при этом остальные исследованные пародонтопатогены после лечения не выявлялись.
Выводы. Применение геля Холисал у пациентов с гингивитом и пародонтитом легкой степени тяжести продемонстрировало выраженный обезболивающий эффект после однократного применения, а также противовоспалительную и антимикробную эффективность после 10-дневного курса комплексной консервативной терапии.
Ключевые слова: хронический гингивит, хронический пародонтит, Холисал, пародонтопатогены, обезболивающий эффект, вербальная шкала боли.
Для цитирования: Петрухина Н.Б., Снегирев М.В., Салтовец М.В. Клиническая эффективность геля Холисал в составе комлексного консервативного лечения пациентов с воспалительными заболеваниями пародонта. Клинический разбор в общей медицине. 2024; 5 (11): 125–134. DOI: 10.47407/kr2024.5.11.00526
Цель. Изучить обезболивающие, противовоспалительные и антимикробные свойства геля Холисал при его применении для консервативного лечения пациентов с гингивитом и пародонтитом.
Материал и методы. Проведено комплексное стоматологическое обследование и лечение 40 пациентов в возрасте от 25 до 54 лет без тяжелой соматической патологии. В 1-ю группу вошли 20 человек с диагнозом «хронический гингивит», во 2-ю – 20 пациентов с пародонтитом легкой степени тяжести. В составе комплексного консервативного лечения в обеих группах применяли стоматологический гель Холисал. Для оценки обезболивающего эффекта геля Холисал проводили опрос пациентов до и после его однократного применения на стоматологическом приеме. Боль оценивали по вербальной шкале. Для оценки эффективности курса лечения проводили стоматологическое обследование пациентов с индексной оценкой состояния тканей пародонта и ПЦР-исследование поддесневой микрофлоры, сравнивая показатели до лечения и через 10 дней от начала лечения.
Результаты. Опрос пациентов показал, что через 10 мин после однократного применения геля Холисал стоматологом после проведения профессиональной гигиены полости рта отмечался выраженный обезболивающий эффект: на отсутствие боли указывали 17 (85,0%) пациентов 1-й группы и 15 (75,0%) – 2-й группы. При проведении курса лечения с применением геля Холисал через 10 дней от начала лечения у пациентов с гингивитом наблюдалось статистически значимое снижение индекса гигиены Green–Vermillion на 72,0% (<0,001), а индекса кровоточивости Muhlemann–Cowell – на 67,3% (р<0,001). У пациентов с пародонтитом индекс гигиены снизился на 64,6% (р<0,001), индекс кровоточивости Muhlemann–Cowell – на 67,8% (р<0,001), а также наблюдалось статистически значимое снижение глубины пародонтальных карманов (с 2,1±0,2 мм до 1,3±0,2 мм, р<0,05). ПЦР-исследование поддесневой микрофлоры показало, что применение геля Холисал в составе комплексной терапии способствовало полной элиминации пародонтопатогенной микрофлоры у пациентов с гингивитом. У пациентов с пародонтитом после завершения курса лечения произошло значительное снижение частоты выявления таких представителей анаэробной микрофлоры, как Aggregatibacter actinomycetemcomitans и Porphyromonas gingivalis, при этом остальные исследованные пародонтопатогены после лечения не выявлялись.
Выводы. Применение геля Холисал у пациентов с гингивитом и пародонтитом легкой степени тяжести продемонстрировало выраженный обезболивающий эффект после однократного применения, а также противовоспалительную и антимикробную эффективность после 10-дневного курса комплексной консервативной терапии.
Ключевые слова: хронический гингивит, хронический пародонтит, Холисал, пародонтопатогены, обезболивающий эффект, вербальная шкала боли.
Для цитирования: Петрухина Н.Б., Снегирев М.В., Салтовец М.В. Клиническая эффективность геля Холисал в составе комлексного консервативного лечения пациентов с воспалительными заболеваниями пародонта. Клинический разбор в общей медицине. 2024; 5 (11): 125–134. DOI: 10.47407/kr2024.5.11.00526
Original Article
1 Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia;
2 National Medical Research Center for Dental and Maxillofacial Surgery, Moscow, Russia;
3 Russian Medical Academy of Continuous Professional Education, Moscow, Russia
petrukhina_n_b@staff.sechenov.ru
Abstract
Aim. To study the analgesic, anti-inflammatory and antimicrobial properties of Holisal gel when used for conservative treatment of patients with gingivitis and periodontitis.
Material and methods. A comprehensive dental examination and treatment of 40 patients aged 25 to 54 years without severe somatic pathology was conducted. The first group included 20 people diagnosed with chronic gingivitis, the second group – 20 patients with mild periodontitis. As part of the comprehensive conservative treatment in both groups, the dental gel Holisal was used. To assess the analgesic effect of the Holisal gel, patients were surveyed before and after its single use at a dental appointment. Pain was assessed using a verbal scale. To assess the effectiveness of the treatment course, a dental examination of patients with an index assessment of the condition of periodontal tissues and a PCR study of subgingival microflora were performed, comparing the indicators before treatment and 10 days after the start of treatment.
Results. A survey of patients showed that 10 minutes after a single application of Holisal gel by a dentist after professional oral hygiene, a pronounced analgesic effect was noted: the absence of pain was reported by 17 (85.0%) patients in the first group and 15 (75.0%) in the second group. During a course of treatment with Holisal gel, 10 days after the start of treatment, patients with gingivitis showed a statistically significant decrease in the Green–Vermillion hygiene index by 72.0% (<0.001), and the Muhlemann–Cowell bleeding index by 67.3% (p<0.001). In patients with periodontitis, the hygiene index decreased by 64.6% (p<0.001), the Muhlemann–Cowell bleeding index by 67.8% (p<0.001), and a statistically significant decrease in the depth of periodontal pockets was observed (from 2.1±0.2 mm to 1.3±0.2 mm, p<0.05). PCR testing of subgingival microflora showed that the use of Holisal gel as part of complex therapy contributed to the complete elimination of periodontopathogenic microflora in patients with gingivitis. In patients with periodontitis, after completion of the treatment, there was a significant decrease in the frequency of detection of such representatives of anaerobic microflora as Aggregatibacter actinomycetemcomitans and Porphyromonas gingivalis, while the rest of the studied periodontopathogens were not detected after treatment.
Conclusions. The use of Holisal gel in patients with gingivitis and mild periodontitis demonstrated a pronounced analgesic effect after a single application, as well as anti-inflammatory and antimicrobial efficacy after a 10-day course of complex conservative therapy.
Keywords: chronic gingivitis, chronic periodontitis, Holisal, periodontopathogens, analgesic effect, verbal pain scale.
For citation: Petrukhina N.B., Snegirev M.V., Saltovets M.V. Clinical efficacy of Holisal gel as part of complex conservative treatment of patients with inflammatory periodontal diseases. Clinical review for general practice. 2024; 5 (11): 125–134 (In Russ.). DOI: 10.47407/kr2024.5.11.00526
Качество жизни, связанное со здоровьем полости рта (Oral Health-Related Quality of Life – OHRQoL), включает в себя такие понятия, как физическое здоровье, психологическое состояние, социальные отношения, окружающую среду и влияние состояния полости рта на повседневную производительность [6]. При воспалительных заболеваниях пародонта физическое здоровье страдает из-за дискомфорта, боли, искажения вкуса, нарушений жевательной функции, речи и гигиены полости рта, при этом боль оказывает сильное влияние на снижение качества жизни пациентов [7].
Современные молекулярно-генетические методы исследования позволили значительно расширить представления об этиологии и патогенезе воспалительных заболеваний пародонта. В настоящее время доказана роль полимикробной биопленки полости рта в инициации воспаления [8, 9]. Агрессивные свойства бактерий проявляются двумя путями: во-первых, прямым токсическим воздействием, вызывающим воспаление и деструкцию в тканях пародонта; во-вторых, опосредованно, когда пародонтопатогенная микрофлора биопленки рта выступает в роли триггерного механизма активации фибробластов, макрофагов и моноцитов, гиперпродукции этими клетками провоспалительных медиаторов, ведущих к нарушению микроциркуляции в тканях пародонта, деструкции периодонтальной связки и резорбции костной ткани [10, 11].
При пародонтите оральный микробиом характеризуется дисбиозом с более высокой численностью анаэробных бактерий, таких как Porphyromonas gingivalis,
Actinobacillus actinomycetemcomitans и Tannerella forsythia, которые относят к пародонтопатогенам первого порядка. Именно они способны проникать в ткани десны и активировать воспалительные сигнальные пути. К пародонтопатогенным видам относят также Prevotella intermedia, Eicenella corrodens, Fusobacterium nucleatum и Treponema denticola, которые часто выявляются в составе микробной биопленки [12, 13]. Микроорганизмы являются основной причиной развития гингивита, но прогрессирование заболевания связывают с аберрантным иммунным ответом, в ходе которого из-за чрезмерной реакции организма-хозяина происходит деструкция собственных тканей [14].
Патогенез воспалительных заболеваний пародонта имеет сложный характер, что требует комплексного лечения и поиска новых современных методов воздействия на определенные звенья имеющихся нарушений. Стоматологический гель Холисал является комбинированным препаратом, что позволяет ему блокировать сразу несколько патогенетических факторов, способствующих воспалению и деструкции тканей пародонта. В состав этого препарата входит цеталкония хлорид, обладающий антимикробными свойствами, и холина салицилат с противовоспалительным и аналгезирующим действием [15, 16].
Холисал обладает рядом преимуществ по сравнению с другими средствами для местного применения в консервативном лечении пародонтита, поскольку имеет гелевую форму, обладает адгезией к слизистой оболочке, заполняет пародонтальные поражения различных форм и размеров благодаря своей текучести, но при этом не вымывается слюной и десневой жидкостью [17, 18]. В ходе биодеградации гелевой матрицы происходит постепенное высвобождение лекарственных компонентов. Это позволяет обеспечить длительное и эффективное воздействие биологически активных веществ в месте поражения тканей пародонта [19, 20].
Цель настоящего исследования – изучить обезболивающие, противовоспалительные и антимикробные свойства геля Холисал при его применении для консервативного лечения пациентов с гингивитом и пародонтитом.
Проведены комплексное стоматологическое обследование и лечение 40 пациентов в возрасте от 25 до 54 лет без тяжелой соматической патологии. Находившиеся под наблюдением пациенты в зависимости от клинического состояния тканей пародонта были распределены на 2 группы: 1-ю группу (n=20) составили лица, у которых выявлен хронический гингивит (шифр K05.1 по Международной классификации болезней 10-го пересмотра), 2-ю группу (n=20) – пациенты с хроническим пародонтитом (K05.31) легкой степени тяжести.
Критерии невключения:
• тяжелые соматические заболевания в стадии декомпенсации;
• онкологические заболевания;
• период беременности и лактации;
• курение;
• аллергические реакции на медикаменты;
• необходимость системного приема любых медикаментов;
• антибиотикотерапия, проводившаяся в ближайший месяц до настоящего исследования.
Из исследования исключались лица, не явившиеся на контрольный осмотр и нарушающие протокол исследования.
Диагноз устанавливали на основании жалоб, данных клинического и рентгенологического исследований (ортопантомограмма). Так, для пародонтита легкой степени глубина пародонтальных карманов не превышала 3 мм, а рентгенологическая картина подтверждала признаки начальной деструкции межзубных перегородок.
Все пациенты, включенные в исследование, в доступной форме были проинформированы о проводимых методах обследования и лечения, мотивированы на соблюдение всех рекомендаций. Каждым участником исследования было подписано добровольное информированное согласие на участие. Пациенты, не понимающие цель исследования и не подписавшие формы согласия, в исследование включены не были.
Клиническое обследование пациентов включало в себя тщательный сбор жалоб и анамнеза, осмотр, определение индекса гигиены рта по J. Green, J. Vermillion (1964 г.) и индекса кровоточивости по H. Muhlemann (H. Muhlemann, S. Son, 1971) в модификации C. Cowell (C. Cowell и соавт., 1975). При выявлении пародонтальных карманов проводили измерение их глубины (в мм) с помощью градуированного пародонтального зонда от дна кармана до десневого края.
Для определения состава микрофлоры исследовали содержимое десневой борозды у пациентов с гингивитом и пародонтальных карманов у пациентов с пародонтитом. Исследование проводили дважды: до лечения и через 10 дней от начала курса лечения. Материал забирали утром натощак до чистки зубов при помощи стерильных бумажных эндодонтических штифтов (размер №25), которые погружали в десневую борозду или в наиболее глубокий пародонтальный карман до его дна, оставляя на 10 с. Затем штифты помещали в пробирку с транспортной средой и транспортировали в лабораторию в охлажденном состоянии в специальных термоконтейнерах.
Выявление пародонтопатогенов в полученных образцах проводили методом мультиплексной полимеразной цепной реакции (ПЦР) с помощью стандартного набора праймеров Дентоскрин (ООО НПФ «Литех», Россия), который позволяет идентифицировать 7 микроорганизмов, ассоциированных с заболеваниями пародонта: Aggregatibacter actinomycetemcomitans, P. gingivalis, P. endodontalis, P. intermedia, T. forsythia, T. denticola, F. nucleatum. Амплификацию осуществляли с помощью программируемого четырехканального термостата ТП4-ПЦР-01-Терцик (ООО «НПО ДНК-Технология», Россия). Амплифицированные образцы идентифицировали методом обратной гибридизации в соответствии с протоколом фирмы-производителя.
Перед началом лечения пациентов обеих групп обучали стандартному методу чистки зубов по Г.Н. Пахомову, правильному использованию флоссов, межзубных ершиков, ирригатора. Тактика лечения была следующей: всем пациентам в одно посещение проводили профессиональную гигиену рта с удалением над- и поддесневых зубных отложений ультразвуковым способом и системой Air Flow, полирование поверхностей зубов.
В 1-й группе сразу после окончания профессиональной гигиены в стоматологическом кресле проводили аппликации на десну геля Холисал (Pharmaceutical Works Jelfa, S.a., Польша) с последующим воздержанием от приема пищи и жидкостей в течение 10 мин.
Во 2-й группе применение геля Холисал было следующим: сочетали аппликации на десну с введением геля в пародонтальные карманы при помощи шприца с тупой канюлей в необходимом количестве. Для оценки обезболивающего эффекта геля Холисал проводили опрос пациентов до его применения и через 10 мин после процедуры. Болевые ощущения оценивали по вербальной шкале (verbal rating scales – VRS). Пациенту предлагали выбрать слово, которое наиболее точно характеризует его ощущения: нет боли – 0, слабая боль – 1, умеренная – 2, сильная – 3, очень сильная – 4, нестерпимая (невыносимая) боль – 5.
В домашних условиях пациентам 1 и 2-й групп назначали самостоятельное применение геля Холисал. Гель рекомендовали наносить на десну после чистки зубов ежедневно 2 раза в день с последующим воздержанием от приема пищи и жидкостей в течение 10 мин.
По истечении 10 дней от начала лечения пациенты обеих групп являлись на прием для проведения повторного обследования.
Для сравнительной оценки клинической эффективности лечения между группами рассчитывали редукцию стоматологических индексов по формуле:
(х1-х2)×100%/х1, где х1 – величина индекса до лечения, х2 – величина индекса через 10 дней от начала лечения. Для оценки антимикробного эффекта проводили сравнительный анализ состава поддесневой микрофлоры до лечения и после завершения курса лечения.
Статистический анализ результатов исследования проводили с помощью компьютерной программы Statistica 12.0 (StatSoft, США). При сравнении показателей индексной оценки в динамике использовали критерий Вилкоксона, сравнение процентных соотношений проводили с помощью точного критерия Фишера.
При первом посещении все пациенты с хроническим гингивитом предъявляли жалобы на кровоточивость при чистке зубов и приеме пищи, на периодически появляющуюся ноющую боль в деснах. Общее состояние пациентов с хроническим гингивитом не страдало.
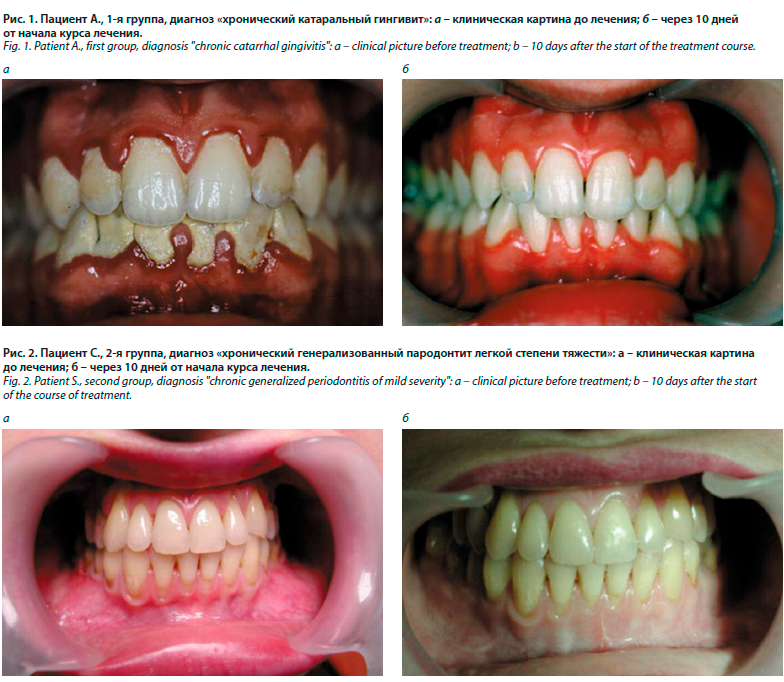
При объективном осмотре у пациентов с гингивитом выявлялась следующая клиническая картина: десневые сосочки рыхлые, отечные, гиперемированные с синюшным оттенком; десневой край отечен, увеличен в объеме, валикообразно утолщен (рис. 1, а).
Пациенты 2-й группы, у которых был выявлен хронический пародонтит легкой степени тяжести, на момент начала исследования чаще всего предъявляли жалобы на неприятный запах изо рта, кровоточивость при чистке зубов и при приеме твердой пищи, припухлость десен, ноющую боль в деснах, боли при приеме пищи, нарушение жевания. У 5 (25,0%) пациентов имелись жалобы на нарушение общего состояния: слабость, недомогание, раздражительность, плохой аппетит.
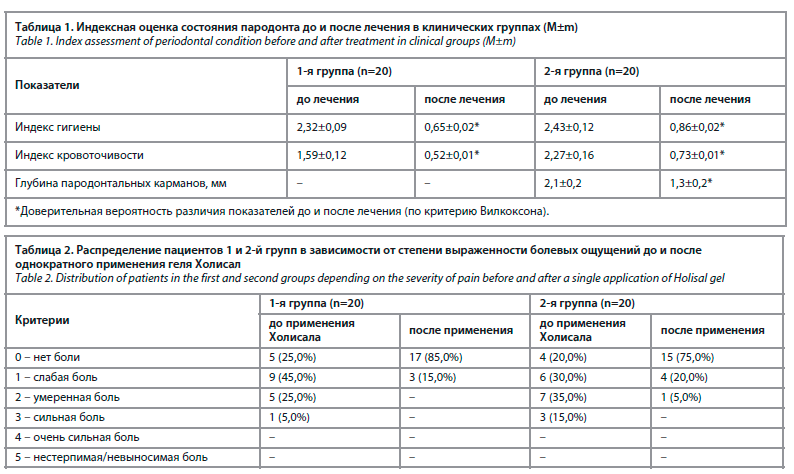
При проведении объективного осмотра диагностирован хронический воспалительный процесс, десневые сосочки и маргинальная часть десны отечны, цианотичны (рис. 2, а). Клинически чаще всего в тканях пародонта выявлялись воспаление в виде отека, гиперемии или пастозности слизистой оболочки десны, наличие над- и поддесневых зубных отложений. У 13 (65,0%) пациентов отмечались оголение шеек и частично корней зубов, гиперестезия.
До лечения у пациентов обеих групп отмечалось неудовлетворительное гигиеническое состояние полости рта, о чем свидетельствовали высокие значения индекса гигиены (табл. 1). Индекс кровоточивости десен Muhlemann–Cowell в 1-й группе составлял в среднем 1,59±0,12, во 2-й – 2,27±0,16. У пациентов 2-й группы имелись пародонтальные карманы, локализующиеся преимущественно в области межзубных промежутков, средняя глубина карманов до лечения составляла 2,1±0,2 мм.
В 1-й группе до аппликации геля Холисал один пациент описывал свои ощущения как «сильную боль», 5 (25,0%) – как «умеренную боль», 9 (45,0%) – как «слабую боль» и 5 (25,0%) – отмечали отсутствие боли (табл. 2). Через 10 мин после аппликации геля Холисал пациентов повторно просили описать свои ощущения. Опрос показал, что после применения геля Холисал 17 (85,0%) пациентов указали на отсутствие боли и лишь 3 (15,0%) оценили свои ощущения как «слабую боль».
Распределение пациентов 2-й группы в зависимости от градации болевых ощущений до применения геля Холисал было следующим: 3 (15,0%) пациента оценили свои ощущения как «сильную боль», 7 (35,0%) – как «умеренную боль», 6 (30,0%) – как «слабую боль» и 4 (20,0%) – отмечали отсутствие боли. После применения геля Холисал у 15 (75,0%) пациентов болевые ощущения отсутствовали, 4 (20,0%) пациента оценили свои ощущения как «слабую боль» и лишь один пациент испытывал «умеренную боль».
Анализ объективных показателей воспаления в тканях пародонта свидетельствовал о том, что у пациентов 1-й группы с диагнозом «гингивит» курс консервативной терапии с применением геля Холисал показал высокую клиническую эффективность. Так, через 10 дней от начала лечения у пациентов 1-й группы произошло достоверное снижение стоматологических показателей: индекс гигиены Green–Vermillion снизился на 72,0% (<0,001 по сравнению с уровнем до лечения), а индекс кровоточивости Muhlemann–Cowell – на 67,3% (р<0,001 по сравнению с уровнем до лечения).
Проведение лечения способствовало значительной регрессии воспалительного процесса в тканях пародонта у всех пациентов с пародонтитом легкой степени тяжести. Индекс гигиены Green–Vermillion после курса лечения снизился на 64,6% (р<0,001), индекс кровоточивости Muhlemann–Cowell – на 67,8% (р<0,001). Также у пациентов 2-й группы после проведенного лечения наблюдалось статистически значимое снижение глубины пародонтальных карманов (с 2,1±0,2 мм до 1,3±0,2 мм; р<0,05); см. табл. 1.
Таким образом, проведение курса консервативной терапии в течение 10 дней позволяло значительно улучшить состояние тканей пародонта у пациентов обеих клинических групп.
По результатам ПЦР-диагностики, у пациентов 1-й группы в большинстве случаев в десневой жидкости выявлялись T. forsythia и F. nucleatum – по 35,0% случаев, порфиромонады обнаружены в 20,0% случаев,
A. actinomycetemcomitans – 15,0%, остальные исследованные пародонтопатогены встречались реже – в 5–10% случаев (табл. 3).
У большинства пациентов 2-й группы (70,0%) было обнаружено присутствие в пародонтальных карманах
P. gingivalis. Наличие T. forsythia было выявлено в содержимом пародонтальных карманов у 1/2 пациентов с пародонтитом, а A. actinomycetemcomitans – в 25,0% случаев. Эти три вида микроорганизмов обладают целым рядом патогенных факторов, оказывающих неблагоприятное воздействие на тканевые структуры пародонта: способностью к инвазии в эпителиальные и эндотелиальные клетки, высокой протеолитической активностью, способностью активировать и подавлять неспецифический ответ организма хозяина.
ПЦР-исследование, проведенное после завершения курса консервативного лечения с применением геля Холисал, показало полную элиминацию пародонтопатогенной микрофлоры у пациентов с гингивитом. У пациентов с пародонтитом отмечалось существенное снижение частоты выявления в пародонтальных карманах таких агрессивных пародонтопатогенов, как A. actinomycetemcomitans и P. gingivalis, а также отсутствие других представителей пародонтопатогенной микрофлоры (см. табл. 3).
Одним из важных свойств Холисала является его обезболивающий эффект. Хотя гингивит и пародонтит обычно не вызывают острой боли, за исключением язвенно-некротических поражений и пародонтальных абсцессов, повышенная чувствительность зубов встречается часто. Потеря пародонтального прикрепления приводит к рецессиям, при которых обнажается корень зуба, вызывая чувствительность. Пародонтологическое лечение, неотъемлемой частью которого является профессиональная гигиена полости рта, также может являться причиной болевых ощущений, даже на фоне адекватного предшествующего местного обезболивания. В связи с этим эффективное устранение болевого синдрома остается важным показателем качества оказываемой пациентам медицинской помощи [21].
Оценка локализации и интенсивности болевых ощущений обычно бывает достаточной в клинической практике. Однако при планировании клинических исследований необходимы точные критерии для оценки интенсивности боли, чтобы обеспечить надежность, валидность, репрезентативность. Для этих целей разработаны различные методы количественной оценки болевых состояний. Шкалы боли полезны для клинической оценки того, насколько интенсивно пациенты чувствуют боль, а также для мониторинга результативности лечения в разные периоды времени [22].
Для оценки обезболивающего эффекта геля Холисал нами использовалась вербальная шкала, которая имеет ряд преимуществ: она удобна в применении, понятна и доступна каждому пациенту, адекватно отражает эффективность проводимой терапии [23].
Опрос пациентов показал, что через 10 мин после однократного применения геля Холисал стоматологом после проведения профессиональной гигиены полости рта отмечался выраженный обезболивающий эффект: на отсутствие боли указывали 17 (85,0%) пациентов 1-й группы и 15 (75,0%) – 2-й группы. Это свойство Холисала в дальнейшем оказало положительное влияние на мотивацию пациентов к ежедневному применению данного препарата в домашних условиях.
Обезболивающий эффект геля Холисал достигается за счет включения в его состав холина салицилата, обладающего прямым и непрямым влиянием на болевые рецепторы. Прямое действие заключается в деполяризации ионных каналов, за счет чего осуществляется быстрое купирование боли. Непрямое местное обезболивающее действие происходит за счет снижения продукции простагландинов, брадикинина и других провоспалительных медиаторов, повышающих чувствительность свободных нервных окончаний к раздражителям. Кроме того, болевые ощущения снижаются в результате уменьшения отека и экссудации, поскольку устраняется механическое раздражение ноцицепторов.
Клиническое обследование пациентов после завершения 10-дневного курса применения геля Холисал в домашних условиях показало, что у пациентов обеих групп отмечалась положительная динамика в состоянии тканей пародонта, что может быть объяснено фармакологическим действием препарата Холисал.
Противовоспалительный эффект геля Холисал основан на блокаде циклооксигеназного пути воспаления. Это приводит к снижению уровня простагландинов, провоспалительных цитокинов интерлейкина-1β, интерлейкина-6, фактора некроза опухоли α и других медиаторов. В результате этого достигаются противовоспалительный и обезболивающий эффекты. Снижение выброса простагландинов и провоспалительных цитокинов позволяет остановить воспалительную резорбцию костных структур пародонта и запустить процесс ремоделирования костной ткани [24, 25].
Салицилаты обладают также циклооксигеназо-независимыми эффектами, которые осуществляются через несколько механизмов, а именно: ингибирование окислительного взрыва нейтрофилов; удаление гидроксильных радикалов и хелатирование переходных металлов; снижение активности синтазы оксида азота; увеличение синтеза липоксинов и резолвинов; ингибирование активаторного белка-1, вовлеченного в регулирование экспрессии большого числа генов [26]. В результате этого уменьшаются проявления оксидативного стресса, снижается выброс протеолитических ферментов, способствующих разрушению тканей при хроническом воспалении. За счет блокады синтеза лейкотриенов и других хемокинов салицилаты предотвращают миграцию лейкоцитов в очаг воспаления, а также ингибируют действие ядерного фактора NF-κB, который опосредует разрушение костной ткани [27, 28]. Эти механизмы обусловливают мощные противовоспалительные, антиоксидантные и цитопротекторные эффекты, способствуя разрешению воспаления в тканях пародонта.
Исследование показало, что применение геля Холисал в составе комплексной терапии способствовало полной элиминации пародонтопатогенной микрофлоры у пациентов с гингивитом. У пациентов с пародонтитом после завершения курса лечения произошло значительное снижение частоты выявления таких представителей анаэробной микрофлоры, как A. actinomycetemcomitans и P. gingivalis, ответственных за прогрессирование воспаления, деструкцию периодонтальной связки и костных структур пародонта, при этом остальные исследованные пародонтопатогены после лечения полностью отсутствовали.
Антимикробный эффект Холисала обусловлен наличием в составе препарата цеталкония хлорида, который относится к группе катионных сурфактантов. Важным свойством этого химического вещества является его способность к биоадгезии, что позволяет ему адсорбироваться на покрытой биопленкой поверхности зубов, оставаться в полости рта в течение длительного времени, сохраняя антимикробную активность. Он проявляет активность против всех возбудителей, обитающих в полости рта: бактерий, вирусов и грибов, что способствует его эффективности независимо от этиологического фактора воспаления.
Механизм антимикробного действия цеталкония хлорида основан на электростатическом взаимодействии с анионными группировками на мембранах бактериальных клеток, приводит к образованию мембранных пор, разрушению мембран и лизису бактерии [29].
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Петрухина Наталья Борисовна – д-р мед. наук, доц., проф. каф. клинической фармакологии и пропедевтики внутренних болезней ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет). E-mail: petrukhina_n_b@staff.sechenov.ru
ORCID: 0000-0003-3840-8127
Nataliia B. Petrukhina – Dr. Sci. (Med.), Associate Professor, Sechenov First Moscow State Medical University (Sechenov University). E-mail: petrukhina_n_b@staff.sechenov.ru ORCID: 0000-0003-3840-8127
Снегирев Михаил Валентинович – канд. мед. наук, ФГБУ НМИЦ ЦНИИСиЧЛХ. ORCID: 0000-0002-4758-2963
Mikhail V. Snegirev – Cand. Sci. (Med.), National Medical Research Center for Dental and Maxillofacial Surgery. ORCID: 0000-0002-4758-2963
Салтовец Мария Владимировна – канд. мед. наук, ФГБОУ ДПО РМАНПО. ORCID: 0000-0003-0673-2555
Mariia V. Saltovets – Cand. Sci. (Med.), Russian Medical Academy of Continuous Professional Education. ORCID: 0000-0003-0673-2555
Поступила в редакцию: 12.11.2024
Поступила после рецензирования: 19.11.2024
Принята к публикации: 21.11.2024
Received: 12.11.2024
Revised: 19.11.2024
Accepted: 21.11.2024
Clinical efficacy of Holisal gel as part of complex conservative treatment of patients with inflammatory periodontal diseases
Nataliia B. Petrukhina1, Mikhail V. Snegirev2, Mariia V. Saltovets31 Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia;
2 National Medical Research Center for Dental and Maxillofacial Surgery, Moscow, Russia;
3 Russian Medical Academy of Continuous Professional Education, Moscow, Russia
petrukhina_n_b@staff.sechenov.ru
Abstract
Aim. To study the analgesic, anti-inflammatory and antimicrobial properties of Holisal gel when used for conservative treatment of patients with gingivitis and periodontitis.
Material and methods. A comprehensive dental examination and treatment of 40 patients aged 25 to 54 years without severe somatic pathology was conducted. The first group included 20 people diagnosed with chronic gingivitis, the second group – 20 patients with mild periodontitis. As part of the comprehensive conservative treatment in both groups, the dental gel Holisal was used. To assess the analgesic effect of the Holisal gel, patients were surveyed before and after its single use at a dental appointment. Pain was assessed using a verbal scale. To assess the effectiveness of the treatment course, a dental examination of patients with an index assessment of the condition of periodontal tissues and a PCR study of subgingival microflora were performed, comparing the indicators before treatment and 10 days after the start of treatment.
Results. A survey of patients showed that 10 minutes after a single application of Holisal gel by a dentist after professional oral hygiene, a pronounced analgesic effect was noted: the absence of pain was reported by 17 (85.0%) patients in the first group and 15 (75.0%) in the second group. During a course of treatment with Holisal gel, 10 days after the start of treatment, patients with gingivitis showed a statistically significant decrease in the Green–Vermillion hygiene index by 72.0% (<0.001), and the Muhlemann–Cowell bleeding index by 67.3% (p<0.001). In patients with periodontitis, the hygiene index decreased by 64.6% (p<0.001), the Muhlemann–Cowell bleeding index by 67.8% (p<0.001), and a statistically significant decrease in the depth of periodontal pockets was observed (from 2.1±0.2 mm to 1.3±0.2 mm, p<0.05). PCR testing of subgingival microflora showed that the use of Holisal gel as part of complex therapy contributed to the complete elimination of periodontopathogenic microflora in patients with gingivitis. In patients with periodontitis, after completion of the treatment, there was a significant decrease in the frequency of detection of such representatives of anaerobic microflora as Aggregatibacter actinomycetemcomitans and Porphyromonas gingivalis, while the rest of the studied periodontopathogens were not detected after treatment.
Conclusions. The use of Holisal gel in patients with gingivitis and mild periodontitis demonstrated a pronounced analgesic effect after a single application, as well as anti-inflammatory and antimicrobial efficacy after a 10-day course of complex conservative therapy.
Keywords: chronic gingivitis, chronic periodontitis, Holisal, periodontopathogens, analgesic effect, verbal pain scale.
For citation: Petrukhina N.B., Snegirev M.V., Saltovets M.V. Clinical efficacy of Holisal gel as part of complex conservative treatment of patients with inflammatory periodontal diseases. Clinical review for general practice. 2024; 5 (11): 125–134 (In Russ.). DOI: 10.47407/kr2024.5.11.00526
Введение
Воспалительные заболевания пародонта – серьезная проблема для здравоохранения, поскольку они характеризуются широкой распространенностью во всех странах мира и негативно влияют на качество жизни людей [1–4]. Заболевания полости рта могут снижать самооценку и чувство собственного достоинства, препятствовать нормальному социальному взаимодействию, приводить к хроническому стрессу и депрессии, вызывать проблемы со здоровьем других органов и систем, а также мешать жизненно важным функциям, таким как дыхание, прием пищи, глотание и речь [5].Качество жизни, связанное со здоровьем полости рта (Oral Health-Related Quality of Life – OHRQoL), включает в себя такие понятия, как физическое здоровье, психологическое состояние, социальные отношения, окружающую среду и влияние состояния полости рта на повседневную производительность [6]. При воспалительных заболеваниях пародонта физическое здоровье страдает из-за дискомфорта, боли, искажения вкуса, нарушений жевательной функции, речи и гигиены полости рта, при этом боль оказывает сильное влияние на снижение качества жизни пациентов [7].
Современные молекулярно-генетические методы исследования позволили значительно расширить представления об этиологии и патогенезе воспалительных заболеваний пародонта. В настоящее время доказана роль полимикробной биопленки полости рта в инициации воспаления [8, 9]. Агрессивные свойства бактерий проявляются двумя путями: во-первых, прямым токсическим воздействием, вызывающим воспаление и деструкцию в тканях пародонта; во-вторых, опосредованно, когда пародонтопатогенная микрофлора биопленки рта выступает в роли триггерного механизма активации фибробластов, макрофагов и моноцитов, гиперпродукции этими клетками провоспалительных медиаторов, ведущих к нарушению микроциркуляции в тканях пародонта, деструкции периодонтальной связки и резорбции костной ткани [10, 11].
При пародонтите оральный микробиом характеризуется дисбиозом с более высокой численностью анаэробных бактерий, таких как Porphyromonas gingivalis,
Actinobacillus actinomycetemcomitans и Tannerella forsythia, которые относят к пародонтопатогенам первого порядка. Именно они способны проникать в ткани десны и активировать воспалительные сигнальные пути. К пародонтопатогенным видам относят также Prevotella intermedia, Eicenella corrodens, Fusobacterium nucleatum и Treponema denticola, которые часто выявляются в составе микробной биопленки [12, 13]. Микроорганизмы являются основной причиной развития гингивита, но прогрессирование заболевания связывают с аберрантным иммунным ответом, в ходе которого из-за чрезмерной реакции организма-хозяина происходит деструкция собственных тканей [14].
Патогенез воспалительных заболеваний пародонта имеет сложный характер, что требует комплексного лечения и поиска новых современных методов воздействия на определенные звенья имеющихся нарушений. Стоматологический гель Холисал является комбинированным препаратом, что позволяет ему блокировать сразу несколько патогенетических факторов, способствующих воспалению и деструкции тканей пародонта. В состав этого препарата входит цеталкония хлорид, обладающий антимикробными свойствами, и холина салицилат с противовоспалительным и аналгезирующим действием [15, 16].
Холисал обладает рядом преимуществ по сравнению с другими средствами для местного применения в консервативном лечении пародонтита, поскольку имеет гелевую форму, обладает адгезией к слизистой оболочке, заполняет пародонтальные поражения различных форм и размеров благодаря своей текучести, но при этом не вымывается слюной и десневой жидкостью [17, 18]. В ходе биодеградации гелевой матрицы происходит постепенное высвобождение лекарственных компонентов. Это позволяет обеспечить длительное и эффективное воздействие биологически активных веществ в месте поражения тканей пародонта [19, 20].
Цель настоящего исследования – изучить обезболивающие, противовоспалительные и антимикробные свойства геля Холисал при его применении для консервативного лечения пациентов с гингивитом и пародонтитом.
Материал и методы
Клиническое исследование проводили на базе отделения терапевтической стоматологии ФГБУ НМИЦ «Центральный научно-исследовательский институт стоматологии и челюстно-лицевой хирургии» Минздрава России. Дизайн исследования – проспективное открытое.Проведены комплексное стоматологическое обследование и лечение 40 пациентов в возрасте от 25 до 54 лет без тяжелой соматической патологии. Находившиеся под наблюдением пациенты в зависимости от клинического состояния тканей пародонта были распределены на 2 группы: 1-ю группу (n=20) составили лица, у которых выявлен хронический гингивит (шифр K05.1 по Международной классификации болезней 10-го пересмотра), 2-ю группу (n=20) – пациенты с хроническим пародонтитом (K05.31) легкой степени тяжести.
Критерии невключения:
• тяжелые соматические заболевания в стадии декомпенсации;
• онкологические заболевания;
• период беременности и лактации;
• курение;
• аллергические реакции на медикаменты;
• необходимость системного приема любых медикаментов;
• антибиотикотерапия, проводившаяся в ближайший месяц до настоящего исследования.
Из исследования исключались лица, не явившиеся на контрольный осмотр и нарушающие протокол исследования.
Диагноз устанавливали на основании жалоб, данных клинического и рентгенологического исследований (ортопантомограмма). Так, для пародонтита легкой степени глубина пародонтальных карманов не превышала 3 мм, а рентгенологическая картина подтверждала признаки начальной деструкции межзубных перегородок.
Все пациенты, включенные в исследование, в доступной форме были проинформированы о проводимых методах обследования и лечения, мотивированы на соблюдение всех рекомендаций. Каждым участником исследования было подписано добровольное информированное согласие на участие. Пациенты, не понимающие цель исследования и не подписавшие формы согласия, в исследование включены не были.
Клиническое обследование пациентов включало в себя тщательный сбор жалоб и анамнеза, осмотр, определение индекса гигиены рта по J. Green, J. Vermillion (1964 г.) и индекса кровоточивости по H. Muhlemann (H. Muhlemann, S. Son, 1971) в модификации C. Cowell (C. Cowell и соавт., 1975). При выявлении пародонтальных карманов проводили измерение их глубины (в мм) с помощью градуированного пародонтального зонда от дна кармана до десневого края.
Для определения состава микрофлоры исследовали содержимое десневой борозды у пациентов с гингивитом и пародонтальных карманов у пациентов с пародонтитом. Исследование проводили дважды: до лечения и через 10 дней от начала курса лечения. Материал забирали утром натощак до чистки зубов при помощи стерильных бумажных эндодонтических штифтов (размер №25), которые погружали в десневую борозду или в наиболее глубокий пародонтальный карман до его дна, оставляя на 10 с. Затем штифты помещали в пробирку с транспортной средой и транспортировали в лабораторию в охлажденном состоянии в специальных термоконтейнерах.
Выявление пародонтопатогенов в полученных образцах проводили методом мультиплексной полимеразной цепной реакции (ПЦР) с помощью стандартного набора праймеров Дентоскрин (ООО НПФ «Литех», Россия), который позволяет идентифицировать 7 микроорганизмов, ассоциированных с заболеваниями пародонта: Aggregatibacter actinomycetemcomitans, P. gingivalis, P. endodontalis, P. intermedia, T. forsythia, T. denticola, F. nucleatum. Амплификацию осуществляли с помощью программируемого четырехканального термостата ТП4-ПЦР-01-Терцик (ООО «НПО ДНК-Технология», Россия). Амплифицированные образцы идентифицировали методом обратной гибридизации в соответствии с протоколом фирмы-производителя.
Перед началом лечения пациентов обеих групп обучали стандартному методу чистки зубов по Г.Н. Пахомову, правильному использованию флоссов, межзубных ершиков, ирригатора. Тактика лечения была следующей: всем пациентам в одно посещение проводили профессиональную гигиену рта с удалением над- и поддесневых зубных отложений ультразвуковым способом и системой Air Flow, полирование поверхностей зубов.
В 1-й группе сразу после окончания профессиональной гигиены в стоматологическом кресле проводили аппликации на десну геля Холисал (Pharmaceutical Works Jelfa, S.a., Польша) с последующим воздержанием от приема пищи и жидкостей в течение 10 мин.
Во 2-й группе применение геля Холисал было следующим: сочетали аппликации на десну с введением геля в пародонтальные карманы при помощи шприца с тупой канюлей в необходимом количестве. Для оценки обезболивающего эффекта геля Холисал проводили опрос пациентов до его применения и через 10 мин после процедуры. Болевые ощущения оценивали по вербальной шкале (verbal rating scales – VRS). Пациенту предлагали выбрать слово, которое наиболее точно характеризует его ощущения: нет боли – 0, слабая боль – 1, умеренная – 2, сильная – 3, очень сильная – 4, нестерпимая (невыносимая) боль – 5.
В домашних условиях пациентам 1 и 2-й групп назначали самостоятельное применение геля Холисал. Гель рекомендовали наносить на десну после чистки зубов ежедневно 2 раза в день с последующим воздержанием от приема пищи и жидкостей в течение 10 мин.
По истечении 10 дней от начала лечения пациенты обеих групп являлись на прием для проведения повторного обследования.
Для сравнительной оценки клинической эффективности лечения между группами рассчитывали редукцию стоматологических индексов по формуле:
(х1-х2)×100%/х1, где х1 – величина индекса до лечения, х2 – величина индекса через 10 дней от начала лечения. Для оценки антимикробного эффекта проводили сравнительный анализ состава поддесневой микрофлоры до лечения и после завершения курса лечения.
Статистический анализ результатов исследования проводили с помощью компьютерной программы Statistica 12.0 (StatSoft, США). При сравнении показателей индексной оценки в динамике использовали критерий Вилкоксона, сравнение процентных соотношений проводили с помощью точного критерия Фишера.
Результаты
По данным анамнеза, первые признаки воспалительных болезней пародонта у пациентов 1-й группы появились в среднем 2,6±0,9 года назад, у пациентов 2-й группы – 5,5±1,3 года назад. При анализе данных анамнеза у всех пациентов заболевание начиналось постепенно, длительно протекало практически бессимптомно, но затем жалобы постепенно нарастали.При первом посещении все пациенты с хроническим гингивитом предъявляли жалобы на кровоточивость при чистке зубов и приеме пищи, на периодически появляющуюся ноющую боль в деснах. Общее состояние пациентов с хроническим гингивитом не страдало.
При объективном осмотре у пациентов с гингивитом выявлялась следующая клиническая картина: десневые сосочки рыхлые, отечные, гиперемированные с синюшным оттенком; десневой край отечен, увеличен в объеме, валикообразно утолщен (рис. 1, а).
Пациенты 2-й группы, у которых был выявлен хронический пародонтит легкой степени тяжести, на момент начала исследования чаще всего предъявляли жалобы на неприятный запах изо рта, кровоточивость при чистке зубов и при приеме твердой пищи, припухлость десен, ноющую боль в деснах, боли при приеме пищи, нарушение жевания. У 5 (25,0%) пациентов имелись жалобы на нарушение общего состояния: слабость, недомогание, раздражительность, плохой аппетит.
При проведении объективного осмотра диагностирован хронический воспалительный процесс, десневые сосочки и маргинальная часть десны отечны, цианотичны (рис. 2, а). Клинически чаще всего в тканях пародонта выявлялись воспаление в виде отека, гиперемии или пастозности слизистой оболочки десны, наличие над- и поддесневых зубных отложений. У 13 (65,0%) пациентов отмечались оголение шеек и частично корней зубов, гиперестезия.
До лечения у пациентов обеих групп отмечалось неудовлетворительное гигиеническое состояние полости рта, о чем свидетельствовали высокие значения индекса гигиены (табл. 1). Индекс кровоточивости десен Muhlemann–Cowell в 1-й группе составлял в среднем 1,59±0,12, во 2-й – 2,27±0,16. У пациентов 2-й группы имелись пародонтальные карманы, локализующиеся преимущественно в области межзубных промежутков, средняя глубина карманов до лечения составляла 2,1±0,2 мм.

Оценка обезболивающего эффекта геля Холисал
Для оценки обезболивающего эффекта геля Холисал проводили опрос пациентов до и после его однократного применения на стоматологическом приеме после проведения профессиональной гигиены полости рта. Для оценки болевых ощущений применяли вербальную шкалу с градацией от 0 (нет боли) до 5 (нестерпимая/невыносимая) боль.В 1-й группе до аппликации геля Холисал один пациент описывал свои ощущения как «сильную боль», 5 (25,0%) – как «умеренную боль», 9 (45,0%) – как «слабую боль» и 5 (25,0%) – отмечали отсутствие боли (табл. 2). Через 10 мин после аппликации геля Холисал пациентов повторно просили описать свои ощущения. Опрос показал, что после применения геля Холисал 17 (85,0%) пациентов указали на отсутствие боли и лишь 3 (15,0%) оценили свои ощущения как «слабую боль».
Распределение пациентов 2-й группы в зависимости от градации болевых ощущений до применения геля Холисал было следующим: 3 (15,0%) пациента оценили свои ощущения как «сильную боль», 7 (35,0%) – как «умеренную боль», 6 (30,0%) – как «слабую боль» и 4 (20,0%) – отмечали отсутствие боли. После применения геля Холисал у 15 (75,0%) пациентов болевые ощущения отсутствовали, 4 (20,0%) пациента оценили свои ощущения как «слабую боль» и лишь один пациент испытывал «умеренную боль».
Оценка противовоспалительной эффективности
Клиническое обследование пациентов после завершения 10-дневного курса применения геля Холисал в домашних условиях показало, что у пациентов 1-й группы отмечалась положительная динамика в состоянии тканей пародонта, жалобы отсутствовали. При объективном осмотре отмечены признаки купирования воспалительного процесса (см. рис. 1, б). Пациенты 2-й группы отмечали субъективное улучшения состояния десны, снижение интенсивности кровоточивости при чистке зубов, исчезновение неприятного запаха изо рта. Осмотр показал: десна бледно-розового цвета, плотно прилегает к поверхности зубов (см. рис. 2, б).Анализ объективных показателей воспаления в тканях пародонта свидетельствовал о том, что у пациентов 1-й группы с диагнозом «гингивит» курс консервативной терапии с применением геля Холисал показал высокую клиническую эффективность. Так, через 10 дней от начала лечения у пациентов 1-й группы произошло достоверное снижение стоматологических показателей: индекс гигиены Green–Vermillion снизился на 72,0% (<0,001 по сравнению с уровнем до лечения), а индекс кровоточивости Muhlemann–Cowell – на 67,3% (р<0,001 по сравнению с уровнем до лечения).
Проведение лечения способствовало значительной регрессии воспалительного процесса в тканях пародонта у всех пациентов с пародонтитом легкой степени тяжести. Индекс гигиены Green–Vermillion после курса лечения снизился на 64,6% (р<0,001), индекс кровоточивости Muhlemann–Cowell – на 67,8% (р<0,001). Также у пациентов 2-й группы после проведенного лечения наблюдалось статистически значимое снижение глубины пародонтальных карманов (с 2,1±0,2 мм до 1,3±0,2 мм; р<0,05); см. табл. 1.
Таким образом, проведение курса консервативной терапии в течение 10 дней позволяло значительно улучшить состояние тканей пародонта у пациентов обеих клинических групп.

Оценка антимикробной эффективности
Исследование поддесневой микрофлоры методом ПЦР до начала лечения показало высокую распространенность пародонтопатогенов у пациентов с гингивитом и пародонтитом.По результатам ПЦР-диагностики, у пациентов 1-й группы в большинстве случаев в десневой жидкости выявлялись T. forsythia и F. nucleatum – по 35,0% случаев, порфиромонады обнаружены в 20,0% случаев,
A. actinomycetemcomitans – 15,0%, остальные исследованные пародонтопатогены встречались реже – в 5–10% случаев (табл. 3).
У большинства пациентов 2-й группы (70,0%) было обнаружено присутствие в пародонтальных карманах
P. gingivalis. Наличие T. forsythia было выявлено в содержимом пародонтальных карманов у 1/2 пациентов с пародонтитом, а A. actinomycetemcomitans – в 25,0% случаев. Эти три вида микроорганизмов обладают целым рядом патогенных факторов, оказывающих неблагоприятное воздействие на тканевые структуры пародонта: способностью к инвазии в эпителиальные и эндотелиальные клетки, высокой протеолитической активностью, способностью активировать и подавлять неспецифический ответ организма хозяина.
ПЦР-исследование, проведенное после завершения курса консервативного лечения с применением геля Холисал, показало полную элиминацию пародонтопатогенной микрофлоры у пациентов с гингивитом. У пациентов с пародонтитом отмечалось существенное снижение частоты выявления в пародонтальных карманах таких агрессивных пародонтопатогенов, как A. actinomycetemcomitans и P. gingivalis, а также отсутствие других представителей пародонтопатогенной микрофлоры (см. табл. 3).

Обсуждение
Результаты клинической оценки и данные мультиплексной ПЦР свидетельствовали об эффективности применения геля Холисал в составе комплексной терапии пациентов с гингивитом и пародонтитом.Одним из важных свойств Холисала является его обезболивающий эффект. Хотя гингивит и пародонтит обычно не вызывают острой боли, за исключением язвенно-некротических поражений и пародонтальных абсцессов, повышенная чувствительность зубов встречается часто. Потеря пародонтального прикрепления приводит к рецессиям, при которых обнажается корень зуба, вызывая чувствительность. Пародонтологическое лечение, неотъемлемой частью которого является профессиональная гигиена полости рта, также может являться причиной болевых ощущений, даже на фоне адекватного предшествующего местного обезболивания. В связи с этим эффективное устранение болевого синдрома остается важным показателем качества оказываемой пациентам медицинской помощи [21].
Оценка локализации и интенсивности болевых ощущений обычно бывает достаточной в клинической практике. Однако при планировании клинических исследований необходимы точные критерии для оценки интенсивности боли, чтобы обеспечить надежность, валидность, репрезентативность. Для этих целей разработаны различные методы количественной оценки болевых состояний. Шкалы боли полезны для клинической оценки того, насколько интенсивно пациенты чувствуют боль, а также для мониторинга результативности лечения в разные периоды времени [22].
Для оценки обезболивающего эффекта геля Холисал нами использовалась вербальная шкала, которая имеет ряд преимуществ: она удобна в применении, понятна и доступна каждому пациенту, адекватно отражает эффективность проводимой терапии [23].
Опрос пациентов показал, что через 10 мин после однократного применения геля Холисал стоматологом после проведения профессиональной гигиены полости рта отмечался выраженный обезболивающий эффект: на отсутствие боли указывали 17 (85,0%) пациентов 1-й группы и 15 (75,0%) – 2-й группы. Это свойство Холисала в дальнейшем оказало положительное влияние на мотивацию пациентов к ежедневному применению данного препарата в домашних условиях.
Обезболивающий эффект геля Холисал достигается за счет включения в его состав холина салицилата, обладающего прямым и непрямым влиянием на болевые рецепторы. Прямое действие заключается в деполяризации ионных каналов, за счет чего осуществляется быстрое купирование боли. Непрямое местное обезболивающее действие происходит за счет снижения продукции простагландинов, брадикинина и других провоспалительных медиаторов, повышающих чувствительность свободных нервных окончаний к раздражителям. Кроме того, болевые ощущения снижаются в результате уменьшения отека и экссудации, поскольку устраняется механическое раздражение ноцицепторов.
Клиническое обследование пациентов после завершения 10-дневного курса применения геля Холисал в домашних условиях показало, что у пациентов обеих групп отмечалась положительная динамика в состоянии тканей пародонта, что может быть объяснено фармакологическим действием препарата Холисал.
Противовоспалительный эффект геля Холисал основан на блокаде циклооксигеназного пути воспаления. Это приводит к снижению уровня простагландинов, провоспалительных цитокинов интерлейкина-1β, интерлейкина-6, фактора некроза опухоли α и других медиаторов. В результате этого достигаются противовоспалительный и обезболивающий эффекты. Снижение выброса простагландинов и провоспалительных цитокинов позволяет остановить воспалительную резорбцию костных структур пародонта и запустить процесс ремоделирования костной ткани [24, 25].
Салицилаты обладают также циклооксигеназо-независимыми эффектами, которые осуществляются через несколько механизмов, а именно: ингибирование окислительного взрыва нейтрофилов; удаление гидроксильных радикалов и хелатирование переходных металлов; снижение активности синтазы оксида азота; увеличение синтеза липоксинов и резолвинов; ингибирование активаторного белка-1, вовлеченного в регулирование экспрессии большого числа генов [26]. В результате этого уменьшаются проявления оксидативного стресса, снижается выброс протеолитических ферментов, способствующих разрушению тканей при хроническом воспалении. За счет блокады синтеза лейкотриенов и других хемокинов салицилаты предотвращают миграцию лейкоцитов в очаг воспаления, а также ингибируют действие ядерного фактора NF-κB, который опосредует разрушение костной ткани [27, 28]. Эти механизмы обусловливают мощные противовоспалительные, антиоксидантные и цитопротекторные эффекты, способствуя разрешению воспаления в тканях пародонта.
Исследование показало, что применение геля Холисал в составе комплексной терапии способствовало полной элиминации пародонтопатогенной микрофлоры у пациентов с гингивитом. У пациентов с пародонтитом после завершения курса лечения произошло значительное снижение частоты выявления таких представителей анаэробной микрофлоры, как A. actinomycetemcomitans и P. gingivalis, ответственных за прогрессирование воспаления, деструкцию периодонтальной связки и костных структур пародонта, при этом остальные исследованные пародонтопатогены после лечения полностью отсутствовали.
Антимикробный эффект Холисала обусловлен наличием в составе препарата цеталкония хлорида, который относится к группе катионных сурфактантов. Важным свойством этого химического вещества является его способность к биоадгезии, что позволяет ему адсорбироваться на покрытой биопленкой поверхности зубов, оставаться в полости рта в течение длительного времени, сохраняя антимикробную активность. Он проявляет активность против всех возбудителей, обитающих в полости рта: бактерий, вирусов и грибов, что способствует его эффективности независимо от этиологического фактора воспаления.
Механизм антимикробного действия цеталкония хлорида основан на электростатическом взаимодействии с анионными группировками на мембранах бактериальных клеток, приводит к образованию мембранных пор, разрушению мембран и лизису бактерии [29].
Заключение
Применение геля Холисал продемонстрировало выраженный обезболивающий эффект после однократного применения, а также противовоспалительную и антимикробную эффективность после 10-дневного курса комплексной консервативной терапии. За счет действия двух активных веществ гель Холисал позволяет значительно улучшить состояние пародонта. Активные компоненты с различными механизмами действия позволяют устранить пародонтопатогенную микрофлору и блокировать выброс провоспалительных медиаторов, что способствует синергетической терапевтической эффективности у пациентов с пародонтитом.Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Петрухина Наталья Борисовна – д-р мед. наук, доц., проф. каф. клинической фармакологии и пропедевтики внутренних болезней ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет). E-mail: petrukhina_n_b@staff.sechenov.ru
ORCID: 0000-0003-3840-8127
Nataliia B. Petrukhina – Dr. Sci. (Med.), Associate Professor, Sechenov First Moscow State Medical University (Sechenov University). E-mail: petrukhina_n_b@staff.sechenov.ru ORCID: 0000-0003-3840-8127
Снегирев Михаил Валентинович – канд. мед. наук, ФГБУ НМИЦ ЦНИИСиЧЛХ. ORCID: 0000-0002-4758-2963
Mikhail V. Snegirev – Cand. Sci. (Med.), National Medical Research Center for Dental and Maxillofacial Surgery. ORCID: 0000-0002-4758-2963
Салтовец Мария Владимировна – канд. мед. наук, ФГБОУ ДПО РМАНПО. ORCID: 0000-0003-0673-2555
Mariia V. Saltovets – Cand. Sci. (Med.), Russian Medical Academy of Continuous Professional Education. ORCID: 0000-0003-0673-2555
Поступила в редакцию: 12.11.2024
Поступила после рецензирования: 19.11.2024
Принята к публикации: 21.11.2024
Received: 12.11.2024
Revised: 19.11.2024
Accepted: 21.11.2024
Список исп. литературыСкрыть список1. World Health Organization. WHO; Geneva: 2022. Global oral health status report – towards universal health coverage for oral health by 2030. https://www.who.int/team/noncommunicable-diseases/global-status-report-on-oral-health-2022.
2. GBD 2016 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 328 diseases and injuries for 195 countries, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet 2017;390(10100):1211-59. DOI: 10.1016/S0140-6736(17)32154-2
3. Tonetti MS, Jepsen S, Jin L, Otomo-Corgel J. Impact of the global burden of periodontal diseases on health, nutrition and wellbeing of mankind: a call for global action. J Clin Periodontol 2017;44:456-62. DOI: 10.1111/jcpe.12732
4. Nazir M, Al-Ansari A, Al-Khalifa K et al. Global Prevalence of Periodontal Disease and Lack of Its Surveillance. Sci World J 2020;2020: 2146160. DOI: 10.1155/2020/2146160
5. Rozier RG, Pahel BT. Patient- and population-reported outcomes in public health dentistry: Oral health-related quality of life. Dent Clin North Am 2008;52:345-65. DOI: 10.1016/j.cden.2007.12.002
6. Moya-Villaescusa MJ, Sánchez-Pérez A, Esparza-Marín J et al. Periodontal Disease and Nonsurgical Periodontal Therapy on the OHRQoL of the Patient: A Pilot Study of Case Series. Dent J (Basel) 2023;11(4):94. DOI: 10.3390/dj11040094
7. Bennadi D, Reddy CVK Oral health related quality of life. J Int Soc Prev Community Dent 2013;3(1):1-6. DOI: 10.4103/2231-0762.115700
8. Van Dyke TE, Bartold PM, Reynolds EC. The Nexus Between Periodontal Inflammation and Dysbiosis. Front Immunol 2020;(11):511. DOI: 10.3389/fimmu.2020.00511
9. Sedghi LM, Bacino M, Kapila YL. Periodontal Disease: The Good, The Bad, and The Unknown. Front Cell Infect Microbiol 2021;11:766944. DOI: 10.3389/fcimb.2021.766944
10. Hasturk H, Kantarci A. Activation and resolution of periodontal inflammation and its systemic impact. Periodontol 2000 2015;69(1):255-73. DOI: 10.1111/prd.12105
11. Yao C, Narumiya S. Prostaglandin-cytokine crosstalk in chronic inflammation. Br J Pharmacol 2019;176(3):337-54. DOI: 10.1111/bph.14530
12. Saliem SS, Bede SY, Cooper PR et al. Pathogenesis of periodontitis – A potential role for epithelial-mesenchymal transition. Jpn Dent Sci Rev 2022;58:268-78. DOI: 10.1016/j.jdsr.2022.09.001
13. Червинец В.М., Червинец Ю.В., Леонтьева А.В. и др. Микробиом полости рта у больных пародонтитом, адгезивные и биопленкообразующие свойства. Клиническая лабораторная диагностика. 2021;66(1):45-51. DOI: 10.18821/0869-2084-2021-66-1-45-51
Chervinets V.M., Chervinets Yu.V., Leont’eva A.V. et al. The microbiome of oral cavity patients with periodontitis, adhesive and biofilm forming properties. Klinicheskaya laboratornaya diagnostika. 2021;66(1):45-51. DOI: 10.18821/0869-2084-2021-66-1-45-51 (in Russian).
14. Lamont RJ, Hajishengallis GN, Jenkinson HF. Oral microbiology and immunology. Wiley-Blackwell, 2013.
15. Рабинович И.М., Петрухина Н.Б., Ших Е.В. и др. Стоматологический гель Холисал на этапе консервативного лечения воспалительных заболеваний пародонта. Стоматология. 2023;102(5):34–9. DOI: 10.17116/stomat202310205134
Rabinovich I.M., Petrukhina N.B., Shikh E.V. et al. Dental gel Cholisal at the stage of conservative treatment of inflammatory periodontal diseases. Stomatologiya. 2023;102(5):34–9. DOI: 10.17116/stomat202310205134 (in Russian).
16. Рабинович И.М., Снегирев М.В., Петрухина Н.Б. и др. Клиническая эффективность консервативного лечения пациентов с хроническим генерализованным пародонтитом с применением геля Холисал. Стоматология. 2024;103(2):24–31. DOI: 10.17116/stomat2024103021
Rabinovich IM, Snegirev MV, Petrukhina NB et al. Dental gel Cholisal at the stage of conservative treatment of inflammatory periodontal diseases. Stomatology. 2024;103(2):24–31. DOI: 10.17116/stomat 2024103021 (in Russian).
17. Максимова О.П. Роль препарата «Холисал»» в комплексном лечении заболеваний пародонта и слизистой оболочки рта. Клиническая стоматология. 2018;2(86):46-9. DOI: 10.37988/1811-153X_2018_2_46
Maksimova O.P. The role of the drug «Cholisal» in complex treatment of periodontal disease and oral mucosa. Klinicheskaya stomatologiya. 2018;2(86):46-9. DOI: 10.37988/1811-153X_2018_2_46 (in Russian).
18. Крихели Н.И., Пустовойт Е.В., Дарсигова З.Т. Эффективность применения препарата Холисал в комплексном лечении заболеваний слизистой оболочки полости рта и пародонта. Стоматология. 2022;101(6):98-102. DOI: 10.17116/stomat202210106198
Krikheli N.I., Pustovoit E.V., Darsigova Z.T. The effectiveness of the drug Cholisal in the complex treatment of oral mucosa and periodontal diseases. Stomatologiia. 2022;101(6):98-102. DOI: 10.17116/stomat202210106198 (in Russian).
19. Величко Э.В., Васильев Ю.Л. Особенности выбора современных аппликационных адгезивных форм лекарственных препаратов для лечения воспалительных заболеваний пародонта и слизистых оболочек рта. Клиническая стоматология. 2022;25(4):64-72. DOI: 10.37988/1811-153X_2022_4_64
Velichko E.V., Vasil’ev Yu.L. Eculiarities of selection of modern adhesive medications for treatment of inflammatory periodontal and oral mucosa diseases. Klinicheskaya stomatologiya. 2022;25(4):64-72. DOI: 10.37988/1811-153X_2022_4_64 (in Russian).
20. Gegout PY, Stutz C, Huck O. Gels as adjuvant to non-surgical periodontal therapy: A systematic review and meta-analysis. Heliyon 2023;9(7):e17789. DOI: 10.1016/j.heliyon.2023.e17789
21. Derman SHM, Lantwin EM, Barbe AG, Noack MJ. Does a pretreatment with a dentine hypersensitivity mouth-rinse compensate the pain caused by professional mechanical plaque removal? A single-blind randomized controlled clinical trial. Clin Oral Investig 2021;25(5):3151-60. DOI: 10.1007/s00784-020-03643-4
22. Gupta R, Kaur S, Parveen D, Kumar M. Comparative evaluation of efficacy of EMLA and needleless jet anesthesia in non-surgical periodontal therapy. J Oral Biol Craniofac Res 2018;8(2):118-21.
23. Морозов A.M., Жуков C.B., Беляк M.A. и др. О возможности оценивания болевого синдрома при помощи наиболее валидизированных шкал боли (обзор литературы). Вестник новых медицинских технологий. 2020;2:62-8. DOI: 10.24411/1609-2163-2020-16663
Morozov A.M., Zhukov S.V., Belyak M.A. et al. About the possibilities of evaluating a pain syndrome using the most validized pain scales. Journal of New Medical Technologies. 2020;2:62-8. DOI: 10.24411/1609-2163-2020-16663 (in Russian).
24. Орехова Л.Ю., Лобода Е.С., Атрушкевич В.Г. и др. Актуальность применения нестероидных противовоспалительных препаратов в пародонтологии. Пародонтология. 2021;26(3):211-22. DOI: 10.33925/1683-3759-2021-26-3-211-222
Orekhova L.Yu., Loboda E.S., Atrushkevich V.G. et al. Relevance of non-steroidal anti-inflammatory drugs in periodontology. Parodontologiya. 2021;26(3):211-22. DOI: 10.33925/1683-3759-2021-26-3-211-222 (in Russian)
25. Reynolds MA, Prudencio A, Aichelmann-Reidy ME et al. Curr Drug Non-steroidal anti-inflammatory drug (NSAID)-derived poly(anhydride-esters) in bone and periodontal regeneration. Deliv 2007;4(3):233-9. DOI: 10.2174/156720107781023866
26. Baltazar MT, Dinis-Oliveira RJ, Duarte JA et al. Antioxidant properties and associated mechanisms of salicylates. Curr Med Chem 2011;18(21):3252-64. DOI: 10.2174/092986711796391552
27. Kotowska-Rodziewicz A., Zalewska A., Maciejczyk M. A Review of Preclinical and Clinical Studies in Support of the Role of Non-Steroidal Anti-Inflammatory Drugs in Dentistry. Med Sci Monit 2023;29:e940635. DOI: 10.12659/MSM.940635
28. Lingappan K. NF-κB in oxidative stress. Curr Opin Toxicol 2018;(7):
81-6. DOI: 10.1016/j.cotox.2017.11.002
29. Mao X, Auer DL, Buchalla W et al. Cetylpyridinium Chloride: Mechanism of Action, Antimicrobial Efficacy in Biofilms, and Potential Risks of Resistance. Antimicrob Agents Chemother 2020. PMID: 32513792
18 декабря 2024
Количество просмотров: 988


