Клинический разбор в общей медицине №12 2024
Клинический разбор в общей медицине №12 2024
Современное состояние вопроса диагностики и лечения немеланомного рака кожи у пожилых пациентов
Номера страниц в выпуске:56-66
Аннотация
Введение. Пожилой возраст является существенным фактором риска для всех видов рака кожи. Немеланомный рак кожи (НМРК) является наиболее часто диагностируемым видом рака во всем мире и особенно поражает пожилых людей. В 2019 г. в Российской Федерации НМРК составлял 10,6% от общего числа онкологических заболеваний у мужчин и 15,2% у женщин. За тот же период отмечался рост заболеваемости: на 7,9% у мужчин и на 17,9% у женщин. Средний возраст пациентов с данным заболеванием составил 69,7 года.
Цель. Проанализировать литературу, посвященную распространенности НМРК среди пожилых людей, уникальным проблемам, с которыми сталкиваются пациенты, а также последние достижения в области лечения.
Материалы и методы. Поиск научных работ проводился в базах данных ELibrary, PubMed и Google Scholar до сентября 2024 г. Отбор публикаций осуществлялся согласно рекомендациям PRISMA. В обзор включены 78 исследований.
Результаты. В обзоре подчеркивается важность адаптированных подходов к лечению НМРК у пожилых людей. Учитывая растущую распространенность НМРК у пожилых людей, удовлетворение их особых потребностей и проблем имеет первостепенное значение. Продолжающиеся исследования в этой области могут улучшить результаты лечения и повысить качество жизни пожилых пациентов с НМРК. Будущее гериатрической дерматологии, вероятно, будет зависеть от этих достижений, обеспечивающих более полное понимание методов лечения НМРК у пожилых людей.
Заключение. Поскольку область дерматологии продолжает развиваться, индивидуальный подход к лечению НМРК у пожилых людей будет иметь решающее значение. Активное сотрудничество между медицинскими работниками, пациентами и их семьями имеет важное значение для принятия обоснованных решений о лечении. Необходимы дальнейшие исследования для уточнения рекомендаций и стратегий лечения пожилых людей с особым акцентом на оптимизацию терапевтических результатов при минимизации физического, эмоционального и социального воздействия НМРК и его лечения.
Ключевые слова: немеланомный рак кожи, плоскоклеточный рак кожи, базальноклеточный рак кожи, пожилые, лечение, диагностика, кожа.
Для цитирования: Пирожникова А.А., Стецюк М.В., Кудревич К.А., Абдурахманова Э.Э., Умерова А.И., Тамасян Э.Г., Ковали Д.Ю., Товмасян К.А., Филипова В.А., Диарова А.А., Немирова О.В., Багдасарян А.А., Шадиев Х-А.А. Современное состояние вопроса диагностики и лечения немеланомного рака кожи у пожилых пациентов. Клинический разбор в общей медицине. 2024; 5 (12): 56–66. DOI: 10.47407/kr2024.5.12.00538
Введение. Пожилой возраст является существенным фактором риска для всех видов рака кожи. Немеланомный рак кожи (НМРК) является наиболее часто диагностируемым видом рака во всем мире и особенно поражает пожилых людей. В 2019 г. в Российской Федерации НМРК составлял 10,6% от общего числа онкологических заболеваний у мужчин и 15,2% у женщин. За тот же период отмечался рост заболеваемости: на 7,9% у мужчин и на 17,9% у женщин. Средний возраст пациентов с данным заболеванием составил 69,7 года.
Цель. Проанализировать литературу, посвященную распространенности НМРК среди пожилых людей, уникальным проблемам, с которыми сталкиваются пациенты, а также последние достижения в области лечения.
Материалы и методы. Поиск научных работ проводился в базах данных ELibrary, PubMed и Google Scholar до сентября 2024 г. Отбор публикаций осуществлялся согласно рекомендациям PRISMA. В обзор включены 78 исследований.
Результаты. В обзоре подчеркивается важность адаптированных подходов к лечению НМРК у пожилых людей. Учитывая растущую распространенность НМРК у пожилых людей, удовлетворение их особых потребностей и проблем имеет первостепенное значение. Продолжающиеся исследования в этой области могут улучшить результаты лечения и повысить качество жизни пожилых пациентов с НМРК. Будущее гериатрической дерматологии, вероятно, будет зависеть от этих достижений, обеспечивающих более полное понимание методов лечения НМРК у пожилых людей.
Заключение. Поскольку область дерматологии продолжает развиваться, индивидуальный подход к лечению НМРК у пожилых людей будет иметь решающее значение. Активное сотрудничество между медицинскими работниками, пациентами и их семьями имеет важное значение для принятия обоснованных решений о лечении. Необходимы дальнейшие исследования для уточнения рекомендаций и стратегий лечения пожилых людей с особым акцентом на оптимизацию терапевтических результатов при минимизации физического, эмоционального и социального воздействия НМРК и его лечения.
Ключевые слова: немеланомный рак кожи, плоскоклеточный рак кожи, базальноклеточный рак кожи, пожилые, лечение, диагностика, кожа.
Для цитирования: Пирожникова А.А., Стецюк М.В., Кудревич К.А., Абдурахманова Э.Э., Умерова А.И., Тамасян Э.Г., Ковали Д.Ю., Товмасян К.А., Филипова В.А., Диарова А.А., Немирова О.В., Багдасарян А.А., Шадиев Х-А.А. Современное состояние вопроса диагностики и лечения немеланомного рака кожи у пожилых пациентов. Клинический разбор в общей медицине. 2024; 5 (12): 56–66. DOI: 10.47407/kr2024.5.12.00538
Original article
Emine E. Abdurakhmanova2, Amina I. Umerova2, Edgar G. Tamasyan2, Dilyara Yu. Kovali2,
Koryun A. Tovmasyan2, Veronika A. Filipova3, Aliya A. Diarova3, Olga V. Nemirova4,
Askina A. Bagdasaryan5, Khozh-Akhmed A. Shadiev6
1 Mechnikov North-Western State Medical University, Saint Petersburg, Russia;
2 Georgievsky Order of the Red Banner Medical Institute, Simferopol, Russia;
3 Bashkir State Medical University, Ufa, Russia;
4 Moscow University of Humanities and Economics, Moscow, Russia;
5 Rostov State Medical University, Rostov-on-Don, Russia;
6 Astrakhan State Medical University, Astrakhan, Russia
vkomissiya@inbox.ru
Abstract
Introduction. Old age is a significant risk factor for all types of skin cancer. Non-melanoma skin cancer (NSCLC) is the most commonly diagnosed type of cancer worldwide and especially affects the elderly. In 2019, in the Russian Federation, NSCLC accounted for 10.6% of the total number of oncological diseases in men and 15.2% in women. During the same period, there was an increase in the incidence: by 7.9% in men and by 17.9% in women. The average age of patients with this disease was 69.7 years.
Aim. to analyze the literature on the prevalence of NSCLC among the elderly, the unique problems faced by patients, as well as recent advances in treatment.
Materials and methods. Research papers were searched in the databases eLibrary, PubMed and Google Scholar until September 2024. The selection of publications was carried out according to the recommendations of PRISMA. 78 studies were included in the review.
Results. The review highlights the importance of adapted approaches to the treatment of NSCLC in the elderly. Given the increasing prevalence of NSCLC in older people, meeting their special needs and concerns is of paramount importance. Ongoing research in this area can improve treatment outcomes and improve the quality of life of elderly patients with NSCLC. The future of geriatric dermatology is likely to depend on these advances providing a more complete understanding of treatments for NSCLC in the elderly.
Conclusion. As the field of dermatology continues to evolve, an individual approach to the treatment of NSCLC in the elderly will be crucial. Active collaboration between healthcare professionals, patients and their families is essential for making informed treatment decisions. Further research is needed to clarify the recommendations and treatment strategies for older people, with a particular focus on optimizing therapeutic outcomes while minimizing the physical, emotional and social impact of NSCLC and its treatment.
Keywords: non-melanoma skin cancer, squamous cell skin cancer, basal cell skin cancer, elderly, treatment, diagnosis, skin.
For citation: Pirozhnikova A.A., Stetsyuk M.V., Kudrevich K.A., Abdurakhmanova E.E., Umerova A.I., Tamasyan E.G., Kovali D.Yu.,
Tovmasyan K.A., Filipova V.A., Diarova A.A., Nemirova O.V., Bagdasaryan A.A., Shadiev Kh.-A.A. The current state of the issue of diagnosis and treatment of non-melanoma skin cancer in elderly patients. Clinical review for general practice. 2024; 5 (12): 56–66 (In Russ.).
DOI: 10.47407/kr2024.5.12.00538
Цель обзора – проанализировать литературу, посвященную распространенности НМРК среди пожилых людей, уникальным проблемам, с которыми сталкиваются пациенты, а также последние достижения в области лечения.
 Методология поиска исследований
Методология поиска исследований
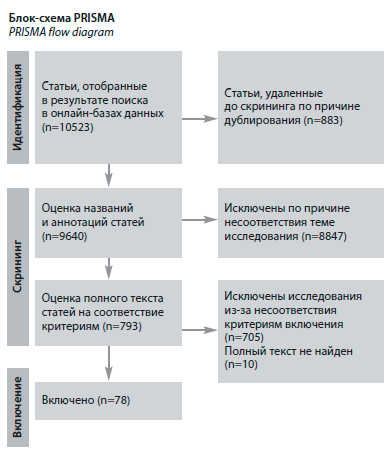
Поиск научных работ проводился в базах данных ELibrary, PubMed и Google Scholar до сентября 2024 г. Отбор публикаций осуществлялся согласно рекомендациям PRISMA. Все авторы независимо друг от друга занимались поиском публикаций, а в случае возникновения разногласий принимали решение путем консенсуса. Для поиска использовались следующие ключевые слова и их сочетания на русском и английском языках: «немеланомный рак кожи», «плоскоклеточный рак кожи», «базальноклеточный рак кожи», «пожилые», «лечение», «диагностика», «кожа», non-melanoma skin cancer, squamous cell skin cancer, basal cell skin cancer, elderly, treatment, diagnosis, skin. В результате поиска было выявлено 10 523 статьи. На этапе скрининга проводилась оценка приемлемости исследований по следующим критериям включения:
• исследование опубликовано на русском или английском языке;
• исследование опубликовано в рецензируемом научном издании;
• исследование является обзором литературы, описанием клинического случая или оригинальным исследованием с участием людей и описывающим проблемы диагностики и лечения НМРК у пожилых людей.
В итоге в обзор были включены 78 исследований. Блок-схема PRISMA с подробным алгоритмом поиска исследований представлена на рисунке.
Возраст, бесспорно, является основным фактором риска развития рака кожи, и поскольку ожидаемая продолжительность жизни возросла, число случаев рака кожи будет увеличиваться, если не будут предприняты дополнительные усилия по профилактике [3]. Заболеваемость НМРК ежегодно растет, и сегодня рак кожи является наиболее часто диагностируемым злокачественным новообразованием в развитых странах [6, 7]. НМРК чаще встречается среди пожилого населения, причем увеличение заболеваемости прямо коррелирует с возрастом. Риск развития НМРК заметно повышается после 50 лет, причем наиболее подвержены ему пожилые люди, особенно в возрасте 70 лет и старше [8]. БРК является наиболее распространенным из них, за ним следует ПРК [2].
В дополнение к генетическим факторам риска и иммуносупрессии такие факторы окружающей среды как длительное воздействие ультрафиолетовых (УФ) лучей, ионизирующее излучение и канцерогены играют значимую роль в развитии НМРК [9]. Географическое положение также играет важную роль, так некоторые регионы характеризуются более высокими уровнями УФ-излучения, что приводит к увеличению показателей заболеваемости НМРК [10]. Такие факторы, как бледность кожи, солнечные ожоги в анамнезе и возрастные изменения кожи, включая уменьшение толщины дермы, снижение васкуляризации и нарушение иммунных реакций, еще больше усугубляют эту уязвимость [11]. Более того, иммуносупрессивные состояния и некоторые медикаментозные препараты, которые часто более распространены среди пожилых людей из-за сопутствующих возрастных заболеваний, подвергают их повышенному риску развития НМРК [12].
В следующих разделах рассматриваются хирургические и неинвазивные методы лечения НМРК, а также положительные и отрицательные моменты применения каждого терапевтического подхода в пожилом возрасте.
Хирургические варианты лечения: Микрографическая хирургия по методу Мооса или хирургическое иссечение. Выбор между микрграфической хирургией по Моосу (МХМ) и широким иссечением (ШИ) при первичном лечении НМРК зависит от таких факторов, как локализация, размер и тип опухоли. МХМ, признанный золотым стандартом, обеспечивает эффективное удаление опухоли и позволяет максимально сохранить близлежащие здоровые ткани [19]. Этот метод включает тщательное обследование удаленных тканей, что позволяет точно определить наличие опухолевых клеток и их расположение. Если в процессе анализа выявляются опухолевые клетки на краях резекции, это указывает на необходимость повторных вмешательств для полного удаления новообразования. Таким образом, повторная локальная эксцизия тканей продолжается до тех пор, пока края резекции не станут отрицательными, что является критически важным для снижения риска рецидива и увеличения шансов на успешный исход лечения. Кроме того, такой подход способствует снижению травматичности и улучшает косметический результат, что особенно важно для пациентов [19]. Критерии надлежащего применения (англ. Appropriate Use Criteria, AUC), разработанные Американской академией дерматологии, помогают определить приемлемость МХМ на основе клинических, патологических и индивидуальных критериев пациента [17]. Разработанное приложение «Mohs Surgery AUC» также может предоставить подробные рекомендации по надлежащей интерпретации критериев в режиме реального времени во время осмотра пациента.
ШИ включает в себя иссечение краев вокруг опухоли с гистологическим исследованием путем выполнения параллельных разрезов (техника «нарезка хлеба») [20]. Оптимальные границы ШИ остаются неопределенными, но данные свидетельствуют о том, что иссечение 4 мм от края опухоли обеспечивают приемлемые результаты для всех случаев ПРК, за исключением опухолей высокого риска (т.е. тех, которые проникают в подкожную клетчатку более глубоко), при которых рекомендуется иссекать 6 мм [21]. Идеальным хирургическим методом лечения БРК диаметром менее 2 см является полное иссечение 3–4 мм здоровой кожи вокруг опухоли [22]. Для поражений диаметром более 2 см или в группе высокого риска может быть достаточно иссечения 5 мм для достижения четких результатов, в то время как для рецидивирующих поражений рекомендуется иссекать 6 мм или проведение МХМ [22].
Рентабельное и экономичное по времени ШИ является хорошим методом лечения НМРК, однако тщательный контроль заживления ран имеет решающее значение у пожилых людей, учитывая возрастные физиологические изменения, влияющие на этот процесс [23]. Врачи должны учитывать эти соображения, поскольку нарушение процесса заживления ран может привести к таким осложнениям, как расхождение швов или инфицирование [23]. Кроме того, потенциальная потребность в реконструктивной хирургии у пожилых людей требует оценки оптимальных косметических и функциональных результатов [23].
Последние научно обоснованные рекомендации подчеркивают эффективность как МХМ, так и ШИ для лечения первичного БРК, при этом МХМ демонстрирует значительно более низкую частоту рецидивов при 5- и 10-летнем наблюдении по сравнению с ШИ при локализации опухоли на лице [19, 24]. МХМ также продемонстрировала более благоприятные показатели по сравнению с ШИ для лечения ПРК, с локальными 5-летними показателями рецидива 1,2–2,6% [25] по сравнению с 5,7–8,1% соответственно [26].
Электродиссекация и кюретаж (ЭДК) – это деструктивная процедура, которая предлагает альтернативу ШИ и МХМ для лечения НМРК с низким уровнем риска. Она обычно используется при поверхностных или узловых БРК и ПРК in situ (ПРК-IS), когда опухоль хорошо выражена и неглубока [27]. Используя кюретку для удаления злокачественной ткани путем санации (из-за плохой межклеточной адгезии, проявляемой раковыми клетками) с последующей электрокоагуляцией, врач может удалить опухоль менее инвазивным способом по сравнению с хирургическим иссечением [27]. Несмотря на то что показатели излечения за 5 лет у пациентов, перенесших ЭДК, составляют 91–99%, гистологическая оценка краев невозможна, учитывая разрушительный характер процедуры, и, как следствие, как пациенты, так и лечащий врач должны уделять пристальное внимание на предмет признаков рецидива [28].
Преимущества таких методов лечения заключаются в том, что они не требуют проведения хирургической процедуры и минимизируют образование рубцов, в то время как недостатки заключаются в том, что местные препараты могут быть дорогостоящими и использоваться только для лечения поверхностных поражений, а также такое лечение характеризуется более высокой частотой рецидивов [30]. Результаты лечения варьируются в зависимости от различных местных методов лечения: сообщается, что в 94,9% случаев ПРК-IS рецидив после лечения 5-ФУ не наблюдался [31], а частота излечения ПРК-IS после местного лечения имиквимодом составляет 73–86% [32]. В недавнем всеобъемлющем обзоре нехирургических методов лечения БРК сообщалось, что долгосрочная эффективность (> 3 лет без рецидива) местного лечения имиквимодом составляет 75–87%, а краткосрочная эффективность (<1 года без рецидива) при местном лечении 5-ФУ – 90–93%, но при этом отдаленная частота рецидивов составляет 21% [33]. Необходимы дополнительные исследования для дальнейшей характеристики и сравнения показателей излечения и рецидивов наиболее эффективных местных методов лечения.
Системная терапия. Несмотря на то что МХМ остается золотым стандартом инвазивного лечения НМРК, начиная с 2018 г. исследования расширили возможности неинвазивных методов лечения. Некоторые из стратегий неинвазивного лечения подразумевали использование совершенно новых препаратов, в то время как другие подразумевали использование уже известных препаратов, которые применялись для лечения других заболеваний [34]. Сонидегиб, ингибитор пути hedgehog (HhI), был одобрен FDA в 2015 г. в качестве системной терапии местнораспространенного БРК [35]. Недавнее исследование местного применения препарата сонидегибон у 8 пациентов с невоидным БРК выявило 3 (23,1%) полных ответа, 9 (69,2%) частичных ответов и 1 (7,7%) отсутствие ответа, что свидетельствует о необходимости проведения дальнейших исследований [36]. Однако необходимо учитывать переносимость сонидегиба, поскольку лечение часто ограничено из-за увеличения выраженности побочных эффектов, наименее переносимые из которых включают мышечные спазмы, алопецию и дисгевзию [37].
В дополнение к новым препаратам местного применения, таким как HhI (сонидегиб), системные ингибиторы иммунных контрольных точек также предлагают неинвазивные методы лечения пожилых пациентов с НМРК, особенно когда хирургическое вмешательство невозможно [30]. Цемиплимаб, одобренное FDA антитело против PD-1 [38], продемонстрировало 50% (13/26) ответов при метастатическом ПРК в исследовании I фазы и 47,5% (28/59) ответов в исследовании
II фазы при распространенном ПРК [39].
В ходе исследования I фазы таладегиб, низкомолекулярный антагонист сглаженного рецептора клеточной поверхности лиганда Hedgehog (SMO), выявил 68,8% отклик у пациентов, которые ранее не получали HhI, и 35,5% отклик у тех, кто получал HhI [40]. Эти результаты позволяют предположить, что таладегиб может обладать лучшей фармакокинетикой и фармакодинамикой по сравнению с висмодегибом. Висмодегиб является антагонистом SMO, одобренным FDA в 2012 г., но его применение ограничено проблемами, связанными с резистентностью к лечению и переносимостью [41, 42].
Внутриочаговая терапия. Внутриочаговая терапия с использованием 5-ФУ представляет собой недорогой, эффективный и неинвазивный метод лечения пациентов с НМРК с множественными сопутствующими заболеваниями, которые могут ограничивать хирургическое лечение [43]. Метаанализ показал, что 5-ФУ обеспечивает более высокие показатели излечения НМРК, включая БРК и ПРК, по сравнению с другими препаратами для внутриочаговой терапии, такими как интерферон и интерлейкин-2 [44]. Более поздние исследования показывают, что более низкие дозы 5-ФУ для внутриочагового введения могут служить многообещающим средством снижения кумулятивной дозы и дозозависимых побочных реакций при сохранении клинической эффективности, о чем свидетельствует частота ответа в 96% (48/50) случаев при терапии ПРК и кератоакантиомы [45].
Лучевая терапия. Лучевая терапия (ЛТ) играет важную роль в лечении НМРК, особенно для пожилых пациентов с множественными сопутствующими заболеваниями, у которых проведение хирургического вмешательства может быть опасным [46]. Одним из заметных нововведений является появление контактной гипофракционированной ЛТ, которая обеспечивает значительный контроль над целевыми поражениями при выраженном сокращении количества необходимых сеансов лечения [47]. Это не только повышает удобство проводимой терапии, но и сводит к минимуму общее негативное влияние на качество жизни пациентов, что является важным фактором при ведении НМРК в пожилом возрасте [48].
Методы интервенционной радиологии, примером которых является брахитерапия, представляют собой еще одно важное достижение [47]. Брахитерапия позволяет точно доставлять излучение непосредственно к опухоли, сохраняя при этом окружающие здоровые ткани, что не только сводит к минимуму сопутствующий ущерб прилегающим структурам, но и помогает сохранить важнейшие функции, которые часто нарушаются в пожилом возрасте [49].
Комбинация ЛТ с таргетной терапией (висмодегиб) также показала обнадеживающие результаты [50, 51]. Подобный синергетический подход обладает высоким потенциалом для улучшения реакции и контроля заболевания, особенно у пожилых людей [52]. В настоящее время в двух исследованиях 2-й фазы изучается возможность одновременного применения висмодегиба и ЛТ, что определяет эффективность комбинированного подхода для пациентов с запущенным БРК, которым не рекомендовано проведение хирургического вмешательства (ClinicalTrials.gov Идентификаторы NCT02956889 и NCT01835626).
Кроме того, лучевая терапия с визуальным контролем (ЛТВК) стала прорывным методом лечения в амбулаторных условиях, особенно при раннем НМРК [53]. Эта высокоразвитая технология улучшает доставку излучения в поверхностные слои кожи и позволяет визуализировать конфигурацию и глубину опухоли на протяжении всего лечения, обеспечивая беспрецедентный уровень точности при воздействии на очаги поражения и обеспечивая превосходный косметический эффект [54]. ЛТВК обеспечивает максимальную эффективность лечения и сводит к минимуму патогенное воздействие на окружающие здоровые ткани, снижая вероятность побочных эффектов [54].
Лазерная терапия. Абляционные лазеры, такие как CO2 и эрбиевый лазер (Er: YAG), функционируют путем испарения тканевой воды, эффективно устраняя опухоли [56]. Напротив, неабляционные лазеры, включая импульсные лазеры на красителях (PDL) и Nd:YAG-лазеры, нацелены на сосудистую сеть опухоли, сохраняя при этом окружающие ткани [55]. Однако отсутствие стандартизированных протоколов лечения или лазерных установок для лечения НМРК представляет собой актуальную проблему в этой области [55]. Недавний систематический обзор и метаанализ лазерного лечения НМРК продемонстрировал, что Nd:YAG-лазер является безопасным и эффективным методом лечения БРК с низким риском, частота рецидивов которого составляет всего 3,1% [56]. С другой стороны, CO2-лазер был признан менее эффективным, чем Nd:YAG-лазер, с частотой рецидивов до 9,4%, и поэтому не рекомендовался для лечения БРК [56]. Кроме того, абляционные лазеры потенциально увеличивают время заживления, остаточную опухолевую нагрузку или рецидивы, которые могут быть не так легко визуализированы в рубцовой ткани по сравнению с неабляционным лечением [57].
Было обнаружено, что интенсивная фотодинамическая терапия (иФДТ) в сочетании с фракционной абляцией CO2-лазером сокращает время, необходимое для проникновения фотосенсибилизатора в очаг поражения [58, 59]. Таким образом, иФДТ увеличивает поглощение фотосенсибилизатора и может повысить терапевтическую эффективность. Недавние исследования продемонстрировали более высокую отдаленную эффективность (6 мес) лечения НМРК при применении иФДТ и абляции по сравнению с изолированной ФДТ [58, 59].
В исследовании, опубликованном в 2019 г., оценивалось комбинированное лечение с использованием PDL с длиной волны 595 нм и фракционного лазера с длиной волны 1927 нм для лечения 93 пациентов с БРК. По результатам исследования была продемонстрирована высокая эффективность лечения в 95,7% (89/93) случаев и в 4,5% (4/89) отмечался рецидив [55]. В более крупном ретроспективном когортном исследовании оценивалась эффективность PDL (595 нм) в терапии НМРК у пожилых людей путем оценки 121 пациента с локализацией опухоли на руках [59]. Частота рецидивов во всех случаях ПРК составила 9,6%, при отсутствии рецидивов у пациентов с БРК, что позволяет эффективно проводить серию PDL-процедур для лечения НМРК на коже рук пожилых пациентов [59].
Эти последние достижения в области лазерной терапии НМРК у пожилых людей подчеркивают постоянные усилия по совершенствованию и расширению возможностей, доступных этой категории пациентов. Сочетая точность, минимально инвазивные методы и усовершенствованный мониторинг, лазерная терапия становится все более привлекательным выбором лечения пожилых пациентов с НМРК, способствуя получению эффективных результатов лечения и улучшению качества жизни.
Хирургическое вмешательство обеспечивает высокие показатели излечения и точный контроль за удалением опухоли, но решение о проведении хирургического вмешательства должно приниматься с учетом общего состояния здоровья пациента, характеристик опухоли и косметических результатов. Местная терапия и лучевая терапия не являются инвазивными альтернативами, но пациенты и медицинские работники должны тщательно оценивать их пригодность в зависимости от типа и локализации опухолевого поражения. При принятии решения также необходимо учитывать возможные осложнения и долгосрочные косметические результаты. Влияние лечения на качество жизни пожилого пациента является важнейшим фактором. Хирургические вмешательства могут привести к длительному периоду восстановления и возможному образованию рубцов, что может быть менее приемлемо для пожилых людей. И наоборот, местное лечение и лучевая терапия могут обеспечить более быстрое выздоровление и более благоприятные косметические результаты, но, возможно, увеличить число посещений амбулатории. Эти соображения подчеркивают необходимость разработки индивидуальных планов лечения, учитывающих уникальные потребности и предпочтения пожилых пациентов с НМРК.
Использование инструментов, учитывающих сопутствующие заболевания наряду с возрастом, является распространенным подходом к оценке ограниченной продолжительности жизни (LLE – Limited Life Expectancy) пациентов. Для этой цели часто используется индекс коморбидности Чарльсона (CCI) [62, 63]. Однако не существует установленных рекомендаций по оценке CCI, которые могли бы дать окончательный прогноз. Исследования различались в определении LLE, в некоторых исследованиях использовались оценки CCI 3+, основанные на 44% смертности за 2 года, в то время как другие предполагают оценку CCI 7+ с вероятностью смертности менее 40% через 2 года [62–64]. Отсутствие надежности в этом показателе подчеркивает необходимость учета факторов, не связанных с сопутствующими заболеваниями при выборе лечения НМРК у пожилых людей.
Оценка функциональных возможностей пациента может помочь определить степень агрессивности лечения НМРК. Шкала функционального состояния Карнофски (KPS) является надежной и позволяет сбалансировать нагрузку на системные заболевания и возможности пациента в повседневной деятельности. Учитывая полезность функциональной оценки как показателя общего состояния здоровья пациента и предиктора выживаемости в пожилом возрасте, рекомендуется включать KPS в процесс принятия решений о лечении для всех пациентов [65, 66]. Это особенно актуально при рассмотрении менее инвазивного метода лечения для пациента
с плохим функциональным состоянием, даже если опухоль соответствует AUC [67].
Физические последствия рака и его лечения у пожилых людей могут быть значительными и часто усугубляются возрастными особенностями. Риск развития осложнений, более длительное время восстановления и влияние на повседневную деятельность являются важными факторами при принятии решения об интенсивности проводимого лечения [30]. Кровотечение из опухоли является распространенным осложнением, которое может побудить врача удалять новообразование, а не прибегать к паллиативным мерам. Локализацию и размер опухоли также следует рассматривать как патологический фактор, поскольку большие очаги могут привести к обезображиванию, в то время как при определенных методах лечения шрамы могут быть сопоставимы с опухолевым поражением [30].
Эмоциональные и психологические аспекты лечения НМРК имеют первостепенное значение, поскольку многочисленные психологические проблемы пожилых людей влияют на их способность переносить операции на коже. Эти проблемы включают снижение когнитивных способностей, ухудшение памяти, влияющее на комплаенс в процессе лечения, эмоциональную неустойчивость и повышенную тревогу по поводу увечий, боли, неизвестности, зависимости от других или смерти, что создает различные психологические и когнитивные ограничения [68]. Таким образом, особое внимание к когнитивным и физиологическим ограничениям пациентов может свести к минимуму периоперационный риск во время операций на коже у пожилых людей [68].
Врачи также должны учитывать социальные аспекты лечения пожилых людей. Необходимость интенсивного лечения, включая поездки для проведения многочисленных хирургических вмешательств или интенсивной ЛТ, может нарушить их повседневную жизнь и вызвать дополнительный стресс как у пациентов, так и у родственников. Кроме того, финансовые аспекты лечения могут вызывать серьезные опасения у пожилых пациентов.
Врачи должны учитывать важную роль скрининга на рак кожи у пожилых людей. Тотальное обследование кожи тела (TBSE – Total Body Skin Examination) относится к систематическому обследованию кожи пациента, ногтей, волос и соответствующих поверхностей слизистых оболочек с целью выявления единичных случаев новообразований кожи, которые пациент, возможно, не в состоянии увидеть, что способствует более раннему выявлению рака [6]. Однако результаты скрининга населения в целом с использованием TBSE остаются спорными [69], а рутинное использование TBSE дерматологами варьируется [70]. В прошлом году Целевая группа по профилактическим услугам США пришла к выводу, что имеющихся данных недостаточно для оценки баланса пользы и вреда визуального осмотра кожи врачом для выявления рака кожи у подростков и взрослых [71]. Таким образом, врачи должны использовать клиническую оценку при определении полезности TBSE у пожилых пациентов, особенно в связи с растущим использованием теледерматологических методов, где TBSE в значительной степени исключен [72].
Учитывая вышеописанные факторы, паллиативная помощь может обеспечить более сбалансированный подход, который в определенных случаях соответствует общему качеству жизни пациента. Исследования демонстрируют спорные мнения о целесообразности использования медицинских процедур и методов лечения в конце жизни и утверждают, что преимущества скрининга и лечения не всегда могут перевешивать потенциальные риски, поскольку пациенты могут прожить недостаточно долго, чтобы получить пользу, а последующие осложнения лечения могут снизить качество жизни [73, 74]. В конечном счете, врачам необходимо учитывать общее состояние здоровья пациента, ожидаемую продолжительность жизни и личные предпочтения, сбалансированные с физическими, эмоциональными и социальными последствиями рака, при определении надлежащего курса лечения.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Источник финансирования. Авторы заявляют об отсутствии внешнего финансирования при проведении исследования. Исследование выполнено в рамках межвузовского взаимодействия по научному кружку «Дерматопатология».
Funding source. This study was not supported by any external sources of funding. The study was carried out within the framework of interuniversity cooperation in the scientific community «Dermatopathology».
Вклад авторов. Авторы подтверждают соответствие своего авторства международным критериям ICMJE (все авторы внесли существенный вклад в разработку концепции, проведение исследования и подготовку статьи, прочли и одобрили финальную версию перед публикацией). Наибольший вклад распределен следующим образом: А.А. Пирожникова, М.В. Стецюк, К.А. Кудревич, О.В. Немирова – концепция исследования, согласование финальной версии рукописи; Э.Э. Абдурахманова, А.И. Умерова, Э.Г. Тамасян, Д.Ю. Ковали, К.А. Товмасян, В.А. Филипова, А.А. Диарова, А.А. Багдасарян, Х-А. А. Шадиев – обзор литературы, анализ данных, написание текста статьи.
Author contribution. The authors confirm that their authorship meets the international ICMJE criteria (all authors have made a significant contribution to the development of the concept, research and preparation of the article, read and approved the final version before publication). The greatest contribution is distributed as follows: A.A. Pirozhnikova, M.V. Stetsyuk, K.A. Kudrevich, O.V. Nemirova – the concept of research, coordination of the final version of the manuscript; E.E. Abdurakhmanova, A.I. Umerova, E.G. Tamasyan, D.Y. Kovali, K.A. Tovmasyan, V.A. Filipova, A.A. Diarova, A.A. Bagdasaryan, Kh-A.A. Shadiev ― literature review, data analysis, writing the text of the article.
Информация об авторах
Information about the authors
Пирожникова Александра Алексеевна – ординатор, ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова». E-mail: vkomissiya@inbox.ru; ORCID: 0009-0004-5294-1360
Aleksandra A. Pirozhnikova – Resident, Mechnikov North-Western State Medical University. E-mail: vkomissiya@inbox.ru; ORCID: 0009-0004-5294-1360
Стецюк Максим Валерьевич – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: m2002.like@yandex.ru; ORCID: 0009-0002-0725-8867
Maksim V. Stetsyuk – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: m2002.like@yandex.ru; ORCID: 0009-0002-0725-8867
Кудревич Ксения Антоновна – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: ksukud25@gmail.com; ORCID: 0009-0003-3435-7059
Kseniya A. Kudrevich – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: ksukud25@gmail.com; ORCID: 0009-0003-3435-7059
Абдурахманова Эмине Энверовна – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: abdurakhmanovaemine1@gmail.com; ORCID: 0009-0009-5674-7772
Emine E. Abdurakhmanova – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: abdurakhmanovaemine1@ gmail.com; ORCID: 0009-0009-5674-7772
Умерова Амина Ильдаровна – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: aminaumerova2310@gmail.com; ORCID: 0009-0009-5750-9258
Amina I. Umerova – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: aminaumerova2310@gmail.com; ORCID: 0009-0009-5750-9258
Тамасян Эдгар Гарегинович – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: ed_tamasyan12.04@icloud.com; ORCID: 0009-0004-9608-0187
Edgar G. Tamasyan – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: ed_tamasyan12.04@icloud.com;
ORCID: 0009-0004-9608-0187
Ковали Диляра Юсуф къызы – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: dilyara_kovali@mail.ru; ORCID: 0009-0009-4692-7382
Dilyara Yu. Kovali – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: dilyara_kovali@mail.ru; ORCID: 0009-0009-4692-7382
Товмасян Корюн Арманович – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: koryun_t228@icloud.com; ORCID: 0009-0009-7199-7358
Koryun A. Tovmasyan – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: koryun_t228@icloud.com; ORCID: 0009-0009-7199-7358
Филипова Вероника Андреевна – студент, ФГБОУ ВО БГМУ. E-mail: verofilipova@yandex.ru; ORCID: 0009-0006-7758-2151
Veronika A. Filipova – Student, Bashkir State Medical University. E-mail: verofilipova@yandex.ru; ORCID: 0009-0006-7758-2151
Диарова Алия Амировна – студент, ФГБОУ ВО БГМУ. E-mail: diarovaalia@yandex.ru; ORCID: 0009-0007-1120-7292
Aliya A. Diarova – Student, Bashkir State Medical University.
E-mail: diarovaalia@yandex.ru; ORCID: 0009-0007-1120-7292
Немирова Ольга Владимировна – зав. медицинским кабинетом, врач, АНО ВО МГЭУ. E-mail: olga605794@yandex.ru; ORCID: 0009-0006-3565-4751
Olga V. Nemirova – Head of the Medical Office, Doctor, Moscow University of Humanities and Economics. E-mail: olga605794@yandex.ru; ORCID: 0009-0006-3565-4751
Багдасарян Аскина Аркадьевна – студент, ФГБОУ ВО «Ростовский ГМУ». E-mail: Verner.liza@bk.ru; ORCID: 0009-0006-7712-7888
Askina A. Bagdasaryan – Student, Rostov State Medical University. E-mail: Verner.liza@bk.ru; ORCID: 0009-0006-7712-7888
Шадиев Хож-Ахмед Аптиевич – студент, ФГБОУ ВО «Астраханский ГМУ». E-mail: shadiev8999@gmail.com; ORCID: 0009-0003-5290-7704
Khozh-Akhmed A. Shadiev – Student, Astrakhan State Medical University. E-mail: shadiev8999@gmail.com; ORCID: 0009-0003-5290-7704
Поступила в редакцию: 12.11.2024
Поступила после рецензирования: 19.11.2024
Принята к публикации: 21.11.2024
Received: 12.11.2024
Revised: 19.11.2024
Accepted: 21.11.2024
The current state of the issue of diagnosis and treatment of non-melanoma skin cancer in elderly patients
Aleksandra A. Pirozhnikova1, Maksim V. Stetsyuk2, Kseniya A. Kudrevich2,Emine E. Abdurakhmanova2, Amina I. Umerova2, Edgar G. Tamasyan2, Dilyara Yu. Kovali2,
Koryun A. Tovmasyan2, Veronika A. Filipova3, Aliya A. Diarova3, Olga V. Nemirova4,
Askina A. Bagdasaryan5, Khozh-Akhmed A. Shadiev6
1 Mechnikov North-Western State Medical University, Saint Petersburg, Russia;
2 Georgievsky Order of the Red Banner Medical Institute, Simferopol, Russia;
3 Bashkir State Medical University, Ufa, Russia;
4 Moscow University of Humanities and Economics, Moscow, Russia;
5 Rostov State Medical University, Rostov-on-Don, Russia;
6 Astrakhan State Medical University, Astrakhan, Russia
vkomissiya@inbox.ru
Abstract
Introduction. Old age is a significant risk factor for all types of skin cancer. Non-melanoma skin cancer (NSCLC) is the most commonly diagnosed type of cancer worldwide and especially affects the elderly. In 2019, in the Russian Federation, NSCLC accounted for 10.6% of the total number of oncological diseases in men and 15.2% in women. During the same period, there was an increase in the incidence: by 7.9% in men and by 17.9% in women. The average age of patients with this disease was 69.7 years.
Aim. to analyze the literature on the prevalence of NSCLC among the elderly, the unique problems faced by patients, as well as recent advances in treatment.
Materials and methods. Research papers were searched in the databases eLibrary, PubMed and Google Scholar until September 2024. The selection of publications was carried out according to the recommendations of PRISMA. 78 studies were included in the review.
Results. The review highlights the importance of adapted approaches to the treatment of NSCLC in the elderly. Given the increasing prevalence of NSCLC in older people, meeting their special needs and concerns is of paramount importance. Ongoing research in this area can improve treatment outcomes and improve the quality of life of elderly patients with NSCLC. The future of geriatric dermatology is likely to depend on these advances providing a more complete understanding of treatments for NSCLC in the elderly.
Conclusion. As the field of dermatology continues to evolve, an individual approach to the treatment of NSCLC in the elderly will be crucial. Active collaboration between healthcare professionals, patients and their families is essential for making informed treatment decisions. Further research is needed to clarify the recommendations and treatment strategies for older people, with a particular focus on optimizing therapeutic outcomes while minimizing the physical, emotional and social impact of NSCLC and its treatment.
Keywords: non-melanoma skin cancer, squamous cell skin cancer, basal cell skin cancer, elderly, treatment, diagnosis, skin.
For citation: Pirozhnikova A.A., Stetsyuk M.V., Kudrevich K.A., Abdurakhmanova E.E., Umerova A.I., Tamasyan E.G., Kovali D.Yu.,
Tovmasyan K.A., Filipova V.A., Diarova A.A., Nemirova O.V., Bagdasaryan A.A., Shadiev Kh.-A.A. The current state of the issue of diagnosis and treatment of non-melanoma skin cancer in elderly patients. Clinical review for general practice. 2024; 5 (12): 56–66 (In Russ.).
DOI: 10.47407/kr2024.5.12.00538
Введение
Пожилой возраст является существенным фактором риска для всех видов рака кожи [1]. Немеланомный рак кожи (НМРК) является наиболее часто диагностируемым видом рака во всем мире и особенно часто поражает пожилых людей [2, 3]. В 2019 г. в Российской Федерации НМРК составлял 10,6% от общего числа онкологических заболеваний у мужчин и 15,2% у женщин. За тот же период отмечался рост заболеваемости: на 7,9% у мужчин и на 17,9% у женщин. Средний возраст пациентов с данным заболеванием составил 69,7 года. Уровень смертности (для обоих полов) составил 1,03 на 100 тыс. населения, а стандартизованный показатель – 0,46 на 100 тыс. населения (0,33 у женщин и 0,75 у мужчин) [4]. В США базальноклеточный рак кожи (БРК) составляет 50% всех онкологических заболеваний [5]. НМРК охватывает целый ряд злокачественных новообразований, включая БРК, плоскоклеточный рак (ПРК), карциному Меркеля, ангиосаркому, рак сальных желез, и выбухающую дерматофибросаркому (англ. Dermatofibrosarcoma protuberans – DFSP). Эти заболевания в основном затрагивают пожилых людей, что требует сосредоточения внимания на разработке индивидуальных стратегий лечения для этой демографической группы.Цель обзора – проанализировать литературу, посвященную распространенности НМРК среди пожилых людей, уникальным проблемам, с которыми сталкиваются пациенты, а также последние достижения в области лечения.
 Методология поиска исследований
Методология поиска исследованийПоиск научных работ проводился в базах данных ELibrary, PubMed и Google Scholar до сентября 2024 г. Отбор публикаций осуществлялся согласно рекомендациям PRISMA. Все авторы независимо друг от друга занимались поиском публикаций, а в случае возникновения разногласий принимали решение путем консенсуса. Для поиска использовались следующие ключевые слова и их сочетания на русском и английском языках: «немеланомный рак кожи», «плоскоклеточный рак кожи», «базальноклеточный рак кожи», «пожилые», «лечение», «диагностика», «кожа», non-melanoma skin cancer, squamous cell skin cancer, basal cell skin cancer, elderly, treatment, diagnosis, skin. В результате поиска было выявлено 10 523 статьи. На этапе скрининга проводилась оценка приемлемости исследований по следующим критериям включения:
• исследование опубликовано на русском или английском языке;
• исследование опубликовано в рецензируемом научном издании;
• исследование является обзором литературы, описанием клинического случая или оригинальным исследованием с участием людей и описывающим проблемы диагностики и лечения НМРК у пожилых людей.
В итоге в обзор были включены 78 исследований. Блок-схема PRISMA с подробным алгоритмом поиска исследований представлена на рисунке.
Результаты и обсуждение
Эпидемиология и распространенность НМРК у пожилых людейВозраст, бесспорно, является основным фактором риска развития рака кожи, и поскольку ожидаемая продолжительность жизни возросла, число случаев рака кожи будет увеличиваться, если не будут предприняты дополнительные усилия по профилактике [3]. Заболеваемость НМРК ежегодно растет, и сегодня рак кожи является наиболее часто диагностируемым злокачественным новообразованием в развитых странах [6, 7]. НМРК чаще встречается среди пожилого населения, причем увеличение заболеваемости прямо коррелирует с возрастом. Риск развития НМРК заметно повышается после 50 лет, причем наиболее подвержены ему пожилые люди, особенно в возрасте 70 лет и старше [8]. БРК является наиболее распространенным из них, за ним следует ПРК [2].
В дополнение к генетическим факторам риска и иммуносупрессии такие факторы окружающей среды как длительное воздействие ультрафиолетовых (УФ) лучей, ионизирующее излучение и канцерогены играют значимую роль в развитии НМРК [9]. Географическое положение также играет важную роль, так некоторые регионы характеризуются более высокими уровнями УФ-излучения, что приводит к увеличению показателей заболеваемости НМРК [10]. Такие факторы, как бледность кожи, солнечные ожоги в анамнезе и возрастные изменения кожи, включая уменьшение толщины дермы, снижение васкуляризации и нарушение иммунных реакций, еще больше усугубляют эту уязвимость [11]. Более того, иммуносупрессивные состояния и некоторые медикаментозные препараты, которые часто более распространены среди пожилых людей из-за сопутствующих возрастных заболеваний, подвергают их повышенному риску развития НМРК [12].
Клинические проявления НМРК у пожилых людей
НМРК проявляется в различных формах, каждая из которых имеет уникальные клинические характеристики [3]. БРК, наиболее распространенная форма, обычно появляется на открытых участках тела, таких как лицо и шея, в виде жемчужных узелков или язвенных поражений [3]. Пигментированный БРК, клинический и гистологический вариант БРК, который чаще встречается у пациентов с более темным типом кожи, может напоминать меланому с синими или черными пигментированными папулами или узелками [11]. ПРК часто проявляется в виде чешуйчатых, покрытых коркой бляшек или узлов и обычно локализуется на голове и шее [3]. Карцинома Меркеля представляет собой твердые, безболезненные, быстро растущие узлы, обычно на голове, шее или конечностях, и характеризуется своей агрессивной природой [13]. Ангиосаркома часто проявляется в виде пурпурных или красноватых пятен, обычно обнаруживаемых на голове и шее, и, как правило, имеет более агрессивное течение у пожилых людей [14]. Рак кожи из сальных желез обычно проявляется в виде безболезненного, твердого желтоватого узелка на веке или в других периокулярных областях [15]. DFSP, редкий подтип НМРК, характеризуется медленно растущими узелками от телесного до красновато-коричневого цвета, чаще всего встречающимися на туловище [16].Диагностические трудности
Диагностика НМРК у пожилых людей представляет собой многогранную проблему. Возрастные изменения кожи, такие как снижение эластичности и истончение, могут сделать поражения менее заметными, что затрудняет их обнаружение [11]. Кроме того, пожилые люди часто имеют сопутствующие патологии, включая сердечно-сосудистые заболевания, сахарный диабет и иммуносупрессию, которые могут влиять на клиническую картину НМРК или ограничивать доступ пациентов к специализированной медицинской помощи [17, 18].Варианты лечения НМРК с учетом возрастных особенностей
При выборе метода лечения НМРК у пожилых пациентов необходимо учитывать возраст пациента, сопутствующие заболевания и локализацию поражения.В следующих разделах рассматриваются хирургические и неинвазивные методы лечения НМРК, а также положительные и отрицательные моменты применения каждого терапевтического подхода в пожилом возрасте.
Хирургические варианты лечения: Микрографическая хирургия по методу Мооса или хирургическое иссечение. Выбор между микрграфической хирургией по Моосу (МХМ) и широким иссечением (ШИ) при первичном лечении НМРК зависит от таких факторов, как локализация, размер и тип опухоли. МХМ, признанный золотым стандартом, обеспечивает эффективное удаление опухоли и позволяет максимально сохранить близлежащие здоровые ткани [19]. Этот метод включает тщательное обследование удаленных тканей, что позволяет точно определить наличие опухолевых клеток и их расположение. Если в процессе анализа выявляются опухолевые клетки на краях резекции, это указывает на необходимость повторных вмешательств для полного удаления новообразования. Таким образом, повторная локальная эксцизия тканей продолжается до тех пор, пока края резекции не станут отрицательными, что является критически важным для снижения риска рецидива и увеличения шансов на успешный исход лечения. Кроме того, такой подход способствует снижению травматичности и улучшает косметический результат, что особенно важно для пациентов [19]. Критерии надлежащего применения (англ. Appropriate Use Criteria, AUC), разработанные Американской академией дерматологии, помогают определить приемлемость МХМ на основе клинических, патологических и индивидуальных критериев пациента [17]. Разработанное приложение «Mohs Surgery AUC» также может предоставить подробные рекомендации по надлежащей интерпретации критериев в режиме реального времени во время осмотра пациента.
ШИ включает в себя иссечение краев вокруг опухоли с гистологическим исследованием путем выполнения параллельных разрезов (техника «нарезка хлеба») [20]. Оптимальные границы ШИ остаются неопределенными, но данные свидетельствуют о том, что иссечение 4 мм от края опухоли обеспечивают приемлемые результаты для всех случаев ПРК, за исключением опухолей высокого риска (т.е. тех, которые проникают в подкожную клетчатку более глубоко), при которых рекомендуется иссекать 6 мм [21]. Идеальным хирургическим методом лечения БРК диаметром менее 2 см является полное иссечение 3–4 мм здоровой кожи вокруг опухоли [22]. Для поражений диаметром более 2 см или в группе высокого риска может быть достаточно иссечения 5 мм для достижения четких результатов, в то время как для рецидивирующих поражений рекомендуется иссекать 6 мм или проведение МХМ [22].
Рентабельное и экономичное по времени ШИ является хорошим методом лечения НМРК, однако тщательный контроль заживления ран имеет решающее значение у пожилых людей, учитывая возрастные физиологические изменения, влияющие на этот процесс [23]. Врачи должны учитывать эти соображения, поскольку нарушение процесса заживления ран может привести к таким осложнениям, как расхождение швов или инфицирование [23]. Кроме того, потенциальная потребность в реконструктивной хирургии у пожилых людей требует оценки оптимальных косметических и функциональных результатов [23].
Последние научно обоснованные рекомендации подчеркивают эффективность как МХМ, так и ШИ для лечения первичного БРК, при этом МХМ демонстрирует значительно более низкую частоту рецидивов при 5- и 10-летнем наблюдении по сравнению с ШИ при локализации опухоли на лице [19, 24]. МХМ также продемонстрировала более благоприятные показатели по сравнению с ШИ для лечения ПРК, с локальными 5-летними показателями рецидива 1,2–2,6% [25] по сравнению с 5,7–8,1% соответственно [26].
Электродиссекация и кюретаж (ЭДК) – это деструктивная процедура, которая предлагает альтернативу ШИ и МХМ для лечения НМРК с низким уровнем риска. Она обычно используется при поверхностных или узловых БРК и ПРК in situ (ПРК-IS), когда опухоль хорошо выражена и неглубока [27]. Используя кюретку для удаления злокачественной ткани путем санации (из-за плохой межклеточной адгезии, проявляемой раковыми клетками) с последующей электрокоагуляцией, врач может удалить опухоль менее инвазивным способом по сравнению с хирургическим иссечением [27]. Несмотря на то что показатели излечения за 5 лет у пациентов, перенесших ЭДК, составляют 91–99%, гистологическая оценка краев невозможна, учитывая разрушительный характер процедуры, и, как следствие, как пациенты, так и лечащий врач должны уделять пристальное внимание на предмет признаков рецидива [28].
Неинвазивные методы лечения НМРК: местная терапия, системная терапия, внутриочаговая терапия, лучевая терапия, лазерная терапия
Местная терапия. Местные методы лечения предоставляют консервативные альтернативы для отдельных случаев НМРК, включая поверхностные поражения, а разработка новых препаратов предлагает многообещающие перспективы пациентам с поздней стадией заболевания. Местные препараты, такие как 5-фторурацил (5-ФУ), 5-ФУ плюс кальципотриен и имиквимод, служат неинвазивным методом лечения локализованных подтипов НМРК с низким уровнем риска [29].Преимущества таких методов лечения заключаются в том, что они не требуют проведения хирургической процедуры и минимизируют образование рубцов, в то время как недостатки заключаются в том, что местные препараты могут быть дорогостоящими и использоваться только для лечения поверхностных поражений, а также такое лечение характеризуется более высокой частотой рецидивов [30]. Результаты лечения варьируются в зависимости от различных местных методов лечения: сообщается, что в 94,9% случаев ПРК-IS рецидив после лечения 5-ФУ не наблюдался [31], а частота излечения ПРК-IS после местного лечения имиквимодом составляет 73–86% [32]. В недавнем всеобъемлющем обзоре нехирургических методов лечения БРК сообщалось, что долгосрочная эффективность (> 3 лет без рецидива) местного лечения имиквимодом составляет 75–87%, а краткосрочная эффективность (<1 года без рецидива) при местном лечении 5-ФУ – 90–93%, но при этом отдаленная частота рецидивов составляет 21% [33]. Необходимы дополнительные исследования для дальнейшей характеристики и сравнения показателей излечения и рецидивов наиболее эффективных местных методов лечения.
Системная терапия. Несмотря на то что МХМ остается золотым стандартом инвазивного лечения НМРК, начиная с 2018 г. исследования расширили возможности неинвазивных методов лечения. Некоторые из стратегий неинвазивного лечения подразумевали использование совершенно новых препаратов, в то время как другие подразумевали использование уже известных препаратов, которые применялись для лечения других заболеваний [34]. Сонидегиб, ингибитор пути hedgehog (HhI), был одобрен FDA в 2015 г. в качестве системной терапии местнораспространенного БРК [35]. Недавнее исследование местного применения препарата сонидегибон у 8 пациентов с невоидным БРК выявило 3 (23,1%) полных ответа, 9 (69,2%) частичных ответов и 1 (7,7%) отсутствие ответа, что свидетельствует о необходимости проведения дальнейших исследований [36]. Однако необходимо учитывать переносимость сонидегиба, поскольку лечение часто ограничено из-за увеличения выраженности побочных эффектов, наименее переносимые из которых включают мышечные спазмы, алопецию и дисгевзию [37].
В дополнение к новым препаратам местного применения, таким как HhI (сонидегиб), системные ингибиторы иммунных контрольных точек также предлагают неинвазивные методы лечения пожилых пациентов с НМРК, особенно когда хирургическое вмешательство невозможно [30]. Цемиплимаб, одобренное FDA антитело против PD-1 [38], продемонстрировало 50% (13/26) ответов при метастатическом ПРК в исследовании I фазы и 47,5% (28/59) ответов в исследовании
II фазы при распространенном ПРК [39].
В ходе исследования I фазы таладегиб, низкомолекулярный антагонист сглаженного рецептора клеточной поверхности лиганда Hedgehog (SMO), выявил 68,8% отклик у пациентов, которые ранее не получали HhI, и 35,5% отклик у тех, кто получал HhI [40]. Эти результаты позволяют предположить, что таладегиб может обладать лучшей фармакокинетикой и фармакодинамикой по сравнению с висмодегибом. Висмодегиб является антагонистом SMO, одобренным FDA в 2012 г., но его применение ограничено проблемами, связанными с резистентностью к лечению и переносимостью [41, 42].
Внутриочаговая терапия. Внутриочаговая терапия с использованием 5-ФУ представляет собой недорогой, эффективный и неинвазивный метод лечения пациентов с НМРК с множественными сопутствующими заболеваниями, которые могут ограничивать хирургическое лечение [43]. Метаанализ показал, что 5-ФУ обеспечивает более высокие показатели излечения НМРК, включая БРК и ПРК, по сравнению с другими препаратами для внутриочаговой терапии, такими как интерферон и интерлейкин-2 [44]. Более поздние исследования показывают, что более низкие дозы 5-ФУ для внутриочагового введения могут служить многообещающим средством снижения кумулятивной дозы и дозозависимых побочных реакций при сохранении клинической эффективности, о чем свидетельствует частота ответа в 96% (48/50) случаев при терапии ПРК и кератоакантиомы [45].
Лучевая терапия. Лучевая терапия (ЛТ) играет важную роль в лечении НМРК, особенно для пожилых пациентов с множественными сопутствующими заболеваниями, у которых проведение хирургического вмешательства может быть опасным [46]. Одним из заметных нововведений является появление контактной гипофракционированной ЛТ, которая обеспечивает значительный контроль над целевыми поражениями при выраженном сокращении количества необходимых сеансов лечения [47]. Это не только повышает удобство проводимой терапии, но и сводит к минимуму общее негативное влияние на качество жизни пациентов, что является важным фактором при ведении НМРК в пожилом возрасте [48].
Методы интервенционной радиологии, примером которых является брахитерапия, представляют собой еще одно важное достижение [47]. Брахитерапия позволяет точно доставлять излучение непосредственно к опухоли, сохраняя при этом окружающие здоровые ткани, что не только сводит к минимуму сопутствующий ущерб прилегающим структурам, но и помогает сохранить важнейшие функции, которые часто нарушаются в пожилом возрасте [49].
Комбинация ЛТ с таргетной терапией (висмодегиб) также показала обнадеживающие результаты [50, 51]. Подобный синергетический подход обладает высоким потенциалом для улучшения реакции и контроля заболевания, особенно у пожилых людей [52]. В настоящее время в двух исследованиях 2-й фазы изучается возможность одновременного применения висмодегиба и ЛТ, что определяет эффективность комбинированного подхода для пациентов с запущенным БРК, которым не рекомендовано проведение хирургического вмешательства (ClinicalTrials.gov Идентификаторы NCT02956889 и NCT01835626).
Кроме того, лучевая терапия с визуальным контролем (ЛТВК) стала прорывным методом лечения в амбулаторных условиях, особенно при раннем НМРК [53]. Эта высокоразвитая технология улучшает доставку излучения в поверхностные слои кожи и позволяет визуализировать конфигурацию и глубину опухоли на протяжении всего лечения, обеспечивая беспрецедентный уровень точности при воздействии на очаги поражения и обеспечивая превосходный косметический эффект [54]. ЛТВК обеспечивает максимальную эффективность лечения и сводит к минимуму патогенное воздействие на окружающие здоровые ткани, снижая вероятность побочных эффектов [54].
Лазерная терапия. Абляционные лазеры, такие как CO2 и эрбиевый лазер (Er: YAG), функционируют путем испарения тканевой воды, эффективно устраняя опухоли [56]. Напротив, неабляционные лазеры, включая импульсные лазеры на красителях (PDL) и Nd:YAG-лазеры, нацелены на сосудистую сеть опухоли, сохраняя при этом окружающие ткани [55]. Однако отсутствие стандартизированных протоколов лечения или лазерных установок для лечения НМРК представляет собой актуальную проблему в этой области [55]. Недавний систематический обзор и метаанализ лазерного лечения НМРК продемонстрировал, что Nd:YAG-лазер является безопасным и эффективным методом лечения БРК с низким риском, частота рецидивов которого составляет всего 3,1% [56]. С другой стороны, CO2-лазер был признан менее эффективным, чем Nd:YAG-лазер, с частотой рецидивов до 9,4%, и поэтому не рекомендовался для лечения БРК [56]. Кроме того, абляционные лазеры потенциально увеличивают время заживления, остаточную опухолевую нагрузку или рецидивы, которые могут быть не так легко визуализированы в рубцовой ткани по сравнению с неабляционным лечением [57].
Было обнаружено, что интенсивная фотодинамическая терапия (иФДТ) в сочетании с фракционной абляцией CO2-лазером сокращает время, необходимое для проникновения фотосенсибилизатора в очаг поражения [58, 59]. Таким образом, иФДТ увеличивает поглощение фотосенсибилизатора и может повысить терапевтическую эффективность. Недавние исследования продемонстрировали более высокую отдаленную эффективность (6 мес) лечения НМРК при применении иФДТ и абляции по сравнению с изолированной ФДТ [58, 59].
В исследовании, опубликованном в 2019 г., оценивалось комбинированное лечение с использованием PDL с длиной волны 595 нм и фракционного лазера с длиной волны 1927 нм для лечения 93 пациентов с БРК. По результатам исследования была продемонстрирована высокая эффективность лечения в 95,7% (89/93) случаев и в 4,5% (4/89) отмечался рецидив [55]. В более крупном ретроспективном когортном исследовании оценивалась эффективность PDL (595 нм) в терапии НМРК у пожилых людей путем оценки 121 пациента с локализацией опухоли на руках [59]. Частота рецидивов во всех случаях ПРК составила 9,6%, при отсутствии рецидивов у пациентов с БРК, что позволяет эффективно проводить серию PDL-процедур для лечения НМРК на коже рук пожилых пациентов [59].
Эти последние достижения в области лазерной терапии НМРК у пожилых людей подчеркивают постоянные усилия по совершенствованию и расширению возможностей, доступных этой категории пациентов. Сочетая точность, минимально инвазивные методы и усовершенствованный мониторинг, лазерная терапия становится все более привлекательным выбором лечения пожилых пациентов с НМРК, способствуя получению эффективных результатов лечения и улучшению качества жизни.
Выбор метода лечения НМРК у пожилых пациентов
При выборе метода лечения НМРК у пожилых людей следует учитывать множество факторов, включая тип рака кожи, локализацию, частоту излечения и потенциальные осложнения. Важно учитывать необходимость лечения и его влияние на общее качество жизни пациента. Выбор между хирургическим вмешательством, местной терапией и лучевой терапией должен определяться индивидуальными потребностями пациента и его клиническими особенностями. Частота излечения, косметические результаты и потенциальные осложнения – все это важные факторы, учитываемые при подборе лечения для пожилых людей.Хирургическое вмешательство обеспечивает высокие показатели излечения и точный контроль за удалением опухоли, но решение о проведении хирургического вмешательства должно приниматься с учетом общего состояния здоровья пациента, характеристик опухоли и косметических результатов. Местная терапия и лучевая терапия не являются инвазивными альтернативами, но пациенты и медицинские работники должны тщательно оценивать их пригодность в зависимости от типа и локализации опухолевого поражения. При принятии решения также необходимо учитывать возможные осложнения и долгосрочные косметические результаты. Влияние лечения на качество жизни пожилого пациента является важнейшим фактором. Хирургические вмешательства могут привести к длительному периоду восстановления и возможному образованию рубцов, что может быть менее приемлемо для пожилых людей. И наоборот, местное лечение и лучевая терапия могут обеспечить более быстрое выздоровление и более благоприятные косметические результаты, но, возможно, увеличить число посещений амбулатории. Эти соображения подчеркивают необходимость разработки индивидуальных планов лечения, учитывающих уникальные потребности и предпочтения пожилых пациентов с НМРК.
Проблемы принятия решений о лечении НМРК у пожилых пациентов
Процесс принятия решения о лечении НМРК у пожилых людей включает многогранную оценку, учитывающую такие факторы, как функциональный статус, влияние на качество жизни, стоимость, ожидаемая продолжительность жизни, неблагоприятные исходы и индивидуальные предпочтения [30]. Получив полное представление об общем состоянии здоровья пациента, врачи могут избежать проведения ненужных и инвазивных процедур, которые могут принести ограниченную пользу с точки зрения выживаемости или качества жизни. Некоторые исследователи предлагают возраст в качестве относительного критерия для лечения НМРК, ссылаясь на наблюдения о том, что более половины пациентов в возрасте 90 лет и старше умерли в течение года после лечения по не связанным с этим причинам [60]. Напротив, другие исследования демонстрируют, что МХМ хорошо переносится пациентами в возрасте 90 лет и старше без летального исхода, связанного с процедурой [61]. Разнообразие результатов исследований подчеркивает необходимость учета дополнительных аспектов состояния здоровья при принятии решений о лечении.Использование инструментов, учитывающих сопутствующие заболевания наряду с возрастом, является распространенным подходом к оценке ограниченной продолжительности жизни (LLE – Limited Life Expectancy) пациентов. Для этой цели часто используется индекс коморбидности Чарльсона (CCI) [62, 63]. Однако не существует установленных рекомендаций по оценке CCI, которые могли бы дать окончательный прогноз. Исследования различались в определении LLE, в некоторых исследованиях использовались оценки CCI 3+, основанные на 44% смертности за 2 года, в то время как другие предполагают оценку CCI 7+ с вероятностью смертности менее 40% через 2 года [62–64]. Отсутствие надежности в этом показателе подчеркивает необходимость учета факторов, не связанных с сопутствующими заболеваниями при выборе лечения НМРК у пожилых людей.
Оценка функциональных возможностей пациента может помочь определить степень агрессивности лечения НМРК. Шкала функционального состояния Карнофски (KPS) является надежной и позволяет сбалансировать нагрузку на системные заболевания и возможности пациента в повседневной деятельности. Учитывая полезность функциональной оценки как показателя общего состояния здоровья пациента и предиктора выживаемости в пожилом возрасте, рекомендуется включать KPS в процесс принятия решений о лечении для всех пациентов [65, 66]. Это особенно актуально при рассмотрении менее инвазивного метода лечения для пациента
с плохим функциональным состоянием, даже если опухоль соответствует AUC [67].
Физические последствия рака и его лечения у пожилых людей могут быть значительными и часто усугубляются возрастными особенностями. Риск развития осложнений, более длительное время восстановления и влияние на повседневную деятельность являются важными факторами при принятии решения об интенсивности проводимого лечения [30]. Кровотечение из опухоли является распространенным осложнением, которое может побудить врача удалять новообразование, а не прибегать к паллиативным мерам. Локализацию и размер опухоли также следует рассматривать как патологический фактор, поскольку большие очаги могут привести к обезображиванию, в то время как при определенных методах лечения шрамы могут быть сопоставимы с опухолевым поражением [30].
Эмоциональные и психологические аспекты лечения НМРК имеют первостепенное значение, поскольку многочисленные психологические проблемы пожилых людей влияют на их способность переносить операции на коже. Эти проблемы включают снижение когнитивных способностей, ухудшение памяти, влияющее на комплаенс в процессе лечения, эмоциональную неустойчивость и повышенную тревогу по поводу увечий, боли, неизвестности, зависимости от других или смерти, что создает различные психологические и когнитивные ограничения [68]. Таким образом, особое внимание к когнитивным и физиологическим ограничениям пациентов может свести к минимуму периоперационный риск во время операций на коже у пожилых людей [68].
Врачи также должны учитывать социальные аспекты лечения пожилых людей. Необходимость интенсивного лечения, включая поездки для проведения многочисленных хирургических вмешательств или интенсивной ЛТ, может нарушить их повседневную жизнь и вызвать дополнительный стресс как у пациентов, так и у родственников. Кроме того, финансовые аспекты лечения могут вызывать серьезные опасения у пожилых пациентов.
Врачи должны учитывать важную роль скрининга на рак кожи у пожилых людей. Тотальное обследование кожи тела (TBSE – Total Body Skin Examination) относится к систематическому обследованию кожи пациента, ногтей, волос и соответствующих поверхностей слизистых оболочек с целью выявления единичных случаев новообразований кожи, которые пациент, возможно, не в состоянии увидеть, что способствует более раннему выявлению рака [6]. Однако результаты скрининга населения в целом с использованием TBSE остаются спорными [69], а рутинное использование TBSE дерматологами варьируется [70]. В прошлом году Целевая группа по профилактическим услугам США пришла к выводу, что имеющихся данных недостаточно для оценки баланса пользы и вреда визуального осмотра кожи врачом для выявления рака кожи у подростков и взрослых [71]. Таким образом, врачи должны использовать клиническую оценку при определении полезности TBSE у пожилых пациентов, особенно в связи с растущим использованием теледерматологических методов, где TBSE в значительной степени исключен [72].
Учитывая вышеописанные факторы, паллиативная помощь может обеспечить более сбалансированный подход, который в определенных случаях соответствует общему качеству жизни пациента. Исследования демонстрируют спорные мнения о целесообразности использования медицинских процедур и методов лечения в конце жизни и утверждают, что преимущества скрининга и лечения не всегда могут перевешивать потенциальные риски, поскольку пациенты могут прожить недостаточно долго, чтобы получить пользу, а последующие осложнения лечения могут снизить качество жизни [73, 74]. В конечном счете, врачам необходимо учитывать общее состояние здоровья пациента, ожидаемую продолжительность жизни и личные предпочтения, сбалансированные с физическими, эмоциональными и социальными последствиями рака, при определении надлежащего курса лечения.
Стратегии профилактики
Для пациентов с высоким риском крайне важно применять ряд профилактических стратегий. Меры по предотвращению воздействия УФ-излучения являются основополагающими, включая избегание воздействия прямы солнечных лучей, ношение защитной одежды и использование солнцезащитных средств широкого спектра действия. Хотя есть некоторые основания полагать, что никотинамид в качестве химиопрофилактической меры может снижать риск развития БРК и ПРК [75], полный спектр его эффективности и безопасности все еще является предметом исследований, и к нему следует подходить с осторожностью. Кроме того, пожилым пациентам, которым часто назначают несколько препаратов для лечения сопутствующих заболеваний, рекомендуется пересмотреть схемы лечения с исключением препаратов, которые могут повысить риск развития рака кожи. Всякий раз, когда это возможно, врачи должны рассматривать альтернативы таким лекарствам, как гидрохлоротиазид [76], метотрексат [77] и иммунодепрессанты, такие как азатиоприн [78].Заключение
В обзоре подчеркивается важность адаптированных подходов к лечению НМРК у пожилых людей. Учитывая растущую распространенность НМРК у пожилых людей, удовлетворение их особых потребностей и проблем имеет первостепенное значение. Продолжающиеся исследования в этой области могут улучшить результаты лечения и повысить качество жизни пожилых пациентов с НМРК. Будущее гериатрической дерматологии, вероятно, будет зависеть от этих достижений, обеспечивающих более полное понимание методов лечения НМРК у пожилых людей. Поскольку область дерматологии продолжает развиваться, индивидуальный подход к лечению НМРК у пожилых людей будет иметь решающее значение. Активное сотрудничество между медицинскими работниками, пациентами и их семьями имеет важное значение для принятия обоснованных решений о лечении. Необходимы дальнейшие исследования для уточнения рекомендаций и стратегий лечения пожилых людей с особым акцентом на оптимизацию терапевтических результатов при минимизации физического, эмоционального и социального воздействия НМРК и его лечения.Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Источник финансирования. Авторы заявляют об отсутствии внешнего финансирования при проведении исследования. Исследование выполнено в рамках межвузовского взаимодействия по научному кружку «Дерматопатология».
Funding source. This study was not supported by any external sources of funding. The study was carried out within the framework of interuniversity cooperation in the scientific community «Dermatopathology».
Вклад авторов. Авторы подтверждают соответствие своего авторства международным критериям ICMJE (все авторы внесли существенный вклад в разработку концепции, проведение исследования и подготовку статьи, прочли и одобрили финальную версию перед публикацией). Наибольший вклад распределен следующим образом: А.А. Пирожникова, М.В. Стецюк, К.А. Кудревич, О.В. Немирова – концепция исследования, согласование финальной версии рукописи; Э.Э. Абдурахманова, А.И. Умерова, Э.Г. Тамасян, Д.Ю. Ковали, К.А. Товмасян, В.А. Филипова, А.А. Диарова, А.А. Багдасарян, Х-А. А. Шадиев – обзор литературы, анализ данных, написание текста статьи.
Author contribution. The authors confirm that their authorship meets the international ICMJE criteria (all authors have made a significant contribution to the development of the concept, research and preparation of the article, read and approved the final version before publication). The greatest contribution is distributed as follows: A.A. Pirozhnikova, M.V. Stetsyuk, K.A. Kudrevich, O.V. Nemirova – the concept of research, coordination of the final version of the manuscript; E.E. Abdurakhmanova, A.I. Umerova, E.G. Tamasyan, D.Y. Kovali, K.A. Tovmasyan, V.A. Filipova, A.A. Diarova, A.A. Bagdasaryan, Kh-A.A. Shadiev ― literature review, data analysis, writing the text of the article.
Информация об авторах
Information about the authors
Пирожникова Александра Алексеевна – ординатор, ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова». E-mail: vkomissiya@inbox.ru; ORCID: 0009-0004-5294-1360
Aleksandra A. Pirozhnikova – Resident, Mechnikov North-Western State Medical University. E-mail: vkomissiya@inbox.ru; ORCID: 0009-0004-5294-1360
Стецюк Максим Валерьевич – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: m2002.like@yandex.ru; ORCID: 0009-0002-0725-8867
Maksim V. Stetsyuk – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: m2002.like@yandex.ru; ORCID: 0009-0002-0725-8867
Кудревич Ксения Антоновна – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: ksukud25@gmail.com; ORCID: 0009-0003-3435-7059
Kseniya A. Kudrevich – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: ksukud25@gmail.com; ORCID: 0009-0003-3435-7059
Абдурахманова Эмине Энверовна – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: abdurakhmanovaemine1@gmail.com; ORCID: 0009-0009-5674-7772
Emine E. Abdurakhmanova – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: abdurakhmanovaemine1@ gmail.com; ORCID: 0009-0009-5674-7772
Умерова Амина Ильдаровна – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: aminaumerova2310@gmail.com; ORCID: 0009-0009-5750-9258
Amina I. Umerova – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: aminaumerova2310@gmail.com; ORCID: 0009-0009-5750-9258
Тамасян Эдгар Гарегинович – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: ed_tamasyan12.04@icloud.com; ORCID: 0009-0004-9608-0187
Edgar G. Tamasyan – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: ed_tamasyan12.04@icloud.com;
ORCID: 0009-0004-9608-0187
Ковали Диляра Юсуф къызы – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: dilyara_kovali@mail.ru; ORCID: 0009-0009-4692-7382
Dilyara Yu. Kovali – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: dilyara_kovali@mail.ru; ORCID: 0009-0009-4692-7382
Товмасян Корюн Арманович – студент, Ордена Трудового Красного Знамени Медицинский институт им. С.И. Георгиевского. E-mail: koryun_t228@icloud.com; ORCID: 0009-0009-7199-7358
Koryun A. Tovmasyan – Student, Georgievsky Order of the Red Banner Medical Institute. E-mail: koryun_t228@icloud.com; ORCID: 0009-0009-7199-7358
Филипова Вероника Андреевна – студент, ФГБОУ ВО БГМУ. E-mail: verofilipova@yandex.ru; ORCID: 0009-0006-7758-2151
Veronika A. Filipova – Student, Bashkir State Medical University. E-mail: verofilipova@yandex.ru; ORCID: 0009-0006-7758-2151
Диарова Алия Амировна – студент, ФГБОУ ВО БГМУ. E-mail: diarovaalia@yandex.ru; ORCID: 0009-0007-1120-7292
Aliya A. Diarova – Student, Bashkir State Medical University.
E-mail: diarovaalia@yandex.ru; ORCID: 0009-0007-1120-7292
Немирова Ольга Владимировна – зав. медицинским кабинетом, врач, АНО ВО МГЭУ. E-mail: olga605794@yandex.ru; ORCID: 0009-0006-3565-4751
Olga V. Nemirova – Head of the Medical Office, Doctor, Moscow University of Humanities and Economics. E-mail: olga605794@yandex.ru; ORCID: 0009-0006-3565-4751
Багдасарян Аскина Аркадьевна – студент, ФГБОУ ВО «Ростовский ГМУ». E-mail: Verner.liza@bk.ru; ORCID: 0009-0006-7712-7888
Askina A. Bagdasaryan – Student, Rostov State Medical University. E-mail: Verner.liza@bk.ru; ORCID: 0009-0006-7712-7888
Шадиев Хож-Ахмед Аптиевич – студент, ФГБОУ ВО «Астраханский ГМУ». E-mail: shadiev8999@gmail.com; ORCID: 0009-0003-5290-7704
Khozh-Akhmed A. Shadiev – Student, Astrakhan State Medical University. E-mail: shadiev8999@gmail.com; ORCID: 0009-0003-5290-7704
Поступила в редакцию: 12.11.2024
Поступила после рецензирования: 19.11.2024
Принята к публикации: 21.11.2024
Received: 12.11.2024
Revised: 19.11.2024
Accepted: 21.11.2024
Список исп. литературыСкрыть список1. Кубанов А.А., Кондрахина И.Н., Плахова К.И., Сайтбурханов Р.Р. Современное представление о патогенезе базальноклеточного рака кожи. Вестник дерматологии и венерологии. 2021;97(5):38-51.
Kubanov A.A., Kondrakhina I.N., Plakhova X.I., Saytburkhanov R.R. Modern understanding of the pathogenesis of basal cell skin cancer. Vestnik Dermatologii i Venerologii. 2021;97(5):38-51 DOI: 10.25208/ vdv1277 (in Russian).
2. Sordi E, Piscitelli P, Albanese C et al. Incidence of Non-Melanoma Skin Cancers in Salento (Southern Italy): A 15-Year Retrospective Analysis from the Cancer Registry of Lecce. Epidemiologia (Basel) 2023;5(1):1-10. DOI: 10.3390/epidemiologia5010001
3. Albert A, Knoll MA, Conti JA, Zbar RIS. Non-Melanoma Skin Cancers in the Older Patient. Curr Oncol Rep 2019 ;21(9):79. DOI: 10.1007/s11912-019-0828-9
4. Каприн А.Д., Старинский В.В., Шахзадова А.О. Злокачественные новообразования в России в 2019 году (заболеваемость и смертность). М., 2020.
Kaprin A.D., Starinsky V.V., Shakhzadova A.O. Malignant neoplasms in Russia in 2019 (morbidity and mortality). Moscow, 2020 (in Russian).
5. Apalla Z, Nashan D, Weller RB, Castellsagué X. Skin Cancer: Epidemiology, Disease Burden, Pathophysiology, Diagnosis, and Therapeutic Approaches. Dermatol Ther (Heidelb) 2017;7(Suppl 1):5-19. DOI: 10.1007/s13555-016-0165-y
6. Leiter U, Keim U, Garbe C. Epidemiology of Skin Cancer: Update 2019. Adv Exp Med Biol 2020;1268:123-39. DOI: 10.1007/978-3-030-46227-7_6
7. McFerran E, Donaldson S, Dolan O, Lawler M. Skin in the game: The cost consequences of skin cancer diagnosis, treatment and care in Northern Ireland. J Cancer Policy 2024;39:100468. DOI: 10.1016/j.jcpo. 2024.100468
8. Sinikumpu SP, Jokelainen J, Keinänen-Kiukaanniemi S, Huilaja L. Skin cancers and their risk factors in older persons: a population-based study. BMC Geriatr 2022;22(1):269. DOI: 10.1186/s12877-022-02964-1
9. Рыбкина В.Л., Азизова Т.В., Адамова Г.В. Факторы риска развития злокачественных новообразований кожи. Клиническая дерматология и венерология. 2019;18(5):548-55. DOI: 10.17116/klinderma201918051548
Rybkina V.L., Azizova T.V., Adamova G.V. Risk factors of malignant neoplasms of the skin. Russian Journal of Clinical Dermatology and Venereology. 2019;18(5):548-55. DOI: 10.17116/klinderma2019 18051548 (in Russian).
10. Wendt A, Möhner M. Occupational solar exposure and basal cell carcinoma. A review of the epidemiologic literature with meta-analysis focusing on particular methodological aspects. Eur J Epidemiol 2024 Jan;39(1):13-25. DOI: 10.1007/s10654-023-01061-w
11. Зорина А.И., Зорин В.Л., Копнин П.Б. и др. Старение кожи, ассоциированное с инволюционными изменениями фибробластического дифферона и внеклеточного матрикса дермы. Клиническая дерматология и венерология. 2023;22(3):338-45. DOI: 10.17116/ klinderma202322031338
Zorina A.I., Zorin V.L., Kopnin P.B. et al. Skin aging associated with involutional changes in fibroblastic differon and extracellular matrix of the dermis. Russian Journal of Clinical Dermatology and Venereology. 2023;22(3):338-45. DOI: 10.17116/klinderma202322031338 (in Russian).
12. Перлин Д.В., Александров И.В., Перлина А.Д. и др. Злокачественные новообразования кожи у пациентов после трансплантации почки. Вестник урологии. 2022;10(3):36-43. DOI: 10.21886/2308-6424-2022-10-3-36-43
Perlin D.V., Alexandrov I.V., Perlina A.D., Shmanev A.O., Dymkov I.N. Malignant skin neoplasms in patients after kidney transplantation. Urology Herald. 2022;10(3):36-43. DOI: 10.21886/2308-6424-2022-10-3-36-43 (in Russian).
13. Владимирова Л.Ю., Алькина А.К. Карцинома Меркеля. Современные возможности лекарственной терапии. Злокачественные опухоли. 2023;13(3s1):49-52. DOI: 10.18027/2224-5057-2023-13-3s1-49-52
Vladimirova L.Yu., Alkina A.K. Merkel’s carcinoma. Modern possibilities of drug therapy. Malignant tumours. 2023;13(3s1):49-52. DOI: 10.18027/2224-5057-2023-13-3s1-49-52 (in Russian).
14. Щава С.Н., Сердюкова Е.А., Редькина Н.А. и др. Клинический случай ангиосаркомы: дифференциально-диагностический путь. Клиническая дерматология и венерология. 2019;18(6):699-703. DOI: 10.17116/klinderma201918061699
Shchava S.N., Serdjukova E.A., Redkina N.A. et al. Clinical case of angiosarcoma: differential diagnostic pathway. Russian Journal of Clinical Dermatology and Venereology. 2019;18(6):699-703. DOI: 10.17116/klinderma201918061699 (in Russian).
15. Титов К.С., Джамилов Ш.Р., Лебединский И.Н. и др. Клинический случай диагностики и лечения рака кожи из сальных желез. Саркомы костей, мягких тканей и опухоли кожи. 2024;16(2):87-93. DOI: 10.17650/2219-4614-2024-16-2-87-93
Titov K.S., Dzhamilov Sh.R., Lebedinsky I.N. et al. Clinical Case of Diagnosis and Treatment of Skin Cancer from Sebaceous Glands. Bone and soft tissue sarcomas, tumors of the skin. 2024;16(2):87-93. DOI: 10.17650/2219-4614-2024-16-2-87-93 (in Russian).
16. Катина М.А., Лесничая О.В., Рязанова Н.В. Дерматофибросаркома выбухающая в дерматологической практике. Клинический случай. Consilium Medicum. 2022;24(8):523-8. DOI: 10.26442/20751753.2022. 8.201721
Katina M.A., Lesnichaya O.V., Ryazanova N.V. Dermatofibrosarcoma protuberans in dermatological practice. Case report. Consilium Medicum. 2022;24(8):523-8. DOI: 10.26442/20751753.2022.8.201721 (in Russian).
17. Garcovich S, Colloca G, Sollena P et al. Skin Cancer Epidemics in the Elderly as An Emerging Issue in Geriatric Oncology. Aging Dis 2017;8(5):643-61. DOI: 10.14336/AD.2017.0503
18. Zheng DX, Cwalina TB, Mulligan KM et al. Prevalence and predictors of transportation barriers to health care among US adults with a history of skin cancer. J Am Acad Dermatol 2023;88(1):201-203. DOI: 10.1016/j.jaad.2022.04.023
19. Shelton ME, Adamson AS. Review and Update on Evidence-Based Surgical Treatment Recommendations for Nonmelanoma Skin Cancer. Dermatol Clin 2019;37(4):425-33. DOI: 10.1016/j.det.2019.05.002
20. Бройнингер X., Белова И.А. Микроскопически контролируемая хирургия с трехмерным гистологическим контролем, тумесцентная локальная анестезия и внутрикожная шовная техника под натяжением в лечении злокачественных новообразований кожи. Опухоли головы и шеи. 2018;8(3):21-36. DOI: 10.17650/2222-1468-2018-8-3-21-36
Breuninger H., Belova I.A. Microscopically controlled surgery with three-dimensional histology, tumescent local anesthesia and intracutaneous sutures for high tension in the treatment of skin cancer. Head and Neck Tumors (HNT). 2018;8(3):21-36. DOI: 10.17650/2222-1468-2018-8-3-21-36 (in Russian).
21. Brodland DG, Zitelli JA. Surgical margins for excision of primary cutaneous squamous cell carcinoma. J Am Acad Dermatol 1992;27(2 Pt 1):241-8. DOI: 10.1016/0190-9622(92)70178-i
22. Quazi SJ, Aslam N, Saleem H et al. Surgical Margin of Excision in Basal Cell Carcinoma: A Systematic Review of Literature. Cureus 2020;12(7):e9211. DOI: 10.7759/cureus.9211
23. Coady-Fariborzian L, Anstead C, Anna Paul S. Surgical Treatment of Nonmelanoma Skin Cancer in Older Adult Veterans. Fed Pract 2022;39(Suppl 3):S45-S49. DOI: 10.12788/fp.0283
24. Smeets NW, Krekels GA, Ostertag JU et al. Surgical excision vs Mohs‘ micrographic surgery for basal-cell carcinoma of the face: randomised controlled trial. Lancet 2004;364(9447):1766-72. DOI: 10.1016/S0140-6736(04)17399-6
25. Leibovitch I, Huilgol SC, Selva D et al. Cutaneous squamous cell carcinoma treated with Mohs micrographic surgery in Australia I. Experience over 10 years. J Am Acad Dermatol 2005;53(2):253-60. DOI: 10.1016/j.jaad.2005.02.059
26. Rowe DE, Carroll RJ, Day CL Jr. Prognostic factors for local recurrence, metastasis, and survival rates in squamous cell carcinoma of the skin, ear, and lip. Implications for treatment modality selection. J Am Acad Dermatol 1992;26(6):976-90. DOI: 10.1016/0190-9622(92)70144-5
27. Ferry AM, Sarrami SM, Hollier PC et al. Treatment of Non-melanoma Skin Cancers in the Absence of Mohs Micrographic Surgery. Plast Reconstr Surg Glob Open 2020;8(12):e3300. DOI: 10.1097/GOX.0000000000003300
28. Mendez BM, Thornton JF. Current Basal and Squamous Cell Skin Cancer Management. Plast Reconstr Surg 2018;142(3):373e-387e. DOI: 10.1097/PRS.0000000000004696.
29. Tongdee E, Psomadakis CE, Paka P et al. Emerging noninvasive treatments of nonmelanoma skin cancers. Cutis 2020;105(3):138-42.
30. Renzi M Jr, Schimmel J, Decker A, Lawrence N. Management of Skin Cancer in the Elderly. Dermatol Clin 2019;37(3):279-86. DOI: 10.1016/j.det.2019.02.003
31. Neale H, Michelon M, Jacob S et al. Topical 5% 5-fluorouracil versus procedural modalities for squamous cell carcinoma in situ and superficial basal cell carcinoma: A retrospective cohort analysis. J Am Acad Dermatol 2022;87(2):423-5. DOI: 10.1016/j.jaad.2021.08.045
32. Alessi SS, Sanches JA, Oliveira WR et al. Treatment of cutaneous tumors with topical 5% imiquimod cream. Clinics (Sao Paulo) 2009;64(10):961-6. DOI: 10.1590/S1807-59322009001000005
33. Lanoue J, Goldenberg G. Basal Cell Carcinoma: A Comprehensive Review of Existing and Emerging Nonsurgical Therapies. J Clin Aesthet Dermatol 2016;9(5):26-36.
34. Casey D, Demko S, Shord S et al. FDA Approval Summary: Sonidegib for Locally Advanced Basal Cell Carcinoma. Clin Cancer Res 2017;23(10):2377-81. DOI: 10.1158/1078-0432.CCR-16-2051
35. Раджабова З.А., Котов М.А., Бекяшева З.С. и др. Опыт применения ингибитора сигнального пути Hedgehog в лечении рецидивирующего местно-распространенного и метастатического базальноклеточного рака кожи. Опухоли головы и шеи. 2019;9(4):38-42. DOI: 10.17650/2222-1468-2019-9-4-38-42
Radzhabova Z.A., Kotov M.A., Bekyasheva Z.S. et al. Use of the Hedgehog signaling pathway inhibitor in the treatment of recurrent locally advanced and metastatic basal cell skin cancer. Head and Neck Tumors (HNT). 2019;9(4):38-42. DOI: 10.17650/2222-1468-2019-9-4-38-42 (in Russian).
36. Skvara H, Kalthoff F, Meingassner JG et al. Topical treatment of Basal cell carcinomas in nevoid Basal cell carcinoma syndrome with a smoothened inhibitor. J Invest Dermatol 2011;131(8):1735-44. DOI: 10.1038/jid.2011.48
37. Brancaccio G, Pea F, Moscarella E, Argenziano G. Sonidegib for the Treatment of Advanced Basal Cell Carcinoma. Front Oncol 2020;10:582866. DOI: 10.3389/fonc.2020.582866
38. Markham A, Duggan S. Cemiplimab: First Global Approval. Drugs 2018;78(17):1841-6. DOI: 10.1007/s40265-018-1012-5
39. Migden MR, Rischin D, Schmults CD et al. PD-1 Blockade with Cemiplimab in Advanced Cutaneous Squamous-Cell Carcinoma. N Engl J Med 2018;379(4):341-51. DOI: 10.1056/NEJMoa1805131
40. Bendell J, Andre V, Ho A et al. Phase I Study of LY2940680, a Smo Antagonist, in Patients with Advanced Cancer Including Treatment-Naïve and Previously Treated Basal Cell Carcinoma. Clin Cancer Res 2018;24(9):2082-91. DOI: 10.1158/1078-0432.CCR-17-0723
41. Lear JT, Corner C, Dziewulski P et al. Challenges and new horizons in the management of advanced basal cell carcinoma: a UK perspective. Br J Cancer 2014;111(8):1476-81. DOI: 10.1038/bjc.2014.270
42. Basset-Seguin N, Sharpe HJ, de Sauvage FJ. Efficacy of Hedgehog pathway inhibitors in Basal cell carcinoma. Mol Cancer Ther 2015;14(3):633-41. DOI: 10.1158/1535-7163.MCT-14-0703
43. Mackey M, Shahsavari A, Mackey VT. Intralesional 5-Fluorouracil in the Treatment of Lower Leg Squamous Cell Carcinoma. J Drugs Dermatol 2018;17(11):1241-3.
44. Good LM, Miller MD, High WA. Intralesional agents in the management of cutaneous malignancy: a review. J Am Acad Dermatol 2011;64(2):413-22. DOI: 10.1016/j.jaad.2009.12.013
45. Marka A, Rodgers D, Zelaya Castillo L et al. Dilute Intralesional 5-Fluorouracil for the Treatment of Squamous Cell Carcinomas and Keratoacanthomas: A Case Series. J Drugs Dermatol 2023;22(5):507-8. DOI: 10.36849/JDD.5058
46. Nestor MS, Berman B, Goldberg D et al. Consensus Guidelines on the Use of Superficial Radiation Therapy for Treating Nonmelanoma Skin Cancers and Keloids. J Clin Aesthet Dermatol 2019;12(2):12-8.
47. Benkhaled S, Van Gestel D, Gomes da Silveira Cauduro C et al. The State of the Art of Radiotherapy for Non-melanoma Skin Cancer: A Review of the Literature. Front Med (Lausanne) 2022;9:913269. DOI: 10.3389/fmed.2022.913269
48. Gunaratne DA, Veness MJ. Efficacy of hypofractionated radiotherapy in patients with non-melanoma skin cancer: Results of a systematic review. J Med Imaging Radiat Oncol 2018;62(3):401-11. DOI: 10.1111/1754-9485.12718
49. Chicheł A, Chyrek AJ, Kluska A, Burchardt WM. Advanced non-melanoma skin cancer in elderly patients: When surgery says NO, interventional radiotherapy (brachytherapy) says YES. J Contemp Brachytherapy 2023;15(4):235-44. DOI: 10.5114/jcb.2023.130715
50. Conforti C, Corneli P, Harwood C, Zalaudek I. Evolving Role of Systemic Therapies in Non-melanoma Skin Cancer. Clin Oncol (R Coll Radiol) 2019;31(11):759-68. DOI: 10.1016/j.clon.2019.08.011
51. Barker CA, Dufault S, Arron ST et al. Phase II, Single-Arm Trial of Induction and Concurrent Vismodegib With Curative-Intent Radiation Therapy for Locally Advanced, Unresectable Basal Cell Carcinoma. J Clin Oncol 2024;42(19):2327-35. DOI: 10.1200/JCO.23.01708
52. Pollom EL, Bui TT, Chang AL et al. Concurrent Vismodegib and Radiotherapy for Recurrent, Advanced Basal Cell Carcinoma. JAMA Dermatol 2015;151(9):998-1001. DOI: 10.1001/jamadermatol.2015.0326
53. Гешева Э.М., Печатникова Е.А., Потекаев Н.Н. и др. Лучевая диагностика и лучевая терапия в дерматоонкологии. Клиническая дерматология и венерология. 2021;20(5):74-82. DOI: 10.17116/klinderma20212005174
Gesheva E.M., Pechatnikova E.A., Potekaev N.N. et al. Radiation diagnostics and radiation therapy in dermato-oncology. Russian Journal of Clinical Dermatology and Venereology. 2021;20(5):74-82. DOI: 10.17116/klinderma20212005174 (in Russian).
54. Tran A, Moloney M, Kaczmarski P et al. Analysis of image-guided superficial radiation therapy (IGSRT) on the treatment of early-stage non-melanoma skin cancer (NMSC) in the outpatient dermatology setting. J Cancer Res Clin Oncol 2023;149(9):6283-91. DOI: 10.1007/s00432-023-04597-2
55. Markowitz O, Tongdee E, Levine A. Optimal cosmetic outcomes for basal cell carcinoma: a retrospective study of nonablative laser management. Cutis 2019 May;103(5):292-7.
56. Sharon E, Snast I, Lapidoth M et al. Laser Treatment for Non-Melanoma Skin Cancer: A Systematic Review and Meta-Analysis. Am J Clin Dermatol 2021;22(1):25-38. DOI: 10.1007/s40257-020-00562-8
57. Soleymani T, Abrouk M, Kelly KM. An Analysis of Laser Therapy for the Treatment of Nonmelanoma Skin Cancer. Dermatol Surg 2017;43(5):615-24. DOI: 10.1097/DSS.0000000000001048
58. Farberg AS, Marson JW, Soleymani T. Advances in Photodynamic Therapy for the Treatment of Actinic Keratosis and Nonmelanoma Skin Cancer: A Narrative Review. Dermatol Ther (Heidelb) 2023;13(3):689-716. DOI: 10.1007/s13555-023-00888-1
59. Herron ED, Snyder AM, Hull CM et al. Fragile hands: targeting nonmelanoma skin cancer on older hands using 595 nm pulsed dye laser. Lasers Med Sci 2024;39(1):101. DOI: 10.1007/s10103-024-04047-6
60. Chauhan R, Munger BN, Chu MW et al. Age at Diagnosis as a Relative Contraindication for Intervention in Facial Nonmelanoma Skin Cancer. JAMA Surg 2018;153(4):390-2. DOI: 10.1001/jamasurg.2017.5073
61. Delaney A, Shimizu I, Goldberg LH, MacFarlane DF. Life expectancy after Mohs micrographic surgery in patients aged 90 years and older. J Am Acad Dermatol 2013;68(2):296-300. DOI: 10.1016/j.jaad.2012.1 0.016
62. Linos E, Parvataneni R, Stuart SE et al. Treatment of nonfatal conditions at the end of life: nonmelanoma skin cancer. JAMA Intern Med 2013;173(11):1006-12. DOI: 10.1001/jamainternmed.2013.639
63. Rogers EM, Connolly KL, Nehal KS et al. Comorbidity scores associated with limited life expectancy in the very elderly with nonmelanoma skin cancer. J Am Acad Dermatol 2018;78(6):1119-24. DOI: 10.1016/j.jaad. 2017.12.048
64. Yourman LC, Lee SJ, Schonberg MA et al. Prognostic indices for older adults: a systematic review. JAMA 2012;307(2):182-92. DOI: 10.1001/jama.2011.1966
65. Keeler E, Guralnik JM, Tian H et al. The impact of functional status on life expectancy in older persons. J Gerontol A Biol Sci Med Sci 2010;65(7):727-33. DOI: 10.1093/gerona/glq029
66. Hwang SS, Scott CB, Chang VT et al. Prediction of survival for advanced cancer patients by recursive partitioning analysis: role of Karnofsky performance status, quality of life, and symptom distress. Cancer Invest 2004;22(5):678-87. DOI: 10.1081/cnv-200032911
67. Renzi MA Jr, Belcher M, Brod B et al. Assessment of Functionality in Elderly Patients When Determining Appropriate Treatment for Nonmelanoma Skin Cancers. Dermatol Surg 2020;46(3):319-26. DOI: 10.1097/DSS.0000000000002028
68. Alam M, Norman RA, Goldberg LH. Dermatologic surgery in geriatric patients: psychosocial considerations and perioperative decision-making. Dermatol Surg 2002;28(11):1043-50. DOI: 10.1046/j.1524-4725.2002.02102.x
69. Wernli KJ, Henrikson NB, Morrison CC et al. Screening for Skin Cancer in Adults: Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA 2016;316(4):436-47. DOI: 10.1001/jama.2016.5415
70. Federman DG, Kravetz JD, Kirsner RS. Skin cancer screening by dermatologists: prevalence and barriers. J Am Acad Dermatol 2002;46(5):710-4. DOI: 10.1067/mjd.2002.120531
71. US Preventive Services Task Force; Mangione CM, Barry MJ et al. Screening for Skin Cancer: US Preventive Services Task Force Recommendation Statement. JAMA 2023;329(15):1290-5. DOI: 10.1001/jama.2023.4342
72. Omara S, Wen D, Ng B et al. Identification of Incidental Skin Cancers Among Adults Referred to Dermatologists for Suspicious Skin Lesions. JAMA Netw Open 2020;3(12):e2030107. DOI: 10.1001/jamanetworkopen.2020.30107
73. Schoenborn NL, Massare J, Park R et al. Assessment of Clinician Decision-making on Cancer Screening Cessation in Older Adults With Limited Life Expectancy. JAMA Netw Open 2020;3(6):e206772. DOI: 10.1001/jamanetworkopen.2020.6772
74. Sima CS, Panageas KS, Schrag D. Cancer screening among patients with advanced cancer. JAMA 2010;304(14):1584-91. DOI: 10.1001/jama.2010.1449
75. Mainville L, Smilga AS, Fortin PR. Effect of Nicotinamide in Skin Cancer and Actinic Keratoses Chemoprophylaxis, and Adverse Effects Related to Nicotinamide: A Systematic Review and Meta-Analysis. J Cutan Med Surg 2022;26(3):297-308. DOI: 10.1177/12034754221078201
76. Haisma MS, Greven N, Logendran M et al. Chronic Use of Hydrochlorothiazide and Risk of Skin Cancer in Caucasian Adults: A PharmLines Initiative Inception Cohort Study. Acta Derm Venereol 2023;103:adv3933. DOI: 10.2340/actadv.v103.3933
77. Polesie S, Gillstedt M, Schmidt SAJ et al. Use of methotrexate and risk of skin cancer: a nationwide case-control study. Br J Cancer 2023;128(7):1311-9. DOI: 10.1038/s41416-023-02172-7
78. Peters MG. Long-Term Use of Azathioprine in the Management of Autoimmune Hepatitis. Gastroenterol Hepatol (NY) 2019;15(5):277-9.
26 декабря 2024
Количество просмотров: 392


