Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№02 2012
Психофармакотерапия – неотъемлемый блок в лечении онкологических заболеваний №02 2012
Номера страниц в выпуске:32-36
Формирование нервно-психических расстройств у онкологических больных на этапе специального лечения делает необходимым наряду с традиционным противоопухолевым и/или симптоматическим лечением проведение индивидуальных комплексных психофармакологических и психотерапевтических лечебно-реабилитационных программ всем онкологическим больным. Онкологические больные, получившие соответствующее своевременное психофармакологическое и психотерапевтическое лечение, характеризуются лучшей и более быстрой психосоциальной адаптацией к своему заболеванию и новым условиям жизни. Для купирования депрессивной симптоматики у онкологических больных применяли Вальдоксан (агомелатин) как препарат выбора. Его широкий спектр эффективности и хорошая переносимость способствовали быстрому восстановлению эмоционального, функционального и социального благополучия, активному вовлечению в лечебный процесс и борьбу с опухолевым заболеванием.
Резюме. Формирование нервно-психических расстройств у онкологических больных на этапе специального лечения делает необходимым наряду с традиционным противоопухолевым и/или симптоматическим лечением проведение индивидуальных комплексных психофармакологических и психотерапевтических лечебно-реабилитационных программ всем онкологическим больным. Онкологические больные, получившие соответствующее своевременное психофармакологическое и психотерапевтическое лечение, характеризуются лучшей и более быстрой психосоциальной адаптацией к своему заболеванию и новым условиям жизни. Для купирования депрессивной симптоматики у онкологических больных применяли Вальдоксан (агомелатин) как препарат выбора. Его широкий спектр эффективности и хорошая переносимость способствовали быстрому восстановлению эмоционального, функционального и социального благополучия, активному вовлечению в лечебный процесс и борьбу с опухолевым заболеванием.
Ключевые слова: психофармакотерапия, антидепрессанты, Вальдоксан, агомелатин, онкологические заболевания.
Psychopharmacotherapy – essential unit in the treatment
of oncological diseases
E.P.Komkova
Regional Clinical Cancer Center, Kemerovo
Summary. Formation of the neuro-psychiatric disorders in oncological patients during specific treatment makes it necessary, in addition to traditional anticancer and (or) symptomatic treatment, individual psychotherapy and psycho-complex treatment and rehabilitation programs in all oncologiсal patients. Cancer patients, who receive timely appropriate psychopharmacological and psychotherapeutic treatment, are characterized by a better and more rapid psychosocial adaptation to their disease and new conditions of life. We used Valdoxan as a drug of choice for relief of depressive symptoms in oncological patients. Its wide range of performance contributed to the rapid recovery of emotional, functional and social well-being, involvement in the process of treatment and control of neoplastic disease.
Key words: psychopharmacоtherapy, antidepressants, Valdoxan, agomelatin, oncological diseases.
У онкологических больных на этапе специального лечения наблюдается формирование нервно-психических расстройств, утяжеляющих соматическое состояние, ухудшающих прогноз и затрудняющих проведение терапии основного заболевания [1].
В большинстве случаев возникновение нервно-психических расстройств обусловлено психотравмирующим воздействием информации о диагнозе онкологического заболевания, последующим послеоперационным физическим обезображиванием, инвалидизацией, необходимостью длительного проведения специального лечения, страхом перед побочными действиями химиотерапии, лучевой болезнью и болевым синдромом, а также существующим представлением о смертельном исходе заболевания [2].
Необходимость психофармакотерапии и психотерапии для купирования нервно-психических расстройств у больных онкологическими заболеваниями не вызывает сомнений. Онкологические больные, получившие соответствующее своевременное психофармакологическое и психотерапевтическое лечение, характеризуются лучшей и более быстрой психосоциальной адаптацией к своему заболеванию и новым условиям жизни [2–5]. Формирование нервно-психических расстройств у онкологических больных на этапе специального лечения делает необходимым наряду с традиционным противоопухолевым и/или симптоматическим лечением проведение индивидуальных комплексных психофармакологических и психотерапевтических лечебно-реабилитационных программ всем онкологическим больным [4, 5].
Для онкологических больных с нервно-психическими расстройствами в отделении восстановительного лечения Областного клинического онкологического диспансера г. Кемерово успешно проводятся разработанные и внедренные нами индивидуальные комплексные лечебно-реабилитационные программы, включающие психофармакотерапию и различные виды психотерапии.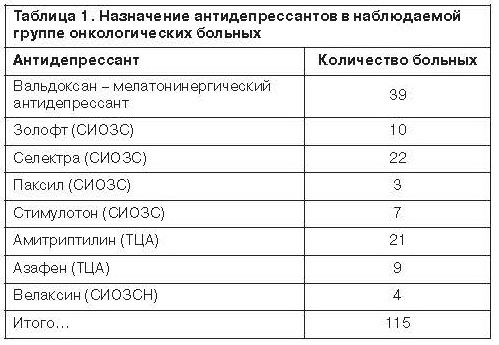 Их целью является купирование нервно-психических расстройств, активное формирование установки «на жизнь», мобилизация резервных возможностей психических функций пациентов. Применение программ показало их эффективность, подтвержденную клинико-динамическим, экспериментально-психологическим и клинико-катамнестическим исследованиями.
Их целью является купирование нервно-психических расстройств, активное формирование установки «на жизнь», мобилизация резервных возможностей психических функций пациентов. Применение программ показало их эффективность, подтвержденную клинико-динамическим, экспериментально-психологическим и клинико-катамнестическим исследованиями.
Цель настоящего исследования – анализ опыта психофармакотерапии, назначаемой онкологическим больным с нервно-психическими расстройствами в рамках проводимых лечебно-реабилитационных программ.
Материал исследования
Проанализировано 585 историй болезни онкологических больных (89% женщин и 11% мужчин) в возрасте от 18 до 65 лет, направленных в отделение восстановительного лечения в 2009–2010 гг. для проведения лечебно-реабилитационных мероприятий. Критериями отбора больных для лечения было формирование у них различного уровня выраженности нервно-психических расстройств вне зависимости от диагноза онкологического заболевания.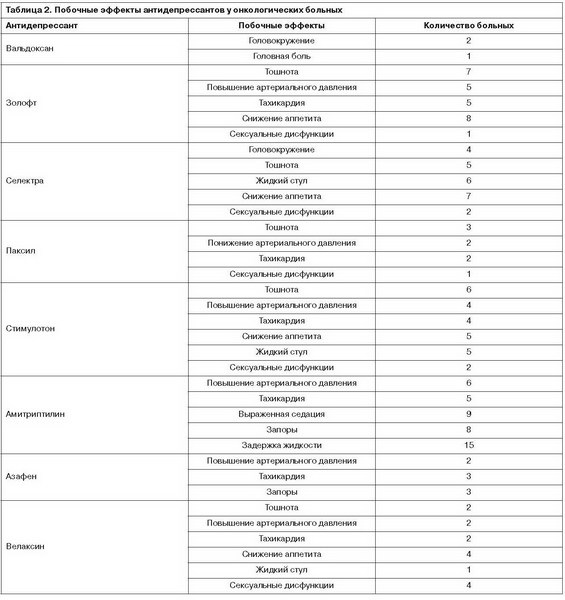

 При обследовании пациентов использовали клинико-психопатологический, клинико-динамический (Н.М.Жариков, 1983, 1988; А.В.Снежневский, 1983; В.Я.Семке, 1987–2001) и математико-статистический методы (А.М.Мерков, Л.Е.Дашков, 1974).
При обследовании пациентов использовали клинико-психопатологический, клинико-динамический (Н.М.Жариков, 1983, 1988; А.В.Снежневский, 1983; В.Я.Семке, 1987–2001) и математико-статистический методы (А.М.Мерков, Л.Е.Дашков, 1974).
Также применяли ряд экспериментально-психологических методик: исследование реактивной тревожности (РТ) и личностной тревожности (ЛТ) по Спилбергеру (в модификации Ю.Л.Ханина, 1978); исследование самооценки по Дембо–Рубинштейн (1970 г.).
Для выявления и оценки тяжести депрессии и тревоги использовалась госпитальная шкала тревоги и депрессии (HADS), разработанная А.Zigmond и R.Shaith (1983 г.).
 С целью оценки эмоционального состояния больного, критического отношения к болезни, установок на прогноз заболевания использовали проективный метод визуализации представлений в рисунках больных (К.Саймонтон, С.Саймонтон, 2001) ввиду простоты применения и наглядности.
С целью оценки эмоционального состояния больного, критического отношения к болезни, установок на прогноз заболевания использовали проективный метод визуализации представлений в рисунках больных (К.Саймонтон, С.Саймонтон, 2001) ввиду простоты применения и наглядности.
Результаты
У наблюдаемых больных при обследовании выявлены тревожно-депрессивные (47,5%), депрессивные (24,5%) и субдепрессивные (28,0%) реакции и состояния, которые, согласно Международной классификации болезней 10-го пересмотра, квалифицированы как невротические, связанные со стрессом расстройства.
В целом преобладала тревожно-депрессивная симптоматика. Средняя РТ до лечения составила 48,82±0,21; средняя ЛТ – 51,97±0,38. Средний уровень тревоги до лечения составил 14,0±0,1; средний уровень депрессии – 12,41±0,11 (по шкале HADS).
Симптоматическую психофармакотерапию, направленную на купирование ведущего синдрома в структуре заболевания, проводили 492 пациентам. Комплекс медикаментозных мероприятий также включал седативные средства, фитотерапию, поливитамины и адаптогены.
В первую очередь мы воздействовали на симптомы тревоги. Для этого назначали транквилизаторы с выраженным противотревожным действием. Наиболее широкое применение получили: алпразолам 0,0005– 0,001 г, сибазон 0,5% – 2,0 на ночь 3–5 дней. Однако развитие нежелательных явлений при использовании препаратов из группы бензодиазепинов, в том числе сонливости, снижения концентрации, мышечной слабости, значительно ограничивали их применение.
Параллельно с воздействием на тревожную симптоматику или в самостоятельном плане проводили коррекцию аффективных расстройств (у 115 пациентов). Назначали антидепрессанты различных химических групп (табл. 1). Предпочтение отдавали антидепрессантам с минимальным числом побочных эффектов, что давало возможность их использования при проведении «агрессивных» методов специального лечения (химиотерапии и лучевой терапии).
Препаратом выбора был Вальдоксан – первый мелатонинергический антидепрессант, эффективный в отношении всех основных симптомов депрессии [1, 6]. Его широкий спектр эффективности способствовал быстрому восстановлению эмоционального, функционального и социального благополучия, активному вовлечению в лечебный процесс и борьбу с опухолевым заболеванием.
Вальдоксан, будучи антидепрессантом с хронобиотическими свойствами, улучшал функцию сна за счет непосредственного влияния на механизмы регуляции сна, а не вследствие седативного эффекта [1, 6].
Вальдоксан (39 пациентов: 26 женщин, 13 мужчин) назначали по 25 мг на ночь, при необходимости дозу увеличивали до 50 мг. Срок лечения составил от 6 нед до 3 мес.
Первые эффекты, проявляющиеся в уменьшении соматической и психической тревоги, улучшении сна, появлялись уже в 1–2-е сутки приема препарата (рис. 1). Антидепрессивный эффект (оценка по шкале HADS) (рис. 2) появлялся к концу 1-й недели лечения (значительно раньше, чем у антидепрессантов других групп).
У препарата отсутствовали характерные для других антидепрессантов побочные эффекты со стороны сердечно-сосудистой системы, не было отмечено чрезмерной седации, сексуальных дисфункций, увеличения массы тела, подавления аппетита (табл. 2).
Побочные эффекты в виде головокружения (2 больных) и головной боли [1] проявлялись в первые 2 нед лечения, носили краткосрочный характер (см. табл. 2).
Также назначали антидепрессанты серотонинергической структуры (селектра до 10 мг; паксил 10–20 мг; золофт, стимулотон 25–50 мг в сутки), которые вызывали достаточно быстрый терапевтический эффект, заметную редукцию депрессивных расстройств, стабилизировали вегетативный тонус. Препараты данной группы применяли реже в связи с негативным влиянием на аппетит и массу тела, что было нежелательным при проведении специального лечения (см. табл. 2). Часто наблюдали появление тошноты, что еще более ухудшало качество жизни пациентов, страдающих от негативных последствий специального лечения (химиотерапии и лучевой терапии).
Учитывая невысокую стоимость и доступность, использовали амитриптилин, азафен до 50 мг в сутки. Соматорегулирующие эффекты препарата также потенцировали действие анальгетиков, снижали тяжесть телесных ощущений, обусловленных оперативным вмешательством, наличием опухоли или метастазов.
Широкое применение у больных получили препараты, оказывающие мягкое антидепрессивное, анксиолитическое, антиневротическое действие и практически не имеющие побочных эффектов: гелариум до 900 мкг 3 раза в сутки, грандаксин до 6 таблеток в сутки, афобазол до 30 мг в сутки в течение 1 мес.
Для коррекции астенических симптомов в послеоперационном периоде и на химиотерапевтическом лечении пациентам рекомендовали применение энериона по 200 мг 2 раза в сутки в течение 1 мес.
Важным условием реализации лечебно-реабилитационных программ для больных на этапе специального лечения являлось применение сборов трав, изготовленных по рецептам Алтайского онкологического фитоцентра, уменьшающих негативные последствия самого онкологического заболевания и специального лечения.
В медикаментозном лечении также использовались седативные средства, приготовленные из растительного сырья: экстракт валерианы, пустырника, персен, ново-пассит, специальные сборы успокоительных трав, выпускаемые фармацевтической промышленностью. Обязательно назначались адаптогены (родиола розовая, женьшень, элеутерококк по 5–10 капель 2 раза в день), поливитамины с минеральными комплексами (компливит, витрум, центрум, дуовит, триовит и др.).
Оценка клинических и экспериментально-психологических данных после проведения лечебно-реабилитационных программ показала значительное улучшение психического состояния онкологических больных.
Так, у больных с тревожно-депрессивным синдромом выявлялось уменьшение глубины тревожных и депрессивных проявлений, что подтверждалось результатами экспериментально-психологических исследований. Показателями эффективности лечения являлись также стабилизация артериального давления, улучшение сна и аппетита, купирование осложнений, связанных с последствиями хирургического лечения (боли, лимфостаз, ограничение объема движений в конечностях). Пациенты начинали следить за своим внешним видом, активно участвовали в проводимом лечении, в общении с близкими и знакомыми смогли преодолеть внутренний барьер и сообщить им о болезни. При условии удовлетворительного физического состояния больные могли возвратиться к профессиональной деятельности даже при необходимости продолжения специального лечения.
При этом у большинства больных сохранялось чувство неуверенности в благоприятном прогнозе заболевания. Периодически появлялись мысли о собственной ущербности, потере привлекательности, женственности и связанные с этим проблемы в общении с окружающими и в интимной жизни пациентов (ограничение общения, отсутствие, избегание интимных отношений).
РТ после лечения снизилась на 21,3% (с 53,12±0,24 до 41,8±0,33), ЛТ – на 5,2% (с 41,7±0,32 до 39,52±0,27). Уровень тревоги по госпитальной шкале HADS уменьшился на 30,3% (с 17,3±0,18 до 12,05±0,06), уровень депрессии – на 25,4% (с 13,29±0,13 до 9,91±0,05). По данным методики Дембо–Рубинштейн (1970 г.), у всех больных повысился уровень отметки по линиям счастья и здоровья.
У пациентов с депрессивным синдромом после лечения отмечались оптимизация настроения, улучшение сна и аппетита, стабилизация артериального давления, уменьшение болевых ощущений, связанных с последствиями оперативного вмешательства, повышение самооценки, подтверждавшиеся выравниванием экспериментально-психологических данных. Больные проявляли интерес к лечению, своему внешнему виду, общению, чтению, просмотру телепередач, возрастала их физическая активность.
У больных с субдепрессивным синдромом после проведения лечебно-реабилитационных программ улучшались сон, аппетит, возрастала физическая активность. Уменьшались тревожные опасения по поводу соматического состояния, возможных осложнений химиотерапии, лучевой терапии. Больные активно включались в лечебный процесс, что положительно влияло на самооценку и критическое отношение к заболеванию. У пациенток после радикальной мастэктомии отмечалось уменьшение болевого синдрома в верхних конечностях.
Уровень РТ после лечения снизился на 10,8% (с 43,38±0,31 до 38,68±0,3), ЛТ – на 3,2% (с 54,0±0,49 до 52,3±0,51). Уровень тревоги по госпитальной шкале HADS уменьшился на 11,6% (с 10,45±0,33 до 9,24±0,22), депрессии – на 9,6% (с 9,52±0,23 до 8,61±0,19). По данным методики Дембо–Рубинштейн (1970 г.), повышалась самооценка больных по шкалам здоровья и счастья.
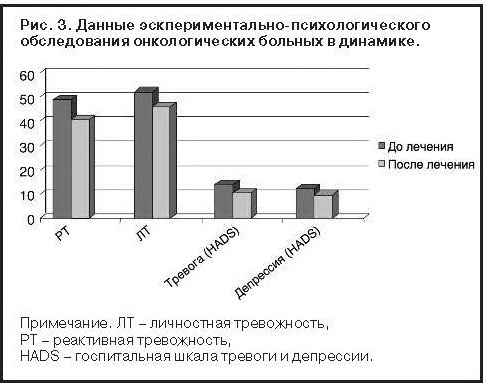
В целом РТ снизилась на 16,9% (с 48,82±0,21 до 40,56±0,32) и у всех пациентов соответствовала умеренным показателям, ЛТ – на 11,7% (с 51,97±0,38 до 45,9±0,25). По данным шкалы HADS, наблюдалось снижение выраженности тревоги на 23,4% (с 14,0±0,11 до 0,72±0,09), депрессии – на 21,2% (с 12,41±0,11 до 9,78±0,09) (рис. 3).
Психофармакотерапия во всех случаях была целесообразна и результативна, способствовала сглаживанию или купированию нервно-психических расстройств, что облегчало проведение специального лечения, улучшало психическое и соматическое благополучие онкологических больных и, возможно, прогноз заболевания.
Таким образом, дифференцированное применение комплексных лечебно-реабилитационных мероприятий, включающих психофармакотерапию и психотерапию, позволило судить об их эффективности, подтвержденной клинико-динамическим и экспериментально-психологическим исследованиями.
Сведения об авторе
Комкова Елена Павловна – канд. мед. наук, зав. отд-нием восстановительного лечения ГУЗ Областной клинический онкологический диспансер, врач-психотерапевт высшей категории
Ключевые слова: психофармакотерапия, антидепрессанты, Вальдоксан, агомелатин, онкологические заболевания.
Psychopharmacotherapy – essential unit in the treatment
of oncological diseases
E.P.Komkova
Regional Clinical Cancer Center, Kemerovo
Summary. Formation of the neuro-psychiatric disorders in oncological patients during specific treatment makes it necessary, in addition to traditional anticancer and (or) symptomatic treatment, individual psychotherapy and psycho-complex treatment and rehabilitation programs in all oncologiсal patients. Cancer patients, who receive timely appropriate psychopharmacological and psychotherapeutic treatment, are characterized by a better and more rapid psychosocial adaptation to their disease and new conditions of life. We used Valdoxan as a drug of choice for relief of depressive symptoms in oncological patients. Its wide range of performance contributed to the rapid recovery of emotional, functional and social well-being, involvement in the process of treatment and control of neoplastic disease.
Key words: psychopharmacоtherapy, antidepressants, Valdoxan, agomelatin, oncological diseases.
У онкологических больных на этапе специального лечения наблюдается формирование нервно-психических расстройств, утяжеляющих соматическое состояние, ухудшающих прогноз и затрудняющих проведение терапии основного заболевания [1].
В большинстве случаев возникновение нервно-психических расстройств обусловлено психотравмирующим воздействием информации о диагнозе онкологического заболевания, последующим послеоперационным физическим обезображиванием, инвалидизацией, необходимостью длительного проведения специального лечения, страхом перед побочными действиями химиотерапии, лучевой болезнью и болевым синдромом, а также существующим представлением о смертельном исходе заболевания [2].
Необходимость психофармакотерапии и психотерапии для купирования нервно-психических расстройств у больных онкологическими заболеваниями не вызывает сомнений. Онкологические больные, получившие соответствующее своевременное психофармакологическое и психотерапевтическое лечение, характеризуются лучшей и более быстрой психосоциальной адаптацией к своему заболеванию и новым условиям жизни [2–5]. Формирование нервно-психических расстройств у онкологических больных на этапе специального лечения делает необходимым наряду с традиционным противоопухолевым и/или симптоматическим лечением проведение индивидуальных комплексных психофармакологических и психотерапевтических лечебно-реабилитационных программ всем онкологическим больным [4, 5].
Для онкологических больных с нервно-психическими расстройствами в отделении восстановительного лечения Областного клинического онкологического диспансера г. Кемерово успешно проводятся разработанные и внедренные нами индивидуальные комплексные лечебно-реабилитационные программы, включающие психофармакотерапию и различные виды психотерапии.
 Их целью является купирование нервно-психических расстройств, активное формирование установки «на жизнь», мобилизация резервных возможностей психических функций пациентов. Применение программ показало их эффективность, подтвержденную клинико-динамическим, экспериментально-психологическим и клинико-катамнестическим исследованиями.
Их целью является купирование нервно-психических расстройств, активное формирование установки «на жизнь», мобилизация резервных возможностей психических функций пациентов. Применение программ показало их эффективность, подтвержденную клинико-динамическим, экспериментально-психологическим и клинико-катамнестическим исследованиями.
Цель настоящего исследования – анализ опыта психофармакотерапии, назначаемой онкологическим больным с нервно-психическими расстройствами в рамках проводимых лечебно-реабилитационных программ.
Материал исследования
Проанализировано 585 историй болезни онкологических больных (89% женщин и 11% мужчин) в возрасте от 18 до 65 лет, направленных в отделение восстановительного лечения в 2009–2010 гг. для проведения лечебно-реабилитационных мероприятий. Критериями отбора больных для лечения было формирование у них различного уровня выраженности нервно-психических расстройств вне зависимости от диагноза онкологического заболевания.


 При обследовании пациентов использовали клинико-психопатологический, клинико-динамический (Н.М.Жариков, 1983, 1988; А.В.Снежневский, 1983; В.Я.Семке, 1987–2001) и математико-статистический методы (А.М.Мерков, Л.Е.Дашков, 1974).
При обследовании пациентов использовали клинико-психопатологический, клинико-динамический (Н.М.Жариков, 1983, 1988; А.В.Снежневский, 1983; В.Я.Семке, 1987–2001) и математико-статистический методы (А.М.Мерков, Л.Е.Дашков, 1974).
Также применяли ряд экспериментально-психологических методик: исследование реактивной тревожности (РТ) и личностной тревожности (ЛТ) по Спилбергеру (в модификации Ю.Л.Ханина, 1978); исследование самооценки по Дембо–Рубинштейн (1970 г.).
Для выявления и оценки тяжести депрессии и тревоги использовалась госпитальная шкала тревоги и депрессии (HADS), разработанная А.Zigmond и R.Shaith (1983 г.).
 С целью оценки эмоционального состояния больного, критического отношения к болезни, установок на прогноз заболевания использовали проективный метод визуализации представлений в рисунках больных (К.Саймонтон, С.Саймонтон, 2001) ввиду простоты применения и наглядности.
С целью оценки эмоционального состояния больного, критического отношения к болезни, установок на прогноз заболевания использовали проективный метод визуализации представлений в рисунках больных (К.Саймонтон, С.Саймонтон, 2001) ввиду простоты применения и наглядности.
Результаты
У наблюдаемых больных при обследовании выявлены тревожно-депрессивные (47,5%), депрессивные (24,5%) и субдепрессивные (28,0%) реакции и состояния, которые, согласно Международной классификации болезней 10-го пересмотра, квалифицированы как невротические, связанные со стрессом расстройства.
В целом преобладала тревожно-депрессивная симптоматика. Средняя РТ до лечения составила 48,82±0,21; средняя ЛТ – 51,97±0,38. Средний уровень тревоги до лечения составил 14,0±0,1; средний уровень депрессии – 12,41±0,11 (по шкале HADS).
Симптоматическую психофармакотерапию, направленную на купирование ведущего синдрома в структуре заболевания, проводили 492 пациентам. Комплекс медикаментозных мероприятий также включал седативные средства, фитотерапию, поливитамины и адаптогены.
В первую очередь мы воздействовали на симптомы тревоги. Для этого назначали транквилизаторы с выраженным противотревожным действием. Наиболее широкое применение получили: алпразолам 0,0005– 0,001 г, сибазон 0,5% – 2,0 на ночь 3–5 дней. Однако развитие нежелательных явлений при использовании препаратов из группы бензодиазепинов, в том числе сонливости, снижения концентрации, мышечной слабости, значительно ограничивали их применение.
Параллельно с воздействием на тревожную симптоматику или в самостоятельном плане проводили коррекцию аффективных расстройств (у 115 пациентов). Назначали антидепрессанты различных химических групп (табл. 1). Предпочтение отдавали антидепрессантам с минимальным числом побочных эффектов, что давало возможность их использования при проведении «агрессивных» методов специального лечения (химиотерапии и лучевой терапии).
Препаратом выбора был Вальдоксан – первый мелатонинергический антидепрессант, эффективный в отношении всех основных симптомов депрессии [1, 6]. Его широкий спектр эффективности способствовал быстрому восстановлению эмоционального, функционального и социального благополучия, активному вовлечению в лечебный процесс и борьбу с опухолевым заболеванием.
Вальдоксан, будучи антидепрессантом с хронобиотическими свойствами, улучшал функцию сна за счет непосредственного влияния на механизмы регуляции сна, а не вследствие седативного эффекта [1, 6].
Вальдоксан (39 пациентов: 26 женщин, 13 мужчин) назначали по 25 мг на ночь, при необходимости дозу увеличивали до 50 мг. Срок лечения составил от 6 нед до 3 мес.
Первые эффекты, проявляющиеся в уменьшении соматической и психической тревоги, улучшении сна, появлялись уже в 1–2-е сутки приема препарата (рис. 1). Антидепрессивный эффект (оценка по шкале HADS) (рис. 2) появлялся к концу 1-й недели лечения (значительно раньше, чем у антидепрессантов других групп).
У препарата отсутствовали характерные для других антидепрессантов побочные эффекты со стороны сердечно-сосудистой системы, не было отмечено чрезмерной седации, сексуальных дисфункций, увеличения массы тела, подавления аппетита (табл. 2).
Побочные эффекты в виде головокружения (2 больных) и головной боли [1] проявлялись в первые 2 нед лечения, носили краткосрочный характер (см. табл. 2).
Также назначали антидепрессанты серотонинергической структуры (селектра до 10 мг; паксил 10–20 мг; золофт, стимулотон 25–50 мг в сутки), которые вызывали достаточно быстрый терапевтический эффект, заметную редукцию депрессивных расстройств, стабилизировали вегетативный тонус. Препараты данной группы применяли реже в связи с негативным влиянием на аппетит и массу тела, что было нежелательным при проведении специального лечения (см. табл. 2). Часто наблюдали появление тошноты, что еще более ухудшало качество жизни пациентов, страдающих от негативных последствий специального лечения (химиотерапии и лучевой терапии).
Учитывая невысокую стоимость и доступность, использовали амитриптилин, азафен до 50 мг в сутки. Соматорегулирующие эффекты препарата также потенцировали действие анальгетиков, снижали тяжесть телесных ощущений, обусловленных оперативным вмешательством, наличием опухоли или метастазов.
Широкое применение у больных получили препараты, оказывающие мягкое антидепрессивное, анксиолитическое, антиневротическое действие и практически не имеющие побочных эффектов: гелариум до 900 мкг 3 раза в сутки, грандаксин до 6 таблеток в сутки, афобазол до 30 мг в сутки в течение 1 мес.
Для коррекции астенических симптомов в послеоперационном периоде и на химиотерапевтическом лечении пациентам рекомендовали применение энериона по 200 мг 2 раза в сутки в течение 1 мес.
Важным условием реализации лечебно-реабилитационных программ для больных на этапе специального лечения являлось применение сборов трав, изготовленных по рецептам Алтайского онкологического фитоцентра, уменьшающих негативные последствия самого онкологического заболевания и специального лечения.
В медикаментозном лечении также использовались седативные средства, приготовленные из растительного сырья: экстракт валерианы, пустырника, персен, ново-пассит, специальные сборы успокоительных трав, выпускаемые фармацевтической промышленностью. Обязательно назначались адаптогены (родиола розовая, женьшень, элеутерококк по 5–10 капель 2 раза в день), поливитамины с минеральными комплексами (компливит, витрум, центрум, дуовит, триовит и др.).
Оценка клинических и экспериментально-психологических данных после проведения лечебно-реабилитационных программ показала значительное улучшение психического состояния онкологических больных.
Так, у больных с тревожно-депрессивным синдромом выявлялось уменьшение глубины тревожных и депрессивных проявлений, что подтверждалось результатами экспериментально-психологических исследований. Показателями эффективности лечения являлись также стабилизация артериального давления, улучшение сна и аппетита, купирование осложнений, связанных с последствиями хирургического лечения (боли, лимфостаз, ограничение объема движений в конечностях). Пациенты начинали следить за своим внешним видом, активно участвовали в проводимом лечении, в общении с близкими и знакомыми смогли преодолеть внутренний барьер и сообщить им о болезни. При условии удовлетворительного физического состояния больные могли возвратиться к профессиональной деятельности даже при необходимости продолжения специального лечения.
При этом у большинства больных сохранялось чувство неуверенности в благоприятном прогнозе заболевания. Периодически появлялись мысли о собственной ущербности, потере привлекательности, женственности и связанные с этим проблемы в общении с окружающими и в интимной жизни пациентов (ограничение общения, отсутствие, избегание интимных отношений).
РТ после лечения снизилась на 21,3% (с 53,12±0,24 до 41,8±0,33), ЛТ – на 5,2% (с 41,7±0,32 до 39,52±0,27). Уровень тревоги по госпитальной шкале HADS уменьшился на 30,3% (с 17,3±0,18 до 12,05±0,06), уровень депрессии – на 25,4% (с 13,29±0,13 до 9,91±0,05). По данным методики Дембо–Рубинштейн (1970 г.), у всех больных повысился уровень отметки по линиям счастья и здоровья.
У пациентов с депрессивным синдромом после лечения отмечались оптимизация настроения, улучшение сна и аппетита, стабилизация артериального давления, уменьшение болевых ощущений, связанных с последствиями оперативного вмешательства, повышение самооценки, подтверждавшиеся выравниванием экспериментально-психологических данных. Больные проявляли интерес к лечению, своему внешнему виду, общению, чтению, просмотру телепередач, возрастала их физическая активность.
У больных с субдепрессивным синдромом после проведения лечебно-реабилитационных программ улучшались сон, аппетит, возрастала физическая активность. Уменьшались тревожные опасения по поводу соматического состояния, возможных осложнений химиотерапии, лучевой терапии. Больные активно включались в лечебный процесс, что положительно влияло на самооценку и критическое отношение к заболеванию. У пациенток после радикальной мастэктомии отмечалось уменьшение болевого синдрома в верхних конечностях.
Уровень РТ после лечения снизился на 10,8% (с 43,38±0,31 до 38,68±0,3), ЛТ – на 3,2% (с 54,0±0,49 до 52,3±0,51). Уровень тревоги по госпитальной шкале HADS уменьшился на 11,6% (с 10,45±0,33 до 9,24±0,22), депрессии – на 9,6% (с 9,52±0,23 до 8,61±0,19). По данным методики Дембо–Рубинштейн (1970 г.), повышалась самооценка больных по шкалам здоровья и счастья.
В целом РТ снизилась на 16,9% (с 48,82±0,21 до 40,56±0,32) и у всех пациентов соответствовала умеренным показателям, ЛТ – на 11,7% (с 51,97±0,38 до 45,9±0,25). По данным шкалы HADS, наблюдалось снижение выраженности тревоги на 23,4% (с 14,0±0,11 до 0,72±0,09), депрессии – на 21,2% (с 12,41±0,11 до 9,78±0,09) (рис. 3).
Психофармакотерапия во всех случаях была целесообразна и результативна, способствовала сглаживанию или купированию нервно-психических расстройств, что облегчало проведение специального лечения, улучшало психическое и соматическое благополучие онкологических больных и, возможно, прогноз заболевания.
Таким образом, дифференцированное применение комплексных лечебно-реабилитационных мероприятий, включающих психофармакотерапию и психотерапию, позволило судить об их эффективности, подтвержденной клинико-динамическим и экспериментально-психологическим исследованиями.
Сведения об авторе
Комкова Елена Павловна – канд. мед. наук, зав. отд-нием восстановительного лечения ГУЗ Областной клинический онкологический диспансер, врач-психотерапевт высшей категории
Список исп. литературыСкрыть список1. Иванов С.В. Вальдоксан при терапии умеренных и тяжелых депрессий непсихотического уровня в амбулаторной и госпитальной практике. Психиатр. и психофармакотер. 2009; 6: 15–9.
2. Комкова Е.П. Нервно-психические расстройства у онкологических больных на различных этапах лечения (лечебно-реабилитационные аспекты). Автореф. дис. … канд. мед. наук. Томск, 2006; с. 13–7.
3. Комкова Е.П., Кокорина Н.П., Магарилл Ю.А. Психопатологические расстройства на различных этапах онкологических заболеваний и комплексные программы их психотерапевтической и психофармакологической коррекции (методические рекомендации). Кемерово, 2005.
4. Комкова Е.П., Кокорина Н.П., Магарилл Ю.А. Нервно-психические расстройства у онкологических больных (лечебно-реабилитационные аспекты). Сиб. онкол. журн. Томск, 2009; 2 (32): 40–3.
5. Комкова Е.П., Кокорина Н.П., Магарилл Ю.А. Антидепрессанты в лечении нервно-психических расстройств у онкологических больных. Вестник кузбасского научного центра: актуальные вопросы здравоохранения. Кемерово, 2010; 11: 91–2.
6. Смулевич А.Б., Андрющенко А.В., Бескова Д.А. Результаты исследования РИТМ: терапия непсихотических депрессий Вальдоксаном. Психиатр. и психофармакотер. 2010; 4: 4–12.


