Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№03 2012
Эффективность и безопасность Кортексина при лечении астенических расстройств у пациентов кардиологического стационара №03 2012
Номера страниц в выпуске:16-20
В открытом контролируемом клинико-терапевтическом исследовании изучена эффективность препарата Кортексин® при терапии астенических состояний у пациентов кардиологического стационара, страдающих ишемической болезнью сердца и коморбидным астеническим состоянием (по 30 больных в основной и контрольной выборках).
Резюме. В открытом контролируемом клинико-терапевтическом исследовании изучена эффективность препарата Кортексин® при терапии астенических состояний у пациентов кардиологического стационара, страдающих ишемической болезнью сердца и коморбидным астеническим состоянием (по 30 больных в основной и контрольной выборках). Результаты свидетельствуют о высокой эффективности и безопасности Кортексина при лечении широкого круга астенических состояний (соматогенная астения, нозогенные астено-невротические и астено-депрессивные реакции) у пациентов с сердечно-сосудистой патологией. Хорошая переносимость препарата, совместимость с кардиотропной терапией и высокая комплаентность больных позволяет рекомендовать Кортексин® для использования в терапии астенических расстройств в кардиологической практике.
Ключевые слова: Кортексин®, терапия астении.
The efficacy and safety of Cortexin® in the treatment of asthenic
disorders in cardiac inpatients
A.B.Smulevich, B.A.Volel, D.A.Andreyev, E.A.Makukh
I.M.Sechenov First Moscow State Medical University, Ministry of Health and Social Development of the Russian Federation
Summary. The open-label controlled clinical and therapeutic trial investigated the efficacy of Cortexin® in the therapy for asthenic states in cardiac inpatients with coronary heart disease and comorbid asthenic state (30 patients in each study and control groups). The findings suggest that Cortexin® is highly effective and safe in treating a wide range of asthenic states (somatogenic asthenia, nosogenic asthenoneurotic and asthenodepressive reactions) in patients with cardiovascular disease. The good tolerance of the drug, its compatibility with cardiotropic therapy, and high patient compliance permit Cortexin® to be recommended for the therapy of asthenic disorders in cardiac care.
Key words: Cortexin®, therapy of astenia.
Введение
Распространенность астенических расстройств при сердечно-сосудистых заболеваниях (CCЗ) достигает 30% [1], причем повышается доля больных с диагностированными астеническими нарушениями, получающих лечение в условиях общемедицинской практики [2]. Астения1, определяющаяся широким диапазоном субсиндромальных и синдромально завершенных расстройств, является фактором риска негативного прогноза сердечно-сосудистой патологии и снижения качества жизни и работоспособности пациентов.
Астения, сопряженная с кардиальной патологией, формируется вследствие непосредственного влияния ССЗ на центральную нервную систему (ишемическая болезнь сердца – ИБС, атеросклероз церебральных артерий, гипертоническая болезнь – ГБ, анемия, хирургические вмешательства – аортокоронарное шунтирование – АКШ, стентирование) и представляет собой один из наиболее распространенных типов соматогений. Проявления астении могут выступать уже в продроме и персистировать на всем протяжении заболевания. В некоторых случаях астения отчетливо проявляется лишь в период реконвалесценции – после прекращения острых проявлений сердечно-сосудистой патологии. При лечении астении в качестве препаратов выбора традиционно рассматриваются ноотропы, транквилизаторы и психостимуляторы. Однако в настоящее время представляется бесспорным тот факт, что назначение этих средств связано с целым рядом ограничений. Последние вытекают из нежелательных явлений, сопряженных с развитием явлений зависимости, синдрома отмены, а также другими рисками, обусловленными основным соматическим заболеванием.
В качестве средства, эффективного и безопасного при терапии астении, коморбидной сердечно-сосудистой патологии, позиционируется отечественный препарат Кортексин® [3].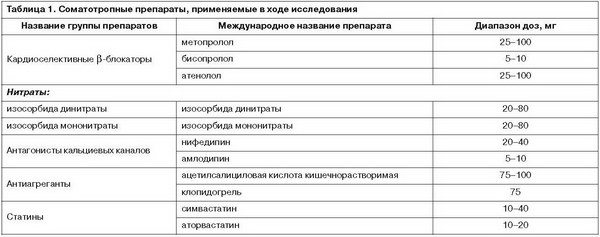
 Кортексин® относится к группе пептидов с низкой молекулярной массой, активно участвующих в межклеточном взаимодействии [4] и обладающих выраженной тканеспецифичной активностью. Согласно экспериментальным и клиническим данным Кортексин® способствует нормализации обмена нейромедиаторов в ткани мозга и обладает антиоксидантной активностью. Механизм действия Кортексина связан с метаболической активностью входящих в его состав пептидов, пулученных из коры головного мозга скота. Препарат регулирует соотношение тормозных и возбуждающих аминокислот серотонина и дофамина, оказывает ГАМКергическое воздействие, обладает антиоксидантной активностью и способностью восстанавливать биоэлектрическую активность головного мозга. По некоторым данным [5], Кортексин® оказывает нейропротекторное действие, улучшает память и работоспособность больных с дисциркуляторной энцефалопатией.
Кортексин® относится к группе пептидов с низкой молекулярной массой, активно участвующих в межклеточном взаимодействии [4] и обладающих выраженной тканеспецифичной активностью. Согласно экспериментальным и клиническим данным Кортексин® способствует нормализации обмена нейромедиаторов в ткани мозга и обладает антиоксидантной активностью. Механизм действия Кортексина связан с метаболической активностью входящих в его состав пептидов, пулученных из коры головного мозга скота. Препарат регулирует соотношение тормозных и возбуждающих аминокислот серотонина и дофамина, оказывает ГАМКергическое воздействие, обладает антиоксидантной активностью и способностью восстанавливать биоэлектрическую активность головного мозга. По некоторым данным [5], Кортексин® оказывает нейропротекторное действие, улучшает память и работоспособность больных с дисциркуляторной энцефалопатией.
В связи с изложенными выше фактами представляется актуальным проведение исследования эффективности и переносимости Кортексина при лечении широкого круга астенических состояний у пациентов с сердечно-сосудистой патологией.
Цель исследования – оценка эффективности, безопасности и переносимости Кортексина при лечении широкого круга астенических нарушений, формирующихся у пациентов с сердечно-сосудистой патологией. Задачами исследования явились изучение эффективности Кортексина с помощью клинического и психометрического обследования; оценка безопасности и переносимости Кортексина с привлечением данных соматического обследования пациентов; анализ влияния терапии Кортексином на показатели комплаентности к соматотропной терапии; изучение переносимости комбинированной соматотропной и психотропной терапии.
Материалы и методы исследования
Обследовались мужчины и женщины в возрасте от 18 до 65 лет, находящиеся на лечении в Клинике кардиологии (дир. – проф. А.Л.Сыркин) Университетской клинической больницы №1 Первого МГМУ им. И.М.Сеченова с верифицированным диагнозом: ИБС, стенокардия напряжения I–III функционального класса (ФК), постинфарктный кардиосклероз, состояние после АКШ, сопутствующая ГБ I–II стадии (уровень артериального давления – АД до 179/109 мм рт. ст. включительно), I–III стадии. Наличие в клинической картине коморбидной ССЗ астенической/астеноневротической симптоматики: астения БДУ (R53.0), неврастения (F48.0), недомогание и утомляемость (R54.0). Выраженность астении по шкале самооценки астении (MFI-20) более 50 баллов; по визуальной аналоговой шкале астении (VAS-A) более 5 баллов.
Представляемое рандомизированное открытое контролируемое клинико-терапевтическое исследование проводилось в 2 параллельных группах (основная и контрольная) и состояло из 2 фаз (диагностическая и терапевтическая). Рандомизация проводилась методом конвертов с помощью таблиц случайных чисел. Врачом-исследователем были сформированы 2 выборки, сопоставимые по полу, возрасту, проявлениям ССЗ и психическим расстройствам: 1) основная группа – 30 пациентов, получавшие Кортексин® в сочетании с базисной кардиотропной терапией; 2) контрольная группа – 30 пациентов, получавшие базисную кардиотропную терапию (без Кортексина).
Исследование предполагало пребывание пациента в стационаре в течение всего 10-дневного периода введения Кортексина. По окончании этого срока допускалась выписка пациента (по решению лечащего врача стационара). В этом случае пациент приглашался на амбулаторный визит на 20-й день от начала исследования для оценки окончательных результатов лечения.
Больные контрольной выборки (30 наблюдений) получали рекомендованную базисную кардиотропную терапию.
Для пациентов 2 выборок обследование проводилось по соответствующей схеме в течение всего периода исследования – Д (день) 0 (скрининг), Д1 (начало терапии Кортексином), Д10 (завершение терапии Кортексином), Д20 (оценка результатов – визит follow-up); прием препарата строго по установленной схеме.
Оценка эффективности терапии проводилась по результатам лечения пациентов, прошедших полный курс терапии Кортексином (в сравнении с пациентами контрольной группы). Если по той или иной причине лечение прекращалось до визита 2 (Д10), пациент не включался в анализ.
Основными критериями эффективности препарата были оценка динамики астенической симптоматики по шкале самооценки астении (MFI-20), визуальной аналоговой шкале астении (VAS-A). Для оценки общего состояния пациента использовалась шкала общего клинического впечатления (CGI – подшкала CGI-S).
Результаты исследования и обсуждение
В исследование включены 60 пациентов (23 мужчины, 37 женщин; средний возраст 59,5±8,3 года), находящихся на стационарном лечении по поводу сердечно-сосудистой патологии (ИБС, фибрилляции предсер-дий – ФП и ГБ) с коморбидными астеническими нарушениями (соматогенная астения, нозогенные астено-невротические и астено-депрессивные реакции).
В исследование включены 60 пациентов с диагнозом: стенокардия напряжения II ФК – 12 (20%) больных, стенокардия напряжения III ФК – 18 (30%) больных, постинфарктный кардиосклероз – 13 (21,7%) больных. Срок после перенесенного инфаркта миокарда – от 2 мес до 14 лет. У 17 из 60 (28,3%) пациентов зарегистрирована ФП (пароксизмальная форма – 9, постоянная форма – 8 наблюдений).
У 37 (61,7%) отмечена сопутствующая недостаточность кровообращения (НК): стадия IIА – 19 (51,4%) больных, стадия IIБ – 18 (48,6%) больных. У 31 (51,7%) пациента диагностирована сопутствующая ГБ (II стадия – 21, III стадия – 10 больных). Диагноз и синдромальная структура астенических расстройств в изученных наблюдениях (60 пациентов) распределялись следующим образом: соматогенная астения – 41 (68,3%) наблюдение, нозогенная астено-невротическая реакция – 10 (16,7%) наблюдений, нозогенная астено-депрессивная реакция – 9 (15%) наблюдений.
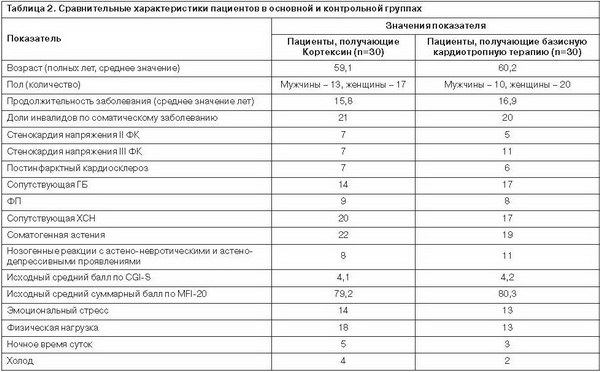
В основной группе (30 пациентов) отмечено следующее распределение по формам сердечно-сосудистой патологии (табл. 2): стенокардия напряжения II ФК – 7 пациентов, стенокардия напряжения III ФК – 7 пациентов, постинфарктный кардиосклероз – 7 пациентов, период после перенесенного инфаркта миокарда – от 2 мес до 14 лет.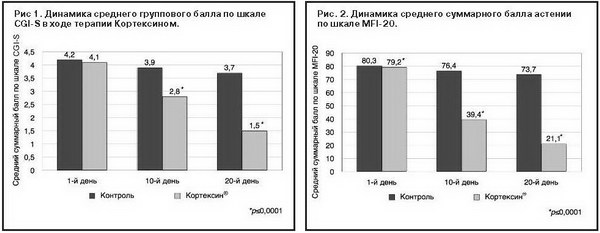 ФП отмечена у 9 пациентов: пароксизмальная форма ФП – у 5 больных, постоянная форма ФП – у 4 больных. Хроническая сердечная недостаточность (ХСН) кровообращения отмечена у 20 пациентов основной выборки: НК ХСН IIА стадии – у 11 больных, НК ХСН IIБ стадии – у 9 больных. Сопутствующая ГБ (на фоне ИБС) отмечалась у 14 пациентов: II стадия ГБ – у 10 больных, III стадия ГБ – у 4 больных. Диагноз и синдромальная структура астенического расстройства в основной выборке распределялись следующим образом: соматогенная астения – 22 наблюдения, нозогенная астено-невротическая реакция – 5 наблюдений, нозогенная астено-депрессивная реакция – 3 наблюдения.
ФП отмечена у 9 пациентов: пароксизмальная форма ФП – у 5 больных, постоянная форма ФП – у 4 больных. Хроническая сердечная недостаточность (ХСН) кровообращения отмечена у 20 пациентов основной выборки: НК ХСН IIА стадии – у 11 больных, НК ХСН IIБ стадии – у 9 больных. Сопутствующая ГБ (на фоне ИБС) отмечалась у 14 пациентов: II стадия ГБ – у 10 больных, III стадия ГБ – у 4 больных. Диагноз и синдромальная структура астенического расстройства в основной выборке распределялись следующим образом: соматогенная астения – 22 наблюдения, нозогенная астено-невротическая реакция – 5 наблюдений, нозогенная астено-депрессивная реакция – 3 наблюдения.
В контрольной группе (30 пациентов) отмечено сходное с основной выборкой распределение по формам кардиальной патологии (см. табл. 2): стенокардия напряжения II ФК – 5 пациентов; стенокардия напряжения III ФК – 11 пациентов; постинфарктный кардиосклероз – 6 пациентов, период после перенесенного инфаркта миокарда – от 3 мес до 14 лет. ФП – у 8 пациентов, пароксизмальная форма ФП – у 4 больных; постоянная форма ФП – у 4 пациентов. ХСН кровообращения отмечена у 17 пациентов контрольной выборки: НК ХСН IIА стадии – у 8 больных, НК ХСН IIБ стадии – у 9 больных. Сопутствующая ГБ у 17 пациентов: II стадия ГБ – у 11 больных; III стадия ГБ – у 6 пациентов.
Отмечено также сходное с основной выборкой распределение астенических расстройств по диагнозу и синдромальной структуре: соматогенная астения – 19 наблюдений, нозогенная астено-невротическая реакция – 5 наблюдений, нозогенная астено-депрессивная реакция – 6 наблюдений.
Таким образом, данные о долевом распределении соматических синдромов свидетельствуют о сопоставимости основной и контрольной групп. Распределение факторов, провоцирующих ухудшение состояния (эмоциональный стресс, физическая нагрузка, ночное время суток, холод), обнаружило некоторые отличия (см. табл. 2), однако они не были клинически значимыми и не оказывали влияния на подходы и методы терапии астенических расстройств Кортексином в динамике, а также на окончательный результат лечения. По ключевым социодемографическим, клиническим и психометрическим параметрам (исходный балл CGI-S, MFI-20, VAS) основная и контрольная группы сопоставимы (см. табл. 2).
По результатам лечения Кортексином пациентов основной группы с широким кругом астенических расстройств на фоне сердечно-сосудистой патологии получены следующие данные об эффективности и переносимости препарата.
Показатели динамики среднего суммарного балла по шкале CGI-S продемонстрировали следующие результаты. Достоверные межгрупповые различия (р≤0,0001) регистрируются достаточно быстро – уже на 2-й неделе терапии, к 10-му дню. Если в начале терапии исходный балл в группах свидетельствовал о преобладании умеренно выраженных астенических нарушений, то к 10-му дню в основной выборке отмечено существенное улучшение с преобладанием «пограничных» нарушений. При окончательной оценке результатов исследования (20-й день – визит follow-up) отмечается дальнейшая редукция астенических расстройств до уровня «легкой степени» нарушений или их «отсутствия» (рис. 1).
Важно отметить, что такого рода устойчивый положительный эффект при терапии астенических состояний Кортексином, возможно, объясняется пролонгированным действием препарата.
Анализ доли респондеров по шкале CGI-S также выявил значимые (р<0,05) различия между основной и контрольной группами.
Сравнительная оценка динамики средних общих баллов по шкале MFI-20 на визитах исследования (рис. 2) также выявила различия выраженности астении в основной и контрольной выборках. Статистически значимые межгрупповые различия достигаются с очень высокой степенью достоверности (р≤0,0001) к концу 10-го дня терапии: 76,4 балла в контрольной группе против 39,4 балла в основной. При этом к 20-му дню исследования (окончательная оценка результатов) соответствующие показатели составили 73,7 балла против 21,1 балла.
Необходимо отметить, что уже к 10-му дню исследования наблюдались статистически достоверные (р≤0,0001) изменения в основной группе (Кортексин®) по субшкалам теста: «общая астения», «пониженная активность», «снижение мотивации», «физическая астения». В контрольной группе не отмечалось значимых изменений ни по одной из субшкал теста.
Анализ внутригрупповой и межгрупповой динамики по субшкалам VAS-A «физическая астения» и «психическая астения» выявил следующее. Средний балл по шкале VAS-A в ходе терапии статистически значимо снижается в группе Кортексина уже к 10-му дню терапии (р≤0,05) по сравнению со стартовым визитом по субшкалам теста: «общая астения», «пониженная активность», «снижение мотивации», «физическая астения».
С очень высокой степенью достоверности (р≤0,0001) различия между группами Кортексина и контроля по субшкалам VAS-A «физическая астения» и «психическая астения» регистрируются к 20-му дню терапии.
Анализ клинической динамики и жалоб пациентов показал также отсутствие влияния терапии Кортексином на жалобы и симптомы, связанные с соматической патологией, включая кардиалгии при стенокардии и проявления аритмии. При этом у большинства больных основной группы– 23 (76,7%) наблюдения отмечена положительная динамика в отношении астенических симптомов. У больных с соматогенной астенией в большинстве – 86,3% (19 из 22 пациентов) случаев уже к 7–10-му дню терапии отмечалось повышение физической активности при снижении истощаемости в дневные часы, затрудняющей повседневную активность.
У больных с нозогенными астено-невротическими и астено-депрессивными расстройствами также в большинстве наблюдений (87,5% – 7 из 8 пациентов) уже в первые 3–5 дней терапии (в субъективной оценке пациентов) отмечено уменьшение проявлений раздражительной слабости и связанных с этим синдромом повышенной тревожности и мнительности, эмоциональной лабильности, чувствительности к воздействию стрессорных факторов (нозогенных или психосоциальных), что облегчало взаимодействие пациента с кардиологом и улучшало приверженность терапии.
Результаты исследования свидетельствуют об эффективности использования адекватной психофармакотерапии для улучшения психического состояния и качества жизни больных с ССЗ, а также более быстрой стабилизации соматического состояния. В качестве дополнительного преимущества Кортексина выступает высокая согласованность субъективных (мнение пациента) и объективных (мнение врача) оценок результатов терапии, что позволяет прогнозировать высокую комплаентность больных.
В изученной группе достоверных изменений лабораторных показателей, а также инструментальных методов обследования до и после лечения Кортексином получено не было. Прием Кортексина не влиял на показатели как общего (гемоглобин, лейкоциты, СОЭ), так и биохимического анализов крови.
Безопасность определяли путем оценки нежелательных явлений и отклонений лабораторных показателей, степени их выраженности, серьезности, длительности и возможной связи с терапией Кортексином.
Препарат продемонстрировал хорошую переносимость: побочных эффектов (взбудораженность, тахикардия, повышение АД, сокращение продолжительности сна или изменение его привычного ритма), а также аллергических реакций не зарегистрировано.
Полученные данные свидетельствуют о высоком уровне безопасности и хорошей переносимости Кортексина при лечении широкого спектра астенических состояний, формирующихся у пациентов с сердечно-сосудистой патологией.
Заключение
Результаты исследования свидетельствуют о высокой эффективности и безопасности препарата Кортексин® при лечении широкого круга астенических состояний (соматогенная астения, нозогенные астено-невротические и астено-депрессивные реакции) у пациентов с сердечно-сосудистой патологией. Учитывая хорошую переносимость препарата, совместимость с кардиотропной терапией и высокую комплаентность больных, препарат Кортексин® может быть рекомендован для использования в терапии астенических расстройств у пациентов с ССЗ.
1Астения – психопатологическое расстройство, картина которого определяется явлениями повышенной физической и/или психической утомляемости со снижением уровня активности (дефицит бодрости, энергии, мотивации), влекущим за собой клинически и социально значимые последствия: потребность в дополнительном отдыхе, снижение объема и эффективности деятельности (даже привычной). Астенический комплекс включает полиморфные невротические проявления (мышечные боли, головные боли напряжения, головокружения, диспептические нарушения, инсомния).
2В период активного лечения по данной программе не проводилась титрация статинов.
Сведения об авторах
Смулевич Анатолий Болеславович – д-р мед. наук, проф., акад. РАМН, зав. психосоматическим отд-нием ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава РФ
Волель Беатриса Альбертовна – д-р мед. наук, проф. каф. психиатрии и психосоматики ФППОВ ГБОУ ВПО
Первый МГМУ им. И.М.Сеченова Минздрава РФ
Андреев Денис Анатольевич – д-р мед. наук, проф., зав. отд-нием клиники кардиологии (директор – проф. А.Л.Сыркин) УКБ №1 Первого МГМУ им. И.М.Сеченова Минздрава РФ
Макух Елена Александровна – врач-психиатр психосоматического отд-ния ГБОУ ВПО Первый МГМУ
им. И.М.Сеченова Минздрава РФ
Ключевые слова: Кортексин®, терапия астении.
The efficacy and safety of Cortexin® in the treatment of asthenic
disorders in cardiac inpatients
A.B.Smulevich, B.A.Volel, D.A.Andreyev, E.A.Makukh
I.M.Sechenov First Moscow State Medical University, Ministry of Health and Social Development of the Russian Federation
Summary. The open-label controlled clinical and therapeutic trial investigated the efficacy of Cortexin® in the therapy for asthenic states in cardiac inpatients with coronary heart disease and comorbid asthenic state (30 patients in each study and control groups). The findings suggest that Cortexin® is highly effective and safe in treating a wide range of asthenic states (somatogenic asthenia, nosogenic asthenoneurotic and asthenodepressive reactions) in patients with cardiovascular disease. The good tolerance of the drug, its compatibility with cardiotropic therapy, and high patient compliance permit Cortexin® to be recommended for the therapy of asthenic disorders in cardiac care.
Key words: Cortexin®, therapy of astenia.
Введение
Распространенность астенических расстройств при сердечно-сосудистых заболеваниях (CCЗ) достигает 30% [1], причем повышается доля больных с диагностированными астеническими нарушениями, получающих лечение в условиях общемедицинской практики [2]. Астения1, определяющаяся широким диапазоном субсиндромальных и синдромально завершенных расстройств, является фактором риска негативного прогноза сердечно-сосудистой патологии и снижения качества жизни и работоспособности пациентов.
Астения, сопряженная с кардиальной патологией, формируется вследствие непосредственного влияния ССЗ на центральную нервную систему (ишемическая болезнь сердца – ИБС, атеросклероз церебральных артерий, гипертоническая болезнь – ГБ, анемия, хирургические вмешательства – аортокоронарное шунтирование – АКШ, стентирование) и представляет собой один из наиболее распространенных типов соматогений. Проявления астении могут выступать уже в продроме и персистировать на всем протяжении заболевания. В некоторых случаях астения отчетливо проявляется лишь в период реконвалесценции – после прекращения острых проявлений сердечно-сосудистой патологии. При лечении астении в качестве препаратов выбора традиционно рассматриваются ноотропы, транквилизаторы и психостимуляторы. Однако в настоящее время представляется бесспорным тот факт, что назначение этих средств связано с целым рядом ограничений. Последние вытекают из нежелательных явлений, сопряженных с развитием явлений зависимости, синдрома отмены, а также другими рисками, обусловленными основным соматическим заболеванием.
В качестве средства, эффективного и безопасного при терапии астении, коморбидной сердечно-сосудистой патологии, позиционируется отечественный препарат Кортексин® [3].


 Кортексин® относится к группе пептидов с низкой молекулярной массой, активно участвующих в межклеточном взаимодействии [4] и обладающих выраженной тканеспецифичной активностью. Согласно экспериментальным и клиническим данным Кортексин® способствует нормализации обмена нейромедиаторов в ткани мозга и обладает антиоксидантной активностью. Механизм действия Кортексина связан с метаболической активностью входящих в его состав пептидов, пулученных из коры головного мозга скота. Препарат регулирует соотношение тормозных и возбуждающих аминокислот серотонина и дофамина, оказывает ГАМКергическое воздействие, обладает антиоксидантной активностью и способностью восстанавливать биоэлектрическую активность головного мозга. По некоторым данным [5], Кортексин® оказывает нейропротекторное действие, улучшает память и работоспособность больных с дисциркуляторной энцефалопатией.
Кортексин® относится к группе пептидов с низкой молекулярной массой, активно участвующих в межклеточном взаимодействии [4] и обладающих выраженной тканеспецифичной активностью. Согласно экспериментальным и клиническим данным Кортексин® способствует нормализации обмена нейромедиаторов в ткани мозга и обладает антиоксидантной активностью. Механизм действия Кортексина связан с метаболической активностью входящих в его состав пептидов, пулученных из коры головного мозга скота. Препарат регулирует соотношение тормозных и возбуждающих аминокислот серотонина и дофамина, оказывает ГАМКергическое воздействие, обладает антиоксидантной активностью и способностью восстанавливать биоэлектрическую активность головного мозга. По некоторым данным [5], Кортексин® оказывает нейропротекторное действие, улучшает память и работоспособность больных с дисциркуляторной энцефалопатией.
В связи с изложенными выше фактами представляется актуальным проведение исследования эффективности и переносимости Кортексина при лечении широкого круга астенических состояний у пациентов с сердечно-сосудистой патологией.
Цель исследования – оценка эффективности, безопасности и переносимости Кортексина при лечении широкого круга астенических нарушений, формирующихся у пациентов с сердечно-сосудистой патологией. Задачами исследования явились изучение эффективности Кортексина с помощью клинического и психометрического обследования; оценка безопасности и переносимости Кортексина с привлечением данных соматического обследования пациентов; анализ влияния терапии Кортексином на показатели комплаентности к соматотропной терапии; изучение переносимости комбинированной соматотропной и психотропной терапии.
Материалы и методы исследования
Обследовались мужчины и женщины в возрасте от 18 до 65 лет, находящиеся на лечении в Клинике кардиологии (дир. – проф. А.Л.Сыркин) Университетской клинической больницы №1 Первого МГМУ им. И.М.Сеченова с верифицированным диагнозом: ИБС, стенокардия напряжения I–III функционального класса (ФК), постинфарктный кардиосклероз, состояние после АКШ, сопутствующая ГБ I–II стадии (уровень артериального давления – АД до 179/109 мм рт. ст. включительно), I–III стадии. Наличие в клинической картине коморбидной ССЗ астенической/астеноневротической симптоматики: астения БДУ (R53.0), неврастения (F48.0), недомогание и утомляемость (R54.0). Выраженность астении по шкале самооценки астении (MFI-20) более 50 баллов; по визуальной аналоговой шкале астении (VAS-A) более 5 баллов.
Представляемое рандомизированное открытое контролируемое клинико-терапевтическое исследование проводилось в 2 параллельных группах (основная и контрольная) и состояло из 2 фаз (диагностическая и терапевтическая). Рандомизация проводилась методом конвертов с помощью таблиц случайных чисел. Врачом-исследователем были сформированы 2 выборки, сопоставимые по полу, возрасту, проявлениям ССЗ и психическим расстройствам: 1) основная группа – 30 пациентов, получавшие Кортексин® в сочетании с базисной кардиотропной терапией; 2) контрольная группа – 30 пациентов, получавшие базисную кардиотропную терапию (без Кортексина).
Исследование предполагало пребывание пациента в стационаре в течение всего 10-дневного периода введения Кортексина. По окончании этого срока допускалась выписка пациента (по решению лечащего врача стационара). В этом случае пациент приглашался на амбулаторный визит на 20-й день от начала исследования для оценки окончательных результатов лечения.
Больные контрольной выборки (30 наблюдений) получали рекомендованную базисную кардиотропную терапию.
Для пациентов 2 выборок обследование проводилось по соответствующей схеме в течение всего периода исследования – Д (день) 0 (скрининг), Д1 (начало терапии Кортексином), Д10 (завершение терапии Кортексином), Д20 (оценка результатов – визит follow-up); прием препарата строго по установленной схеме.
Оценка эффективности терапии проводилась по результатам лечения пациентов, прошедших полный курс терапии Кортексином (в сравнении с пациентами контрольной группы). Если по той или иной причине лечение прекращалось до визита 2 (Д10), пациент не включался в анализ.
Основными критериями эффективности препарата были оценка динамики астенической симптоматики по шкале самооценки астении (MFI-20), визуальной аналоговой шкале астении (VAS-A). Для оценки общего состояния пациента использовалась шкала общего клинического впечатления (CGI – подшкала CGI-S).
Результаты исследования и обсуждение
В исследование включены 60 пациентов (23 мужчины, 37 женщин; средний возраст 59,5±8,3 года), находящихся на стационарном лечении по поводу сердечно-сосудистой патологии (ИБС, фибрилляции предсер-дий – ФП и ГБ) с коморбидными астеническими нарушениями (соматогенная астения, нозогенные астено-невротические и астено-депрессивные реакции).
В исследование включены 60 пациентов с диагнозом: стенокардия напряжения II ФК – 12 (20%) больных, стенокардия напряжения III ФК – 18 (30%) больных, постинфарктный кардиосклероз – 13 (21,7%) больных. Срок после перенесенного инфаркта миокарда – от 2 мес до 14 лет. У 17 из 60 (28,3%) пациентов зарегистрирована ФП (пароксизмальная форма – 9, постоянная форма – 8 наблюдений).
У 37 (61,7%) отмечена сопутствующая недостаточность кровообращения (НК): стадия IIА – 19 (51,4%) больных, стадия IIБ – 18 (48,6%) больных. У 31 (51,7%) пациента диагностирована сопутствующая ГБ (II стадия – 21, III стадия – 10 больных). Диагноз и синдромальная структура астенических расстройств в изученных наблюдениях (60 пациентов) распределялись следующим образом: соматогенная астения – 41 (68,3%) наблюдение, нозогенная астено-невротическая реакция – 10 (16,7%) наблюдений, нозогенная астено-депрессивная реакция – 9 (15%) наблюдений.
В основной группе (30 пациентов) отмечено следующее распределение по формам сердечно-сосудистой патологии (табл. 2): стенокардия напряжения II ФК – 7 пациентов, стенокардия напряжения III ФК – 7 пациентов, постинфарктный кардиосклероз – 7 пациентов, период после перенесенного инфаркта миокарда – от 2 мес до 14 лет.
 ФП отмечена у 9 пациентов: пароксизмальная форма ФП – у 5 больных, постоянная форма ФП – у 4 больных. Хроническая сердечная недостаточность (ХСН) кровообращения отмечена у 20 пациентов основной выборки: НК ХСН IIА стадии – у 11 больных, НК ХСН IIБ стадии – у 9 больных. Сопутствующая ГБ (на фоне ИБС) отмечалась у 14 пациентов: II стадия ГБ – у 10 больных, III стадия ГБ – у 4 больных. Диагноз и синдромальная структура астенического расстройства в основной выборке распределялись следующим образом: соматогенная астения – 22 наблюдения, нозогенная астено-невротическая реакция – 5 наблюдений, нозогенная астено-депрессивная реакция – 3 наблюдения.
ФП отмечена у 9 пациентов: пароксизмальная форма ФП – у 5 больных, постоянная форма ФП – у 4 больных. Хроническая сердечная недостаточность (ХСН) кровообращения отмечена у 20 пациентов основной выборки: НК ХСН IIА стадии – у 11 больных, НК ХСН IIБ стадии – у 9 больных. Сопутствующая ГБ (на фоне ИБС) отмечалась у 14 пациентов: II стадия ГБ – у 10 больных, III стадия ГБ – у 4 больных. Диагноз и синдромальная структура астенического расстройства в основной выборке распределялись следующим образом: соматогенная астения – 22 наблюдения, нозогенная астено-невротическая реакция – 5 наблюдений, нозогенная астено-депрессивная реакция – 3 наблюдения.
В контрольной группе (30 пациентов) отмечено сходное с основной выборкой распределение по формам кардиальной патологии (см. табл. 2): стенокардия напряжения II ФК – 5 пациентов; стенокардия напряжения III ФК – 11 пациентов; постинфарктный кардиосклероз – 6 пациентов, период после перенесенного инфаркта миокарда – от 3 мес до 14 лет. ФП – у 8 пациентов, пароксизмальная форма ФП – у 4 больных; постоянная форма ФП – у 4 пациентов. ХСН кровообращения отмечена у 17 пациентов контрольной выборки: НК ХСН IIА стадии – у 8 больных, НК ХСН IIБ стадии – у 9 больных. Сопутствующая ГБ у 17 пациентов: II стадия ГБ – у 11 больных; III стадия ГБ – у 6 пациентов.
Отмечено также сходное с основной выборкой распределение астенических расстройств по диагнозу и синдромальной структуре: соматогенная астения – 19 наблюдений, нозогенная астено-невротическая реакция – 5 наблюдений, нозогенная астено-депрессивная реакция – 6 наблюдений.
Таким образом, данные о долевом распределении соматических синдромов свидетельствуют о сопоставимости основной и контрольной групп. Распределение факторов, провоцирующих ухудшение состояния (эмоциональный стресс, физическая нагрузка, ночное время суток, холод), обнаружило некоторые отличия (см. табл. 2), однако они не были клинически значимыми и не оказывали влияния на подходы и методы терапии астенических расстройств Кортексином в динамике, а также на окончательный результат лечения. По ключевым социодемографическим, клиническим и психометрическим параметрам (исходный балл CGI-S, MFI-20, VAS) основная и контрольная группы сопоставимы (см. табл. 2).
По результатам лечения Кортексином пациентов основной группы с широким кругом астенических расстройств на фоне сердечно-сосудистой патологии получены следующие данные об эффективности и переносимости препарата.
Показатели динамики среднего суммарного балла по шкале CGI-S продемонстрировали следующие результаты. Достоверные межгрупповые различия (р≤0,0001) регистрируются достаточно быстро – уже на 2-й неделе терапии, к 10-му дню. Если в начале терапии исходный балл в группах свидетельствовал о преобладании умеренно выраженных астенических нарушений, то к 10-му дню в основной выборке отмечено существенное улучшение с преобладанием «пограничных» нарушений. При окончательной оценке результатов исследования (20-й день – визит follow-up) отмечается дальнейшая редукция астенических расстройств до уровня «легкой степени» нарушений или их «отсутствия» (рис. 1).
Важно отметить, что такого рода устойчивый положительный эффект при терапии астенических состояний Кортексином, возможно, объясняется пролонгированным действием препарата.
Анализ доли респондеров по шкале CGI-S также выявил значимые (р<0,05) различия между основной и контрольной группами.
Сравнительная оценка динамики средних общих баллов по шкале MFI-20 на визитах исследования (рис. 2) также выявила различия выраженности астении в основной и контрольной выборках. Статистически значимые межгрупповые различия достигаются с очень высокой степенью достоверности (р≤0,0001) к концу 10-го дня терапии: 76,4 балла в контрольной группе против 39,4 балла в основной. При этом к 20-му дню исследования (окончательная оценка результатов) соответствующие показатели составили 73,7 балла против 21,1 балла.
Необходимо отметить, что уже к 10-му дню исследования наблюдались статистически достоверные (р≤0,0001) изменения в основной группе (Кортексин®) по субшкалам теста: «общая астения», «пониженная активность», «снижение мотивации», «физическая астения». В контрольной группе не отмечалось значимых изменений ни по одной из субшкал теста.
Анализ внутригрупповой и межгрупповой динамики по субшкалам VAS-A «физическая астения» и «психическая астения» выявил следующее. Средний балл по шкале VAS-A в ходе терапии статистически значимо снижается в группе Кортексина уже к 10-му дню терапии (р≤0,05) по сравнению со стартовым визитом по субшкалам теста: «общая астения», «пониженная активность», «снижение мотивации», «физическая астения».
С очень высокой степенью достоверности (р≤0,0001) различия между группами Кортексина и контроля по субшкалам VAS-A «физическая астения» и «психическая астения» регистрируются к 20-му дню терапии.
Анализ клинической динамики и жалоб пациентов показал также отсутствие влияния терапии Кортексином на жалобы и симптомы, связанные с соматической патологией, включая кардиалгии при стенокардии и проявления аритмии. При этом у большинства больных основной группы– 23 (76,7%) наблюдения отмечена положительная динамика в отношении астенических симптомов. У больных с соматогенной астенией в большинстве – 86,3% (19 из 22 пациентов) случаев уже к 7–10-му дню терапии отмечалось повышение физической активности при снижении истощаемости в дневные часы, затрудняющей повседневную активность.
У больных с нозогенными астено-невротическими и астено-депрессивными расстройствами также в большинстве наблюдений (87,5% – 7 из 8 пациентов) уже в первые 3–5 дней терапии (в субъективной оценке пациентов) отмечено уменьшение проявлений раздражительной слабости и связанных с этим синдромом повышенной тревожности и мнительности, эмоциональной лабильности, чувствительности к воздействию стрессорных факторов (нозогенных или психосоциальных), что облегчало взаимодействие пациента с кардиологом и улучшало приверженность терапии.
Результаты исследования свидетельствуют об эффективности использования адекватной психофармакотерапии для улучшения психического состояния и качества жизни больных с ССЗ, а также более быстрой стабилизации соматического состояния. В качестве дополнительного преимущества Кортексина выступает высокая согласованность субъективных (мнение пациента) и объективных (мнение врача) оценок результатов терапии, что позволяет прогнозировать высокую комплаентность больных.
В изученной группе достоверных изменений лабораторных показателей, а также инструментальных методов обследования до и после лечения Кортексином получено не было. Прием Кортексина не влиял на показатели как общего (гемоглобин, лейкоциты, СОЭ), так и биохимического анализов крови.
Безопасность определяли путем оценки нежелательных явлений и отклонений лабораторных показателей, степени их выраженности, серьезности, длительности и возможной связи с терапией Кортексином.
Препарат продемонстрировал хорошую переносимость: побочных эффектов (взбудораженность, тахикардия, повышение АД, сокращение продолжительности сна или изменение его привычного ритма), а также аллергических реакций не зарегистрировано.
Полученные данные свидетельствуют о высоком уровне безопасности и хорошей переносимости Кортексина при лечении широкого спектра астенических состояний, формирующихся у пациентов с сердечно-сосудистой патологией.
Заключение
Результаты исследования свидетельствуют о высокой эффективности и безопасности препарата Кортексин® при лечении широкого круга астенических состояний (соматогенная астения, нозогенные астено-невротические и астено-депрессивные реакции) у пациентов с сердечно-сосудистой патологией. Учитывая хорошую переносимость препарата, совместимость с кардиотропной терапией и высокую комплаентность больных, препарат Кортексин® может быть рекомендован для использования в терапии астенических расстройств у пациентов с ССЗ.
1Астения – психопатологическое расстройство, картина которого определяется явлениями повышенной физической и/или психической утомляемости со снижением уровня активности (дефицит бодрости, энергии, мотивации), влекущим за собой клинически и социально значимые последствия: потребность в дополнительном отдыхе, снижение объема и эффективности деятельности (даже привычной). Астенический комплекс включает полиморфные невротические проявления (мышечные боли, головные боли напряжения, головокружения, диспептические нарушения, инсомния).
2В период активного лечения по данной программе не проводилась титрация статинов.
Сведения об авторах
Смулевич Анатолий Болеславович – д-р мед. наук, проф., акад. РАМН, зав. психосоматическим отд-нием ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава РФ
Волель Беатриса Альбертовна – д-р мед. наук, проф. каф. психиатрии и психосоматики ФППОВ ГБОУ ВПО
Первый МГМУ им. И.М.Сеченова Минздрава РФ
Андреев Денис Анатольевич – д-р мед. наук, проф., зав. отд-нием клиники кардиологии (директор – проф. А.Л.Сыркин) УКБ №1 Первого МГМУ им. И.М.Сеченова Минздрава РФ
Макух Елена Александровна – врач-психиатр психосоматического отд-ния ГБОУ ВПО Первый МГМУ
им. И.М.Сеченова Минздрава РФ
Список исп. литературыСкрыть список1. De Jonge P, Ormel J. Depression and anxiety after myocardial infarction. Br J Psychiat 2007; 190: 272–3.
2. Андрющенко А.В., Смулевич А.Б., Романов Д.В. Пограничные психические и психосоматические расстройства в общей медицине (эпидемиологические аспекты). В кн. Психические расстройства в клинической практике. М., 2011.
3. Скоромец А.А., Дьяконов М.М. Кортексин: 5-летний опыт отечественной неврологии, 2005.
4. Яковлев Г.М., Новиков В.С., Смирнов В.С. и др. Механизмы биорегуляции. СПб.: Наука, 1992.
5. Левин О.С., Сагова М.М. Кортексин в комплексном лечении дисциркуляторной энцефалопатии. Кортексин: 5-летний опыт отечественной неврологии. 2005; с. 89–98.
1 марта 2012
Количество просмотров: 3437


