Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№01 2013
Совершенствование организационной и лечебной помощи пациентам с кардиологической патологией, сочетанной с аффективными расстройствами и инсомнией №01 2013
Номера страниц в выпуске:28-32
В целях совершенствования организации медицинской помощи больным с сердечно-сосудистыми заболеваниями, сочетанными с аффективными расстройствами и расстройствами сна, уточнен комплекс организационных мероприятий, что позволило определить четкий, структурированный по этапам, управляемый, менее затратный по времени как для терапевта, кардиолога, так и для пациента алгоритм помощи. Присоединение антидепрессанта Вальдоксана (агомелатин) к стандартной антиангинальной терапии позволяет оптимизировать терапевтический процесс, уменьшить объем базовой терапии.
Резюме. В целях совершенствования организации медицинской помощи больным с сердечно-сосудистыми заболеваниями, сочетанными с аффективными расстройствами и расстройствами сна, уточнен комплекс организационных мероприятий, что позволило определить четкий, структурированный по этапам, управляемый, менее затратный по времени как для терапевта, кардиолога, так и для пациента алгоритм помощи. Присоединение антидепрессанта Вальдоксана (агомелатин) к стандартной антиангинальной терапии позволяет оптимизировать терапевтический процесс, уменьшить объем базовой терапии.
Ключевые слова: депрессия, антидепрессант, Вальдоксан, агомелатин.
Improvement of healthcare in cardiologic patients with
affective disturbances and sleep disturbances
N.V.Yaltseva, N.I.Korshunov, A.V.Gageva, T.S.Stoyanova, G.S.Bochek, N.V.Haerova, D.A.Politova
Yaroslavl State Medical Academy
Federal State Department of Organization and Information
Summary. For the purpose of improvement of healthcare in patients with heart diseases in combination with affective and sleep disturbances we developed a system of organizational procedures. As a result an algorithm of healthcare became more structured, well-defined, well-supervised. Addition of antidepressant (agomelatin) to a standard antiischemic therapy improves therapeutic process and reduces the doses of cardiologic drugs.
Key words: depression, antidepressant, Valdoxan, agomelatin.
Введение
Сердечно-сосудистая патология создает условия для нарушения циркадианных ритмов человека, поскольку в этих случаях к проявлениям телесного недуга присоединяются нарушения сна, обусловленные психическими расстройствами, сопровождающие и утяжеляющие течение сердечно-сосудистых заболеваний (ССЗ) [2].
По данным А.Б.Смулевича и соавт. [7–9], 62,7% кардиологических больных нуждаются в назначении психотропных средств, причем у 19,7% из них регистрируется необходимость применения антидепрессантов. Е.И.Чазов [11] подчеркивает увеличение смертности от ССЗ за период с 1990 по 2003 г. и связывает это, в частности, с высокой распространенностью у таких больных депрессивных расстройств. Некоторыми авторами [9] депрессия рассматривается как независимый фактор риска развития кардиоваскулярных заболеваний.
Депрессию выделяют в качестве самостоятельного фактора риска повышения смертности после перенесенного инфаркта миокарда. У этих больных более чем на 7% в год увеличивается доля повторных коронарных катастроф или вмешательств на сердце [20]. По данным А.Б.Смулевича [8], распространенность тревожно-депрессивных и панических расстройств у больных артериальной гипертензией (АГ) составляет 40 и 19% соответственно. Коморбидность депрессий с ССЗ рассматривается как неблагоприятный фактор, негативно влияющий как на проявления, так и на исход соматического заболевания. Особого внимания заслуживают нарушения сна у больных АГ в связи с высокой распространенностью данной патологии. По официальной статистике, в России зарегистрированы 4,8 млн больных АГ (30% населения), но по результатам выборочного обследования число таких больных может составлять 42 млн человек.
АГ является причиной ранней инвалидизации и серьезных осложнений течения ССЗ, высокой смертности населения. Ситуация осложняется еще и тем, что эффективно лечатся только 5,6% мужчин и 17,5% женщин.
Одной из причин низкой эффективности гипотензивной терапии являются нарушения сна, которые, по данным литературы, наблюдаются примерно у 42% больных АГ [20]. Нарушение сна приводит к повышению показателей среднесуточного артериального давления (АД) за счет ночного давления. У таких больных удлиняется период бодрствования с более высокими цифрами АД и ростом АД на следующий день, уменьшается степень ночного снижения АД. Все это приводит к появлению патологического типа суточной кривой АД. В то же время в исследованиях отечественных психиатров и кардиологов отмечено, что применение некоторых гипотензивных средств также оказывает отрицательное влияние на продолжительность и глубину сна [8]. У больных АГ, принимающих b-адреноблокаторы, нередко отмечаются побочные эффекты в виде общей слабости, повышенной утомляемости, депрессии. Некоторые сердечно-сосудистые средства, особенно гипотензивные, оказывают отрицательное влияние на ритм сна и бодрствования. Отмечено, что нарушения сна чаще наблюдаются при приеме липофильных (пропранолол), чем гидрофильных (атенолол) b-адреноблокаторов, но эти данные неоднозначны. С целью коррекции нарушений сна у пациентов кардиологического профиля традиционно применяются препараты бензодиазепинового ряда, хотя они не удовлетворяют современным требованиям эффективности и безопасности [4]. Нередко при приеме этих препаратов отмечается чрезмерный седативный эффект, который тяжело воспринимается кардиологическими больными с выраженной астенией. Возможно усиление когнитивного дефицита, что способствует социальной дезадаптации. Некоторые бензодиазепины могут вызывать гипотонию у лиц пожилого возраста и пациентов с вегетососудистой дистонией.
У больных с ишемической болезнью сердца (ИБС) возможно усугубление тахикардии [5]. При коррекции расстройств сна у больных с ССЗ необходимо учитывать наличие других психопатологических симптомов, приводящих к инсомнии или усугубляющих ее течение [15, 19].
При симптомах депрессии необходимо назначение антидепрессивной терапии. Использование антидепрессантов современных генераций имеет ряд преимуществ: удобство режима дозирования, короткий период полувыведения, благоприятный терапевтический профиль, хорошая переносимость [17]. Добавление антидепрессантов к стандартной антиангинальной терапии позволяет оптимизировать терапевтический процесс, уменьшить объем базовой терапии. Адекватное и своевременное лечение депрессивных расстройств позволяет сократить длительность пребывания в стационаре. Основными особенностями лечения расстройств сна у больных с ССЗ являются приоритет оценок переносимости и индивидуальной чувствительности над эффективностью и мощностью психотропного воздействия, а также многофакторность процессов, влияющих на конечный терапевтический результат. При этом на первый план выступает не столько оценка степени выраженности лечебного воздействия на основные характеристики психического расстройства, сколько достижение баланса между полнотой реализации психофармакологического эффекта препарата с минимальной выраженностью его побочных действий.
В настоящем открытом исследовании на основе современных моделей организации помощи больным с депрессивными расстройствами – «интегрированной медицины», «встречного движения» (А.Б.Смулевич и соавт., 2003; А.Б.Смулевич, 2011) – апробированы и оценены усовершенствования в организации медицинской помощи пациентам с ССЗ (ИБС, гипертонической болезнью – ГБ, нейроциркуляторной дистонией – НЦД), коморбидными с аффективными расстройствами в лечебно-профилактических учреждениях первичного звена. Изученная выборка включает 191 пациента, получавшего стационарное лечение в условиях Ярославской областной клинической больницы и МУЗ поликлиники №2 г. Ярославля. Кардиологическая патология у всех пациентов сочеталась с аффективными расстройствами; при этом у всех выявлены также диссомнические расстройства.
Все больные (n=191) были разделены на 2 группы: в 1-ю, основную, группу вошли получавшие курс терапии антидепрессантами в течение 3 мес (158 пациентов: с ИБС – 31, ГБ – 82, НЦД – 45), во 2-ю группу сравнения – отказавшиеся от психофармакотерапии (33 пациента). Пациенты 2 групп были сопоставимы по полу, возрасту, основным клиническим характеристикам кардиологической патологии, объему получаемой соматотропной терапии.
В работе использованы следующие методы: непосредственное наблюдение, организационный эксперимент, статистический. В ходе анализа организации оказания помощи пациентам с сочетанной патологией определены следующие нерешенные задачи:
Результаты
Результаты терапии аффективных расстройств Вальдоксаном в дозе 25 мг/сут у изученных пациентов 1-й группы свидетельствуют о том, что в большинстве случаев наступает отчетливый клинический эффект. Положительная динамика прослеживалась по данным шкал депрессии и тревоги Гамильтона (рис. 1, 2) – в группе пациентов с ИБС, ГБ, НЦД, принимавших Вальдоксан, по сравнению с группой пациентов, отказавшихся принимать антидепрессанты. Так, уровень депрессии, тревоги и ее составляющих (психической и соматической), как это показано в таблице, с высокой степенью достоверности (p<0,000) снижался уже через 1 мес терапии Вальдоксаном вне зависимости от кардиологического диагноза.
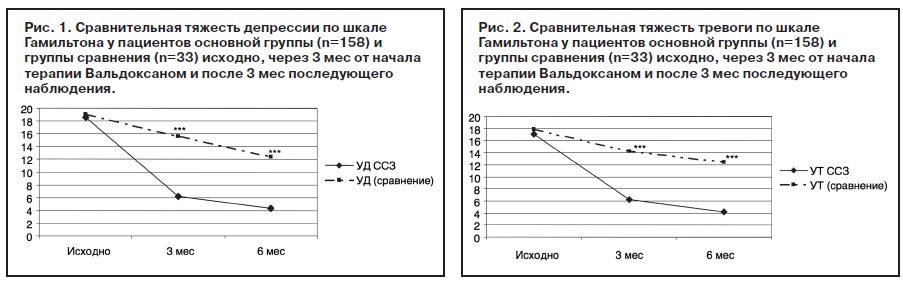
Дальнейшая последовательная достоверная редукция рассматриваемых показателей отмечена и через 2 мес терапии и через 3 мес терапии. В ходе дальнейшего динамического наблюдения (после завершения терапии Вальдоксаном) у пациентов 1-й группы продолжалось достоверное снижение выраженности депрессии и тревоги, а также ее составляющих – психической и соматической.
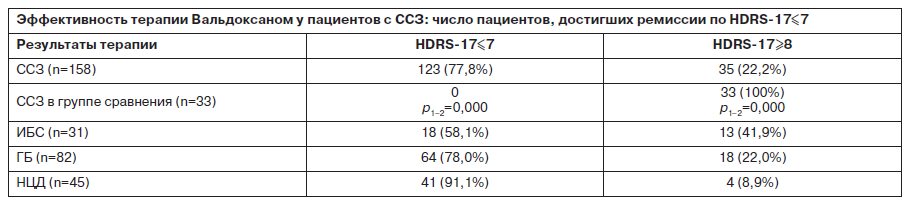
В целом выявлено достоверное снижение показателя уровня депрессии по шкале депрессии Гамильтона (HDRS-17) на 57,7% в группе пациентов с ИБС (с 18,2 до 7,7 балла); на 66,1% (с 18,9 до 6,4 в группе пациентов с ГБ); на 73,4% (с 18,4 до 4,9) в группе пациентов с НЦД через 3 мес терапии. Показатель уровня шкалы тревоги Гамильтона (HARS) на терапии Вальдоксаном редуцировался на 62,5% в группе пациентов с ИБС (с 16,8 до 6,3 балла); на 62,9% (с 17,5 до 6,5) в группе пациентов с ГБ; на 72,6% (с 16,4 до 4,5) в группе пациентов с НЦД. При этом уровень психической тревоги снизился, соответственно, на 55,3% (с 9,4 до 4,2); на 64,2% (с 9,5 до 3,4); на 68,5% (с 8,9 до 2,8). Уровень соматической тревоги в группе пациентов с ИБС снизился на 54,5% (с 7,7 до 3,5); у пациентов с ГБ – на 61,3% (с 8,0 до 3,1); у пациентов с НЦД – на 77,6% (с 7,6 до 1,7).
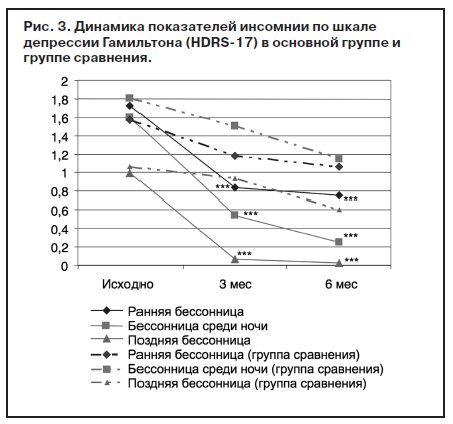 В процессе терапии Вальдоксаном быстро и гармонично редуцировались расстройства сна. При этом в группе сравнения и через 3, и через 6 мес показатели, характеризующие раннюю, среднюю и позднюю бессонницу, были достоверно ниже значений соответствующих показателей в основной группе (рис. 3).
В процессе терапии Вальдоксаном быстро и гармонично редуцировались расстройства сна. При этом в группе сравнения и через 3, и через 6 мес показатели, характеризующие раннюю, среднюю и позднюю бессонницу, были достоверно ниже значений соответствующих показателей в основной группе (рис. 3).
Таким образом, проведенный анализ позволил установить, что включение Вальдоксана в комплексную терапию пациентов с ССЗ (ИБС, ГБ, НЦД) с аффективными расстройствами и расстройствами сна значительно повышает эффективность лечения, улучшает психическое состояние и качество жизни этой категории пациентов. В ходе исследования подтвержден благоприятный профиль переносимости Вальдоксана: нежелательные явления выявлены у 27 (17,1%) пациентов.
Чаще всего (в 15 наблюдениях – 9,5%) наблюдались яркие сновидения в первые дни терапии, сонливость в первые недели терапии (12 наблюдений – 7,6%); эти нежелательные явления во всех случаях разрешились самостоятельно и не требовали отмены препарата.
Сведения об авторе
Яльцева Наталья Викторовна – д-р мед. наук, Ярославская ГМА ФГБУ ЦНИИОИЗ Минздрава РФ.
E-mail: yalceva@yrh.yar.ru
Ключевые слова: депрессия, антидепрессант, Вальдоксан, агомелатин.
Improvement of healthcare in cardiologic patients with
affective disturbances and sleep disturbances
N.V.Yaltseva, N.I.Korshunov, A.V.Gageva, T.S.Stoyanova, G.S.Bochek, N.V.Haerova, D.A.Politova
Yaroslavl State Medical Academy
Federal State Department of Organization and Information
Summary. For the purpose of improvement of healthcare in patients with heart diseases in combination with affective and sleep disturbances we developed a system of organizational procedures. As a result an algorithm of healthcare became more structured, well-defined, well-supervised. Addition of antidepressant (agomelatin) to a standard antiischemic therapy improves therapeutic process and reduces the doses of cardiologic drugs.
Key words: depression, antidepressant, Valdoxan, agomelatin.
Введение
Сердечно-сосудистая патология создает условия для нарушения циркадианных ритмов человека, поскольку в этих случаях к проявлениям телесного недуга присоединяются нарушения сна, обусловленные психическими расстройствами, сопровождающие и утяжеляющие течение сердечно-сосудистых заболеваний (ССЗ) [2].
По данным А.Б.Смулевича и соавт. [7–9], 62,7% кардиологических больных нуждаются в назначении психотропных средств, причем у 19,7% из них регистрируется необходимость применения антидепрессантов. Е.И.Чазов [11] подчеркивает увеличение смертности от ССЗ за период с 1990 по 2003 г. и связывает это, в частности, с высокой распространенностью у таких больных депрессивных расстройств. Некоторыми авторами [9] депрессия рассматривается как независимый фактор риска развития кардиоваскулярных заболеваний.
Депрессию выделяют в качестве самостоятельного фактора риска повышения смертности после перенесенного инфаркта миокарда. У этих больных более чем на 7% в год увеличивается доля повторных коронарных катастроф или вмешательств на сердце [20]. По данным А.Б.Смулевича [8], распространенность тревожно-депрессивных и панических расстройств у больных артериальной гипертензией (АГ) составляет 40 и 19% соответственно. Коморбидность депрессий с ССЗ рассматривается как неблагоприятный фактор, негативно влияющий как на проявления, так и на исход соматического заболевания. Особого внимания заслуживают нарушения сна у больных АГ в связи с высокой распространенностью данной патологии. По официальной статистике, в России зарегистрированы 4,8 млн больных АГ (30% населения), но по результатам выборочного обследования число таких больных может составлять 42 млн человек.
АГ является причиной ранней инвалидизации и серьезных осложнений течения ССЗ, высокой смертности населения. Ситуация осложняется еще и тем, что эффективно лечатся только 5,6% мужчин и 17,5% женщин.
Одной из причин низкой эффективности гипотензивной терапии являются нарушения сна, которые, по данным литературы, наблюдаются примерно у 42% больных АГ [20]. Нарушение сна приводит к повышению показателей среднесуточного артериального давления (АД) за счет ночного давления. У таких больных удлиняется период бодрствования с более высокими цифрами АД и ростом АД на следующий день, уменьшается степень ночного снижения АД. Все это приводит к появлению патологического типа суточной кривой АД. В то же время в исследованиях отечественных психиатров и кардиологов отмечено, что применение некоторых гипотензивных средств также оказывает отрицательное влияние на продолжительность и глубину сна [8]. У больных АГ, принимающих b-адреноблокаторы, нередко отмечаются побочные эффекты в виде общей слабости, повышенной утомляемости, депрессии. Некоторые сердечно-сосудистые средства, особенно гипотензивные, оказывают отрицательное влияние на ритм сна и бодрствования. Отмечено, что нарушения сна чаще наблюдаются при приеме липофильных (пропранолол), чем гидрофильных (атенолол) b-адреноблокаторов, но эти данные неоднозначны. С целью коррекции нарушений сна у пациентов кардиологического профиля традиционно применяются препараты бензодиазепинового ряда, хотя они не удовлетворяют современным требованиям эффективности и безопасности [4]. Нередко при приеме этих препаратов отмечается чрезмерный седативный эффект, который тяжело воспринимается кардиологическими больными с выраженной астенией. Возможно усиление когнитивного дефицита, что способствует социальной дезадаптации. Некоторые бензодиазепины могут вызывать гипотонию у лиц пожилого возраста и пациентов с вегетососудистой дистонией.
У больных с ишемической болезнью сердца (ИБС) возможно усугубление тахикардии [5]. При коррекции расстройств сна у больных с ССЗ необходимо учитывать наличие других психопатологических симптомов, приводящих к инсомнии или усугубляющих ее течение [15, 19].
При симптомах депрессии необходимо назначение антидепрессивной терапии. Использование антидепрессантов современных генераций имеет ряд преимуществ: удобство режима дозирования, короткий период полувыведения, благоприятный терапевтический профиль, хорошая переносимость [17]. Добавление антидепрессантов к стандартной антиангинальной терапии позволяет оптимизировать терапевтический процесс, уменьшить объем базовой терапии. Адекватное и своевременное лечение депрессивных расстройств позволяет сократить длительность пребывания в стационаре. Основными особенностями лечения расстройств сна у больных с ССЗ являются приоритет оценок переносимости и индивидуальной чувствительности над эффективностью и мощностью психотропного воздействия, а также многофакторность процессов, влияющих на конечный терапевтический результат. При этом на первый план выступает не столько оценка степени выраженности лечебного воздействия на основные характеристики психического расстройства, сколько достижение баланса между полнотой реализации психофармакологического эффекта препарата с минимальной выраженностью его побочных действий.
В настоящем открытом исследовании на основе современных моделей организации помощи больным с депрессивными расстройствами – «интегрированной медицины», «встречного движения» (А.Б.Смулевич и соавт., 2003; А.Б.Смулевич, 2011) – апробированы и оценены усовершенствования в организации медицинской помощи пациентам с ССЗ (ИБС, гипертонической болезнью – ГБ, нейроциркуляторной дистонией – НЦД), коморбидными с аффективными расстройствами в лечебно-профилактических учреждениях первичного звена. Изученная выборка включает 191 пациента, получавшего стационарное лечение в условиях Ярославской областной клинической больницы и МУЗ поликлиники №2 г. Ярославля. Кардиологическая патология у всех пациентов сочеталась с аффективными расстройствами; при этом у всех выявлены также диссомнические расстройства.
Все больные (n=191) были разделены на 2 группы: в 1-ю, основную, группу вошли получавшие курс терапии антидепрессантами в течение 3 мес (158 пациентов: с ИБС – 31, ГБ – 82, НЦД – 45), во 2-ю группу сравнения – отказавшиеся от психофармакотерапии (33 пациента). Пациенты 2 групп были сопоставимы по полу, возрасту, основным клиническим характеристикам кардиологической патологии, объему получаемой соматотропной терапии.
В работе использованы следующие методы: непосредственное наблюдение, организационный эксперимент, статистический. В ходе анализа организации оказания помощи пациентам с сочетанной патологией определены следующие нерешенные задачи:
1) Отсутствие четко сформулированных критериев по выявлению и ведению больных с кардиологическими заболеваниями, сочетанными с аффективными и установленными диссомническими расстройствами;В результате анализа существовавшей до организационного эксперимента системы оказания медицинской помощи пациентам с сочетанной патологией выявлен ряд проблем:
2) Недостаточный уровень знаний и навыков по лечению аффективных расстройств, диссомнических расстройств у терапевтов и кардиологов;
3) Отсутствие преемственности в деятельности врачей-психиатров и терапевтов/ кардиологов;
4) Недоверие населения к психиатрической помощи: опасения стигматизации.
1. При выявлении жалоб на психические расстройства (чаще всего на нарушения сна) врач первичного звена направлял пациента к психиатру, как правило, в психиатрический диспансер. В связи с предубеждением населения (опасения стигматизации) такие пациенты редко посещали психиатра.На основании анализа нерешенных проблем в организациии медицинской помощи для пациентов с ССЗ, сочетанными с аффективными расстройствами и расстройствами сна с учетом современных моделей организации помощи больным с депрессивными расстройствами – «интегрированной медицины», «встречного движения» (А.Б.Смулевич и соавт., 2003; А.Б.Смулевич, 2011) – сформулирован и апробирован комплекс организационных мероприятий и технологий:
2. Если такой визит и состоялся (одна из причин – действующее законодательство), у направившего врача отсутствовала информация о дальнейшей судьбе пациента.
3. Как следствие, взаимодействия кардиолога/терапевта, осуществляющих лечение ССЗ, и психиатра, который начинает лечение аффективного расстройства, не происходит.
1. Обучение специалистов первичного звена диагностике и дальнейшему ведению пациентов с ССЗ, сочетанными с аффективными расстройствами и расстройствами сна.Разработанный в настоящем исследовании алгоритм оказания медицинской помощи больным с ССЗ, сочетанными с аффективными расстройствами и расстройствами сна, включает следующие этапы:
2. Методика скринингового исследования.
3. Адаптированные психиатрические шкалы (шкала депрессии и тревоги Гамильтона) для диагностики аффективных расстройств.
4. Алгоритм ведения пациентов кардиологом.
5. Применение антидепрессантов по схеме с учетом взаимодействия с лекарственными средствами, применяемыми для лечения заболеваний кардиологического профиля.
1. Выявление больных с аффективными расстройствами и расстройствами сна (скрининг). Используется скрининговая анкета для выявления аффективных расстройств и расстройств сна у пациентов общесоматической сети. Результаты скрининга оцениваются на основании критериев, позволяющих предположить наличие у больных аффективных расстройств [6].
2. Клиническая диагностика аффективных расстройств (в соответствии с критериями Международной классификации болезней 10-го пересмотра – МКБ-10) включает уточнение как психиатрического, так и кардиологического диагноза. Для оценки степени выраженности депрессивных расстройств используются психометрические шкалы депрессии и тревогиГамильтона (HDRS-17, HARS). В случаях выявления тяжелой депрессии для более детальной оценки психического состояния пациентов и назначения адекватной терапии необходима консультация психиатра. Для уточнения кардиологического диагноза дополнительно проводится лабораторное и клинико-инструментальное обследование, по результатам которого устанавливается (уточняется) кардиологический диагноз.
3. Лечение больных с аффективными расстройствами и расстройствами сна – медикаментозное и немедикаментозное. После уточнения кардиологического диагноза пациентам назначают стандартные схемы терапии. При выраженности депрессивных нарушений менее 8 баллов по шкале Гамильтона (HDRS-17) используются седативные, вегетостабилизирующие средства [6], а при возрастании депрессивных нарушений до 8–24 баллов назначаются современные антидепрессанты с учетом их безопасности, взаимодействия с другими лекарственными средствами, в том числе кардиотропными. Среди антидепрессантов, отвечающих этим требованиям, с успехом применяется агомелатин (Вальдоксан). Исходно Вальдоксан
изучался в качестве хронобиотика. В эксперименте препарат продемонстрировал сходное с мелатонином действие на биоритмы и терморегуляцию [12, 13, 23]. Обнаружение у препарата антагонизма по отношению к серотониновым рецепторам 2-го типа привлекло особое внимание к изучению его анксиолитического и антидепрессивного эффекта [5, 10, 18].
4. Медицинская оценка эффективности терапии включает оценку редукции депрессивных расстройств с использованием психометрических и клинических показателей и клинических показателей, характеризующих динамику соматического заболевания. Курс медикаментозной терапии аффективных расстройств и расстройств сна составляет 3 мес (оценка состояния пациента проводится до назначения терапии, через 10, 20, 30, 60, 90 дней от начала курса лечения), далее 3 мес наблюдения (продолжается терапия кардиологического заболевания).
Результаты
Результаты терапии аффективных расстройств Вальдоксаном в дозе 25 мг/сут у изученных пациентов 1-й группы свидетельствуют о том, что в большинстве случаев наступает отчетливый клинический эффект. Положительная динамика прослеживалась по данным шкал депрессии и тревоги Гамильтона (рис. 1, 2) – в группе пациентов с ИБС, ГБ, НЦД, принимавших Вальдоксан, по сравнению с группой пациентов, отказавшихся принимать антидепрессанты. Так, уровень депрессии, тревоги и ее составляющих (психической и соматической), как это показано в таблице, с высокой степенью достоверности (p<0,000) снижался уже через 1 мес терапии Вальдоксаном вне зависимости от кардиологического диагноза.

Дальнейшая последовательная достоверная редукция рассматриваемых показателей отмечена и через 2 мес терапии и через 3 мес терапии. В ходе дальнейшего динамического наблюдения (после завершения терапии Вальдоксаном) у пациентов 1-й группы продолжалось достоверное снижение выраженности депрессии и тревоги, а также ее составляющих – психической и соматической.

В целом выявлено достоверное снижение показателя уровня депрессии по шкале депрессии Гамильтона (HDRS-17) на 57,7% в группе пациентов с ИБС (с 18,2 до 7,7 балла); на 66,1% (с 18,9 до 6,4 в группе пациентов с ГБ); на 73,4% (с 18,4 до 4,9) в группе пациентов с НЦД через 3 мес терапии. Показатель уровня шкалы тревоги Гамильтона (HARS) на терапии Вальдоксаном редуцировался на 62,5% в группе пациентов с ИБС (с 16,8 до 6,3 балла); на 62,9% (с 17,5 до 6,5) в группе пациентов с ГБ; на 72,6% (с 16,4 до 4,5) в группе пациентов с НЦД. При этом уровень психической тревоги снизился, соответственно, на 55,3% (с 9,4 до 4,2); на 64,2% (с 9,5 до 3,4); на 68,5% (с 8,9 до 2,8). Уровень соматической тревоги в группе пациентов с ИБС снизился на 54,5% (с 7,7 до 3,5); у пациентов с ГБ – на 61,3% (с 8,0 до 3,1); у пациентов с НЦД – на 77,6% (с 7,6 до 1,7).
 В процессе терапии Вальдоксаном быстро и гармонично редуцировались расстройства сна. При этом в группе сравнения и через 3, и через 6 мес показатели, характеризующие раннюю, среднюю и позднюю бессонницу, были достоверно ниже значений соответствующих показателей в основной группе (рис. 3).
В процессе терапии Вальдоксаном быстро и гармонично редуцировались расстройства сна. При этом в группе сравнения и через 3, и через 6 мес показатели, характеризующие раннюю, среднюю и позднюю бессонницу, были достоверно ниже значений соответствующих показателей в основной группе (рис. 3).
Таким образом, проведенный анализ позволил установить, что включение Вальдоксана в комплексную терапию пациентов с ССЗ (ИБС, ГБ, НЦД) с аффективными расстройствами и расстройствами сна значительно повышает эффективность лечения, улучшает психическое состояние и качество жизни этой категории пациентов. В ходе исследования подтвержден благоприятный профиль переносимости Вальдоксана: нежелательные явления выявлены у 27 (17,1%) пациентов.
Чаще всего (в 15 наблюдениях – 9,5%) наблюдались яркие сновидения в первые дни терапии, сонливость в первые недели терапии (12 наблюдений – 7,6%); эти нежелательные явления во всех случаях разрешились самостоятельно и не требовали отмены препарата.
Сведения об авторе
Яльцева Наталья Викторовна – д-р мед. наук, Ярославская ГМА ФГБУ ЦНИИОИЗ Минздрава РФ.
E-mail: yalceva@yrh.yar.ru
Список исп. литературыСкрыть список1. Александровский Ю.А. Пограничные психические расстройства. М.: Медицина, 2000; с. 409–21.
2. Артюхова М.Г. Нарушения сна у кардиологических больных. РМЖ. 2010; 18 (8).
3. Иванов С.В. Совместимость психотропных и соматотропных средств. Cons. Med. (Прил.). 2002; с. 10–2.
4. Иванов С.В. Агомелатин при терапии умеренных и тяжелых депрессий непсихотического уровня в амбулаторной и госпитальной практике (результаты российского многоцентрового исследования ХРОНОС). Психиатр. и психофармакотер. 2009; 6: 14–7.
5. Ольбинская Л.И., Морозова Т.Е. Современные аспекты фармакотерапии ишемической болезни сердца. Лечащий врач. 2003; 6: 14–9.
6. Организационная модель помощи лицам, страдающим депрессиями, в условиях территориальной поликлиники. Метод. рекомендации. М., 2000.
7. Смулевич А.Б. Депрессивные расстройства в кардиологии. Cons. Med. 2003; (Экстравыпуск): 3–6.
8. Смулевич А.Б., Сыркин А.Л. Психокардиология. 2005; с. 777.
9. Смулевич А.Б., Тхостов А.Ш., Сыркин А.Л. и др. Клинические и психологические аспекты реакции на болезнь (к проблеме нозогений). Журн. неврол. и психиатр. им. С.С.Корсакова. 1997; 97: 4–9.
10. Смулевич А.Б., Андрющенко А.А., Бескова Д.А. Терапия непсихотических депрессий антидепрессантом агомелатином (Вальдоксан): результаты наблюдательного многоцентрового исследования РИТМ. Психиатр. и психофармакотер. 2010; 4: 4–11.
11. Чазов Е.И. Психосоциальные факторы как риск возникновения сердечно-сосудистых заболеваний. Легкое сердце. 2004; 3: 2–4.
12. Arendt J. Melatonin and its agonists: an update. Br J Psych 2008; 193: 267–9.
13. Audinot V, Mailliet F, Lahaye-Brasseur C et al. New selective ligands of human clined melatonin MT1- and MT2-receptors. Naunyn Schmiedebergs Arch Pharmacol 2003; 367 (6): 553–61.
14. Ball EM. Sleep disorders in primary care. Compr Psychiat 1997; 23: 25–30.
15. Evans DL, Straab J, Ward H et al. Depression Anxiety 1996–1997; 4: 199–208.
16. George CF. Perspectives on the management of insomnia in patients with chronic respiratory disorders. Sleep 2000; 23 (Suppl. 1): s31–5.
17. Goldberg RS. Selective serotonin reuptake inhibitors: infrequent medical effects. Arch Fam Med 1998; 7: 78–84.
18. Kasper S, Hajak G, Wulff K et al. Superior antidepressant agomelatine on the circadian and anxiety symptoms in patients with major depressive disorders: a randomized double-blind comparison with sertraline. J Clin Psychiat 2010; 71: 109–20.
19. Kupfer DJ. Pathophysiology and management of insomnia during depression. Ann Clin Psychiat 1999; 11: 267–76.
20. Newman AB, Enright PL, Manolio TA et al. Sleep disturbance, psychosocial correlates, and cardiovascular disease in 5201 older adults: the Cardiovascular Health Study. J Am Geriat Soc 1997; 45 (1): 1–7.
21. Olie JP, Kasper S. Efficacy of agomelatine, a MT1/MT2-receptor agonist with 5HT2C-antagonistic properties, in major depressive disorder. Int J Neuropsychopharmacol 2007; 10: 661–73.
22. Touchon J. Sleep induction. Encephale 1992; 18: 369–77.
23.Turek FW, Gillette MU. Melatonin, sleep and circadian rhythms: rational for development of specific melatonin agonists. Sleep Med 2004; 5 (6): 523–32.


