Психиатрия Психические расстройства в общей медицине
№04 2008
Антидепрессанты в реабилитации пациентов с заболеваниями и травмами периферической нервной системы №04 2008
Повреждения периферической нервной системы обычно возникают вследствие техногенных и природных катастроф, огнестрельных, дорожно-транспортных, спортивных, производственных, бытовых и вызванных медицинскими манипуляциями (послеоперационные, постинъекционные, родовые и др.) ранений и травм, а также дегенеративных заболеваний костно-мышечного аппарата, приводящих к раздражению и ишемизации нервных стволов. Несмотря на большой опыт, накопленный в лечении и реабилитации больных с повреждениями нервов конечностей, результаты остаются не вполне удовлетворительными, а у 6–17% больных положительная динамика отсутствует вовсе [2, 6].
Одними из наиболее актуальных проблем в лечении заболеваний и травм периферической нервной системы являются боль и длительный период восстановления.
Боль (согласно определению Международной ассоциации по изучению боли) – неприятное сенсорное и эмоциональное переживание, связанное с существующими или возможными повреждениями ткани или описываемое в терминах такого повреждения. Таким образом, боль – сложный психофизиологический феномен. Так, в частности, боль является наиболее частой причиной обращения к врачам различного профиля (40% всех первичных обращений), при этом 58–84% населения хотя бы раз в жизни испытывали боли в спине, а 15–20% населения страдают хронической болью, которая является наиболее частой причиной нетрудоспособности. Известно, что патогенез болевого синдрома включает в себя элемент образования патологического порочного круга, когда возникшие повреждение и боль приводят к ответной реакции организма, которая усугубляет процесс, что в свою очередь приводит к усилению боли. При длительности болевого синдрома более 2–3 нед в центральной нервной системе формируется господствующий очаг возбуждения, или патологическая доминанта, оказывающая выраженное влияние на течение болезни, ее эмоциональное восприятие и, являясь включенной в сферу обеспечения эмоционально-волевой деятельности по механизмам обратной связи, взаимно потенцирует замедление процессов саногенеза. Отсутствие положительной динамики более 10–14 дней, как правило, вызывает фиксацию пациента на своих ощущениях и развитие элементов депрессии и астеноневротического синдрома даже у индивидов, характерологически не склонных к этому. При этом удлиняются сроки восстановления, больной не отмечает положительной динамики, нарушается обратная связь с лечащим врачом, что осложняет оценку эффективности лечения [3–7].
Кроме того, условия существования в современном мире приводят к тому, что у значительной части населения зачастую присутствует преморбидный невротический фон, что является потенцирующим фактором для хронизации болевых синдромов. Так, выраженная депрессия в 4 раза повышает риск обострения болевого синдрома, что определяет депрессию как независимый предиктор развития интенсивной боли. Также известно, что депрессию имеют при хронических мышечно-скелетных болях до 25% пациентов, а при фибромиалгии более 40% пациентов [8–10].
В настоящее время установлено, что патогенез болевого синдрома и депрессии затрагивает во многом одни и те же структуры нервной системы и развивается схожим путем, вовлекая одни и те же рецепторно-медиаторные взаимодействия. Так, основными общими звеньями патогенеза депрессии и боли являются: гиперреактивность гипоталамо-гипофизарно-надпочечниковой и лимбико-ретикулярных систем, повышение активности глутамата, недостаточность ГАМК, нарушение взаимоотношения глутаматергических и моноаминергических путей, нарушение метаболизма субстанции Р и нейрокининов, недостаточность моноаминов. Также известно, что нарушение регуляции 5-HT-рецепторов в головном мозге напрямую связано и с развитием депрессии, и с регуляцией эффектов субстанции Р, глутамата, GABA и других медиаторов боли. Дисфункция нисходящих NE- и 5-HТ-систем, характерная для депрессии, может привести к интерпретации организмом обычных стимулов как дискомфорт или даже болезненные ощущения [11–17].
Таким образом, боль является отрицательной эмоцией, порождающей реактивную депрессию, которая делает пациента более чувствительным к боли (усиливает восприятие боли), при этом депрессия и чувство боли частично обеспечиваются общими механизмами и, следовательно, сосуществующие боль и депрессия усугубляют друг друга, формируя порочный круг боль – депрессия – боль – депрессия.
Еще одним важным фактором, влияющим на восстановление повреждений периферической нервной системы, является мотивация и готовность пациента к длительной и упорной работе над восстановлением утраченной функции. Высокий риск инвалидизации больных при травмах периферической нервной системы сформировал безотчетное отношения к исходам травм. Так, при тяжелой травме с серьезным травматологическим дефектом (разрыв связок, суставной сумки и т.п.), сопутствующих чувствительных расстройствах, синдроме выраженного двигательного дефицита и данных электронейромиографии, свидетельствующих о степени неврального повреждения (низкоамлитудный полифазный М-ответ, блокада моторной или сенсорной проводимости и снижение потенциала действия нерва и ВПСМ), медицинский персонал и пациент превентивно настраиваются на незначительную эффективность лечения и последующую инвалидизацию. Данные литературы зачастую также не формируют иного, более оптимистичного взгляда на исход серьезных травматических невро- и плексопатий. Недостаточность штатов и персонала приводит к ограничению возможностей лечебных учреждений к скрупулезной непрерывной и долговременной работе с больным как в сфере восстановительных занятий, так и в психологической подготовке пациента к длительной каждодневной работе, значительную часть которой в наших условиях он должен брать на себя. В этом случае формируется упование на лекарственные препараты, улучшающие регенераторный спрутинг и, соответственно, снижение мотивации к самостоятельной работе над дефектом. По мере течения времени и недостаточности эффекта формируется синдром “неисполненных ожиданий” с последующим развитием депрессии и полным прекращением реабилитационных занятий. Данные явления, как правило, происходят приблизительно через 1–4 мес после травмы или заболевания в зависимости от изначального психологического статуса пациента и его правильной мотивации, формирование которой во многом зависит от медицинского персонала и родственников [2, 18, 19].
При выборе лекарственных средств в условиях стационара основными критериями являются быстрота развития ожидаемого эффекта, отсутствие побочных эффектов при применении и резкой отмене препарата. Если купируемое состояние является вторичным, то препарат наряду с указанными свойствами должен быть доступен и с финансовой точки зрения, так как основные силы и средства уходят на лечение основного заболевания.
Как правило, к препаратам рутинного назначения, применяемым в терапевтических и неврологических клиниках для купирования элементов депрессии и астеноневротического синдрома, относятся бензодиазепиновые транквилизаторы и антидепрессанты. Основными назначаемыми препаратами, представляющими эти группы, являются феназепам и амитриптилин. Этими широко известными и эффективными препаратами традиционно и повсеместно обычно снабжается большинство стационаров России. При этом одним из основных минусов применения бензодиазепинов является прежде всего выраженный седативный эффект. Кроме того, не контролируемо индивидуально могут проявляться миорелаксирующий, противосудорожный и амнестический эффекты. Побочные явления при применении трициклических антидепрессантов связаны с их влиянием на сердечно-сосудистую систему и с блокадой м-холинорецепторов [21–23].
В целом группа антидепрессантов широко представлена на фармакологическом рынке, в частности, общий список препаратов антидепрессивного действия включает в себя:
1. Трициклические антидепрессанты (амитриптилин, мелипрамин).
2. Ингибиторы МАО-А – пиразидол, моклобемид (аурорикс), ипрониазид, ниаламид.
3. Селективные стимуляторы обратного захвата серотонина (ССОЗС) – тианептин (коаксил).
4. Селективные ингибиторы обратного захвата серотонина – флуоксетин (прозак, профлузак), сертралин (золофт), пароксетин (паксил, рексетин), флувоксамин (феварин), циталопрам (ципрамил).
5. Норадренергические специфические серотонинергические антидепрессанты (НССА) – миртазапин (ремерон).
6. Ингибиторы обратного захвата серотонинина и норадреналина – дулоксетин (симбалта), венлафаксин (эффексор), милнаципран (иксел).
7. Селективные ингибиторы обратного захвата норадреналина – миансерин (леривон).
8. Игибиторы повторного/возобновляющегося усвоения антагонистов серотонина-2 (SARI) – тразодон, нефазодон.
При рассмотрении возможностей применения антидепрессантов различных групп в сферу нашего внимания попала достаточно редко практикуемая группа ингибиторов обратного захвата серотонина с антагонизмом к рецепторам серотонина-2 (SARI), в частности тразодон (Триттико®). Обладая преимущественно антидепрессивным действием, тразодон, однако, отличается от традиционных антидепрессантов как по своей структуре (он является производным триазодопиридина, который ранее в терапевтической практике не применялся), так и по фармакологическим свойствам, не обладая при этом некоторыми свойствами, присущими известным психотропным препаратам. Так, он не оказывает воздействия на моноаминоксидазы (МАО), что отличает его от МАО-ингибиторов, а также не обладает действием трициклидов, например, возвратным действием резерпининдуцированной депрессии и потенцированием допамина, поскольку на нейрональный захват норадреналина и дофамина влияет мало. Гипотеза действия тразодона основана на том, что депрессия ассоциируется со снижением порога восприятия неприятных стимулов и действие препарата заключается в нормализации этого порога.
В отличие от многих других психотропных препаратов тразодон не противопоказан при глаукоме и дизурических расстройствах, не вызывает экстрапирамидальных явлений, не проявляет характерного воздействия трициклических антидепрессантов на сердечную проводимость. При этом быстро и эффективно воздействует как на психические (аффективная напряженность, раздражительность, страх, бессонница), так и на соматические симптомы тревоги (сердцебиение, головная боль, мышечные боли, учащенное мочеиспускание, потливость, гипервентиляция). Может назначаться пациентам пожилого возраста, страдающим гипертрофией предстательной железы, глаукомой, нарушениями когнитивных функций. Нежелательные побочные явления связаны с адренолитической активностью, тразодон может вызвать брадикардию и снижение артериального давления с возможной компенсаторной тахикардией, может развиваться ортостатическая неустойчивость.
1) простота и удобство в применении (желателен однократный прием);
2) финансовая доступность;
3) минимальные побочные эффекты;
4) достаточная эффективность по сравнению с другими антидепрессантами;
5) достаточная быстрота развития эффекта и удобство при отмене.
Материалы и методы
Под нашим наблюдением находились 37 больных с пояснично-крестцовым радикулитом затяжного течения и 17 больных с последствиями травм периферических нервов (табл. 1).

Критериями включения больных в исследование являлись наличие затяжного болевого синдрома, отсутствие положительной динамики в жалобах пациента при положительной динамике, отмечаемой при объективном обследовании, жалобы невротического плана. К невротическим жалобам относилась симптоматика, подпадающая согласно МКБ-10 под диагноз “генерализованное тревожное расстройство”, т.е. повышенная утомляемость, усталость, раздражительность, эмоциональная лабильность, рассеянность, нарушение сна, симптомы, связанные с дисфункцией вегетативной иннервации и т.п. Из исследования исключали пациентов с обнаруженной эндокринной патологией.
На момент начала терапии препаратом Триттико часть больных уже получали медикаментозную терапию и физические методы лечения в соответствии с основным диагнозом (заболевания и травмы периферической нервной системы).
Группу контроля составили 15 пациентов с аналогичной патологией, которым не проводили терапию препаратами анксиолитического и антидепрессивного действий.
Обследование проводили в стандартных условиях. Всем больным выполняли исследование неврологического статуса, общеклинический и биохимический анализ крови, коагулограмму, контролировали артериальное давление, для оценки степени повреждения нервных стволов и динамики их восстановления проводили электронейромиографию. Личностную и реактивную тревожность оценивали с помощью психологического тестирования по методике Спилберга–Ханина по трем основным точкам: фоновое обследование, на 3-и и 21-е сутки приема препарата. Динамику жалоб пациентов оценивали по шкале оценки состояния (ШОС). Кроме того, для оценки состояния вегетативной нервной системы (ВНС) применялись методики спектрального анализа ритма сердца (САРС) и вызванных кожных вегетативных потенциалов (ВКВП).
В качестве основных “конечных точек” исследования были выбраны временные, неврологические и субъективные параметры: прием Триттико на протяжении 3 нед в базовой дозировке 75 мг/сут, положительная динамика в течении основного заболевания, нивелирование жалоб невротического характера и увеличение мотивации к лечению.
Результаты
По возрасту, полу, фоновым заболеваниям, основной терапии в остром и восстановительном периодах заболевания достоверных различий между группами не было. Отбор исследуемой группы и группы контроля производили с учетом одинаковости оцениваемых параметров, и при фоновом обследовании статистически значимых различий не выявлено.
В ходе исследования установлена в целом хорошая переносимость Триттико, у 3 пациентов развилась ортостатическая неустойчивость, у остальных неблагоприятных реакций на применение препарата не отмечено.
В группе больных, принимавших тразодон, отмечена достоверная положительная динамика по улучшению самочувствия и данным функциональной диагностики по сравнению с группой контроля (табл. 2).
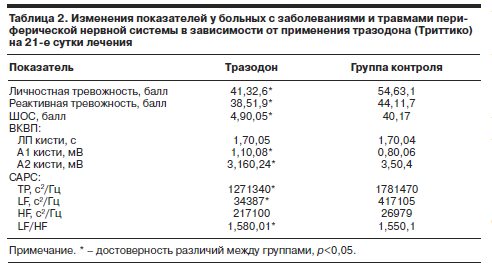
Так, показатели “личностная тревожность”, “реактивная тревожность” и ШОС практически достигли нормальных значений (41, 38 и 5 баллов соответственно), в то время как в группе без применения антидепрессантной терапии показатели личностной тревожности практически не изменились, а показатели реактивной тревожности хотя и показали статистически достоверную положительную тенденцию, но остались далеки от нормальных показателей (44 балла). Анализ показателей ВКВП и САРС между группами сравнения показал одинаковые тенденции к их нормализации. В целом можно отметить, что в группе больных, не принимавших тразодон, сохранился более высокий уровень симпатикотонии и нормализация показателей происходила медленнее. Статистически значимы отличия по общей мощности (ТР) в группе больных, не принимавших препарат, больше, что свидетельствует о более значительном напряжении в функционировании вегетативной нервной системы. При сравнении с фоновыми значениями все показатели в обеих группах значительно улучшились с достоверной значимостью (p<0,05) или близко к этому.
Последующий анализ сроков стационарного лечения больных с дорсопатиями показал, что произошло достоверное сокращение сроков госпитализации в группе больных, применявших тразодон (Триттико), в среднем на 2 дня.
Заключение
Таким образом, применение препаратов антидепрессантного ряда у больных с заболеваниями и травмами периферической нервной системы, снижая выраженность симптомов депрессии и тревоги, повышает мотивацию к реабилитационным занятиям, позволяет правильно отнестись к своему недугу и возможным перспективам восстановления, облегчает работу персонала и родственников. Все это позволяет больше внимания уделять непосредственно занятиям по восстановлению поврежденной функции и опосредованно сокращать период восстановления и сроки госпитализации. Препараты групп ингибиторов повторного/возобновляющегося усвоения антагонистов серотонина-2, а также, видимо, СИОЗС предпочтительнее препаратов прочих групп антидепрессантов, так как селективно снижают симпатическую активность, потенцируя при этом трофотропную функцию ВНС, что должно положительно сказываться на эффективности восстановительного лечения.
Можно сделать вывод, что применение препарата тразодон (Триттико®) в схеме восстановительного лечения у больных с заболеваниями и травмами периферической нервной системы в базовой дозировке от 75 до 150 мг/сут является целесообразным и повышает эффективность терапии.
Список исп. литературыСкрыть список1. Белова А.Н. Нейрореабилитация: Руководство для врачей. М., 2000.
2. Живолупов С.А. Патогенетические варианты травматических невропатий и плексопатий. Избранные вопросы клинической неврологии. Сб. статей. Под ред. Н.М.Жулева и С.В.Лобзина. СПб., 1999; 89–91.
3. Акимов Г.А., Одинак М.М., Живолупов С.А. и др. Современные представления о патогенезе, диагностике и лечении травматических поражений нервных стволов конечностей (обзор). Журн. невропатол. и психиат. им. Корсакова. 1989; 89 (5): 126–32.
4. Головных Л. Л. Вопросы организации и лечения травмы нервной системы в РСФСР. Л., 1977; 143–44.
5. Любан-Плоцца Б., Пельдингер В., Крегер Ф. Психосоматические расстройства в общей медицинской практике. СПб., 2000.
6. Lepine JP. L\'epidemiologie des troubles anxieux et depressifs dans une population generale franeaise. Confrontations Psychiatriques 1993; 35: 139–61.
7. Martin P. Copreseriptions, antidepresseurs et anxiolytiques: сonsequences pratiques de la
meilleure connaissance des mecanismes d\'action putatifs des anxiolytiques. Actual Psychat 2001; 19 (1/2): 2–7.
8. Schondorf R. The Rule of the Sympathetic Skin Response in the Assessment of Autonomic Function. Clinical Autonomic Disorders. Boston: Little, Brown and Company. 1993; 231–42.
9. Verma S, Gallagher RM. Int Rev Psychiat 2000; 12: 103–14.
10. Carroll L et al. Pain 2004; 107 (1–2): 134–9.
11. Одинак М.М., Семин Г.Ф., Иванов Ю.С., Котельников С.А. Оценка функционального состояния структур вегетативной нервной системы методом вызванных потенциалов. Актуал. вопр. клиники, диагностики и лечения. СПб.: ВМедА, 1995; 542–3.
12. Одинак М.М., Шанин Ю.Н., Загрядский П.В. и др. Методические рекомендации по медицинской реабилитации при заболеваниях и травмах нервной системы. СПБ.: Специальная литература, 1997.
13. Abraham I, Sampson KE, Powers EA et al. Increased PKA and PKC activities ac-company neuronal differentiation of NT2/D1 cells. J Neurosci Res 1991; 28: 29–39.
14. Iannotti JP, Suk-Kee T, Williams Jr GR et al. Prognosis and management of peripheral nerve lesions affecting the shoulder girdle. American Shoulder and Elbow Surgeons, Fourteenth Open Meeting, 1998; 44.
15. Yuen EC, So YT, Olney RK. The electrophysiologic features of sciatic neuropathy in 100 patients. Muscle-Nerve 1995; 18 (4): 414–20.
16. Stahl SM. J Clin Psychiat 2002; 63 (5): 382–3.
17. Blier P, Abbott FV. J Psychiatry Neurosci 2001; 26 (1): 37–43.
18. Смулевич А.Б. Депрессии в общей практике. Руководство для врачей. СПб.: 2001.
19. Krebs MO. Le trouble anxieux: clinique et implications neurobioiogiques. Rev Entret Bichat 2001; 2 (5).
20. Chignon JM. Le Trouble Anxiete Generaiisee: du probleme diagnostique ou defi therapeutique, Nervure 1998; 11 (suppl.): 1–16.
21. Карвасарский Б.Д. Психотерапевтическая энциклопедия. СПб.: Питер, 2000.
22. Коновалов А.Н., Лихтерман Л.Б. Нейротравматология. М., 1994.
23. Физиология вегетативной нервной системы. Л.: Наука, 1981.


