Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№03 2013
Коррекция синдрома ночной еды у пациентов с тревожно-депрессивными расстройствами №03 2013
Номера страниц в выпуске:36-39
В современном мире актуальность проблемы лишней массы тела настолько высока, что ряд авторов приравнивают распространенность ожирения к эпидемии. Значимую роль в развитии избыточной массы тела играют расстройства пищевого поведения: нервная булимия, синдром ночной еды, пищевые «кутежи», стресс-зависимое расстройство пищевого поведения.
Резюме. При назначении агомелатина пациентам с синдромом ночной еды и сопутствующими тревожно-депрессивными расстройствами происходит достоверное снижение выраженности общего балла ночной еды до порогового значения, а также имеется динамика по показателю ангедонии, симптомам тревоги и депрессии. Полученные результаты позволяют рекомендовать назначение агомелатина в дозе 25 мг/сут больным с тревожно-депрессивными расстройствами и синдромом ночной еды.
Ключевые слова: синдром ночной еды, тревога, депрессия, ангедония, агомелатин.
Correction of night eating syndrome in patients with anxiety
and depressive disorders
I.S.Mahortova3, B.D.Tsygankov1, O.Yu.Shiryaev2
1MSMD A.I.Evdokimov University, Health Ministry
2Voronezh State N.N.Burdenko Medical Academy, Health Ministry
3OOO "LION-MED", Voronezh
Summary. In using agomelatine in patients with Night Eating Syndrome (NES) and comorbid anxiety and depression a significant decrease of NES score to the borderline level along with dynamics of anhedonia and symptoms of anxiety and depression are observed. The results obtained allow us to recommend prescribing agomelatine in dose of 25 mg per day to the patients with anxiety and depression comorbid with NES.
Key words: night eating syndrome, anxiety, depression, anhedonia, agomelatine.
В современном мире актуальность проблемы лишней массы тела настолько высока, что ряд авторов приравнивают распространенность ожирения к эпидемии [1]. Значимую роль в развитии избыточной массы тела играют расстройства пищевого поведения: нервная булимия, синдром ночной еды, пищевые «кутежи», стресс-зависимое расстройство пищевого поведения [2].
Синдром ночной еды впервые был описан Stunkard и соавт. в 1955 г. С этого момента вышло большое количество исследований, посвященных данной проблеме [3]. Были обсуждены вопросы клинической валидности, независимости синдрома, а также необходимости его отдельной диагностики [3]. На сегодняшний день синдром ночной еды признан самостоятельной диагностической единицей и [4] и включен в 5-е издание Diagnostic and Statistical Manual of Mental Disorders (DSM-5, 2013) [4].
Установлено, что синдром ночной еды относится к расстройствам циркадианных ритмов, и проявляется диссоциацией между процессом принятия пищи и сном [5, 6]. Базовые диагностические критерии диагностики данного синдрома включают повышение количества пищи, потребляемой после ужина (более 25% суточной калорийности) и/или ночью (хотя бы 2 раза в неделю), снижение качества жизни, утреннюю анорексию, длительность жалоб не менее 2 мес [3].
Распространенность данного состояния варьирует в населении в диапазоне от 1,5 [7] до 5,2% [8] в общей популяции, до 14% среди амбулаторных пациентов с психическими расстройствами достигает 14% [9] и 10–50% – среди лиц, страдающих ожирением [4]. Среди пациентов с синдромом ночной еды достоверно чаще встречается депрессия (56% имеют эпизод депрессии в течение жизни) [10].
Цель работы – повышение эффективности коррекции синдрома ночной еды у пациентов с тревожно-депрессивными расстройствами.
Материалы и методы
Для достижения поставленной цели в Центре здоровья на базе поликлиники №4 г. Воронежа была обследована выборка пациентов (n=59; 43 женщины, 16 мужчин) в возрасте от 31 до 65 лет (средний возраст 41,29±3,51) с синдромом ночной еды в картине тревожно-депрессивного состояния.
Критерии исключения: признаки патологии эндокринной системы (нарушение функции щитовидной железы, сахарный диабет и резистентность к инсулину, нарушение функции гипофиза и надпочечников), психические расстройства (шизофрения, биполярное расстройство, деменция, нарушения психического развития), органического поражения ЦНС (вследствие черепно-мозговой травмы, нейроинфекции) тяжелой неконтролируемой соматической патологии, беременность, лактация, климактерический синдром у женщин, нарушения, ограничивающие подвижность пациентов (переломы костей, остеоартроз и т.д.), прием препаратов, влияющих на массу тела (гормоны, нейролептики, антидепрессанты и т.д.).
Работа проводилась с использованием психометрических методов исследования. В ходе беседы были выявлены основные жалобы, краткие анамнестические сведения, проведено обследование с использованием шкал тревоги и депрессии Гамильтона (HAM-A, HAM-D), опросников для оценки синдрома ночной еды Night Eating Questionnaire (NEQ) и выраженности ангедонии.
Выраженность тревожно-депрессивных расстройств (в средних баллах по HAM-A и HAM-D) составила 17,02±0,75 и 15,13±0,62 соответственно. Выраженность проявления синдрома ночной еды по опроснику NEQ составила в среднем 42,00±0,75 балла.
Пациенты разделены на 2 группы: контрольную (n=34; 28 женщин, 6 мужчин), в которой применялись СИОЗС (пароксетин 20–40 мг/сут, сертралин 50–100 мг/сут, флуоксетин 20–60 мг/сут), и основную (n=25; 15 женщин, 10 мужчин) – пациенты, получавшие агомелатин (Вальдоксан) в дозе 25 мг однократно на ночь. Обследование проводилось в начале исследования (D0), через
2 нед (D15) и через 1 мес (D30).
Результаты исследования
Сравнительная динамика выраженности депрессии в баллах в основной и контрольной группах представлена в табл. 1–2.
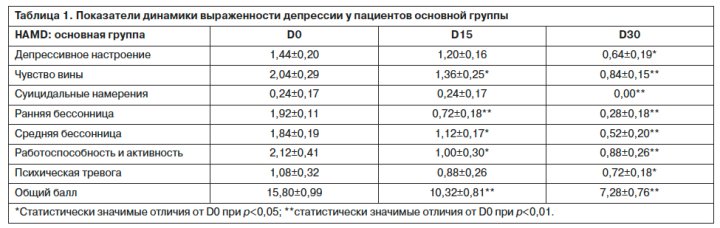
Как видно из табл. 1, уже через 2 нед от начала исследования в основной группе пациентов были выявлены статистически значимые различия от исходных значений (снижение средней суммы баллов) по пунктам HAMD: «общий балл», «работоспособность и активность», «чувство вины», «ранняя бессонница», «средняя бессонница», возрастающие к моменту окончания исследования по всем параметрам.
Из табл. 2 видно, что в контрольной группе (в оценке по HAMD) на 15-е сутки терапии СИОЗС выявлены статистически значимые (p<0,05) отличия от показателей на момент начала терапии по следующим пунктам: «общий балл» и «критичность отношения к болезни», а на момент завершения курса лечения – и по пунктам «генитальные симптомы», «соматическая тревога», «психическая тревога», «работоспособность и активность», «суицидальные намерения», «депрессивное настроение», «чувство вины». Иными словами, положительный эффект Вальдоксана наступает быстрее и реализуется более полной редукцией (судя по сравнительной динамике) средней суммы баллов HAMD в основной и контрольной выборках – 7,28±0,76 против 9,09±0,63 соответственно на момент окончания курса терапии.
На рис. 1 графически представлена динамика показателя «депрессивное наст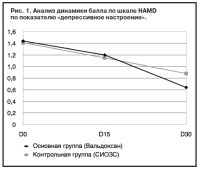 роение» шкалы HAMD в сравниваемых группах, позволяющая наглядно убедиться в эффективности Вальдоксана.
роение» шкалы HAMD в сравниваемых группах, позволяющая наглядно убедиться в эффективности Вальдоксана.
Далее в таблицах представлена повизитная динамика проявлений тревоги (в оценке по HAMA) в сравниваемых группах.
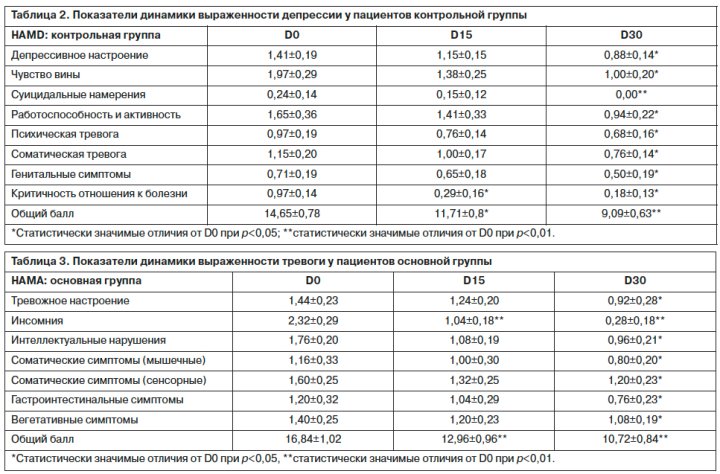
Данные табл. 3 указывают на статистически достоверные отличия от исходных показателей в основной группе пациентов (терапия Вальдоксаном) на 15-й день терапии по следующим пунктам: «инсомния» и «общий балл», к которым на 30-й день присоединяется значимая редукция «тревожного настроения», «интеллектуальных нарушений», «соматических симптомов мышечных, сенсорных)», «гастроинтестинальных симптомов», «вегетативных симптомов». В то же время у пациентов, получавших СИОЗС (контрольная группа), на
15-й день терапии зарегистрированы достоверные отличия от исходных значений по следующим пунктам: «напряжение», «инсомния», «соматические симптомы (сенсорные)», «общий балл»; на 30-й день редуцируются также «тревожное настроение», «депрессивное настроение», «интеллектуальные нарушения», «сердечно-сосудистые симптомы», «респираторные симптомы», «гастроинтестинальные симптомы», «вегетативные симптомы» (табл. 4). При этом сравнительные значения общего балла на момент окончания терапии составляют 10,72±0,84 в основной выборке против 8,21±0,83 в контрольной.
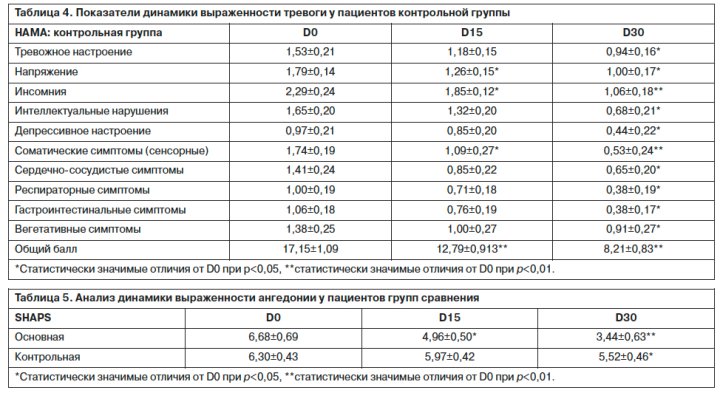
Как видно из табл. 5 и рис. 2, у пациентов основной группы отмечена статистически значимая редукция анге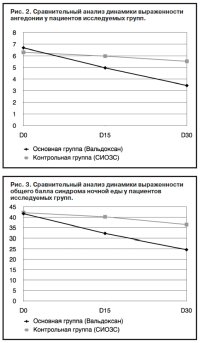 донии уже на 15-й день терапии, в то время как у больных контрольной группы различия достигают уровня значимости лишь на 30-й день.
донии уже на 15-й день терапии, в то время как у больных контрольной группы различия достигают уровня значимости лишь на 30-й день.
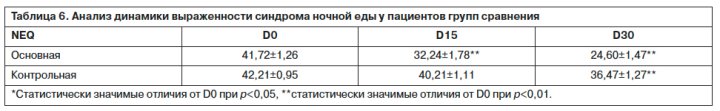
Данные табл. 6 и рис. 3 иллюстрируют динамику синдрома ночной еды в группах сравнения – на терапии Вальдоксаном и СИОЗС. Если статистически значимые признаки редукции нарушений пищевого поведения у пациентов основной группы регстрируются уже на
15-й, то в контрольной группе они достигают уровня значимости лишь на 30-й день терапии, причем средняя выраженность общего балла ночной еды у больных основной группы к завершению курса лечения составляет 24,60±1,47, т.е. снижается сравнительно с пороговым значением (25 баллов по NEQ).
Таким образом, при назначении агомелатина (Вальдоксана) пациентам с синдромом ночной еды и сопутствующими тревожно-депрессивными расстройствами происходит достоверное снижение выраженности общего балла ночной еды до порогового значения, что не было отмечено у больных контрольной группы.
Среди получающих агомелатин (Вальдоксан) пациентов регистрируется также более быстрая редукция (статистически значимые отличия на к 15-му дню терапии) ангедонии и проявлений тревоги и депрессии, связанных с расстройствами сна. Полученные результаты позволяют рекомендовать назначение агомелатина (Вальдоксана) в дозе 25 мг/сут больным с тревожно-депрессивными расстройствами и синдромом ночной еды.
Сведения об авторах
Махортова Ирина Сергеевна – врач-психиатр ООО «ЛИОН-МЕД». E-mail: mirairina@yandex.ru
Цыганков Борис Дмитриевич – зав. каф. психиатрии, наркологии и психотерапии ГБОУ ВПО МГМСУ им. А.И.Евдокимова Минздрава РФ, гл. психиатр г. Москвы. E-mail: boristsygankov@yahoo.com
Ширяев Олег Юрьевич – д-р мед. наук, проф., зав. каф. психиатрии и наркологии ГБОУ ВПО ВГМА им. Н.Н.Бурденко Минздрава РФ. E-mail: shiryaevou2009@yandex.ru
Ключевые слова: синдром ночной еды, тревога, депрессия, ангедония, агомелатин.
Correction of night eating syndrome in patients with anxiety
and depressive disorders
I.S.Mahortova3, B.D.Tsygankov1, O.Yu.Shiryaev2
1MSMD A.I.Evdokimov University, Health Ministry
2Voronezh State N.N.Burdenko Medical Academy, Health Ministry
3OOO "LION-MED", Voronezh
Summary. In using agomelatine in patients with Night Eating Syndrome (NES) and comorbid anxiety and depression a significant decrease of NES score to the borderline level along with dynamics of anhedonia and symptoms of anxiety and depression are observed. The results obtained allow us to recommend prescribing agomelatine in dose of 25 mg per day to the patients with anxiety and depression comorbid with NES.
Key words: night eating syndrome, anxiety, depression, anhedonia, agomelatine.
В современном мире актуальность проблемы лишней массы тела настолько высока, что ряд авторов приравнивают распространенность ожирения к эпидемии [1]. Значимую роль в развитии избыточной массы тела играют расстройства пищевого поведения: нервная булимия, синдром ночной еды, пищевые «кутежи», стресс-зависимое расстройство пищевого поведения [2].
Синдром ночной еды впервые был описан Stunkard и соавт. в 1955 г. С этого момента вышло большое количество исследований, посвященных данной проблеме [3]. Были обсуждены вопросы клинической валидности, независимости синдрома, а также необходимости его отдельной диагностики [3]. На сегодняшний день синдром ночной еды признан самостоятельной диагностической единицей и [4] и включен в 5-е издание Diagnostic and Statistical Manual of Mental Disorders (DSM-5, 2013) [4].
Установлено, что синдром ночной еды относится к расстройствам циркадианных ритмов, и проявляется диссоциацией между процессом принятия пищи и сном [5, 6]. Базовые диагностические критерии диагностики данного синдрома включают повышение количества пищи, потребляемой после ужина (более 25% суточной калорийности) и/или ночью (хотя бы 2 раза в неделю), снижение качества жизни, утреннюю анорексию, длительность жалоб не менее 2 мес [3].
Распространенность данного состояния варьирует в населении в диапазоне от 1,5 [7] до 5,2% [8] в общей популяции, до 14% среди амбулаторных пациентов с психическими расстройствами достигает 14% [9] и 10–50% – среди лиц, страдающих ожирением [4]. Среди пациентов с синдромом ночной еды достоверно чаще встречается депрессия (56% имеют эпизод депрессии в течение жизни) [10].
Цель работы – повышение эффективности коррекции синдрома ночной еды у пациентов с тревожно-депрессивными расстройствами.
Материалы и методы
Для достижения поставленной цели в Центре здоровья на базе поликлиники №4 г. Воронежа была обследована выборка пациентов (n=59; 43 женщины, 16 мужчин) в возрасте от 31 до 65 лет (средний возраст 41,29±3,51) с синдромом ночной еды в картине тревожно-депрессивного состояния.
Критерии исключения: признаки патологии эндокринной системы (нарушение функции щитовидной железы, сахарный диабет и резистентность к инсулину, нарушение функции гипофиза и надпочечников), психические расстройства (шизофрения, биполярное расстройство, деменция, нарушения психического развития), органического поражения ЦНС (вследствие черепно-мозговой травмы, нейроинфекции) тяжелой неконтролируемой соматической патологии, беременность, лактация, климактерический синдром у женщин, нарушения, ограничивающие подвижность пациентов (переломы костей, остеоартроз и т.д.), прием препаратов, влияющих на массу тела (гормоны, нейролептики, антидепрессанты и т.д.).
Работа проводилась с использованием психометрических методов исследования. В ходе беседы были выявлены основные жалобы, краткие анамнестические сведения, проведено обследование с использованием шкал тревоги и депрессии Гамильтона (HAM-A, HAM-D), опросников для оценки синдрома ночной еды Night Eating Questionnaire (NEQ) и выраженности ангедонии.
Выраженность тревожно-депрессивных расстройств (в средних баллах по HAM-A и HAM-D) составила 17,02±0,75 и 15,13±0,62 соответственно. Выраженность проявления синдрома ночной еды по опроснику NEQ составила в среднем 42,00±0,75 балла.
Пациенты разделены на 2 группы: контрольную (n=34; 28 женщин, 6 мужчин), в которой применялись СИОЗС (пароксетин 20–40 мг/сут, сертралин 50–100 мг/сут, флуоксетин 20–60 мг/сут), и основную (n=25; 15 женщин, 10 мужчин) – пациенты, получавшие агомелатин (Вальдоксан) в дозе 25 мг однократно на ночь. Обследование проводилось в начале исследования (D0), через
2 нед (D15) и через 1 мес (D30).
Результаты исследования
Сравнительная динамика выраженности депрессии в баллах в основной и контрольной группах представлена в табл. 1–2.

Как видно из табл. 1, уже через 2 нед от начала исследования в основной группе пациентов были выявлены статистически значимые различия от исходных значений (снижение средней суммы баллов) по пунктам HAMD: «общий балл», «работоспособность и активность», «чувство вины», «ранняя бессонница», «средняя бессонница», возрастающие к моменту окончания исследования по всем параметрам.
Из табл. 2 видно, что в контрольной группе (в оценке по HAMD) на 15-е сутки терапии СИОЗС выявлены статистически значимые (p<0,05) отличия от показателей на момент начала терапии по следующим пунктам: «общий балл» и «критичность отношения к болезни», а на момент завершения курса лечения – и по пунктам «генитальные симптомы», «соматическая тревога», «психическая тревога», «работоспособность и активность», «суицидальные намерения», «депрессивное настроение», «чувство вины». Иными словами, положительный эффект Вальдоксана наступает быстрее и реализуется более полной редукцией (судя по сравнительной динамике) средней суммы баллов HAMD в основной и контрольной выборках – 7,28±0,76 против 9,09±0,63 соответственно на момент окончания курса терапии.

На рис. 1 графически представлена динамика показателя «депрессивное наст
 роение» шкалы HAMD в сравниваемых группах, позволяющая наглядно убедиться в эффективности Вальдоксана.
роение» шкалы HAMD в сравниваемых группах, позволяющая наглядно убедиться в эффективности Вальдоксана.
Далее в таблицах представлена повизитная динамика проявлений тревоги (в оценке по HAMA) в сравниваемых группах.
Данные табл. 3 указывают на статистически достоверные отличия от исходных показателей в основной группе пациентов (терапия Вальдоксаном) на 15-й день терапии по следующим пунктам: «инсомния» и «общий балл», к которым на 30-й день присоединяется значимая редукция «тревожного настроения», «интеллектуальных нарушений», «соматических симптомов мышечных, сенсорных)», «гастроинтестинальных симптомов», «вегетативных симптомов». В то же время у пациентов, получавших СИОЗС (контрольная группа), на
15-й день терапии зарегистрированы достоверные отличия от исходных значений по следующим пунктам: «напряжение», «инсомния», «соматические симптомы (сенсорные)», «общий балл»; на 30-й день редуцируются также «тревожное настроение», «депрессивное настроение», «интеллектуальные нарушения», «сердечно-сосудистые симптомы», «респираторные симптомы», «гастроинтестинальные симптомы», «вегетативные симптомы» (табл. 4). При этом сравнительные значения общего балла на момент окончания терапии составляют 10,72±0,84 в основной выборке против 8,21±0,83 в контрольной.

Как видно из табл. 5 и рис. 2, у пациентов основной группы отмечена статистически значимая редукция анге
 донии уже на 15-й день терапии, в то время как у больных контрольной группы различия достигают уровня значимости лишь на 30-й день.
донии уже на 15-й день терапии, в то время как у больных контрольной группы различия достигают уровня значимости лишь на 30-й день.
Данные табл. 6 и рис. 3 иллюстрируют динамику синдрома ночной еды в группах сравнения – на терапии Вальдоксаном и СИОЗС. Если статистически значимые признаки редукции нарушений пищевого поведения у пациентов основной группы регстрируются уже на
15-й, то в контрольной группе они достигают уровня значимости лишь на 30-й день терапии, причем средняя выраженность общего балла ночной еды у больных основной группы к завершению курса лечения составляет 24,60±1,47, т.е. снижается сравнительно с пороговым значением (25 баллов по NEQ).
Таким образом, при назначении агомелатина (Вальдоксана) пациентам с синдромом ночной еды и сопутствующими тревожно-депрессивными расстройствами происходит достоверное снижение выраженности общего балла ночной еды до порогового значения, что не было отмечено у больных контрольной группы.

Среди получающих агомелатин (Вальдоксан) пациентов регистрируется также более быстрая редукция (статистически значимые отличия на к 15-му дню терапии) ангедонии и проявлений тревоги и депрессии, связанных с расстройствами сна. Полученные результаты позволяют рекомендовать назначение агомелатина (Вальдоксана) в дозе 25 мг/сут больным с тревожно-депрессивными расстройствами и синдромом ночной еды.
Сведения об авторах
Махортова Ирина Сергеевна – врач-психиатр ООО «ЛИОН-МЕД». E-mail: mirairina@yandex.ru
Цыганков Борис Дмитриевич – зав. каф. психиатрии, наркологии и психотерапии ГБОУ ВПО МГМСУ им. А.И.Евдокимова Минздрава РФ, гл. психиатр г. Москвы. E-mail: boristsygankov@yahoo.com
Ширяев Олег Юрьевич – д-р мед. наук, проф., зав. каф. психиатрии и наркологии ГБОУ ВПО ВГМА им. Н.Н.Бурденко Минздрава РФ. E-mail: shiryaevou2009@yandex.ru
Список исп. литературыСкрыть список1. Вознюк Н.Е., Иванов В.Б., Лосев А.В., Прилепа С.А. Ожирение – хроническая неинфекционная эпидемия. Вестник новых мед. технологий. 2006; 13 (2): 94.
2. Вознесенская Т.Г. Расстройства пищевого поведения при ожирении. Ожирение и метаболизм. 2004; 2.
3. Striegel-Moore RH, Franko DL, Garcia J. The validity and clinical utility of night eating syndrome. Int J Eat Dis 2009; 42: 720–38.
4. Cleator J, Abbott J, Judd P et al. Night eating syndrome: implications for severe obesity. Nutrition Diabetes 2012; 2: 44. http://doi:10.1038/nutd.2012.16
5. Goel N, Stunkard AJ, Rogers NL et al. Circadian rhythm profiles in women with night eating syndrome. J Biol Rhythms 2009; 24: 85–94.
6. Rogers NL, Dinges DF, Allison KC et al. Assessment of sleep in women with night eating syndrome. Sleep 2006; 29: 814–9.
7. Rand CS, Macgregor AM, Stunkard AJ. The night eating syndrome in the general population and among postoperative obesity surgery patients. Int J Eat Dis 1997; 22: 65–9.
8. Lamerz A, Kuepper-Nybelen J, Bruning N et al. Prevalence of obesity, binge eating, and night eating in a cross-sectional field survey of
6-year-old children and their parents in a German urban population.
J Child Psychol Psychiat 2005; 46: 385–93.
9. Lundgren JD, Allison KC, O’Reardon JP et al. Prevalence of the Night Eating Syndrome in a Psychiatric Population. Am J Psychiat 2006; 163: 156–8.
10. Zwaan M, Burgard MA, Schenk CH, Mitchell JE. Night time eating: a review of the literature. Eur Eat Dis Rev 2003; 11: 7–24.
25 декабря 2013
Количество просмотров: 3451


