Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№02-03 2015
Оптимизация подхода к терапии психоэмоциональных нарушений и диссомнии при болезни Паркинсона №02-03 2015
Номера страниц в выпуске:54-58
Двигательные нарушения составляют основу клинической картины болезни Паркинсона, однако у большинства пациентов они сочетаются с немоторными. Ряд немоторных симптомов: расстройства сна, депрессия, деменция – могут служить ведущими факторами снижения качества жизни. Целью исследования было уточнение клинической эффективности и безопасности Вальдоксана для оптимизации терапии немоторных проявлений болезни Паркинсона. Обследованы 18 пациентов в возрасте от 58 до 76 лет с болезнью Паркинсона с депрессивными расстройствами средней степени, тревогой и диссомнией. Было показано, что особенностью действия антидепрессанта нового класса – Вальдоксана, реализующего свой эффект за счет влияния как на серотонин-, так и мелатонинергическую систему, является одновременное уменьшение тревожно-депрессивных и диссомнических расстройств у пациентов с болезнью Паркинсона. Одним из механизмов действия Вальдоксана является коррекция хронобиологических ритмов. Вальдоксан показал свою хорошую совместимость со всеми классами противопаркинсонических средств и переносимость.
Ключевые слова: болезнь Паркинсона, немоторные нарушения, диссомния, депрессия, Вальдоксан.
Двигательные нарушения составляют основу клинической картины болезни Паркинсона, однако у большинства пациентов они сочетаются с немоторными. Ряд немоторных симптомов: расстройства сна, депрессия, деменция – могут служить ведущими факторами снижения качества жизни. Целью исследования было уточнение клинической эффективности и безопасности Вальдоксана для оптимизации терапии немоторных проявлений болезни Паркинсона. Обследованы 18 пациентов в возрасте от 58 до 76 лет с болезнью Паркинсона с депрессивными расстройствами средней степени, тревогой и диссомнией. Было показано, что особенностью действия антидепрессанта нового класса – Вальдоксана, реализующего свой эффект за счет влияния как на серотонин-, так и мелатонинергическую систему, является одновременное уменьшение тревожно-депрессивных и диссомнических расстройств у пациентов с болезнью Паркинсона. Одним из механизмов действия Вальдоксана является коррекция хронобиологических ритмов. Вальдоксан показал свою хорошую совместимость со всеми классами противопаркинсонических средств и переносимость.
Ключевые слова: болезнь Паркинсона, немоторные нарушения, диссомния, депрессия, Вальдоксан.
official@semashko.nnov.ru
Для цитирования: Густов А.В., Александрова Е.А., Паршина Е.В. и др. Оптимизация подхода к терапии психоэмоциональных нарушений и диссомнии при болезни Паркинсона. Психические расстройства в общей медицине. 2015; 2–3: 54–58.
Optimization approach to therapy and psycho-emotional disorders and dyssomnia in Parkinson's disease
A.V.Gustov1, E.A.Aleksandrova1,2, E.V.Parshina2, S.V.Makushina2, O.A.Podlitok1, K.M.Belyakov2
1Nizhny Novgorod State Medical Academy of the Ministry of Health of the Russian Federation. 603005, Russian Federation, Nizhny Novgorod, pl. Minina i Pozharskogo, d. 10/1;
2N.A.Semashko Nizhny Novgorod State сlinical hospital. 603126, Russian Federation, Nizhny Novgorod, ul. Rodionova, d. 190
Movement disorders are the basis of the clinical picture of Parkinson's disease, but the majority of patients they are combined with non-motor symptoms. A number of non-motor symptoms: sleep disturbances, depression, dementia – can serve as a driving factor for reduced quality of life. The aim of the study was to clarify the clinical efficacy and safety of agomelatine to optimize therapy non-motorized manifestations of Parkinson's disease. We examined 18 patients aged 58 to 76 years with Parkinson's disease with an average degree deperssive disorders, anxiety and dyssomnia. It has been shown that feature a new class of antidepressant – agomelatine realizing its effect by influencing both on serotonin and melatoninergic system is a simultaneous decrease in anxiety and depressive disorders and dyssomnia in patients with Parkinson's disease. One of the mechanisms of action of agomelatine is the correction of chronobiological rhythms.
Key words: Parkinson's disease, non-motor disorders, dyssomnias, depression, agomelatine.
official@semashko.nnov.ru
For citation: Gustov A.V., Aleksandrova E.A., Parshina E.V. et al. Optimization approach to therapy and psycho-emotional disorders and dyssomnia in Parkinson's disease. Mental Disorders in General Medicine. 2015; 2–3: 54–58.
В настоящее время болезнь Паркинсона (БП) рассматривается как мультисистемное нейродегенеративное заболевание с поражением различных медиаторных систем и широким спектром нарушений [8, 12]
Двигательные нарушения составляют основу клинической картины БП, однако у большинства пациентов они сочетаются с немоторными [10, 13, 14, 19]. Ряд немоторных симптомов: расстройства сна, депрессия, деменция – могут служить ведущими факторами снижения качества жизни [9].
Более того, такие нарушения, как депрессия и деменция, могут стать противопоказанием для нейрохирургического лечения БП [6]. Таким образом, оптимизация подходов к повышению качества жизни пациентов с БП должна проводиться не только за счет уменьшения выраженности моторных расстройств, но и за счет коррекции немоторных проявлений заболевания, ведущими из которых являются психоэмоциональные нарушения.
Депрессия – наиболее частый и социально значимый симптом БП. В среднем она встречается у 40% больных. Особенностью депрессии являются сочетание ощущения безысходности и пустоты, ангедонии с пессимизмом, раздражительностью и грустью. Часто депрессия сопровождается другими эмоционально-аффективными нарушениями – апатией, сужением круга интересов, отсутствием мотивации. На начальных этапах терапии депрессии коррекция психоэмоциональных нарушений возможна за счет изменения противопаркинсонической терапии и назначения агонистов дофаминовых рецепторов – АДР (прамипексола, пирибедила). Эти препараты действуют через дофаминовые рецепторы D3-типа, локализованные в лимбической системе, и способны уменьшать выраженность симптомов депрессии, особенно на ранней стадии заболевания. Если коррекция противопаркинсонической терапии не привела к достаточному ослаблению симптомов депрессии, показано назначение антидепрессантов [11].
Патогенетической основой возникновения депрессии и других эмоционально-волевых нарушений при БП является дегенерация второго, мезолимбического, дофаминового пути, ведущего к лимбической системе [9]. В то же время существует еще и хронобиологическая концепция развития депрессивных расстройств, которая говорит о том, что депрессивные состояния нередко сопровождаются десинхронизацией биологических ритмов, так что, в свою очередь, нормализация циркадианных ритмов может привести к редуцированию симптомов депрессии [27, 29]. Ключевую роль в синхронизации циркадианных ритмов выполняет синтезирующийся в эпифизе хронобиотический гормон мелатонин [28].
У пациентов с БП выявлены нарушения мелатонинового обмена. Обнаружено сокращение числа мелатонин-ергических рецепторов в черной субстанции и миндалине у пациентов с БП по сравнению с группой контроля [19]. Выявлено смещение ночного пика выделения мелатонина, развивающееся, возможно, по мере прогрессирования и увеличения длительности БП и на фоне терапии леводопой. Так, отсрочка достижения пика секреции мелатонина отмечена у больных, получавших препараты леводопы, по сравнению с возрастной группой контроля и пациентами с наиболее ранними стадиями БП без соответствующей терапии [19, 21, 23]. Терапевтическое действие агомелатина (Вальдоксан, «Сервье», Франция) реализуется посредством влияния на мелатонинергическую систему (агонизм к MT1- и МТ2-рецепторам), что приводит к ресинхронизации циркадианных ритмов. Также Вальдоксан воздействует на серотонинергическую систему (антагонизм к 5-НТ2С-рецепторам). При этом антагонизм к 5-НТ2С-рецепторам в силу реципрокных отношений приводит к специфическому и опосредованному высвобождению двух основных нейротрансмиттеров во фронтальной коре, играющих важную роль при депрессии, – норадреналина и дофамина [4, 22, 27]. Вальдоксан, обладающий тимоаналептическим эффектом, является перспективным препаратом для лечения депрессивных нарушений, сочетающихся с инсомнией. Это фактически первый из нового класса «стабилизирующих ритм антидепрессантов» [24]. Эффективность и хорошая переносимость Вальдоксана у пациентов с умеренной и тяжелой депрессией отмечены в разных исследованиях [2–4, 23, 25]. Клиническая эффективность Вальдоксана подтверждена в крупных международных исследованиях при лечении больных как с большим депрессивным расстройством, так и биполярным расстройством 2-го типа, в том числе при тяжелой депрессии [16, 26]. В то же время о применении Вальдоксана при БП имеются единичные сообщения [17]. Его эффективность и безопасность у пациентов с БП с депрессивным расстройством средней степени изучены недостаточно. Цель исследования: уточнение клинической эффективности и безопасности Вальдоксана для оптимизации терапии немоторных проявлений БП.
Задачи исследования:
1. Изучить влияние препарата Вальдоксан на депрессивные нарушения средней степени тяжести у пациентов с БП.
2. Исследовать влияние Вальдоксана на диссомнию при БП.
3. Изучить безопасность применения препарата Вальдоксан в комплексной терапии моторных и немоторных нарушений при БП.
Материалы и методы
Исследование проводилось на базе областной клинической больницы им. Н.А.Семашко. Лекарственный препарат Вальдоксан применялся в комплексном лечении пациентов с БП. Группу больных составили 18 пациентов – 10 женщин и 8 мужчин в возрасте от 58 до 76 лет (средний возраст составил 65,0±6,5 года) с БП с депрессивными расстройствами средней степени, возникшими нарушениями, несмотря на оптимизированную терапию препаратами леводопы и АДР. Средняя продолжительность заболевания – 5,6±1,1 года. Большую часть пациентов составляли люди пожилого возраста, с длительным течением БП, которым назначение традиционных трициклических антидепрессантов было противопоказано в связи с высоким риском возникновения отрицательных побочных эффектов, что могло привести к существенному снижению качества жизни. Как противопаркинсоническую терапию пациенты получали препараты леводопы – Наком, Мадопар; АДР – прамипексол, пирибедил, амантадин. Пятеро больных получали разагилин, что ограничивало применение селективных ингибиторов обратного захвата серотонина (СИОЗС) у данной категории пациентов. У 2 пациентов наличие депрессии ограничивало возможность проведения нейрохирургического лечения (нейростимуляции – deep brain stimulation, DBS). Исследование носило характер проспективного открытого рандомизированного. Критерием включения было наличие у пациентов депрессивных расстройств и нарушений сна. Всем больным проведено клинико-неврологическое исследование, которое кроме рутинного осмотра, оценки по шкале UPDRS включало определение выраженности инсомнии по анкете оценки сна, а также нейровизуализация – компьютерная и магнитно-резонансная томография головного мозга. Уровень депрессивных расстройств оценивался по Госпитальной шкале оценки тревоги и депрессии (HADS), шкале депрессии Бека, уровень тревоги – по шкале тревоги Спилберга. Данные шкалы обладают высокой информативностью при использовании в амбулаторной практике, в том числе у пациентов с БП [2, 4]. Вальдоксан назначался пациентам на 2 мес однократно вечером перед сном в дозе 25 мг/сут.
Статистическая обработка материала выполнена с помощью пакета прикладных программ Statistica 6.0. Для характеристики полученных данных использовались критерии описательной статистики: среднее арифметическое, среднеквадратичное отклонение. Данные представлены в формате М±s, где М – среднее арифметическое значение, а s – среднеквадратичное отклонение. Сравнение групп проводилось с использованием t-критерия Стьюдента. Различия, полученные при сравнительном анализе, считались статистически достоверными при p<0,05 [15].
Результаты исследования и обсуждение
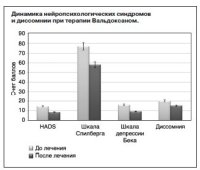
При обследовании пациентов до начала терапии у них наблюдались тревога и депрессия средней степени тяжести, а также инсомния. Особенностью депрессии являлось сочетание ощущения безысходности и пустоты, ангедония с пессимизмом, раздражительностью и грустью. Часто депрессия сопровождалась другими эмоционально-аффективными нарушениями – апатией, сужением круга интересов, отсутствием мотивации. Характерным было наличие тревожных расстройств. В ходе проводимой терапии все пациенты отмечали уменьшение депрессивных и тревожных расстройств, улучшение самочувствия и общего состояния. Средний балл по HADS снизился с 14,6±4,4 до 8,6±4,1 балла (р=0,001). Уровень тревоги и депрессии по данным HADS снизился с клинически значимого уровня до нормы у 10 пациентов. Счет пунктов по данным шкалы тревоги Спилберга уменьшился с 77±2 до 68±12 пунктов (р=0,0048). Отмечалось значительное снижение уровня депрессии по шкале Бека с 16,1±5,2 до 9,3±3,6 пункта (р=0,0002). Диссомния уменьшилась соответственно с 20,13±3,8 до 15,25±4,3 пункта (р=0,002). Одна пациентка после купирования депрессии была направлена на нейрохирургическое лечение (DBS). В послеоперационном периоде тревожных и депрессивных расстройств у больной отмечено не было, моторная функция являлась удовлетворительной на протяжении 6-месячного наблюдения.

Данные по динамике нейропсихологических синдромов и диссомнии приводятся на рисунке.
В ходе комплексной терапии с применением антидепрессанта Вальдоксан снижение уровня тревожных и депрессивных расстройств и инсомнии было отмечено у всех пациентов. У 9 больных депрессивные нарушения удалось купировать полностью. Антидепрессивный эффект несколько превышал противотревожный. Такой эффект Вальдоксана обусловлен его уникальным фармакологическим действием – антагонизмом по отношению к серотониновым 5-HT2C-рецепторам, но одновременно препарат является и агонистом к мелатониновым MT1- и MT2-рецепторам. Агонизм по отношению к мелатониновым рецепторам обусловливает хороший эффект препарата в отношении нарушений сна [12], однако нельзя исключать роль нарушения мелатонинового обмена и в развитии депрессии [25].
Сложность патогенеза нейромедиаторных расстройств объясняет существование проблемы купирования депрессивных нарушений при БП. При данной болезни выявляется более низкая, по сравнению с первичной депрессией, эффективность антидепрессантов. В контролируемых исследованиях у пациентов с БП доказана эффективность лишь трициклических антидепрессантов. В то же время эти препараты могут вызвать неприемлемые побочные эффекты: усугубление когнитивных нарушений, провоцирование психотических расстройств, ортостатической гипотензии, дневной сонливости. Таким образом, трициклические антидепрессанты рассматриваются как препараты второго выбора [7, 18].
Хотя более безопасными у пожилых пациентов являются СИОЗС, а также ингибиторы обратного захвата серотонина и норадреналина, у пациентов с БП имеются ограничения по применению препаратов этих фармакологических групп. Флуоксетин и флувоксамин не рекомендуется назначать при применении ингибитора моноаминоксидазы типа В разагилина, а при комбинации антидепрессантов с ингибитором моноаминоксидазы типа В селегилином имеется угроза серотонинового синдрома [8]. При применении Вальдоксана у пациентов с БП не было выявлено отрицательных побочных эффектов терапии.
Заключение
Значимость ряда немоторных проявлений БП, таких как психоэмоциональные расстройства и инсомния, для качества жизни пациентов, сложность патогенеза немоторных нарушений, резистентность их к терапии леводопой и ограничения использования традиционных препаратов требуют оптимизации подходов к терапии этих расстройств. Было показано, что особенностью действия антидепрессанта нового класса – Вальдоксана, реализующего свой эффект за счет влияния как на серотонин-, так и на мелатонинергическую систему, является одновременное уменьшение тревожно-депрессивных и диссомнических расстройств у пациентов с БП. Одним из механизмов действия Вальдоксана является коррекция хронобиологических ритмов. Вальдоксан показал свою хорошую совместимость со всеми классами противопаркинсонических средств и переносимость. Таким образом, Вальдоксан может рассматриваться не только как альтернативный традиционным антидепрессантам препарат для коррекции психоэмоциональных нарушений, но и средство для лечения диссомнии при депрессии средней тяжести у пациентов с БП.
Сведения об авторах
Густов А.В. – д-р мед. наук, проф., зав. каф. неврологии, нейрохирургии и психиатрии Центра повышения квалификации и профессиональной переподготовки специалистов ФПКВ ГБОУ ВПО НижГМА
Александрова Е.А. – канд. мед. наук, ассистент каф. неврологии, психиатрии и наркологии ФПКВ ГБОУ ВПО НижГМА, невролог кабинета экстрапирамидных расстройств ГБУЗ НО НОКБ им. Н.А.Семашко
Паршина Е.В. – канд. мед. наук, врач высшей категории, зав. 2-м неврологическим отд-нием ГБУЗ НО НОКБ им. Н.А.Семашко. Е-mail: official@semashko.nnov.ru
Список исп. литературыСкрыть список1. Медведев В.Э., Епифанов А.В., Ларцева О.А. Терапия кардионевроза («нейроциркуляторная дистония») в общей медицинской сети: опыт применения препарата вальдоксан. Врач. 2013; 4: 66–71. / Medvedev V.E., Epifanov A.V., Lartseva O.A. Terapiia kardionevroza (“neirotsirkuliatornaia distoniia”) v obshchei meditsinskoi seti: opyt primeneniia preparata val'doksan. Vrach. 2013; 4: 66–71. [in Russian]
2. Медведев В.Э., Епифанов А.В. Терапия депрессий у пациентов с гипертонической болезнью в условиях общемедицинского стационара. Психиатрия и психофармакотерапия. 2012; 14 (5): 14–8. / Medvedev V.E., Epifanov A.V. Terapiia depressii u patsientov s gipertonicheskoi bolezn'iu v usloviiakh obshchemeditsinskogo statsionara. Psychiatry and Psychopharmacotherapy. 2012; 14 (5): 14–8. [in Russian]
3. Медведев В.Э. и др. Терапия депрессий с явлениями ангедонии (опыт применения Вальдоксана). Психиатрия и психофармакотерапия. 2014; 16 (3): 4–8. / Medvedev V.E. i dr. Terapiia depressii s iavleniiami angedonii (opyt primeneniia Val'doksana). Psychiatry and Psychopharmacotherapy. 2014; 16 (3): 4–8. [in Russian]
4. Амон М., Буае П.Т., Моке Е. Перспективы в изучении патогенеза и терапии аффективных расстройств: роль мелатонина и серотонина. Журн. неврологии и психиатрии им. С.С.Корсакова. 2007; 11: 77–82. / Amon M., Buae P.T., Moke E. Perspektivy v izuchenii patogeneza i terapii affektivnykh rasstroistv: rol' melatonina i serotonina. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2007; 11: 77–82. [in Russian]
5. Белова А.Н., Щепетова О.Н. Шкалы, тесты и опросники в медицинской реабилитации. Руководство для врачей и научных работников. М.: Антидор, 2002; с. 439. / Belova A.N., Shchepetova O.N. Shkaly, testy i oprosniki v meditsinskoi reabilitatsii. Rukovodstvo dlia vrachei i nauchnykh rabotnikov. M.: Antidor, 2002; s. 439. [in Russian]
6. Бриль Е.В., Томский А.А., Федорова Н.В. и др. Нейрохирургическое лечение болезни Паркинсона. К 35-летию основания Центра экстрапирамидных заболеваний. Экстрапирамидные расстройства вчера, сегодня, завтра. Сб. статей под ред. проф. О.С.Левина. М., 2013; с. 156–62. / Bril' E.V., Tomskii A.A., Fedorova N.V. i dr. Neirokhirurgicheskoe lechenie bolezni Parkinsona. K 35-letiiu osnovaniia Tsentra ekstrapiramidnykh zabolevanii. Ekstrapiramidnye rasstroistva vchera, segodnia, zavtra. Sb. statei pod red. prof. O.S.Levina. M., 2013; s. 156–62. [in Russian]
7. Воробьев П.А. Протокол ведения больных. Болезнь Паркинсона. М.: Ньюдиамед, 2006; с 184. / Vorob'ev P.A. Protokol vedeniia bol'nykh. Bolezn' Parkinsona. M.: N'iudiamed, 2006; s 184. [in Russian]
8. Иванова-Смоленская И.А., Левин О.С., Шток В.Н. Экстрапирамидные расстройства. Руководство по диагностике и лечению. М.: МЕДпресс-информ, 2002; с. 606. / Ivanova-Smolenskaia I.A., Levin O.S., Shtok V.N. Ekstrapiramidnye rasstroistva. Rukovodstvo po diagnostike i lecheniiu. M.: MEDpress-inform, 2002; s. 606. [in Russian]
9. Иллариошкин С.Н. Немоторные проявления болезни Паркинсона. Нервы. 2007; 1: 27–30. / Illarioshkin S.N. Nemotornye proiavleniia bolezni Parkinsona. Nervy. 2007; 1: 27–30. [in Russian]
10. Левин О.С. Психические расстройства при болезни Паркинсона и их коррекция. Экстрапирамидные расстройства. Руководство по диагностике и лечению. Под ред. В.Н.Штока, И.А.Ивановой-Смоленской, О.С.Левина. М.: МЕДпресс-информ, 2002; с. 125–51. / Levin O.S. Psikhicheskie rasstroistva pri bolezni Parkinsona i ikh korrektsiia. Ekstrapiramidnye rasstroistva. Rukovodstvo po diagnostike i lecheniiu. Pod red. V.N.Shtoka, I.A.Ivanovoi-Smolenskoi, O.S.Levina. M.: MEDpress-inform, 2002; s. 125–51. [in Russian]
11. Левин О.С. Болезнь Паркинсона как нейропсихиатрическое заболевание. Неврология/ревматология. 2011; 2: 18–22. / Levin O.S. Bolezn' Parkinsona kak neiropsikhiatricheskoe zabolevanie. Nevrologiia/revmatologiia. 2011; 2: 18–22. [in Russian]
12. Левин О.С., Федорова Н.В. Болезнь Паркинсона. Изд. 3-е. М., 2012. / Levin O.S., Fedorova N.V. Bolezn' Parkinsona. Izd. 3-e. M., 2012. [in Russian]
13. Нодель М.Р., Яхно Н.Н.. Недвигательные проявления болезни Паркинсона и их влияние на качество жизни. Болезнь Паркинсона и расстройства движений. Руководство для врачей по материалам 1-го Национального конгресса. Москва, 22–23 сентября 2008 г. С. 92–4. / Nodel' M.R., Iakhno N.N.. Nedvigatel'nye proiavleniia bolezni Parkinsona i ikh vliianie na kachestvo zhizni. Bolezn' Parkinsona i rasstroistva dvizhenii. Rukovodstvo dlia vrachei po materialam 1-go Natsional'nogo kongressa. Moskva, 22–23 sentiabria 2008 g. S. 92–4. [in Russian]
14. Нодель М.Р. Недвигательные нарушения болезни Паркинсона. Неврология. 2009; 4: 12–6. / Nodel' M.R. Nedvigatel'nye narusheniia bolezni Parkinsona. Nevrologiia. 2009; 4: 12–6. [in Russian]
15. Нодель М.Р. Нарушения сна и бодрствования при болезни Паркинсона: комплексный подход к терапии. Неврология, нейропсихиатрия, психосоматика. Вып. 1. 2012; с 43–8. / Nodel' M.R. Narusheniia sna i bodrstvovaniia pri bolezni Parkinsona: kompleksnyi podkhod k terapii. Nevrologiia, neiropsikhiatriia, psikhosomatika. Vyp. 1. 2012; s 43–8. [in Russian]
16. Олье Ж.-П., Каспер З. Эффективность Вальдоксана (агомелатина), агониста МТ1/МТ2-рецепторов и антагониста
5-НТ2с-рецепторов при большом депрессивном расстройстве. Рос. психиатр. журн. 2009; 2: 85–95. / Ol'e Zh.-P., Kasper Z. Effektivnost' Val'doksana (agomelatina), agonista MT1/MT2-retseptorov i antagonista 5-NT2s-retseptorov pri bol'shom depressivnom rasstroistve. Ros. psikhiatr. zhurn. 2009; 2: 85–95. [in Russian]
17. Полуэктов М.Г., Левин Я.И. Результаты российского мультицентрового открытого обсервационного несравнительного исследования эффективности и безопасности вальдоксана (агомелатин) при лечении пациентов с большим депрессивным расстройством и нарушениями сна (исследование ВИВАЛЬДИ). Журн. неврологии и психиатрии им. С.С.Корсакова. 2013; 12: 39–45. / Poluektov M.G., Levin Ia.I. Rezul'taty rossiiskogo mul'titsentrovogo otkrytogo observatsionnogo nesravnitel'nogo issledovaniia effektivnosti i bezopasnosti val'doksana (agomelatin) pri lechenii patsientov s bol'shim depressivnym rasstroistvom i narusheniiami sna (issledovanie
VIVAL''DI). Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2013; 12: 39–45. [in Russian]
18. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. М.: МедиаСфера, 2002. / Rebrova O.Iu. Statisticheskii analiz meditsinskikh dannykh. Primenenie paketa prikladnykh programm STATISTICA. M.: MediaSfera, 2002. [in Russian]
19. Федорова Н.В., Мирецкая А.В., Кулуа Т.К. Депрессия и тревога при болезни Паркинсона. Трудный пациент. Архив. 2006; 7. / Fedorova N.V., Miretskaia A.V., Kulua T.K. Depressiia i trevoga pri bolezni Parkinsona. Trudnyi patsient. Arkhiv. 2006; 7. / [in Russian]
20. Adi N, Mash DC, Ali E et al. Melatonin MT1 and MT2 receptors expression in Parkinsons disease. Med Sci Monit 2010; BR61–BR67.
21. Ardouin C, Lhomme E, Thobois S et al. Piribedil improves apathy, depression and anxiety in Parkinson’s disease. Mov Disord 2009; 24 (Suppl. 1): S233.
22. Bordet R, Devos D, Brique S et al. Study of circadian melatonine secretion pattern at different stages of Parkinsons disease. Clin Neuropharmacol 2003; 26 (2): 65–72.
23. Hardeland R, Poeggeler B, Srinivasan V et al. Melatonergic drugs in clinical practice. Arzneimittelforschung 2008; 58 (1): 1–10.
24. Goodwin GM. Clinical studies on the efficacy of agomelatine on depressive symptoms. CNS Drugs 2009; 23 (Suppl. 2): 35–9.
25. Fertl E, Auff E, Doppelbauer A et al. Circadian secretion pattern of melatonin in de novo parkinsonian patients: evidence for phase-shifting properties of l-dopa. J Neural Transm Park Dis Dement Sect 1993; 5 (3): 227–34.
26. Fountoulakis KN. Disruption of biological rhythms as a core problem and therapeutic target in mood disorders: the emerging concept of “rhythm regulators”. Annals of General Psychiat 2010; 9: 3.
27. Kasper S, Hamon M. Beyond the monoaminergic hypothesis: agomelatine, a new antidepressant with an innovative mechanism of action. World J Biol Psychiat 2009; 10 (2): 117–26.
28. Lemoine P, Guilleminault C, Alvarez E. Improvement of subjective sleep in Major depressive disorder with a novel antidepressant agomelatine: randomized, double blind comparison with venlafaxine. J Clin Psychiat 2007; 68: 11: 1723–32.
29. Racagni G, Riva MA, Popoli M. The interaction between the internal clock and antidepressant efficacy. Int Clin Psychopharmacol 2007; Suppl. 2: 9–14.
30. Srinivasan V, Pandi-Perumal SR, Trakht I et al. Pathophysiology of depression: role of sleep and the melatonergic system. Psychiatry Res 2009; 3: 201–14.
31. Turek F, Gillette M. Melatonin, sleep and circadian rhythms: rationale for the development of specific melatonin agonists. Slepp Med 2004; 5: 526–32.
