Психиатрия Всемирная психиатрия
Психиатрия Всемирная психиатрия
№03 2018
Психологические вмешательства, направленные на редукцию позитивных симптомов при шизофрении: систематический обзор и сетевой мета-анализ №03 2018
Номера страниц в выпуске:308-321
Психологическая помощь все чаще рассматривается в числе полезных видов вмешательств при шизофрении. Однако многосторонняя оценка имеющихся тому доказательств отсутствует, а преимущество психологических вмешательств для пациентов, имеющих позитивные симптомы, до сих пор остается предметом дискуссий. Целью данного исследования является оценка эффективности, допустимости и переносимости психологических методов лечения при позитивных симптомах шизофрении при помощи сетевого мета-анализа, способного интегрировать как прямые, так и косвенные сравнения. По базам EMBASE, MEDLINE, PsychINFO, PubMed, BIOSIS, Кокрановская библиотека, Международный реестр клинических исследований Всемирной организации здравоохранения и ClinicalTrials.gov был выполнен поиск рандомизированных контролируемых исследований, посвященных психологическому лечению при позитивных симптомах шизофрении, опубликованных до 10 января 2018 г. Были рассмотрены исследования с участием взрослых пациентов, имеющих диагноз шизофрении или расстройства шизофренического спектра, сопровождаемого позитивными симптомами. Первичным клиническим исходом считалось изменение в позитивных симптомах, измеряемое при помощи валидированных рейтинговых шкал. Мы отобрали 53 рандомизированных контролируемых исследования семи разновидностей психологических вмешательств с участием 4068 пациентов, получавших психологическую помощь в дополнение к лечению антипсихотиками. В среднем на исходном уровне пациенты имели психическое расстройство умеренной степени выраженности. Сетевой мета-анализ продемонстрировал, что когнитивно-поведенческая терапия (КПТ; 40 исследований) больше способствует редукции позитивной симптоматики, чем неактивный контроль [стандартизованная разность средних (standardized mean difference – SMD) = –0,29; 95% доверительный интервал (ДИ) от –0,55 до –0,03], стандартное лечение (SMD=–0,30; 95% ДИ от –0,45 до –0,14) и поддерживающая терапия (SMD=–0,47; 95% ДИ от –0,91 до –0,03). КПТ ассоциирована с более высоким числом случаев выбытия пациентов из лечения по сравнению со стандартным лечением [соотношение рисков (risk ratio) RR=0,74; 95% ДИ 0,58–0,95]. Достоверность оценок колебалась от умеренной до очень низкой. Другие методы лечения способствовали созданию сети с меньшим количеством исследований. Результаты в целом показали согласованность в анализе чувствительности с исключением ряда факторов, в том числе роли приверженности исследователей и использования слепого метода в отношении лиц, оценивавших исходы. КПТ представляется эффективной в отношении работы с позитивными симптомами у пациентов с умеренной формой расстройства при шизофрении, с величиной эффекта в нижнем и среднем диапазоне, в зависимости от контрольного условия.
Ключевые слова: шизофрения, позитивные симптомы, психологические вмешательства, когнитивно-поведенческая терапия, сетевой мета-анализ.
Ключевые слова: шизофрения, позитивные симптомы, психологические вмешательства, когнитивно-поведенческая терапия, сетевой мета-анализ.
Перевод: Шкурина Ж.В. (Москва)
Редактура: к.м.н. Чумаков Е.М. (Санкт-Петербург)
Психологическая помощь все чаще рассматривается в числе полезных видов вмешательств при шизофрении. Однако многосторонняя оценка имеющихся тому доказательств отсутствует, а преимущество психологических вмешательств для пациентов, имеющих позитивные симптомы, до сих пор остается предметом дискуссий. Целью данного исследования является оценка эффективности, допустимости и переносимости психологических методов лечения при позитивных симптомах шизофрении при помощи сетевого мета-анализа, способного интегрировать как прямые, так и косвенные сравнения. По базам EMBASE, MEDLINE, PsychINFO, PubMed, BIOSIS, Кокрановская библиотека, Международный реестр клинических исследований Всемирной организации здравоохранения и ClinicalTrials.gov был выполнен поиск рандомизированных контролируемых исследований, посвященных психологическому лечению при позитивных симптомах шизофрении, опубликованных до 10 января 2018 г. Были рассмотрены исследования с участием взрослых пациентов, имеющих диагноз шизофрении или расстройства шизофренического спектра, сопровождаемого позитивными симптомами. Первичным клиническим исходом считалось изменение в позитивных симптомах, измеряемое при помощи валидированных рейтинговых шкал. Мы отобрали 53 рандомизированных контролируемых исследования семи разновидностей психологических вмешательств с участием 4068 пациентов, получавших психологическую помощь в дополнение к лечению антипсихотиками. В среднем на исходном уровне пациенты имели психическое расстройство умеренной степени выраженности. Сетевой мета-анализ продемонстрировал, что когнитивно-поведенческая терапия (КПТ; 40 исследований) больше способствует редукции позитивной симптоматики, чем неактивный контроль [стандартизованная разность средних (standardized mean difference – SMD) = –0,29; 95% доверительный интервал (ДИ) от –0,55 до –0,03], стандартное лечение (SMD=–0,30; 95% ДИ от –0,45 до –0,14) и поддерживающая терапия (SMD=–0,47; 95% ДИ от –0,91 до –0,03). КПТ ассоциирована с более высоким числом случаев выбытия пациентов из лечения по сравнению со стандартным лечением [соотношение рисков (risk ratio) RR=0,74; 95% ДИ 0,58–0,95]. Достоверность оценок колебалась от умеренной до очень низкой. Другие методы лечения способствовали созданию сети с меньшим количеством исследований. Результаты в целом показали согласованность в анализе чувствительности с исключением ряда факторов, в том числе роли приверженности исследователей и использования слепого метода в отношении лиц, оценивавших исходы. КПТ представляется эффективной в отношении работы с позитивными симптомами у пациентов с умеренной формой расстройства при шизофрении, с величиной эффекта в нижнем и среднем диапазоне, в зависимости от контрольного условия.
Ключевые слова: шизофрения, позитивные симптомы, психологические вмешательства, когнитивно-поведенческая терапия, сетевой мета-анализ.
(World Psychiatry 2018;17(3):316-329)
Психологические вмешательства при шизофрении разрабатывались в отношении многих аспектов этого расстройства и, согласно рекомендациям Национального института совершенствования качества охраны здоровья (National Institute for Health and Care Excellence – NICE)1 Великобритании и Группы исследований исходов при шизофрении (Schizophrenia Patient Outcomes Research Team – PORT)2 в США, признаются в качестве полезных.
Применительно к этим видам лечения выполнялся ряд систематических обзоров рандомизированных исследований3. Однако результаты представляются неясными и зачастую противоречивыми. Например, в то время как некоторые обзоры4,5 выявили преимущество когнитивно-поведенческой терапии (КПТ) перед стандартным лечением, другие авторы не смогли подтвердить эти выводы, как только ими были исключены неслепые рандомизированные контролируемые исследования (РКИ)6. Кокрановский обзор говорит об эффективности КПТ в долгосрочной перспективе, но не в краткосрочной или среднесрочной7; при этом другой мета-анализ не нашел у КПТ никаких преимуществ8.
Более того, имеющиеся доказательные данные обладают несколькими недостатками. Прежде всего, во всех существующих обзорах единовременно сравнивались два метода лечения путем попарного мета-анализа. Этот способ обобщает результаты, только когда два метода уже сопоставлялись между собой в предыдущих исследованиях, что оставляет открытым вопрос о всех других возможных сравнениях. Даже в обзоре Turner и соавт.9, включавшем только исследования по сравнению двух «активных психологических вмешательств», попарный мета-анализ применялся для сравнения каждого вида вмешательства со всеми другими в совокупности, снова не предоставляя информации о сравнениях, которые не рассматривались в исследованиях.
Помимо этого, для существующих обзоров характерна неоднородная выборка, состоящая из пациентов с различными наборами симптомов. Ни один обзор не фокусировался отдельно на пациентах, имеющих позитивную симптоматику, которая – по крайней мере, в своей острой фазе – формирует ядро расстройства. Также в обзоре Zimmermann и соавт.5, посвященном оценке воздействия КПТ на позитивные симптомы, выборка не была ограничена только лишь пациентами с этим видом симптомов.
С учетом этих ограничений в существующих доказательных данных до сих пор остается неясным, имеются ли эффективные и приемлемые виды психологических вмешательств, позволяющие лечить позитивные симптомы при шизофрении.
Целью настоящего исследования было превзойти указанные ограничения путем проведения сетевого мета-анализа, который интегрирует как прямые, так и косвенные сравнения видов вмешательств10 и предоставляет данные о различиях между ними даже там, где прямые сравнения невозможны. Подобный мета-анализ требует определенного уровня однородности генеральной совокупности, условий и методов исследования. Таким образом, для получения информации, полезной для клинической практики, необходим тщательный подход к определению целевой генеральной совокупности.
Данный сетевой мета-анализ рассматривает психологические вмешательства, направленные на работу с позитивными симптомами шизофрении у пациентов, имеющих эти симптомы в настоящий момент, чтобы получить результаты, актуальные для этой конкретной генеральной совокупности.
Дизайн исследования и участники
Детализированная методология настоящего систематического обзора и сетевого мета-анализа приведена в протоколе исследования, зарегистрированном априори на PROSPERO (№ CRD42017067795) и опубликованном3. В описании результатов мы руководствовались заявлением PRISMA для сетевых мета-анализов11,12.
Были отобраны исследования с участием взрослых пациентов с диагнозом шизофрении или расстройства шизофренического спектра (таких как шизофрениформное или шизоаффективное расстройство) с активной позитивной симптоматикой или в фазе обострения, согласно формулировке критерия включения в исследование, без ограничений по условиям лечения, гендерной и этнической принадлежности. Мы обеспечили гомогенность исследований в рамках и за пределами сравнений видов вмешательств, исключив исследования на пациентах с преобладающими негативными симптомами, сопутствующими заболеваниями или психическими расстройствами, а также пациентов с первым психотическим эпизодом или риском психоза. Исследования включались, если как минимум 80% пациентов имели шизофрению или расстройство шизофренического спектра. В случае смешанной генеральной совокупности данные о пациентах с шизофренией извлекались при условии их доступности. Исследования включались независимо от использованных критериев диагностики.
Группы сравнения были классифицированы следующим образом: а) вмешательства (например, когнитивная реабилитация, психообразование) с первичной целью, отличной от работы с позитивными симптомами (например, когнитивные функции, информирование о болезни, соблюдение режима приема препаратов, функционирование), которые изначально анализировались в качестве отдельных узлов, а затем комбинировались в анализе чувствительности;
б) неактивный контроль, определяемый как вмешательства, контролирующие неспецифические аспекты терапии (например, выслушивание, рекреация и поддержка, терапия социальной активности, поддерживающее консультирование) и иногда также именуемые «психологическим плацебо»; в) стандартное лечение (т. е. пациенты, продолжающие получать стандартное психиатрическое лечение);
г) лист ожидания.
В качестве вторичных исходов рассматривались: выбытие из исследования по любой причине, воздействие на общие симптомы шизофрении, влияние на негативные симптомы, ответ на терапию (как определено в исследовании), рецидив (определяемый при помощи рейтинговых шкал или, в случае невозможности, по повторной госпитализации из-за психопатологии), приверженность лечению и осознание, изменения в депрессивной симптоматике, качество жизни и функционирования, неблагоприятные события, которые могут быть связаны с психологическим лечением (по Linden и соавт.15) и смертность (рассматриваемая как смерть по любой причине, смерть по естественным причинам, смерть в результате суицида). Все исходы оценивались в конечной точке исследования, что определялось в каждом отдельном исследовании.
Ограничений по языку не вводилось, с тем лишь исключением, что не осуществлялся поиск по базам данных Китая. Мы обращались к авторам исследований, опубликованных в последние 30 лет, за недостающей или дополнительной информацией об их работах.
Два исследователя независимо друг от друга извлекали данные из отобранных исследований, принимая во внимание как основные тексты, так и дополнительные материалы, вносили необходимые сведения в базу Microsoft Access, созданную специально для настоящего исследования, и измеряли риск систематической ошибки инструментом оценки риска систематической ошибки Кокрановского сотрудничества16. Рассматривались следующие области возможного смещения: генерация случайной последовательности, сокрытие распределения участников в группы, использование слепого метода в отношении участников и лиц, оценивавших исходы, неполные исходные данные, выборочная отчетность, предвзятость исследователей17,18, другие систематические ошибки. Мы также сформировали общий рейтинг риска систематической ошибки для каждого исследования, основываясь на критериях, примененных в сетевом мета-анализе для антидепрессантов19.
Перед выполнением сетевого мета-анализа мы попытались оценить предположение о транзитивности. Оно подразумевает, что исследования, сравнивающие различные наборы методов вмешательств, достаточно схожи для того, чтобы обеспечить корректные косвенные выводы, что мы и пытались обеспечить, установив узкие критерии включения и добиваясь как можно большей однородности генеральной совокупности как в рамках сравнения видов лечения, так и за его пределами. Также мы рассмотрели вопрос о том, распределяются ли похожим образом и модификаторы потенциального эффекта во всех доступных прямых сравнениях.
Мы взяли общий параметр неоднородности для различных сравнений видов лечения и вычислили дисперсию между исследованиями (tau2) для каждого исхода. Уровень неоднородности был охарактеризован как низкий, умеренный или высокий на основе первого и третьего квантилей их эмпирических распределений23. Статистическая несогласованность была оценена путем отделения прямых доказательств от косвенных, предоставленных всей сетью, и дальнейшей проверки на соответствие этих двух видов доказательств24. Величина коэффициентов несогласованности (различия между прямыми и косвенными SMD) и соответствующие им значения p использовались для определения наличия несогласованности. Мы также применили модель для оценки взаимодействия результатов лечения, которая позволяет оценить непостоянство в сети в совокупности25.
Для исследования возможных источников неоднородности и непостоянства мы спланировали априорный анализ субгрупп для первичного исхода по следующим модификаторам потенциального эффекта: количество сессий, продолжительность исследования, сеттинг (индивидуальная или групповая терапия), компетентность терапевта, изначальная тяжесть состояния. Был выполнен анализ чувствительности с исключением открытых исследований, исследований только лишь с анализом полученного и завершенного лечения, исследований с общим высоким риском систематической ошибки19, исследований с высоким риском предвзятости исследователей, исследований, сфокусированных на резистентных к лечению пациентах и исследований с неактивной группой сравнения. Нами также были оценены эффекты небольших исследований (потенциально ассоциированных с риском предвзятости при публикации) путем анализа воронкообразных участков в попарном мета-анализе и скорректированных по размерам воронкообразных участков, если исследований было 10 и больше26.
В дополнение к этому мы измерили достоверность оценок первичного исхода с помощью инструмента оценки достоверности CINeMA (Confidence in Network Meta-Analysis), адаптации системы градации измерения, разработки и оценки качества рекомендаций (Grading of Recommendations Assessment, Development and Evaluation framework – GRADE), разработанной специально для сетевого мета-анализа27.
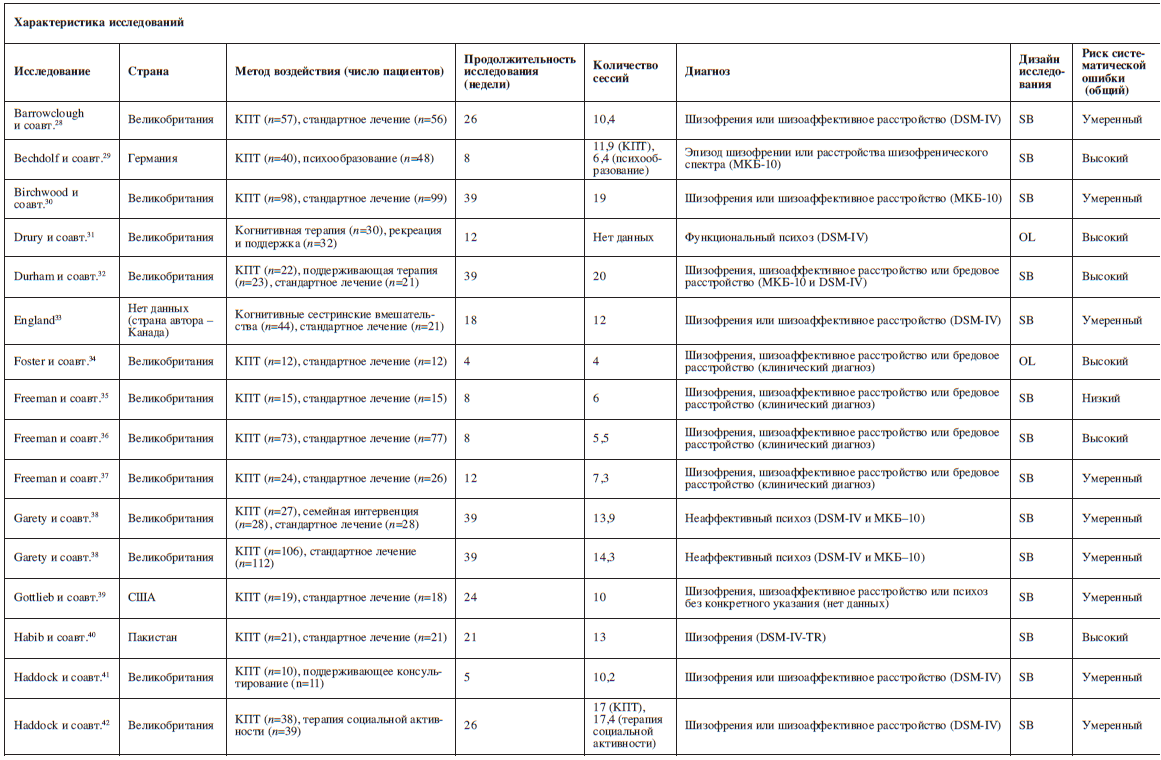
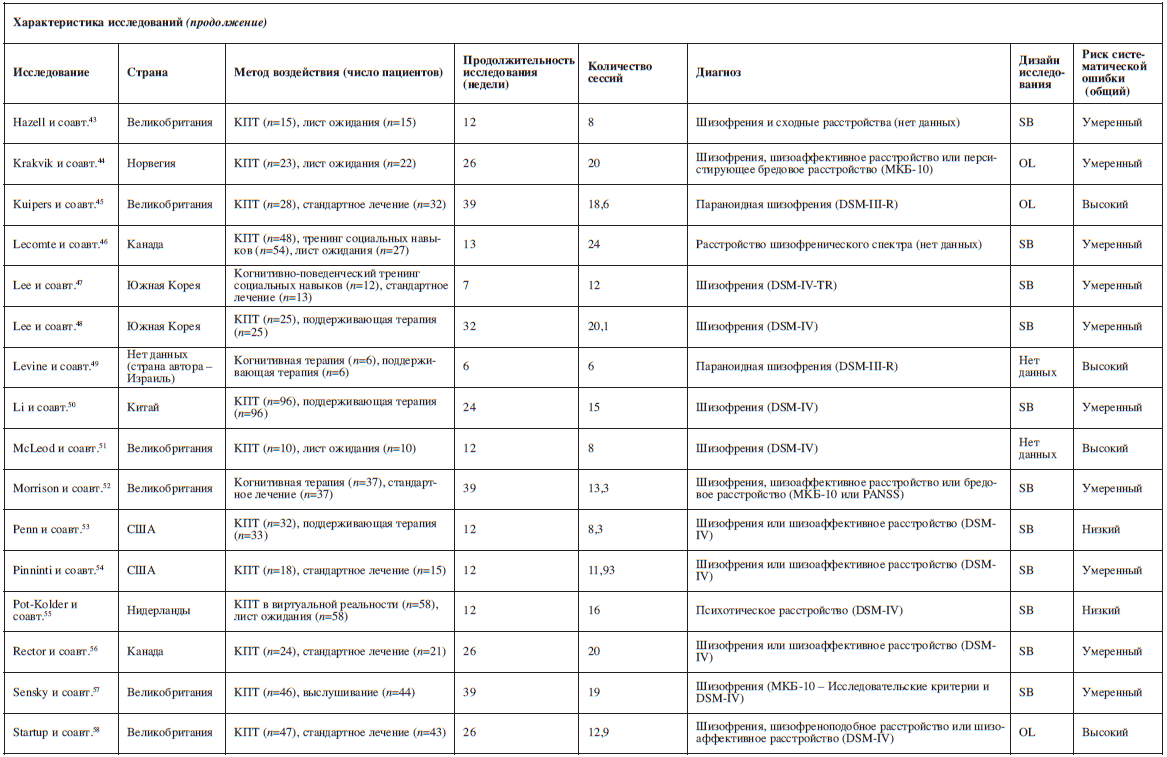
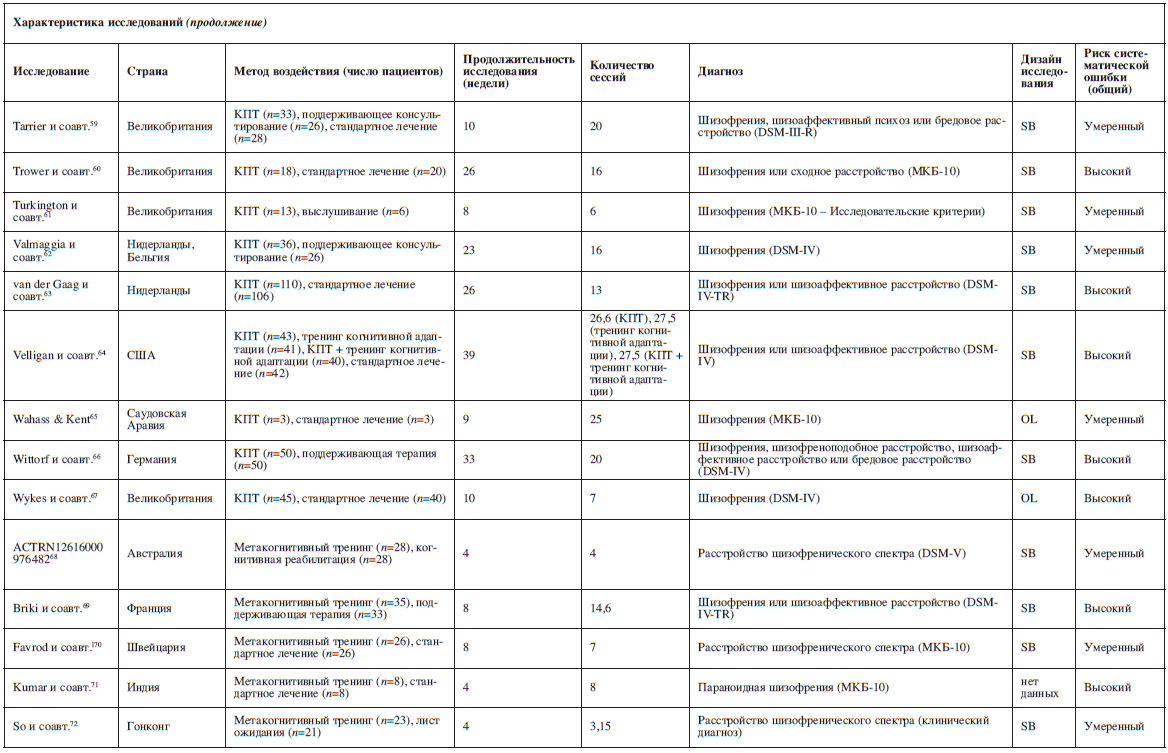
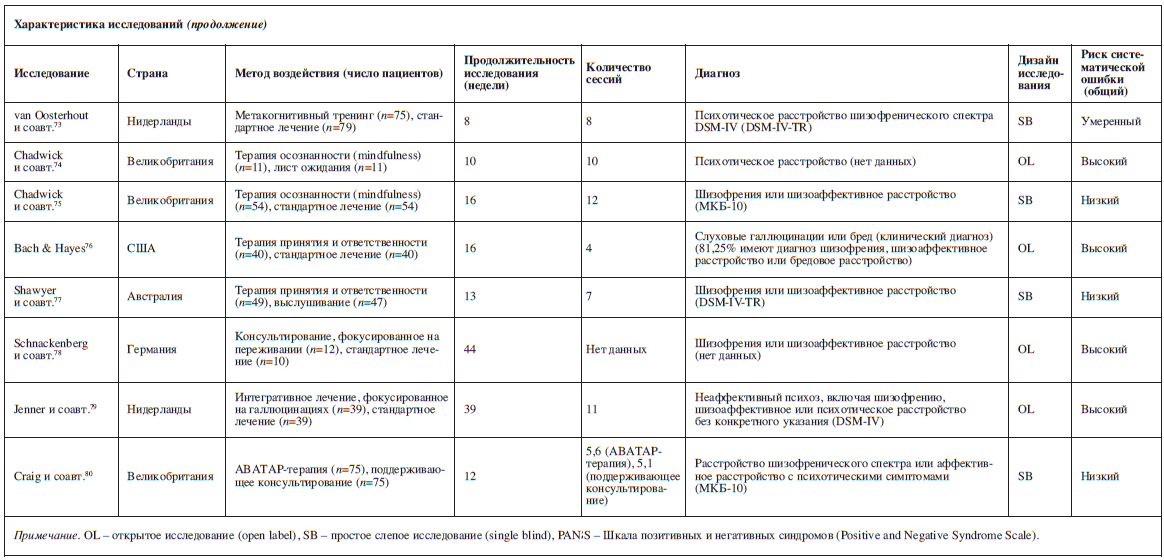
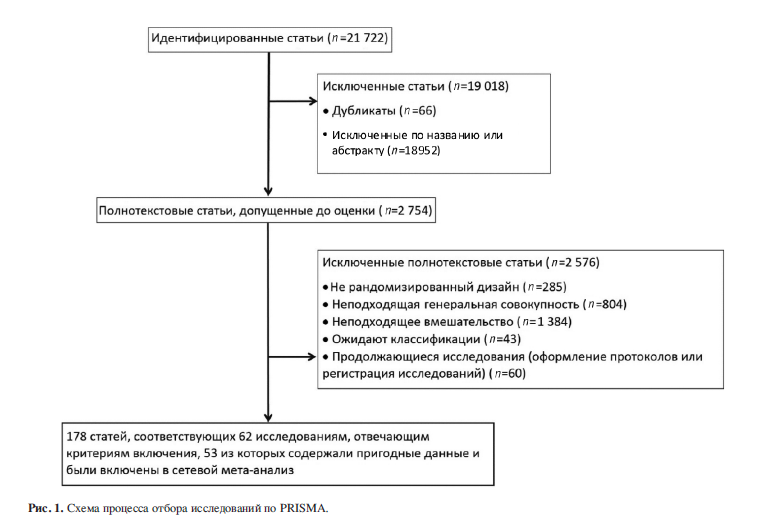
В результате поиска было найдено 21 772 ссылки (дата последнего обращения – 10 января 2018 г.), 2754 статьи были получены в полном тексте (рис. 1). Мы отобрали 62 рандомизированных контролируемых исследования, 53 из которых содержали пригодные данные и вошли в сетевой мета-анализ (с участием 4068 пациентов; см. таблицу).
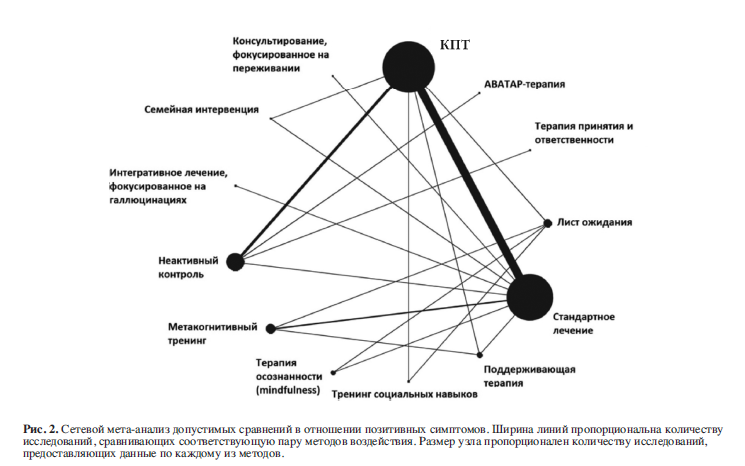
В этих исследованиях сравнивались следующие методы психологического лечения: КПТ (n=40)28–67, метакогнитивный тренинг (n=6)68–73, терапия осознанности (mindfulness) (n=2)74,75, терапия принятия и ответственности (n=2)76,77, консультирование, фокусированное на переживании (n=1)78, интегративное лечение, фокусированное на галлюцинациях (n=1)79, и АВАТАР-терапия (n=1)80.
Средний объем выборки составил 76,5 пациента (размах колебаний 6–218), а средняя продолжительность исследования – 13 недель (размах колебаний 4–44 недели). Из 3941 пациента с известными данными о поле 2361 были мужчинами (59,9%). Средняя продолжительность расстройства составляла 12,4 года, средний возраст пациентов – 37,4 года. В 9 исследованиях рассматривались только пациенты стационара, в 15 – только амбулаторные пациенты, в 14 – оба типа пациентов, а в 15 исследованиях информация о форме лечения пациентов не предоставлялась. В среднем пациенты имели симптомы шизофрении умеренной степени выраженности со средним баллом 68,26 по шкале PANSS81,82. Благодаря готовности авторов к сотрудничеству нам удалось включить и неопубликованные данные для нескольких исследований36,37,41–43,57,61,68,72.
Результаты сетевого мета-анализа для первичного исхода показали ассоциированность КПТ с более высоким уровнем редукции позитивной симптоматики по сравнению с неактивным контролем (SMD=−0,29; 95% ДИ от –0,55 до −0,03, семь РКИ предоставили прямые доказательства в сетевой мета-анализ с низкой достоверностью оценок), стандартным лечением (SMD=−0,30; 95% ДИ от –0,45 до −0,14; 18 РКИ предоставили прямые доказательства со средней достоверностью оценок) и поддерживающей терапией (SMD=−0,47; 95% ДИ от –0,91 до −0,03; два РКИ предоставили прямые доказательства с низкой достоверностью оценок). В сопоставлении с листом ожидания разница была незначимой (SMD=−0,24; 95% ДИ: от –0,65 до 0,16), однако прямые доказательства в это сравнение предоставили лишь два небольших исследования с 30 и 45 участниками, соответственно43,44 (рис. 3).
Одно из исследований, посвященное интегративной терапии, фокусированной на галлюцинациях, продемонстрировало снижение выраженности симптоматики по сравнению со стандартным лечением и поддерживающей терапией (умеренная и низкая достоверность оценок, соответственно). Относительные эффекты от всех прочих методов лечения были очень неопределенными, но в среднем отражали преимущество активного психологического лечения перед методами неактивного контроля.
Неоднородность дисперсии (tau2) составила 0,0514, что расценивается как значение в диапазоне от низкого до умеренного23. Тест оценки взаимодействия результатов лечения не выявил значительной несогласованности (p=0,35). Разделив прямые и косвенные доказательства для каждого сравнения, мы не нашли подтверждений несоответствия между двумя видами доказательств для любого из сравнений. Ни один из использованных нами методов не предоставил серьезной несогласованности, но, с учетом небольшого количества исследований для большинства из сравнений, мощность этих тестов невысока. Измерение достоверности оценок с помощью CINeMA показало уровень достоверности от умеренного к очень низкому, в основном из-за ограничений исследования (высокий риск систематической ошибки) и неточностей.
Интерпретация анализа субгрупп ограничена ввиду недостаточного количества исследований для разных субгрупп. Мы не обнаружили какого-либо явного указания на то, что преимущество КПТ перед стандартным лечением определяется количеством сессий, продолжительностью исследования, сеттингом (индивидуальной или групповой терапией), компетентностью терапевта или изначальной тяжестью состояния.
Аналогичным образом, после исключения различных исследований в анализе чувствительности осталось небольшое количество исследований для большинства методов лечения. После исключения открытых исследований результаты сравнения КПТ со стандартным лечением и поддерживающей терапией сохранили согласованность с основным анализом (SMD=−0,27; 95% ДИ от –0,41 до −0,13 и SMD=−0,47; 95% ДИ от –0,86 до −0,08, соответственно), в то время как различия между КПТ и неактивным контролем утратили значимость (SMD=−0,14; 95% ДИ от –0,37 до 0,09).
Анализ чувствительности с исключением только исследований с анализом полученного и завершенного лечения, исследований с высоким риском систематической ошибки, исследований с высоким риском систематической ошибки ввиду предвзятости исследователей, а также исследований, сфокусированных на пациентах, резистентных к лечению, в целом соответствовал результатам основного анализа.
Результаты post-hoc анализа чувствительности с объединением групп сравнения «активного контроля» не отличались от основных.
Изучение эффекта небольших исследований и риска предвзятости при публикации с использованием обычного графика воронки не выявило никакой связи между точностью исследования и величиной эффекта (применимо только к сопоставлению КПТ со стандартным лечением). Однако график воронки, скорректированный по размеру, позволяет предположить, что небольшие исследования, которые не продемонстрировали никаких преимуществ новых методов психологического лечения перед старыми, недопредставлены в наших материалах (возможно, они остаются неопубликованными).
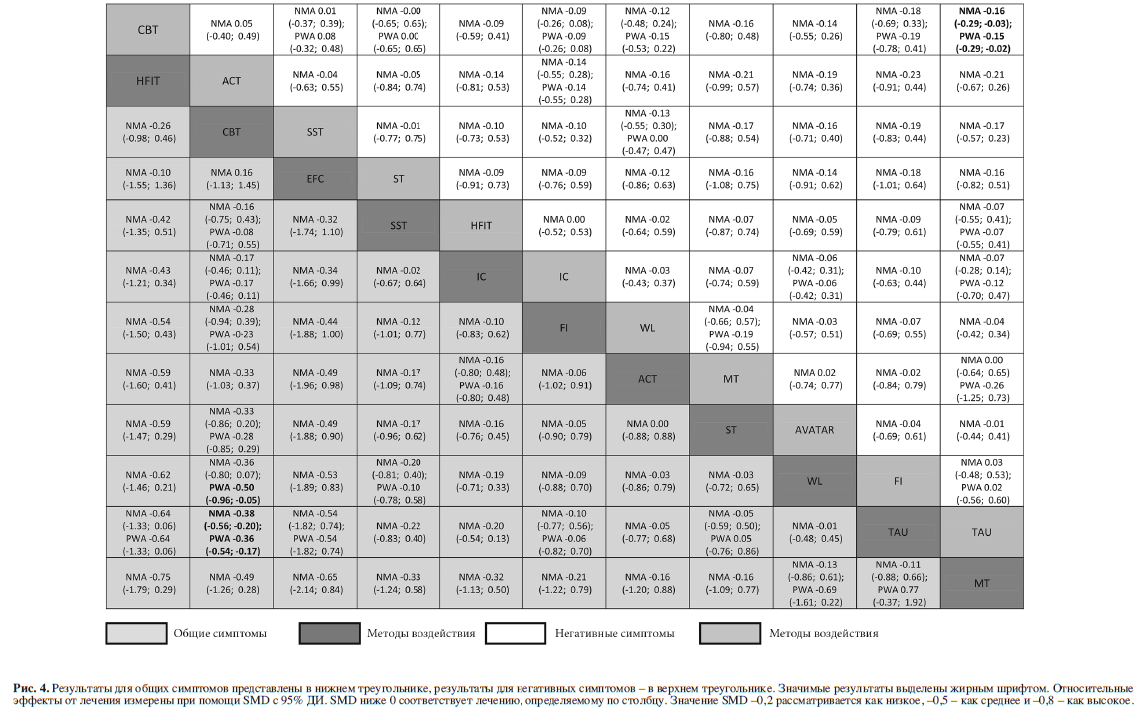
Также КПТ была связана с более высоким уровнем редукции общих симптомов по сравнению с листом ожидания и стандартным лечением и с более высоким уровнем редукции негативной симптоматики по сравнению со стандартным лечением (рис. 4). Интегративное лечение, фокусированное на галлюцинациях, и КПТ ассоциированы с большей вероятностью ответа на лечение в сравнении со стандартным лечением и неактивным контролем.
С точки зрения приверженности лечению и осознания, метакогнитивный тренинг, тренинг социальных навыков, КПТ и стандартное лечение приводили к большим улучшениям по сравнению с поддерживающей терапией. КПТ была более эффективна, чем стандартное лечение, в отношении качества жизни и функционирования. Никаких значимых различий в отношении депрессии не наблюдалось. Смертность в целом была достаточно редка и не различалась в зависимости от методов лечения. Данных о рецидивах, неблагоприятных событиях и смертельных исходах было предоставлено очень мало.
Неоднородность дисперсии (tau2) колебалась от 0 до 0,0649, т. е. от полного отсутствия до низкого и умеренного уровня. Модель оценки взаимодействия результатов лечения продемонстрировала некоторую несогласованность вторичных исходов применительно к депрессии (p=0,03).
В 40 исследованиях наиболее часто встречающимся методом среди других стала КПТ. Мы обнаружили существенно более высокую эффективность КПТ по сравнению со стандартным лечением в отношении многих исходов (позитивные, общие и негативные симптомы, отклик на лечение, качество жизни и функционирования), большую эффективность по сравнению с неактивным контролем в отношении позитивных симптомов и отклика на лечение и по сравнению с поддерживающей терапией – в отношении приверженности лечению. Убедительных доказательств эффективности других методов получено не было, возможно, ввиду малого количества исследований.
КПТ также была ассоциирована с большим процентом выбытия пациентов из лечения по сравнению со стандартным лечением (18,8 против 12%). КПТ не всегда может быть подходящим методом, и не все пациенты могут захотеть участвовать в столь трудоемком лечении; впрочем, мы убеждены, что сопоставление КПТ по параметру числа пациентов, выбывших из лечения, с группой находящихся на стандартном лечении может быть некорректным. Последние по определению продолжают свое обычное лечение, и у них может быть меньше причин бросать его, в сравнении с теми, кому был назначен новый метод, который может представляться для них обязывающим или сложным, или от которого они слишком многого ожидают и оказываются разочарованы, не получив результата за несколько сессий. Подтверждением этой гипотезы может служить тот факт, что при неактивном контрольном условии (когда сессии с пациентами ведутся в формате выслушивания или досуговых мероприятий) также наблюдался более высокий процент выбытия пациентов из лечения, нежели при стандартном лечении.
В рассмотренных исследованиях пациенты в среднем имели психическое расстройство умеренной степени выраженности, в отличие от мета-аналитических исследований, посвященных тестированиям антипсихотических препаратов в сравнении с плацебо, где принимали участие пациенты с выраженным расстройством82. Похоже, что пациенты, имеющие тяжелое состояние, обычно не участвуют в психотерапевтических исследованиях. Но это лишь отражает клиническую практику: психотерапия требует от пациента минимальной способности к сотрудничеству, которая отсутствует у многих, кто находится в крайне остром состоянии.
Интерпретация анализа субгрупп и анализ чувствительности были ограничены ввиду небольшого числа доступных исследований. Впрочем, результаты, касающиеся КПТ, сохраняли стабильность после проведения всех запланированных анализов чувствительности, что подтверждает надежность этого метода вмешательства. Мы также проверили потенциальную роль приверженности исследователей18, исключив работы, в которых авторы апробируют эффективность методов, разработанных ими самими, – и не обнаружили существенных различий по сравнению с результатами основного анализа.
Открытым и чрезвычайно актуальным остается вопрос о том, могут ли психологические воздействия причинять вред15. Мы собрали все доступные материалы о неблагоприятных событиях, вероятно связанных с психологическими воздействиями, но обнаружили, что этот аспект очень мало затронут в исследованиях. Мы убеждены, что эту информацию необходимо собирать и освещать в последующих работах, чтобы внести больше ясности в обсуждение этой проблемы83.
Наши результаты согласуются с данными нескольких предшествующих попарных мета-анализов, в которых отмечалась эффективность КПТ в отношении как общих, так и позитивных и негативных симптомов шизофрении по сравнению с контролируемыми условиями4–6, но не с другими видами психотерапии7. Однако результаты прошлых исследований и обзоров эффективности КПТ при шизофрении противоречивы.
В этом смысле решающе важную роль может играть фактор слепых исследований8. Здесь наши результаты контрастируют с выводами Jauhar и соавт.6: исключив исследования с участием не «ослепленных» экспертов, они не обнаружили различий между КПТ и любым другим контролируемым условием. Мы же, напротив, выяснили, что преимущество КПТ перед стандартным лечением и неактивным контролем сохранялось и в слепых исследованиях. Преимуществ не отмечалось перед поддерживающей терапией и листом ожидания, однако лишь небольшое число исследований (два и одно соответственно) предоставили прямые доказательства для этих групп сравнения.
Тем не менее нашу работу нельзя напрямую сравнивать с работой Jauhar и соавт.6, поскольку они фокусировались на любых пациентах с шизофренией, не ограничиваясь лишь имеющими позитивную симптоматику, а также использовали несколько иные критерии оценки риска систематической ошибки и объединяли все группы сравнения вместе в своем попарном мета-анализе.
Наши выводы имеют следующие ограничения. Во-первых, полученные данные для других методов лечения, помимо КПТ, и для КПТ в сравнении с другими узлами, помимо стандартного лечения, базируются лишь на нескольких исследованиях, что дает низкую мощность для обнаружения возможных различий. Следовательно, результаты следует интерпретировать с осторожностью, особенно в части анализа чувствительности и анализа субгрупп. По этой причине мы в своей интерпретации не фокусировались на иерархиях (распределение SUCRA): был риск создать обманчивое впечатление, так как отсутствуют статистически значимые различия между активными методами лечения.
Во-вторых, нас интересовало лечение позитивной симптоматики, а наблюдения, полученные для других исходов, могли быть производными от эффективного лечения позитивных симптомов. К примеру, пациент может страдать от синдрома отмены, недостатка спонтанности, депрессивных симптомов или сниженного качества функционирования из-за проблем, причиняемых бредом и галлюцинациями. Избавление от этого положительно сказывается как на качестве жизни, так и на других симптомах. Поэтому наши интерпретации касались главным образом позитивной симптоматики.
В-третьих, пациенты в охваченных нами исследованиях параллельно получали антипсихотические препараты. Мы собирали всю доступную информацию, касающуюся использования антипсихотиков, однако эти сведения предоставлялись редко, а в отношении экспериментальной и контрольной групп по отдельности – никогда. Единственным исключением является работа Morrison и соавт.52, где пациенты не получали лечения антипсихотиками (post-hoc анализ чувствительности с исключением этой работы существенно не изменил результатов). В результате оценить роль фактора фармакологического лечения оказалось невозможным. Впрочем, по нашему предположению, прием препаратов может иметь сходный эффект во всех группах исследования ввиду рандомизации. Более того, мы убеждены, что ситуация в исследованиях отражает и происходящее в реальной клинической практике, где психологическое воздействие рассматривается как дополнение к фармакотерапии, а пациенты обычно продолжают принимать свои лекарства.
С другой стороны, настоящая работа имеет и серьезные сильные стороны. Во-первых, исследование было тщательно спланировано в соответствии с руководством PRISMA и выполнялось в соответствии с основательной методологией, априори опубликованной в протоколе3. Все это подразумевало обстоятельный подход к критериям оценки исходов и оценке качества на уровне исследования (риска систематической ошибки), а также достоверности результатов на уровне исходов (CINeMA). Во-вторых, рассмотрение стандартного лечения и листа ожидания в качестве отдельных контролируемых условий позволило оценить их относительную эффективность. Это представляется особенно важным, так как в отношении листа ожидания были выявлены предположения о связи с эффектом ноцебо83.
В-третьих, строгие критерии отбора обеспечили гомогенность генеральной совокупности, что подтверждалось крайне низкой неоднородностью, согласованностью между прямыми и косвенными сравнениями, тестом разделения и тестом оценки взаимодействия результатов лечения. Это позволяет утверждать, что результаты данного исследования надежны.
В заключение следует отметить, что когнитивно-поведенческая терапия, по-видимому, эффективна в работе с позитивной симптоматикой у пациентов с умеренно выраженной степенью расстройства при шизофрении, с размерами эффекта в нижнем и среднем диапазоне, в зависимости от контролируемого условия.
DOI:10.1002/wps.20577
Редактура: к.м.н. Чумаков Е.М. (Санкт-Петербург)
Психологическая помощь все чаще рассматривается в числе полезных видов вмешательств при шизофрении. Однако многосторонняя оценка имеющихся тому доказательств отсутствует, а преимущество психологических вмешательств для пациентов, имеющих позитивные симптомы, до сих пор остается предметом дискуссий. Целью данного исследования является оценка эффективности, допустимости и переносимости психологических методов лечения при позитивных симптомах шизофрении при помощи сетевого мета-анализа, способного интегрировать как прямые, так и косвенные сравнения. По базам EMBASE, MEDLINE, PsychINFO, PubMed, BIOSIS, Кокрановская библиотека, Международный реестр клинических исследований Всемирной организации здравоохранения и ClinicalTrials.gov был выполнен поиск рандомизированных контролируемых исследований, посвященных психологическому лечению при позитивных симптомах шизофрении, опубликованных до 10 января 2018 г. Были рассмотрены исследования с участием взрослых пациентов, имеющих диагноз шизофрении или расстройства шизофренического спектра, сопровождаемого позитивными симптомами. Первичным клиническим исходом считалось изменение в позитивных симптомах, измеряемое при помощи валидированных рейтинговых шкал. Мы отобрали 53 рандомизированных контролируемых исследования семи разновидностей психологических вмешательств с участием 4068 пациентов, получавших психологическую помощь в дополнение к лечению антипсихотиками. В среднем на исходном уровне пациенты имели психическое расстройство умеренной степени выраженности. Сетевой мета-анализ продемонстрировал, что когнитивно-поведенческая терапия (КПТ; 40 исследований) больше способствует редукции позитивной симптоматики, чем неактивный контроль [стандартизованная разность средних (standardized mean difference – SMD) = –0,29; 95% доверительный интервал (ДИ) от –0,55 до –0,03], стандартное лечение (SMD=–0,30; 95% ДИ от –0,45 до –0,14) и поддерживающая терапия (SMD=–0,47; 95% ДИ от –0,91 до –0,03). КПТ ассоциирована с более высоким числом случаев выбытия пациентов из лечения по сравнению со стандартным лечением [соотношение рисков (risk ratio) RR=0,74; 95% ДИ 0,58–0,95]. Достоверность оценок колебалась от умеренной до очень низкой. Другие методы лечения способствовали созданию сети с меньшим количеством исследований. Результаты в целом показали согласованность в анализе чувствительности с исключением ряда факторов, в том числе роли приверженности исследователей и использования слепого метода в отношении лиц, оценивавших исходы. КПТ представляется эффективной в отношении работы с позитивными симптомами у пациентов с умеренной формой расстройства при шизофрении, с величиной эффекта в нижнем и среднем диапазоне, в зависимости от контрольного условия.
Ключевые слова: шизофрения, позитивные симптомы, психологические вмешательства, когнитивно-поведенческая терапия, сетевой мета-анализ.
(World Psychiatry 2018;17(3):316-329)
Психологические вмешательства при шизофрении разрабатывались в отношении многих аспектов этого расстройства и, согласно рекомендациям Национального института совершенствования качества охраны здоровья (National Institute for Health and Care Excellence – NICE)1 Великобритании и Группы исследований исходов при шизофрении (Schizophrenia Patient Outcomes Research Team – PORT)2 в США, признаются в качестве полезных.
Применительно к этим видам лечения выполнялся ряд систематических обзоров рандомизированных исследований3. Однако результаты представляются неясными и зачастую противоречивыми. Например, в то время как некоторые обзоры4,5 выявили преимущество когнитивно-поведенческой терапии (КПТ) перед стандартным лечением, другие авторы не смогли подтвердить эти выводы, как только ими были исключены неслепые рандомизированные контролируемые исследования (РКИ)6. Кокрановский обзор говорит об эффективности КПТ в долгосрочной перспективе, но не в краткосрочной или среднесрочной7; при этом другой мета-анализ не нашел у КПТ никаких преимуществ8.
Более того, имеющиеся доказательные данные обладают несколькими недостатками. Прежде всего, во всех существующих обзорах единовременно сравнивались два метода лечения путем попарного мета-анализа. Этот способ обобщает результаты, только когда два метода уже сопоставлялись между собой в предыдущих исследованиях, что оставляет открытым вопрос о всех других возможных сравнениях. Даже в обзоре Turner и соавт.9, включавшем только исследования по сравнению двух «активных психологических вмешательств», попарный мета-анализ применялся для сравнения каждого вида вмешательства со всеми другими в совокупности, снова не предоставляя информации о сравнениях, которые не рассматривались в исследованиях.
Помимо этого, для существующих обзоров характерна неоднородная выборка, состоящая из пациентов с различными наборами симптомов. Ни один обзор не фокусировался отдельно на пациентах, имеющих позитивную симптоматику, которая – по крайней мере, в своей острой фазе – формирует ядро расстройства. Также в обзоре Zimmermann и соавт.5, посвященном оценке воздействия КПТ на позитивные симптомы, выборка не была ограничена только лишь пациентами с этим видом симптомов.
С учетом этих ограничений в существующих доказательных данных до сих пор остается неясным, имеются ли эффективные и приемлемые виды психологических вмешательств, позволяющие лечить позитивные симптомы при шизофрении.
Целью настоящего исследования было превзойти указанные ограничения путем проведения сетевого мета-анализа, который интегрирует как прямые, так и косвенные сравнения видов вмешательств10 и предоставляет данные о различиях между ними даже там, где прямые сравнения невозможны. Подобный мета-анализ требует определенного уровня однородности генеральной совокупности, условий и методов исследования. Таким образом, для получения информации, полезной для клинической практики, необходим тщательный подход к определению целевой генеральной совокупности.
Данный сетевой мета-анализ рассматривает психологические вмешательства, направленные на работу с позитивными симптомами шизофрении у пациентов, имеющих эти симптомы в настоящий момент, чтобы получить результаты, актуальные для этой конкретной генеральной совокупности.
МЕТОДЫ
Дизайн исследования и участники
Детализированная методология настоящего систематического обзора и сетевого мета-анализа приведена в протоколе исследования, зарегистрированном априори на PROSPERO (№ CRD42017067795) и опубликованном3. В описании результатов мы руководствовались заявлением PRISMA для сетевых мета-анализов11,12.
Были отобраны исследования с участием взрослых пациентов с диагнозом шизофрении или расстройства шизофренического спектра (таких как шизофрениформное или шизоаффективное расстройство) с активной позитивной симптоматикой или в фазе обострения, согласно формулировке критерия включения в исследование, без ограничений по условиям лечения, гендерной и этнической принадлежности. Мы обеспечили гомогенность исследований в рамках и за пределами сравнений видов вмешательств, исключив исследования на пациентах с преобладающими негативными симптомами, сопутствующими заболеваниями или психическими расстройствами, а также пациентов с первым психотическим эпизодом или риском психоза. Исследования включались, если как минимум 80% пациентов имели шизофрению или расстройство шизофренического спектра. В случае смешанной генеральной совокупности данные о пациентах с шизофренией извлекались при условии их доступности. Исследования включались независимо от использованных критериев диагностики.
Вмешательства и группы сравнения
Как было априори определено в протоколе3, под вмешательствами понимались любые методы психологического лечения, применяемые в процессе взаимодействия между терапевтом и пациентом в рамках индивидуальной или групповой терапии с основной целью редукции позитивных симптомов.Группы сравнения были классифицированы следующим образом: а) вмешательства (например, когнитивная реабилитация, психообразование) с первичной целью, отличной от работы с позитивными симптомами (например, когнитивные функции, информирование о болезни, соблюдение режима приема препаратов, функционирование), которые изначально анализировались в качестве отдельных узлов, а затем комбинировались в анализе чувствительности;
б) неактивный контроль, определяемый как вмешательства, контролирующие неспецифические аспекты терапии (например, выслушивание, рекреация и поддержка, терапия социальной активности, поддерживающее консультирование) и иногда также именуемые «психологическим плацебо»; в) стандартное лечение (т. е. пациенты, продолжающие получать стандартное психиатрическое лечение);
г) лист ожидания.
Клинические исходы
Первичным исходом считалось изменение в позитивных симптомах при шизофрении, оцениваемое при помощи рейтинговых шкал, таких как позитивная субшкала Шкалы позитивных и негативных синдромов (Positive and Negative Syndrome Scale – PANSS)13, позитивная субшкала Краткой психиатрической рейтинговой шкалы (Brief Psychiatric Rating Scale – BPRS)14 или какая-либо другая опубликованная шкала.В качестве вторичных исходов рассматривались: выбытие из исследования по любой причине, воздействие на общие симптомы шизофрении, влияние на негативные симптомы, ответ на терапию (как определено в исследовании), рецидив (определяемый при помощи рейтинговых шкал или, в случае невозможности, по повторной госпитализации из-за психопатологии), приверженность лечению и осознание, изменения в депрессивной симптоматике, качество жизни и функционирования, неблагоприятные события, которые могут быть связаны с психологическим лечением (по Linden и соавт.15) и смертность (рассматриваемая как смерть по любой причине, смерть по естественным причинам, смерть в результате суицида). Все исходы оценивались в конечной точке исследования, что определялось в каждом отдельном исследовании.
Стратегия поиска и критерии отбора
По базам EMBASE, MEDLINE, PsychINFO, PubMed, BIOSIS, Кокрановская библиотека, Международный реестр клинических исследований Всемирной организации здравоохранения и ClinicalTrials.gov нами был выполнен поиск РКИ, опубликованных до 10 января 2018 г. и посвященных сравнению психологических методов воздействия между собой или с нефармакологическими контрольными условиями у пациентов с шизофренией, имеющих активную позитивную симптоматику. Дополнительно мы искали библиографические списки предыдущих обзоров.Ограничений по языку не вводилось, с тем лишь исключением, что не осуществлялся поиск по базам данных Китая. Мы обращались к авторам исследований, опубликованных в последние 30 лет, за недостающей или дополнительной информацией об их работах.




Извлечение данных и оценка риска систематической ошибки
Все тезисы исследований, идентифицированные поиском, изучались двумя исследователями из группы независимо друг от друга. Разногласия разрешались путем обсуждения, а в случае сомнений анализу подвергался текст работы целиком. Для всех подошедших работ оформлялись полные отчеты, которые затем вновь рассматривались двумя независимыми рецензентами. Разногласия обсуждались с ведущим автором исследования, а при необходимости за дополнительной информацией обращались к авторам работы.Два исследователя независимо друг от друга извлекали данные из отобранных исследований, принимая во внимание как основные тексты, так и дополнительные материалы, вносили необходимые сведения в базу Microsoft Access, созданную специально для настоящего исследования, и измеряли риск систематической ошибки инструментом оценки риска систематической ошибки Кокрановского сотрудничества16. Рассматривались следующие области возможного смещения: генерация случайной последовательности, сокрытие распределения участников в группы, использование слепого метода в отношении участников и лиц, оценивавших исходы, неполные исходные данные, выборочная отчетность, предвзятость исследователей17,18, другие систематические ошибки. Мы также сформировали общий рейтинг риска систематической ошибки для каждого исследования, основываясь на критериях, примененных в сетевом мета-анализе для антидепрессантов19.
Статистический анализ
Мы выполнили попарный мета-анализ с использованием модели случайных эффектов и сетевой мета-анализ в частотном подходе с помощью пакета netmeta в R (версия 3.4.3)20,21. Была подсчитана стандартизованная разность средних (standardized mean difference – SMD) для непрерывных исходов и соотношение рисков (risk ratio – RR) для бинарных исходов, оба с 95% доверительным интервалом (ДИ). Также для каждого вида вмешательства было рассчитано относительное распределение путем определения поверхности под кумулятивной кривой распределения (Surface Under the Cumulative Ranking Curve – SUCRA) в частотном подходе (как P-значения)22.Перед выполнением сетевого мета-анализа мы попытались оценить предположение о транзитивности. Оно подразумевает, что исследования, сравнивающие различные наборы методов вмешательств, достаточно схожи для того, чтобы обеспечить корректные косвенные выводы, что мы и пытались обеспечить, установив узкие критерии включения и добиваясь как можно большей однородности генеральной совокупности как в рамках сравнения видов лечения, так и за его пределами. Также мы рассмотрели вопрос о том, распределяются ли похожим образом и модификаторы потенциального эффекта во всех доступных прямых сравнениях.
Мы взяли общий параметр неоднородности для различных сравнений видов лечения и вычислили дисперсию между исследованиями (tau2) для каждого исхода. Уровень неоднородности был охарактеризован как низкий, умеренный или высокий на основе первого и третьего квантилей их эмпирических распределений23. Статистическая несогласованность была оценена путем отделения прямых доказательств от косвенных, предоставленных всей сетью, и дальнейшей проверки на соответствие этих двух видов доказательств24. Величина коэффициентов несогласованности (различия между прямыми и косвенными SMD) и соответствующие им значения p использовались для определения наличия несогласованности. Мы также применили модель для оценки взаимодействия результатов лечения, которая позволяет оценить непостоянство в сети в совокупности25.
Для исследования возможных источников неоднородности и непостоянства мы спланировали априорный анализ субгрупп для первичного исхода по следующим модификаторам потенциального эффекта: количество сессий, продолжительность исследования, сеттинг (индивидуальная или групповая терапия), компетентность терапевта, изначальная тяжесть состояния. Был выполнен анализ чувствительности с исключением открытых исследований, исследований только лишь с анализом полученного и завершенного лечения, исследований с общим высоким риском систематической ошибки19, исследований с высоким риском предвзятости исследователей, исследований, сфокусированных на резистентных к лечению пациентах и исследований с неактивной группой сравнения. Нами также были оценены эффекты небольших исследований (потенциально ассоциированных с риском предвзятости при публикации) путем анализа воронкообразных участков в попарном мета-анализе и скорректированных по размерам воронкообразных участков, если исследований было 10 и больше26.
В дополнение к этому мы измерили достоверность оценок первичного исхода с помощью инструмента оценки достоверности CINeMA (Confidence in Network Meta-Analysis), адаптации системы градации измерения, разработки и оценки качества рекомендаций (Grading of Recommendations Assessment, Development and Evaluation framework – GRADE), разработанной специально для сетевого мета-анализа27.
РЕЗУЛЬТАТЫ
Характеристики включенных исследованийВ результате поиска было найдено 21 772 ссылки (дата последнего обращения – 10 января 2018 г.), 2754 статьи были получены в полном тексте (рис. 1). Мы отобрали 62 рандомизированных контролируемых исследования, 53 из которых содержали пригодные данные и вошли в сетевой мета-анализ (с участием 4068 пациентов; см. таблицу).
В этих исследованиях сравнивались следующие методы психологического лечения: КПТ (n=40)28–67, метакогнитивный тренинг (n=6)68–73, терапия осознанности (mindfulness) (n=2)74,75, терапия принятия и ответственности (n=2)76,77, консультирование, фокусированное на переживании (n=1)78, интегративное лечение, фокусированное на галлюцинациях (n=1)79, и АВАТАР-терапия (n=1)80.
Средний объем выборки составил 76,5 пациента (размах колебаний 6–218), а средняя продолжительность исследования – 13 недель (размах колебаний 4–44 недели). Из 3941 пациента с известными данными о поле 2361 были мужчинами (59,9%). Средняя продолжительность расстройства составляла 12,4 года, средний возраст пациентов – 37,4 года. В 9 исследованиях рассматривались только пациенты стационара, в 15 – только амбулаторные пациенты, в 14 – оба типа пациентов, а в 15 исследованиях информация о форме лечения пациентов не предоставлялась. В среднем пациенты имели симптомы шизофрении умеренной степени выраженности со средним баллом 68,26 по шкале PANSS81,82. Благодаря готовности авторов к сотрудничеству нам удалось включить и неопубликованные данные для нескольких исследований36,37,41–43,57,61,68,72.

Оценка риска систематической ошибки
Соответственно 6, 27 и 21 исследование были классифицированы как имеющие низкий, умеренный и высокий общий риск систематической ошибки (см. таблицу). Низкий риск показали: 26 (50%) исследований – относительно генерации случайной последовательности; 13 (25%) – относительно сокрытия распределения участников по группам; ни одно исследование – относительно использования слепого метода в отношении участников и персонала; 18 (34,6%) исследований – относительно использования слепого метода при оценках исходов; 7 (13,5%) – относительно систематической ошибки, связанной с выбыванием участников; 11 (21,1%) – относительно выборочной отчетности; 6 (11,5%) – относительно предвзятости исследователей и 41 исследование (78,8%) – относительно других возможных ошибок.Первичный исход: позитивная симптоматика
На рис. 2 изображена сеть методов воздействия для первичных исходов. Два исследования не вошли в анализ, поскольку не обнаружили связей с остальной сетью, не предоставив ни прямых, ни косвенных доказательств29,68.
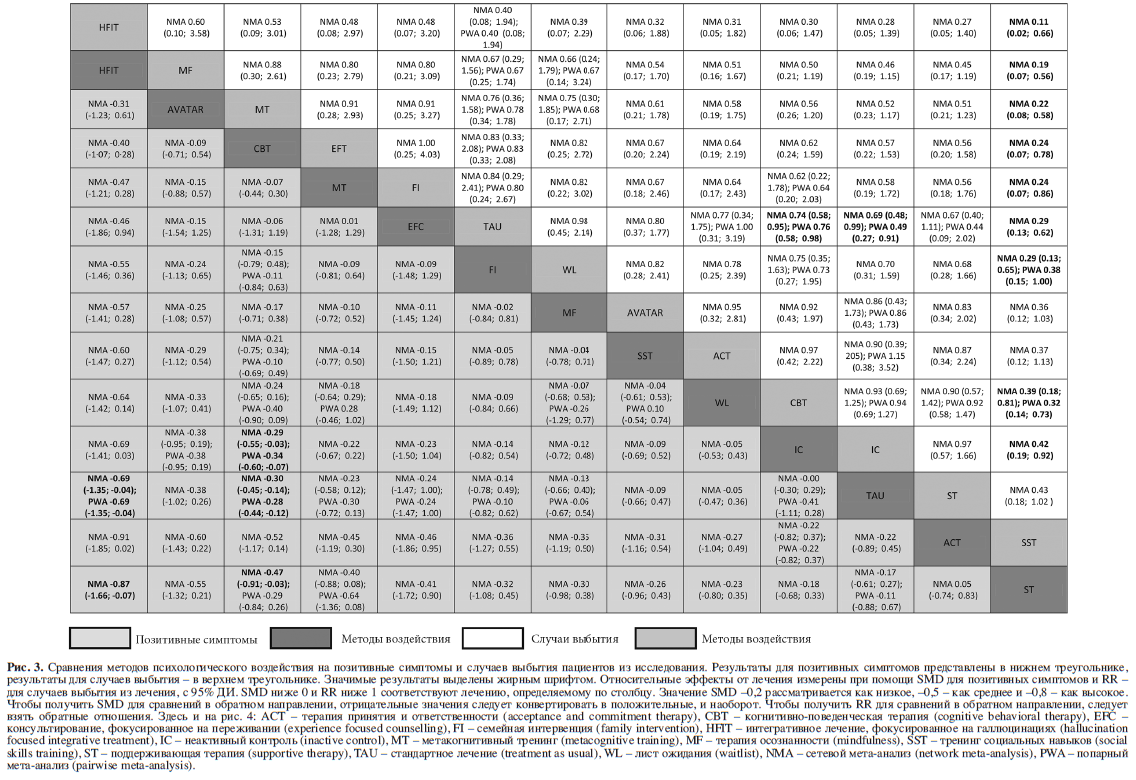
Результаты сетевого мета-анализа для первичного исхода показали ассоциированность КПТ с более высоким уровнем редукции позитивной симптоматики по сравнению с неактивным контролем (SMD=−0,29; 95% ДИ от –0,55 до −0,03, семь РКИ предоставили прямые доказательства в сетевой мета-анализ с низкой достоверностью оценок), стандартным лечением (SMD=−0,30; 95% ДИ от –0,45 до −0,14; 18 РКИ предоставили прямые доказательства со средней достоверностью оценок) и поддерживающей терапией (SMD=−0,47; 95% ДИ от –0,91 до −0,03; два РКИ предоставили прямые доказательства с низкой достоверностью оценок). В сопоставлении с листом ожидания разница была незначимой (SMD=−0,24; 95% ДИ: от –0,65 до 0,16), однако прямые доказательства в это сравнение предоставили лишь два небольших исследования с 30 и 45 участниками, соответственно43,44 (рис. 3).
Одно из исследований, посвященное интегративной терапии, фокусированной на галлюцинациях, продемонстрировало снижение выраженности симптоматики по сравнению со стандартным лечением и поддерживающей терапией (умеренная и низкая достоверность оценок, соответственно). Относительные эффекты от всех прочих методов лечения были очень неопределенными, но в среднем отражали преимущество активного психологического лечения перед методами неактивного контроля.
Неоднородность дисперсии (tau2) составила 0,0514, что расценивается как значение в диапазоне от низкого до умеренного23. Тест оценки взаимодействия результатов лечения не выявил значительной несогласованности (p=0,35). Разделив прямые и косвенные доказательства для каждого сравнения, мы не нашли подтверждений несоответствия между двумя видами доказательств для любого из сравнений. Ни один из использованных нами методов не предоставил серьезной несогласованности, но, с учетом небольшого количества исследований для большинства из сравнений, мощность этих тестов невысока. Измерение достоверности оценок с помощью CINeMA показало уровень достоверности от умеренного к очень низкому, в основном из-за ограничений исследования (высокий риск систематической ошибки) и неточностей.
Интерпретация анализа субгрупп ограничена ввиду недостаточного количества исследований для разных субгрупп. Мы не обнаружили какого-либо явного указания на то, что преимущество КПТ перед стандартным лечением определяется количеством сессий, продолжительностью исследования, сеттингом (индивидуальной или групповой терапией), компетентностью терапевта или изначальной тяжестью состояния.


Аналогичным образом, после исключения различных исследований в анализе чувствительности осталось небольшое количество исследований для большинства методов лечения. После исключения открытых исследований результаты сравнения КПТ со стандартным лечением и поддерживающей терапией сохранили согласованность с основным анализом (SMD=−0,27; 95% ДИ от –0,41 до −0,13 и SMD=−0,47; 95% ДИ от –0,86 до −0,08, соответственно), в то время как различия между КПТ и неактивным контролем утратили значимость (SMD=−0,14; 95% ДИ от –0,37 до 0,09).
Анализ чувствительности с исключением только исследований с анализом полученного и завершенного лечения, исследований с высоким риском систематической ошибки, исследований с высоким риском систематической ошибки ввиду предвзятости исследователей, а также исследований, сфокусированных на пациентах, резистентных к лечению, в целом соответствовал результатам основного анализа.
Результаты post-hoc анализа чувствительности с объединением групп сравнения «активного контроля» не отличались от основных.
Изучение эффекта небольших исследований и риска предвзятости при публикации с использованием обычного графика воронки не выявило никакой связи между точностью исследования и величиной эффекта (применимо только к сопоставлению КПТ со стандартным лечением). Однако график воронки, скорректированный по размеру, позволяет предположить, что небольшие исследования, которые не продемонстрировали никаких преимуществ новых методов психологического лечения перед старыми, недопредставлены в наших материалах (возможно, они остаются неопубликованными).
Вторичные исходы
КПТ и неактивный контроль оказались менее предпочтительны по сравнению со стандартным лечением с позиции частоты случаев выбытия из исследования (по всем причинам). Для всех методов лечения количество выбывших пациентов было меньше, чем для тренинга социальных навыков (за исключением АВАТАР-терапии, терапии принятия и ответственности и поддерживающей терапии; рис. 3).Также КПТ была связана с более высоким уровнем редукции общих симптомов по сравнению с листом ожидания и стандартным лечением и с более высоким уровнем редукции негативной симптоматики по сравнению со стандартным лечением (рис. 4). Интегративное лечение, фокусированное на галлюцинациях, и КПТ ассоциированы с большей вероятностью ответа на лечение в сравнении со стандартным лечением и неактивным контролем.
С точки зрения приверженности лечению и осознания, метакогнитивный тренинг, тренинг социальных навыков, КПТ и стандартное лечение приводили к большим улучшениям по сравнению с поддерживающей терапией. КПТ была более эффективна, чем стандартное лечение, в отношении качества жизни и функционирования. Никаких значимых различий в отношении депрессии не наблюдалось. Смертность в целом была достаточно редка и не различалась в зависимости от методов лечения. Данных о рецидивах, неблагоприятных событиях и смертельных исходах было предоставлено очень мало.
Неоднородность дисперсии (tau2) колебалась от 0 до 0,0649, т. е. от полного отсутствия до низкого и умеренного уровня. Модель оценки взаимодействия результатов лечения продемонстрировала некоторую несогласованность вторичных исходов применительно к депрессии (p=0,03).
ОБСУЖДЕНИЕ
Насколько нам известно, это первый сетевой мета-анализ психологических воздействий в отношении пациентов с позитивными симптомами при шизофрении.В 40 исследованиях наиболее часто встречающимся методом среди других стала КПТ. Мы обнаружили существенно более высокую эффективность КПТ по сравнению со стандартным лечением в отношении многих исходов (позитивные, общие и негативные симптомы, отклик на лечение, качество жизни и функционирования), большую эффективность по сравнению с неактивным контролем в отношении позитивных симптомов и отклика на лечение и по сравнению с поддерживающей терапией – в отношении приверженности лечению. Убедительных доказательств эффективности других методов получено не было, возможно, ввиду малого количества исследований.
КПТ также была ассоциирована с большим процентом выбытия пациентов из лечения по сравнению со стандартным лечением (18,8 против 12%). КПТ не всегда может быть подходящим методом, и не все пациенты могут захотеть участвовать в столь трудоемком лечении; впрочем, мы убеждены, что сопоставление КПТ по параметру числа пациентов, выбывших из лечения, с группой находящихся на стандартном лечении может быть некорректным. Последние по определению продолжают свое обычное лечение, и у них может быть меньше причин бросать его, в сравнении с теми, кому был назначен новый метод, который может представляться для них обязывающим или сложным, или от которого они слишком многого ожидают и оказываются разочарованы, не получив результата за несколько сессий. Подтверждением этой гипотезы может служить тот факт, что при неактивном контрольном условии (когда сессии с пациентами ведутся в формате выслушивания или досуговых мероприятий) также наблюдался более высокий процент выбытия пациентов из лечения, нежели при стандартном лечении.
В рассмотренных исследованиях пациенты в среднем имели психическое расстройство умеренной степени выраженности, в отличие от мета-аналитических исследований, посвященных тестированиям антипсихотических препаратов в сравнении с плацебо, где принимали участие пациенты с выраженным расстройством82. Похоже, что пациенты, имеющие тяжелое состояние, обычно не участвуют в психотерапевтических исследованиях. Но это лишь отражает клиническую практику: психотерапия требует от пациента минимальной способности к сотрудничеству, которая отсутствует у многих, кто находится в крайне остром состоянии.
Интерпретация анализа субгрупп и анализ чувствительности были ограничены ввиду небольшого числа доступных исследований. Впрочем, результаты, касающиеся КПТ, сохраняли стабильность после проведения всех запланированных анализов чувствительности, что подтверждает надежность этого метода вмешательства. Мы также проверили потенциальную роль приверженности исследователей18, исключив работы, в которых авторы апробируют эффективность методов, разработанных ими самими, – и не обнаружили существенных различий по сравнению с результатами основного анализа.
Открытым и чрезвычайно актуальным остается вопрос о том, могут ли психологические воздействия причинять вред15. Мы собрали все доступные материалы о неблагоприятных событиях, вероятно связанных с психологическими воздействиями, но обнаружили, что этот аспект очень мало затронут в исследованиях. Мы убеждены, что эту информацию необходимо собирать и освещать в последующих работах, чтобы внести больше ясности в обсуждение этой проблемы83.
Наши результаты согласуются с данными нескольких предшествующих попарных мета-анализов, в которых отмечалась эффективность КПТ в отношении как общих, так и позитивных и негативных симптомов шизофрении по сравнению с контролируемыми условиями4–6, но не с другими видами психотерапии7. Однако результаты прошлых исследований и обзоров эффективности КПТ при шизофрении противоречивы.
В этом смысле решающе важную роль может играть фактор слепых исследований8. Здесь наши результаты контрастируют с выводами Jauhar и соавт.6: исключив исследования с участием не «ослепленных» экспертов, они не обнаружили различий между КПТ и любым другим контролируемым условием. Мы же, напротив, выяснили, что преимущество КПТ перед стандартным лечением и неактивным контролем сохранялось и в слепых исследованиях. Преимуществ не отмечалось перед поддерживающей терапией и листом ожидания, однако лишь небольшое число исследований (два и одно соответственно) предоставили прямые доказательства для этих групп сравнения.
Тем не менее нашу работу нельзя напрямую сравнивать с работой Jauhar и соавт.6, поскольку они фокусировались на любых пациентах с шизофренией, не ограничиваясь лишь имеющими позитивную симптоматику, а также использовали несколько иные критерии оценки риска систематической ошибки и объединяли все группы сравнения вместе в своем попарном мета-анализе.
Наши выводы имеют следующие ограничения. Во-первых, полученные данные для других методов лечения, помимо КПТ, и для КПТ в сравнении с другими узлами, помимо стандартного лечения, базируются лишь на нескольких исследованиях, что дает низкую мощность для обнаружения возможных различий. Следовательно, результаты следует интерпретировать с осторожностью, особенно в части анализа чувствительности и анализа субгрупп. По этой причине мы в своей интерпретации не фокусировались на иерархиях (распределение SUCRA): был риск создать обманчивое впечатление, так как отсутствуют статистически значимые различия между активными методами лечения.
Во-вторых, нас интересовало лечение позитивной симптоматики, а наблюдения, полученные для других исходов, могли быть производными от эффективного лечения позитивных симптомов. К примеру, пациент может страдать от синдрома отмены, недостатка спонтанности, депрессивных симптомов или сниженного качества функционирования из-за проблем, причиняемых бредом и галлюцинациями. Избавление от этого положительно сказывается как на качестве жизни, так и на других симптомах. Поэтому наши интерпретации касались главным образом позитивной симптоматики.
В-третьих, пациенты в охваченных нами исследованиях параллельно получали антипсихотические препараты. Мы собирали всю доступную информацию, касающуюся использования антипсихотиков, однако эти сведения предоставлялись редко, а в отношении экспериментальной и контрольной групп по отдельности – никогда. Единственным исключением является работа Morrison и соавт.52, где пациенты не получали лечения антипсихотиками (post-hoc анализ чувствительности с исключением этой работы существенно не изменил результатов). В результате оценить роль фактора фармакологического лечения оказалось невозможным. Впрочем, по нашему предположению, прием препаратов может иметь сходный эффект во всех группах исследования ввиду рандомизации. Более того, мы убеждены, что ситуация в исследованиях отражает и происходящее в реальной клинической практике, где психологическое воздействие рассматривается как дополнение к фармакотерапии, а пациенты обычно продолжают принимать свои лекарства.
С другой стороны, настоящая работа имеет и серьезные сильные стороны. Во-первых, исследование было тщательно спланировано в соответствии с руководством PRISMA и выполнялось в соответствии с основательной методологией, априори опубликованной в протоколе3. Все это подразумевало обстоятельный подход к критериям оценки исходов и оценке качества на уровне исследования (риска систематической ошибки), а также достоверности результатов на уровне исходов (CINeMA). Во-вторых, рассмотрение стандартного лечения и листа ожидания в качестве отдельных контролируемых условий позволило оценить их относительную эффективность. Это представляется особенно важным, так как в отношении листа ожидания были выявлены предположения о связи с эффектом ноцебо83.
В-третьих, строгие критерии отбора обеспечили гомогенность генеральной совокупности, что подтверждалось крайне низкой неоднородностью, согласованностью между прямыми и косвенными сравнениями, тестом разделения и тестом оценки взаимодействия результатов лечения. Это позволяет утверждать, что результаты данного исследования надежны.
В заключение следует отметить, что когнитивно-поведенческая терапия, по-видимому, эффективна в работе с позитивной симптоматикой у пациентов с умеренно выраженной степенью расстройства при шизофрении, с размерами эффекта в нижнем и среднем диапазоне, в зависимости от контролируемого условия.
БЛАГОДАРНОСТИ
Данное исследование было профинансировано Программой научных исследований и инноваций Европейского Союза «Горизонт 2020», грант Марии Склодовской-Кюри № 701717. Спонсор не имел никакого отношения к разработке дизайна исследования, сбору данных, анализу или интерпретации, написанию отчета или решению предоставить работу к публикации. Авторы благодарят S. Roberts за помощь в поиске литературы, P. Kratochwill за содействие в подготовке полного текста и его вычитке, Y. Zhu за помощь в подборе и получении данных китайских исследований и C. Carmi за помощь в извлечении данных. Они благодарят авторов всех рассмотренных исследований, в особенности тех, кто предоставил дополнительную информацию и данные. На веб-сайте http://www.psykl.mri.tum.de/node/69 можно найти расширенную информацию о стратегии поиска, отобранных методах воздействия, оценке риска систематической ошибки, результатах для вторичных исходов, распределениях SUCRA, оценке неоднородности и непостоянства, анализе субгрупп и анализе чувствительности, определении достоверности оценок. Эти сведения также можно получить у авторов по запросу.DOI:10.1002/wps.20577
Список исп. литературыСкрыть список1. National Collaborating Centre for Mental Health. Core interventions in the treatment and management of schizophrenia in adults in primary and secondary care (Clinical Guideline CG82). London: National Collaborating Centre for Mental Health, 2009.
2. Buchanan RW, Kreyenbuhl J, Kelly DL et al. The 2009 schizophrenia PORT psychopharmacological treatment recommendations and summary statements. Schizophr Bull 2010;36:71-93.
3. Bighelli I, Salanti G, Reitmeir C et al. Psychological interventions for positive symptoms in schizophrenia: protocol for a network meta-analysis of randomised controlled trials. BMJ Open 2018;8:e019280.
4. Wykes T, Steel C, Everitt B et al. Cognitive behavior therapy for schizophrenia: effect sizes, clinical models, and methodological rigor. Schizophr Bull 2008;34:523-37.
5. Zimmermann G, Favrod J, Trieu VH et al. The effect of cognitive behavioral treatment on the positive symptoms of schizophrenia spectrum disorders: a meta-analysis. Schizophr Res 2005;77:1-9.
6. Jauhar S, McKenna PJ, Radua J et al. Cognitive-behavioural therapy for the symptoms of schizophrenia: systematic review and meta-analysis with examination of potential bias. Br J Psychiatry 2014;204:20-9.
7. Jones C, Hacker D, Cormac I et al. Cognitive behaviour therapy versus other psychosocial treatments for schizophrenia. Cochrane Database Syst Rev 2012;4:CD008712.
8. Lynch D, Laws KR, McKenna PJ. Cognitive behavioural therapy for major psychiatric disorder: does it really work? A meta-analytical review of well-controlled trials. Psychol Med 2010;40:9-24.
9. Turner DT, van der Gaag M, Karyotaki E et al. Psychological interventions for psychosis: a meta-analysis of comparative outcome studies. Am J Psychiatry 2014;171:523-38.
10. Salanti G. Indirect and mixed-treatment comparison, network, or multiple-treatments meta-analysis: many names, many benefits, many concerns for the next generation evidence synthesis tool. Res Synth Methods 2012;3:80-97.
11. Hutton B, Salanti G, Caldwell DM et al. The PRISMA extension statement for reporting of systematic reviews incorporating network meta-analyses of health care interventions: checklist and explanations. Ann Intern Med 2015;162:777-84.
12. Shamseer L, Moher D, Clarke M et al. Preferred reporting items for systematic review and meta-analysis protocols (PRISMA-P) 2015: elaboration and explanation. BMJ 2015;349:g7647.
13. Kay SR, Fiszbein A, Opler LA. The positive and negative syndrome scale (PANSS) for schizophrenia. Schizophr Bull 1987;13:261-76.
14. Overall JE, Gorham DR. The brief psychiatric rating scale. Psychol Rep 1962;10:799-812.
15. Linden M, Schermuly-Haupt M-L. Definition, assessment and rate of psychotherapy side effects. World Psychiatry 2014;13:306-9.
16. Higgins JPT, Churchill R, Chandler J et al (eds). Cochrane handbook for systematic reviews of interventions, Version 5.2.0, Cochrane, 2017.
17. Munder T, Brütsch O, Leonhart R et al. Researcher allegiance in psychotherapy outcome research: an overview of reviews. Clin Psychol Rev 2013;33:501-11.
18. Lieb K. von der Osten-Sacken J, Stoffers-Winterling J et al. Conflicts of interest and spin in reviews of psychological therapies: a systematic review. BMJ Open 2016;6:e010606.
19. Furukawa TA, Salanti G, Atkinson LZ et al. Comparative efficacy and acceptability of first-generation and second-generation antidepressants in the acute treatment of major depression: protocol for a network meta-analysis. BMJ Open 2016;6:e010919.
20. Schwarzer G. meta: an R package for meta-analysis. R News 2007;7:40-5.
21. Schwarzer G, Carpenter JR, Rücker G. Meta-analysis with R (Use-R!). Basel: Springer, 2015.
22. Rücker G, Schwarzer G. Ranking treatments in frequentist network meta-analysis works without resampling methods. BMC Med Res Methodol 2015;15:58.
23. Rhodes KM, Turner RM, Higgins JPT. Predictive distributions were developed for the extent of heterogeneity in meta-analyses of continuous outcome data. J Clin Epidemiol 2015;68:52-60.
24. Dias S, Welton NJ, Caldwell DM et al. Checking consistency in mixed treatment comparison meta-analysis. Stat Med 2010;29:932-44.
25. Higgins JPT, Jackson D, Barrett JK et al. Consistency and inconsistency in network meta-analysis: concepts and models for multi-arm studies. Res Synth Methods 2012;3:98-110.
26. Chaimani A, Salanti G. Using network meta-analysis to evaluate the existence of small-study effects in a network of interventions. Res Synth Methods 2012;3:161-76.
27. Salanti G, Del Giovane C, Chaimani A et al. Evaluating the quality of evidence from a network meta-analysis. PLoS One 2014;9:e99682.
28. Barrowclough C, Haddock G, Lobban F et al. Group cognitive-behavioural therapy for schizophrenia. Randomised controlled trial. Br J Psychiatry 2006;189:527-32.
29. Bechdolf A, Knost B, Kuntermann C et al. A randomized comparison of group cognitive-behavioural therapy and group psychoeducation in patients with schizophrenia. Acta Psychiatr Scand 2004;110:21-8.
30. Birchwood M, Michail M, Meaden A et al. Cognitive behaviour therapy to prevent harmful compliance with command hallucinations
(COMMAND): a randomized controlled trial. Lancet Psychiatry 2014;1:23-33.
31. Drury V, Birchwood M, Cochrane R et al. Cognitive therapy and recovery from acute psychosis: a controlled trial. I. Impact on psychotic symptoms. Br J Psychiatry 1996;169:593-601.
32. Durham RC, Guthrie M, Morton RV et al. Tayside-Fife clinical trial of cognitive-behavioural therapy for medication-resistant psychotic symptoms. Results to 3-month follow-up. Br J Psychiatry 2003;182:303-11.
33. England M. Efficacy of cognitive nursing intervention for voice hearing. Perspect Psychiatr Care 2007;43:69-76.
34. Foster C, Startup H, Potts L et al. A randomised controlled trial of a worry intervention for individuals with persistent persecutory delusions. J Behav Ther Exper Psychiatry 2010;41:45-51.
35. Freeman D, Pugh K, Dunn G et al. An early Phase II randomised controlled trial testing the effect on persecutory delusions of using CBT to reduce negative cognitions about the self: the potential benefits of enhancing self confidence. Schizophr Res 2014;160:186-92.
36. Freeman D, Dunn G, Startup H et al. Effects of cognitive behaviour therapy for worry on persecutory delusions in patients with psychosis (WIT): a parallel, single-blind, randomised controlled trial with a mediation analysis. Lancet Psychiatry 2015;2:305-13.
37. Freeman D, Waite F, Startup H et al. Efficacy of cognitive behavioural therapy for sleep improvement in patients with persistent delusions and hallucinations (BEST): a prospective, assessor-blind, randomised controlled pilot trial. Lancet Psychiatry 2015;2:975-83.
38. Garety PA, Fowler DG, Freeman D et al. Cognitive-behavioural therapy and family intervention for relapse prevention and symptom reduction in psychosis: randomised controlled trial. Br J Psychiatry 2008;192:412-23.
39. Gottlieb JD, Gidugu V, Maru M et al. Randomized controlled trial of an internet cognitive behavioral skills-based program for auditory hallucinations in persons with psychosis. Psychiatr Rehabil J 2017;40:283-92.
40. Habib N, Dawood S, Kingdon D et al. Preliminary evaluation of culturally adapted CBT for psychosis (CA-CBTp): findings from developing culturally-sensitive CBT project (DCCP). Behav Cogn Psychother 2015;43:200-8.
41. Haddock G, Tarrier N, Morrison AP et al. A pilot study evaluating the effectiveness of individual inpatient cognitive-behavioural therapy in early psychosis. Soc Psychiatry Psychiatr Epidemiol 1999;34:254-8.
42. Haddock G, Barrowclough C, Shaw JJ et al. Cognitive-behavioural therapy v. social activity therapy for people with psychosis and a history of violence: randomised controlled trial. Br J Psychiatry 2009;194:152-7.
43. Hazell CM, Hayward M, Cavanagh K et al. Guided self-help cognitive behavioral intervention for VoicEs (GiVE): study protocol for a pilot randomized controlled trial. Trials 2016;17:351.
44. Krakvik B, Grawe RW, Hagen R et al. Cognitive behaviour therapy for psychotic symptoms: a randomized controlled effectiveness trial. Behav Cogn Psychother 2013;41:511-24.
45. Kuipers E, Garety P, Fowler D et al. London-East Anglia randomised controlled trial of cognitive-behavioural therapy for psychosis. I: Effects of the treatment phase. Br J Psychiatry 1997;171:319-27.
46. Lecomte T, Leclerc C, Corbiere M et al. Group cognitive behavior therapy or social skills training for individuals with a recent onset of psychosis? Results of a randomized controlled trial. J Nerv Ment Dis 2008;196:866-75.
47. Lee DH, Ko SM, Choi YS et al. A randomized controlled pilot study of cognitive behavioral social skills training (Korean version) for middle- or older-aged patients with schizophrenia: a pilot study. J Korean Neuropsychiatr Assoc 2012;51:192-201.
48. Lee DE, Lee HJ, Yoon OS et al. The effect of cognitive behavioral therapy in drug-resistant patients with schizophrenia. J Korean Neuropsychiatr Assoc 2013;52:26-32.
49. Levine J, Barak Y, Granek I. Cognitive group therapy for paranoid schizophrenics: applying cognitive dissonance. J Cogn Psychother 1998;12:3-12.
50. Li ZJ, Guo ZH, Wang N et al. Cognitive-behavioural therapy for patients with schizophrenia: a multicentre randomized controlled trial in Beijing, China. Psychol Med 2015;45:1893-905.
51. McLeod T, Morris M, Birchwood M et al. Cognitive behavioural therapy group work with voice hearers. Part 1. Br J Nurs 2007;16:248-52.
52. Morrison AP, Turkington D, Pyle M et al. Cognitive therapy for people with schizophrenia spectrum disorders not taking antipsychotic drugs: a single-blind randomised controlled trial. Lancet 2014;383:1395-403.
53. Penn DL, Meyer PS, Evans E et al. A randomized controlled trial of group cognitive-behavioral therapy vs. enhanced supportive therapy for auditory hallucinations. Schizophr Res 2009;109:52-9.
54. Pinninti NR, Rissmiller DJ, Steer RA. Cognitive-behavioral therapy as an adjunct to second-generation antipsychotics in the treatment of schizophrenia. Psychiatr Serv 2010;61:940-3.
55. Pot-Kolder RMCA, Geraets CNW, Veling W et al. Virtual-reality- based cognitive behavioural therapy versus waiting list control for paranoid ideation and social avoidance in patients with psychotic disorders: a single-blind randomised controlled trial. Lancet Psychiatry 2018;5:217-26.
56. Rector NA, Seeman MV, Segal ZV. Cognitive therapy for schizophrenia: a preliminary randomized controlled trial. Schizophr Res 2003;63:1-11.
57. Sensky T, Turkington D, Kingdon D et al. A randomized controlled trial of cognitive-behavioral therapy for persistent symptoms in schizophrenia resistant to medication. Arch Gen Psychiatry 2000;57:165-72.
58. Startup M, Jackson MC, Bendix S. North Wales randomized controlled trial of cognitive behaviour therapy for acute schizophrenia spectrum disorders: outcomes at 6 and 12 months. Psychol Med 2004;34:413-22.
59. Tarrier N, Yusupoff L, Kinney C et al. Randomised controlled trial of intensive cognitive behaviour therapy for patients with chronic schizophrenia. BMJ 1998;317:303-7.
60. Trower P, Birchwood M, Meaden A et al. Cognitive therapy for command hallucinations: randomised controlled trial. Br J Psychiatry 2004;184:312-20.
61. Turkington D, Kingdon D. Cognitive-behavioural techniques for general psychiatrists in the management of patients with psychoses. Br J Psychiatry 2000;177:101-6.
62. Valmaggia LR, van der Gaag M, Tarrier N et al. Cognitive-behavioural therapy for refractory psychotic symptoms of schizophrenia resistant to atypical antipsychotic medication. Randomised controlled trial. Br J Psychiatry 2005;186:324-30.
63. van der Gaag M, Stant AD, Wolters KJ et al. Cognitive-behavioural therapy for persistent and recurrent psychosis in people with schizophrenia-spectrum disorder: cost-effectiveness analysis. Br J Psychiatry 2011;198:59-65.
64. Velligan DI, Tai S, Roberts DL et al. A randomized controlled trial comparing cognitive behavior therapy, cognitive adaptation training, their combination and treatment as usual in chronic schizophrenia. Schizophr Bull 2015;41:597-603.
65. Wahass S, Kent G. The modification of psychological interventions for persistent auditory hallucinations to an Islamic culture. Behav Cogn Psychother 1997;25:351.
66. Wittorf A, Jakobi UE, Bannert KK et al. Does the cognitive dispute of psychotic symptoms do harm to the therapeutic alliance? J Nerv Ment Dis 2010;198:478-85.
67. Wykes T, Hayward P, Thomas N et al. What are the effects of group cognitive behaviour therapy for voices? A randomised control trial. Schizophr Res 2005;77:201-10.
68. ACTRN12616000976482. Efficacy of individualised metacognitive therapy (MCT+) for delusions in psychosis. Australian New Zealand Clinical Trial Registry, 2016.
69. Briki M, Monnin J, Haffen E et al. Metacognitive training for schizophrenia: a multicentre randomised controlled trial. Schizophr Res 2014;157:99-106.
70. Favrod J, Rexhaj S, Bardy S et al. Sustained antipsychotic effect of metacognitive training in psychosis: a randomized-controlled study. Eur Psychiatry 2014;29:275-81.
71. Kumar D, Zia Ul Haq M, Dubey I et al. Effect of meta-cognitive training in the reduction of positive symptoms in schizophrenia. Eur J Psychother Couns 2010;12:149-58.
72. So SH, Chan AP, Chong CS et al. Metacognitive training for delusions (MCTd): effectiveness on data-gathering and belief flexibility in a Chinese sample. Front Psychol 2015;6:730.
73. van Oosterhout B, Krabbendam L, de Boer K et al. Metacognitive group training for schizophrenia spectrum patients with delusions: a randomized controlled trial. Psychol Med 2014;44:3025-35.
74. Chadwick P, Hughes S, Russell D et al. Mindfulness groups for distressing voices and paranoia: a replication and randomized feasibility trial. Behav Cogn Psychother 2009;37:403-12.
75. Chadwick P, Strauss C, Jones AM et al. Group mindfulness-based intervention for distressing voices: a pragmatic randomised controlled trial. Schizophr Res 2016;175:168-73.
76. Bach P, Hayes SC. The use of acceptance and commitment therapy to prevent the rehospitalization of psychotic patients: a randomized controlled trial. J Consult Clin Psychol 2002;70:1129-39.
77. Shawyer F, Farhall J, Thomas N et al. Acceptance and commitment therapy for psychosis: randomised controlled trial. Br J Psychiatry 2016;210:140-8.
78. Schnackenberg J, Fleming M, Martin CR. A randomised controlled pilot study of Experience Focused Counselling with voice hearers. Psychosis 2017;9:12-24.
79. Jenner JA, Nienhuis FJ, Wiersma D et al. Hallucination focused integrative treatment: a randomized controlled trial. Schizophr Bull 2004;30:133-45.
80. Craig TK, Rus-Calafell M, Ward T et al. AVATAR therapy for auditory verbal hallucinations in people with psychosis: a single-blind, randomised controlled trial. Lancet Psychiatry 2018;5:31-40.
81. Adams CE, Coutinho E, Davis JM et al. Cochrane Schizophrenia Group. The Cochrane library. Chichester: Wiley, 2011.
82. Leucht S, Kane JM, Kissling W et al. What does the PANSS mean? Schizophr Res 2005;79:231-8.
83. Hutton P. Should people with psychosis be supported in choosing cognitive therapy as an alternative to antipsychotic medication: a commentary on a commentary. Schizophr Res (in press).
