Психиатрия Всемирная психиатрия
Психиатрия Всемирная психиатрия
№03 2019
Оценка и тактика терапии бессонницы: последние данные №03 2019
Номера страниц в выпуске:345-359
состояние, которое связано с выраженными нарушениями функционирования и качества жизни, психическими и физическими заболеваниями, несчастными случаями. Поэтому в клинической практике необходимы эффективные подходы к лечению этого состояния. В связи с этим в данной статье рассматриваются важнейшие аспекты оценки бессонницы и доступные варианты лечения. Терапия включает в себя как немедикаментозное лечение, прежде всего когнитивно-поведенческую терапию, так и различные фармакологические методы лечения: бензодиазепины, z-препараты, агонисты мелатониновых рецепторов, селективные антагонисты гистамина H1, антагонисты орексина, антидепрессанты, антипсихотики, антиконвульсанты и неселективные антигистаминные препараты. Обзор имеющихся исследований показывает, что для некоторых из наиболее часто используемых методов лечения бессонницы отсутствуют двойные слепые рандомизированные контролируемые исследования со строгим дизайном. Тем не менее, существует целый ряд вмешательств с доказанным в исследованиях подобного качества терапевтическим эффектом, и чьи профили риска/пользы хорошо охарактеризованы. Эти интервенции могут служить основой для систематического, научно обоснованного лечения бессонницы в клинической практике. Мы приводим обзор доказательной базы, подчеркивая области, где необходимы дополнительные исследования, с целью предоставления ресурса для улучшения качества помощи многим пациентам с бессонницей.
Ключевые слова: бессонница, когнитивно-поведенческая терапия, фармакотерапия, бензодиазепины, z-препараты, антагонисты орексина, агонисты мелатониновых рецепторов, антидепрессанты, антипсихотики, антиконвульсанты
Ключевые слова: бессонница, когнитивно-поведенческая терапия, фармакотерапия, бензодиазепины, z-препараты, антагонисты орексина, агонисты мелатониновых рецепторов, антидепрессанты, антипсихотики, антиконвульсанты
Перевод: Пальчикова Е.И. (Санкт-Петербург)
Редактура: к.м.н. Захарова Н. В. (Москва)
Krystal A.D., Prather A.A., Ashbrook L.H. The assessment and management of insomnia: an update. World Psychiatry 2019;18(3);337-352
состояние, которое связано с выраженными нарушениями функционирования и качества жизни, психическими и физическими заболеваниями, несчастными случаями. Поэтому в клинической практике необходимы эффективные подходы к лечению этого состояния. В связи с этим в данной статье рассматриваются важнейшие аспекты оценки бессонницы и доступные варианты лечения. Терапия включает в себя как немедикаментозное лечение, прежде всего когнитивно-поведенческую терапию, так и различные фармакологические методы лечения: бензодиазепины, z-препараты, агонисты мелатониновых рецепторов, селективные антагонисты гистамина H1, антагонисты орексина, антидепрессанты, антипсихотики, антиконвульсанты и неселективные антигистаминные препараты. Обзор имеющихся исследований показывает, что для некоторых из наиболее часто используемых методов лечения бессонницы отсутствуют двойные слепые рандомизированные контролируемые исследования со строгим дизайном. Тем не менее, существует целый ряд вмешательств с доказанным в исследованиях подобного качества терапевтическим эффектом, и чьи профили риска/пользы хорошо охарактеризованы. Эти интервенции могут служить основой для систематического, научно обоснованного лечения бессонницы в клинической практике. Мы приводим обзор доказательной базы, подчеркивая области, где необходимы дополнительные исследования, с целью предоставления ресурса для улучшения качества помощи многим пациентам с бессонницей.
Ключевые слова: бессонница, когнитивно-поведенческая терапия, фармакотерапия, бензодиазепины, z-препараты, антагонисты орексина, агонисты мелатониновых рецепторов, антидепрессанты, антипсихотики, антиконвульсанты
Бессонница возникает несмотря на наличие надлежащих условий для сна и определяется жалобами на трудности засыпания или поддержания сна с последующими значительными нарушениями дневного функционирования1,2. Это распространенное состояние, с приблизительной встречаемостью около 10% среди населения3-6.
В подавляющем большинстве случаев бессонница сочетается с психическими или соматическими расстройствами. Долгое время считалось, что бессонница является симптомом этих расстройств, но имеющиеся данные свидетельствуют о том, что связь между такими состояниями и бессонницей носит комплексный и иногда двунаправленный характер. На самом деле, бессонница является фактором риска развития тяжелой депрессии, тревожных расстройств, употребления психоактивных веществ, суицидальности, гипертонии и диабета11-23. С учетом этого, а также в связи с тем, что бессонница ассоциирована с ухудшением качества жизни и повышенным риском несчастных случаев и травм, рекомендуется, чтобы лечение было направлено конкретно на устранение бессонницы всякий раз, когда она возникает, в том числе наряду с физическими или психическими расстройствами24,25.
В случае соответствия клинической картины пациента диагностическим критериям бессонницы, доступен ряд эмпирически обоснованных методов лечения. Они включают в себя как медикаментозную терапию, так и немедикаментозные вмешательства25-28. Негативное влияние этого состояния на здравоохранение с точки зрения распространенности, заболеваемости и последствий для здоровья подчеркивает необходимость эффективной диагностики и лечения в клинической практике. В этой статье рассматриваются имеющиеся на настоящий момент научно-обоснованные средства для оптимальной диагностики и лечения бессонницы.
Нарушение дневного функционирования может проявляться в виде утомляемости, чувства общего недомогания; нарушением внимания, сложностью концентрации внимания или запоминания; аффективными нарушениями с раздражительностью, сонливостью, гиперактивностью, импульсивностью, агрессией, снижением мотивации, склонностью допускать ошибки, обеспокоенностью или неудовлетворенностью сном2.
Бессонница может возникать несмотря на наличие надлежащих условий для сна – безопасного и затемненного помещения. Продолжительность бессонницы тоже имеет значение: для установления диагноза хронической бессонницы согласно международной классификации расстройств сна (ICSD-3) или стойкой бессонницы по DSM-5 необходимо сохранение симптомов как минимум в течение трех дней в неделю на протяжении трех месяцев. Кратковременная (ICSD-3) или эпизодическая (DSM-5) бессонница включает те же критерии, что и хроническая, но ее длительность не достигает трех месяцев.
Если жалобы на нарушения сна объясняются каким-либо соматическим, психическим расстройством, то диагноз бессонницы не ставится. Бессонница – это не только симптом психического расстройства, как считалось ранее29. Случаи, когда психическое расстройство послужило причиной бессонницы (по миновании острой фазы нарушения сна сохраняются), требуют особого клинического внимания. Бессонница в этих случаях должна диагностироваться как дискретное коморбидное расстройство.
Прошлые версии ICSD и DSM включают различные подтипы бессонницы. Например, психофизиологическую, парадоксальную, идиопатическую бессонницу, поведенческую бессонницу детского возраста, бессонницу вследствие психического расстройства, бессонницу вследствие соматического недуга и бессонницу вследствие употребления лекарственных или психоактивных веществ. Однако механизмы возникновения бессонницы изучены недостаточно, и различные подтипы трудно дифференцировать в клинической практике30. По этой причине все подтипы объединены в диагнозы «хроническая бессонница» (ICSD-3) и «стойкая бессонница» (DSM-5).
Ранее и по сей день отмечается вероятная связь бессонницы с недостаточной продолжительностью сна и соматическим неблагополучием. Это касается пациентов, чье состояние соответствует критериям хронической бессонницы с объективной продолжительностью сна менее 6 часов в сутки. Комбинация бессонницы с недостаточной продолжительностью сна ассоциирована с гипертензией, диабетом 2 типа и ухудшением нейрокогнитивного функционирования17,31,32. В связи с этим, в следующих классификациях данный тип бессонницы, в конечном счете, может стать отдельной категорией.
Если брать во внимание жалобы только на нарушения сна в ночное время, то показатели значительно выше. В большой выборке населения Франции 57% предъявляют жалобы на трудности с засыпанием, 53% на частые пробуждения и 41% на сон, не приносящий отдыха, при этом только 19% удовлетворяют временным критериям DSM-IV о возникновении жалоб, как минимум, 3 раза в неделю в течение одного месяца36.
Для многих бессонница является постоянным состоянием, при этом 74% сообщают о сохранении симптомом в течение по крайней мере одного года37. Стойкость симптоматики наиболее характерна для женщин, пожилых и людей с наиболее тяжелой бессонницей. В 3-хлетнем исследовании у более, чем половины участников достигнута ремиссия, но, тем не менее, частота рецидивов составляет 27%37. Распространены и семейные случаи бессонницы, которые встречаются в 35% наблюдений38.
Женщины чаще жалуются на симптомы бессонницы и ее последствия в дневное время, и диагноз бессонницы так же чаще устанавливается у женщин, чем у мужчин. Соотношение мужчин к женщинам составляет 1 к 1,4 по симптомам бессонницы и 1 к 2 по диагнозу бессонницы5. И у мужчин, и у женщин встречаемость бессонницы увеличивается с возрастом5,39,40.
Выявлена связь бессонницы с низким уровнем доходов и образования, а также с разводом или вдовством5,36,41. Также имеется взаимосвязь между бессонницей и соматическими заболеваниями: половина пациентов с жалобами на расстройства сна предъявляют и другие соматические жалобы34,41. Лица с бессонницей чаще характеризуют свое здоровье как неудовлетворительное42,43.
Бессонница тесно связана с психическими расстройствами, чаще всего депрессией, тревогой и посттравматическим стрессовым расстройством. В разных культурах большинство людей с БДР сообщают о бессоннице44, в то же время те, кто страдает бессонницей, более склонны к депрессивному настроению42,43,45-47. Бессонница также является предиктором развития психических расстройств, включая депрессию, тревогу, биполярное расстройство и суицид45.
Основная жалоба при бессоннице – трудности засыпания, поверхностный сон с частыми пробуждениями и раннее утреннее пробуждение без чувства отдыха. Раннее утреннее пробуждение – это пробуждение по крайней мере за 30 минут до желаемого времени, с учетом привычного времени сна, общего времени сна и преморбидной картины.
Специфичные жалобы могут изменяться со временем и часто включают в себя более одной проблемы со сном. Следует уточнить продолжительность, частоту и тяжесть этой проблемы, а также факторы, усугубляющие и облегчающие ее. Жалобы на бессонницу часто возникают только при обследовании на предмет другого расстройства, несмотря на влияние бессонницы на многочисленные проблемы со здоровьем.
Текущий анамнез сна
Тщательный сбор анамнеза сна обязателен для подтверждения диагноза бессонницы и выбора наилучшего вмешательства для пациента. Он включает в себя график отхода ко сну и пробуждения, подготовку ко сну, поведение ночью и нарушение дневного функционирования.
Также важно, что делает пациент, когда не засыпает. Например, пациент, который встает с постели, когда не может уснуть, и ест мороженое или смотрит любимое шоу, обеспечивает положительное подкрепление бодрствования, что является контрпродуктивным. Такие поведенческие стереотипы необходимо нивелировать в ходе лечения.
Необходимо уточнить график отхода ко сну как в рабочие/учебные дни, так и в выходные, и в период отпуска. Множество вариаций может говорить о нарушении циркадного ритма и являться мишенью для вмешательства.
Дремлет ли пациент днем? Дневная дрема может отсрочить время ночного засыпания, и, соответственно, быть мишенью терапии. Если пациент сообщает о выраженной склонности к дневному сну, стоит подумать о другом расстройстве сна.
В то время как состояние пациента с истинной бессонницей не будет улучшаться при обеспечении темной, спокойной среды для сна, врач для того чтобы подтвердить диагноз, все же должен убедиться, что плохой сон не является следствием ненадлежащих условий сна.
Детализация процесса подготовки ко сну может также выделить области для вмешательства в ходе лечения. Например, использование мобильного телефона связано с меньшей продолжительностью сна22.
В данном случае может быть полезна информация от партнера, который спит рядом. Часто, когда пациент жалуется на полное отсутствие сна ночью, его партнер отмечает наличие достаточно долгих периодов сна, что может говорить о нарушении чувства сна/ложном восприятии сна.
Нарушения дневного функционирования
Нарушение дневного функционирования является одним из обязательных критериев бессонницы и также требует оценки. Речь идет об ухудшении качества жизни, беспокойства по поводу памяти, чувстве усталости, повышенной утомляемости, изменения настроения и снижения продуктивности на работе или в учебе.
Три «П» возникают последовательно: факторы, предрасполагающие (predisposing) человека к бессоннице, факторы, провоцирующие (precipitating) острый эпизод бессонницы, и факторы, способствующие хронификации бессонницы (perpetuating). Предрасполагающие факторы включают генетические и личностные особенности, приводящие к физиологическому и когнитивному перевозбуждению50,51. Провоцирующие факторы являются триггерами, после которых начинается цикл бессонницы и, как правило, представляют собой стрессовые события, в том числе и позитивные (потерю любимого человека, выход на пенсию, свадьбу). Факторы, способствующие хронификации позволяют бессоннице сохраняться, даже когда триггер удален. Эти факторы включают в себя поведенческие и когнитивные конструкты, которые приносят краткосрочное облегчение, но причиняют долгосрочный вред, например, увеличение времени пребывания в постели и снижение дневной активности.
При лечении бессонницы важно убедиться, что коморбидные состояния компенсированы.
Антидепрессанты, такие как селективные ингибиторы обратного захвата серотонина (СИОЗС), ингибиторы обратного захвата серотонина и норадреналина (СИОЗН) и ингибиторы моноаминоксидазы (иМАО), могут вызывать седацию или стимуляцию в зависимости от индивидуальной реакции. Поэтому пациент может попытаться перенести суточную дозу с утра на вечер или наоборот, чтобы определить, как это влияет на сон.
Безрецептурные антигистаминные препараты часто содержат стимуляторы, такие как псевдоэфедрин или фенилэфрин, и пациенты могут не понимать, что эти вещества способствуют развитию бессонницы. Отказ от алкоголя, бензодиазепинов или опиоидов так же может способствовать развитию бессонницы. То же касается средств для лечения заболеваний легких, в том числе альбутерола и теофиллина.
В инструкциях к некоторым препаратам (например, антигипертензивным средствам) бессонница указана как нежелательное явление (побочное действие), а бета-блокаторы, как известно, снижают уровень мелатонина, данные о непосредственном влиянии этих препаратов на сон противоречивы5,52,53.
Бытовые и профессиональные условия жизни
Когда пациент жалуется на дневную сонливость, профессия является ключевым элементом анамнеза сна для обеспечения безопасности вождения. Рабочее или школьное расписание также важны, поскольку их изменение, сменная работа и частые поездки со сменой часовых поясов могут нарушить сон.
Следует также уточнить об употреблении никотина, кофеина, алкоголя и других веществ.
Физикальное обследование
Бессонница не имеет специфических признаков при исследовании соматического или психического статуса. Тем не менее, обследование может дать представление о наличии иного заболевания или коморбидных состояний. В обследование должны входить: расчет индекса массы тела, измерение обхвата шеи и проходимости дыхательных путей для исключения синдрома ночного апноэ54.
Другие нарушения сна, которые могут сопровождаться жалобами на бессонницу, включают нарушения циркадного ритма сна и бодрствования, синдром беспокойных ног, синдром периодических движений конечностями во сне и обструктивное ночное апноэ.
Полезные вопросы для различения циркадных нарушений включают время отхода ко сну и бодрствования в выходные дни, праздники и каникулы по сравнению с рабочими учебными буднями, и наличие нормальной продолжительности сна, приносящего ощущение отдыха.. Если сон с 3 утра до 10 утра приносит ощущение отдыха, при этом пациент ложится в постель в полночь и надеется встать в 7 утра, но не может заснуть в течение нескольких часов, это может говорить о нарушении фазы медленного сна, и мишенью терапии должен быть рассогласованный внутренний ритм.
Синдром беспокойных ног подразумевает под собой непреодолимое желание совершать движения ногами, при этом движения приносят небольшое облегчение; обычно этому предшествуют парестезии и, как правило, состояние возникает во время отдыха в конце дня. Поскольку синдром может вызвать проблемы с засыпанием, его следует исключить или лечить непосредственно.
Обструктивное ночное апноэ может сопровождаться симптомами бессонницы, чаще у женщин, чем у мужчин. Следует уточнить наличие храпа, частых пробуждений, приостановки дыхания и, при наличии нарушений, провести полисомнографию55,56.
Дневник сна – это анкета, заполняемая пациентом, как правило, в течение не менее двух недель подряд, в которой он/она отражает время, когда он/она лег в постель, время отбоя, продолжительность сна, время и продолжительность пробуждений ночью, время утреннего пробуждения, время подъема из постели, сон, воспринимаемую продолжительность сна, и иногда качество и глубину сна. Употребление снотворного и алкоголя тоже иногда учитывается.
Дневник может быть очень полезен для диагностики бессонницы и является ключевым в подборе тактики терапии, потому что это помогает детально охарактеризовать нарушения сна, выявить дезадаптивное поведение и определить индикатор результата лечения. Если подозревается нарушение циркадного ритма, дневник сна может быть очень полезен для постановки правильного диагноза.
Он имеет достаточную надежность наряду с «золотым стандартом» – полисомнографией у «долго спящих», кто проводит мало времени бодрствуя и неподвижно, но не у тех, у кого нарушения сна со значительными периодами бодрствования57-60. Он часто совмещен с датчиком света для того, чтобы измерить время между выключением света и наступлением сна.
Актиграфия не является необходимой для оценки бессонницы, но она может быть полезна для пациента с недостаточно надежными дневником сна или анамнезом, или когда подозреваются циркадные нарушения.
Ограниченные данные свидетельствуют о том, что некоторые из этих устройств не точно отражают структуру сна, эффективность или латентность сна и склонны переоценивать продолжительность сна у «нормально спящих» и значительно сильнее искажать результаты у пациентов с бессонницей61,62. Поэтому эти устройства не рекомендуются для принятия клинических решений до тех пор, пока не будут проведены тщательные исследования, устанавливающие валидность и надежность. Простота использования и энтузиазм потребителей, однако, позволяют предположить, что эти устройства могут играть все большую роль в достижении прогресса оценки и терапии бессонницы.
Полисомнография может быть полезна для исключения других причин нарушения сна, таких как апноэ или синдром периодических движений конечностями. Таким образом, это исследование может быть показано при подозрении на ночное апноэ или в случае недостаточного ответа на терапию.
Во многих сомнологических клиниках каждый пациент заполняет Эпвортскую шкалу сонливости64 ввиду проблемы безопасности дневной сонливости при вождении или эксплуатации сложной техники. Индекс тяжести бессонницы65 обычно используется для оценки результатов терапии. Шкала дисфункциональных убеждений и представлений о сне66 может помочь получить дополнительную информацию относительно направления терапии. Питтсбургский индекс качества сна67 также обычно используется для предоставления информации о качестве сна с точки зрения пациента.
Несколько протоколов КПТБ эффективны в лечении бессонницы и улучшении качества сна у разных категорий больных68-77, на основании чего Американская коллегия врачей рекомендует этот способ в качестве первой линии терапии взрослых пациентов с бессонницей74.
Краткосрочные курсы КПТБ сравнимы по эффективности с фармакотерапией, при этом достигнутый результат сохраняется более длительный период по окончании курса72. В отличие от действия лекарственных препаратов, КПТБ имеет минимальные побочные эффекты. Ниже изложен клинический обзор компонентов КПТБ с последующими доказательствами ее эффективности, в т.ч. среди пациентов с сопутствующими заболеваниями, и примеры использования метода при различных схемах лечения.
Обычно достаточно 4-7 сессий КПТБ. Не известно, какое количество сеансов дают оптимальные результаты, однако имеющиеся данные свидетельствуют о том, что менее четырех сеансов терапии недостаточно для эффекта69,78.
Пациентам также следует напомнить, что нельзя употреблять вещества, нарушающие сон, такие как кофеин, никотин и алкоголь, особенно перед сном. Точно так же следует избегать энергичных упражнений за три-четыре часа до сна.
Кроме того, процедура отхода ко сну может быть полезна в подготовке пациента к постели. Она должна включать прекращение возбуждающей деятельности, в т.ч. яркого света (например, экрана компьютера), который может негативно повлиять на циркадные ритмы человека.
Чтобы устранить условный рефлекс, пациентам рекомендуется покинуть постель и спальню, если не хочется спать, посидеть в тихом месте до тех пор, пока снова не захочется. Точно так же перед сном рекомендуется не ложиться спать, если они не чувствуют сонливости. Использование кровати и спальни ограничивается сном и сексом, что означает, что пациентам рекомендуется не заниматься другими видами деятельности в постели, включая чтение или просмотр телевизора. Кроме того, пациентам рекомендуется просыпаться в одно и то же время каждое утро, семь дней в неделю, и вставать с постели в течение 10-15 минут после пробуждения.
Для того, чтобы эффективно выполнять следующую технику, пациенты должны по крайней мере одну неделю вести дневник сна (две недели предпочтительнее). Цель техники состоит в том, чтобы сократить время пребывания пациента в постели исходя из заявленного общего времени сна. Например, если в дневнике пациента указано среднее общее время сна шесть часов, но время в постели девять часов (отход ко сну в 9 вечера и время пробуждения в 6 утра), то новый график сна должен обеспечить время в постели только в течение шести часов (время отхода ко сну – полночь и время пробуждения – 6 утра).
Важно отметить, что пациентам рекомендуется не ложиться спать до нового назначенного времени и ложиться только тогда, когда хочется спать. При выборе окна возможности сна важно учитывать хронотип пациента.
Из соображений безопасности, связанными с ограничением сна (например, возможные когнитивные нарушения, вождение в состоянии сонливости), в литературе рекомендуется минимальное время пребывания в постели в течение пяти часов79. Кроме того, ограничение сна может усугубить сопутствующие заболевания. Например, показано, что ограничение сна снижает порог судорожной активности, повышает болевую чувствительность и способно индуцировать манию у пациентов с биполярным расстройством 80-82.
Пациентам рекомендуется вести дневник сна на протяжении всего лечения. Время пребывания в кровати должно пересматриваться на каждом сеансе КПТБ, с учетом периодичности сеансов раз в одну-две недели. Дневники сна позволяют врачу рассчитать среднюю эффективность сна, которая представляет собой процент времени, когда пациент спит от положенного времени пребывания в постели. Мы рекомендуем среднюю эффективность сна 85% и выше в качестве индикатора «хорошего» качества сна и порогового значения, которого необходимо придерживаться при корректировке времени пребывания в постели.
Как только эффективность сна пациента будет достаточно высока, врач может начать увеличивать время пребывания в постели, изменяя предписанное время на 15 мин каждый раз и отслеживая улучшение субъективного качества сна и уменьшение дневной сонливости пациента.
Ограничение сна, как правило, является компонентом КПТБ, который выполняется хуже всего. В случае, если пациент не может или не хочет проводить предписанное время в постели, следует применить метод сокращения сна. Этот метод состоит в медленном уменьшения времени пребывания в постели с течением времени для того, чтобы выявить рекомендуемое время сна. Этот метод может быть более понятен пациентам с выраженной тревогой относительно асомнии в дальнейшем.
Эти поведенческие методы дополняют стимульный контроль и ограничение сна, предоставляя пациенту инструменты для снижения возбуждения перед сном и в случае ночных пробуждений.
Методы релаксации различаются, но обычно включают диафрагмальное дыхание, напряжение и расслабление групп мышц и представление зрительных образов. Парадоксальность в том, что беспокойство о засыпании препятствует наступлению сна. Используя эту технику, пациентов просят бодрствовать как можно дольше, что приводит к снижению тревожности и облегчению наступления сна.
Одним из методов противодействия катастрофическим мыслям является изучение фактов из опыта пациента. Например, если у пациента есть убеждение, что плохой сон ухудшит работоспособность, врач может помочь пациенту выявить случаи, когда он/она был в достаточно работоспособном состоянии, несмотря на плохой сон ночью. Кроме того, может быть полезным предоставить пациенту техники для снижения беспокойства перед сном.
Другой метод, известный как упражнение конструктивного беспокойства требует, чтобы пациенты перечисляли ранним вечером три или более проблемы, которые, по их мнению, помешают их ночному сну. Для каждой проблемы пациенты приводят шаг к ее решению. Упражнение прекращается и откладывается, и если пациенты бодрствуют в течение ночи, они должны напомнить себе, что они уже совершили необходимый шаг к решению этой проблемы в наилучшее для этого время (т. е. не в середине ночи).
Кроме того, данные свидетельствуют о том, что КПТБ эффективна среди лиц с сопутствующими заболеваниями психиатрического и соматического профиля70, при этом, увеличивается число подтверждений того, что КПТБ оказывает положительное влияние на исходы сопутствующих заболеваний82,83.
Эффект КПТБ более выражен для психических, чем соматических сопутствующих заболеваний70. КПТБ осуществляется разными способами, включая индивидуальную очную терапию, групповую и интернет-опосредованную терапию. Кроме того, разработаны пособия по самопомощи, книги и видеоролики, которые позволяют пациентам самостоятельно проходить лечение. В целом, все методы эффективны, хотя согласно некоторым данным, психотерапия лицом к лицу более эффективна, чем самопомощь. Интернет-опосредованная терапия сопоставима по эффективности, с очной84,85; однако вполне вероятно, что в более сложных случаях может потребоваться очный контроль86.
В этом разделе мы рассмотрим характеристики всех этих препаратов (бензодиазепины, «z-препараты», агонисты мелатониновых рецепторов, селективные антагонисты гистамина Н1, антагонисты орексина, антидепрессанты, антипсихотики, противосудорожные и неселективные антигистаминные препараты) и представим имеющиеся данные об их эффективности и безопасности в качестве основы для принятия клинических решений.
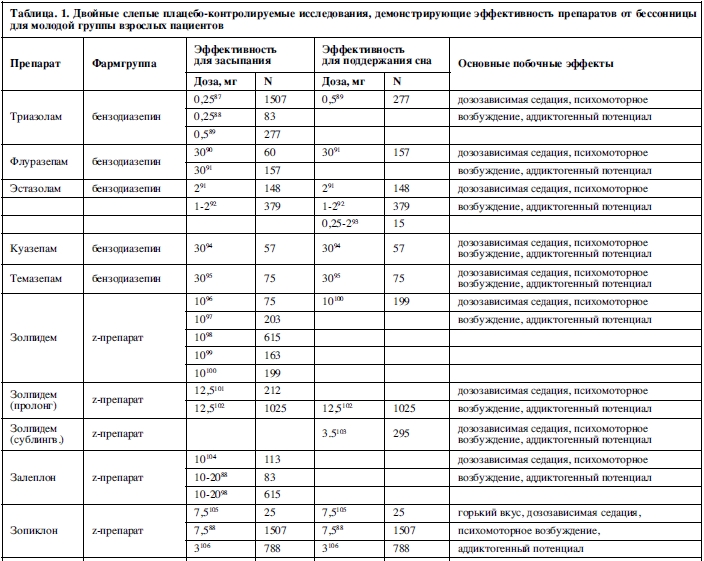
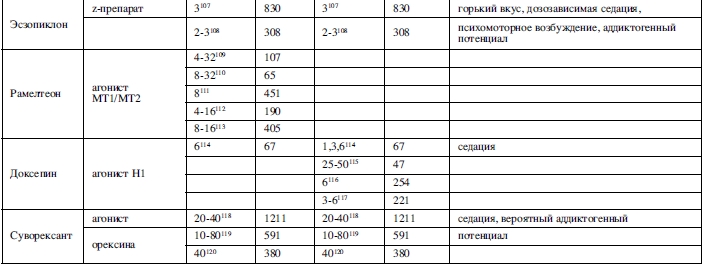
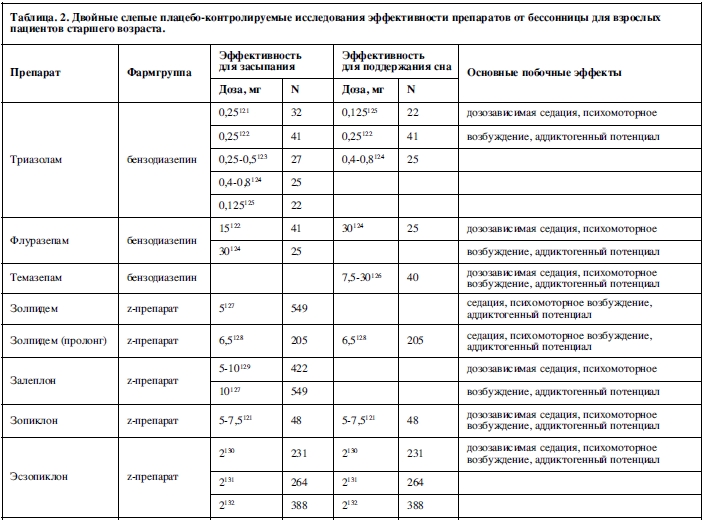
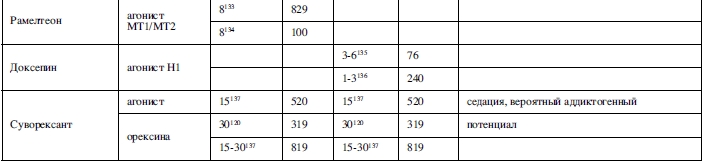
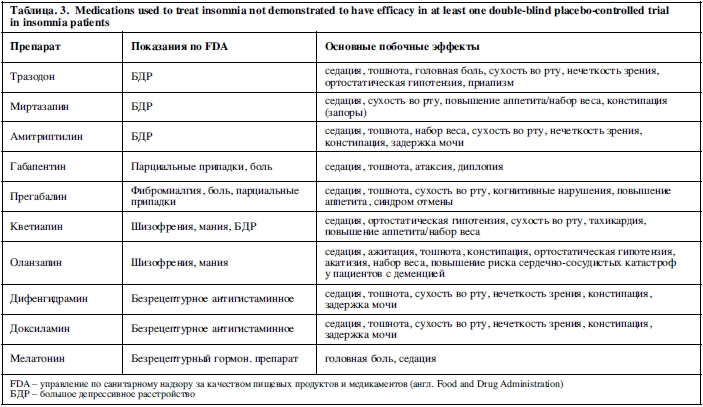
Среди препаратов бензодиазепинового ряда выявлено, что триазолам, флуразепам, темазепам, куазепам и эстазолам оказывают терапевтическое воздействие как на индукцию сна, так и на его поддержание в двойных слепых плацебо-контролируемых исследованиях у молодых людей (Таблица 1). У пожилых людей было обнаружено, что триазолам и флуразепам оказывают терапевтическое воздействие на индукцию и поддержание сна в двойных слепых плацебо-контролируемых исследованиях, в то время как темазепам оказывает терапевтическое воздействие только на поддержание сна (Таблица 2).
В течение многих лет преобладало мнение о препаратах этой группы и лекарствах, используемых для лечения бессонницы в целом, что к ним неизбежно формируется толерантность (т. е., потеря терапевтической пользы с течением времени) и синдром зависимости (т. е., симптомы отмены при прекращении приема) при длительном применении на ночь143. Однако до недавнего времени не было данных, позволяющих реально оценить, так ли это25. По мере появления новых исследований стало ясно, что толерантность и зависимость формируются не во всех случаях и не являются обязательным осложнением длительной фармакотерапии бессонницы.
Данные о длительном лечении имеются только по некоторым лекарственным препаратам, и имеющаяся информация позволяет допустить возможность формирования зависимости у некоторых лиц25. Это ограничение особенно заметно для бензодиазепинов: самым продолжительным исследованием применения бензодиазепинов на ночь было 8-недельное исследование темазепама, где синдром зависимости не формировался126. Исследования продолжительностью 2-4 недели были проведены с триазоламом (3) и флуразепамом (1), без доказательств формирования зависимости 87,121,122.
Побочные эффекты бензодиазепинов носят дозозависимый характер и отражают ингибирующее воздействие на центральную нервную систему. К ним относятся: седация, психомоторные нарушения и потенциальная возможность злоупотребления некоторыми пациентами143. Анксиолитический и миорелаксирующий эффект этой группы препаратов могут быть полезны при коморбидной тревоге или боли.
Среди доступных вариантов, эти препараты относительно эффективны при лечении проблем с засыпанием и, как следствие, могут быть необходимы пациентам с этим типом расстройства сна. Единственным относительным противопоказанием к их применению является злоупотребление психоактивными веществами в анамнезе или специфическая предрасположенность к злоупотреблению бензодиазепинами.
Двойные слепые плацебо-контролируемые исследования демонстрируют эффективность залеплона для индукции сна и золпидема пролонгированного действия, зопиклона и эзопиклона (S-изомер зопиклона) для индукции и поддержания сна как у молодых, так и у пожилых людей. Золпидем имеет доказанную эффективность относительно и индукции, и поддержания сна в более молодой группе, и только индукции сна у пациентов старшей возрастной группы (таблицы 1 и 2).
Для “z-препаратов” имеется больше данных о длительном лечении, чем для бензодиазепинов. Устойчивая эффективность зопиклона и золпидема продемонстрирована в исследованиях ночного применения длительностью до одного года без каких-либо признаков формирования зависимости, а также не была обнаружена зависимость в 6-месячном исследовании не ночного применения золпидема пролонгированного действия101,106,107.
Потенциальные побочные эффекты «z-препаратов» такие же, как и у бензодиазепинов. Из-за относительно узкого спектра терапевтических эффектов некоторых из этих препаратов не так же эффективны, как бензодиазепины в лечении сопутствующей тревоги или боли. Это, по-видимому, относится к золпидему. Однако обнаружено, что эзопиклон и золпидем пролонгированного действия оказывают терапевтическое воздействие на боль, тревогу и депрессию, сопутствующие бессоннице144-151.
Как и бензодиазепины, эти препараты относительно более эффективны, чем другие варианты лечения при нарушениях поддержания сна, и их применение спорно для пациентов, предрасположенных к злоупотреблению психоактивными веществами.
Мелатонин – это гормон, который принимают многие пациенты с бессонницей. Обычно он выделяется шишковидной железой в темное время суток. Он связывается преимущественно с рецепторами MT1 и MT2, хотя механизм, с помощью которого это может улучшить сон, не до конца изучен.
Для использования мелатонина при лечении бессонницы не установлено четкой зависимости доза-реакция, и есть некоторые доказательства того, что улучшение сна может зависеть от времени суток и не может произойти ранее 3-4 часов после приема препарата153-155.
Имеется значительное количество исследований по оценке влияния разных дозировок, времени приема, и форм немедленного и пролонгированного высвобождения этого препарата на бессонницу156,157. Имеющиеся данные свидетельствуют о том, что препарат обладает терапевтическим эффектом у лиц с синдромом отсроченного наступления фаз сна, и отличным профилем безопасности, а также может наблюдаться умеренный терапевтический эффект при задержке наступления сна у лиц с бессонницей (хотя остается неясным, имеет ли этот эффект клиническое значение). Некоторые предварительные данные подтверждают использование мелатонина для лечения проблем со сном у детей с нарушениями нервно-психического развития, у которых этот препарат, как установлено, также имеет отличный профиль безопасности158-163.
Наиболее распространенным побочным эффектом мелатонина является головная боль, а также снижение скорости реакции и седация, которые могут возникать в течение дня. Мелатонин не обладает аддиктогенным потенциалом, поэтому его можно назначать людям, страдающим бессонницей и имеющим склонность к формированию химической зависимости. Поскольку это гормон, косвенно влияющий на фертильность, прием мелатонина в более высоких дозировках может теоретически ухудшать фертильность. Поэтому рекомендовано не назначать его пациенткам, планирующим беременность164-167.
Как и мелатонин, рамелтеон является агонистом MT1 и MT2 рецепторов. Однако, является более сильным агонистом этих рецепторов, чем мелатонин. Двойные слепые плацебо-контролируемые исследования демонстрируют эффективность рамелтеона для лечения бессонницы с нарушением засыпания как у молодых, так и у пожилых людей (таблицы 1 и 2). Эффективность была более выражена при проведении полисомнографического исследовании, чем согласно самостоятельной оценке засыпания. Проводилась оценка приема препарата на ночь в течение шести месяцев, и не было зарегистрировано никаких признаков формирования зависимости111.
Рамелтеон имеет относительно мягкий профиль побочных эффектов, среди которых наиболее часто отмечаются головная боль, седация, усталость и тошнота. Он не имеет значительного аддиктогенного потенциала и может использоваться для лиц, имеющим склонность к формированию зависимости с нарушениями засыпания, хотя на настоящий момент нет исследований по оценке его терапевтических эффектов в этой популяции. В соответствии со своим хорошим профилем безопасности, он может использоваться для пациентов только с проблемами засыпания.
Доксепин, первоначально разработанный в качестве антидепрессанта в дозах 75-150 мг / сут, обладает антагонизмом к Н1-рецепторм, что является его наиболее мощным фармакологическим эффектом168. Таким образом, по мере уменьшения дозы увеличивается его специфический антагонизм к Н1-рецепторам.
Двойные слепые рандомизированные плацебо-контролируемые исследования, проведенные как с участием молодых, с участием пожилых пациентов, включавшие как самоотчет, так и полисомнографические данные, демонстрируют эффективность этого препарата в дозе 3-6 мг для поддержания сна (таблицы 1 и 2). Примечательно, что наибольший терапевтический эффект достигается к концу ночи, не ухудшая самочувствие утром. В сущности, это означает, что доксепин уникальным образом подходит для пациентов, страдающих ранними пробуждениями и имея затруднениями возвращения к сну. В ходе исследования назначения препарата на ночь в течение 3-х месяцев признаков формирования зависимости выявлено не было136.
Наиболее распространенным побочным эффектом препарата является дневная сонливость. Однако при сравнении группы пациентов старшего возраста, получающих доксепин и группы, получающей плацебо, не было выявлено разницы в частоте появления побочных эффектов.
В таком случае, целевой группой для лечения этим препаратом могут быть пожилые люди с жалобами на ранние пробуждения. Кроме того, с учетом антагонизма к Н1-рецепторам, стоит рассматривать доксепин как препарат выбора для пациентов с расстройствами сна по причине наличия аллергических симптомов. С учетом того, что препарат не обладает аддиктогенным потенциалом, он может использоваться для лечения пациентов с жалобами на трудности поддержания сна и имеющих склонность к формированию синдрома зависимости, не смотря на отсутствия исследований препарата на данной группе населения.
Суворексант является блокатором обоих типов рецепторов орексина (А и В), который в двойных слепых плацебо-контролируемых исследованиях продемонстрировал терапевтический воздействие на индукцию и поддержание сна (в том числе в последней трети ночи) как у молодых, так и у пожилых пациентов с бессонницей в дозах от 10 до 40 мг (таблицы 1 и 2). В том числе имеется плацебо-контролируемое исследование назначения препарата на ночь в течение года с устойчивым терапевтическим эффектом и отсутствием значительного рецидива бессонницы при прекращении лечения120.
Наиболее значимым побочным эффектом суворексанта является дневная седация. Имеющиеся исследования показывают, что этот препарат обладает небольшим наркогенным потенциалом, приблизительно сопоставимым с золпидемом, поэтому, вероятно, лучше избегать его использования у пациентов, склонных к формированию синдрома зависимости.
Суворексант является единственным средством, оказывающим терапевтическое воздействие в последнюю треть ночи без существенного увеличения степени утренней седации, обладая при этом терапевтическим воздействием на индукцию сна. Таким образом, препарат можно рассматривать для назначения пациентам с жалобами на нарушение засыпания и ранние пробуждениями одновременно.
Наиболее часто используемым антидепрессантом для лечения бессонницы является тразодон в дозе 50-150мг, доксепин в дозе 10-75мг, миртазапин в дозе 15мг и амитриптилин в дозе 10-100мг25. Из перечисленных препаратов только эффективность доксепина в дозе 25-50мг была подтверждена в одном двойном слепом рандомизированном плацебо-контролируемом исследовании с маленькой выборкой (N=47) (Таб.1).
Несмотря на то, что тразодон широко используется для лечения бессонницы, его эффективность не была подтверждена ни в одном двойном слепом рандомизированном плацебо-контролируемом исследовании. Имеется одно исследование эффективности у молодой группы пациентов, однако в ходе него не было выявлено различий по сравнению с плацебо97. Не стоит интерпретировать эти результаты как доказательство отсутствия эффективности тразодона при бессоннице. В действительности, исследование проводилось только относительно одной дозы (50мг), в то время как диапазон эффективности, согласно аннотации, варьирует от 50 до 150мг 25.
Имеются данные об эффективности и побочных эффектов S-изомера миртазапина, которые сейчас доступны для назначения. S-миртазапин, подобно доксепину, является селективным антагонистом Н1-рецепторов и также проявляет эффективность в отношении бессонницы и селективное воздействие на Н1 в гораздо более низких дозах, чем терапевтические169-171. В двойных слепых рандомизированных плацебо-контролируемых исследованиях была продемонстрирована схожая с доксепином эффективность в отношении поддержания сна и менее выраженная – в отношении инициации сна169-171.
Побочные эффекты антидепрессантов, используемых для лечения бессонницы разнообразны. Каждый из них способен вызывать дневную сонливость и большинство – ортостатическую гипотензию. Трициклические антидепрессанты доксепин (25-50мг) и амитриптилин могут вызывать сухость во рту, констипацию, нечеткость зрения, задержку мочи, когнитивные нарушения, нарушения ритма, повышение аппетита/набор веса. К наиболее важным побочным эффектам тразодона относится седация и ортостатическая гипотензия; так же может отмечаться приапизм25.
Поскольку ни один из препаратов этой группы не обладает аддиктогенным потенциалом, они могут рассматриваться для назначения пациентам, склонным к формированию синдрома зависимости. Также эти препараты можно рассматривать при неэффективности традиционной терапии и наличии коморбидных расстройств настроения, тревоги или боли, учитывая их основные фармакологические эффекты25. Доксепин и амитриптилин стоит с осторожностью назначать лицам с когнитивными нарушениями, задержкой мочи или глаукомой. Использование всех этих препаратов затруднено для пациентов с биполярной депрессией из-за риска возникновения лекарственно-обусловленной мании172.
Наиболее часто используемый антипсихотик для лечения бессонницы– кветиапин в дозе 25-250мг и оланзапин в дозе 2,5-20мг. Двойные слепые рандомизированные плацебо-контролируемые исследования эффективности антипсихотических препаратов в отношении бессонницы отсутствуют.
Проведено несколько небольших исследований эффективности кветиапина. Выявлено улучшение относительно времени пробуждения после засыпания по сравнению с плацебо в группе из 20 пациентов с синдромом зависимости от алкоголя и нарушениями сна173. Двойное слепое рандомизированное плацебо-контролируемое исследование эффективности кветиапина в дозе 25мг с выборкой в 13 пациентов также продемонстрировало эффективность кветиапина при первичной бессоннице и его положительный эффект в отношении времени засыпания и общего времени сна, тем не менее, эти эффекты не достигали статистической значимости174.
Основные побочные эффекты этих препаратов: седация, ортостатическая гипотензия, сухость во рту, тахикардия, повышение аппетита/набор веса, возбуждение, тошнота, констипация и акатизия. Более тревожный, хоть и реже встречающийся побочный эффект – риск тардивной дискинезии. Так же стоит учитывать риск цереброваскулярных катастроф у пациентов с деменцией.
Поскольку ни один из препаратов этой группы не обладает аддиктогенным потенциалом, они могут рассматриваться для назначения пациентам, склонным к формированию синдрома зависимости. Также они должны выступать препаратами выбора при бессоннице, возникающей у пациентов с психозом или биполярным расстройством.
Стоит с осторожностью применять эти препараты при наличии у пациента деменции, гипотензии, риска инфаркта миокарда, закрытоугольной глаукомы, констипации или задержке мочи.
Крайне мало доказательств эффективности этих препаратов в отношении бессонницы. Имеются данные двойного слепого рандомизированного плацебо-контролируемого исследования эффективности 50мг дифенгидрамина в отношении самостоятельно оцениваемого количества пробуждений, но не качества, общего времени сна и времени засыпания на выборке из 20 пациентов с первичной бессонницей175. Дифенгидрамин в дозе 25 мг также оценивался в исследовании с параллельными группами вместе с комбинацией валерианы и хмеля на выборке из 184 пациентов с бессонницей, и была выявлена значимо большая эффективность по сравнению с плацебо согласно самостоятельной оценке, но не полисомнографическим данным в отношении задержки наступления сна, общего времени сна, или полисомнографической эффективности сна176.
Наиболее значимые побочные эффекты этих препаратов: седация, тошнота, сухость во рту, нечеткость зрения, констипация, задержка мочи и набор веса. Менее распространенные побочные эффекты дифенгидрамина включают ажитацию и бессонницу, в то время как в отношении доксиламина приводились данные о развитии комы и рабдомиолиза177.
Поскольку ни один из препаратов этой группы не обладает аддиктогенным потенциалом, теоретически, они могут рассматриваться для назначения пациентам, склонным к формированию синдрома зависимости. Они являются препаратами выбора при бессоннице, вызванной симптомами аллергии или заболеванием верхних дыхательных путей. Следует избегать назначения этих препаратов пациентам с закрытоугольной глаукомой, замедлением моторики ЖКТ, задержкой мочи, астмой и ХОБЛ.
Двойные слепые рандомизированные плацебо-контролируемые исследования эффективности антиконвульсантов в терапии бессонницы отсутствуют. В двух двойных слепых рандомизированных плацебо-контролируемых исследованиях была выявлена эффективность 250-500мг габапентина в отношении бессонницы при условии отхождения ко сну на 5 часов раньше обычного (пятичасовая модель опережения фазы сна). Отмечалось существенное улучшение в отношении времени после индукции сна и общего времени сна, но не в отношении задержки наступления сна в группе габапентина по сравнению с плацебо как по данным самостоятельной оценки, так и по полисомнографическим данным180,181.
Терапевтический эффект габапентина и прегабалина на бессонницу так же был выявлен в исследованиях пациентов с болевым синдромом, синдромом беспокойных ног, ГТР и эпилепсией182-185.
Наиболее значимые побочные эффекты габапентина – седация, тошнота, атаксия и диплопия, в то время как для прегабалина– седация, тошнота, сухость во рту, когнитивные нарушения, повышение аппетита. В отличие от габапентина, прегабалин обладает аддиктогенным потенциалом186.
Эти препараты могут рассматриваться для назначения пациентам с болевым синдромом, парциальными припадками или синдромом беспокойных ног в качестве терапии бессонницы. Имеются данные об эффективности прегабалина в терапии бессонницы у пациентов с синдромом зависимости от алкоголя187,188. Следует избегать назначения этих препаратов пациентам с почечной недостаточностью.
Нам не хватило информации о специфических эффектах компонентов КПТБ, которые демонстрировали бы большую эффективность в лечении и адаптации. С одной стороны, имеются мета-анализы, демонстрирующие ценность КПТБ, с другой – данные исследований слишком гетерогенны. Вариабельность компонентов КПТБ в исследованиях затрудняет понимания, какие из них привносят больше в улучшение состояния. Таким образом, имеется нехватка исследований, направленных на уточнение этой информации.
Также имеются пробелы в отношении фармакотерапии. Самый очевидный – нехватка двойных слепых рандомизированных плацебо-контролируемых исследований эффективности того или иного препарата для детей и подростков. Однозначно, имеется необходимость в срочном проведении таких исследований для определения надлежащей тактики ведения бессонницы у более молодых групп пациентов.
Следующий пробел в психофармакологических исследованиях бессонницы – нехватка строгих двойных слепых рандомизированных плацебо-контролируемых исследований препаратов, часто используемых для лечения этого состояния. Например, тразодона, кветиапина и габапентина. Огромной ценностью было бы, если бы клиницисты, использующие эти препараты, обладали информацией для определения рисков и преимуществ с целью принятия клинических решений.
Не хватает исследований фармакотерапии бессонницы при наличии нескольких ключевых заболеваний в клинической картине, когда лечение зачастую необходимо, например, при деменции, мягком когнитивном расстройстве или химических аддикциях.
И наконец, наиболее значимый пробел в данных, отраженный в приведенном обзоре, касается нехватки исследований для персонализации терапии. Большинство исследований выявляют эффекты монотерапии и плацебо или другого вмешательства в качестве группы контроля. Необходимо больше исследований комбинаций различных вмешательств с целью выявления наиболее эффективных из них для конкретных групп пациентов, чтобы в конечном итоге обеспечить лучшую персонализированность в клинической практике.
DOI:10.1002/wps.20674
Редактура: к.м.н. Захарова Н. В. (Москва)
Krystal A.D., Prather A.A., Ashbrook L.H. The assessment and management of insomnia: an update. World Psychiatry 2019;18(3);337-352
состояние, которое связано с выраженными нарушениями функционирования и качества жизни, психическими и физическими заболеваниями, несчастными случаями. Поэтому в клинической практике необходимы эффективные подходы к лечению этого состояния. В связи с этим в данной статье рассматриваются важнейшие аспекты оценки бессонницы и доступные варианты лечения. Терапия включает в себя как немедикаментозное лечение, прежде всего когнитивно-поведенческую терапию, так и различные фармакологические методы лечения: бензодиазепины, z-препараты, агонисты мелатониновых рецепторов, селективные антагонисты гистамина H1, антагонисты орексина, антидепрессанты, антипсихотики, антиконвульсанты и неселективные антигистаминные препараты. Обзор имеющихся исследований показывает, что для некоторых из наиболее часто используемых методов лечения бессонницы отсутствуют двойные слепые рандомизированные контролируемые исследования со строгим дизайном. Тем не менее, существует целый ряд вмешательств с доказанным в исследованиях подобного качества терапевтическим эффектом, и чьи профили риска/пользы хорошо охарактеризованы. Эти интервенции могут служить основой для систематического, научно обоснованного лечения бессонницы в клинической практике. Мы приводим обзор доказательной базы, подчеркивая области, где необходимы дополнительные исследования, с целью предоставления ресурса для улучшения качества помощи многим пациентам с бессонницей.
Ключевые слова: бессонница, когнитивно-поведенческая терапия, фармакотерапия, бензодиазепины, z-препараты, антагонисты орексина, агонисты мелатониновых рецепторов, антидепрессанты, антипсихотики, антиконвульсанты
Бессонница возникает несмотря на наличие надлежащих условий для сна и определяется жалобами на трудности засыпания или поддержания сна с последующими значительными нарушениями дневного функционирования1,2. Это распространенное состояние, с приблизительной встречаемостью около 10% среди населения3-6.
В подавляющем большинстве случаев бессонница сочетается с психическими или соматическими расстройствами. Долгое время считалось, что бессонница является симптомом этих расстройств, но имеющиеся данные свидетельствуют о том, что связь между такими состояниями и бессонницей носит комплексный и иногда двунаправленный характер. На самом деле, бессонница является фактором риска развития тяжелой депрессии, тревожных расстройств, употребления психоактивных веществ, суицидальности, гипертонии и диабета11-23. С учетом этого, а также в связи с тем, что бессонница ассоциирована с ухудшением качества жизни и повышенным риском несчастных случаев и травм, рекомендуется, чтобы лечение было направлено конкретно на устранение бессонницы всякий раз, когда она возникает, в том числе наряду с физическими или психическими расстройствами24,25.
В случае соответствия клинической картины пациента диагностическим критериям бессонницы, доступен ряд эмпирически обоснованных методов лечения. Они включают в себя как медикаментозную терапию, так и немедикаментозные вмешательства25-28. Негативное влияние этого состояния на здравоохранение с точки зрения распространенности, заболеваемости и последствий для здоровья подчеркивает необходимость эффективной диагностики и лечения в клинической практике. В этой статье рассматриваются имеющиеся на настоящий момент научно-обоснованные средства для оптимальной диагностики и лечения бессонницы.
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ БЕССОННИЦЫ
Диагноз бессонницы выставляется в случае наличия жалоб на затрудненное засыпание, частые ночные или ранние утренние пробуждения с последующим нарушением функционирования в дневное время1,2.Нарушение дневного функционирования может проявляться в виде утомляемости, чувства общего недомогания; нарушением внимания, сложностью концентрации внимания или запоминания; аффективными нарушениями с раздражительностью, сонливостью, гиперактивностью, импульсивностью, агрессией, снижением мотивации, склонностью допускать ошибки, обеспокоенностью или неудовлетворенностью сном2.
Бессонница может возникать несмотря на наличие надлежащих условий для сна – безопасного и затемненного помещения. Продолжительность бессонницы тоже имеет значение: для установления диагноза хронической бессонницы согласно международной классификации расстройств сна (ICSD-3) или стойкой бессонницы по DSM-5 необходимо сохранение симптомов как минимум в течение трех дней в неделю на протяжении трех месяцев. Кратковременная (ICSD-3) или эпизодическая (DSM-5) бессонница включает те же критерии, что и хроническая, но ее длительность не достигает трех месяцев.
Если жалобы на нарушения сна объясняются каким-либо соматическим, психическим расстройством, то диагноз бессонницы не ставится. Бессонница – это не только симптом психического расстройства, как считалось ранее29. Случаи, когда психическое расстройство послужило причиной бессонницы (по миновании острой фазы нарушения сна сохраняются), требуют особого клинического внимания. Бессонница в этих случаях должна диагностироваться как дискретное коморбидное расстройство.
Прошлые версии ICSD и DSM включают различные подтипы бессонницы. Например, психофизиологическую, парадоксальную, идиопатическую бессонницу, поведенческую бессонницу детского возраста, бессонницу вследствие психического расстройства, бессонницу вследствие соматического недуга и бессонницу вследствие употребления лекарственных или психоактивных веществ. Однако механизмы возникновения бессонницы изучены недостаточно, и различные подтипы трудно дифференцировать в клинической практике30. По этой причине все подтипы объединены в диагнозы «хроническая бессонница» (ICSD-3) и «стойкая бессонница» (DSM-5).
Ранее и по сей день отмечается вероятная связь бессонницы с недостаточной продолжительностью сна и соматическим неблагополучием. Это касается пациентов, чье состояние соответствует критериям хронической бессонницы с объективной продолжительностью сна менее 6 часов в сутки. Комбинация бессонницы с недостаточной продолжительностью сна ассоциирована с гипертензией, диабетом 2 типа и ухудшением нейрокогнитивного функционирования17,31,32. В связи с этим, в следующих классификациях данный тип бессонницы, в конечном счете, может стать отдельной категорией.
ДЕМОГРАФИЯ БЕССОННИЦЫ
Симптомы бессонницы весьма распространены: приблизительно каждый третий человек сообщает о наличии тех или иных симптомов на протяжении предыдущего года33,34. Распространенность официально установленного диагноза бессонницы составляет от 6 до 15%, в то время как заболеваемость варьирует в зависимости от исследуемого критерия35.Если брать во внимание жалобы только на нарушения сна в ночное время, то показатели значительно выше. В большой выборке населения Франции 57% предъявляют жалобы на трудности с засыпанием, 53% на частые пробуждения и 41% на сон, не приносящий отдыха, при этом только 19% удовлетворяют временным критериям DSM-IV о возникновении жалоб, как минимум, 3 раза в неделю в течение одного месяца36.
Для многих бессонница является постоянным состоянием, при этом 74% сообщают о сохранении симптомом в течение по крайней мере одного года37. Стойкость симптоматики наиболее характерна для женщин, пожилых и людей с наиболее тяжелой бессонницей. В 3-хлетнем исследовании у более, чем половины участников достигнута ремиссия, но, тем не менее, частота рецидивов составляет 27%37. Распространены и семейные случаи бессонницы, которые встречаются в 35% наблюдений38.
Женщины чаще жалуются на симптомы бессонницы и ее последствия в дневное время, и диагноз бессонницы так же чаще устанавливается у женщин, чем у мужчин. Соотношение мужчин к женщинам составляет 1 к 1,4 по симптомам бессонницы и 1 к 2 по диагнозу бессонницы5. И у мужчин, и у женщин встречаемость бессонницы увеличивается с возрастом5,39,40.
Выявлена связь бессонницы с низким уровнем доходов и образования, а также с разводом или вдовством5,36,41. Также имеется взаимосвязь между бессонницей и соматическими заболеваниями: половина пациентов с жалобами на расстройства сна предъявляют и другие соматические жалобы34,41. Лица с бессонницей чаще характеризуют свое здоровье как неудовлетворительное42,43.
Бессонница тесно связана с психическими расстройствами, чаще всего депрессией, тревогой и посттравматическим стрессовым расстройством. В разных культурах большинство людей с БДР сообщают о бессоннице44, в то же время те, кто страдает бессонницей, более склонны к депрессивному настроению42,43,45-47. Бессонница также является предиктором развития психических расстройств, включая депрессию, тревогу, биполярное расстройство и суицид45.
КЛИНИЧЕСКАЯ ОЦЕНКА БЕССОННИЦЫ
Основная жалобаОсновная жалоба при бессоннице – трудности засыпания, поверхностный сон с частыми пробуждениями и раннее утреннее пробуждение без чувства отдыха. Раннее утреннее пробуждение – это пробуждение по крайней мере за 30 минут до желаемого времени, с учетом привычного времени сна, общего времени сна и преморбидной картины.
Специфичные жалобы могут изменяться со временем и часто включают в себя более одной проблемы со сном. Следует уточнить продолжительность, частоту и тяжесть этой проблемы, а также факторы, усугубляющие и облегчающие ее. Жалобы на бессонницу часто возникают только при обследовании на предмет другого расстройства, несмотря на влияние бессонницы на многочисленные проблемы со здоровьем.
Текущий анамнез сна
Тщательный сбор анамнеза сна обязателен для подтверждения диагноза бессонницы и выбора наилучшего вмешательства для пациента. Он включает в себя график отхода ко сну и пробуждения, подготовку ко сну, поведение ночью и нарушение дневного функционирования.
График отхода ко сну и пробуждения
Необходимо получить детальный отчет о том, когда пациент ложится в постель, когда он засыпает, как часто просыпается ночью и как быстро засыпает вновь, необходимо уточнить время пробуждения утром и времени подъема с постели.Также важно, что делает пациент, когда не засыпает. Например, пациент, который встает с постели, когда не может уснуть, и ест мороженое или смотрит любимое шоу, обеспечивает положительное подкрепление бодрствования, что является контрпродуктивным. Такие поведенческие стереотипы необходимо нивелировать в ходе лечения.
Необходимо уточнить график отхода ко сну как в рабочие/учебные дни, так и в выходные, и в период отпуска. Множество вариаций может говорить о нарушении циркадного ритма и являться мишенью для вмешательства.
Дремлет ли пациент днем? Дневная дрема может отсрочить время ночного засыпания, и, соответственно, быть мишенью терапии. Если пациент сообщает о выраженной склонности к дневному сну, стоит подумать о другом расстройстве сна.
Подготовка ко сну
Важно иметь правильные условия качественного сна.В то время как состояние пациента с истинной бессонницей не будет улучшаться при обеспечении темной, спокойной среды для сна, врач для того чтобы подтвердить диагноз, все же должен убедиться, что плохой сон не является следствием ненадлежащих условий сна.
Детализация процесса подготовки ко сну может также выделить области для вмешательства в ходе лечения. Например, использование мобильного телефона связано с меньшей продолжительностью сна22.
Поведение ночью
Что делает пациент во время сна? Имеются ли поведенческие признаки, такие как храп или подергивание ногами, которые могут говорить о наличии иных заболеваний или коморбидных состояний?В данном случае может быть полезна информация от партнера, который спит рядом. Часто, когда пациент жалуется на полное отсутствие сна ночью, его партнер отмечает наличие достаточно долгих периодов сна, что может говорить о нарушении чувства сна/ложном восприятии сна.
Нарушения дневного функционирования
Нарушение дневного функционирования является одним из обязательных критериев бессонницы и также требует оценки. Речь идет об ухудшении качества жизни, беспокойства по поводу памяти, чувстве усталости, повышенной утомляемости, изменения настроения и снижения продуктивности на работе или в учебе.
Модель «3П»
Поведенческая модель бессонницы «3П», разработанная Spielman48, может помочь клиницисту сфокусироваться на анамнезе сна49. Модель подчеркивает, почему бессонница возникает у некоторых людей и что способствует хронификации бессонницы.Три «П» возникают последовательно: факторы, предрасполагающие (predisposing) человека к бессоннице, факторы, провоцирующие (precipitating) острый эпизод бессонницы, и факторы, способствующие хронификации бессонницы (perpetuating). Предрасполагающие факторы включают генетические и личностные особенности, приводящие к физиологическому и когнитивному перевозбуждению50,51. Провоцирующие факторы являются триггерами, после которых начинается цикл бессонницы и, как правило, представляют собой стрессовые события, в том числе и позитивные (потерю любимого человека, выход на пенсию, свадьбу). Факторы, способствующие хронификации позволяют бессоннице сохраняться, даже когда триггер удален. Эти факторы включают в себя поведенческие и когнитивные конструкты, которые приносят краткосрочное облегчение, но причиняют долгосрочный вред, например, увеличение времени пребывания в постели и снижение дневной активности.
Перенесенные заболевания
Взаимосвязь между соматическими заболеваниями или психическими расстройствами и бессонницей велика и принято считать, что эта связь имеет двунаправленный характер, когда физическое или психическое состояние усугубляет бессонницу и наоборот. Широкий диапазон соматических сопутствующих заболеваний – включая легочные, сердечные, желудочно-кишечные, эндокринные, неврологические, связанные с опорно-двигательной и мочеполовой системой – могут вносить вклад в течение бессонницы.При лечении бессонницы важно убедиться, что коморбидные состояния компенсированы.
Препараты
Множество лекарственных средств оказывают влияние на сон, поэтому должен быть собран точный список принимаемых лекарств, включая безрецептурные препараты и психоактивные вещества.Антидепрессанты, такие как селективные ингибиторы обратного захвата серотонина (СИОЗС), ингибиторы обратного захвата серотонина и норадреналина (СИОЗН) и ингибиторы моноаминоксидазы (иМАО), могут вызывать седацию или стимуляцию в зависимости от индивидуальной реакции. Поэтому пациент может попытаться перенести суточную дозу с утра на вечер или наоборот, чтобы определить, как это влияет на сон.
Безрецептурные антигистаминные препараты часто содержат стимуляторы, такие как псевдоэфедрин или фенилэфрин, и пациенты могут не понимать, что эти вещества способствуют развитию бессонницы. Отказ от алкоголя, бензодиазепинов или опиоидов так же может способствовать развитию бессонницы. То же касается средств для лечения заболеваний легких, в том числе альбутерола и теофиллина.
В инструкциях к некоторым препаратам (например, антигипертензивным средствам) бессонница указана как нежелательное явление (побочное действие), а бета-блокаторы, как известно, снижают уровень мелатонина, данные о непосредственном влиянии этих препаратов на сон противоречивы5,52,53.
Бытовые и профессиональные условия жизни
Когда пациент жалуется на дневную сонливость, профессия является ключевым элементом анамнеза сна для обеспечения безопасности вождения. Рабочее или школьное расписание также важны, поскольку их изменение, сменная работа и частые поездки со сменой часовых поясов могут нарушить сон.
Следует также уточнить об употреблении никотина, кофеина, алкоголя и других веществ.
Физикальное обследование
Бессонница не имеет специфических признаков при исследовании соматического или психического статуса. Тем не менее, обследование может дать представление о наличии иного заболевания или коморбидных состояний. В обследование должны входить: расчет индекса массы тела, измерение обхвата шеи и проходимости дыхательных путей для исключения синдрома ночного апноэ54.
Дифференциальный диагноз
Для постановки диагноза бессонницы необходимо наличие трех критериев: жалобы на проблемы с засыпанием при соблюдении надлежащих условий сна с нарушением дневного функционирования. Если пациент сообщает о невозможности спать в течение необходимых 7-8 часов, но не имеет последствий в дневное время, то он/она может относиться к группе «быстро высыпающихся». С другой стороны, если сон недостаточный и имеются нарушения дневного функционирования, но пациент может спать, когда предоставляется возможность, это нарушение сна, вероятно, обусловлено паттерном. Оценка сна во время каникул и выходных может быть полезна, чтобы дифференцировать эти состояния.Другие нарушения сна, которые могут сопровождаться жалобами на бессонницу, включают нарушения циркадного ритма сна и бодрствования, синдром беспокойных ног, синдром периодических движений конечностями во сне и обструктивное ночное апноэ.
Полезные вопросы для различения циркадных нарушений включают время отхода ко сну и бодрствования в выходные дни, праздники и каникулы по сравнению с рабочими учебными буднями, и наличие нормальной продолжительности сна, приносящего ощущение отдыха.. Если сон с 3 утра до 10 утра приносит ощущение отдыха, при этом пациент ложится в постель в полночь и надеется встать в 7 утра, но не может заснуть в течение нескольких часов, это может говорить о нарушении фазы медленного сна, и мишенью терапии должен быть рассогласованный внутренний ритм.
Синдром беспокойных ног подразумевает под собой непреодолимое желание совершать движения ногами, при этом движения приносят небольшое облегчение; обычно этому предшествуют парестезии и, как правило, состояние возникает во время отдыха в конце дня. Поскольку синдром может вызвать проблемы с засыпанием, его следует исключить или лечить непосредственно.
Обструктивное ночное апноэ может сопровождаться симптомами бессонницы, чаще у женщин, чем у мужчин. Следует уточнить наличие храпа, частых пробуждений, приостановки дыхания и, при наличии нарушений, провести полисомнографию55,56.
Инструменты для оценки бессонницы
Дневник снаДневник сна – это анкета, заполняемая пациентом, как правило, в течение не менее двух недель подряд, в которой он/она отражает время, когда он/она лег в постель, время отбоя, продолжительность сна, время и продолжительность пробуждений ночью, время утреннего пробуждения, время подъема из постели, сон, воспринимаемую продолжительность сна, и иногда качество и глубину сна. Употребление снотворного и алкоголя тоже иногда учитывается.
Дневник может быть очень полезен для диагностики бессонницы и является ключевым в подборе тактики терапии, потому что это помогает детально охарактеризовать нарушения сна, выявить дезадаптивное поведение и определить индикатор результата лечения. Если подозревается нарушение циркадного ритма, дневник сна может быть очень полезен для постановки правильного диагноза.
Актиграфия
Актиграф – это устройство, носимое на запястье, которое регистрирует двигательную активность и вычисляет периоды сна и бодрствования.Он имеет достаточную надежность наряду с «золотым стандартом» – полисомнографией у «долго спящих», кто проводит мало времени бодрствуя и неподвижно, но не у тех, у кого нарушения сна со значительными периодами бодрствования57-60. Он часто совмещен с датчиком света для того, чтобы измерить время между выключением света и наступлением сна.
Актиграфия не является необходимой для оценки бессонницы, но она может быть полезна для пациента с недостаточно надежными дневником сна или анамнезом, или когда подозреваются циркадные нарушения.
Персональные отслеживающие устройства
Имеющиеся на рынке устройства, которые предназначены для оценки сна, зачастую способны дифференцировать поверхностный и глубокий сон, становятся все более доступными. Существует мало опубликованных данных, указывающих на производительность почти всех этих потребительских устройств, и поэтому точность информации о периодах сна и бодрствования неизвестна.Ограниченные данные свидетельствуют о том, что некоторые из этих устройств не точно отражают структуру сна, эффективность или латентность сна и склонны переоценивать продолжительность сна у «нормально спящих» и значительно сильнее искажать результаты у пациентов с бессонницей61,62. Поэтому эти устройства не рекомендуются для принятия клинических решений до тех пор, пока не будут проведены тщательные исследования, устанавливающие валидность и надежность. Простота использования и энтузиазм потребителей, однако, позволяют предположить, что эти устройства могут играть все большую роль в достижении прогресса оценки и терапии бессонницы.
Полисомнография
Полисомнография – это золотой стандарт, позволяющий отличить сон от бодрствования. Исследование не требуется для диагностики бессонницы, основанной на самоотчете пациента. Это связано с тем, что показатели полисомнографии, получаемые в ходе исследования, не отражают жалобы приблизительно 40% пациентов с бессонницей63.Полисомнография может быть полезна для исключения других причин нарушения сна, таких как апноэ или синдром периодических движений конечностями. Таким образом, это исследование может быть показано при подозрении на ночное апноэ или в случае недостаточного ответа на терапию.
Опросники
Существует несколько шкал, полезных в оценке бессонницы.Во многих сомнологических клиниках каждый пациент заполняет Эпвортскую шкалу сонливости64 ввиду проблемы безопасности дневной сонливости при вождении или эксплуатации сложной техники. Индекс тяжести бессонницы65 обычно используется для оценки результатов терапии. Шкала дисфункциональных убеждений и представлений о сне66 может помочь получить дополнительную информацию относительно направления терапии. Питтсбургский индекс качества сна67 также обычно используется для предоставления информации о качестве сна с точки зрения пациента.
ТАКТИКА ТЕРАПИИ БЕССОННИЦЫ
Когда пациенту выставлен диагноз бессонницы, лечение может быть начато с одного из ряда доступных вмешательств. Они могут быть условно поделены на немедикаментозные и фармакологические методы. В следующих разделах мы рассмотрим эти вмешательства, сосредоточив внимание на имеющихся данных слепых контролируемых исследований, где оценивались их эффективность и неблагоприятные последствия.Немедикаментозные вмешательства
Существует несколько различных нефармакологических схем терапии, апробированных и разработанных для бессонницы. Здесь мы рассмотрим составляющие и обоснованность немедикаментозных вмешательств с наилучшей доказательной базой и широкой распространенностью, т. е. когнитивно-поведенческую терапию бессонницы (КПТБ).Несколько протоколов КПТБ эффективны в лечении бессонницы и улучшении качества сна у разных категорий больных68-77, на основании чего Американская коллегия врачей рекомендует этот способ в качестве первой линии терапии взрослых пациентов с бессонницей74.
Краткосрочные курсы КПТБ сравнимы по эффективности с фармакотерапией, при этом достигнутый результат сохраняется более длительный период по окончании курса72. В отличие от действия лекарственных препаратов, КПТБ имеет минимальные побочные эффекты. Ниже изложен клинический обзор компонентов КПТБ с последующими доказательствами ее эффективности, в т.ч. среди пациентов с сопутствующими заболеваниями, и примеры использования метода при различных схемах лечения.
Обычно достаточно 4-7 сессий КПТБ. Не известно, какое количество сеансов дают оптимальные результаты, однако имеющиеся данные свидетельствуют о том, что менее четырех сеансов терапии недостаточно для эффекта69,78.
Образовательный компонент КПТБ
Несмотря на то, что большинство пациентов с бессонницей, как правило, осведомлены о некоторых стратегиях поведения, укладывающихся в понятие гигиены сна, важно обучить их необходимым основам. Они включают в себя важность создания благоприятной среды для сна, сохраняя спальню темной, тихой и прохладной.Пациентам также следует напомнить, что нельзя употреблять вещества, нарушающие сон, такие как кофеин, никотин и алкоголь, особенно перед сном. Точно так же следует избегать энергичных упражнений за три-четыре часа до сна.
Кроме того, процедура отхода ко сну может быть полезна в подготовке пациента к постели. Она должна включать прекращение возбуждающей деятельности, в т.ч. яркого света (например, экрана компьютера), который может негативно повлиять на циркадные ритмы человека.
Поведенческий компонент КПТБ
Стимульный контрольЧтобы устранить условный рефлекс, пациентам рекомендуется покинуть постель и спальню, если не хочется спать, посидеть в тихом месте до тех пор, пока снова не захочется. Точно так же перед сном рекомендуется не ложиться спать, если они не чувствуют сонливости. Использование кровати и спальни ограничивается сном и сексом, что означает, что пациентам рекомендуется не заниматься другими видами деятельности в постели, включая чтение или просмотр телевизора. Кроме того, пациентам рекомендуется просыпаться в одно и то же время каждое утро, семь дней в неделю, и вставать с постели в течение 10-15 минут после пробуждения.
Ограничение сна
Еще одним распространенным фактором, способствующим развитию и сохранению бессонницы, является склонность пациентов проводить лишнее время в постели. На первый взгляд, это имеет разумный смысл, учитывая, что пациенты стремятся “поймать” сон в любой момент. Но, к сожалению, избыток времени в постели приводит к условному возбуждению и фрагментированному сну.Для того, чтобы эффективно выполнять следующую технику, пациенты должны по крайней мере одну неделю вести дневник сна (две недели предпочтительнее). Цель техники состоит в том, чтобы сократить время пребывания пациента в постели исходя из заявленного общего времени сна. Например, если в дневнике пациента указано среднее общее время сна шесть часов, но время в постели девять часов (отход ко сну в 9 вечера и время пробуждения в 6 утра), то новый график сна должен обеспечить время в постели только в течение шести часов (время отхода ко сну – полночь и время пробуждения – 6 утра).
Важно отметить, что пациентам рекомендуется не ложиться спать до нового назначенного времени и ложиться только тогда, когда хочется спать. При выборе окна возможности сна важно учитывать хронотип пациента.
Из соображений безопасности, связанными с ограничением сна (например, возможные когнитивные нарушения, вождение в состоянии сонливости), в литературе рекомендуется минимальное время пребывания в постели в течение пяти часов79. Кроме того, ограничение сна может усугубить сопутствующие заболевания. Например, показано, что ограничение сна снижает порог судорожной активности, повышает болевую чувствительность и способно индуцировать манию у пациентов с биполярным расстройством 80-82.
Пациентам рекомендуется вести дневник сна на протяжении всего лечения. Время пребывания в кровати должно пересматриваться на каждом сеансе КПТБ, с учетом периодичности сеансов раз в одну-две недели. Дневники сна позволяют врачу рассчитать среднюю эффективность сна, которая представляет собой процент времени, когда пациент спит от положенного времени пребывания в постели. Мы рекомендуем среднюю эффективность сна 85% и выше в качестве индикатора «хорошего» качества сна и порогового значения, которого необходимо придерживаться при корректировке времени пребывания в постели.
Как только эффективность сна пациента будет достаточно высока, врач может начать увеличивать время пребывания в постели, изменяя предписанное время на 15 мин каждый раз и отслеживая улучшение субъективного качества сна и уменьшение дневной сонливости пациента.
Ограничение сна, как правило, является компонентом КПТБ, который выполняется хуже всего. В случае, если пациент не может или не хочет проводить предписанное время в постели, следует применить метод сокращения сна. Этот метод состоит в медленном уменьшения времени пребывания в постели с течением времени для того, чтобы выявить рекомендуемое время сна. Этот метод может быть более понятен пациентам с выраженной тревогой относительно асомнии в дальнейшем.
Эти поведенческие методы дополняют стимульный контроль и ограничение сна, предоставляя пациенту инструменты для снижения возбуждения перед сном и в случае ночных пробуждений.
Методы релаксации различаются, но обычно включают диафрагмальное дыхание, напряжение и расслабление групп мышц и представление зрительных образов. Парадоксальность в том, что беспокойство о засыпании препятствует наступлению сна. Используя эту технику, пациентов просят бодрствовать как можно дольше, что приводит к снижению тревожности и облегчению наступления сна.
Когнитивные компоненты КПТБ
Дезадаптивным представлениям и мыслям о сне, как правило, уделяется внимание на протяжении всего лечения. Для клинициста важно отслеживать связанные со сном переживания, поскольку они, как правило, приводят к дезадаптивному поведению, способствующему хронификации бессонницы. К числу этих переживаний относятся нереалистичные ожидания относительно сна и катастрофические размышления о последствиях асомнии.Одним из методов противодействия катастрофическим мыслям является изучение фактов из опыта пациента. Например, если у пациента есть убеждение, что плохой сон ухудшит работоспособность, врач может помочь пациенту выявить случаи, когда он/она был в достаточно работоспособном состоянии, несмотря на плохой сон ночью. Кроме того, может быть полезным предоставить пациенту техники для снижения беспокойства перед сном.
Другой метод, известный как упражнение конструктивного беспокойства требует, чтобы пациенты перечисляли ранним вечером три или более проблемы, которые, по их мнению, помешают их ночному сну. Для каждой проблемы пациенты приводят шаг к ее решению. Упражнение прекращается и откладывается, и если пациенты бодрствуют в течение ночи, они должны напомнить себе, что они уже совершили необходимый шаг к решению этой проблемы в наилучшее для этого время (т. е. не в середине ночи).
Доказательства эффективности КПТБ
Несколько мета-анализов подтверждают эффективность КПТБ по сравнению с тактикой активного контроля и обычной терапией68-70, 72, 78-81. В мета-анализе van Straten et al69, включившем суммарно 3 724 пациента и 2 579 человек в группе контроля, объединены данные 87 рандомизированных контролируемых исследований, в которых использовался по крайней мере один компонент КПТБ. Самые выраженные улучшения были зафиксированы согласно индексу тяжести бессонницы (коэффициент хеджирования g =0.98) для эффективности сна (g=0,71), прерывистости сна (g=0,63), задержки наступления сна (g=0,71) и субъективного качества сна (g=0.40). Небольшой эффект наблюдался относительно изменения общего времени сна (g=0,16).Кроме того, данные свидетельствуют о том, что КПТБ эффективна среди лиц с сопутствующими заболеваниями психиатрического и соматического профиля70, при этом, увеличивается число подтверждений того, что КПТБ оказывает положительное влияние на исходы сопутствующих заболеваний82,83.
Эффект КПТБ более выражен для психических, чем соматических сопутствующих заболеваний70. КПТБ осуществляется разными способами, включая индивидуальную очную терапию, групповую и интернет-опосредованную терапию. Кроме того, разработаны пособия по самопомощи, книги и видеоролики, которые позволяют пациентам самостоятельно проходить лечение. В целом, все методы эффективны, хотя согласно некоторым данным, психотерапия лицом к лицу более эффективна, чем самопомощь. Интернет-опосредованная терапия сопоставима по эффективности, с очной84,85; однако вполне вероятно, что в более сложных случаях может потребоваться очный контроль86.
Фармакотерапия
Ряд препаратов различных групп апробированы в рандомизированных двойных слепых плацебо-контролируемых испытаниях терапии бессонницы. Те из них, для которых сообщалось о статистически значимом терапевтическом эффекте по сравнению с плацебо, представлены в таблицах 1 и 2. Кроме того, существует ряд препаратов, обычно используемых для лечения бессонницы, эффективность которых не была продемонстрирована ни в одном двойном слепом рандомизированном плацебо-контролируемом исследовании. Они представлены в таблице 3.В этом разделе мы рассмотрим характеристики всех этих препаратов (бензодиазепины, «z-препараты», агонисты мелатониновых рецепторов, селективные антагонисты гистамина Н1, антагонисты орексина, антидепрессанты, антипсихотики, противосудорожные и неселективные антигистаминные препараты) и представим имеющиеся данные об их эффективности и безопасности в качестве основы для принятия клинических решений.





Бензодиазепины
Бензодиазепины представляют собой группу препаратов со сходной химической структурой. Их снотворный эффект является результатом положительной аллостерической модуляции рецептора гамма-аминомасляной кислоты (ГАМК) типа А138,139. Эти вещества осуществляют модуляцию путем связывания с определенным участком ГАМК-рецепторного комплекса (называемого сайтом связывания бензодиазепина), тем самым изменяя конформацию составляющих рецептор белков, что приводит к усилению ингибирования, возникающего при связывании ГАМК с этими рецепторами. Усиление ингибирования связано с широким спектром дозозависимых клинических эффектов, включая седацию, снижение тревоги, уменьшение судорог и миорелаксацию139, 140, 142.Среди препаратов бензодиазепинового ряда выявлено, что триазолам, флуразепам, темазепам, куазепам и эстазолам оказывают терапевтическое воздействие как на индукцию сна, так и на его поддержание в двойных слепых плацебо-контролируемых исследованиях у молодых людей (Таблица 1). У пожилых людей было обнаружено, что триазолам и флуразепам оказывают терапевтическое воздействие на индукцию и поддержание сна в двойных слепых плацебо-контролируемых исследованиях, в то время как темазепам оказывает терапевтическое воздействие только на поддержание сна (Таблица 2).
В течение многих лет преобладало мнение о препаратах этой группы и лекарствах, используемых для лечения бессонницы в целом, что к ним неизбежно формируется толерантность (т. е., потеря терапевтической пользы с течением времени) и синдром зависимости (т. е., симптомы отмены при прекращении приема) при длительном применении на ночь143. Однако до недавнего времени не было данных, позволяющих реально оценить, так ли это25. По мере появления новых исследований стало ясно, что толерантность и зависимость формируются не во всех случаях и не являются обязательным осложнением длительной фармакотерапии бессонницы.
Данные о длительном лечении имеются только по некоторым лекарственным препаратам, и имеющаяся информация позволяет допустить возможность формирования зависимости у некоторых лиц25. Это ограничение особенно заметно для бензодиазепинов: самым продолжительным исследованием применения бензодиазепинов на ночь было 8-недельное исследование темазепама, где синдром зависимости не формировался126. Исследования продолжительностью 2-4 недели были проведены с триазоламом (3) и флуразепамом (1), без доказательств формирования зависимости 87,121,122.
Побочные эффекты бензодиазепинов носят дозозависимый характер и отражают ингибирующее воздействие на центральную нервную систему. К ним относятся: седация, психомоторные нарушения и потенциальная возможность злоупотребления некоторыми пациентами143. Анксиолитический и миорелаксирующий эффект этой группы препаратов могут быть полезны при коморбидной тревоге или боли.
Среди доступных вариантов, эти препараты относительно эффективны при лечении проблем с засыпанием и, как следствие, могут быть необходимы пациентам с этим типом расстройства сна. Единственным относительным противопоказанием к их применению является злоупотребление психоактивными веществами в анамнезе или специфическая предрасположенность к злоупотреблению бензодиазепинами.
«Z-препараты»
Эти лекарственные средства представляют собой химически неоднородную группу со схожим с бензодиазепинами механизмом действия, но не являющуюся бензодиазепиновой по химической структуре138-142. Имеются данные о том, что они могут несколько отличаться от бензодиазепинов, т.к. их действие относительно ограничено подвидами ГАМК-А рецепторов. Таким образом, z-препараты могут иметь менее широкий спектр клинических эффектов 25,138-142.Двойные слепые плацебо-контролируемые исследования демонстрируют эффективность залеплона для индукции сна и золпидема пролонгированного действия, зопиклона и эзопиклона (S-изомер зопиклона) для индукции и поддержания сна как у молодых, так и у пожилых людей. Золпидем имеет доказанную эффективность относительно и индукции, и поддержания сна в более молодой группе, и только индукции сна у пациентов старшей возрастной группы (таблицы 1 и 2).
Для “z-препаратов” имеется больше данных о длительном лечении, чем для бензодиазепинов. Устойчивая эффективность зопиклона и золпидема продемонстрирована в исследованиях ночного применения длительностью до одного года без каких-либо признаков формирования зависимости, а также не была обнаружена зависимость в 6-месячном исследовании не ночного применения золпидема пролонгированного действия101,106,107.
Потенциальные побочные эффекты «z-препаратов» такие же, как и у бензодиазепинов. Из-за относительно узкого спектра терапевтических эффектов некоторых из этих препаратов не так же эффективны, как бензодиазепины в лечении сопутствующей тревоги или боли. Это, по-видимому, относится к золпидему. Однако обнаружено, что эзопиклон и золпидем пролонгированного действия оказывают терапевтическое воздействие на боль, тревогу и депрессию, сопутствующие бессоннице144-151.
Как и бензодиазепины, эти препараты относительно более эффективны, чем другие варианты лечения при нарушениях поддержания сна, и их применение спорно для пациентов, предрасположенных к злоупотреблению психоактивными веществами.
Агонисты мелатониновых рецепторов
Для лечения бессонницы используются два агониста рецепторов мелатонина: мелатонин и рамелтеон.Мелатонин – это гормон, который принимают многие пациенты с бессонницей. Обычно он выделяется шишковидной железой в темное время суток. Он связывается преимущественно с рецепторами MT1 и MT2, хотя механизм, с помощью которого это может улучшить сон, не до конца изучен.
Для использования мелатонина при лечении бессонницы не установлено четкой зависимости доза-реакция, и есть некоторые доказательства того, что улучшение сна может зависеть от времени суток и не может произойти ранее 3-4 часов после приема препарата153-155.
Имеется значительное количество исследований по оценке влияния разных дозировок, времени приема, и форм немедленного и пролонгированного высвобождения этого препарата на бессонницу156,157. Имеющиеся данные свидетельствуют о том, что препарат обладает терапевтическим эффектом у лиц с синдромом отсроченного наступления фаз сна, и отличным профилем безопасности, а также может наблюдаться умеренный терапевтический эффект при задержке наступления сна у лиц с бессонницей (хотя остается неясным, имеет ли этот эффект клиническое значение). Некоторые предварительные данные подтверждают использование мелатонина для лечения проблем со сном у детей с нарушениями нервно-психического развития, у которых этот препарат, как установлено, также имеет отличный профиль безопасности158-163.
Наиболее распространенным побочным эффектом мелатонина является головная боль, а также снижение скорости реакции и седация, которые могут возникать в течение дня. Мелатонин не обладает аддиктогенным потенциалом, поэтому его можно назначать людям, страдающим бессонницей и имеющим склонность к формированию химической зависимости. Поскольку это гормон, косвенно влияющий на фертильность, прием мелатонина в более высоких дозировках может теоретически ухудшать фертильность. Поэтому рекомендовано не назначать его пациенткам, планирующим беременность164-167.
Как и мелатонин, рамелтеон является агонистом MT1 и MT2 рецепторов. Однако, является более сильным агонистом этих рецепторов, чем мелатонин. Двойные слепые плацебо-контролируемые исследования демонстрируют эффективность рамелтеона для лечения бессонницы с нарушением засыпания как у молодых, так и у пожилых людей (таблицы 1 и 2). Эффективность была более выражена при проведении полисомнографического исследовании, чем согласно самостоятельной оценке засыпания. Проводилась оценка приема препарата на ночь в течение шести месяцев, и не было зарегистрировано никаких признаков формирования зависимости111.
Рамелтеон имеет относительно мягкий профиль побочных эффектов, среди которых наиболее часто отмечаются головная боль, седация, усталость и тошнота. Он не имеет значительного аддиктогенного потенциала и может использоваться для лиц, имеющим склонность к формированию зависимости с нарушениями засыпания, хотя на настоящий момент нет исследований по оценке его терапевтических эффектов в этой популяции. В соответствии со своим хорошим профилем безопасности, он может использоваться для пациентов только с проблемами засыпания.
Селективные антагонисты гистамина Н1
Единственный систематически изучаемый селективный антагонист гистамина Н1 – это доксепин в диапазоне доз от 3 до 6мг25.Доксепин, первоначально разработанный в качестве антидепрессанта в дозах 75-150 мг / сут, обладает антагонизмом к Н1-рецепторм, что является его наиболее мощным фармакологическим эффектом168. Таким образом, по мере уменьшения дозы увеличивается его специфический антагонизм к Н1-рецепторам.
Двойные слепые рандомизированные плацебо-контролируемые исследования, проведенные как с участием молодых, с участием пожилых пациентов, включавшие как самоотчет, так и полисомнографические данные, демонстрируют эффективность этого препарата в дозе 3-6 мг для поддержания сна (таблицы 1 и 2). Примечательно, что наибольший терапевтический эффект достигается к концу ночи, не ухудшая самочувствие утром. В сущности, это означает, что доксепин уникальным образом подходит для пациентов, страдающих ранними пробуждениями и имея затруднениями возвращения к сну. В ходе исследования назначения препарата на ночь в течение 3-х месяцев признаков формирования зависимости выявлено не было136.
Наиболее распространенным побочным эффектом препарата является дневная сонливость. Однако при сравнении группы пациентов старшего возраста, получающих доксепин и группы, получающей плацебо, не было выявлено разницы в частоте появления побочных эффектов.
В таком случае, целевой группой для лечения этим препаратом могут быть пожилые люди с жалобами на ранние пробуждения. Кроме того, с учетом антагонизма к Н1-рецепторам, стоит рассматривать доксепин как препарат выбора для пациентов с расстройствами сна по причине наличия аллергических симптомов. С учетом того, что препарат не обладает аддиктогенным потенциалом, он может использоваться для лечения пациентов с жалобами на трудности поддержания сна и имеющих склонность к формированию синдрома зависимости, не смотря на отсутствия исследований препарата на данной группе населения.
Антагонисты рецепторов орексина
Название «орексины» было дано двум относительно недавно обнаруженным пептидам, синтезируемым латеральным гипоталамусом и способным регулировать бодрствование/возбуждение118-120. Препараты, являющиеся антагонистами рецепторов орексина, способствуют наступлению сна за счет способности блокировать возбуждение, опосредованное орексинами.Суворексант является блокатором обоих типов рецепторов орексина (А и В), который в двойных слепых плацебо-контролируемых исследованиях продемонстрировал терапевтический воздействие на индукцию и поддержание сна (в том числе в последней трети ночи) как у молодых, так и у пожилых пациентов с бессонницей в дозах от 10 до 40 мг (таблицы 1 и 2). В том числе имеется плацебо-контролируемое исследование назначения препарата на ночь в течение года с устойчивым терапевтическим эффектом и отсутствием значительного рецидива бессонницы при прекращении лечения120.
Наиболее значимым побочным эффектом суворексанта является дневная седация. Имеющиеся исследования показывают, что этот препарат обладает небольшим наркогенным потенциалом, приблизительно сопоставимым с золпидемом, поэтому, вероятно, лучше избегать его использования у пациентов, склонных к формированию синдрома зависимости.
Суворексант является единственным средством, оказывающим терапевтическое воздействие в последнюю треть ночи без существенного увеличения степени утренней седации, обладая при этом терапевтическим воздействием на индукцию сна. Таким образом, препарат можно рассматривать для назначения пациентам с жалобами на нарушение засыпания и ранние пробуждениями одновременно.
Антидепрессанты
Имеется несколько препаратов, изначально предназначенных для лечения БДР, но зачастую используемых для лечения бессонницы. Эти лекарственные средства могут улучшать сон посредством воздействия на рецепторы нейротрансмиттеров, стимулирующих пробужение, таких как норадреналин, гистамин, ацетилхолин и серотонин25.Наиболее часто используемым антидепрессантом для лечения бессонницы является тразодон в дозе 50-150мг, доксепин в дозе 10-75мг, миртазапин в дозе 15мг и амитриптилин в дозе 10-100мг25. Из перечисленных препаратов только эффективность доксепина в дозе 25-50мг была подтверждена в одном двойном слепом рандомизированном плацебо-контролируемом исследовании с маленькой выборкой (N=47) (Таб.1).
Несмотря на то, что тразодон широко используется для лечения бессонницы, его эффективность не была подтверждена ни в одном двойном слепом рандомизированном плацебо-контролируемом исследовании. Имеется одно исследование эффективности у молодой группы пациентов, однако в ходе него не было выявлено различий по сравнению с плацебо97. Не стоит интерпретировать эти результаты как доказательство отсутствия эффективности тразодона при бессоннице. В действительности, исследование проводилось только относительно одной дозы (50мг), в то время как диапазон эффективности, согласно аннотации, варьирует от 50 до 150мг 25.
Имеются данные об эффективности и побочных эффектов S-изомера миртазапина, которые сейчас доступны для назначения. S-миртазапин, подобно доксепину, является селективным антагонистом Н1-рецепторов и также проявляет эффективность в отношении бессонницы и селективное воздействие на Н1 в гораздо более низких дозах, чем терапевтические169-171. В двойных слепых рандомизированных плацебо-контролируемых исследованиях была продемонстрирована схожая с доксепином эффективность в отношении поддержания сна и менее выраженная – в отношении инициации сна169-171.
Побочные эффекты антидепрессантов, используемых для лечения бессонницы разнообразны. Каждый из них способен вызывать дневную сонливость и большинство – ортостатическую гипотензию. Трициклические антидепрессанты доксепин (25-50мг) и амитриптилин могут вызывать сухость во рту, констипацию, нечеткость зрения, задержку мочи, когнитивные нарушения, нарушения ритма, повышение аппетита/набор веса. К наиболее важным побочным эффектам тразодона относится седация и ортостатическая гипотензия; так же может отмечаться приапизм25.
Поскольку ни один из препаратов этой группы не обладает аддиктогенным потенциалом, они могут рассматриваться для назначения пациентам, склонным к формированию синдрома зависимости. Также эти препараты можно рассматривать при неэффективности традиционной терапии и наличии коморбидных расстройств настроения, тревоги или боли, учитывая их основные фармакологические эффекты25. Доксепин и амитриптилин стоит с осторожностью назначать лицам с когнитивными нарушениями, задержкой мочи или глаукомой. Использование всех этих препаратов затруднено для пациентов с биполярной депрессией из-за риска возникновения лекарственно-обусловленной мании172.
Антипсихотики
Антипсихотики – группа препаратов, предназначенная для лечения психотических расстройств и иногда используемая в клинической практике для лечения бессонницы, как правило, в значительно меньших дозах, чем при лечении психозов25. Эти препараты могут быть эффективны при бессоннице ввиду выраженного антагонизма к рецепторам нейротрансмиттеров, стимулирующим пробуждение, таких как дофамин, гистамин, серотонин, а также к холинергическим и адренергическим рецепторам.Наиболее часто используемый антипсихотик для лечения бессонницы– кветиапин в дозе 25-250мг и оланзапин в дозе 2,5-20мг. Двойные слепые рандомизированные плацебо-контролируемые исследования эффективности антипсихотических препаратов в отношении бессонницы отсутствуют.
Проведено несколько небольших исследований эффективности кветиапина. Выявлено улучшение относительно времени пробуждения после засыпания по сравнению с плацебо в группе из 20 пациентов с синдромом зависимости от алкоголя и нарушениями сна173. Двойное слепое рандомизированное плацебо-контролируемое исследование эффективности кветиапина в дозе 25мг с выборкой в 13 пациентов также продемонстрировало эффективность кветиапина при первичной бессоннице и его положительный эффект в отношении времени засыпания и общего времени сна, тем не менее, эти эффекты не достигали статистической значимости174.
Основные побочные эффекты этих препаратов: седация, ортостатическая гипотензия, сухость во рту, тахикардия, повышение аппетита/набор веса, возбуждение, тошнота, констипация и акатизия. Более тревожный, хоть и реже встречающийся побочный эффект – риск тардивной дискинезии. Так же стоит учитывать риск цереброваскулярных катастроф у пациентов с деменцией.
Поскольку ни один из препаратов этой группы не обладает аддиктогенным потенциалом, они могут рассматриваться для назначения пациентам, склонным к формированию синдрома зависимости. Также они должны выступать препаратами выбора при бессоннице, возникающей у пациентов с психозом или биполярным расстройством.
Стоит с осторожностью применять эти препараты при наличии у пациента деменции, гипотензии, риска инфаркта миокарда, закрытоугольной глаукомы, констипации или задержке мочи.
Неселективные антигистаминные препараты
Зачастую для терапии бессонницы используются неселективные антигистаминные средства, такие как дифенгидрамин и доксиламин, которые составляют множество безрецептурных тактик лечения бессонницы. Оба препарата в дополнении к антагонизму к гистамину, проявляют клинически значимый антагонизм к мускариновызм холинергическим рецепторам М1.Крайне мало доказательств эффективности этих препаратов в отношении бессонницы. Имеются данные двойного слепого рандомизированного плацебо-контролируемого исследования эффективности 50мг дифенгидрамина в отношении самостоятельно оцениваемого количества пробуждений, но не качества, общего времени сна и времени засыпания на выборке из 20 пациентов с первичной бессонницей175. Дифенгидрамин в дозе 25 мг также оценивался в исследовании с параллельными группами вместе с комбинацией валерианы и хмеля на выборке из 184 пациентов с бессонницей, и была выявлена значимо большая эффективность по сравнению с плацебо согласно самостоятельной оценке, но не полисомнографическим данным в отношении задержки наступления сна, общего времени сна, или полисомнографической эффективности сна176.
Наиболее значимые побочные эффекты этих препаратов: седация, тошнота, сухость во рту, нечеткость зрения, констипация, задержка мочи и набор веса. Менее распространенные побочные эффекты дифенгидрамина включают ажитацию и бессонницу, в то время как в отношении доксиламина приводились данные о развитии комы и рабдомиолиза177.
Поскольку ни один из препаратов этой группы не обладает аддиктогенным потенциалом, теоретически, они могут рассматриваться для назначения пациентам, склонным к формированию синдрома зависимости. Они являются препаратами выбора при бессоннице, вызванной симптомами аллергии или заболеванием верхних дыхательных путей. Следует избегать назначения этих препаратов пациентам с закрытоугольной глаукомой, замедлением моторики ЖКТ, задержкой мочи, астмой и ХОБЛ.
Антиконвульсанты
Некоторые противосудорожные препараты иногда используются для терапии бессонницы. К ним относятся габапентин и прегабалин, чей снотворный эффект объясняется уменьшением высвобождения глутамата и норадреналина посредством связывания с альфа-2-дельта субъединицей потенциалзависимых кальциевых каналов типа N178,179.Двойные слепые рандомизированные плацебо-контролируемые исследования эффективности антиконвульсантов в терапии бессонницы отсутствуют. В двух двойных слепых рандомизированных плацебо-контролируемых исследованиях была выявлена эффективность 250-500мг габапентина в отношении бессонницы при условии отхождения ко сну на 5 часов раньше обычного (пятичасовая модель опережения фазы сна). Отмечалось существенное улучшение в отношении времени после индукции сна и общего времени сна, но не в отношении задержки наступления сна в группе габапентина по сравнению с плацебо как по данным самостоятельной оценки, так и по полисомнографическим данным180,181.
Терапевтический эффект габапентина и прегабалина на бессонницу так же был выявлен в исследованиях пациентов с болевым синдромом, синдромом беспокойных ног, ГТР и эпилепсией182-185.
Наиболее значимые побочные эффекты габапентина – седация, тошнота, атаксия и диплопия, в то время как для прегабалина– седация, тошнота, сухость во рту, когнитивные нарушения, повышение аппетита. В отличие от габапентина, прегабалин обладает аддиктогенным потенциалом186.
Эти препараты могут рассматриваться для назначения пациентам с болевым синдромом, парциальными припадками или синдромом беспокойных ног в качестве терапии бессонницы. Имеются данные об эффективности прегабалина в терапии бессонницы у пациентов с синдромом зависимости от алкоголя187,188. Следует избегать назначения этих препаратов пациентам с почечной недостаточностью.
ВОЗМОЖНЫЕ ОГРАНИЧЕНИЯ
Бессонница –изнуряющее расстройство, связанное со значительными неблагоприятными последствиями для физического здоровья и благополучия. К счастью, существуют поведенческие и фармакологические методы лечения этого состояния. В статье мы рассмотрели доказательную базу вмешательств, с целью создания источника информации для практикующих врачей, с надеждой, что это улучшит качество ведения бессонницы. Однако обзор также показывает, что существует ряд важных пробелов в исследованиях, проведенных на сегодняшний день.Нам не хватило информации о специфических эффектах компонентов КПТБ, которые демонстрировали бы большую эффективность в лечении и адаптации. С одной стороны, имеются мета-анализы, демонстрирующие ценность КПТБ, с другой – данные исследований слишком гетерогенны. Вариабельность компонентов КПТБ в исследованиях затрудняет понимания, какие из них привносят больше в улучшение состояния. Таким образом, имеется нехватка исследований, направленных на уточнение этой информации.
Также имеются пробелы в отношении фармакотерапии. Самый очевидный – нехватка двойных слепых рандомизированных плацебо-контролируемых исследований эффективности того или иного препарата для детей и подростков. Однозначно, имеется необходимость в срочном проведении таких исследований для определения надлежащей тактики ведения бессонницы у более молодых групп пациентов.
Следующий пробел в психофармакологических исследованиях бессонницы – нехватка строгих двойных слепых рандомизированных плацебо-контролируемых исследований препаратов, часто используемых для лечения этого состояния. Например, тразодона, кветиапина и габапентина. Огромной ценностью было бы, если бы клиницисты, использующие эти препараты, обладали информацией для определения рисков и преимуществ с целью принятия клинических решений.
Не хватает исследований фармакотерапии бессонницы при наличии нескольких ключевых заболеваний в клинической картине, когда лечение зачастую необходимо, например, при деменции, мягком когнитивном расстройстве или химических аддикциях.
И наконец, наиболее значимый пробел в данных, отраженный в приведенном обзоре, касается нехватки исследований для персонализации терапии. Большинство исследований выявляют эффекты монотерапии и плацебо или другого вмешательства в качестве группы контроля. Необходимо больше исследований комбинаций различных вмешательств с целью выявления наиболее эффективных из них для конкретных групп пациентов, чтобы в конечном итоге обеспечить лучшую персонализированность в клинической практике.
DOI:10.1002/wps.20674
Список исп. литературыСкрыть список1. American Psychiatric Association. Diagnostic and statistical manual of mental disorders, 5th ed. Arlington: American Psychiatric Association, 2013.
2. American Academy of Sleep Medicine. International classification of sleep disorders, 3rd ed. Darien: American Academy of Sleep Medicine, 2014.
3. Ohayon MM, Reynolds CF. Epidemiological and clinical relevance of insomnia diagnosis algorithms according to the DSM-IV and the Intern-tional Classification of Sleep Disorders (ICSD). Sleep Med 2009;10:952-60.
4. Roth T, Coulouvrat C, Hajak G et al. Prevalence and perceived health associated with insomnia based on DSM-IV-TR; International Statistical Clas-sification of Diseases and Related Health Problems, tenth revision; and Research Diagnostic Criteria/International Classification of Sleep Disorders. Biol Psychiatry 2011;69:592-600.
5. Ohayon MM. Epidemiology of insomnia: what we know and what we still need to learn. Sleep Med Rev 2002;6:97-111.
6. Morin CM, LeBlanc M, Bélanger L et al. Prevalence of insomnia and its treatment in Canada. Can J Psychiatry 2011;56:540-8.
7. Pearson NJ, Johnson LL, Nahin RL. Insomnia, trouble sleeping, and com-plementary and alternative medicine: analysis of the 2002 National Health Interview Survey data. Arch Intern Med 2006;166:1775-82.
8. Roth T, Jaeger S, Jin R et al. Sleep problems, comorbid mental disorders, and role functioning in the National Comorbidity Survey Replication. Biol Psychiatry 2006;60:1364-71.
9. Sarsour K, Morin CM, Foley K et al. Association of insomnia severity and comorbid medical and psychiatric disorders in a health plan-based sample: insomnia severity and comorbidities. Sleep Med 2010;11:69-74.
10. Budhiraja R, Roth T, Hudgel DW et al. Prevalence and polysomnographic correlates of insomnia comorbid with medical disorders. Sleep 2011;34:859-67.
11. Baglioni C, Battagliese G, Feige B et al. Insomnia as a predictor of depression: a meta-analytic evaluation of longitudinal epidemiological studies. J Affect Disord 2011;135:10-9.
12. Breslau N, Roth T, Rosenthal L et al. Sleep disturbance and psychiatric dis-orders: a longitudinal epidemiological study of young adults. Biol Psychiatry 1996;39:411-8.
13. Drake CL, Pillai V, Roth T. Stress and sleep reactivity: a prospective investigation of the stress diathesis model of insomnia. Sleep 2014;37:1295-304.
14. Johnson EO, Chilcoat HD, Breslau N. Trouble sleeping and anxiety/depression in childhood. Psychiatry Res 2000;94:93-102.
15. Johnson EO, Roth T, Breslau N. The association of insomnia with anxiety disorders and depression: exploration of the direction of risk. J Psychiatr Res 2006;40:700-8.
16. Pigeon WR, Pinquart M, Conner K. Meta-analysis of sleep disturbance and suicidal thoughts and behaviors. J Clin Psychiatry 2012;73:e1160-7.
17. Vgontzas AN, Liao D, Bixler EO et al. Insomnia with objective short sleep duration is associated with a high risk for hypertension. Sleep 2009;32:491-7.
18. Fernandez-Mendoza J, Vgontzas AN, Liao D et al. Insomnia with objective short sleep duration and incident hypertension: the Penn State Cohort. Hypertension 2012;60:929-35.
19. Parthasarathy S, Vasquez MM, Halonen M et al. Persistent insomnia is associated with mortality risk. Am J Med 2015;128:268-75.
20. Kessler RC, Berglund PA, Coulouvrat C et al. Insomnia, comorbidity, and risk of injury among insured Americans: results from the America Insomnia Survey. Sleep 2012;35:825-34.
21. Koski K, Luukinen H, Laippala P et al. Risk factors for major injurious falls among the home dwelling elderly by functional abilities. A prospective population-based study. Gerontology 1998;44:232-8.
22. Avidan AY, Fries BE, James ML et al. Insomnia and hypnotic use, recorded in the minimum data set, as predictors of falls and hip fractures in Michigan nursing homes. J Am Geriatr Soc 2005;53:955-62.
23. Stone KL, Blackwell TL, Ancoli-Israel S et al. Sleep disturbances and risk of falls in older community-dwelling men: the outcomes of Sleep Disorders in Older Men (MrOS Sleep) Study. J Am Geriatr Soc 2014;62:299-305.
24. National Institutes of Health. National Institutes of Health state of the science conference statement on manifestations and management of chronic insomnia in adults, June 13-15, 2005. Sleep 2005;28:1049-57.
25. Krystal AD. A compendium of placebo-controlled trials of the risks/benefits of pharmacological treatments for insomnia: the empirical basis for U.S. clinical practice. Sleep Med Rev 2009;13:265-74.
26. Sateia MJ, Buysse DJ, Krystal AD et al. Clinical practice guideline for the pharmacologic treatment of chronic insomnia in adults: an American Academy of Sleep Medicine clinical practice guideline. J Clin Sleep Med 2017;13:307-49.
27. Miller CB, Espie CA, Epstein DR et al. The evidence base of sleep restriction therapy for treating insomnia disorder. Sleep Med Rev 2014;18:415-24.
28. Morin CM, Bootzin RR, Buysse DJ et al. Psychological and behavioral treatment of insomnia: update of the recent evidence. Sleep 2006;29:1398-414.
29. Matteson-Rusby SE, Pigeon WR, Gehrman P et al. Why treat insomnia? Prim Care Companion J Clin Psychiatry 2010;12:PCC.08r00743.
30. Edinger JD, Wyatt JK, Stepanski EJ et al. Testing the reliability and validity of DSM-IV-TR and ICSD-2 insomnia diagnoses. Arch Gen Psychiatry 2011;68:992-1002.
31. Vgontzas AN, Liao D, Pejovic S et al. Insomnia with objective short sleep duration is associated with type 2 diabetes: a population-based study. Diabetes Care 2009;32:1980-5.
32. Fernandez-Mendoza J, Calhoun S, Bixler EO et al. Insomnia with objective short sleep duration is associated with deficits in neuropsychological performance: a general population study. Sleep 2010;33:459-65.
33. Johnson EO. Epidemiology of insomnia: from adolescence to old age. Sleep Med Clin 2006;1:305-17.
34. Mellinger GD, Balter MB, Uhlenhuth EH. Insomnia and its treatment. Prevalence and correlates. Arch Gen Psychiatry 1985;42:225-32.
35. Roth T. Insomnia: definition, prevalence, etiology, and consequences. J Clin Sleep Med 2007;3(Suppl.5):S7-10.
36. Leger D, Guilleminault C, Dreyfus JP et al. Prevalence of insomnia in a survey of 12,778 adults in France. J Sleep Res 2000;9:35-42.
37. Morin CM, Bélanger L, LeBlanc M et al. The natural history of insomnia: a population-based 3-year longitudinal study. Arch Intern Med 2009;169:447-53.
38. Beaulieu-Bonneau S, LeBlanc M, Mérette C et al. Family history of insomnia in a population-based sample. Sleep 2007;30:1739-45.
39. Kim K, Uchiyama M, Okawa M et al. An epidemiological study of insomnia among the Japanese general population. Sleep 2000;23:41-7.
40. Ohayon M. Epidemiological study on insomnia in the general population. Sleep 1996;19(Suppl. 3):S7-15.
41. Bixler EO, Kales A, Soldatos CR et al. Prevalence of sleep disorders in the Los Angeles metropolitan area. Am J Psychiatry 1979;136:1257-62.
42. Maggi S, Langlois JA, Minicuci N et al. Sleep complaints in community-dwelling older persons: prevalence, associated factors, and reported caus-es. J Am Geriatr Soc 1998;46:161-8.
43. Foley DJ, Monjan AA, Brown SL et al. Sleep complaints among elderly per-sons: an epidemiologic study of three communities. Sleep 1995;18:425-32.
44. Weissman MM, Bland RC, Canino GJ et al. Cross-national epidemiology of major depression and bipolar disorder. JAMA 1996;276:293-9.
45. Ford DE, Kamerow DB. Epidemiologic study of sleep disturbances and psychiatric disorders. An opportunity for prevention? JAMA 1989;262:1479-84.
46. Henderson S, Jorm AF, Scott LR et al. Insomnia in the elderly: its prevalence and correlates in the general population. Med J Aust 1995;162:22-4.
47. Tamura H, Nishida T, Tsuji A et al. Association between excessive use of mobile phone and insomnia and depression among Japanese adoles-cents. Int J Environ Res Publ Health 2017;14:701.
48. Spielman AJ, Caruso LS, Glovinsky PB. A behavioral-perspective on insomnia treatment. Psychiatr Clin North Am 1987;10:541-53.
49. Brainard GC, Hanifin JP, Greeson JM et al. Action spectrum for melatonin regulation in humans: evidence for a novel circadian photoreceptor. J Neurosci 2001;21:6405-12.
50. Yang C-M, Spielman AJ, Glovinsky P. Nonpharmacologic strategies in the management of insomnia. Psychiatr Clin North Am 2006;29:895-919.
51. Ebben MR, Spielman AJ. Non-pharmacological treatments for insomnia. J Behav Med 2009;32:244-54.
52. Gislason T, Almqvist M. Somatic diseases and sleep complaints. An epidemiological study of 3,201 Swedish men. Acta Med Scand 1987;221:475-81.
53. Stoschitzky K, Sakotnik A, Lercher P et al. Influence of beta-blockers on melatonin release. Eur J Clin Pharmacol 1999;55:111-5.
54. Schutte-Rodin S, Broch L, Buysse D et al. Clinical guideline for the evaluation and management of chronic insomnia in adults. J Clin Sleep Med 2008;4:487-504.
55. Theorell-Haglow J, Miller CB, Bartlett DJ et al. Gender differences in obstructive sleep apnoea, insomnia and restless legs syndrome in adults– What do we know? A clinical update. Sleep Med Rev 2018;38:28-38.
56. Valipour A, Lothaller H, Rauscher H et al. Gender-related differences in symptoms of patients with suspected breathing disorders in sleep: a clini-cal population study using the sleep disorders questionnaire. Sleep 2007;30:312-9.
57. Morgenthaler T, Alessi C, Friedman L et al. Practice parameters for the use of actigraphy in the assessment of sleep and sleep disorders: an update for 2007. Sleep 2007;30:519-29.
58. Hyde M, O’Driscoll DM, Binette S et al. Validation of actigraphy for deter-mining sleep and wake in children with sleep disordered breathing. J Sleep Res 2007;16:213-6.
59. Hedner J, Pillar G, Pittman SD et al. A novel adaptive wrist actigraphy algorithm for sleep-wake assessment in sleep apnea patients. Sleep 2004;27:1560-6.
60. Martin JL, Hakim AD. Wrist actigraphy. Chest 2011;139:1514-27.
61. Gruwez A, Libert W, Ameye L et al. Reliability of commercially available sleep and activity trackers with manual switch-to-sleep mode activation in free-living healthy individuals. Int J Med Inform 2017;102:87-92.
62. Ko PR, Kientz JA, Choe EK et al. Consumer sleep technologies: a review of the landscape. J Clin Sleep Med 2015;11:1455-61.
63. Krystal AD, Edinger JD, Wohlgemuth WK et al. NREM sleep EEG frequency spectral correlates of sleep complaints in primary insomnia subtypes. Sleep 2002;25:630-40.
64. Johns MW. A new method for measuring daytime sleepiness: the Ep-worth Sleepiness Scale. Sleep 1991;14:540-5.
65. Morin CM, Belleville G, Bélanger L et al. The Insomnia Severity Index: psychometric indicators to detect insomnia cases and evaluate treatment response. Sleep 2011;34:601-8.
66. Morin CM, Vallières A, Ivers H. Dysfunctional beliefs and attitudes about sleep (DBAS): validation of a brief version (DBAS-16). Sleep 2007;30:1547-54.
67. Buysse DJ, Reynolds CF 3rd, Monk TH et al. The Pittsburgh Sleep Quality Index: a new instrument for psychiatric practice and research. Psychiatr Res 1989;28:193-213.
68. Koffel EA, Koffel JB, Gehrman PR. A meta-analysis of group cognitive behavioral therapy for insomnia. Sleep Med Rev 2015;19:6-16.
69. van Straten A, van der Zweerde T, Kleiboer A et al. Cognitive and behavioral therapies in the treatment of insomnia: a meta-analysis. Sleep Med Rev 2018;38:3-16.
70. Wu JQ, Appleman ER, Salazar RD et al. Cognitive behavioral therapy for insomnia comorbid with psychiatric and medical conditions: a meta-analysis. JAMA Intern Med 2015;175:1461-72.
71. Irwin MR, Cole JC, Nicassio PM. Comparative meta-analysis of behavioral interventions for insomnia and their efficacy in middle-aged adults and in older adults 55+ years of age. Health Psychol 2006;25:3-14.
72. Smith MT, Perlis ML, Park A et al. Comparative meta-analysis of pharmacotherapy and behavior therapy for persistent insomnia. Am J Psychiatry 2002;159:5-11.
73. Seyffert M, Lagisetty P, Landgraf J et al. Internet-delivered cognitive behavioral therapy to treat insomnia: a systematic review and meta-analysis. PLoS One 2016;11:e0149139.
74. Qaseem A, Kansagara D, Forciea MA et al. Management of chronic insomnia disorder in adults: a clinical practice guideline from the American Col-lege of Physicians. Ann Intern Med 2016;165:
125-33.
75. Manber R, Carney C. Treatment plans and interventions for insomnia: a case formulation approach. New York: Guilford, 2015.
76. Edinger J, Carney C. Overcoming insomnia: a cognitive-behavioral therapy approach. Oxford: Oxford University Press, 2015.
77. Edinger JD, Wohlgemuth WK, Radtke RA et al. Cognitive behavioral therapy for treatment of chronic primary insomnia: a randomized controlled trial. JAMA 2001;285:1856-64.
78. Haack M, Scott-Sutherland J, Santangelo G et al. Pain sensitivity and modulation in primary insomnia. Eur J Pain 2012;16:522-33.
79. Colombo C, Benedetti F, Barbini B et al. Rate of switch from depression into mania after therapeutic sleep deprivation in bipolar depression. Psy-chiatry Res 1999;86:267-70.
80. Trauer JM, Qian MY, Doyle JS et al. Cognitive behavioral therapy for chronic insomnia: a systematic review and meta-analysis. Ann Intern Med 163;191-204.
81. Geiger-Brown JM, Rogers VE, Liu W et al. Cognitive behavioral therapy in persons with comorbid insomnia: a meta-analysis. Sleep Med Rev 2015;23:54-67.
82. Ho FY, Chan CS, Tang KN. Cognitive-behavioral therapy for sleep disturbances in treating posttraumatic stress disorder symptoms: a meta-analy-sis of randomized controlled trials. Clin Psychol Rev 2016;43:90-102.
83. Belleville G, Cousineau H, Levrier K et al. Meta-analytic review of the impact of cognitive-behavior therapy for insomnia on concomitant anxiety. Clin Psychol Rev 2011;31:638-52.
84. Ye YY, Zhang YF, Chen J et al. Internet-based cognitive behavioral therapy for insomnia (ICBT-I) improves comorbid anxiety and depression – a me-ta-analysis of randomized controlled trials. PLoS One 2015;10:e0142258.
85. Espie CA, Emsley R, Kyle SD et al. Effect of digital cognitive behavioral therapy for insomnia on health, psychological well-being and sleep-related quality of life: a randomized clinical trial. JAMA Psychiatry 2019;76:21-30.
86. Krystal AD, Prather AA. Should internet cognitive behavioral therapy for insomnia be the primary treatment option for insomnia?: Toward getting more SHUTi. JAMA Psychiatry 2017;74:15-6.
87. Hajak G, Clarenbach P, Fischer W et al. Zopiclone improves sleep quality and daytime well-being in insomniac patients: comparison with triazolam, flunitrazepam and placebo. Int Clin Psychopharmacol 1994;9:251-61.
88. Drake CL, Roehrs TA, Mangano RM et al. Dose-response effects of zaleplon as compared with triazolam (0.25 mg) and placebo in chronic pri-mary insomnia. Hum Psychopharmacol 2000;15:595-604.
89. Fabre LF Jr, Brachfeld J, Meyer LR et al. Multi-clinic double-blind comparison of triazolam (Halcion) and placebo administered for 14 consecutive nights in outpatients with insomnia. J Clin Psychiatry 1978;39:679-82.
90. Nair NP, Schwartz G, Dimitri R et al. A dose-range finding study of zopiclone in insomniac patients. Int Clin Psychopharmacol 1990;5(Suppl. 2):1-10.
91. Scharf MB, Roth PB, Dominguez RA et al. Estazolam and flurazepam: a multicenter, placebo-controlled comparative study in outpatients with in-somnia. J Clin Pharmacol 1990;30:461-7.
92. Walsh JK, Targum SD, Pegram V. A multi-center clinical investigation of estazolam: short-term efficacy. Curr Ther Res 1984;36:866-74.
93. Roehrs T, Zorick F, Lord N et al. Dose-related effects of estazolam on sleep of patients with insomnia. J Clin Psychopharmacol 1983;3:152-6.
94. Aden GC, Thatcher C. Quazepam in the short-term treatment of insomnia in outpatients. J Clin Psychiatry 1983;44:454-6.
95. Fillingim JM. Double-blind evaluation of the efficacy and safety of temazepam in outpatients with insomnia. Br J Clin Pharmacol 1979;8:73S-7.
96. Scharf MB, Roth T, Vogel GW et al. A multicenter, placebo-controlled study evaluating zolpidem in the treatment of chronic insomnia. J Clin Psychiatry 1994;55:192-9.
97. Walsh JK, Erman M, Erwin CW et al. Subjective hypnotic efficacy of trazodone and zolpidem in DSM-III-R primary insomnia. Hum Psychopharma-col 1998;13:191-8.
98. Elie R, Ruther E, Farr I et al. Sleep latency is shortened during 4 weeks of treatment with zaleplon, a novel nonbenzodiazepine hypnotic. Zaleplon Clinical Study Group. J Clin Psychiatry 1999;60:536-44.
99.Walsh JK, Roth T, Randazzo A et al. Eight weeks of non-nightly use of zolpidem for primary insomnia. Sleep 2000;23:1087-96.
100. Perlis ML, McCall WV, Krystal AD et al. Long-term, non-nightly administration of zolpidem in the treatment of patients with primary insomnia. J Clin Psychiatry 2004;65:1128-37.
101. Roth T, Soubrane C, Titeux L et al. Zoladult Study Group. Efficacy and safety of zolpidem-MR: a double-blind, placebo-controlled study in adults with primary insomnia. Sleep Med 2006;7:397-406.
102. Krystal AD, Erman M, Zammit GK et al. Long-term efficacy and safety of zolpidem extended-release 12.5 mg, administered 3 to 7 nights per week for 24 weeks, in patients with chronic primary insomnia: a 6-month, randomized, double-blind, placebo-controlled, parallel-group, multicenter study. Sleep 2008;31:79-90.
103. Roth T, Krystal A, Steinberg FJ et al. Novel sublingual low-dose zolpidem tablet reduces latency to sleep onset following spontaneous middle-of-the-night awakening in insomnia in a randomized, double-blind, placebo-controlled, outpatient study. Sleep 2013;36:189-96.
104. Walsh JK, Vogel GW, Scharf M et al. A five week, polysomnographic assessment of zaleplon 10 mg for the treatment of primary insomnia. Sleep Med 2000;1:41-9.
105. Ngen CC, Hassan R. A double-blind placebo-controlled trial of zopiclone 7.5 mg and temazepam 20 mg in insomnia. Int Clin Psychopharmacol 1990;5:165-71.
106. Krystal AD, Walsh JK, Laska E et al. Sustained efficacy of eszopiclone over six months of nightly treatment: results of a randomized, double-blind, placebo controlled study in adults with chronic insomnia. Sleep 2003;26:793-9.
107. Walsh JK, Krystal AD, Amata DA et al. Nightly treatment of primary insomnia with eszopiclone for six months: effect on sleep, quality of life, and work limitations. Sleep 2007;30:959-68.
108. Zammit GK, McNabb LJ, Caron J et al. Efficacy and safety of eszopiclone across 6-weeks of treatment for primary insomnia. Curr Med Res Opin 2004;20:1979-91.
109. Erman M, Seiden D, Zammit G et al. An efficacy, safety, and dose-response study of ramelteon in patients with chronic primary insomnia. Sleep Med 2006;7:17-24.
110. Kohsaka M, Kanemura T, Taniguchi M et al. Efficacy and tolerability of ramelteon in a double-blind, placebo-controlled, crossover study in Jap-anese patients with chronic primary insomnia. Expert Rev Neurother 2011;11:1389-97.
111. Mayer G, Wang-Weigand S, Roth-Schechter B et al. Efficacy and safety of 6-month nightly ramelteon administration in adults with chronic primary insomnia. Sleep 2009;32:351-60.
112. Uchiyama M, Hamamura M, Kuwano T et al. Long-term safety and efficacyof ramelteon in Japanese patients with chronic insomnia. Sleep Med 2011;12:127-33.
113. Zammit G, Erman M, Wang-Weigand S et al. Evaluation of the efficacy and safety of ramelteon in subjects with chronic insomnia. J Clin Sleep Med 2007;3:495-504.
114. Roth T, Rogowski R, Hull S et al. Efficacy and safety of doxepin 1 mg, 3 mg, and 6 mg in adults with primary insomnia. Sleep 2007;30:1555-61.
115. Hajak G, Rodenbeck A, Voderholzer U et al. Doxepin in the treatment of primary insomnia: a placebo-controlled, double blind, polysomnograph-ic study. J Clin Psychiatry 2001;62:453-63.
116. Lankford A, Rogowski R, Essink B et al. Efficacy and safety of doxepin 6 mg in a four-week outpatient trial of elderly adults with chronic primary insomnia. Sleep Med 2012;13:133-8.
117. Krystal AD, Lankford A, Durrence HH et al. Efficacy and safety of doxepin 3 and 6 mg in a 35-day sleep laboratory trial in adults with chronic pri-mary insomnia. Sleep 2011;34:1433-42.118. Herring WJ, Connor KM, Ivgy-May N et al. Suvorexant in patients with in-somnia: results from two 3-month randomized controlled clinical trials. Biol Psychiatry 2016;79:136-48.
119. Herring WJ, Snyder E, Budd K et al. Orexin receptor antagonism for treat-ment of insomnia: a randomized clinical trial of suvorexant. Neurology 2012;79:2265-74.
120. Michelson D, Snyder E, Paradis E et al. Safety and efficacy of suvorexant during 1-year treatment of insomnia with subsequent abrupt treatment discontinuation: a phase 3 randomised, double-blind, placebo-controlled trial. Lancet Neurol 2014;13:461-71.
121. Elie R, Frenay M, Le Morvan P et al. Efficacy and safety of zopiclone and triazolam in the treatment of geriatric insomniacs. Int Clin Psychophar-macol 1990;5(Suppl. 2):39-46.
122. Reeves RL. Comparison of triazolam, flurazepam, and placebo as hypnotics in geriatric patients with insomnia. J Clin Pharmacol 1977;17:319-23.
123. Piccione P, Zorick F, Lutz T et al. The efficacy of triazolam and chloral hydrate in geriatric insomniacs. J Int Med Res 1980;8:361-7.
124. Sunshine A. Comparison of the hypnotic activity of triazolam, flurazepam hydrochloride, and placebo. Clin Pharmacol Ther 1975;17:573-7.
125. Roehrs T, Zorick F, Wittig R et al. Efficacy of a reduced triazolam dose in elderly insomniacs. Neurobiol Aging 1985;6:293-6.
126. Morin CM, Colecchi C, Stone J et al. Behavioral and pharmacological therapies for late-life insomnia: a randomized controlled trial. JAMA 1999;281:991-9.
127. Ancoli-Israel S, Walsh JK, Mangano RM et al. Zaleplon, a novel nonbenzodiazepine hypnotic, effectively treats insomnia in elderly patients without caus-ing rebound effects. Prim Care Companion J Clin Psychiatry 1999;1:114-20.
128. Walsh JK, Soubrane C, Roth T. Efficacy and safety of zolpidem extended release in elderly primary insomnia patients. Am J Geriatr Psychiatry 2008;16:44-57.
129. Hedner J, Yaeche R, Emilien G et al. Zaleplon shortens subjective sleep latency and improves subjective sleep quality in elderly patients with in-somnia. The Zaleplon Clinical Investigator Study Group. Int J Geriatr Psy-chiatry 2000;15:704-12.
130. Scharf M, Erman M, Rosenberg R et al. A 2-week efficacy and safety study of eszopiclone in elderly patients with primary insomnia. Sleep 2005;28:720-7.
131. McCall WV, Erman M, Krystal AD et al. A polysomnography study of eszopiclone in elderly patients with insomnia. Curr Med Res Opin 2006;22:1633-42.
132. Ancoli-Israel S, Krystal AD, McCall WV et al. A 12-week, randomized, double-blind, placebo-controlled study evaluating the effect of eszopiclone 2 mg on sleep/wake function in older adults with primary and comorbid insomnia. Sleep 2010;33:225-34.
133. Roth T, Seiden D, Wang-Weigand S et al. A 2-night, 3-period, crossover study of ramelteon’s efficacy and safety in older adults with chronic in-somnia. Curr Med Res Opin 2007;23:1005-14.
134. Roth T, Seiden D, Sainati S et al. Effects of ramelteon on patient-reported sleep latency in older adults with chronic insomnia. Sleep Med 2006;7:312-8.
135. Scharf M, Rogowski R, Hull S et al. Efficacy and safety of doxepin 1 mg, 3 mg, and 6 mg in elderly patients with primary insomnia: a randomized, double-blind, placebo-controlled crossover study. J Clin Psychiatry 2008;69:1557-64.
136. Krystal AD, Durrence HH, Scharf M et al. Efficacy and safety of doxepin 1 mg and 3 mg in a 12-week sleep laboratory and outpatient trial of elderly subjects with chronic primary insomnia. Sleep 2010;33:1553-61.
137. Herring WJ, Connor KM, Snyder E et al. Suvorexant in elderly patients with insomnia: pooled analyses of data from phase III randomized con-trolled clinical trials. Am J Geriatr Psychiatry 2017;25:791-802.
138. Downing SS, Lee YT, Farb DH et al. Benzodiazepine modulation of partial agonist efficacy and spontaneously active GABA receptors supports an al-losteric model of modulation. Br J Pharmacol 2005;145:894-906.
139. Katzung BG, Masters SB, Trevor AJ. Basic and clinical pharmacology. New York: McGraw-Hill Medical, 2009.
140. Sieghart W, Sperk G. Subunit composition, distribution and function of GABA(A) receptor subtypes, Curr Top Med Chem 2002;2:795-816.
141. Krogsgaard-Larsen P, Frolund B, Liljefors T. Specific GABA(A) agonists and partial agonists. Chem Rec 2002;2:419-30.
142. Morin CM, Drake CL, Harvey AG et al. Insomnia disorder. Nat Rev Dis Primers 2015;1:15026
143. National Institutes of Health. Consensus conference. Drugs and insomnia. The use of medications to promote sleep. JAMA 1984;251:2410-4.
144. Krystal AD, McCall WV, Fava M et al. Eszopiclone treatment for insomnia: effect size comparisons in patients with primary insomnia and insomnia with medical and psychiatric comorbidity. Prim Care Companion CNS Disord 2012;14(4).
145. Pollack MH, Hoge EA, Worthington JJ et al. Eszopiclone for the treatment of posttraumatic stress disorder and associated insomnia: a randomized, double-blind, placebo-controlled trial. J Clin Psychiatry 2011;72:892-7.
146. Pollack M, Kinrys G, Krystal A et al. Eszopiclone coadministered with escitalopram in patients with insomnia and comorbid generalized anxi-ety disorder. Arch Gen Psychiatry 2008;65:551-62.
147. Goforth HW, Preud’homme XA, Krystal AD. A randomized, double-blind, placebo-controlled trial of eszopiclone for the treatment of insomnia in patients with chronic low back pain. Sleep 2014;37:1053-60.
148. Krystal A, Fava M, Rubens R et al. Evaluation of eszopiclone discontinuation after cotherapy with fluoxetine for insomnia with coexisting depres-sion. J Clin Sleep Med 2007;3:48-55.
149. Fava M, McCall WV, Krystal A et al. Eszopiclone co-administered with fluoxetine in patients with insomnia coexisting with major depressive dis-order. Biol Psychiatry 2006;59:1052-60.
150. Fava M, Asnis GM, Shrivastava RK et al. Improved insomnia symptoms and sleep-related next-day functioning in patients with comorbid major depressive disorder and insomnia following concomitant zolpidem ex-tended-release 12.5 mg and escitalopram treatment: a randomized con-trolled trial. J Clin Psychiatry 2011;72:914-28.
151. Fava M, Asnis GM, Shrivastava R et al. Zolpidem extended-release improves sleep and next-day symptoms in comorbid insomnia and general-ized anxiety disorder. J Clin Psychopharmacol 2009;29:222-30.
152. Ng KY, Leong MK, Liang H et al. Melatonin receptors: distribution in mammalian brain and their respective putative functions. Brain Struct Funct 2017;222:2921-39.
153. Krystal A. The possibility of preventing functional impairment due to sleep loss by pharmacologically enhancing sleep. Sleep 2005;28:16-7.
154. Slotten H, Krekling S. Does melatonin have an effect on cognitive performance. Psychoneuroendocrinology 1996;21:673-80.
155. Hughes R, Badia P. Sleep-promoting and hypothermic effects of daytime melatonin administration in humans. Sleep 1997;20:124-31.
156. Ferracioli-Oda E, Qawasmi A, Bloch MH. Meta-analysis: melatonin for the treatment of primary sleep disorders. PLoS One 2013;8:e63773.
157. Buscemi N, Vandermeer B, Hooton N et al. The efficacy and safety of exogenous melatonin for primary sleep disorders. A meta-analysis. J Gen Intern Med 2005;20:1151-8.
158. Smits M, Nagtegaal EE, van der Heijden J et al. Melatonin for chronic sleep onset insomnia in children: a randomized placebo-controlled trial. J Child Neurol 2001;16:86-92.
159. Zhdanova I, Wurtman RJ, Morabito C et al. Effects of low oral doses of melatonin, given 2-4 hours before habitual bedtime, on sleep in normal young humans. Sleep 1996;19:423-31.
160. Zhdanova I, Wurtman RJ, Wagstaff J. Effects of a low dose of melatonin on sleep in children with Angelman syndrome. J Pediatr Endocrinol 1999;12:57-67.
161. Van der Heijden K, Smits MG, Van Someren EJ et al. Effect of melatonin on sleep, behavior, and cognition in ADHD and chronic sleep-onset insom-nia. J Am Acad Child Adolesc Psychiatry 2007;46:
233-41.
162. Wasdell M, Jan JE, Bomben MM et al. A randomized, placebo-controlled trial of controlled release melatonin treatment of delayed sleep phase syn-drome and impaired sleep maintenance in children with neurodevelopmental disabilities. J Pineal Res 2008;44:57-64.
163. Braam W, Didden R, Smits M et al. Melatonin treatment in individuals with intellectual disability and chronic insomnia: a randomized placebo-controlled study. J Intellect Disabil Res 2008;52:256-64.
164. Lerchl A. Melatonin administration alters semen quality in normal men. J Androl 2004;25:185-6.
165. Ianas O, Manda D, Câmpean D et al. Effects of melatonin and its relation to the hypothalamic-hypophyseal-gonadal axis. Adv Exp Med Biol 1999;460:321-8.
166. Partonen T. Melatonin-dependent infertility. Med Hypotheses 1999;52:269-70.
167. Pang SF, Li L, Ayre EA et al. Neuroendocrinology of melatonin in repro-duction: recent developments. J Chem Neuroanat 1998;14:
157-66.
168. Krystal AD, Richelson E, Roth T. Review of the histamine system and the clinical effects of H1 antagonists: basis for a new model for understanding the effects of insomnia medications. Sleep Med Rev 2013;17:263-72.
169. Ruwe F, IJzerman-Boon P, Roth T et al. A phase 2 randomized dose-finding study with esmirtazapine in patients with primary insomnia. J Clin Psychopharmacol 2016;36:457-64.
170. Ivgy-May N, Ruwe F, Krystal A et al. Esmirtazapine in non-elderly adult patients with primary insomnia: efficacy and safety from a randomized, 6-week sleep laboratory trial. Sleep Med 2015;16:838-44.
171. Ivgy-May N, Roth T, Ruwe F et al. Esmirtazapine in non-elderly adult patients with primary insomnia: efficacy and safety from a 2-week rand-omized outpatient trial. Sleep Med 2015;16:831-7.
172. Suppes T, Kelly DI, Perla JM et al. Challenges in the management of bipolar depression. J Clin Psychiatry 2005;66(Suppl. 5):11-6.
173. Chakravorty S, Hanlon AL, Kuna ST et al. The effects of quetiapine on sleep in recovering alcohol-dependent subjects: a pilot study. J Clin Psy-chopharmacol 2014;34:350-4.
174. Tassniyom K, Paholpak S, Tassniyom S et al. Quetiapine for primary insomnia: a double blind, randomized controlled trial. J Med Assoc Thai 2010;93:729-34.
175. Glass JR, Sproule BA, Herrmann N et al. Effects of 2-week treatment with temazepam and diphenhydramine in elderly insomniacs: a randomized, placebo-controlled trial. J Clin Psychopharmacol 2008;28:182-8.
176. Morin CM, Koetter U, Bastien C et al. Valerian-hops combination and diphenhydramine for treating insomnia: a randomized placebo-controlled clinical trial. Sleep 2005;28:1465-71.
177. Koppel C, Tenczer J, Ibe K. Poisoning with over-the-counter doxylamine preparations: an evaluation of 109 cases. Hum Toxicol 1987;6:355-9.
178. Rose M, Kam CA. Gabapentin: pharmacology and its use in pain management. Anaesthesia 2002;57:451-62.
179. Gajraj N. Pregabalin: its pharmacology and use in pain management. Anesth Analg 2007;105:1805-15.
180. Furey SA, Hull SG, Leibowitz MT et al. A randomized, double-blind, placebo-controlled, multicenter, 28-day, polysomnographic study of gaba-pentin in transient insomnia induced by sleep phase advance. J Clin Sleep Med 2014;10:1101-9.
181. Rosenberg RP, Hull SG, Lankford DA et al. A randomized, double-blind, single-dose, placebo-controlled, multicenter, polysomnographic study of gabapentin in transient insomnia induced by sleep phase advance. J Clin Sleep Med 2014;10:1093-100.
182. Gilron I. Gabapentin and pregabalin for chronic neuropathic and early postsurgical pain: current evidence and future directions. Curr Opin An-aesthesiol 2007;20:456-72.
183. de Haas S, Otte A, de Weerd A et al. Exploratory polysomnographic evaluation of pregabalin on sleep disturbance in patients with epilepsy. J Clin Sleep Med 2007;3:473-8.
184. Garcia-Borreguero D, Larrosa O, de la Llave Y et al. Treatment of restless legs syndrome with gabapentin: a double-blind, cross-over study. Neurol-ogy 2002;59:1573-9.
185. Holsboer-Trachsler E, Prieto R. Effects of pregabalin on sleep in generalized anxiety disorder. Int J Neuropsychopharmacol 2013;16:925-36.
186. Guay D. Pregabalin in neuropathic pain: a more “pharmaceutically elegant” gabapentin? Am J Geriatr Pharmacother 2005;3:274-87.
187. Brower K, Myra Kim H, Strobbe S et al. A randomized double-blind pilot trial of gabapentin versus placebo to treat alcohol dependence and co-morbid insomnia. Alcohol Clin Exp Res 2008;32:1429-38.
188. Voris J, Smith NL, Rao SM et al. Gabapentin for the treatment of ethanol withdrawal. Subst Abus 2003;24:129-32.


