Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№03 2009
Факторы риска обменных нарушений у больных шизофренией №03 2009
Номера страниц в выпуске:13-17
С целью изучения связи обменных нарушений с особенностями клинической картины шизофрении и образом жизни больных обследованы 163 больных с параноидной шизофренией (81 мужчина и 82 женщины), госпитализированных в одну из психиатрических больниц Санкт-Петербурга. Полученные данные оценивали с использованием методов корреляционных плеяд и логистической регрессии. Связи с длительностью заболевания и продолжительностью антипсихотической терапии не выявлено. Предполагается, что высокая частота метаболических расстройств у больных шизофренией обусловлена особенностями обмена веществ, существовавшими у больных еще до появления отчетливой симптоматики шизофрении.
Резюме. С целью изучения связи обменных нарушений с особенностями клинической картины шизофрении и образом жизни больных обследованы 163 больных с параноидной шизофренией (81 мужчина и 82 женщины), госпитализированных в одну из психиатрических больниц Санкт-Петербурга. Средний возраст мужчин составил 39 лет, женщин – 45,1 года. Средняя длительность заболевания – 12,7±11,1 года. Полученные данные оценивали с использованием методов корреляционных плеяд и логистической регрессии. Связи с длительностью заболевания и продолжительностью антипсихотической терапии не выявлено. Предполагается, что высокая частота метаболических расстройств у больных шизофренией обусловлена особенностями обмена веществ, существовавшими у больных еще до появления отчетливой симптоматики шизофрении.
Ключевые слова: шизофрения, метаболический синдром, сердечно-сосудистые заболевания, факторы риска, шизофрения.
Risk factors of metabolic syndrome in patients with schizophrenia
N.G.Neznanov1,2, I.A.Martynikhin2, N.A.Sokolian1, D.A.Tanyansky3
1St.-Petersburg Bekhterev Psychoneurological Research Institute; 2St.-Petersburg I.P.Pavlov State Medical
University; 3Institute of Experimental Medicine of the NorthWest Branch of the Russian Academy
of Medical Sciences
Summary. Schizophrenic patients have high risk of metabolic syndrome (MS). Our hypothesis was that three groups of factors may lead to this disorder: psychopathology of schizophrenia (stress, depression, apathy, unhealthy lifestyle et al.), effects of antipsychotic medications, potential association between pathogenesis of schizophrenia and metabolic disturbances. One hundred sixty three paranoid schizophrenia patients (81 men, 82 women) admitted to one of the Saint-Petersburg psychiatry hospital were examined. The average male age was 39 and female age – 45,1. The average schizophrenia duration was 12,7±11,1 (SD). There were no significant correlations between metabolic disturbances, schizophrenia clinical features and lifestyle. Neither duration of schizophrenia nor years of antipsychotic exposure were significant predictors of MS status. For this reason metabolic disturbances existing before manifestation of schizophrenia appear to have a key role in the association between schizophrenia and metabolic syndrome.
Key words: schizophrenia, metabolic syndrome, cardiovascular diseases, risk factors, schizophrenia.
Введение
Смертность от сердечно-сосудистых заболеваний среди пациентов с шизофренией значительно больше, чем среди психически здоровых [1, 2]. У больных шизофренией в США, Западной Европе, а теперь и в России обнаружена высокая частота метаболического синдрома (МС) [3–9] – важнейшего фактора риска сердечно-сосудистых катастроф и сахарного диабета (СД) типа 2. Поэтому изучение причин и механизмов развития метаболических расстройств у больных шизофренией представляется чрезвычайно важным для разработки мер снижения преждевременной смертности при этом психическом заболевании.
Задачей данного исследования было определение факторов, вызывающих нарушение обмена веществ у больных параноидной шизофренией, обследованных в одной из психиатрических больниц Санкт-Петербурга.
В качестве исходной рабочей гипотезы было выдвинуто предположение, что повышение риска метаболических расстройств среди больных шизофренией связано с влиянием нескольких групп факторов:
Методы
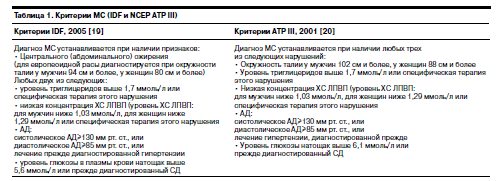
В исследование были включены пациенты (жители одного из районов Санкт-Петербурга), госпитализированные на момент обследования в городскую психиатрическую больницу по поводу параноидной шизофрении (диагноз установлен по критериям МКБ-10). С целью формирования выборки, наиболее точно соответствующей общей популяции больных шизофренией, использовали метод сплошного отбора. У всех пациентов натощак, после 12-часового воздержания от приема пищи, производили забор образцов венозной крови, измеряли АД, рост, массу тела, окружность талии. В день забора крови в клинико-диагностической лаборатории НИПНИ им. В.М.Бехтерева оценивали показатели глюкозы, триглицеридов, общего ХС, ХС липопротеидов высокой плотности (ХС ЛПВП) и липопротеидов низкой плотности (ХС ЛПНП) ферментативным методом на биохимическом анализаторе «Sapphire 400» (Япония) с использованием реагентов фирмы «RANDOX» (Великобритания). Оставшиеся образцы крови замораживали при температуре -20°C. В последующем иммуноферментным методом определяли концентрации аполипопротеинов А1 и В, кортизола, пролактина и инсулина. Уровни соматотропного гормона, дегидроэпиандростерон-сульфата (ДГЭА-С), фактора некроза опухоли a (ФНОa), интерлейкина (ИЛ) 1b, лептина, адипонектина, неэстерифицированных жирных кислот (НЭЖК) были определены только для первых 80 больных. Три последних параметра определяли в отделе биохимии НИИ экспериментальной медицины СЗО РАМН (руководитель – проф. А.Д.Денисенко). Оценивали коэффициент атерогенности [КА; КА = (общий ХС–ХС ЛПВП)/ХС ЛПВП], индекс массы тела [ИМТ; ИМТ = масса тела (кг)/рост2 (м2)], соотношение кортизола и ДГЭА-С (кортизол/ДГЭА-С) и индекс инсулинорезистентности HOMA-IR [HOMA-IR = глюкоза (ммоль/л) і инсулин (мкЕД/мл)/22,5]. МС диагностировали по критериям ATP III и IDF (табл. 1).
Всего в анализ включили 64 фактора. Перечень всех факторов и дефиниции факторов, определявшихся по собственным критериям, приведены в табл. 2.

Для определения взаимосвязей изучаемых факторов использовали метод корреляционных плеяд, при котором анализируются корреляции между всеми изучаемыми признаками с визуализацией выявленных связей на схеме. Для статистической обработки использовали метод ранговой корреляции Спирмена. Учитывая принцип множественных сравнений, значимыми считали связи с коэффициентом корреляции более 0,3 и статистической значимостью p<0,001. Факторы располагали на схеме таким образом, чтобы взаимосвязанные факторы были расположены друг к другу максимально близко. Факторы, имевшие меньшее количество разнонаправленных связей, таким образом, оказывались дальше от центра схемы. Факторы, не имевшие значимых связей с другими факторами, в схему не включали. Для анализа независимой значимости длительности шизофрении и длительности антипсихотической терапии, т.е. оценки вклада этих факторов в повышение риска развития МС, выполнен бинарный логистический регрессионный анализ с МС в качестве зависимой переменной, и полом, возрастом и длительностью шизофрении либо антипсихотической терапии – в качестве ковариат. Статистический анализ проведен с использованием программы SPSS 17.0.
Результаты
В соответствии с критериями включения для обследования первоначально был отобран 181 больной шизофренией (из них 12 отказались от обследования, 5 исключены в связи с недостаточно обоснованным диагнозом шизофрении по МКБ-10, данные еще 1 больной были исключены в связи с наличием у нее декомпенсированного СД типа 1). Итого в статистическую обработку были включены данные 163 больных (81 мужчина и 82 женщины). Средний возраст мужчин составил 39 лет, женщин – 45,1 года. Средняя длительность шизофрении – 12,7 года (SD 11,1). У 110 (67,5%) больных зарегистрировано непрерывное течение шизофрении, у остальных 53 (32,5%) – эпизодическое или эпизодическое с нарастающим дефектом. В течение 6 мес перед обследованием 81 (49,7%) пациент получал атипичные антипсихотики (в том числе клозапин – 41 больной, оланзапин – 14).
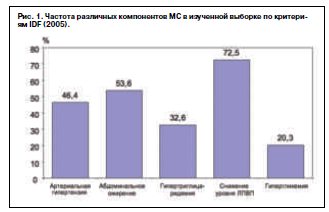
Частота МС по критериям NCEP ATP III cоставила 36,2% (среди мужчин – 27,2%, среди женщин – 45,1%), по критериям IDF – 38,0% (среди мужчин – 22,2%, среди женщин – 53,6%). Частоты выявления отдельных параметров МС по критериям IDF приведены на рис. 1. Средний ИМТ среди мужчин составил 23,6 кг/м2 (SD 3,66), а среди женщин – 24,9 кг/м2 (SD 5,03). При этом 41,6% от общего числа обследованных имели избыточную массу тела (ИМТ>25 кг/м2), ожирение различных степеней (ИМТ>30 кг/м2) – 8,5%.
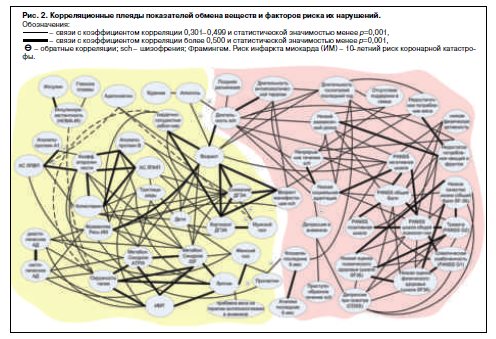
При построении корреляционных плеяд в схему было включено 54 фактора, остальные факторы не имели значимых связей. Корреляционные плеяды показателей обмена веществ и факторов риска их нарушений изображены на рис. 2. С факторами, большая часть связей с которыми были обратными, для облегчения восприятия схемы произведены обратные трансформации (например, физическая активность в снижение физической активности). Связи окружность талии – инсулинорезистентность (r=0,290, p=0,0008), окружность талии – сердечно-сосудистые заболевания (r=0,287, p=0,0003), адипонектин – ХС ЛПВП (r=0,344, p=0,0011), адипонектин – мужской пол (r=-0,290, p=0,0006) были включены в схему условно и обозначены пунктирной линией, так как их значения не достигали заданных условий, но были близки к ним.
По результатам логистического регрессионного анализа после включения в модель в качестве ковариат пола и возраста ни длительность шизофрении, ни длительность антипсихотической терапии не оказывали влияния на частоту МС.
Обсуждение
Приведенные корреляционные плеяды дают возможность взвешенно оценить всю совокупность связей метаболических показателей у больных шизофренией с параметрами, которые принято считать факторами риска обменных нарушений. При этом можно выделить следующие особенности, выявленные при построении плеяд.
1. Параметры метаболизма практически не имеют значимых связей с особенностями клинической картины шизофрении, социальным статусом, образом жизни и оценкой больными качества жизни. Ни длительность шизофрении, ни длительность приема антипсихотиков не выявили связи с наличием МС как при анализе плеяд, так и при регрессионном анализе с контролем по полу и возрасту. Так как эти параметры можно рассматривать в качестве критериев для интегральной оценки влияния психопатологической симптоматики шизофрении и антипсихотической терапии на обменные процессы, можно сделать предположение, что высокая частота метаболических расстройств у больных шизофренией, выявленная как в нашей работе, так и в зарубежных исследованиях, обусловлена особенностями обмена веществ, имеющимися у больных еще до появления отчетливой симптоматики шизофрении. Однако подтвердить или опровергнуть подобное предположение сможет лишь более детальное сопоставление обменных процессов у впервые заболевших больных шизофренией и психически здоровых лиц.
2. МС, диагностированный по современным международным критериям, у больных шизофренией не имел взаимосвязи с увеличением риска сердечно-сосудистых заболеваний. Таким образом, возможно, у этой категории больных он не выполняет ту прогностическую функцию, ради которой был разработан. Однако для подтверждения этого тезиса требуются дальнейшие проспективные исследования. Кроме того, связь МС с качеством жизни больных шизофрений в настоящем исследовании не подтвердилась.
3. Течение МС у пациентов с шизофренией имеет существенное отличие от общей популяции: отсутствует связь МС с инсулинорезистентностью, которая является ключевым механизмом патогенеза МС у психически здоровых людей. Наиболее сильные связи МС у больных шизофренией наблюдаются с ожирением, в том числе абдоминального фенотипа, и с гормоном жировой ткани лептином. Кроме того, МС имеет множественные связи с атерогенными липидами. Таким образом, высокая частота МС, выявленного у обследованных нами больных, отражает высокую частоту дислипидемий и абдоминального ожирения в обследованной выборке, но не инсулинорезистентность.
4. Концентрация ДГЭА-С и отношение кортизол/ДГЭА-С оказались в центре схемы за счет множества связей, имеющихся у них с большинством параметров липидного обмена и сердечно-сосудистыми заболеваниями. Известно, что ДГЭА-С оказывает нейропротективное и стресс-протективное действие, защищая организм от пагубного влияния повышенной секреции кортизола. Согласно недавнему исследованию [21] данные гормоны и их соотношение являются значимыми предикторами ответа на антипсихотическую терапию. Кроме того, отмечена их связь с тревогой и депрессией, когнитивными расстройствами и, по аналогии с нашими результатами, была выявлена связь этих показателей с возрастом манифестации шизофрении [21]. Не исключено, что в дальнейшем это позволит рекомендовать ДГЭА для применения в качестве средства вспомогательной терапии при шизофрении.
5. Выявлены значимые связи между характеристиками течения шизофрении, образом жизни и социально-экономическим статусом больных. Так, среди обследованных нами больных шизофренией курили 73% человек, а имели хотя бы какие-то физические нагрузки только 22% больных. Среди обследованных пациентов средний доход составил 3 тыс. руб. в месяц (цены 2008 г.). Снижение социального статуса в свою очередь приводит к значимым изменениям в рационе питания: 60% обследованных больных указало, что из-за недостатка денег хотя бы иногда ограничивают себя в употреблении мясных продуктов и сладостей, 54% – во фруктах, а 20% – даже в простой еде (хлеб, крупы).
6. В целом характеристики клиники и течения шизофрении, особенности психического статуса продемонстрировали закономерные и хорошо известные взаимосвязи друг с другом, что может свидетельствовать в пользу достаточной валидности всей схемы даже с учетом ее оценочного характера.
Ключевые слова: шизофрения, метаболический синдром, сердечно-сосудистые заболевания, факторы риска, шизофрения.
Risk factors of metabolic syndrome in patients with schizophrenia
N.G.Neznanov1,2, I.A.Martynikhin2, N.A.Sokolian1, D.A.Tanyansky3
1St.-Petersburg Bekhterev Psychoneurological Research Institute; 2St.-Petersburg I.P.Pavlov State Medical
University; 3Institute of Experimental Medicine of the NorthWest Branch of the Russian Academy
of Medical Sciences
Summary. Schizophrenic patients have high risk of metabolic syndrome (MS). Our hypothesis was that three groups of factors may lead to this disorder: psychopathology of schizophrenia (stress, depression, apathy, unhealthy lifestyle et al.), effects of antipsychotic medications, potential association between pathogenesis of schizophrenia and metabolic disturbances. One hundred sixty three paranoid schizophrenia patients (81 men, 82 women) admitted to one of the Saint-Petersburg psychiatry hospital were examined. The average male age was 39 and female age – 45,1. The average schizophrenia duration was 12,7±11,1 (SD). There were no significant correlations between metabolic disturbances, schizophrenia clinical features and lifestyle. Neither duration of schizophrenia nor years of antipsychotic exposure were significant predictors of MS status. For this reason metabolic disturbances existing before manifestation of schizophrenia appear to have a key role in the association between schizophrenia and metabolic syndrome.
Key words: schizophrenia, metabolic syndrome, cardiovascular diseases, risk factors, schizophrenia.
Введение
Смертность от сердечно-сосудистых заболеваний среди пациентов с шизофренией значительно больше, чем среди психически здоровых [1, 2]. У больных шизофренией в США, Западной Европе, а теперь и в России обнаружена высокая частота метаболического синдрома (МС) [3–9] – важнейшего фактора риска сердечно-сосудистых катастроф и сахарного диабета (СД) типа 2. Поэтому изучение причин и механизмов развития метаболических расстройств у больных шизофренией представляется чрезвычайно важным для разработки мер снижения преждевременной смертности при этом психическом заболевании.
Задачей данного исследования было определение факторов, вызывающих нарушение обмена веществ у больных параноидной шизофренией, обследованных в одной из психиатрических больниц Санкт-Петербурга.
В качестве исходной рабочей гипотезы было выдвинуто предположение, что повышение риска метаболических расстройств среди больных шизофренией связано с влиянием нескольких групп факторов:
1. Прямое и опосредованное влияние психопатологических факторов. Больные шизофренией испытывают значимый стресс как от реальных воздействий (неблагоприятные жизненные события, факт наличия заболевания, трудности социальной адаптации и пр.), так и от «псевдострессоров» (переживания, обусловленные бредом и галлюцинациями). У страдающих шизофренией часто выявляются депрессивные расстройства, связь которых с сердечно-сосудистыми заболеваниями в настоящее время широко обсуждается в кардиологии. Известно, что стресс и депрессия приводят к повышенной активности гипоталамо-гипофизарно-надпочечниковой оси и длительной гиперкортизолемии, что в свою очередь способствует развитию абдоминального ожирения, инсулинорезистентности и повышению артериального давления (АД).Выявляемые при шизофрении эмоционально-волевые расстройства (в частности, апатия) могут, хотя и косвенно, способствовать формированию нездорового образа жизни с гипокинезией, нерациональным питанием, отсутствием заботы о своем здоровье. Отдельную роль играют несбалансированное питание и материально-бытовые условия жизни больных. По данным европейских исследований, страдающие шизофренией чаще здоровых употребляют в пищу жиры и реже – растительную клетчатку [10]. Это объясняют более низким уровнем жизни пациентов. Однако в нашей стране образ и условия жизни многих психически больных в большей мере связаны с недостатком питания, чем с употреблением относительно дорогого и высококалорийного фаст-фуда, поэтому они могут стать факторами, снижающими риск ожирения и обменных нарушений. Длительные госпитализации в психиатрические стационары также способны вносить определенные коррективы в образ жизни больных, поскольку могут быть обусловлены более низкой физической активностью и менее калорийным питанием. Прежде в исследованиях метаболических нарушений у больных шизофренией не учитывался тип течения заболевания, длительность госпитализаций, наличие депрессивных расстройств в анамнезе, экономический статус и характер питания больных. При этом выраженность симптоматики шизофрении на момент обследования не выявляла связи с МС [11]. И хотя в одном из исследований было продемонстрировано повышение частоты нарушений обмена веществ с увеличением длительности заболевания [6], эту связь еще нельзя считать установленной, так как длительность шизофрении увеличивается вместе с возрастом – главным фактором риска кардиометаболических расстройств.
2. Влияние антипсихотической терапии. Больные шизофренией нуждаются в длительном приеме антипсихотиков. Препараты этой группы способны значимо влиять на обменные процессы в организме больного. В большом числе проспективных исследований показано, что антипсихотики воздействуют практически на все компоненты МС: способствуют повышению массы тела, уровня в крови глюкозы, холестерина (ХС) и триглицеридов [12]. При этом значительно большее влияние на обмен веществ оказывают атипичные антипсихотики, в особенности клозапин и оланзапин [13], механизм которого пока недостаточно ясен, хотя обсуждается роль развития инсулино- и лептинорезистентности. Кроме того, пока достоверно не изучены отдаленные последствия антипсихотической терапии (в частности, в исследовании CATIE связь между МС и длительностью предшествующей антипсихотической терапии не выявлена [11]).Предметом изучения в нашей работе стала значительная часть перечисленных выше факторов наряду с биохимическими показателями, прямо или опосредованно связанными с обменными нарушениями. Для анализа неблагоприятных последствий, к которым могут приводить метаболические расстройства, изучалась их связь с сердечно-сосудистыми заболеваниями и качеством жизни больных.
3. Возможное единство патогенетических механизмов обменных нарушений и шизофрении. Предполагать наличие такой взаимосвязи позволяют данные о широкой распространенности нарушений обмена веществ у «первичных» пациентов, недавно заболевших шизофренией [14, 15], высоком семейном отягощении нарушениями обмена веществ и СД при шизофрении у пробанда [16], а также сведения о значимом и устойчивом снижении уровня аполипопротеина А1 у этих пациентов [17, 18].
Методы
В исследование были включены пациенты (жители одного из районов Санкт-Петербурга), госпитализированные на момент обследования в городскую психиатрическую больницу по поводу параноидной шизофрении (диагноз установлен по критериям МКБ-10). С целью формирования выборки, наиболее точно соответствующей общей популяции больных шизофренией, использовали метод сплошного отбора. У всех пациентов натощак, после 12-часового воздержания от приема пищи, производили забор образцов венозной крови, измеряли АД, рост, массу тела, окружность талии. В день забора крови в клинико-диагностической лаборатории НИПНИ им. В.М.Бехтерева оценивали показатели глюкозы, триглицеридов, общего ХС, ХС липопротеидов высокой плотности (ХС ЛПВП) и липопротеидов низкой плотности (ХС ЛПНП) ферментативным методом на биохимическом анализаторе «Sapphire 400» (Япония) с использованием реагентов фирмы «RANDOX» (Великобритания). Оставшиеся образцы крови замораживали при температуре -20°C. В последующем иммуноферментным методом определяли концентрации аполипопротеинов А1 и В, кортизола, пролактина и инсулина. Уровни соматотропного гормона, дегидроэпиандростерон-сульфата (ДГЭА-С), фактора некроза опухоли a (ФНОa), интерлейкина (ИЛ) 1b, лептина, адипонектина, неэстерифицированных жирных кислот (НЭЖК) были определены только для первых 80 больных. Три последних параметра определяли в отделе биохимии НИИ экспериментальной медицины СЗО РАМН (руководитель – проф. А.Д.Денисенко). Оценивали коэффициент атерогенности [КА; КА = (общий ХС–ХС ЛПВП)/ХС ЛПВП], индекс массы тела [ИМТ; ИМТ = масса тела (кг)/рост2 (м2)], соотношение кортизола и ДГЭА-С (кортизол/ДГЭА-С) и индекс инсулинорезистентности HOMA-IR [HOMA-IR = глюкоза (ммоль/л) і инсулин (мкЕД/мл)/22,5]. МС диагностировали по критериям ATP III и IDF (табл. 1).

Всего в анализ включили 64 фактора. Перечень всех факторов и дефиниции факторов, определявшихся по собственным критериям, приведены в табл. 2.

Для определения взаимосвязей изучаемых факторов использовали метод корреляционных плеяд, при котором анализируются корреляции между всеми изучаемыми признаками с визуализацией выявленных связей на схеме. Для статистической обработки использовали метод ранговой корреляции Спирмена. Учитывая принцип множественных сравнений, значимыми считали связи с коэффициентом корреляции более 0,3 и статистической значимостью p<0,001. Факторы располагали на схеме таким образом, чтобы взаимосвязанные факторы были расположены друг к другу максимально близко. Факторы, имевшие меньшее количество разнонаправленных связей, таким образом, оказывались дальше от центра схемы. Факторы, не имевшие значимых связей с другими факторами, в схему не включали. Для анализа независимой значимости длительности шизофрении и длительности антипсихотической терапии, т.е. оценки вклада этих факторов в повышение риска развития МС, выполнен бинарный логистический регрессионный анализ с МС в качестве зависимой переменной, и полом, возрастом и длительностью шизофрении либо антипсихотической терапии – в качестве ковариат. Статистический анализ проведен с использованием программы SPSS 17.0.
Результаты
В соответствии с критериями включения для обследования первоначально был отобран 181 больной шизофренией (из них 12 отказались от обследования, 5 исключены в связи с недостаточно обоснованным диагнозом шизофрении по МКБ-10, данные еще 1 больной были исключены в связи с наличием у нее декомпенсированного СД типа 1). Итого в статистическую обработку были включены данные 163 больных (81 мужчина и 82 женщины). Средний возраст мужчин составил 39 лет, женщин – 45,1 года. Средняя длительность шизофрении – 12,7 года (SD 11,1). У 110 (67,5%) больных зарегистрировано непрерывное течение шизофрении, у остальных 53 (32,5%) – эпизодическое или эпизодическое с нарастающим дефектом. В течение 6 мес перед обследованием 81 (49,7%) пациент получал атипичные антипсихотики (в том числе клозапин – 41 больной, оланзапин – 14).

Частота МС по критериям NCEP ATP III cоставила 36,2% (среди мужчин – 27,2%, среди женщин – 45,1%), по критериям IDF – 38,0% (среди мужчин – 22,2%, среди женщин – 53,6%). Частоты выявления отдельных параметров МС по критериям IDF приведены на рис. 1. Средний ИМТ среди мужчин составил 23,6 кг/м2 (SD 3,66), а среди женщин – 24,9 кг/м2 (SD 5,03). При этом 41,6% от общего числа обследованных имели избыточную массу тела (ИМТ>25 кг/м2), ожирение различных степеней (ИМТ>30 кг/м2) – 8,5%.
При построении корреляционных плеяд в схему было включено 54 фактора, остальные факторы не имели значимых связей. Корреляционные плеяды показателей обмена веществ и факторов риска их нарушений изображены на рис. 2. С факторами, большая часть связей с которыми были обратными, для облегчения восприятия схемы произведены обратные трансформации (например, физическая активность в снижение физической активности). Связи окружность талии – инсулинорезистентность (r=0,290, p=0,0008), окружность талии – сердечно-сосудистые заболевания (r=0,287, p=0,0003), адипонектин – ХС ЛПВП (r=0,344, p=0,0011), адипонектин – мужской пол (r=-0,290, p=0,0006) были включены в схему условно и обозначены пунктирной линией, так как их значения не достигали заданных условий, но были близки к ним.

По результатам логистического регрессионного анализа после включения в модель в качестве ковариат пола и возраста ни длительность шизофрении, ни длительность антипсихотической терапии не оказывали влияния на частоту МС.
Обсуждение
Приведенные корреляционные плеяды дают возможность взвешенно оценить всю совокупность связей метаболических показателей у больных шизофренией с параметрами, которые принято считать факторами риска обменных нарушений. При этом можно выделить следующие особенности, выявленные при построении плеяд.
1. Параметры метаболизма практически не имеют значимых связей с особенностями клинической картины шизофрении, социальным статусом, образом жизни и оценкой больными качества жизни. Ни длительность шизофрении, ни длительность приема антипсихотиков не выявили связи с наличием МС как при анализе плеяд, так и при регрессионном анализе с контролем по полу и возрасту. Так как эти параметры можно рассматривать в качестве критериев для интегральной оценки влияния психопатологической симптоматики шизофрении и антипсихотической терапии на обменные процессы, можно сделать предположение, что высокая частота метаболических расстройств у больных шизофренией, выявленная как в нашей работе, так и в зарубежных исследованиях, обусловлена особенностями обмена веществ, имеющимися у больных еще до появления отчетливой симптоматики шизофрении. Однако подтвердить или опровергнуть подобное предположение сможет лишь более детальное сопоставление обменных процессов у впервые заболевших больных шизофренией и психически здоровых лиц.
2. МС, диагностированный по современным международным критериям, у больных шизофренией не имел взаимосвязи с увеличением риска сердечно-сосудистых заболеваний. Таким образом, возможно, у этой категории больных он не выполняет ту прогностическую функцию, ради которой был разработан. Однако для подтверждения этого тезиса требуются дальнейшие проспективные исследования. Кроме того, связь МС с качеством жизни больных шизофрений в настоящем исследовании не подтвердилась.
3. Течение МС у пациентов с шизофренией имеет существенное отличие от общей популяции: отсутствует связь МС с инсулинорезистентностью, которая является ключевым механизмом патогенеза МС у психически здоровых людей. Наиболее сильные связи МС у больных шизофренией наблюдаются с ожирением, в том числе абдоминального фенотипа, и с гормоном жировой ткани лептином. Кроме того, МС имеет множественные связи с атерогенными липидами. Таким образом, высокая частота МС, выявленного у обследованных нами больных, отражает высокую частоту дислипидемий и абдоминального ожирения в обследованной выборке, но не инсулинорезистентность.
4. Концентрация ДГЭА-С и отношение кортизол/ДГЭА-С оказались в центре схемы за счет множества связей, имеющихся у них с большинством параметров липидного обмена и сердечно-сосудистыми заболеваниями. Известно, что ДГЭА-С оказывает нейропротективное и стресс-протективное действие, защищая организм от пагубного влияния повышенной секреции кортизола. Согласно недавнему исследованию [21] данные гормоны и их соотношение являются значимыми предикторами ответа на антипсихотическую терапию. Кроме того, отмечена их связь с тревогой и депрессией, когнитивными расстройствами и, по аналогии с нашими результатами, была выявлена связь этих показателей с возрастом манифестации шизофрении [21]. Не исключено, что в дальнейшем это позволит рекомендовать ДГЭА для применения в качестве средства вспомогательной терапии при шизофрении.
5. Выявлены значимые связи между характеристиками течения шизофрении, образом жизни и социально-экономическим статусом больных. Так, среди обследованных нами больных шизофренией курили 73% человек, а имели хотя бы какие-то физические нагрузки только 22% больных. Среди обследованных пациентов средний доход составил 3 тыс. руб. в месяц (цены 2008 г.). Снижение социального статуса в свою очередь приводит к значимым изменениям в рационе питания: 60% обследованных больных указало, что из-за недостатка денег хотя бы иногда ограничивают себя в употреблении мясных продуктов и сладостей, 54% – во фруктах, а 20% – даже в простой еде (хлеб, крупы).
6. В целом характеристики клиники и течения шизофрении, особенности психического статуса продемонстрировали закономерные и хорошо известные взаимосвязи друг с другом, что может свидетельствовать в пользу достаточной валидности всей схемы даже с учетом ее оценочного характера.
Список исп. литературыСкрыть список1. Brown S. Excess mortality of schizophrenia: a meta-analysis. Brit J Psychiat 1997; 171: 502–8.
2. Osby U, Correia N, Brandt L et al. Mortality and causes of death in schizophrenia in Stockholm county, Sweden. 2000; 45 (1–2): 21–8.
3. McEvoy J, Meyer J, Goff D et al. Prevalence of the metabolic syndrome in patients with schizophrenia: baseline results from the Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE) schizophrenia trial and comparison with national estimates from NHANES III. Schizophrenia Res 2005; 80 (1): 19–32.
4. Heiskanen T, Niskanen L, Lyytikainen R et al Metabolic syndrome in patients with schizophrenia. J Clin Psychiat 2003; 64: 575–9.
5. Cohn T, Prud’homme D, Streiner D et al. Characterizing Coronary Heart Disease Risk in Chronic Schizophrenia: High Prevalence of the Metabolic Syndrome. Can J Psychiat 2004; 49: 753–60.
6. De Hert M, van Winkel R, Van Eyck D et al. Prevalence of diabetes, metabolic syndrome and metabolic abnormalities in schizophrenia over the course of the illness: a cross-sectional study. Clin Pract Epidemol Ment Health 2006; 27: 14.
7. Капилетти С.Г., Мосолов С.Н., Шафаренко А.А. Частота метаболических расстройств у больных шизофренией, получающих антипсихотическую терапию. Материалы Общероссийской конференции Реализация подпрограммы «Психические расстройства» Федеральной целевой программы «Предупреждение и борьба с социально-значимыми заболеваниями (2007–2011)» Москва 28–30 октября 2008. М., 2008; с. 414–6.
8. Незнанов Н.Г., Мартынихин И.А., Соколян Н.А. Распространенность метаболического синдрома среди госпитализированных больных параноидной формой шизофрении в Санкт-Петербурге. Тезисы научно-практической конференции «Актуальные проблемы оказания психиатрической помощи в Северо-Западном регионе Российской Федерации». СПб., 2008; с. 147–8.
9. Незнанов Н.Г., Мартынихин И.А., Соколян Н.А Частота и характер метаболических нарушений у больных шизофренией. Обозр. психиат. и мед. психол. им. В.М.Бехтерева. 2009; 2: 17–20.
10. Brown S, Birtwistle J, Roe L et al. The unhealthy lifestyle of people with schizophrenia. Psycholog Med 1999; 29: 697–701.
11. Meyer JM, Nasrallah HA, McEvoy JP et al The Clinical Antipsychotic Trials Of Intervention Effectiveness (CATIE) Schizophrenia Trial: clinical comparison of subgroups with and without the metabolic syndrome. 2005; 80 (1): 9–18.
12. American Diabetes Association, American Psychiatric Association, American Association of Clinical Endocrinologists, North American Association for the Study of Obesity. Consensus development conference on antipsychotic drugs and obesity and diabetes. J Clin Psychiat 2004; 65: 267–72.
13. Newcomer JW, Nasrallah HA, Loebel AD. The atypical antipsychotic therapy and metabolic issues national survey: practice patterns and knowledge of psychiatrists. J Clin Psychopharmacol 2004; 24 (5 suppl. 1): S1–6.
14. Ryan MCM, Collins P, Thakore JH. Impaired fasting glucose tolerance in first-episode, drug naive patients with schizophrenia. Am J Psychiat 2003; 160: 284–9.
15. Thakore JH, Vlahoos J, Martin A. Increased visceral fat distribution in drug-naive and drug-free patients with schizophrenia. Internat J Obes Related Metabol Disord 2002; 26: 137–41.
16. Bushe C, Holt R. Prevalence of diabetes and impaired glucose tolerance in patients with schizophrenia. Brit J Psychiat 2004; 18 4 (suppl. 4 7): s67–71.
17. La YJ, Wan CL, Zhu H et al. Decreased levels of apolipoprotein A-I in plasma of schizophrenic patients. J Neural Transm 2007; 114 (5): 657–63.
18. Huang J, Wang L, Prabakaran S et al. Independent protein-profiling studies show a decrease in apolipoprotein A1 levels in schizophrenia CSF, brain and peripheral tissues. Molecular Psychiatry advance online publication 16 October 2007; doi: 10.1038/sj.mp.4002108.
19. The IDF consensus worldwide definition of the metabolic syndrome. International Diabetes Federation, 2006, www.idf.org/metabolic_syndrome, website of the International Diabetes Federation.
20. Executive summary of the Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on detection, evaluation, and treatment of high blood cholesterol in adults (Adult Treatment Panel III). JAMA 2001; 285: 2486–97.
21. Ritsner M, Gibel A, Maayan R et al. State and trait related predictors of serum cortisol to DHEA(S) molar ratios and hormone concentrations in schizophrenia patients. Eur Neuropsychopharmacol 2007; 17 (4): 257–64.


