Психиатрия Психические расстройства в общей медицине
Психиатрия Психические расстройства в общей медицине
№04 2013
Тревожные расстройства и их коррекция в амбулаторной психиатрической практике №04 2013
Номера страниц в выпуске:35-40
Актуальность проблемы тревожных расстройств определяется их клинической гетерогенностью, тенденцией к затяжному течению и формированию коморбидных соотношений с депрессивной и соматоформной симптоматикой. По данным T.Strine и соавт., распространенность тревожных расстройств среди населения составляет 15%. Наиболее часто встречаются легкие или умеренно выраженные тревожные расстройства типа ситуационно обусловленных личностных реакций, нозогенные расстройства и генерализованное тревожное расстройство, что определяет преобладание таких пациентов в амбулаторной практике.
Резюме. Приведен анализ современных подходов к лечению тревожных расстройств, в том числе коморбидных с депрессией. Представлены результаты коррекции тревожных расстройств у больных психосоматического и наркологического профиля с применением анксиолитика нового поколения Афобазола. Показана эффективность препарата в отношении психической и соматической тревоги, диссомнии, депрессии невротического уровня. Продемонстрировано улучшение качества жизни больных на фоне лечения Афобазолом.
Ключевые слова: тревожные расстройства, терапия, психосоматика, наркология.
Anxiety disorders and their correction in outpatient psychiatric practice
N.N.Petrova
Department of Psychiatry and Addiction, Medical Faculty of St.-Petersburg State University
Summary. The analysis of modern approaches to treatment of anxiety disorders, including comorbid with depression was performed. The results of correction in patients with anxiety disorders and substance abuse psychosomatic profile using a new generation of anxiolytic Afobazol was shown. The drug demonstrated the effectiveness against the psychic and somatic anxiety, insomnia, neurotic depression, as well as improvement in the quality of life of patients with Afobazole therapy.
Key words: anxiety disorders, therapy, psychosomatic medicine, drug and alcohol abuse.
Актуальность проблемы тревожных расстройств определяется их клинической гетерогенностью, тенденцией к затяжному течению и формированию коморбидных соотношений с депрессивной и соматоформной симптоматикой [25, 27]. По данным T.Strine и соавт., распространенность тревожных расстройств среди населения составляет 15% [33]. Наиболее часто встречаются легкие или умеренно выраженные тревожные расстройства типа ситуационно обусловленных личностных реакций, нозогенные расстройства и генерализованное тревожное расстройство, что определяет преобладание таких пациентов в амбулаторной практике [32].
Необходимость оптимизации лечебных мероприятий обусловлена широкой распространенностью тревожных расстройств не только среди внебольничного контингента психиатрических пациентов, но и в других областях медицины.
Клинически тревожные расстройства проявляются психическими и соматическими (вегетативными) симптомами, важной отличительной чертой которых является полисистемность. В связи с этим значительное число пациентов, у которых преобладают соматовегетативные проявления тревоги, обращаются не к психиатрам (психотерапевтам), а к врачам-интернистам: терапевтам, кардиологам, гастроэнтерологам, пульмонологам, дерматологам, онкологам и другим специалистам [12, 31].
Психофармакотерапия тревожных расстройств представляется актуальной и достаточно непростой задачей. Основным методом коррекции тревожных расстройств является прием анксиолитических препаратов. Первыми использовавшимися человечеством средствами с анксиолитическим эффектом были алкоголь и опиаты. В ХIX в. начали применять бромиды, в XX в. – барбитураты и резерпин. С середины ХХ в. ведущее место в анксиолитической терапии занимают препараты бензодиазепинового ряда – транквилизаторы (от латинского слова «tranquillo» – успокаивать). Транквилизаторы определяют как лекарственные средства, подавляющие или способные уменьшать выраженность беспокойства, страха и напряженности.
Спектр действия данной группы психотропных препаратов достаточно широк благодаря быстрому развитию неспецифического тормозного ГАМКергического эффекта, за счет которого наступает миорелаксация, купируются судороги и спазмы, развиваются седативный и вегетостабилизирующий эффекты. Транквилизаторы эффективны при фобиях, способны редуцировать как психическую, так и соматическую тревогу. Этим обусловлено их широкое применение во многих областях медицины, в том числе в хирургической практике – для премедикации, в гинекологии – для лечения климактерических расстройств и предменструального синдрома, в психиатрии – при расстройствах адаптации, купировании ажитации и т.д. Однако, обладая выраженными противотревожными свойствами, большинство представителей группы бензодиазепинов вызывают чрезмерную седацию и миорелаксацию, а при длительном применении могут вызывать аддикцию.
Симптомы поведенческой токсичности (дневная сонливость, замедление когнитивных процессов, снижение остроты реакций, внимания и памяти) и риск злоупотребления бензодиазепиновыми транквилизаторами ограничивают возможности их применения в амбулаторной практике [4]. Кроме того, взаимодействие бензодиазепиновых анксиолитиков с некоторыми соматотропными препаратами (a-адреномиметиками, a- и b-адреноблокаторами, блокаторами кальциевых каналов, ингибиторами ангиотензинпревращающего фермента, производными метилксантина) в ряде случаев можно рассматривать как неблагоприятное. Так, при одновременном приеме лекарств бензодиазепинового ряда с клонидином (клофелином) и пропранололом отмечаются усиление гипотензивного эффекта, угнетающее действие на центральную нервную систему, рефлекторная тахикардия. Бензодиазепиновые анксиолитики усиливают адренолитическое действие фентоламина, тропафена, индорамина вплоть до развития тяжелой гипотензивной реакции, что создает трудности при использовании этих препаратов у соматических больных.
Транквилизаторы неэффективны при коморбидных тревожных и депрессивных расстройствах, которые широко распространены в современной клинической практике. В этих случаях целесообразно использовать антидепрессанты из группы селективных ингибиторов обратного захвата серотонина или селективных ингибиторов обратного захвата серотонина и норадреналина.
Опыт изучения транквилизаторов (диазепам, лоразепам, феназепам, клоназепам, оксазепам) позволил развить теорию нейрохимической регуляции тревоги и заложить основы терапии тревожных расстройств, в том числе субклинических форм, установить закономерности проявления фармакологических эффектов (анксиолитического, вегетостабилизирующего, гипноседативного, миорелаксирующего, регулирующего поведение). Дальнейшее развитие фармакотерапии движется по пути формирования селективности противотревожного действия. Результаты клинических исследований подтвердили необходимость создания препаратов, соответствующих по своим противотревожным свойствам бензодиазепиновым транквилизаторам, но свободных от присущих им нежелательных эффектов. Работы, проведенные под руководством академика С.Б.Середенина, позволили сформулировать фармакогенетическую концепцию анксиоселективности [16]. Авторами была показана зависимость преобладания седативного либо анксиолитического эффекта бензодиазепинов от генетически контролируемого фенотипа эмоционально-стрессовых реакций как у животных, так и у человека. Сравнение фенотипов эмоционально-стрессовых реакций: «активных» (стрессоустойчивых) и «пассивных» (стрессонеустойчивых) в стрессе инбредных животных позволило выявить нейрохимическую мишень анксиоселективного действия – падение бензодиазепиновой рецепции на фоне экспериментального стресса только у пассивных животных [17]. Наличие данного эффекта было подтверждено в клинике на добровольцах и у пациентов с реактивными состояниями. В ГУ НИИ фармакологии им. В.В.Закусова РАМН в процессе исследований, проводимых на протяжении более 15 лет, был найден регулятор бензодиазепинового связывания и осуществлен синтез оригинального селективного анксиолитика Афобазола, не относящегося к классу агонистов бензодиазепиновых рецепторов.
По химической структуре Афобазол® – 5-этокси-2-[2-(морфолино)-этилтио] бензилимидазола дигидрохлорид – относится к производным 2-меркаптобензимидазола.
Афобазол – «короткоживущее» средство с периодом полувыведения – 0,82±0,54 ч и быстрым переносом из плазмы крови в ткани и органы.
Во всех исследованиях не было отмечено седативного и миорелаксирующего эффектов, а также негативного влияния на когнитивные функции с явлениями поведенческой токсичности. В то же время при изучении эмоционально-стрессовых реакций было установлено, что препарат не обладает свойствами психомоторного стимулятора, хотя может оказывать умеренно активирующее действие, отражающееся на ряде психофизиологических показателей (сенсомоторные функции, концентрация внимания, кратковременная зрительная память). В качестве преимущества Афобазола подчеркивается возможность использования адекватной терапевтической дозы с 1-го дня лечения [22–24].
Исследования, проводившиеся в крупнейших психиатрических центрах страны, показали высокую эффективность Афобазола, идентичную бензодиазепиновым транквилизаторам при терапии тревожных расстройств пограничного уровня [1], генерализованном тревожном расстройстве [12], а также в комплексном лечении расстройств адаптации [5]. Кроме того, имеются публикации об эффективности Афобазола при лечении тревожных и вегетативных расстройств в общесоматической, неврологической и гинекологической практике [2].
Чрезвычайно актуальной представляется коррекция тревожных расстройств у больных с сердечно-сосудистой патологией [28–30, 34]. Расстройства эмоций могут усугублять симптоматику основного заболевания, ухудшать функциональный статус пациента, повышать вероятность неблагоприятного исхода сердечно-сосудистого заболевания. У 1/3 больных с острым инфарктом миокарда регистрируются тревожные и депрессивные расстройства, разнообразные фобии [3, 6]. По нашим данным, тревожные расстройства выявляются у 63% больных с острым инфарктом миокарда, а у больных с хронической сердечной недостаточностью встречаются более чем в 80% случаев [8].
Медикаментозная терапия тревожных расстройств в кардиологической практике определяется не только эффективностью лекарственного препарата, но прежде всего его безопасностью, отсутствием синдрома отмены и поведенческой токсичности, особой чувствительностью кардиологических пациентов пожилого возраста, значимого влияния на гемодинамику, возможностью сочетания с соматотропными препаратами [13].
Отмечены эффективность и хорошая переносимость Афобазола у пациентов с сердечно-сосудистыми заболеваниями при терапии фобических, соматизированных, легких или умеренно выраженных тревожных расстройств, причем рекомендуемый диапазон доз составил 30–60 мг/сут в зависимости от тяжести состояния при продолжительности терапии не менее 6 нед [9, 15].
Нами был проведен анализ возможности применения Афобазола в раннем периоде (на 2-е сутки) острого инфаркта миокарда непосредственно после купирования болевого синдрома. Скрининг психических расстройств у данного контингента выявил наличие нарушений тревожного спектра в 63% случаев. Афобазол назначался в дозе 10 мг 3 раза в день в течение 30 сут в комбинации с ацетилсалициловой кислотой, гепарином, b-адреноблокаторами, нитратами у 20 больных в возрасте 63±3,0 года. Группу сравнения составили 10 больных, сопоставимых по соматическому и психическому состоянию, половозрастному составу и характеру соматотропной терапии с основной группой исследования, не получавшей Афобазол.
Структура тревожных расстройств в остром периоде инфаркта миокарда была представлена генерализованным тревожным расстройством, изолированными фобиями, смешанным тревожным и депрессивным расстройством. Для обследованных пациентов в остром периоде инфаркта миокарда была характерна коморбидность тревоги и депрессии (79%). Уровень депрессии, как правило, соответствовал малому депрессивному эпизоду (в среднем по группе 11±1,0 балла по шкале Гамильтона). В 37% случаев наблюдалась умеренная и в 26% – выраженная реактивная тревожность по шкале Спилбергера.
Терапевтический ответ отмечался к концу 1-й недели приема Афобазола в виде уменьшения тревожных мыслей, напряженности, нормализации сна. После окончания курса терапии Афобазолом выздоровление было достигнуто в 50% случаев, в то время как в контрольной группе психические расстройства сохранялись, несмотря на положительную динамику соматического состояния. На момент окончания исследования уровень тревоги у больных подгруппы сравнения достоверно превышал таковой в подгруппе Афобазола (25±2,2 балла против 19,7±1,0 балла по шкале Спилбергера соответственно; p<0,05). Выраженность реактивной тревожности после терапии Афобазолом не превышала низкого порога по шкале Спилбергера, также отмечено некоторое снижение выраженности депрессии в среднем по группе (9,0±0,8 балла по шкале Гамильтона). Побочных эффектов зарегистрировано не было, больные отмечали хорошую переносимость препарата.
Эффективность терапии подтверждается динамикой качества жизни пациентов в сравнении с аналогичной группой больных, не получавших анксиолитической терапии.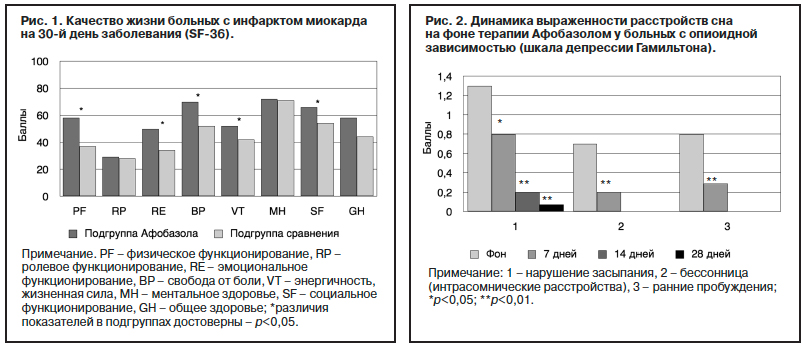
В наркологической практике Афобазол еще не нашел широкого применения. На сегодняшний день имеется исследование, выполненное в Московском НИИ психиатрии, где показана сопоставимая с диазепамом эффективность Афобазола при купировании алкогольного абстинентного синдрома [7]. Авторы указывают, что Афобазол высокоэффективен в отношении соматовегетативных (потливость, жажда, снижение аппетита), неврологических (тремор, атаксия) и аффективных (тревога) проявлений алкогольного абстинентного синдрома. Терапевтическое действие обнаруживалось уже на 2-е сутки применения препарата. Афобазол хорошо переносился пациентами, побочных явлений не было. Особо подчеркивается его безопасность в отношении развития привыкания.
С учетом того, что при применении Афобазола не формируется лекарственная зависимость и не развивается синдром отмены, была изучена возможность его применения в коррекции аффективных расстройств на этапе становления ремиссии опиоидной зависимости как препарата, у которого отсутствует аддиктогенный эффект.
В исследование были включены 30 пациентов с опиоидной зависимостью (F11) в постабстинентном состоянии, проходивших реабилитационную программу по методике 12 шагов (Миннесотская модель). Пациенты случайным образом были разбиты на 2 группы – экспериментальную и контрольную по 15 человек в каждой. Афобазол назначался пациентам экспериментальной группы в дозе 30 мг/сут. Длительность терапии составляла 28 дней. Для оценки состояния до назначения препарата (1-й день), на 7, 14 и 28-й дни курсовой терапии в экспериментальной группе и в те же дни пребывания в отделении в контрольной группе состояние больных оценивалось с помощью объективных клинических шкал тревоги и депрессии Гамильтона, а также Анкеты для оценки синдрома ангедонии.
Аффективные расстройства были представлены тревожно-депрессивным синдромом при превалировании тревоги.
Выраженность тревоги исходно колебалась от 42 до 14 баллов и в среднем составила 28,7 балла, преобладая над депрессивными расстройствами (12,7 балла по шкале Гамильтона). Терапевтический ответ наблюдался уже к концу 1-й недели: выраженность тревоги и депрессии составила 18,2 и 6,1 балла по шкале Гамильтона соответственно. Отчетливая динамика аффективных расстройств и ангедонии отмечалась через 2 нед терапии Афобазолом. На момент окончания курса терапии уровень тревоги достиг 3,4 балла, депрессии – 0,7 балла по шкале Гамильтона (табл. 1).
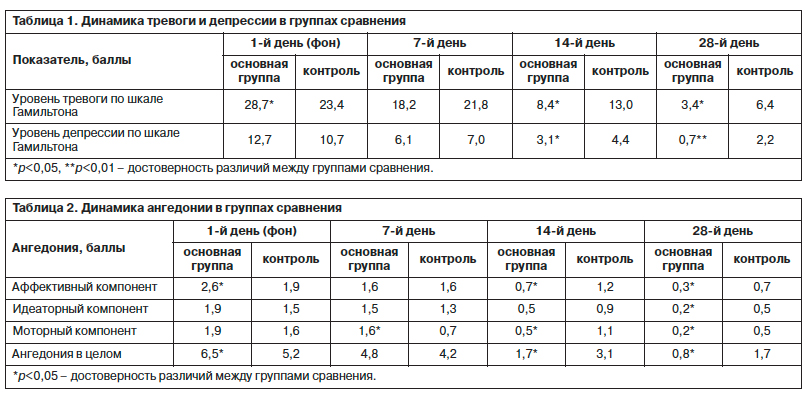
Важно, что в процессе терапии Афобазолом наблюдается достоверное нивелирование всех вариантов диссомнии. Уже через неделю терапии отмечалось заметное снижение выраженности нарушения сна (рис. 2).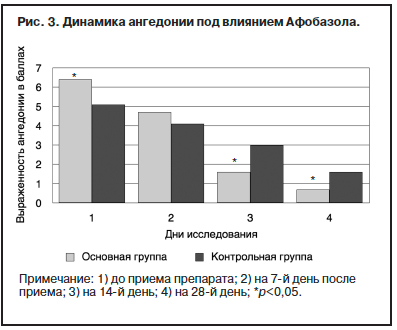
Выраженность ангедонии у пациентов, которые получали Афобазол, достоверно снизилась по сравнению с больными, не получавшими препарат, причем следует отметить наибольшие различия по аффективному компоненту влечения (рис. 3; табл. 2).
В группе больных, принимавших Афобазол, из 15 пациентов покинул реабилитационную программу только 1, в то время как в контрольной группе из программы выбыли 4 пациента из 15 членов группы. Можно утверждать, что Афобазол способствует удержанию амбулаторных наркологических пациентов в реабилитационной программе. Побочных эффектов при терапии Афобазолом на всем протяжении лечения не отмечалось.Проведенное исследование показало, что Афобазол оказался эффективен в терапии тревожно-депрессивных расстройств и ослаблении патологического влечения к наркотику на этапе становления ремиссии у больных опиоидной наркоманией в постабстинентном состоянии.
Таким образом, имеющиеся данные свидетельствуют о том, что анксиолитик Афобазол эффективен в редукции тревоги и коморбидной ей невыраженной депрессии у больных разного профиля. Терапевтический эффект наступает в короткие сроки и отмечается уже к концу 1-й недели с нарастанием положительной динамики при продолжении терапии. Афобазол характеризуется оптимальным соотношением безопасности и эффективности – он позволяет добиться выраженного клинического эффекта, идентичного бензодиазепиновым транквилизаторам и при этом избежать свойственных бензодиазепинам нежелательных явлений, что определяет возможность широкого применения препарата во внебольничной практике в разных областях медицины.
Сведение об авторе
Петрова Наталия Николаевна – д-р мед. наук, зав. каф. психиатрии и наркологии медицинского факультета СПбГУ. E-mail: petrova_nn@mail.ru
Ключевые слова: тревожные расстройства, терапия, психосоматика, наркология.
Anxiety disorders and their correction in outpatient psychiatric practice
N.N.Petrova
Department of Psychiatry and Addiction, Medical Faculty of St.-Petersburg State University
Summary. The analysis of modern approaches to treatment of anxiety disorders, including comorbid with depression was performed. The results of correction in patients with anxiety disorders and substance abuse psychosomatic profile using a new generation of anxiolytic Afobazol was shown. The drug demonstrated the effectiveness against the psychic and somatic anxiety, insomnia, neurotic depression, as well as improvement in the quality of life of patients with Afobazole therapy.
Key words: anxiety disorders, therapy, psychosomatic medicine, drug and alcohol abuse.
Актуальность проблемы тревожных расстройств определяется их клинической гетерогенностью, тенденцией к затяжному течению и формированию коморбидных соотношений с депрессивной и соматоформной симптоматикой [25, 27]. По данным T.Strine и соавт., распространенность тревожных расстройств среди населения составляет 15% [33]. Наиболее часто встречаются легкие или умеренно выраженные тревожные расстройства типа ситуационно обусловленных личностных реакций, нозогенные расстройства и генерализованное тревожное расстройство, что определяет преобладание таких пациентов в амбулаторной практике [32].
Необходимость оптимизации лечебных мероприятий обусловлена широкой распространенностью тревожных расстройств не только среди внебольничного контингента психиатрических пациентов, но и в других областях медицины.
Клинически тревожные расстройства проявляются психическими и соматическими (вегетативными) симптомами, важной отличительной чертой которых является полисистемность. В связи с этим значительное число пациентов, у которых преобладают соматовегетативные проявления тревоги, обращаются не к психиатрам (психотерапевтам), а к врачам-интернистам: терапевтам, кардиологам, гастроэнтерологам, пульмонологам, дерматологам, онкологам и другим специалистам [12, 31].
Психофармакотерапия тревожных расстройств представляется актуальной и достаточно непростой задачей. Основным методом коррекции тревожных расстройств является прием анксиолитических препаратов. Первыми использовавшимися человечеством средствами с анксиолитическим эффектом были алкоголь и опиаты. В ХIX в. начали применять бромиды, в XX в. – барбитураты и резерпин. С середины ХХ в. ведущее место в анксиолитической терапии занимают препараты бензодиазепинового ряда – транквилизаторы (от латинского слова «tranquillo» – успокаивать). Транквилизаторы определяют как лекарственные средства, подавляющие или способные уменьшать выраженность беспокойства, страха и напряженности.
Спектр действия данной группы психотропных препаратов достаточно широк благодаря быстрому развитию неспецифического тормозного ГАМКергического эффекта, за счет которого наступает миорелаксация, купируются судороги и спазмы, развиваются седативный и вегетостабилизирующий эффекты. Транквилизаторы эффективны при фобиях, способны редуцировать как психическую, так и соматическую тревогу. Этим обусловлено их широкое применение во многих областях медицины, в том числе в хирургической практике – для премедикации, в гинекологии – для лечения климактерических расстройств и предменструального синдрома, в психиатрии – при расстройствах адаптации, купировании ажитации и т.д. Однако, обладая выраженными противотревожными свойствами, большинство представителей группы бензодиазепинов вызывают чрезмерную седацию и миорелаксацию, а при длительном применении могут вызывать аддикцию.
Симптомы поведенческой токсичности (дневная сонливость, замедление когнитивных процессов, снижение остроты реакций, внимания и памяти) и риск злоупотребления бензодиазепиновыми транквилизаторами ограничивают возможности их применения в амбулаторной практике [4]. Кроме того, взаимодействие бензодиазепиновых анксиолитиков с некоторыми соматотропными препаратами (a-адреномиметиками, a- и b-адреноблокаторами, блокаторами кальциевых каналов, ингибиторами ангиотензинпревращающего фермента, производными метилксантина) в ряде случаев можно рассматривать как неблагоприятное. Так, при одновременном приеме лекарств бензодиазепинового ряда с клонидином (клофелином) и пропранололом отмечаются усиление гипотензивного эффекта, угнетающее действие на центральную нервную систему, рефлекторная тахикардия. Бензодиазепиновые анксиолитики усиливают адренолитическое действие фентоламина, тропафена, индорамина вплоть до развития тяжелой гипотензивной реакции, что создает трудности при использовании этих препаратов у соматических больных.
Транквилизаторы неэффективны при коморбидных тревожных и депрессивных расстройствах, которые широко распространены в современной клинической практике. В этих случаях целесообразно использовать антидепрессанты из группы селективных ингибиторов обратного захвата серотонина или селективных ингибиторов обратного захвата серотонина и норадреналина.
Опыт изучения транквилизаторов (диазепам, лоразепам, феназепам, клоназепам, оксазепам) позволил развить теорию нейрохимической регуляции тревоги и заложить основы терапии тревожных расстройств, в том числе субклинических форм, установить закономерности проявления фармакологических эффектов (анксиолитического, вегетостабилизирующего, гипноседативного, миорелаксирующего, регулирующего поведение). Дальнейшее развитие фармакотерапии движется по пути формирования селективности противотревожного действия. Результаты клинических исследований подтвердили необходимость создания препаратов, соответствующих по своим противотревожным свойствам бензодиазепиновым транквилизаторам, но свободных от присущих им нежелательных эффектов. Работы, проведенные под руководством академика С.Б.Середенина, позволили сформулировать фармакогенетическую концепцию анксиоселективности [16]. Авторами была показана зависимость преобладания седативного либо анксиолитического эффекта бензодиазепинов от генетически контролируемого фенотипа эмоционально-стрессовых реакций как у животных, так и у человека. Сравнение фенотипов эмоционально-стрессовых реакций: «активных» (стрессоустойчивых) и «пассивных» (стрессонеустойчивых) в стрессе инбредных животных позволило выявить нейрохимическую мишень анксиоселективного действия – падение бензодиазепиновой рецепции на фоне экспериментального стресса только у пассивных животных [17]. Наличие данного эффекта было подтверждено в клинике на добровольцах и у пациентов с реактивными состояниями. В ГУ НИИ фармакологии им. В.В.Закусова РАМН в процессе исследований, проводимых на протяжении более 15 лет, был найден регулятор бензодиазепинового связывания и осуществлен синтез оригинального селективного анксиолитика Афобазола, не относящегося к классу агонистов бензодиазепиновых рецепторов.
По химической структуре Афобазол® – 5-этокси-2-[2-(морфолино)-этилтио] бензилимидазола дигидрохлорид – относится к производным 2-меркаптобензимидазола.
Афобазол – «короткоживущее» средство с периодом полувыведения – 0,82±0,54 ч и быстрым переносом из плазмы крови в ткани и органы.
Во всех исследованиях не было отмечено седативного и миорелаксирующего эффектов, а также негативного влияния на когнитивные функции с явлениями поведенческой токсичности. В то же время при изучении эмоционально-стрессовых реакций было установлено, что препарат не обладает свойствами психомоторного стимулятора, хотя может оказывать умеренно активирующее действие, отражающееся на ряде психофизиологических показателей (сенсомоторные функции, концентрация внимания, кратковременная зрительная память). В качестве преимущества Афобазола подчеркивается возможность использования адекватной терапевтической дозы с 1-го дня лечения [22–24].
Исследования, проводившиеся в крупнейших психиатрических центрах страны, показали высокую эффективность Афобазола, идентичную бензодиазепиновым транквилизаторам при терапии тревожных расстройств пограничного уровня [1], генерализованном тревожном расстройстве [12], а также в комплексном лечении расстройств адаптации [5]. Кроме того, имеются публикации об эффективности Афобазола при лечении тревожных и вегетативных расстройств в общесоматической, неврологической и гинекологической практике [2].
Чрезвычайно актуальной представляется коррекция тревожных расстройств у больных с сердечно-сосудистой патологией [28–30, 34]. Расстройства эмоций могут усугублять симптоматику основного заболевания, ухудшать функциональный статус пациента, повышать вероятность неблагоприятного исхода сердечно-сосудистого заболевания. У 1/3 больных с острым инфарктом миокарда регистрируются тревожные и депрессивные расстройства, разнообразные фобии [3, 6]. По нашим данным, тревожные расстройства выявляются у 63% больных с острым инфарктом миокарда, а у больных с хронической сердечной недостаточностью встречаются более чем в 80% случаев [8].
Медикаментозная терапия тревожных расстройств в кардиологической практике определяется не только эффективностью лекарственного препарата, но прежде всего его безопасностью, отсутствием синдрома отмены и поведенческой токсичности, особой чувствительностью кардиологических пациентов пожилого возраста, значимого влияния на гемодинамику, возможностью сочетания с соматотропными препаратами [13].
Отмечены эффективность и хорошая переносимость Афобазола у пациентов с сердечно-сосудистыми заболеваниями при терапии фобических, соматизированных, легких или умеренно выраженных тревожных расстройств, причем рекомендуемый диапазон доз составил 30–60 мг/сут в зависимости от тяжести состояния при продолжительности терапии не менее 6 нед [9, 15].
Нами был проведен анализ возможности применения Афобазола в раннем периоде (на 2-е сутки) острого инфаркта миокарда непосредственно после купирования болевого синдрома. Скрининг психических расстройств у данного контингента выявил наличие нарушений тревожного спектра в 63% случаев. Афобазол назначался в дозе 10 мг 3 раза в день в течение 30 сут в комбинации с ацетилсалициловой кислотой, гепарином, b-адреноблокаторами, нитратами у 20 больных в возрасте 63±3,0 года. Группу сравнения составили 10 больных, сопоставимых по соматическому и психическому состоянию, половозрастному составу и характеру соматотропной терапии с основной группой исследования, не получавшей Афобазол.
Структура тревожных расстройств в остром периоде инфаркта миокарда была представлена генерализованным тревожным расстройством, изолированными фобиями, смешанным тревожным и депрессивным расстройством. Для обследованных пациентов в остром периоде инфаркта миокарда была характерна коморбидность тревоги и депрессии (79%). Уровень депрессии, как правило, соответствовал малому депрессивному эпизоду (в среднем по группе 11±1,0 балла по шкале Гамильтона). В 37% случаев наблюдалась умеренная и в 26% – выраженная реактивная тревожность по шкале Спилбергера.
Терапевтический ответ отмечался к концу 1-й недели приема Афобазола в виде уменьшения тревожных мыслей, напряженности, нормализации сна. После окончания курса терапии Афобазолом выздоровление было достигнуто в 50% случаев, в то время как в контрольной группе психические расстройства сохранялись, несмотря на положительную динамику соматического состояния. На момент окончания исследования уровень тревоги у больных подгруппы сравнения достоверно превышал таковой в подгруппе Афобазола (25±2,2 балла против 19,7±1,0 балла по шкале Спилбергера соответственно; p<0,05). Выраженность реактивной тревожности после терапии Афобазолом не превышала низкого порога по шкале Спилбергера, также отмечено некоторое снижение выраженности депрессии в среднем по группе (9,0±0,8 балла по шкале Гамильтона). Побочных эффектов зарегистрировано не было, больные отмечали хорошую переносимость препарата.
Эффективность терапии подтверждается динамикой качества жизни пациентов в сравнении с аналогичной группой больных, не получавших анксиолитической терапии.

В наркологической практике Афобазол еще не нашел широкого применения. На сегодняшний день имеется исследование, выполненное в Московском НИИ психиатрии, где показана сопоставимая с диазепамом эффективность Афобазола при купировании алкогольного абстинентного синдрома [7]. Авторы указывают, что Афобазол высокоэффективен в отношении соматовегетативных (потливость, жажда, снижение аппетита), неврологических (тремор, атаксия) и аффективных (тревога) проявлений алкогольного абстинентного синдрома. Терапевтическое действие обнаруживалось уже на 2-е сутки применения препарата. Афобазол хорошо переносился пациентами, побочных явлений не было. Особо подчеркивается его безопасность в отношении развития привыкания.
С учетом того, что при применении Афобазола не формируется лекарственная зависимость и не развивается синдром отмены, была изучена возможность его применения в коррекции аффективных расстройств на этапе становления ремиссии опиоидной зависимости как препарата, у которого отсутствует аддиктогенный эффект.
В исследование были включены 30 пациентов с опиоидной зависимостью (F11) в постабстинентном состоянии, проходивших реабилитационную программу по методике 12 шагов (Миннесотская модель). Пациенты случайным образом были разбиты на 2 группы – экспериментальную и контрольную по 15 человек в каждой. Афобазол назначался пациентам экспериментальной группы в дозе 30 мг/сут. Длительность терапии составляла 28 дней. Для оценки состояния до назначения препарата (1-й день), на 7, 14 и 28-й дни курсовой терапии в экспериментальной группе и в те же дни пребывания в отделении в контрольной группе состояние больных оценивалось с помощью объективных клинических шкал тревоги и депрессии Гамильтона, а также Анкеты для оценки синдрома ангедонии.
Аффективные расстройства были представлены тревожно-депрессивным синдромом при превалировании тревоги.
Выраженность тревоги исходно колебалась от 42 до 14 баллов и в среднем составила 28,7 балла, преобладая над депрессивными расстройствами (12,7 балла по шкале Гамильтона). Терапевтический ответ наблюдался уже к концу 1-й недели: выраженность тревоги и депрессии составила 18,2 и 6,1 балла по шкале Гамильтона соответственно. Отчетливая динамика аффективных расстройств и ангедонии отмечалась через 2 нед терапии Афобазолом. На момент окончания курса терапии уровень тревоги достиг 3,4 балла, депрессии – 0,7 балла по шкале Гамильтона (табл. 1).

Важно, что в процессе терапии Афобазолом наблюдается достоверное нивелирование всех вариантов диссомнии. Уже через неделю терапии отмечалось заметное снижение выраженности нарушения сна (рис. 2).

Выраженность ангедонии у пациентов, которые получали Афобазол, достоверно снизилась по сравнению с больными, не получавшими препарат, причем следует отметить наибольшие различия по аффективному компоненту влечения (рис. 3; табл. 2).
В группе больных, принимавших Афобазол, из 15 пациентов покинул реабилитационную программу только 1, в то время как в контрольной группе из программы выбыли 4 пациента из 15 членов группы. Можно утверждать, что Афобазол способствует удержанию амбулаторных наркологических пациентов в реабилитационной программе. Побочных эффектов при терапии Афобазолом на всем протяжении лечения не отмечалось.Проведенное исследование показало, что Афобазол оказался эффективен в терапии тревожно-депрессивных расстройств и ослаблении патологического влечения к наркотику на этапе становления ремиссии у больных опиоидной наркоманией в постабстинентном состоянии.
Таким образом, имеющиеся данные свидетельствуют о том, что анксиолитик Афобазол эффективен в редукции тревоги и коморбидной ей невыраженной депрессии у больных разного профиля. Терапевтический эффект наступает в короткие сроки и отмечается уже к концу 1-й недели с нарастанием положительной динамики при продолжении терапии. Афобазол характеризуется оптимальным соотношением безопасности и эффективности – он позволяет добиться выраженного клинического эффекта, идентичного бензодиазепиновым транквилизаторам и при этом избежать свойственных бензодиазепинам нежелательных явлений, что определяет возможность широкого применения препарата во внебольничной практике в разных областях медицины.
Сведение об авторе
Петрова Наталия Николаевна – д-р мед. наук, зав. каф. психиатрии и наркологии медицинского факультета СПбГУ. E-mail: petrova_nn@mail.ru
Список исп. литературыСкрыть список1. Аведисова А.С., Чахова В.О., Лесс Ю.Э., Малыгин Я.В. Новый анксиолитик «Афобазол» при терапии генерализованного тревожного расстройства (результаты сравнительного исследования с диазепамом). Психиатр. и психофармакотер. Экстравыпуск. 2006; с. 13–6.
2. Акарачкова Е.С., Шварков С.Б., Мамий В.И. Афобазол в терапии вегетативных проявлений тревоги и дезадаптации у больных неврологической и общесоматической практики. РМЖ. Неврология. 2007; 15 (1): 1–6.
3. Белялов Ф.И. Психосоматические аспекты ишемической болезни сердца. Кардиология. 2002; 42 (8): 63–7.
4. Бородин В.И. Побочные эффекты транквилизаторов и их роль в пограничной психиатрии. Психиатр. и психофармакол. 2000; 3: 72–4.
5. Васильева А.В., Полторак С.В., Поляков А.Ю., Соломонова С.В. Применение Афобазола в комплексном лечении расстройств адаптации. Обозрение психиатрии и мед. психологии им. В.М.Бехтерева. 2006; 4: 31–3.
6. Иванов С.В. Психосоматические расстройства в кардиологии. Сердце. 2002; 1 (4): 169–72.
7. Кожинова Т.А., Гофман А.Г., Варфоломеева Ю.Е., Шевелева О.С. Купирование алкогольного абстинентного синдрома (исследование эффективности и переносимости Афобазола). Наркология. 2007; 7: 34–9.
8. Кутузова А.Э., Петрова Н.Н., Округина О.М., Недошивин А.О. Динамический анализ психического статуса и теста с шестиминутной ходьбой у больных с сердечной недостаточностью на стационарном этапе лечения. Врач. 2004; 3: 36–8.
9. Медведев В.Э., Троснова А.П., Добровольский А.В. Психофармакотерпия тревожных расстройств у больных с сердечно-сосудистыми заболеваниями: применение Афобазола. Журн. неврол. и психиатр. 2007; 107 (7): 25–7.
10. Незнамов Г.Г., Сюняков С.А., Чумаков Д.В. и др. Результаты клинического изучения селективного анксиолитика Афобазол. Эксперим. и клин. фармакология. 2001; 64 (2): 15–9.
11. Незнамов Г.Г., Сюняков С.А., Чумаков Д.В. и др. Новый селективный анксиолитик Афобазол. Журн. неврол. и психиатр. им. С.С.Корсакова. 2005; 4: 35–40.
12. Незнамов Г.Г., Сюняков С.А., Чумаков Д.В. и др. Новый анксиолитик Афобазол: результаты сравнительного клинического исследования с диазепамом при генерализованном тревожном расстройстве. Журн. психиатр. и психофармокотер. им. П.Б.Ганнушкина. 2006; 4: 8–15.
13. Погосова Г.В. Психоэмоциональные расстройства при сердечно-сосудистых заболеваниях: терапевтические аспекты. Cons. Med. 2006; 8 (5): 118–23.
14. Пограничная психическая патология в общемедицинской практике. Под ред. А.Б.Смулевича. М.: Русский врач, 2000; с. 78–105.
15. Подхомутников В.М., Баранова М.Н., Юхно Е.С. Применение Афобазола у больных инфарктом миокарада. Проблемы современной психокардиологии. Материалы Российского национального конгресса кардиологов и Конгресса кардиологов стран СН. М., 2007; с. 50–2.
16. Середенин С.Б., Воронина Т.А., Незнамов Г.Г. и др. Фармакогенетическая концепция анксиоселективного эффекта. Вестник РАМН. 1998; 11: 3–9.
17. Серединин С.Б., Бадыштов Б.А., Незнамов Г.Г. и др. Прогноз индивидуальных реакций на эмоциональный стресс и бензодиазепиновые транквилизаторы. М., 2001.
18. Смулевич А.Б., Дробижев М.Ю., Иванов С.В. Транквилизато-ры – производные бензодиазепинов в психиатрии, психосоматике и общей медицине. М., 2005.
19. Смулевич А.Б., Андрющенко А.В., Романов Д.В. Психофармакотерапия тревожных расстройств пограничного уровня (сравнительное исследование анксиолитического эффекта Афобазола и оксазепама у больных с расстройствами адаптации и генерализованным тревожным расстройством). РМЖ. Неврология и психиатрия. 2006; 14 (9): 1–6.
20. Смулевич А.Б., Андрющенко А.В., Романов Д.В. и др. Терапия пограничных психических расстройств (исследование эффективности и переносимости Афобазола). Психические расстройства в общей медицине. 2006; 6: 10–6.
21. Смулевич А.Б., Андрющенко А.В., Романов Д.В., Сиранчиева О.А. Терапия пограничных психических расстройств (исследование эффективности и переносимости Афобазола). Психиатр. и психофармакотер. Экстравыпуск. 2006; с. 3–9.
22. Сюняков С.А., Чумаков Д.В., Бочкарев В.К. и др. Особенности действия анксиолитика Афобазола у больных с различными индивидуально-типологическими чертами. Соц. и клин. психиатрия. 2006; 1: 38–45.
23. Чумаков Д.В. Клинико-фармакологическая характеристика нового анксиолитика Афобазола. Врач. 2006; 14: 19–22.
24. Яркова М.А. Изучение анксиолитических свойств производных 2-меркаптобензимидазола. Автореф. дис. ... канд. мед. наук. М., 1996.
25. Cottraux J. Recent developments in the research on generalized anxiety disorder. Curr Opin Psychiatry 2004; 17: 49–52.
26. Kolotilinskaya NV, Badyshtov BA, Makhnycheva AL et al. Phase-I investigation of selective anxiolytic afobazole. European Neuropsychopharmacology 2005; p. 161.
27. Lepine JP. The epidemiology of anxiety disorders: prevalence and social costs. J Clin Psychiatry 2002; 63 (Suppl. 14): 4–8.
28. Mayou R, Gill D et al. Depression and anxiety as predictors of outcome after myocardial infarction. Psychosom Med 2000; 62: 212–9.
29. Moser DK. «The Rust of Life»: Impact of Anxiety on Cardiac Patients American Journal of Critical Care 2007; 16 (4): 361–9.
30. Nasilowska-Barud A. Anxiety and fear level in patients after myocardial infarction over five years of rehabilitation. Ann Univ Mariae Curie Sklodowska 2002; 57 (2): 505–13.
31. Roy-Byrne PP, Katon W. Generalized anxiety disorder in primary care: the precursor/modifier pathway to increased health care utilization. J Clin Psychiatry 1997; 58 (Suppl. 3): 4–38.
32. Rouillon F. Long term therapy of generalized anxiety disorder. Eur J Psychiatry 2004; 19 (2): 96–101.
33. Strine TW, Chapman DP, Kobau R et al. Associations of self-reported anxiety symptoms with health-related quality of life and health behaviors. Soc Psychiatry Psychiatr Epidemiol 2005; 40 (6): 432–8.
34. Wyszynski A, Schwartz M et al. The patient with cardiovascular disease. In: Manual of psychiatric care for the medically ill. 1st ed. American Psychiatric Publishing, Inc. Washington, 2004; p. 49–67.


