Клинический разбор в общей медицине №3 2024
Клинический разбор в общей медицине №3 2024
Пресс-релиз: Первый Сеченовский международный форум материнства и детства: достижения, проблемы, перспективы
Номера страниц в выпуске:119-130
Аннотация
В данном обзоре представлены результаты оригинальных исследований, посвященных проблеме преждевременных родов и невынашивания беременности, сохранения репродуктивного потенциала у онкологических больных, ранней диагностике преэклампсии и истмико-цервикальной недостаточности, новым методикам хирургического лечения пролапса гениталий, а также роли малоинвазивных технологий в диагностике внутриматочной патологии. Особого внимания заслуживают доклады Н.С. Трифоновой и соавторов, Е.В. Тимохиной, С.В. Песеговой, Д.В. Брюнина, Т.А. Джибладзе, И.А. Аполихиной и соавтора, И.В. Решетова и Л.А. Ашрафяна.
Ключевые слова: акушерство, гинекология, экстракорпоральное оплодотворение, беременность, истмико-цервикальная недостаточность, преэклампсия, генитоуринарный менопаузальный синдром, атрофия, вирус папилломы человека, онкология, пролапс тазовых органов.
Для цитирования: Первый Сеченовский международный форум материнства и детства: достижения, проблемы, перспективы. Клинический разбор в общей медицине. 2024; 5 (3): 119–130. DOI: 10.47407/kr2023.5.3.00381
В данном обзоре представлены результаты оригинальных исследований, посвященных проблеме преждевременных родов и невынашивания беременности, сохранения репродуктивного потенциала у онкологических больных, ранней диагностике преэклампсии и истмико-цервикальной недостаточности, новым методикам хирургического лечения пролапса гениталий, а также роли малоинвазивных технологий в диагностике внутриматочной патологии. Особого внимания заслуживают доклады Н.С. Трифоновой и соавторов, Е.В. Тимохиной, С.В. Песеговой, Д.В. Брюнина, Т.А. Джибладзе, И.А. Аполихиной и соавтора, И.В. Решетова и Л.А. Ашрафяна.
Ключевые слова: акушерство, гинекология, экстракорпоральное оплодотворение, беременность, истмико-цервикальная недостаточность, преэклампсия, генитоуринарный менопаузальный синдром, атрофия, вирус папилломы человека, онкология, пролапс тазовых органов.
Для цитирования: Первый Сеченовский международный форум материнства и детства: достижения, проблемы, перспективы. Клинический разбор в общей медицине. 2024; 5 (3): 119–130. DOI: 10.47407/kr2023.5.3.00381
Press release
Abstract
The paper provides the review of materials of the 1st Sechenov International Motherhood and Childhood Forum that took place on February 15–16 at the I.M. Sechenov First Moscow State Medical University. The event was held within the framework of the PRIORITY 2030 presidential program that was intended to create the world-class research medical university by the year 2030. Lectors presented the results of original research focused on the issues of preterm birth and miscarriage, preservation of fertility in cancer patients, early diagnosis of preeclampsia and isthmic-cervical incompetence, new methods for surgical treatment of genital prolapse, as well as the role of minimally invasive techniques in the diagnosis of intrauterine abnormalities. The reports of N.S. Trifonova et al., E.V. Timokhina, S.V. Pesegova, D.V. Bryunin, T.A. Jibladze, I.A. Apolikhina, I.V. Reshetov, and L.A. Ashrafyan deserve special attention.
Keywords: obstetrics, gynecology, in vitro fertilization, pregnancy, isthmic-cervical incompetence, preeclampsia, genitourinary syndrome of menopause, atrophy, human papillomavirus, oncology, pelvic organ prolapse.
For citation: First Sechenov International Motherhood and Childhood Forum: achievements, challenges, prospects. Clinical review for general practice. 2024; 5 (3): 119–130. (In Russ.). DOI: 10.47407/kr2023.5.3.00381
 В статье представлен обзор материалов I Сеченовского международного форума материнства и детства, состоявшегося 15–16 февраля 2024 г. на базе ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова». Данное мероприятие проходило в рамках президентской программы «Приоритет-2030», которая призвана создать Исследовательский медицинский университет мирового уровня к 2030 г. Уникальность форума — это акцент на инновационные российские достижения в области охраны здоровья женщин и детей для улучшения качества оказания медицинской помощи и профилактики развития осложнений.
В статье представлен обзор материалов I Сеченовского международного форума материнства и детства, состоявшегося 15–16 февраля 2024 г. на базе ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова». Данное мероприятие проходило в рамках президентской программы «Приоритет-2030», которая призвана создать Исследовательский медицинский университет мирового уровня к 2030 г. Уникальность форума — это акцент на инновационные российские достижения в области охраны здоровья женщин и детей для улучшения качества оказания медицинской помощи и профилактики развития осложнений.
Актуальность. По оценке Всемирной организации здравоохранения (ВОЗ), проблема бесплодия затрагивает порядка 190 млн человек в мире. На сегодняшний день вспомогательные репродуктивные технологии (ВРТ) стали распространенной процедурой, с помощью которой рождаются тысячи детей по всему миру. По данным РАРЧ, доля преодоления бесплодия с помощью ВРТ составила 2,7% в 2021 г. и 2,4% в 2020 г. Доля циклов ВРТ продолжает расти с каждым годом, особенно циклов ВРТ с донорской яйцеклеткой. По данным РАРЧ, доля циклов ВРТ за 2021 г. выросла на 8,7 %, доля циклов с донорской яйцеклеткой – на 6,7%. Однако статистически беременность после ЭКО сопровождается более высокой частотой акушерских осложнений, в том числе и преждевременными родами.
В соответствии с последним информационным бюллетенем ВОЗ, осложнения в результате преждевременных родов являются основной причиной смерти детей в возрасте до 5 лет. В Болонском университете в 2018 г. был проведен метаанализ, содержащий 15 когортных исследований, в который было включено порядка 61 677 одноплодных беременностей, закончившихся родами. По результатам исследования, риск спонтанных преждевременных родов у женщин, чья беременность наступила в результате ЭКО, был выше на 80%, чем у пациенток с самостоятельно наступившей беременностью. Ученые из университета Аристотеля в Греции также провели метаанализ из 9 исследований женщин с одноплодной беременностью, наступившей в результате ЭКО. Ученые выяснили, что у женщин, чья беременность наступила в результате ВРТ, риск спонтанных преждевременных родов также выше в 2 раза. Международная группа исследователей из Китая и Германии провели оценку течения беременности после ЭКО у 4328 женщин. В результате были названы 7 независимых факторов преждевременных родов: возраст менее 25 лет или более 39 лет, многоплодная беременность, предлежание плаценты, редукция эмбрионов, гестационная артериальная гипертензия, повышение уровня триглицеридов, укорочение активированного частичного тромбопластинового времени. В Университете Копенгагена ученые провели исследование женщин с донорской яйцеклеткой и выявили большой риск акушерских осложнений, особенно преждевременных родов и детей с низкой массой тела при рождении.
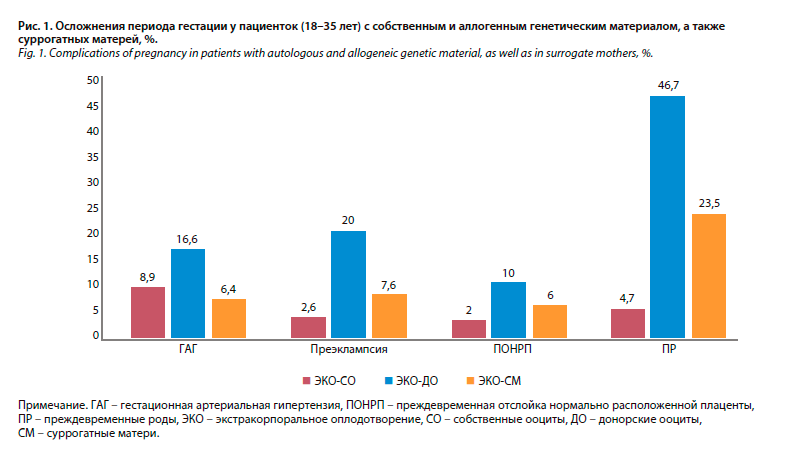
В исследовании, проведенном доктором медицинских наук, профессором Н.С. Трифоновой, кандидатом медицинских наук. Э.В. Жуковой и ассистентом кафедры К.И. Лаврентьевой, на базе клиники акушерства и гинекологии имени В.Ф. Снегирева Университетской клинической больницы №2 приняли участие 1101 пациентка, из которых 895 пациенток были после различных программ ЭКО: собственные ооциты, донорские яйцеклетки и суррогатные матери. В результате выяснено, что частота угрозы преждевременных родов до 34 нед, а также осложнений беременности, таких как истмико-цервикальная недостаточность, артериальная гипертензия, задержка роста плода, внутрипеченочный холестаз, тяжелая преэклампсия (ПЭ) и преждевременная отслойка нормально расположенной плаценты во II и III триместрах была выше у женщин с донорской яйцеклеткой и составила 57,3%. Дети, рожденные в результате ЭКО с донорской яйцеклеткой, статистически имели более низкую массу тела при рождении и более низкую оценку по шкале Апгар. Перинатальная смертность также была статистически выше в группе суррогатного материнства (рис. 1).
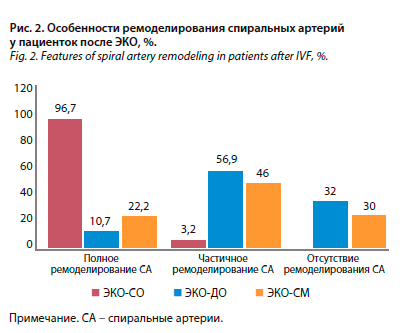
Особое внимание в исследовании заслуживает отсутствие ремоделирования спиральных артерий у порядка 1/3 пациенток с беременностью, наступившей после ЭКО (рис. 2).
Также представлено несколько клинических случаев пациенток, наблюдавшихся в клинике акушерства и гинекологии.
Клинический случай №1. Пациентка М., 29 лет. Перенесенные заболевания: детские инфекции, миопия слабой степени.
Предыдущие беременности:
• I беременность – своевременные самопроизвольные роды, без осложнений;
• II беременность – программа «Суррогатное материнство», неразвивающаяся беременность;
• III беременность – программа «Суррогатное материнство», преждевременные оперативные роды
в 35 нед, преждевременный разрыв плодных оболочек, тазовое предлежание плода (мальчик 2590 г,
47 см, 7–8 баллов);
• IV беременность – программа «Суррогатное материнство», дихориальная диамниотическая двойня, протекала с явлениями угрозы прерывания беременности.
Поступила в Клинику акушерства и гинекологии им. В.Ф. Снегирева с жалобами на излитие околоплодных вод.
Диагноз при поступлении: беременность 30–31 нед (ЭКО). Суррогатное материнство. Дихориальная диамниотическая двойня. Косое положение I плода. Преждевременный разрыв плодных оболочек. Рубец на матке после операции кесарево сечение в 2015 г.
Выполнена операция: поперечное надлобковое чревосечение с иссечением старого кожного рубца. Кесарево сечение в нижнем маточном сегменте.
I – мальчик 1450 г, 40 см, 6–7 баллов
II – мальчик 1687 г, 39 см, 6–7 баллов.
Клинический случай №2. Пациентка К., 34 лет. Перенесенные заболевания: детские инфекции, хронический бронхит.
Предыдущие беременности:
• I беременность – своевременные самопроизвольные роды, без осложнений;
• II беременность – программа «Суррогатное материнство», преждевременные самопроизвольные роды в 35 нед, ПЭ (девочка 2320 г, 48 см, 7–8 баллов).
• III беременность – программа «Суррогатное материнство», дихориальная диамниотическая двойня, протекала с явлениями угрозы прерывания беременности, гестационная артериальная гипертензия с 20 нед.
Поступила в Клинику акушерства и гинекологии им. В.Ф. Снегирева с жалобами на отеки голеней и стоп, повышение артериального давления (АД) до 160/100 мм рт. ст.
При обследовании выявлены явления холестаза беременных: щелочная фосфатаза (ЩФ) – 441 ед/л, полиненасыщенные жирные кислоты (ЖК) – 14,7 мкмоль /л. Проводилась комплексная терапия.
Жалобы на тяжесть в затылочной области, кожный зуд, АД – 150/100 мм рт. ст. Белок в моче – 1 г/л, ЩФ – 492 ед/л, ЖК – 76,7 мкмоль/л.
Клинический диагноз: беременность 34–35 нед (ЭКО). Суррогатное материнство. Дихориальная диамниотическая двойня. Головное предлежание I плода. ПЭ тяжелой степени. Холестаз беременных.
Выполнена операция: поперечное надлобковое чревосечение. Кесарево сечение в нижнем маточном сегменте.
I – мальчик 2160 г, 46 см, 7–8 баллов.
II – девочка 2370 г, 47 см, 7–8 баллов.
Заключение. Таким образом, применение вспомогательных репродуктивных технологий позволило качественно повысить уровень оказания медицинской помощи парам с бесплодием. Однако пациентки, чья беременность наступила в результате ЭКО с собственным или аллогенным генетическим материалом, заслуживают особого внимания и применения персонализированного подхода.
Доктор медицинских наук, доцент, профессор кафедры акушерства, гинекологии и перинатологии
Института клинической медицины им. Н.Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет), Е.В. Тимохина представила современную концепцию патогенеза и прогнозирования различных вариантов ПЭ.
Актуальность. По статистике, у 10 млн женщин ежегодно диагностируется ПЭ, 76 тыс. беременных женщин в мире ежегодно умирают от ПЭ и связанных с ней гипертензивных осложнений. На сегодняшний день принята концепция двухэтапного развития ПЭ, закладывания в I триместре генеза ПЭ, когда происходит инвазия трофобласта, гестационная трансформация спиральных артерий.
К факторам риска ПЭ относятся:
• иммунные факторы: первобеременные, наступление беременности менее чем через 1 год совместного проживания, беременность от нового партнера, интергравидарный интервал >10 лет;
• генетические факторы: наличие ПЭ у матери, сестры, партнер, рожденный от беременности с ПЭ;
• заболевания матери: избыточная масса тела/ожирение, хроническая артериальная гипертензия, сахарный диабет 1 и 2-го типа, антифосфолипидный синдром, заболевания почек, коллагенозы.
Как выделить факторы риска? Существующие клинические рекомендации во всем мире, источником которых является Фетальный фонд медицины, рекомендуют оценивать факторы риска уже в I триместре.
К ним относятся измерение среднего АД и допплерометрическая оценка кровотока в маточных артериях уже в 11–13 нед беременности (пульсационный индекс маточных артерий). Это повышает чувствительность и специфичность прогностических действий, поэтому дальнейшие метаболомические исследования, такие как ростовой фактор роста, плацентарный фактор роста, а также протеин, ассоциированный с беременностью, повышает дальнейшие шансы. Последние наблюдения показали, что включение таких факторов, как растворимый тирозинкиназный рецептор и плацентарный протеин, связанный с беременностью, являются дорогостоящими, но прогностически не слишком важными.
Согласно исследованию, проведенном на кафедре, матриксные металлопротеиназы (ММП) принимают участие в патогенезе как 1-го, так и 2-го этапа развития ПЭ, обладают огромным протеолитическим потенциалом, разрушают соединительнотканный матрикс, участвуют в инвазии и перестройке артерий. Целью исследования явилось определение прогностической значимости МПП-2 и ММП-9 как ранних маркеров ПЭ
в I триместре.
Проведено проспективное исследование 310 пациенток с 11-й по 13-ю неделю беременности за период 2017–2019 гг. Методом иммуноферментного анализа (ИФА) определен уровень ММП-2 и ММП-9 в венозной крови с единицей измерения нг/мл. ПЭ развилась у 34 пациенток, в то время как неосложненное течение беременности наблюдалось у 229 пациенток. Согласно результатам, при развитии ПЭ уровень МПП-2 уже в I триместре в 2 раза выше, чем при неосложненной беременности. В то же время при последующем развитии ПЭ уровень МПП-9 достоверно ниже уже в I триместре.
Установлено, что ММП-2>102 нг/мл уже в I триместре (11–13 нед.) предсказывает развитие ПЭ с чувствительностью 88,24% и специфичностью 82,76%. При концентрации ММП-2 более 380 нг/мл прогнозируется нарастание тяжести ПЭ с чувствительностью и специфичностью метода 70% и 85% соответственно.
МПП-9<980 нг/мл является пороговой для прогнозирования ПЭ в I триместре с чувствительностью 85,29% и специфичностью 84,48%.
Заключение. В результате метаболомного исследования доказано, что ММП принимают участие как в ключевых процессах I триместра беременности, так и могут быть использованы как потенциальные маркеры развития, нарастания тяжести и прогностического маркера ПЭ.
Актуальность. К факторам, вызывающим преждевременные роды, относят: воспалительный процесс, включая асептическое воспаление, дисплазию соединительной ткани и коллагеновых волокон, отягощенный акушерско-гинекологический анамнез (осложнения, потери беременности и т.д.), полиморфизм генов, ответственных за соединительную ткань, гормональные нарушения, генитальный инфантилизм, врожденное укорочение шейки матки или приобретенные деформации шейки матки. ИЦН может возникать и у соматически здоровых пациенток с неотягощенным анамнезом.
ИЦН – бессимптомное осложнение беременности. Зачастую, когда появляется первая симптоматика, проводить какую-либо коррекцию поздно, поэтому УЗ-цервикометрия, начиная с I триместра, обязательна. К основным методам диагностики ИЦН относят трансвагинальную цервикометрию (ТВУЗИ-цервикометрия).
Не менее 80% ИЦН ассоциированы с интраамниальным воспалением, поскольку барьерная функция цервикальной слизи при укорочении шейки матки и расширении цервикального канала нарушается и возникает асептическое воспаление.
Цель исследования. Оценить уровень маркеров интраамниального воспаления [интерлейкин (ИЛ)-6, ИЛ-8, МПП-8] в цервикальной жидкости для разработки персонифицированного подхода к ведению пациенток с данным осложнением беременности. Ведение беременности осуществлялось в соответствии с Приказом МЗ РФ №1130н и клиническим рекомендациям «Нормальная беременность».
В ходе наблюдения определены уровни ИЛ-6, ИЛ-8, МПП-8 в цервикальной жидкости методом ИФА (примерно 23 нед гестации), определены пороговые величины ИЛ-6, ИЛ-8, МПП-8, указывающие на высокий риск экстремально ранних и ранних преждевременных родов. В исследование были включены 2 группы – основная группа (беременные с ИЦН, n=95) и контрольная группа (беременные без признаков ИЦН, n=31), у которых использовался только микронизированный прогестерон.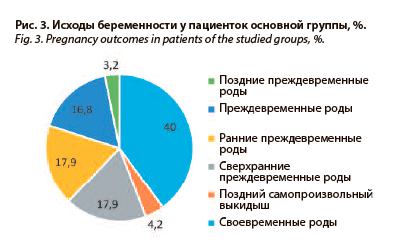
Результаты. В основной группе: у 40% пациенток роды завершились своевременно, у 4,2% – поздний самопроизвольный выкидыш и у 56% беременность закончилась преждевременными родами в различные сроки гестации (рис. 3). Медиана срока родоразрешения в основной группе составила 33,0 нед, а в группе контроля – 38,0 нед (p<0,001). У всех беременных группы контроля беременность завершилась своевременными родами (100%).
Маркеры интраамниального воспаления у пациенток из основной группы и группы контроля значительно различались. Уровень маркеров пропорционально возрастал сроку преждевременного родоразрешения. Хорионамнионит клинически был у 7,4% пациенток и у 38,9% гистологически.
Экстремально ранние и ранние преждевременные роды развивались у пациенток с ИЛ-6>11,1 пг/мл, ИЛ-8>275,4 пг/мл, МПП-8>26,1 нг/мл – преждевременные роды раньше 32 нед в 100% случаев.
Заключение. По результатам исследования рекомендовано опираться на уровень ИЛ-6 – ведущим в принятии решения о методе коррекции ИЦН, так как данный маркер обладает наибольшей чувствительностью и специфичностью по сравнению с остальными.
Актуальность. Различными клиническими формами пролапса гениталий страдают 34–56% женщин (например, в возрастной группе старше 40 лет пролапс имеется примерно у 50% женщин, и с возрастом процент увеличивается).
Хирургическое лечение является основным в лечении пролапса тазовых органов. В среднем 1/10 часть женщин пожилого возраста вынуждена оперироваться в связи с наличием пролапса тазовых органов. По поводу пролапса гениталий выполняется 15% «больших» гинекологических операции, а высокая вероятность рецидива (около 30% случаев) определяет необходимость вновь идти к врачу.
Пролапс гениталий – это заболевание, объединяющее группу нарушений связочного аппарата матки и влагалища, приводящее к опущению и выпадению внутренних половых органов, проявляющееся смещением гениталий до влагалищного входа или выпадением за его пределы.
Пролапс гениталий является результатом патологического перемещения тазовых органов из внутренней позиции наружу под действием внутрибрюшного давления с формированием характерных дефектов стенок и сводов влагалища. Возникает в результате несостоятельности соединительнотканных структур как следствие системной недостаточности, травматического повреждения тазового дна в процессе родов, нарушения синтеза стероидных гормонов, хронических заболеваний, сопровождающихся нарушением обменных процессов и микроциркуляции.
К факторам риска относятся:
• самопроизвольные роды и их количество;
• тяжелые физические нагрузки;
• гормональные нарушения;
• ожирение (индекс массы тела >30);
• гистерэктомия;
• системная дисплазия соединительной ткани.
Клинически проявляется в виде ощущения «инородного тела» в области вульварного кольца, чувства дискомфорта и «тяжести» в области промежности и в нижних отделах живота, боли, сексуальной дисфункции и/или диспареунии, декубитальных изменений на слизистых оболочках, расстройства мочеиспускания, акта дефекации.
К существующим хирургическим доступам относят: трансвагинальный, абдоминальный и лапароскопический (лапароскопическая пектопексия, лапароскопическая сакровагинопексия, лапароскопическая пектовагинопексия).
Лапароскопическая сакровагинопексия показана при коррекции передне- и заднеапикального, апикального пролапса, а также для восстановления физиологического направления влагалищной оси и сохранения влагалищной оси. Установка и фиксация сетки проводится в продольном направлении (ректовагинальное, пузырно-влагалищное пространство).
В настоящее время для определения выраженности пролапса используется классификация POP-Q. Принципы хирургической коррекции пролапса гениталий заключаются в восстановлении правильных анатомо-топографических взаимоотношений и нормализации функции органов, вовлеченных в патологический процесс, расположении органов (культей органов) в правильном анатомо-функциональном соотношении по отношению к стенкам таза, сохранении их в необходимой подвижности, создании влагалища достаточной длины и эластичности, воссоздании правильного соотношения леваторов и стенок влагалища, профилактике рецидивов (использование синтетических имплантируемых материалов – сетки), а также эластическая составляющая хирургии.
Из синтетических имплантируемых материалов используются проленовые, полиэстеровые сетки и титановый шелк.
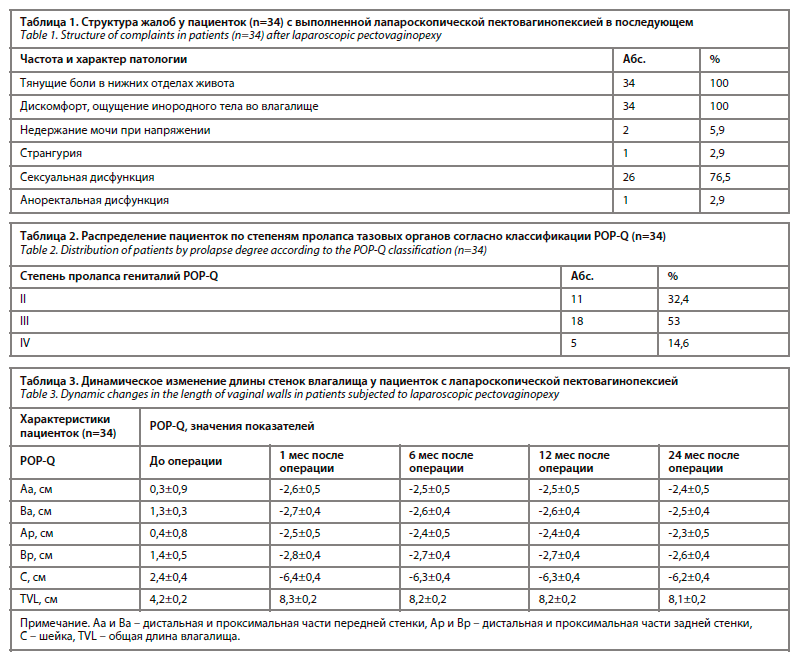
Дизайн исследования. Д.В. Брюниным были отобраны 34 пациентки с жалобами на тянущие боли в нижних отделах живота во время манифестации заболевания, дискомфорт, ощущение инородного тела во влагалище и боли в области промежности, сексуальную дисфункцию (табл. 1, 2).
Результаты
• Пектовагинопексия позволяет провести хирургическую коррекцию переднеапикального, апикального и заднеапикального пролапса гениталий.
• Пектовагинопексия, имея сопоставимый результат по коррекции пролапса путем сакровагинопексии, лишена хирургических рисков работы с «трудным» промонториумом и связанных с этим осложнений.
• Две точки фиксации поперечного имплантата создают более устойчивую на отрыв конструкцию.
• Комбинированная продольно-поперечная установка имплантатов позволяет увеличить длину влагалища и перераспределить вектор внутрибрюшного давления, что является профилактикой различных форм рецидива в дальнейшем (табл. 3).
 Доктор медицинских наук, профессор кафедры акушерства и гинекологии №1 Института клинической медицины им. Н.Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет) Т.А. Джибладзе рассказала о роли офисной гистероскопии в диагностике внутриматочной патологии.
Доктор медицинских наук, профессор кафедры акушерства и гинекологии №1 Института клинической медицины им. Н.Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет) Т.А. Джибладзе рассказала о роли офисной гистероскопии в диагностике внутриматочной патологии.
Актуальность проблемы. По статистике, частота внутриматочной патологии среди женщин с внутриматочными кровотечениями составляет до 87%, среди женщин с бесплодием до 38%, в постменопаузе 28%, до 30% случаев являются случайными находками ультразвукового исследования (УЗИ) и 14% – в результате гистероскопии соответственно.
В современных условиях малоинвазивные стационарозамещающие технологии все больше вытесняют традиционные диагностические и хирургические вмешательства, в том числе и в гинекологии.
Альтернативой для традиционной гистероскопии в последние два десятилетия стала офисная или амбулаторная гистероскопия, которая позволяет проводить большой спектр вмешательств без общей анестезии, расширения цервикального канала и наложения пулевых щипцов. С 1990-х годов офисная гистероскопия стала широко внедряться в практику гинекологов. Плюсами данного метода являются отсутствие воспалительных изменений, перфораций или кровотечений. Также этот метод не требует дополнительной травмы, практически безболезненно проводится в любом возрасте, а эффективность диагностики внутриматочной патологии достигает 98–100%.
Офисная гистероскопия не проводится при воспалительных заболеваниях органов малого таза, наличии достоверных эхо-признаков гиперплазии или полипа эндометрия, беременности, инвазивного рака шейки матки.
В большинстве случаев проводится в I фазу менструального цикла, кроме диагностических исследований в лечении бесплодия – тогда гистероскопия выполняется и в I, и во II фазы цикла. Показаниями к проведению исследования являются: бесплодие, привычное невынашивание беременности, контроль после лечения внутриматочной патологии, подозрение на внутриматочные синехии, подозрение на гиперплазию эндометрия, подозрение на полипы эндометрия и эндоцервикса, подозрение на хронический эндометрит, дифференциальная диагностика внутриматочной патологии.
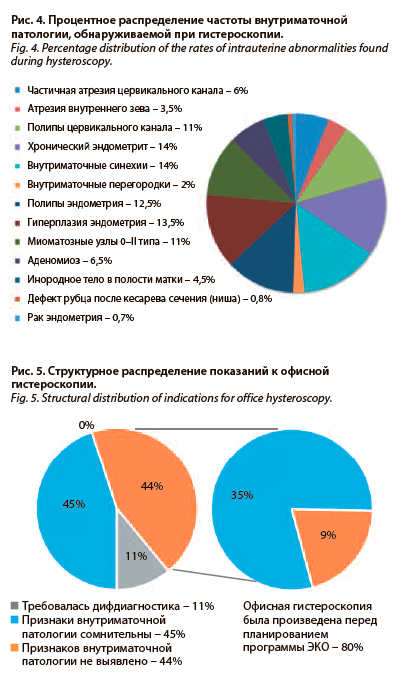
Статистически при обследовании по поводу бесплодия и привычного невынашивания офисной гистероскопией чаще всего выявляется гиперплазия эндометрия, хронический эндометрит и внутриматочные синехии, а также полипы цервикального канала (рис. 4).
Амбулаторное лечение внутриматочной патологии возможно у пациенток с частичной атрезией цервикального канала, единичными мелкими полипами эндоцервикса и эндометрия и тонкими внутриматочными синехиями. Маточные хирургические вмешательства осуществляются с помощью хирургических лазеров с доставкой излучения гибкими световолоконными системами диаметром 400, 600 мкм через операционный канал гистероскопа.
Заключение. Таким образом, офисная гистероскопия позволяет с высокой точностью диагностировать различные виды внутриматочной патологии у пациенток всех возрастных групп и в ряде случаев провести ее лечение без анестезии и дополнительной травматизации, а также осуществить контроль после лечения (рис. 5).
Возможность проведения диагностики и лечения в амбулаторных условиях позволяет избежать у пациенток дополнительных стрессов, связанных с госпитализацией и наркозом.
Актуальность проблемы. Заболевания вульвы являются областью междисциплинарного взаимодействия врачей-акушеров-гинекологов, дерматовенерологов, онкологов, врачей-иммунологов и др.
По статистике, частота плоскоклеточного рака вульвы (VSCC) составляет 1–2:100 000 населения и увеличивается с каждым годом. В настоящее время выявлен ВПЧ-зависимый и ВПЧ-независимый пути развития вульварно-эпителиальной неоплазии (VSCC), а также доказана причинно-следственная связь между вирусом папилломы человека (ВПЧ) и интраэпителиальной неоплазией высокой степени (HSIL), раком вульвы и полового члена.
На сегодняшний день классификация опухолей шейки матки претерпевает изменения (табл. 4).

 ВПЧ статус и иммуногистохимическое исследование (ИГХ) при обнаружении злокачественных новообразований (ЗНО) имеет большое значение в дальнейшей тактике ведения пациента (табл. 5). Поэтому необходимой манипуляцией в случае обнаружения любого патологического процесса является панч-биопсия и дальнейшее гистологическое исследование.
ВПЧ статус и иммуногистохимическое исследование (ИГХ) при обнаружении злокачественных новообразований (ЗНО) имеет большое значение в дальнейшей тактике ведения пациента (табл. 5). Поэтому необходимой манипуляцией в случае обнаружения любого патологического процесса является панч-биопсия и дальнейшее гистологическое исследование.
Докладчиками представлен ряд клинических случаев из работы отделения эстетической гинекологии и реабилитации.
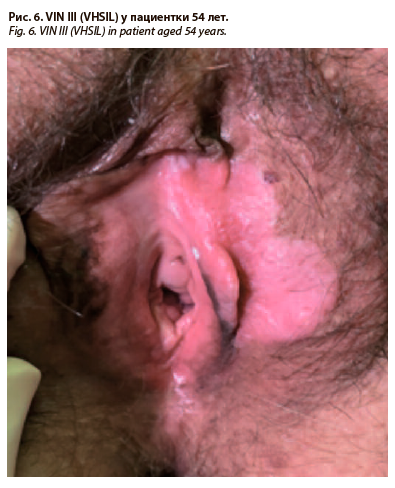
Клинический случай 1. Пациентка, 58 лет, обратилась с жалобами на высыпания на половой губе слева с 50 лет, сопровождавшихся зудом и болью (рис. 6). Менопауза с 54 лет. В анамнезе: ВПЧ 16-го типа, обнаруженный при цитологическом исследовании шейки матки в 2012 г. Получала симптоматическое лечение у врача-дерматовенеролога, акушера-гинеколога.
При вульвоскопии и окрашивании вульвы раствором Люголя было обнаружено равномерное окрашивание большой половой губы слева (за исключением внутренней поверхности) и наружной поверхности малой половой губы слева, вплоть до головки клитора (общая площадь лейкоплакии около 15–22 мм).
14.12.2021 врачом акушером-гинекологом была произведена биопсия вульвы, при гистологическом исследовании – участок 7×3×2 мм, VIN II, паракератоз вульвы, хронический умеренно активный вульвит, в краях резекции фокусы неоплазии.
По результатам пересмотра стекол в онкодиспансере в г. Балашиха от 10.01.2022 был обнаружен фрагмент фиброзной ткани с хроническим воспалением, покрытый метапластическим эпителием с акантозом, гиперкератозом, очагами дисплазии 2–3 ст., в краях резекции признаки дисплазии VIN 2–3 ст. Рекомендована лазерная фотодеструкция очага.
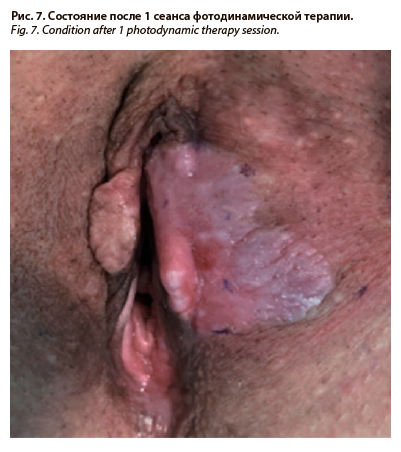
В результате первого сеанса отмечен выраженный положительный эффект (рис. 7).
Заключение. Фотодинамическую терапию (ФТД) из-за ее отличного косметического эффекта, отсутствия осложнений в виде рубцевания или изменения структуры и функции обрабатываемых тканей следует проводить в качестве терапии, предшествующей более инвазивным процедурам. Также к достоинствам метода отнесли возможность проведения ее в амбулаторных условиях.
При фотодинамической терапии сохраняется анатомо-функциональная полноценность органов. Основным недостатком метода является возможная болезненность, а раннее прекращение лечения из-за плохой переносимости может снизить терапевтическую эффективность. Другие недостатки фотодинамической терапии включают отсутствие ее доступности для некоторых пациентов, а также потенциал развития эритемы или эрозий, риск рецидива или прогрессирования в рак вульвы, если процедура неэффективна.
Современным определением синдрома, объединяющего состояния вульвовагинальной атрофии, является генитоуринарный менопаузальный синдром (ГУМС), который может быть вызван как длительным приемом гормональных контрацептивов, так и проявляться вследствие перенесенного гинекологического рака или периодом лактации.
Клинический случай 2. Пациентка 60 лет обратилась на прием с жалобами на сухость, жжение вульвы, сужение влагалища, диспареунию, дизурию в течение 7 лет.
Из анамнеза: постменопауза 7 лет. Цитологическое исследование шейки матки от 2020 г. – NILM. УЗИ органов малого таза 25.02.2021 – остаточные проявления внутреннего эндометриоза.
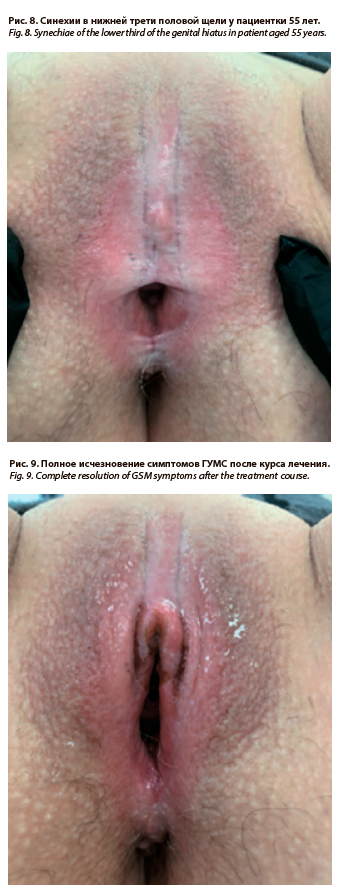
При осмотре: pH=5,5. Синехии в нижней трети половой щели, потеря дифференцировки малых или больших половых губ. Введение зеркала для осмотра невозможно. Слизистая сухая, снижена эластичность, при контакте – трещины и петехии (рис. 8).
Пациентка консультирована совместно с дерматологом – для верификации диагноза решено провести биопсию вульвы.
После осмотра был выставлен диагноз: ГУМС тяжелой степени. Синехии больших и малых половых губ. Красный плоский лишай вульвы?
Назначена местная терапия кремом, содержащим эстриол, рассечение синехий хирургическим СО2 лазером ДЭКА с последующим введением вагинальных расширителей, а также PRP-терапия 1 раз в месяц №3.
После окончания лечения пациенткой был отмечен выраженный эстетический и функциональный эффекты: устранение сухости, зуда и дизурии (рис. 9).
Заключение. Аппаратная и эстетическая гинекология являются относительно новыми, перспективными направлениями специальности. Малоинвазивность и удобство применения данных методик позволяют достигнуть выраженных положительных результатов в лечении пациенток с ВПЧ-ассоциированными заболеваниями вульвы, ГУМС, синехиями больших и малых половых губ, а также красного плоского лишая.
Актуальность проблемы. Сохранение репродуктивного здоровья у онкологических больных стало возможным благодаря их успешному лечению у врачей-онкологов, независимо от локализации опухоли.
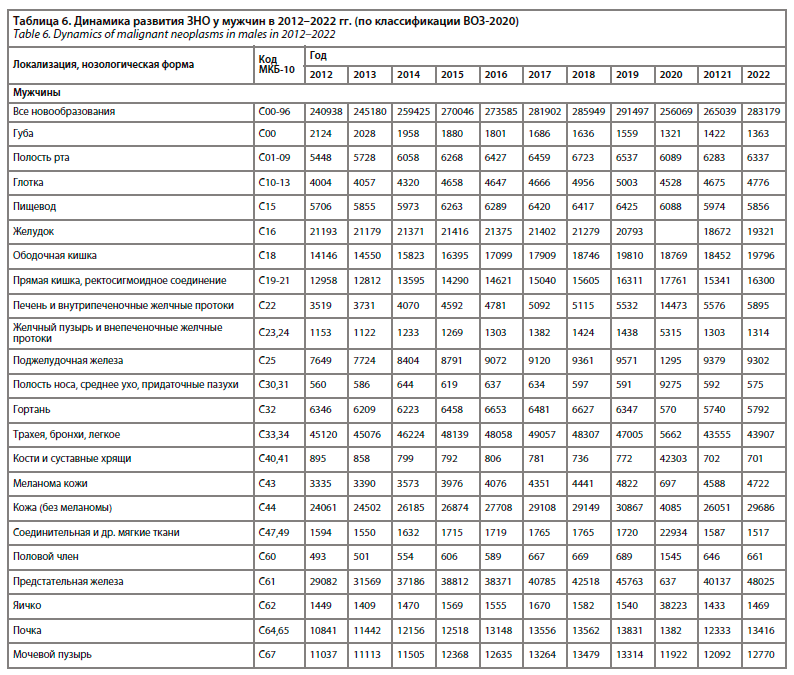
В настоящее время реабилитация онкологических больных является одним из самых перспективных направлений отрасли. Статистически отмечен значительный рост числа злокачественных новообразований (ЗНО) у женщин и мужчин между 2020 и 2022 г. (табл. 6, 7).
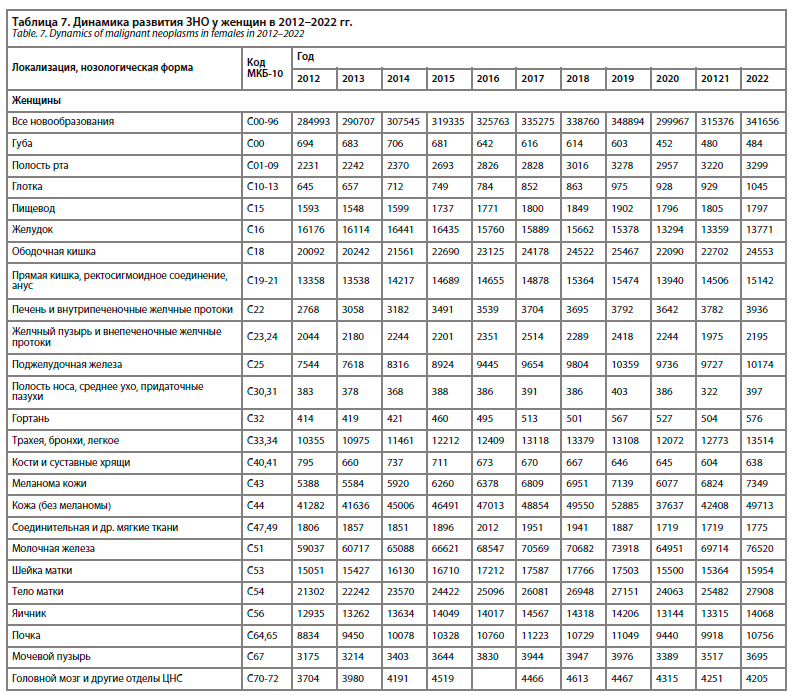
Ведущими локализациями в общей структуре онкологической заболеваемости являются: кожа, кроме меланомы (12,7%), молочная железа (12,3%), трахея, бронхи, легкое (9,2%), предстательная железа (7,5%), ободочная кишка (7,1%), желудок (5,3%), прямая кишка, ректосигмоидное соединение, анус (5,0%), лимфатическая и кроветворная ткани (4,6%), тело матки (4,5%), почка (3,9%), поджелудочная железа (3,1%), мочевой пузырь (2,6%), шейка матки (2,6%), яичник (2,3%).
У мужчин значимую по удельному весу группу составляют злокачественные опухоли органов мочеполовой системы, составляя 27% всех злокачественных новообразований. Наибольший удельный вес в структуре онкологической заболеваемости у женщин имеют злокачественные новообразования органов репродуктивной системы (40,1%), при этом опухоли половых органов составляют 17,7% всех злокачественных новообразований у женщин.
У всех заболевших в возрасте до 30 лет наиболее часто развиваются гемобластозы (32,7%), опухоли щитовидной железы (10,5%), злокачественные опухоли головного мозга и других отделов нервной системы (9,5%), костей и суставных хрящей (4,1%), яичника (4,1%), яичка (4,1%), шейки матки (3,6%), соединительной и других мягких тканей (3,6%), почки (3,0%). В возрастной группе 30–59 лет наибольший удельный вес имеют злокачественные новообразований молочной железы (17,8%), кожи, кроме меланомы (8,0%), шейки матки (6,0%), тела матки (5,4%), лимфатической и кроветворной тканей (5,2%), ободочной кишки (4,9%), щитовидной железы (4,7%), прямой кишки, ректосигмоидного соединения.
ЗНО являются приоритетной проблемой здравоохранения, так как наблюдается неуклонный рост общей заболеваемости онкологией, в первую очередь за счет увеличения выявляемости. Отмечено, что немалую часть онкологической заболеваемости составляют опухоли репродуктивной системы. Тревожным фактом является то, что около 1/3 онкологических больных составляют лица молодого возраста.
В связи с трендом на отложенное материнство все чаще онкологические заболевания сочетаются с беременностью. Сочетание онкологического процесса вместе с беременностью является сложнейшей клинической задачей для врача, так как в этом случае сочетаются сразу 3 самостоятельных процесса: организм матери, развивающийся плод и онкологическое заболевание. Согласно исследованиям, биологические свойства эмбриональных клеток и опухоли, такие как способность к имплантации, инвазивному росту и способность к аутосекреции у раковых и эмбриональных клеток схожи. Таким образом, ранний онкосфероид по своей гистроструктуре, гетерогенности клеточной популяции, спектру антигенов, биохимическим и патофизиологическим параметрам – это микромодель бластоцисты, находящейся на аваскулярной стадии развития.
Согласно статистике, в 2022 г. смертность от рака репродуктивных органов составила 8178 человек, а смертность от рака по всем локализациям составила 15 754 человека. Необоснованные овариоэктомии составляют 36–42%. Через год после химиотерапевтического лечения яичники теряют свою функциональную активность на 15–18%. Вместе с этим, по словам Л.А. Ашрафяна, порядка 83% женщин готовы прервать лечение от онкологических заболеваний ради возможности выносить беременность и родить ребенка. Согласно проведенным исследованиям, число которых достигает 50 тыс., забор биологического материала не влияет на течение онкологического процесса и фертильность женщины в дальнейшем.
Заключение. В настоящее время клинической проблемой является отсутствие персонализированного подхода к ведению пациентки репродуктивного возраста, а именно: проведение радикальных оперативных вмешательств, химио- и лучевой терапии без предварительного забора биологического материала женщины. Перспективным направлением является поиск персонализированных схем лечения онкологических больных, в том числе и во время беременности, а также реабилитации и сохранения генетического материала после химиотерапии, лучевого или хирургического лечения.
Таким образом, представленные доклады демонстрируют актуальные исследования по репродуктивной медицине, прогнозированию и своевременному лечению различных осложнений беременности пациенток групп высокого риска. Также особого внимания заслуживают новые способы хирургического, аппаратного, малоинвазивного и консервативного лечения заболеваний органов малого таза у женщин, поиск персонализированного подхода к терапии и сохранению репродуктивного потенциала онкологических больных. Новейшие исследования, разработки и технологии призваны улучшить качество оказания медицинской помощи, и могут быть использованы в будущем практикующими врачами.
Поступила в редакцию: 22.02.2024
Поступила после рецензирования: 01.03.2024
Принята к публикации: 14.03.2024
Received: 22.02.2024
Revised: 01.03.2024
Accepted: 14.03.2024
First Sechenov International Motherhood and Childhood Forum: achievements, challenges, prospects
Abstract
The paper provides the review of materials of the 1st Sechenov International Motherhood and Childhood Forum that took place on February 15–16 at the I.M. Sechenov First Moscow State Medical University. The event was held within the framework of the PRIORITY 2030 presidential program that was intended to create the world-class research medical university by the year 2030. Lectors presented the results of original research focused on the issues of preterm birth and miscarriage, preservation of fertility in cancer patients, early diagnosis of preeclampsia and isthmic-cervical incompetence, new methods for surgical treatment of genital prolapse, as well as the role of minimally invasive techniques in the diagnosis of intrauterine abnormalities. The reports of N.S. Trifonova et al., E.V. Timokhina, S.V. Pesegova, D.V. Bryunin, T.A. Jibladze, I.A. Apolikhina, I.V. Reshetov, and L.A. Ashrafyan deserve special attention.
Keywords: obstetrics, gynecology, in vitro fertilization, pregnancy, isthmic-cervical incompetence, preeclampsia, genitourinary syndrome of menopause, atrophy, human papillomavirus, oncology, pelvic organ prolapse.
For citation: First Sechenov International Motherhood and Childhood Forum: achievements, challenges, prospects. Clinical review for general practice. 2024; 5 (3): 119–130. (In Russ.). DOI: 10.47407/kr2023.5.3.00381
Вступление
 В статье представлен обзор материалов I Сеченовского международного форума материнства и детства, состоявшегося 15–16 февраля 2024 г. на базе ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова». Данное мероприятие проходило в рамках президентской программы «Приоритет-2030», которая призвана создать Исследовательский медицинский университет мирового уровня к 2030 г. Уникальность форума — это акцент на инновационные российские достижения в области охраны здоровья женщин и детей для улучшения качества оказания медицинской помощи и профилактики развития осложнений.
В статье представлен обзор материалов I Сеченовского международного форума материнства и детства, состоявшегося 15–16 февраля 2024 г. на базе ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова». Данное мероприятие проходило в рамках президентской программы «Приоритет-2030», которая призвана создать Исследовательский медицинский университет мирового уровня к 2030 г. Уникальность форума — это акцент на инновационные российские достижения в области охраны здоровья женщин и детей для улучшения качества оказания медицинской помощи и профилактики развития осложнений.Беременность после экстракорпорального оплодотворения и риски преждевременных родов
Профессор кафедры акушерства и гинекологии №1 Института клинической медицины им. Н.Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет), доктор медицинских наук Н.С. Трифонова и соавторы рассказали о рисках преждевременных родов при беременности, наступившей в результате экстракорпорального оплодотворения (ЭКО).Актуальность. По оценке Всемирной организации здравоохранения (ВОЗ), проблема бесплодия затрагивает порядка 190 млн человек в мире. На сегодняшний день вспомогательные репродуктивные технологии (ВРТ) стали распространенной процедурой, с помощью которой рождаются тысячи детей по всему миру. По данным РАРЧ, доля преодоления бесплодия с помощью ВРТ составила 2,7% в 2021 г. и 2,4% в 2020 г. Доля циклов ВРТ продолжает расти с каждым годом, особенно циклов ВРТ с донорской яйцеклеткой. По данным РАРЧ, доля циклов ВРТ за 2021 г. выросла на 8,7 %, доля циклов с донорской яйцеклеткой – на 6,7%. Однако статистически беременность после ЭКО сопровождается более высокой частотой акушерских осложнений, в том числе и преждевременными родами.
В соответствии с последним информационным бюллетенем ВОЗ, осложнения в результате преждевременных родов являются основной причиной смерти детей в возрасте до 5 лет. В Болонском университете в 2018 г. был проведен метаанализ, содержащий 15 когортных исследований, в который было включено порядка 61 677 одноплодных беременностей, закончившихся родами. По результатам исследования, риск спонтанных преждевременных родов у женщин, чья беременность наступила в результате ЭКО, был выше на 80%, чем у пациенток с самостоятельно наступившей беременностью. Ученые из университета Аристотеля в Греции также провели метаанализ из 9 исследований женщин с одноплодной беременностью, наступившей в результате ЭКО. Ученые выяснили, что у женщин, чья беременность наступила в результате ВРТ, риск спонтанных преждевременных родов также выше в 2 раза. Международная группа исследователей из Китая и Германии провели оценку течения беременности после ЭКО у 4328 женщин. В результате были названы 7 независимых факторов преждевременных родов: возраст менее 25 лет или более 39 лет, многоплодная беременность, предлежание плаценты, редукция эмбрионов, гестационная артериальная гипертензия, повышение уровня триглицеридов, укорочение активированного частичного тромбопластинового времени. В Университете Копенгагена ученые провели исследование женщин с донорской яйцеклеткой и выявили большой риск акушерских осложнений, особенно преждевременных родов и детей с низкой массой тела при рождении.
В исследовании, проведенном доктором медицинских наук, профессором Н.С. Трифоновой, кандидатом медицинских наук. Э.В. Жуковой и ассистентом кафедры К.И. Лаврентьевой, на базе клиники акушерства и гинекологии имени В.Ф. Снегирева Университетской клинической больницы №2 приняли участие 1101 пациентка, из которых 895 пациенток были после различных программ ЭКО: собственные ооциты, донорские яйцеклетки и суррогатные матери. В результате выяснено, что частота угрозы преждевременных родов до 34 нед, а также осложнений беременности, таких как истмико-цервикальная недостаточность, артериальная гипертензия, задержка роста плода, внутрипеченочный холестаз, тяжелая преэклампсия (ПЭ) и преждевременная отслойка нормально расположенной плаценты во II и III триместрах была выше у женщин с донорской яйцеклеткой и составила 57,3%. Дети, рожденные в результате ЭКО с донорской яйцеклеткой, статистически имели более низкую массу тела при рождении и более низкую оценку по шкале Апгар. Перинатальная смертность также была статистически выше в группе суррогатного материнства (рис. 1).


Особое внимание в исследовании заслуживает отсутствие ремоделирования спиральных артерий у порядка 1/3 пациенток с беременностью, наступившей после ЭКО (рис. 2).
Также представлено несколько клинических случаев пациенток, наблюдавшихся в клинике акушерства и гинекологии.
Клинический случай №1. Пациентка М., 29 лет. Перенесенные заболевания: детские инфекции, миопия слабой степени.
Предыдущие беременности:
• I беременность – своевременные самопроизвольные роды, без осложнений;
• II беременность – программа «Суррогатное материнство», неразвивающаяся беременность;
• III беременность – программа «Суррогатное материнство», преждевременные оперативные роды
в 35 нед, преждевременный разрыв плодных оболочек, тазовое предлежание плода (мальчик 2590 г,
47 см, 7–8 баллов);
• IV беременность – программа «Суррогатное материнство», дихориальная диамниотическая двойня, протекала с явлениями угрозы прерывания беременности.
Поступила в Клинику акушерства и гинекологии им. В.Ф. Снегирева с жалобами на излитие околоплодных вод.
Диагноз при поступлении: беременность 30–31 нед (ЭКО). Суррогатное материнство. Дихориальная диамниотическая двойня. Косое положение I плода. Преждевременный разрыв плодных оболочек. Рубец на матке после операции кесарево сечение в 2015 г.
Выполнена операция: поперечное надлобковое чревосечение с иссечением старого кожного рубца. Кесарево сечение в нижнем маточном сегменте.
I – мальчик 1450 г, 40 см, 6–7 баллов
II – мальчик 1687 г, 39 см, 6–7 баллов.
Клинический случай №2. Пациентка К., 34 лет. Перенесенные заболевания: детские инфекции, хронический бронхит.
Предыдущие беременности:
• I беременность – своевременные самопроизвольные роды, без осложнений;
• II беременность – программа «Суррогатное материнство», преждевременные самопроизвольные роды в 35 нед, ПЭ (девочка 2320 г, 48 см, 7–8 баллов).
• III беременность – программа «Суррогатное материнство», дихориальная диамниотическая двойня, протекала с явлениями угрозы прерывания беременности, гестационная артериальная гипертензия с 20 нед.
Поступила в Клинику акушерства и гинекологии им. В.Ф. Снегирева с жалобами на отеки голеней и стоп, повышение артериального давления (АД) до 160/100 мм рт. ст.
При обследовании выявлены явления холестаза беременных: щелочная фосфатаза (ЩФ) – 441 ед/л, полиненасыщенные жирные кислоты (ЖК) – 14,7 мкмоль /л. Проводилась комплексная терапия.
Жалобы на тяжесть в затылочной области, кожный зуд, АД – 150/100 мм рт. ст. Белок в моче – 1 г/л, ЩФ – 492 ед/л, ЖК – 76,7 мкмоль/л.
Клинический диагноз: беременность 34–35 нед (ЭКО). Суррогатное материнство. Дихориальная диамниотическая двойня. Головное предлежание I плода. ПЭ тяжелой степени. Холестаз беременных.
Выполнена операция: поперечное надлобковое чревосечение. Кесарево сечение в нижнем маточном сегменте.
I – мальчик 2160 г, 46 см, 7–8 баллов.
II – девочка 2370 г, 47 см, 7–8 баллов.
Заключение. Таким образом, применение вспомогательных репродуктивных технологий позволило качественно повысить уровень оказания медицинской помощи парам с бесплодием. Однако пациентки, чья беременность наступила в результате ЭКО с собственным или аллогенным генетическим материалом, заслуживают особого внимания и применения персонализированного подхода.
Современная концепция патогенеза
и прогнозирования различных вариантов преэклампсииДоктор медицинских наук, доцент, профессор кафедры акушерства, гинекологии и перинатологии
Института клинической медицины им. Н.Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет), Е.В. Тимохина представила современную концепцию патогенеза и прогнозирования различных вариантов ПЭ.
Актуальность. По статистике, у 10 млн женщин ежегодно диагностируется ПЭ, 76 тыс. беременных женщин в мире ежегодно умирают от ПЭ и связанных с ней гипертензивных осложнений. На сегодняшний день принята концепция двухэтапного развития ПЭ, закладывания в I триместре генеза ПЭ, когда происходит инвазия трофобласта, гестационная трансформация спиральных артерий.
К факторам риска ПЭ относятся:
• иммунные факторы: первобеременные, наступление беременности менее чем через 1 год совместного проживания, беременность от нового партнера, интергравидарный интервал >10 лет;
• генетические факторы: наличие ПЭ у матери, сестры, партнер, рожденный от беременности с ПЭ;
• заболевания матери: избыточная масса тела/ожирение, хроническая артериальная гипертензия, сахарный диабет 1 и 2-го типа, антифосфолипидный синдром, заболевания почек, коллагенозы.
Как выделить факторы риска? Существующие клинические рекомендации во всем мире, источником которых является Фетальный фонд медицины, рекомендуют оценивать факторы риска уже в I триместре.
К ним относятся измерение среднего АД и допплерометрическая оценка кровотока в маточных артериях уже в 11–13 нед беременности (пульсационный индекс маточных артерий). Это повышает чувствительность и специфичность прогностических действий, поэтому дальнейшие метаболомические исследования, такие как ростовой фактор роста, плацентарный фактор роста, а также протеин, ассоциированный с беременностью, повышает дальнейшие шансы. Последние наблюдения показали, что включение таких факторов, как растворимый тирозинкиназный рецептор и плацентарный протеин, связанный с беременностью, являются дорогостоящими, но прогностически не слишком важными.
Согласно исследованию, проведенном на кафедре, матриксные металлопротеиназы (ММП) принимают участие в патогенезе как 1-го, так и 2-го этапа развития ПЭ, обладают огромным протеолитическим потенциалом, разрушают соединительнотканный матрикс, участвуют в инвазии и перестройке артерий. Целью исследования явилось определение прогностической значимости МПП-2 и ММП-9 как ранних маркеров ПЭ
в I триместре.
Проведено проспективное исследование 310 пациенток с 11-й по 13-ю неделю беременности за период 2017–2019 гг. Методом иммуноферментного анализа (ИФА) определен уровень ММП-2 и ММП-9 в венозной крови с единицей измерения нг/мл. ПЭ развилась у 34 пациенток, в то время как неосложненное течение беременности наблюдалось у 229 пациенток. Согласно результатам, при развитии ПЭ уровень МПП-2 уже в I триместре в 2 раза выше, чем при неосложненной беременности. В то же время при последующем развитии ПЭ уровень МПП-9 достоверно ниже уже в I триместре.
Установлено, что ММП-2>102 нг/мл уже в I триместре (11–13 нед.) предсказывает развитие ПЭ с чувствительностью 88,24% и специфичностью 82,76%. При концентрации ММП-2 более 380 нг/мл прогнозируется нарастание тяжести ПЭ с чувствительностью и специфичностью метода 70% и 85% соответственно.
МПП-9<980 нг/мл является пороговой для прогнозирования ПЭ в I триместре с чувствительностью 85,29% и специфичностью 84,48%.
Заключение. В результате метаболомного исследования доказано, что ММП принимают участие как в ключевых процессах I триместра беременности, так и могут быть использованы как потенциальные маркеры развития, нарастания тяжести и прогностического маркера ПЭ.
Выбор метода коррекции истмико-цервикальной недостаточности на основании маркеров интраамниального воспаления в цервикальной жидкости
Кандидат медицинских наук, ассистент кафедры акушерства, гинекологии и перинатологии Института клинической медицины им. Н. Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет) С.В. Песегова предоставила алгоритм выбора метода коррекции истмико-цервикальной недостаточности (ИЦН) на основании маркеров интраамниального воспаления в цервикальной жидкости.Актуальность. К факторам, вызывающим преждевременные роды, относят: воспалительный процесс, включая асептическое воспаление, дисплазию соединительной ткани и коллагеновых волокон, отягощенный акушерско-гинекологический анамнез (осложнения, потери беременности и т.д.), полиморфизм генов, ответственных за соединительную ткань, гормональные нарушения, генитальный инфантилизм, врожденное укорочение шейки матки или приобретенные деформации шейки матки. ИЦН может возникать и у соматически здоровых пациенток с неотягощенным анамнезом.
ИЦН – бессимптомное осложнение беременности. Зачастую, когда появляется первая симптоматика, проводить какую-либо коррекцию поздно, поэтому УЗ-цервикометрия, начиная с I триместра, обязательна. К основным методам диагностики ИЦН относят трансвагинальную цервикометрию (ТВУЗИ-цервикометрия).
Не менее 80% ИЦН ассоциированы с интраамниальным воспалением, поскольку барьерная функция цервикальной слизи при укорочении шейки матки и расширении цервикального канала нарушается и возникает асептическое воспаление.
Цель исследования. Оценить уровень маркеров интраамниального воспаления [интерлейкин (ИЛ)-6, ИЛ-8, МПП-8] в цервикальной жидкости для разработки персонифицированного подхода к ведению пациенток с данным осложнением беременности. Ведение беременности осуществлялось в соответствии с Приказом МЗ РФ №1130н и клиническим рекомендациям «Нормальная беременность».
В ходе наблюдения определены уровни ИЛ-6, ИЛ-8, МПП-8 в цервикальной жидкости методом ИФА (примерно 23 нед гестации), определены пороговые величины ИЛ-6, ИЛ-8, МПП-8, указывающие на высокий риск экстремально ранних и ранних преждевременных родов. В исследование были включены 2 группы – основная группа (беременные с ИЦН, n=95) и контрольная группа (беременные без признаков ИЦН, n=31), у которых использовался только микронизированный прогестерон.

Результаты. В основной группе: у 40% пациенток роды завершились своевременно, у 4,2% – поздний самопроизвольный выкидыш и у 56% беременность закончилась преждевременными родами в различные сроки гестации (рис. 3). Медиана срока родоразрешения в основной группе составила 33,0 нед, а в группе контроля – 38,0 нед (p<0,001). У всех беременных группы контроля беременность завершилась своевременными родами (100%).
Маркеры интраамниального воспаления у пациенток из основной группы и группы контроля значительно различались. Уровень маркеров пропорционально возрастал сроку преждевременного родоразрешения. Хорионамнионит клинически был у 7,4% пациенток и у 38,9% гистологически.
Экстремально ранние и ранние преждевременные роды развивались у пациенток с ИЛ-6>11,1 пг/мл, ИЛ-8>275,4 пг/мл, МПП-8>26,1 нг/мл – преждевременные роды раньше 32 нед в 100% случаев.
Заключение. По результатам исследования рекомендовано опираться на уровень ИЛ-6 – ведущим в принятии решения о методе коррекции ИЦН, так как данный маркер обладает наибольшей чувствительностью и специфичностью по сравнению с остальными.
Лапароскопия в хирургии тазового пролапса: комбинированные подходы
Доктор медицинских наук, профессор кафедры акушерства и гинекологии №1 Института клинической медицины им. Н.Ф. Склифосовского, заведующий гинекологическим отделением клиники акушерства и гинекологии Д.В. Брюнин представил новый комбинированный подход в лапароскопической хирургии тазового пролапса.Актуальность. Различными клиническими формами пролапса гениталий страдают 34–56% женщин (например, в возрастной группе старше 40 лет пролапс имеется примерно у 50% женщин, и с возрастом процент увеличивается).
Хирургическое лечение является основным в лечении пролапса тазовых органов. В среднем 1/10 часть женщин пожилого возраста вынуждена оперироваться в связи с наличием пролапса тазовых органов. По поводу пролапса гениталий выполняется 15% «больших» гинекологических операции, а высокая вероятность рецидива (около 30% случаев) определяет необходимость вновь идти к врачу.
Пролапс гениталий – это заболевание, объединяющее группу нарушений связочного аппарата матки и влагалища, приводящее к опущению и выпадению внутренних половых органов, проявляющееся смещением гениталий до влагалищного входа или выпадением за его пределы.
Пролапс гениталий является результатом патологического перемещения тазовых органов из внутренней позиции наружу под действием внутрибрюшного давления с формированием характерных дефектов стенок и сводов влагалища. Возникает в результате несостоятельности соединительнотканных структур как следствие системной недостаточности, травматического повреждения тазового дна в процессе родов, нарушения синтеза стероидных гормонов, хронических заболеваний, сопровождающихся нарушением обменных процессов и микроциркуляции.
К факторам риска относятся:
• самопроизвольные роды и их количество;
• тяжелые физические нагрузки;
• гормональные нарушения;
• ожирение (индекс массы тела >30);
• гистерэктомия;
• системная дисплазия соединительной ткани.
Клинически проявляется в виде ощущения «инородного тела» в области вульварного кольца, чувства дискомфорта и «тяжести» в области промежности и в нижних отделах живота, боли, сексуальной дисфункции и/или диспареунии, декубитальных изменений на слизистых оболочках, расстройства мочеиспускания, акта дефекации.
К существующим хирургическим доступам относят: трансвагинальный, абдоминальный и лапароскопический (лапароскопическая пектопексия, лапароскопическая сакровагинопексия, лапароскопическая пектовагинопексия).
Лапароскопическая сакровагинопексия показана при коррекции передне- и заднеапикального, апикального пролапса, а также для восстановления физиологического направления влагалищной оси и сохранения влагалищной оси. Установка и фиксация сетки проводится в продольном направлении (ректовагинальное, пузырно-влагалищное пространство).
В настоящее время для определения выраженности пролапса используется классификация POP-Q. Принципы хирургической коррекции пролапса гениталий заключаются в восстановлении правильных анатомо-топографических взаимоотношений и нормализации функции органов, вовлеченных в патологический процесс, расположении органов (культей органов) в правильном анатомо-функциональном соотношении по отношению к стенкам таза, сохранении их в необходимой подвижности, создании влагалища достаточной длины и эластичности, воссоздании правильного соотношения леваторов и стенок влагалища, профилактике рецидивов (использование синтетических имплантируемых материалов – сетки), а также эластическая составляющая хирургии.
Из синтетических имплантируемых материалов используются проленовые, полиэстеровые сетки и титановый шелк.
Дизайн исследования. Д.В. Брюниным были отобраны 34 пациентки с жалобами на тянущие боли в нижних отделах живота во время манифестации заболевания, дискомфорт, ощущение инородного тела во влагалище и боли в области промежности, сексуальную дисфункцию (табл. 1, 2).

Результаты
• Пектовагинопексия позволяет провести хирургическую коррекцию переднеапикального, апикального и заднеапикального пролапса гениталий.
• Пектовагинопексия, имея сопоставимый результат по коррекции пролапса путем сакровагинопексии, лишена хирургических рисков работы с «трудным» промонториумом и связанных с этим осложнений.
• Две точки фиксации поперечного имплантата создают более устойчивую на отрыв конструкцию.
• Комбинированная продольно-поперечная установка имплантатов позволяет увеличить длину влагалища и перераспределить вектор внутрибрюшного давления, что является профилактикой различных форм рецидива в дальнейшем (табл. 3).
Офисная гистероскопия в диагностике внутриматочной патологии
 Доктор медицинских наук, профессор кафедры акушерства и гинекологии №1 Института клинической медицины им. Н.Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет) Т.А. Джибладзе рассказала о роли офисной гистероскопии в диагностике внутриматочной патологии.
Доктор медицинских наук, профессор кафедры акушерства и гинекологии №1 Института клинической медицины им. Н.Ф. Склифосовского ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет) Т.А. Джибладзе рассказала о роли офисной гистероскопии в диагностике внутриматочной патологии. Актуальность проблемы. По статистике, частота внутриматочной патологии среди женщин с внутриматочными кровотечениями составляет до 87%, среди женщин с бесплодием до 38%, в постменопаузе 28%, до 30% случаев являются случайными находками ультразвукового исследования (УЗИ) и 14% – в результате гистероскопии соответственно.
В современных условиях малоинвазивные стационарозамещающие технологии все больше вытесняют традиционные диагностические и хирургические вмешательства, в том числе и в гинекологии.
Альтернативой для традиционной гистероскопии в последние два десятилетия стала офисная или амбулаторная гистероскопия, которая позволяет проводить большой спектр вмешательств без общей анестезии, расширения цервикального канала и наложения пулевых щипцов. С 1990-х годов офисная гистероскопия стала широко внедряться в практику гинекологов. Плюсами данного метода являются отсутствие воспалительных изменений, перфораций или кровотечений. Также этот метод не требует дополнительной травмы, практически безболезненно проводится в любом возрасте, а эффективность диагностики внутриматочной патологии достигает 98–100%.
Офисная гистероскопия не проводится при воспалительных заболеваниях органов малого таза, наличии достоверных эхо-признаков гиперплазии или полипа эндометрия, беременности, инвазивного рака шейки матки.
В большинстве случаев проводится в I фазу менструального цикла, кроме диагностических исследований в лечении бесплодия – тогда гистероскопия выполняется и в I, и во II фазы цикла. Показаниями к проведению исследования являются: бесплодие, привычное невынашивание беременности, контроль после лечения внутриматочной патологии, подозрение на внутриматочные синехии, подозрение на гиперплазию эндометрия, подозрение на полипы эндометрия и эндоцервикса, подозрение на хронический эндометрит, дифференциальная диагностика внутриматочной патологии.
Статистически при обследовании по поводу бесплодия и привычного невынашивания офисной гистероскопией чаще всего выявляется гиперплазия эндометрия, хронический эндометрит и внутриматочные синехии, а также полипы цервикального канала (рис. 4).
Амбулаторное лечение внутриматочной патологии возможно у пациенток с частичной атрезией цервикального канала, единичными мелкими полипами эндоцервикса и эндометрия и тонкими внутриматочными синехиями. Маточные хирургические вмешательства осуществляются с помощью хирургических лазеров с доставкой излучения гибкими световолоконными системами диаметром 400, 600 мкм через операционный канал гистероскопа.
Заключение. Таким образом, офисная гистероскопия позволяет с высокой точностью диагностировать различные виды внутриматочной патологии у пациенток всех возрастных групп и в ряде случаев провести ее лечение без анестезии и дополнительной травматизации, а также осуществить контроль после лечения (рис. 5).
Возможность проведения диагностики и лечения в амбулаторных условиях позволяет избежать у пациенток дополнительных стрессов, связанных с госпитализацией и наркозом.
Оптимизация методов диагностики и лечения заболеваний вульвы у женщин
Доктор медицинских наук, профессор, заслуженный врач РФ, заведующая отделением эстетической гинекологии и реабилитации ФГБУ «НМИЦ АГП им. академика В.И. Кулакова» Минздрава России, профессор кафедры акушерства, гинекологии, перинатологии и репродуктологии ИПО ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет), президент Ассоциации специалистов по эстетической гинекологии (АСЭГ) И.А. Аполихина рассказала об оптимизации методов диагностики и лечения заболеваний вульвы у женщин.Актуальность проблемы. Заболевания вульвы являются областью междисциплинарного взаимодействия врачей-акушеров-гинекологов, дерматовенерологов, онкологов, врачей-иммунологов и др.
По статистике, частота плоскоклеточного рака вульвы (VSCC) составляет 1–2:100 000 населения и увеличивается с каждым годом. В настоящее время выявлен ВПЧ-зависимый и ВПЧ-независимый пути развития вульварно-эпителиальной неоплазии (VSCC), а также доказана причинно-следственная связь между вирусом папилломы человека (ВПЧ) и интраэпителиальной неоплазией высокой степени (HSIL), раком вульвы и полового члена.
На сегодняшний день классификация опухолей шейки матки претерпевает изменения (табл. 4).

 ВПЧ статус и иммуногистохимическое исследование (ИГХ) при обнаружении злокачественных новообразований (ЗНО) имеет большое значение в дальнейшей тактике ведения пациента (табл. 5). Поэтому необходимой манипуляцией в случае обнаружения любого патологического процесса является панч-биопсия и дальнейшее гистологическое исследование.
ВПЧ статус и иммуногистохимическое исследование (ИГХ) при обнаружении злокачественных новообразований (ЗНО) имеет большое значение в дальнейшей тактике ведения пациента (табл. 5). Поэтому необходимой манипуляцией в случае обнаружения любого патологического процесса является панч-биопсия и дальнейшее гистологическое исследование. Докладчиками представлен ряд клинических случаев из работы отделения эстетической гинекологии и реабилитации.
Клинический случай 1. Пациентка, 58 лет, обратилась с жалобами на высыпания на половой губе слева с 50 лет, сопровождавшихся зудом и болью (рис. 6). Менопауза с 54 лет. В анамнезе: ВПЧ 16-го типа, обнаруженный при цитологическом исследовании шейки матки в 2012 г. Получала симптоматическое лечение у врача-дерматовенеролога, акушера-гинеколога.
При вульвоскопии и окрашивании вульвы раствором Люголя было обнаружено равномерное окрашивание большой половой губы слева (за исключением внутренней поверхности) и наружной поверхности малой половой губы слева, вплоть до головки клитора (общая площадь лейкоплакии около 15–22 мм).
14.12.2021 врачом акушером-гинекологом была произведена биопсия вульвы, при гистологическом исследовании – участок 7×3×2 мм, VIN II, паракератоз вульвы, хронический умеренно активный вульвит, в краях резекции фокусы неоплазии.
По результатам пересмотра стекол в онкодиспансере в г. Балашиха от 10.01.2022 был обнаружен фрагмент фиброзной ткани с хроническим воспалением, покрытый метапластическим эпителием с акантозом, гиперкератозом, очагами дисплазии 2–3 ст., в краях резекции признаки дисплазии VIN 2–3 ст. Рекомендована лазерная фотодеструкция очага.
В результате первого сеанса отмечен выраженный положительный эффект (рис. 7).
Заключение. Фотодинамическую терапию (ФТД) из-за ее отличного косметического эффекта, отсутствия осложнений в виде рубцевания или изменения структуры и функции обрабатываемых тканей следует проводить в качестве терапии, предшествующей более инвазивным процедурам. Также к достоинствам метода отнесли возможность проведения ее в амбулаторных условиях.
При фотодинамической терапии сохраняется анатомо-функциональная полноценность органов. Основным недостатком метода является возможная болезненность, а раннее прекращение лечения из-за плохой переносимости может снизить терапевтическую эффективность. Другие недостатки фотодинамической терапии включают отсутствие ее доступности для некоторых пациентов, а также потенциал развития эритемы или эрозий, риск рецидива или прогрессирования в рак вульвы, если процедура неэффективна.
Современным определением синдрома, объединяющего состояния вульвовагинальной атрофии, является генитоуринарный менопаузальный синдром (ГУМС), который может быть вызван как длительным приемом гормональных контрацептивов, так и проявляться вследствие перенесенного гинекологического рака или периодом лактации.
Клинический случай 2. Пациентка 60 лет обратилась на прием с жалобами на сухость, жжение вульвы, сужение влагалища, диспареунию, дизурию в течение 7 лет.
Из анамнеза: постменопауза 7 лет. Цитологическое исследование шейки матки от 2020 г. – NILM. УЗИ органов малого таза 25.02.2021 – остаточные проявления внутреннего эндометриоза.

При осмотре: pH=5,5. Синехии в нижней трети половой щели, потеря дифференцировки малых или больших половых губ. Введение зеркала для осмотра невозможно. Слизистая сухая, снижена эластичность, при контакте – трещины и петехии (рис. 8).
Пациентка консультирована совместно с дерматологом – для верификации диагноза решено провести биопсию вульвы.
После осмотра был выставлен диагноз: ГУМС тяжелой степени. Синехии больших и малых половых губ. Красный плоский лишай вульвы?
Назначена местная терапия кремом, содержащим эстриол, рассечение синехий хирургическим СО2 лазером ДЭКА с последующим введением вагинальных расширителей, а также PRP-терапия 1 раз в месяц №3.
После окончания лечения пациенткой был отмечен выраженный эстетический и функциональный эффекты: устранение сухости, зуда и дизурии (рис. 9).
Заключение. Аппаратная и эстетическая гинекология являются относительно новыми, перспективными направлениями специальности. Малоинвазивность и удобство применения данных методик позволяют достигнуть выраженных положительных результатов в лечении пациенток с ВПЧ-ассоциированными заболеваниями вульвы, ГУМС, синехиями больших и малых половых губ, а также красного плоского лишая.
Современные технологии сохранения репродуктивного здоровья у онкологических больных
Академиком РАН, доктором медицинских наук, профессором кафедры онкологии, радиотерапии и реконструктивной хирургии, директором Института кластерной онкологии им. Л.Л. Левшина ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский университет) И.В. Решетовым и академиком РАН, доктором медицинских наук, профессором кафедры онкологии, радиотерапии и реконструктивной хирургии, директором Института кластерной онкологии им. Л.Л. Левшина ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет) Л.А. Ашрафяном были представлены современные технологии сохранения репродуктивного здоровья у онкологических больных.Актуальность проблемы. Сохранение репродуктивного здоровья у онкологических больных стало возможным благодаря их успешному лечению у врачей-онкологов, независимо от локализации опухоли.
В настоящее время реабилитация онкологических больных является одним из самых перспективных направлений отрасли. Статистически отмечен значительный рост числа злокачественных новообразований (ЗНО) у женщин и мужчин между 2020 и 2022 г. (табл. 6, 7).


Ведущими локализациями в общей структуре онкологической заболеваемости являются: кожа, кроме меланомы (12,7%), молочная железа (12,3%), трахея, бронхи, легкое (9,2%), предстательная железа (7,5%), ободочная кишка (7,1%), желудок (5,3%), прямая кишка, ректосигмоидное соединение, анус (5,0%), лимфатическая и кроветворная ткани (4,6%), тело матки (4,5%), почка (3,9%), поджелудочная железа (3,1%), мочевой пузырь (2,6%), шейка матки (2,6%), яичник (2,3%).
У мужчин значимую по удельному весу группу составляют злокачественные опухоли органов мочеполовой системы, составляя 27% всех злокачественных новообразований. Наибольший удельный вес в структуре онкологической заболеваемости у женщин имеют злокачественные новообразования органов репродуктивной системы (40,1%), при этом опухоли половых органов составляют 17,7% всех злокачественных новообразований у женщин.

У всех заболевших в возрасте до 30 лет наиболее часто развиваются гемобластозы (32,7%), опухоли щитовидной железы (10,5%), злокачественные опухоли головного мозга и других отделов нервной системы (9,5%), костей и суставных хрящей (4,1%), яичника (4,1%), яичка (4,1%), шейки матки (3,6%), соединительной и других мягких тканей (3,6%), почки (3,0%). В возрастной группе 30–59 лет наибольший удельный вес имеют злокачественные новообразований молочной железы (17,8%), кожи, кроме меланомы (8,0%), шейки матки (6,0%), тела матки (5,4%), лимфатической и кроветворной тканей (5,2%), ободочной кишки (4,9%), щитовидной железы (4,7%), прямой кишки, ректосигмоидного соединения.
ЗНО являются приоритетной проблемой здравоохранения, так как наблюдается неуклонный рост общей заболеваемости онкологией, в первую очередь за счет увеличения выявляемости. Отмечено, что немалую часть онкологической заболеваемости составляют опухоли репродуктивной системы. Тревожным фактом является то, что около 1/3 онкологических больных составляют лица молодого возраста.
В связи с трендом на отложенное материнство все чаще онкологические заболевания сочетаются с беременностью. Сочетание онкологического процесса вместе с беременностью является сложнейшей клинической задачей для врача, так как в этом случае сочетаются сразу 3 самостоятельных процесса: организм матери, развивающийся плод и онкологическое заболевание. Согласно исследованиям, биологические свойства эмбриональных клеток и опухоли, такие как способность к имплантации, инвазивному росту и способность к аутосекреции у раковых и эмбриональных клеток схожи. Таким образом, ранний онкосфероид по своей гистроструктуре, гетерогенности клеточной популяции, спектру антигенов, биохимическим и патофизиологическим параметрам – это микромодель бластоцисты, находящейся на аваскулярной стадии развития.
Согласно статистике, в 2022 г. смертность от рака репродуктивных органов составила 8178 человек, а смертность от рака по всем локализациям составила 15 754 человека. Необоснованные овариоэктомии составляют 36–42%. Через год после химиотерапевтического лечения яичники теряют свою функциональную активность на 15–18%. Вместе с этим, по словам Л.А. Ашрафяна, порядка 83% женщин готовы прервать лечение от онкологических заболеваний ради возможности выносить беременность и родить ребенка. Согласно проведенным исследованиям, число которых достигает 50 тыс., забор биологического материала не влияет на течение онкологического процесса и фертильность женщины в дальнейшем.
Заключение. В настоящее время клинической проблемой является отсутствие персонализированного подхода к ведению пациентки репродуктивного возраста, а именно: проведение радикальных оперативных вмешательств, химио- и лучевой терапии без предварительного забора биологического материала женщины. Перспективным направлением является поиск персонализированных схем лечения онкологических больных, в том числе и во время беременности, а также реабилитации и сохранения генетического материала после химиотерапии, лучевого или хирургического лечения.
Таким образом, представленные доклады демонстрируют актуальные исследования по репродуктивной медицине, прогнозированию и своевременному лечению различных осложнений беременности пациенток групп высокого риска. Также особого внимания заслуживают новые способы хирургического, аппаратного, малоинвазивного и консервативного лечения заболеваний органов малого таза у женщин, поиск персонализированного подхода к терапии и сохранению репродуктивного потенциала онкологических больных. Новейшие исследования, разработки и технологии призваны улучшить качество оказания медицинской помощи, и могут быть использованы в будущем практикующими врачами.
Поступила в редакцию: 22.02.2024
Поступила после рецензирования: 01.03.2024
Принята к публикации: 14.03.2024
Received: 22.02.2024
Revised: 01.03.2024
Accepted: 14.03.2024


