Клинический разбор в общей медицине №9 2024
The review provides reviews of original reports and research focused on the issue of uropathy and nephropathy in children, the underlying mechanisms, outpatient follow-up of children with low and extremely low birth weight, as well as perinatal lesions of the central nervous system. In the reports, an important emphasis is placed on the issue of interdisciplinary cooperation of the specialists, who monitor children at risk and children with complex comorbidities. The reports of K.N. Demidova et al., A.V. Degryareva, O.V. Goncharova, U.S. Malyavina, E.S. Zholobova, and N.S. Podchernyaeva deserve special attention.
Keywords: vesicoureteral reflux, neural network, premature baby, medical checkup, rehabilitation, exercise therapy, obstructive sleep apnea syndrome, rheumatic disorders, antiphospholipid syndrome.
For citation: The 1st Sechenov International Motherhood and Childhood Forum. Prospects and advanced technologies in diagnosis and treatment of diseases in children. Clinical review in general practice. 2024; 5 (9): 74–81 (In Russ.). DOI: 10.47407/kr2024.5.9.00482
им. акад. Ю.Е. Вельтищева» ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России К.Н. Демидова, Д.А. Морозов, В.В. Ростовская, Г.И. Кузовлева, Э.К. Айрян представили современное исследование патогенеза пузырно-мочеточникового рефлюкса у детей с помощью нейросетевых технологий.
Актуальность. Пузырно-мочеточниковый рефлюкс (ПМР) занимает одно из ведущих мест в структуре уропатий и может приводить к инвалидизации пациентов в раннем возрасте. В связи с отсутствием четкой связи между возникновением ПМР и нефропатией, возможности частичного или полного регресса в постнатальном периоде, а также субъективности оценки степени тяжести ПМР, возможны частые ошибки в постановке диагноза и выборе тактики лечения.
ПМР диагностируется у 10–20% новорожденных с антенатально выявленным гидронефрозом. Каждый третий ребенок в возрасте до 5 лет с инфекцией мочевых путей имеет ПМР (рис. 1).
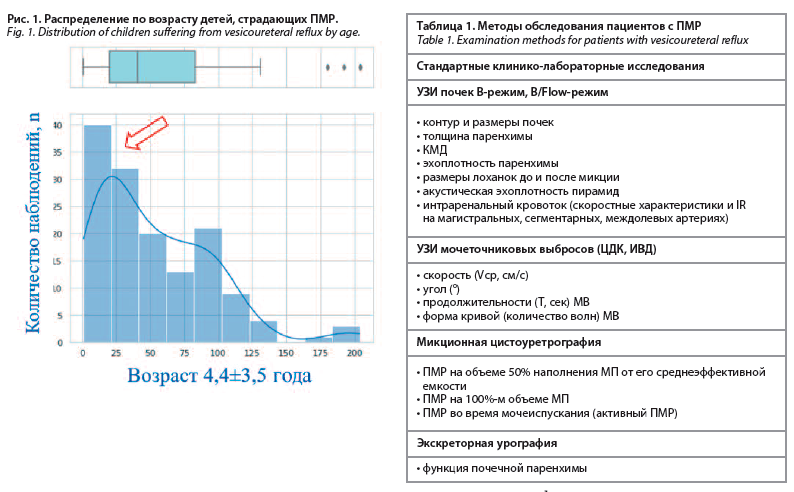
Особенности постнатального течения от спонтанного разрешения ПМР до развития рефлюкс-нефропатии (30–60% случаев) с потерей объема функционирующей почечной паренхимы заключается в отсутствии четкой причинной связи между степенью ПМР и развитием рефлюкс-нефропатии, а также риском формирования нефросклероза при малых степенях (1–2-я степень). Субъективность системы градации ПМР часто приводит к ошибкам в постановке диагноза и выборе тактики лечения. Раздельное использование диагностических критериев не дает возможность объективно оценить и выявить клинически значимый ПМР. Кроме того, отсутствуют математические модели прогнозирования неблагоприятного течения заболевания.
В исследовании, представленном докладчиками, включен 101 пациент с ПМР: дети в возрасте от 1 года до 5 лет с ПМР 2–3-й степени. Диагностика была основана на состоянии верхних и нижних мочевыводящих путей. Методы обследования включали стандартные клинико-лабораторные исследования, такие как ультразвуковое исследование почек, так и специализированные, такие как допплерография мочеточниковых выбросов, микционная цистоуретрография, экстреторная урография. Для объективизации степени ПМР использовался индекс дилатации мочеточника (табл. 1).
В качестве специализированного неизвазивного метода использовались биомаркеры степени повреждения почек: с помощью твердофазного «сендвич»-варианта иммуноферментного анализа определялась экскреция провоспалительных цитокинов-MCP-1, TGF-β1, маркер ангиогенеза VEGF.
Анализ уровней экскреции биомаркеров показал статистически значимое повышение в 3–4 раза относительно контрольной группы вне зависимости от степени ПМР, сторонности процесса и т.д. С помощью кластерного анализа были сформированы паттерны их экскреции и получено 3 паттерна, характеризовавших 3 степени тубулоинтерстициального повреждения почек (далее ТИПП) вместе с параллельным снижением васкулоэндотелиального фактора роста, что может говорить о снижении объема функции паренхимы (табл. 2).
Наибольший процент в исследуемой группе имел легкую степень течения ПМР. Одновременно были проанализированы параметры, отвечающие за анатомо-функциональное состояние артериовезикального сегмента. Выявлены достоверные различия между степенью ПМР и объемом его появления. Также статистически значимо увеличивался индекс дилатации мочеточника, продолжительность выбора, но повышался угол направленности. На основе этих данных была разработана балльная система оценки степени функциональной недостаточности уретеро-везикального сегмента у детей с ПМР. Именно балльная система оценки позволила подойти к разработке прогностической модели выбора оптимальной тактики лечения. Анализируя диагностические переменные, исследователи не смогли выявить определенные параметры, опираясь на которые может быть прогнозирован ПМР, приводящий к структурным и функциональным изменениям в паренхиме органов.
По результатам исследования выявлено, что наиболее важными предикторами в отношении прогноза неблагоприятного течения ПМР были: уровень мочевой экскреции биомаркера ангиогенеза VEGF, размер лоханки после микции (активный ПМР), уровень экскреции провоспалительного цитокина интерлейкина (ИЛ)-8, степень тяжести ПМР, уровень биомаркера фиброгенеза TGF-β1, провоспалительного цитокина ИЛ-18 и хемокина MCP-1, ультразвуковые параметры функционального состояния уретеро-везикального сегмента (время, скорость, угол мочеточниковых выбросов), наличие рецидива фебрильных инфекций мочевыводящих путей, двусторонний ПМР, а также повышение индекса дилатации мочеточника.
В заключение исследователи отметили, что прогностическая модель определения тяжести повреждения почек, созданная на основе искусственной нейронной сети, обученная на клинико-анамнестических, лабораторных, рентгенорадиологических и ультразвуковых данных собственной популяции пациентов с ПМР, имеет высокие предиктивные характеристики по каждому параметру выхода и позволяет классифицировать пациентов по риску развития структурных изменений в почечной паренхиме, создавая основу для реализации персонифицированного подхода к тактике ведения данной группы больных.
Актуальность. Известно, что ребенок, родившийся ранее 32-й недели гестации, считается глубоко недоношенным и не является полностью здоровым к моменту выписки из стационара, так как у таких детей ожидается целый ряд заболеваний со стороны различных систем организма и высокий риск их хронизации. Состояние физического развития у таких детей является своеобразным краеугольным камнем, на которое опираются специалисты при дальнейшем наблюдении ребенка. К моменту выписки из стационара большинство детей имеют дефицит массы тела и дефицит роста. Наиболее уязвимой группой являются дети с задержкой внутриутробного развития, так как дефицит макро- и микронутриентов – это факторы, которые влияют не только на показатели физического, но и нервно-психического развития ребенка в дальнейшем. Однако обратной стороной медали является избыточный рост плода, несущий в себе такие риски, как метаболический синдром, ожирение, инсулинорезистентность, сахарный диабет 2-го типа, сердечно-сосудистые заболевания.
По словам профессора, одной из методик, применяемой в настоящее время на амбулаторном этапе наблюдения за недоношенными детьми, является вскармливание грудным молоком с фортификатором. К важнейшим диагностическим методам, отображающим динамику физического развития в постнатальном периоде, относят измерение индекса массы тела и использование центильных таблиц с учетом скорректированного возраста ребенка. Важным аспектом для практикующего специалиста является выбор субстрата для кормления ребенка, так как потребность в питательных веществах у недоношенного ребенка в постнатальном периоде выше, чем содержание этих микроэлементов в грудном молоке. В настоящее время одним из самых эффективных методов нутритивной поддержки ребенка на амбулаторном этапе является применение специальных белково-витаминных добавок (фортификаторов) для грудного молока. Показаниями к фортификации грудного молока являются: рождение ребенка с экстремально низкой массой тела, дефицитом массы тела при выписке, наличие хронических заболеваний, таких как бронхолегочная дисплазия, пониженное содержание уровня мочевины и фосфора в крови, либо повышенное содержание уровня щелочной фосфатазы в сыворотке крови (табл. 3).
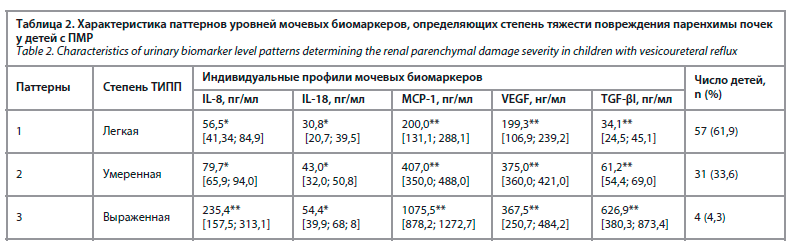
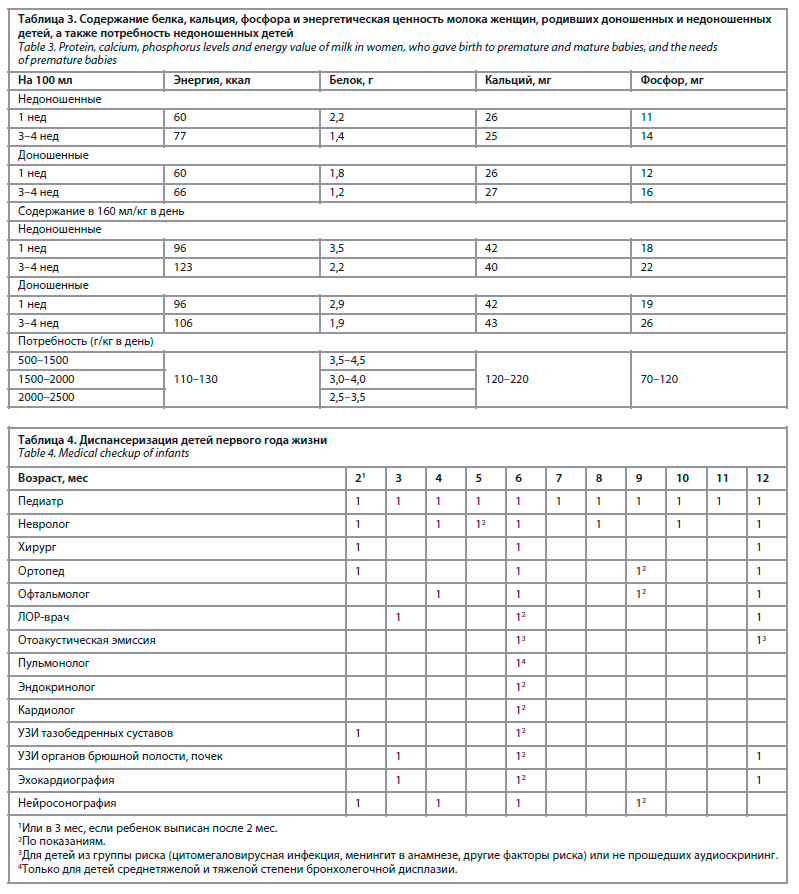
При отсутствии грудного молока оптимальными являются лечебные формулы смесей, разработанные специально для недоношенных детей. Принцип вскармливания детей на амбулаторном этапе основан не только на степени дефицита массы тела, но и проценте усвоения грудного молока или смеси ребенком. Не менее важным является и регулярный осмотр ребенка врачами-специалистами и вакцинация от респираторно-вирусной инфекции. По словам профессора, при отсутствии противопоказаний диспансеризация должна производиться по паспортному, а не скорректированному возрасту (табл. 4).
В завершение доклада Анна Владимировна заключила, что создание служб катамнестического спектра является необходимым этапом для оказания помощи недоношенным детям. Это также позволит определять отдаленные последствия недоношенности на развитие детей и качество оказываемой им помощи.
О.В. Гончарова рассказала о новых методиках в реабилитации детей с перинатальными поражениями нервной системы.
Актуальность. Проблема перинатальных гипоксических поражений центральной нервной системы (ЦНС) представляет особую актуальность в связи с высокой значимостью их влияния на последующее нервно-психическое и физическое развитие детей. Частота их составляет от 73,6% до 90,0%. Дети, анамнез которых был отягощен перинатальной церебральной патологией, представляют категорию высокого риска по формированию систематической неуспеваемости в школе, склонности к поведенческим девиациям в подростковом периоде, социальной дезадаптации. Перинатальные гипоксические поражения ЦНС, способствуя развитию тяжелых нарушений структур головного мозга, служат основной причиной развития детской инвалидности. Усиление неврологической симптоматики у детей с перенесенной гипоксией отмечают в критические периоды развития, такие как период новорожденности, период от 3 до 6 месяцев жизни, дошкольный и начальный школьный возраст.
Клинически данные состояния проявляются как симптомами церебральной ишемии (синдром возбуждения, синдром угнетения, синдром вегето-висцеральных нарушений, синдром мышечной дистонии, синдром внутричерепной гипертензии и др.), так и симптомами внутричерепных кровоизлияний гипоксического генеза.
Профессор подчеркнула, что задачей современного здравоохранения является поиск оптимальных средств и методов, направленных на поддержку и реабилитацию детей с гипоксически-ишемическими поражениями ЦНС как в условиях стационара, так и амбулаторного звена. К этим методам относится внедрение дистанционных технологий оценки развития детей с перинатальными поражениями ЦНС. Учет получаемых различий по отдельным шкалам важен при разработке государственных приоритетных Программ Минздрава России и выборе моделей организации медико-психолого-социальной реабилитации детей в государственных и частных клиниках. Исследование позволяет выявить не только детей с отклонениями в развитии и разработать программы реабилитации, но и детей группы риска и оказывать им своевременную помощь.
В проведенном О.В. Гончаровой исследовании, начиная с 2012 г., проанализированы данные нервно-психического развития 545 детей (г. Москва) от двух месяцев до полутора лет жизни на базе 5 детских городских поликлиник по результатам добровольного анкетирования родителей с помощью компьютерного варианта Шкалы KID (версия Кентской шкалы оценки развития младенцев – Kent Infant Development Scale, KID Scale).
Согласно представленным результатам, у 48,6% детей с перинатальными поражениями ЦНС общее нервно-психическое развитие соответствует возрасту; 21,8% детей отстают в развитии; 29,5% опережают возрастные показатели развития. Установлена зависимость показателей общего развития детей от срока беременности, на котором произошли роды, от показателей общего соматического здоровья детей. Когнитивное развитие у 43,5% из всех протестированных детей соответствует возрасту; 20,6% детей отстают, 36,0% опережают сверстников по данному показателю. Моторное развитие у 51,7% детей соответствует возрасту; 23,3% отстают, а 25% детей опережают остальных. Речевое развитие у 39,3% детей соответствует возрасту; 20,7% детей отстают от своих сверстников по данному показателю; 40% опережают его. По показателям «социальное развитие» и «самообслуживание» нормальное развитие отмечено у 43,2% детей и 45,9% соответственно, отстают 19,5% и 23,9%; опережают нормативные показатели 37,3% и 30,3% соответственно.
Самая большая доля детей с отклонениями в развитии выявлена в областях «моторное развитие» и «самообслуживание». В связи с полученными результатами очевидна необходимость дообследовать детей с выявленными отклонениями. Также рекомендована необходимость для родителей в овладении в «Школах для родителей» методами стимуляции моторного развития (массаж и лечебная физкультура, расширение пространства для детей с целью овладения двигательными навыками и пр.). При наличии нарушений в моторном развитии ребенок не может своевременно овладеть навыками самообслуживания, несмотря на работу с ним родителей/воспитателей – этим можно объяснить и факт большого числа детей с отклонениями в «самообслуживании». На все показатели развития детей влияет срок беременности, на котором произошли роды, что подчеркивает необходимость особого внимания к антенатальному периоду развития ребенка. На втором месте по степени влияния – показатели общего соматического здоровья детей, которые влияют на когнитивное, моторное и социальное развитие детей, на третьем – место воспитания ребенка, влияющее на когнитивное и речевое развитие.
Таким образом, медико-социальная и экономическая эффективность внедрения дистанционных технологий состоит в повышении качества медицинского обслуживания и экономии времени врачей, затрачиваемого на профилактические беседы и демонстрацию реабилитационных методик. Экономия личного времени родителей на посещение полного курса
обучения в очных школах по массажу/обучению, плаванию и проведении профилактических бесед при посещениях кабинета здорового ребенка. Экономия средств государства, затрачиваемых на реабилитацию детей при позднем выявлении отклонений в развитии, использовании помещений для Школ и задействованности врачей в их работе. Подход «родители + компьютер» может применяться при скрининговом исследовании и для создания базы данных, имеет государственную ценность, научную и практическую значимость. В конечном итоге при формировании достаточной базы данных Российская Федерация примет участие в сравнительном анализе уровня развития детей не только в регионах РФ, но и разных странах.
Актуальность. По статистике обзора, проведенного профессором на базе кафедры в 2024 г., 70% родителей отмечают проблемы со сном у детей, храп отмечается у 10–14 % детей, частота синдрома обструктивного апноэ сна (СОАС) в детской популяции варьирует от 1% до 5% и максимальна в возрастной группе от двух до шести лет, чаще встречаясь при сопутствующих заболеваниях, таких как черепно-лицевые аномалии, неврологические нарушения и так далее.
СОАС у детей – это нарушение дыхания во сне, характеризующееся комбинацией повторяющихся эпизодов длительной частичной обструкции и/или периодической полной обструкцией верхних дыхательных путей, которые прерывают нормальную вентиляцию и нормальный паттерн сна. Он может проявляться как ночными симптомами, так и дневными. К ночным симптомам относится: затруднение дыхания во сне или паузы в дыхании, стойкое ротовое дыхание, беспокойный сон, повышенное потоотделение и энурез. К дневным симптомам относятся нейроповеденческие нарушения: дефицит внимания, снижение успеваемости и памяти, нарушение поведения (гиперактивность, агрессивность, дневная сонливость, утомляемость).
К диагностическим критериям СОАС у детей, согласно Международной классификации нарушений сна третьего издания AASM, относятся одно или несколько из следующих критериев:
1. Храп.
2. Затрудненное, парадоксальное или затрудненное дыхание во время сна ребенка.
3. Сонливость, гиперактивность или проблемы с поведением и обучением.
Одно или более одного:
1. Обструктивное или смешанное апноэ или обструктивное гипопноэ на час сна.
2. Характер обструктивной гиповентиляции, определяемый как по меньшей мере 25% общего времени сна с гиперкапнией и/или с десатурией кислорода в артериях в сочетании с одним или несколькими из следующих симптомов: храпом, сглаживанием формы давления в носу при вдохе и парадоксальными движениями грудобрюшной полости.
К согласительным документам, регламентирующим работу с данной группой пациентов, относят:
• Клинические рекомендации: синдром обструктивного апноэ сна у детей, ассоциированный с аденотонзиллярной гипертрофией. Ориентирован преимущественно на врачей-неврологов, однако в выборке участвуют только дети с аденотонзиллярной гипертрофией.
• Практическое руководство для врачей: храп и синдром обструктивного апноэ сна у детей.
• Зарубежные литературные обзоры и консенсусы.
В настоящее время «золотым стандартом» в диагностике данного синдрома является полисомнография. На сегодняшний день исследованию требуется ответить на два вопроса: характере апноэ и степени его тяжести. По рекомендациям Американской академии педиатрии (APP), Европейского респираторного общества (ERS), Американской академии медицины сна (AASM) – всем детям с подозрением на СОАС. AAO-HNS (ассоциация хирургов головы и шеи) – дети с высоким риском (до 2 лет, с ожирением, синдромом Дауна, краниофациальными синдромами, нейромышечными заболеваниями, серповидно-клеточной анемией, мукополисахаридозами) или при сомнениях в необходимости хирургического лечения или несоответствии данных анамнеза.
К недостаткам данного метода относят сложность его выполнения и стоимость исследования.
Достойной альтернативой полисомнографии является кардиореспираторный мониторинг – регистрация дыхательного потока и дыхательных усилий, сатурации крови кислородом и регистрация электрокардиограммы. Данное исследование может выполняться амбулаторно, в том числе в домашних условиях. К другим альтернативным методам относят ночную непрерывную пульсоксиметрию и периферическую артериальную тонометрию. Также активно используется такой скрининговый метод, как анкетирование, например опросник PSQ (Pediatric Square Questionnaire). Данный опросник обладает высокой чувствительностью и специфичностью. Не менее важным методом является аудио и видеодокументирование и клинический осмотр, эндоскопическое исследование носоглотки. Примечательно, что роль небных миндалин небольшого размера в обструкции верхних дыхательных путей следует оценивать по результатам слипэндоскопии.
После установления диагноза СОАС лечение можно условно разделить на три группы: хирургическое, консервативное и реабилитационное. К дополнительным факторам, без которых любое лечение будет неэффективным, относят: изменение образа жизни, снижение массы тела, ортодонтическое лечение и миогимнастику. В настоящее время основной проблемой для семей, где ребенку диагностирован СОАС, является отсутствие междисциплинарных центров маршрутизации для постановки диагноза, а также реабилитации после проведенного оперативного лечения.
Результаты. Так, в условиях современного здравоохранения возникают следующие задачи:
1. Объединение в одном учреждении специалистов для постановки диагноза СОАС;
2. Проведение обследования в соответствии с современным алгоритмом для детей с СОАС;
3. Оптимальная маршрутизация детей с СОАС на основании проведенного обследования;
4. Выбор оптимальной тактики лечения.
Современным ответом на эти задачи, по мнению Ульяны Станиславовны, является создание междисциплинарного центра лечения СОАС, где может быть проведено комплексное обследование и выбор оптимальной тактики ведения каждого конкретного ребенка с нарушением дыхания во сне с применением современных методов диагностики, в соответствии с принципами доказательной медицины.
 Доктор медицинских наук, профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России, профессор
Доктор медицинских наук, профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России, профессор
Е.С. Жолобова, а также доктор медицинских наук, профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» Минздрава России, профессор Н.С. Подчерняева представили обзор на современное состояние проблемы наблюдения и лечения за детьми с ревматологическими заболеваниями.
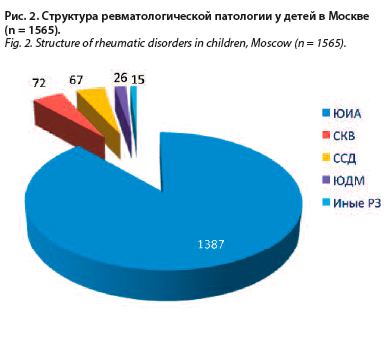
Актуальность. В настоящее время ревматические заболевания включают более сотни нозологий. Среди них можно выделить две большие группы: ревматические заболевания суставов и диффузные заболевания соединительной ткани. В Москве в структуре ревматических заболеваний ревматический артрит занимает лидирующее место (рис. 2).
Это заболевание определяется как артрит неустановленной причины, присутствующий в течение 6 недель и возникающий до достижения ребенком 16-летнего возраста, при исключении других заболеваний. Этиология заболевания многофакторна и до сих пор пока не
изучена, однако характерна наследственная предрасположенность и связь с перенесенной инфекцией, травмой или стрессом. Одной из самых серьезных проблем на сегодняшний момент является существование одновременно двух классификаций: Международной классификации болезней и Классификации Международной ассоциации ревматологов (ILAR), так как несоответствие между ними не всегда понятно специалисту. До 2005 г. прогноз ювенильного артрита был крайне неблагоприятным. Но все изменило изобретение биологической терапии, которая произвела настоящую революцию в лечении этой группы заболеваний.
В настоящее время используется стратегия терапии «Treat to target», целью которой является ремиссия или достижение неактивной фазы заболевания.
Настоящей клинический проблемой является необходимость в новых подходах в терапии и использование преимущественно парентерального пути введения существующих препаратов.
Хотя ювенильный идиопатический артрит занимает почти 80% в структуре аутоиммунных заболеваний, остальные заболевания также составляют большой класт. Среди них существуют как и более «старые» нозологии (системные васкулиты, острая ревматическая лихорадка и т.д.), так и новые заболевания (IgG4-ассоциированное заболевание). Таким образом, спектр заболеваний, лечением которых должен владеть ревматолог, расширяется. К нерешенным проблемам детской ревматологии относятся:
• отсутствие точных данных об этиологии заболевания, и, как следствие, отсутствие этиотропной терапии;
• необходимость уточнения генеза имеющихся симптомов и синдромов;
• поздняя диагностика и позднее начало лечения;
• резистентность ряда пациентов к стандартной терапии;
• «токсичность» традиционных противоревматических препаратов;
• малое количество клинических исследований у детей по сравнению со взрослыми;
• инвалидизация и/или низкое качество жизни при длительно сохраняющейся активности и прогрессировании заболеваний;
• формирование коморбидностей.
За последние 25 лет существенно изменилось отношение профессионального сообщества к синдрому/болезни Кавасаки, который является ведущей причиной приобретенных сердечно-сосудистых заболеваний у детей. До 2010 г. у половины всех обследуемых детей отмечалось увеличение диаметра коронарных артерий, что впоследствии приводило к формированию ишемической болезни сердца и являлось основной причиной возникновения инфаркта миокарда в детском и молодом возрасте. В настоящее время частота формирования коронарных аневризм составляет менее 5%. Поэтому основными направлениями исследований в настоящее время являются:
• применение новых препаратов у пациентов, резистентных к назначению внутривенных иммуноглобулинов;
• разработка схем антикоагулянтной и антиагрегантной терапии для предупреждения формирования тромбов в аневризмах;
• предупреждение инфаркта миокарда у больных с постаневризматическим стенозом;
• разработка показаний для аортокоронарного шунтирования.
Еще одной серьезной проблемой является системная красная волчанка – системное аутоиммунное заболевание неизвестной этиологии, в основе которого лежит генетически обусловленное нарушение иммунной регуляции, определяющее образование антител (АТ) к антигенам ядер клеток с развитием иммунного воспаления в тканях различных органов.
Проблемы лечения системной красной волчанки у детей:
• Стандартная терапия не эффективна при лечении наиболее тяжелых вариантов системной красной волчанки у детей.
• Применение глюкокортикостероидов и неселективных цитотоксических препаратов сопряжено с высоким риском развития осложнений.
• Длительное применение глюкокортикоидов приводит к формированию коморбидной патологии.
Антифосфолипидный синдром – системное аутоиммунное заболевание, характеризующееся венозным и/или артериальным тромбозом и/или рецидивирующим синдромом потери плода, которые обусловлены персистирующими антифосфолипидными антителами. Частота антифосфолипидного синдрома в популяции составляет 1–5%, частота новых случаев составляет 5:100 000 в год с распространенностью 40–50 случаев на 100 тыс. населения. Препараты выбора работают не всегда, например в случае фагоцитарного синдрома, легочных геморрагий, тяжелых поражений, связанных с гемолитическими изменениями и нарушением функции органа (например, почек или центральной нервной системы), что может значительно влиять на качество жизни ребенка в последующем. В настоящее время активно изучаются возможности различных генно-инженерных биологических препаратов, например ритуксимаба и билимумаба. Вместе с этим, в последние годы показано, что главным патогенетическим механизмом является гиперинтерферонемия и гиперактивация сигнальных путей, обусловленных синтезом этих цитокинов. Наиболее эффективными считаются препараты, направленные против этих механизмов. Одним из характерных проявлений данного синдрома является тромбоз мелких сосудов и трудность титровки парентеральных дозировок.
Ювенильный дерматомиозит – системное заболевание аутоиммунной этиологии, характеризующееся поражением мелких сосудов кожи, скелетной мускулатуры и внутренних органов с типичными клиническими проявлениями в виде лиловой эритемы в параорбитальной области и над суставами и проксимальной мышечной слабостью. Центральную роль в патогенезе ювенильного дерматомиозита играет васкулопатия: в начальной стадии имеет место васкулит, развивающийся с участием интерферонов I типа (ИФН I) и других цитокинов; в последующем наблюдается невоспалительная окклюзивная васкулопатия с уменьшением количества функционирующих капилляров. Применение тофацитиниба в лечении дерматомиозита оказало эффективность в лечении резистетного к стандартной терапии кожного синдрома, купирование миопатии, эффективность в лечении кальциноза, снижение суточной дозы глюкокортикостероидов, вплоть до полной отмены.
Исследователями также еще раз отмечена роль холекальциферола (витамин D 25-ОН) при системных аутоиммунных ревматических заболеваний, таких как ювенильный идиопатический артрит и системная красная волчанка. Особое внимание заслуживает тот факт, что частота дефицита/недостаточности холекальциферола (витамина D 25-ОН) у детей с САРЗ превышает таковую в популяции.
По словам Е.С. Жолобовой, прием препаратов, содержащих холекальциферол, способствует снижению активности воспаления у пациентов с ревматическими заболеваниями, активирует клеточный и подавляет гуморальный иммунитет, влияет на активность САРЗ, предупреждает развитие коморбидной патологии (снижает кардиоваскулярный риск, предупреждает развитие остеопороза и переломов, снижает риск развития диабета, ожирения и др.);
Также, по словам докладчиков, холекальциферол (витамин D 25-ОН) может быть использован в качестве дополнительного средства профилактики обострений у пациентов в ремиссии.
Поступила в редакцию: 22.02.2024
Поступила после рецензирования: 01.03.2024
Принята к публикации: 14.03.2024
Received: 22.02.2024
Revised: 01.03.2024
Accepted: 14.03.2024
Клинический разбор в общей медицине №9 2024
Первый Сеченовский международный форум материнства и детства. Перспективы и современные технологии в диагностике и лечении заболеваний у детей
Номера страниц в выпуске:74-81
Аннотация
Представлены обзоры на оригинальные доклады и исследования, посвященные проблеме уро- и нефропатий у детей, механизмам их формирования, амбулаторному наблюдению за детьми, родившимися с низкой и экстремально низкой массой тела, а также перинатальными поражениями центральной нервной системы. Важный акцент в докладах сделан на проблеме междисциплинарного сотрудничества специалистов, наблюдающих детей из групп риска и сложных коморбидных патологий. Особого внимания заслуживают доклады К.Н. Демидовой и соавторов, А. В.Дегтяревой, О.В. Гончаровой, У.С. Малявиной, Е.С. Жолобовой и Н.С. Подчерняевой.
Ключевые слова: пузырно-мочеточниковый рефлюкс, нейросеть, недоношенный ребенок, диспансеризация, реабилитация, лечебная физкультура, синдром обструктивного апноэ сна, ревматические заболевания, антифосфолипидный синдром.
Для цитирования: Первый Сеченовский международный форум материнства и детства. Перспективы и современные технологии в диагностике и лечении заболеваний у детей. Клинический разбор в общей медицине. 2024; 5 (9): 74–81. DOI: 10.47407/kr2024.5.9.00482
Представлены обзоры на оригинальные доклады и исследования, посвященные проблеме уро- и нефропатий у детей, механизмам их формирования, амбулаторному наблюдению за детьми, родившимися с низкой и экстремально низкой массой тела, а также перинатальными поражениями центральной нервной системы. Важный акцент в докладах сделан на проблеме междисциплинарного сотрудничества специалистов, наблюдающих детей из групп риска и сложных коморбидных патологий. Особого внимания заслуживают доклады К.Н. Демидовой и соавторов, А. В.Дегтяревой, О.В. Гончаровой, У.С. Малявиной, Е.С. Жолобовой и Н.С. Подчерняевой.
Ключевые слова: пузырно-мочеточниковый рефлюкс, нейросеть, недоношенный ребенок, диспансеризация, реабилитация, лечебная физкультура, синдром обструктивного апноэ сна, ревматические заболевания, антифосфолипидный синдром.
Для цитирования: Первый Сеченовский международный форум материнства и детства. Перспективы и современные технологии в диагностике и лечении заболеваний у детей. Клинический разбор в общей медицине. 2024; 5 (9): 74–81. DOI: 10.47407/kr2024.5.9.00482
The 1st Sechenov International Motherhood and Childhood Forum. Prospects and advanced technologies in diagnosis and treatment of diseases in children
AbstractThe review provides reviews of original reports and research focused on the issue of uropathy and nephropathy in children, the underlying mechanisms, outpatient follow-up of children with low and extremely low birth weight, as well as perinatal lesions of the central nervous system. In the reports, an important emphasis is placed on the issue of interdisciplinary cooperation of the specialists, who monitor children at risk and children with complex comorbidities. The reports of K.N. Demidova et al., A.V. Degryareva, O.V. Goncharova, U.S. Malyavina, E.S. Zholobova, and N.S. Podchernyaeva deserve special attention.
Keywords: vesicoureteral reflux, neural network, premature baby, medical checkup, rehabilitation, exercise therapy, obstructive sleep apnea syndrome, rheumatic disorders, antiphospholipid syndrome.
For citation: The 1st Sechenov International Motherhood and Childhood Forum. Prospects and advanced technologies in diagnosis and treatment of diseases in children. Clinical review in general practice. 2024; 5 (9): 74–81 (In Russ.). DOI: 10.47407/kr2024.5.9.00482
Вступление
В статье представлен обзор материалов I Сеченовского международного форума материнства и детства, состоявшегося 15–16 февраля 2024 г. на базе ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова». Данное мероприятие проходило в рамках президентской программы «Приоритет-2030», которая призвана создать Исследовательский медицинский университет мирового уровня к 2030 г. Уникальность форума — это акцент на инновационные российские достижения в области охраны здоровья женщин и детей, направленные на диагностику, лечение и реабилитацию пациентов акушерско-гинекологического и педиатрического профиля.Нейросетевые технологии прогнозирования течения пузырно-мочеточникового рефлюкса
Врачи Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова», ГБУЗ «Детская городская клиническая больница №9 им. Г.Н. Сперанского» Департамента здравоохранения г. Москвы, Научно-исследовательского клинического института педиатрии и детской хирургииим. акад. Ю.Е. Вельтищева» ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России К.Н. Демидова, Д.А. Морозов, В.В. Ростовская, Г.И. Кузовлева, Э.К. Айрян представили современное исследование патогенеза пузырно-мочеточникового рефлюкса у детей с помощью нейросетевых технологий.
Актуальность. Пузырно-мочеточниковый рефлюкс (ПМР) занимает одно из ведущих мест в структуре уропатий и может приводить к инвалидизации пациентов в раннем возрасте. В связи с отсутствием четкой связи между возникновением ПМР и нефропатией, возможности частичного или полного регресса в постнатальном периоде, а также субъективности оценки степени тяжести ПМР, возможны частые ошибки в постановке диагноза и выборе тактики лечения.
ПМР диагностируется у 10–20% новорожденных с антенатально выявленным гидронефрозом. Каждый третий ребенок в возрасте до 5 лет с инфекцией мочевых путей имеет ПМР (рис. 1).

Особенности постнатального течения от спонтанного разрешения ПМР до развития рефлюкс-нефропатии (30–60% случаев) с потерей объема функционирующей почечной паренхимы заключается в отсутствии четкой причинной связи между степенью ПМР и развитием рефлюкс-нефропатии, а также риском формирования нефросклероза при малых степенях (1–2-я степень). Субъективность системы градации ПМР часто приводит к ошибкам в постановке диагноза и выборе тактики лечения. Раздельное использование диагностических критериев не дает возможность объективно оценить и выявить клинически значимый ПМР. Кроме того, отсутствуют математические модели прогнозирования неблагоприятного течения заболевания.
В исследовании, представленном докладчиками, включен 101 пациент с ПМР: дети в возрасте от 1 года до 5 лет с ПМР 2–3-й степени. Диагностика была основана на состоянии верхних и нижних мочевыводящих путей. Методы обследования включали стандартные клинико-лабораторные исследования, такие как ультразвуковое исследование почек, так и специализированные, такие как допплерография мочеточниковых выбросов, микционная цистоуретрография, экстреторная урография. Для объективизации степени ПМР использовался индекс дилатации мочеточника (табл. 1).
В качестве специализированного неизвазивного метода использовались биомаркеры степени повреждения почек: с помощью твердофазного «сендвич»-варианта иммуноферментного анализа определялась экскреция провоспалительных цитокинов-MCP-1, TGF-β1, маркер ангиогенеза VEGF.
Анализ уровней экскреции биомаркеров показал статистически значимое повышение в 3–4 раза относительно контрольной группы вне зависимости от степени ПМР, сторонности процесса и т.д. С помощью кластерного анализа были сформированы паттерны их экскреции и получено 3 паттерна, характеризовавших 3 степени тубулоинтерстициального повреждения почек (далее ТИПП) вместе с параллельным снижением васкулоэндотелиального фактора роста, что может говорить о снижении объема функции паренхимы (табл. 2).
Наибольший процент в исследуемой группе имел легкую степень течения ПМР. Одновременно были проанализированы параметры, отвечающие за анатомо-функциональное состояние артериовезикального сегмента. Выявлены достоверные различия между степенью ПМР и объемом его появления. Также статистически значимо увеличивался индекс дилатации мочеточника, продолжительность выбора, но повышался угол направленности. На основе этих данных была разработана балльная система оценки степени функциональной недостаточности уретеро-везикального сегмента у детей с ПМР. Именно балльная система оценки позволила подойти к разработке прогностической модели выбора оптимальной тактики лечения. Анализируя диагностические переменные, исследователи не смогли выявить определенные параметры, опираясь на которые может быть прогнозирован ПМР, приводящий к структурным и функциональным изменениям в паренхиме органов.
По результатам исследования выявлено, что наиболее важными предикторами в отношении прогноза неблагоприятного течения ПМР были: уровень мочевой экскреции биомаркера ангиогенеза VEGF, размер лоханки после микции (активный ПМР), уровень экскреции провоспалительного цитокина интерлейкина (ИЛ)-8, степень тяжести ПМР, уровень биомаркера фиброгенеза TGF-β1, провоспалительного цитокина ИЛ-18 и хемокина MCP-1, ультразвуковые параметры функционального состояния уретеро-везикального сегмента (время, скорость, угол мочеточниковых выбросов), наличие рецидива фебрильных инфекций мочевыводящих путей, двусторонний ПМР, а также повышение индекса дилатации мочеточника.
В заключение исследователи отметили, что прогностическая модель определения тяжести повреждения почек, созданная на основе искусственной нейронной сети, обученная на клинико-анамнестических, лабораторных, рентгенорадиологических и ультразвуковых данных собственной популяции пациентов с ПМР, имеет высокие предиктивные характеристики по каждому параметру выхода и позволяет классифицировать пациентов по риску развития структурных изменений в почечной паренхиме, создавая основу для реализации персонифицированного подхода к тактике ведения данной группы больных.
Амбулаторное наблюдение за детьми, родившимися с очень низкой и экстремально низкой массой тела: клинические рекомендации Института неонатологии и педиатрии ФГБУ «НМИЦ АГП им. акад. В И. Кулакова» Минздрава России
Профессор кафедры неонатологии КИДЗ им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет), доктор медицинских наук А.В. Дегтярева проанализировала существующие методики по амбулаторному наблюдению за детьми, родившимися с низкой и экстремально низкой массой тела.Актуальность. Известно, что ребенок, родившийся ранее 32-й недели гестации, считается глубоко недоношенным и не является полностью здоровым к моменту выписки из стационара, так как у таких детей ожидается целый ряд заболеваний со стороны различных систем организма и высокий риск их хронизации. Состояние физического развития у таких детей является своеобразным краеугольным камнем, на которое опираются специалисты при дальнейшем наблюдении ребенка. К моменту выписки из стационара большинство детей имеют дефицит массы тела и дефицит роста. Наиболее уязвимой группой являются дети с задержкой внутриутробного развития, так как дефицит макро- и микронутриентов – это факторы, которые влияют не только на показатели физического, но и нервно-психического развития ребенка в дальнейшем. Однако обратной стороной медали является избыточный рост плода, несущий в себе такие риски, как метаболический синдром, ожирение, инсулинорезистентность, сахарный диабет 2-го типа, сердечно-сосудистые заболевания.
По словам профессора, одной из методик, применяемой в настоящее время на амбулаторном этапе наблюдения за недоношенными детьми, является вскармливание грудным молоком с фортификатором. К важнейшим диагностическим методам, отображающим динамику физического развития в постнатальном периоде, относят измерение индекса массы тела и использование центильных таблиц с учетом скорректированного возраста ребенка. Важным аспектом для практикующего специалиста является выбор субстрата для кормления ребенка, так как потребность в питательных веществах у недоношенного ребенка в постнатальном периоде выше, чем содержание этих микроэлементов в грудном молоке. В настоящее время одним из самых эффективных методов нутритивной поддержки ребенка на амбулаторном этапе является применение специальных белково-витаминных добавок (фортификаторов) для грудного молока. Показаниями к фортификации грудного молока являются: рождение ребенка с экстремально низкой массой тела, дефицитом массы тела при выписке, наличие хронических заболеваний, таких как бронхолегочная дисплазия, пониженное содержание уровня мочевины и фосфора в крови, либо повышенное содержание уровня щелочной фосфатазы в сыворотке крови (табл. 3).


При отсутствии грудного молока оптимальными являются лечебные формулы смесей, разработанные специально для недоношенных детей. Принцип вскармливания детей на амбулаторном этапе основан не только на степени дефицита массы тела, но и проценте усвоения грудного молока или смеси ребенком. Не менее важным является и регулярный осмотр ребенка врачами-специалистами и вакцинация от респираторно-вирусной инфекции. По словам профессора, при отсутствии противопоказаний диспансеризация должна производиться по паспортному, а не скорректированному возрасту (табл. 4).
В завершение доклада Анна Владимировна заключила, что создание служб катамнестического спектра является необходимым этапом для оказания помощи недоношенным детям. Это также позволит определять отдаленные последствия недоношенности на развитие детей и качество оказываемой им помощи.
Новые методы реабилитации детей с последствиями перинатальных поражений центральной нервной системы
Профессор кафедры спортивной и медицинской реабилитации ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» Минздрава России, доктор медицинских наукО.В. Гончарова рассказала о новых методиках в реабилитации детей с перинатальными поражениями нервной системы.
Актуальность. Проблема перинатальных гипоксических поражений центральной нервной системы (ЦНС) представляет особую актуальность в связи с высокой значимостью их влияния на последующее нервно-психическое и физическое развитие детей. Частота их составляет от 73,6% до 90,0%. Дети, анамнез которых был отягощен перинатальной церебральной патологией, представляют категорию высокого риска по формированию систематической неуспеваемости в школе, склонности к поведенческим девиациям в подростковом периоде, социальной дезадаптации. Перинатальные гипоксические поражения ЦНС, способствуя развитию тяжелых нарушений структур головного мозга, служат основной причиной развития детской инвалидности. Усиление неврологической симптоматики у детей с перенесенной гипоксией отмечают в критические периоды развития, такие как период новорожденности, период от 3 до 6 месяцев жизни, дошкольный и начальный школьный возраст.
Клинически данные состояния проявляются как симптомами церебральной ишемии (синдром возбуждения, синдром угнетения, синдром вегето-висцеральных нарушений, синдром мышечной дистонии, синдром внутричерепной гипертензии и др.), так и симптомами внутричерепных кровоизлияний гипоксического генеза.
Профессор подчеркнула, что задачей современного здравоохранения является поиск оптимальных средств и методов, направленных на поддержку и реабилитацию детей с гипоксически-ишемическими поражениями ЦНС как в условиях стационара, так и амбулаторного звена. К этим методам относится внедрение дистанционных технологий оценки развития детей с перинатальными поражениями ЦНС. Учет получаемых различий по отдельным шкалам важен при разработке государственных приоритетных Программ Минздрава России и выборе моделей организации медико-психолого-социальной реабилитации детей в государственных и частных клиниках. Исследование позволяет выявить не только детей с отклонениями в развитии и разработать программы реабилитации, но и детей группы риска и оказывать им своевременную помощь.
В проведенном О.В. Гончаровой исследовании, начиная с 2012 г., проанализированы данные нервно-психического развития 545 детей (г. Москва) от двух месяцев до полутора лет жизни на базе 5 детских городских поликлиник по результатам добровольного анкетирования родителей с помощью компьютерного варианта Шкалы KID (версия Кентской шкалы оценки развития младенцев – Kent Infant Development Scale, KID Scale).
Согласно представленным результатам, у 48,6% детей с перинатальными поражениями ЦНС общее нервно-психическое развитие соответствует возрасту; 21,8% детей отстают в развитии; 29,5% опережают возрастные показатели развития. Установлена зависимость показателей общего развития детей от срока беременности, на котором произошли роды, от показателей общего соматического здоровья детей. Когнитивное развитие у 43,5% из всех протестированных детей соответствует возрасту; 20,6% детей отстают, 36,0% опережают сверстников по данному показателю. Моторное развитие у 51,7% детей соответствует возрасту; 23,3% отстают, а 25% детей опережают остальных. Речевое развитие у 39,3% детей соответствует возрасту; 20,7% детей отстают от своих сверстников по данному показателю; 40% опережают его. По показателям «социальное развитие» и «самообслуживание» нормальное развитие отмечено у 43,2% детей и 45,9% соответственно, отстают 19,5% и 23,9%; опережают нормативные показатели 37,3% и 30,3% соответственно.
Самая большая доля детей с отклонениями в развитии выявлена в областях «моторное развитие» и «самообслуживание». В связи с полученными результатами очевидна необходимость дообследовать детей с выявленными отклонениями. Также рекомендована необходимость для родителей в овладении в «Школах для родителей» методами стимуляции моторного развития (массаж и лечебная физкультура, расширение пространства для детей с целью овладения двигательными навыками и пр.). При наличии нарушений в моторном развитии ребенок не может своевременно овладеть навыками самообслуживания, несмотря на работу с ним родителей/воспитателей – этим можно объяснить и факт большого числа детей с отклонениями в «самообслуживании». На все показатели развития детей влияет срок беременности, на котором произошли роды, что подчеркивает необходимость особого внимания к антенатальному периоду развития ребенка. На втором месте по степени влияния – показатели общего соматического здоровья детей, которые влияют на когнитивное, моторное и социальное развитие детей, на третьем – место воспитания ребенка, влияющее на когнитивное и речевое развитие.
Таким образом, медико-социальная и экономическая эффективность внедрения дистанционных технологий состоит в повышении качества медицинского обслуживания и экономии времени врачей, затрачиваемого на профилактические беседы и демонстрацию реабилитационных методик. Экономия личного времени родителей на посещение полного курса
обучения в очных школах по массажу/обучению, плаванию и проведении профилактических бесед при посещениях кабинета здорового ребенка. Экономия средств государства, затрачиваемых на реабилитацию детей при позднем выявлении отклонений в развитии, использовании помещений для Школ и задействованности врачей в их работе. Подход «родители + компьютер» может применяться при скрининговом исследовании и для создания базы данных, имеет государственную ценность, научную и практическую значимость. В конечном итоге при формировании достаточной базы данных Российская Федерация примет участие в сравнительном анализе уровня развития детей не только в регионах РФ, но и разных странах.
Состояние и перспективы современной диагностики и лечения синдрома обструктивного апноэ сна у детей
Доктор медицинских наук, заведующая лабораторией научных основ оториноларингологии ФГАУ «НМИЦ здоровья детей» ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России, У.С. Малявина проанализировала имеющиеся нормативные документы и систематизировала имеющиеся знания о СОАС, а также предложила оптимальную схему лечения и реабилитации детей со сложной междисциплинарной патологией.Актуальность. По статистике обзора, проведенного профессором на базе кафедры в 2024 г., 70% родителей отмечают проблемы со сном у детей, храп отмечается у 10–14 % детей, частота синдрома обструктивного апноэ сна (СОАС) в детской популяции варьирует от 1% до 5% и максимальна в возрастной группе от двух до шести лет, чаще встречаясь при сопутствующих заболеваниях, таких как черепно-лицевые аномалии, неврологические нарушения и так далее.
СОАС у детей – это нарушение дыхания во сне, характеризующееся комбинацией повторяющихся эпизодов длительной частичной обструкции и/или периодической полной обструкцией верхних дыхательных путей, которые прерывают нормальную вентиляцию и нормальный паттерн сна. Он может проявляться как ночными симптомами, так и дневными. К ночным симптомам относится: затруднение дыхания во сне или паузы в дыхании, стойкое ротовое дыхание, беспокойный сон, повышенное потоотделение и энурез. К дневным симптомам относятся нейроповеденческие нарушения: дефицит внимания, снижение успеваемости и памяти, нарушение поведения (гиперактивность, агрессивность, дневная сонливость, утомляемость).
К диагностическим критериям СОАС у детей, согласно Международной классификации нарушений сна третьего издания AASM, относятся одно или несколько из следующих критериев:
1. Храп.
2. Затрудненное, парадоксальное или затрудненное дыхание во время сна ребенка.
3. Сонливость, гиперактивность или проблемы с поведением и обучением.
Одно или более одного:
1. Обструктивное или смешанное апноэ или обструктивное гипопноэ на час сна.
2. Характер обструктивной гиповентиляции, определяемый как по меньшей мере 25% общего времени сна с гиперкапнией и/или с десатурией кислорода в артериях в сочетании с одним или несколькими из следующих симптомов: храпом, сглаживанием формы давления в носу при вдохе и парадоксальными движениями грудобрюшной полости.
К согласительным документам, регламентирующим работу с данной группой пациентов, относят:
• Клинические рекомендации: синдром обструктивного апноэ сна у детей, ассоциированный с аденотонзиллярной гипертрофией. Ориентирован преимущественно на врачей-неврологов, однако в выборке участвуют только дети с аденотонзиллярной гипертрофией.
• Практическое руководство для врачей: храп и синдром обструктивного апноэ сна у детей.
• Зарубежные литературные обзоры и консенсусы.
В настоящее время «золотым стандартом» в диагностике данного синдрома является полисомнография. На сегодняшний день исследованию требуется ответить на два вопроса: характере апноэ и степени его тяжести. По рекомендациям Американской академии педиатрии (APP), Европейского респираторного общества (ERS), Американской академии медицины сна (AASM) – всем детям с подозрением на СОАС. AAO-HNS (ассоциация хирургов головы и шеи) – дети с высоким риском (до 2 лет, с ожирением, синдромом Дауна, краниофациальными синдромами, нейромышечными заболеваниями, серповидно-клеточной анемией, мукополисахаридозами) или при сомнениях в необходимости хирургического лечения или несоответствии данных анамнеза.
К недостаткам данного метода относят сложность его выполнения и стоимость исследования.
Достойной альтернативой полисомнографии является кардиореспираторный мониторинг – регистрация дыхательного потока и дыхательных усилий, сатурации крови кислородом и регистрация электрокардиограммы. Данное исследование может выполняться амбулаторно, в том числе в домашних условиях. К другим альтернативным методам относят ночную непрерывную пульсоксиметрию и периферическую артериальную тонометрию. Также активно используется такой скрининговый метод, как анкетирование, например опросник PSQ (Pediatric Square Questionnaire). Данный опросник обладает высокой чувствительностью и специфичностью. Не менее важным методом является аудио и видеодокументирование и клинический осмотр, эндоскопическое исследование носоглотки. Примечательно, что роль небных миндалин небольшого размера в обструкции верхних дыхательных путей следует оценивать по результатам слипэндоскопии.
После установления диагноза СОАС лечение можно условно разделить на три группы: хирургическое, консервативное и реабилитационное. К дополнительным факторам, без которых любое лечение будет неэффективным, относят: изменение образа жизни, снижение массы тела, ортодонтическое лечение и миогимнастику. В настоящее время основной проблемой для семей, где ребенку диагностирован СОАС, является отсутствие междисциплинарных центров маршрутизации для постановки диагноза, а также реабилитации после проведенного оперативного лечения.
Результаты. Так, в условиях современного здравоохранения возникают следующие задачи:
1. Объединение в одном учреждении специалистов для постановки диагноза СОАС;
2. Проведение обследования в соответствии с современным алгоритмом для детей с СОАС;
3. Оптимальная маршрутизация детей с СОАС на основании проведенного обследования;
4. Выбор оптимальной тактики лечения.
Современным ответом на эти задачи, по мнению Ульяны Станиславовны, является создание междисциплинарного центра лечения СОАС, где может быть проведено комплексное обследование и выбор оптимальной тактики ведения каждого конкретного ребенка с нарушением дыхания во сне с применением современных методов диагностики, в соответствии с принципами доказательной медицины.
Лечение ревматических заболеваний у детей: достижения и перспективы
 Доктор медицинских наук, профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России, профессор
Доктор медицинских наук, профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России, профессор Е.С. Жолобова, а также доктор медицинских наук, профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» Минздрава России, профессор Н.С. Подчерняева представили обзор на современное состояние проблемы наблюдения и лечения за детьми с ревматологическими заболеваниями.
Актуальность. В настоящее время ревматические заболевания включают более сотни нозологий. Среди них можно выделить две большие группы: ревматические заболевания суставов и диффузные заболевания соединительной ткани. В Москве в структуре ревматических заболеваний ревматический артрит занимает лидирующее место (рис. 2).
Это заболевание определяется как артрит неустановленной причины, присутствующий в течение 6 недель и возникающий до достижения ребенком 16-летнего возраста, при исключении других заболеваний. Этиология заболевания многофакторна и до сих пор пока не
изучена, однако характерна наследственная предрасположенность и связь с перенесенной инфекцией, травмой или стрессом. Одной из самых серьезных проблем на сегодняшний момент является существование одновременно двух классификаций: Международной классификации болезней и Классификации Международной ассоциации ревматологов (ILAR), так как несоответствие между ними не всегда понятно специалисту. До 2005 г. прогноз ювенильного артрита был крайне неблагоприятным. Но все изменило изобретение биологической терапии, которая произвела настоящую революцию в лечении этой группы заболеваний.
В настоящее время используется стратегия терапии «Treat to target», целью которой является ремиссия или достижение неактивной фазы заболевания.
Настоящей клинический проблемой является необходимость в новых подходах в терапии и использование преимущественно парентерального пути введения существующих препаратов.
Хотя ювенильный идиопатический артрит занимает почти 80% в структуре аутоиммунных заболеваний, остальные заболевания также составляют большой класт. Среди них существуют как и более «старые» нозологии (системные васкулиты, острая ревматическая лихорадка и т.д.), так и новые заболевания (IgG4-ассоциированное заболевание). Таким образом, спектр заболеваний, лечением которых должен владеть ревматолог, расширяется. К нерешенным проблемам детской ревматологии относятся:
• отсутствие точных данных об этиологии заболевания, и, как следствие, отсутствие этиотропной терапии;
• необходимость уточнения генеза имеющихся симптомов и синдромов;
• поздняя диагностика и позднее начало лечения;
• резистентность ряда пациентов к стандартной терапии;
• «токсичность» традиционных противоревматических препаратов;
• малое количество клинических исследований у детей по сравнению со взрослыми;
• инвалидизация и/или низкое качество жизни при длительно сохраняющейся активности и прогрессировании заболеваний;
• формирование коморбидностей.
За последние 25 лет существенно изменилось отношение профессионального сообщества к синдрому/болезни Кавасаки, который является ведущей причиной приобретенных сердечно-сосудистых заболеваний у детей. До 2010 г. у половины всех обследуемых детей отмечалось увеличение диаметра коронарных артерий, что впоследствии приводило к формированию ишемической болезни сердца и являлось основной причиной возникновения инфаркта миокарда в детском и молодом возрасте. В настоящее время частота формирования коронарных аневризм составляет менее 5%. Поэтому основными направлениями исследований в настоящее время являются:
• применение новых препаратов у пациентов, резистентных к назначению внутривенных иммуноглобулинов;
• разработка схем антикоагулянтной и антиагрегантной терапии для предупреждения формирования тромбов в аневризмах;
• предупреждение инфаркта миокарда у больных с постаневризматическим стенозом;
• разработка показаний для аортокоронарного шунтирования.
Еще одной серьезной проблемой является системная красная волчанка – системное аутоиммунное заболевание неизвестной этиологии, в основе которого лежит генетически обусловленное нарушение иммунной регуляции, определяющее образование антител (АТ) к антигенам ядер клеток с развитием иммунного воспаления в тканях различных органов.
Проблемы лечения системной красной волчанки у детей:
• Стандартная терапия не эффективна при лечении наиболее тяжелых вариантов системной красной волчанки у детей.
• Применение глюкокортикостероидов и неселективных цитотоксических препаратов сопряжено с высоким риском развития осложнений.
• Длительное применение глюкокортикоидов приводит к формированию коморбидной патологии.
Антифосфолипидный синдром – системное аутоиммунное заболевание, характеризующееся венозным и/или артериальным тромбозом и/или рецидивирующим синдромом потери плода, которые обусловлены персистирующими антифосфолипидными антителами. Частота антифосфолипидного синдрома в популяции составляет 1–5%, частота новых случаев составляет 5:100 000 в год с распространенностью 40–50 случаев на 100 тыс. населения. Препараты выбора работают не всегда, например в случае фагоцитарного синдрома, легочных геморрагий, тяжелых поражений, связанных с гемолитическими изменениями и нарушением функции органа (например, почек или центральной нервной системы), что может значительно влиять на качество жизни ребенка в последующем. В настоящее время активно изучаются возможности различных генно-инженерных биологических препаратов, например ритуксимаба и билимумаба. Вместе с этим, в последние годы показано, что главным патогенетическим механизмом является гиперинтерферонемия и гиперактивация сигнальных путей, обусловленных синтезом этих цитокинов. Наиболее эффективными считаются препараты, направленные против этих механизмов. Одним из характерных проявлений данного синдрома является тромбоз мелких сосудов и трудность титровки парентеральных дозировок.
Ювенильный дерматомиозит – системное заболевание аутоиммунной этиологии, характеризующееся поражением мелких сосудов кожи, скелетной мускулатуры и внутренних органов с типичными клиническими проявлениями в виде лиловой эритемы в параорбитальной области и над суставами и проксимальной мышечной слабостью. Центральную роль в патогенезе ювенильного дерматомиозита играет васкулопатия: в начальной стадии имеет место васкулит, развивающийся с участием интерферонов I типа (ИФН I) и других цитокинов; в последующем наблюдается невоспалительная окклюзивная васкулопатия с уменьшением количества функционирующих капилляров. Применение тофацитиниба в лечении дерматомиозита оказало эффективность в лечении резистетного к стандартной терапии кожного синдрома, купирование миопатии, эффективность в лечении кальциноза, снижение суточной дозы глюкокортикостероидов, вплоть до полной отмены.
Исследователями также еще раз отмечена роль холекальциферола (витамин D 25-ОН) при системных аутоиммунных ревматических заболеваний, таких как ювенильный идиопатический артрит и системная красная волчанка. Особое внимание заслуживает тот факт, что частота дефицита/недостаточности холекальциферола (витамина D 25-ОН) у детей с САРЗ превышает таковую в популяции.
По словам Е.С. Жолобовой, прием препаратов, содержащих холекальциферол, способствует снижению активности воспаления у пациентов с ревматическими заболеваниями, активирует клеточный и подавляет гуморальный иммунитет, влияет на активность САРЗ, предупреждает развитие коморбидной патологии (снижает кардиоваскулярный риск, предупреждает развитие остеопороза и переломов, снижает риск развития диабета, ожирения и др.);
Также, по словам докладчиков, холекальциферол (витамин D 25-ОН) может быть использован в качестве дополнительного средства профилактики обострений у пациентов в ремиссии.
Поступила в редакцию: 22.02.2024
Поступила после рецензирования: 01.03.2024
Принята к публикации: 14.03.2024
Received: 22.02.2024
Revised: 01.03.2024
Accepted: 14.03.2024


