Клинический разбор в общей медицине №02 2021
Burdenko National Medical Research Center for Neurosurgery, Moscow, Russia
ova@nsi.ru
Abstract
Chronic subdural hematoma (cSDH) is a multifactorial extensive intracranial hemorrhage, causing the local and/or general brain compression. Hematoma has a delimiting capsule, which defines all pathophysiological features, clinical course and treatment tactics. The paper reports contemporary views on ethiology and clinical course of cSDH. Emphasis is placed on the diagnosis. Based on the analysis of 558 verified cSDH observations, the phasal course and brain imaging data are reported. CT and MRI signs of cSDH are defined.
Key words: chronic subdural hematoma, phasal course, CT recognition, MRI recognition.
For citation: Likhterman L.B., Kravchuk A.D., Okhlopkov V.A. Chronic subdural hematomas: challenges and solutions. Part I. Clinical variants and diagnosis. Clinical review for general practice. 2021; 2: 21–27. DOI: 10.47407/kr2021.2.2.00038
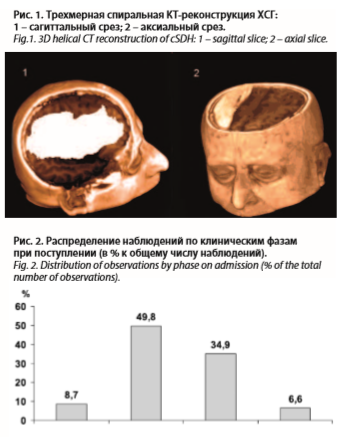 Хроническая субдуральная гематома (ХСГ) – полиэтиологическое объемное внутричерепное кровоизлияние, располагающееся под твердой мозговой оболочкой, вызывающее местную и/или общую компрессию головного мозга и имеющее (в отличие от острых и подострых субдуральных гематом) отграничительную капсулу, определяющую все особенности церебральных патофизиологических реакций, клинического течения и лечебной тактики (рис. 1).
Хроническая субдуральная гематома (ХСГ) – полиэтиологическое объемное внутричерепное кровоизлияние, располагающееся под твердой мозговой оболочкой, вызывающее местную и/или общую компрессию головного мозга и имеющее (в отличие от острых и подострых субдуральных гематом) отграничительную капсулу, определяющую все особенности церебральных патофизиологических реакций, клинического течения и лечебной тактики (рис. 1).
Формирование отграничительной капсулы имеет принципиальное значение, так как приводит к появлению во внутричерепном пространстве относительно независимого образования, во многом подчиняющегося собственным закономерностям развития [1].
Следующим по частоте этиологическим фактором ХСГ являются сосудистые катастрофы: разрывы артериальных аневризм и артерио-венозных мальформаций, геморрагические инсульты, кровоизлияния из первичных и метастатических опухолей головного мозга [2, 3].
Другими причинами образования ХСГ могут быть коагулопатии на фоне длительного приема антикоагулянтов, гемофилии, геморрагического диатеза, поражений печени, сепсиса, а также хронический алкоголизм, инфекционные заболевания, токсические поражения, краниоцеребральные диспропорции и т.д. [4].
Следует указать, что все чаще ХСГ являются ятрогенными, особенно в связи с распространением шунтирующих операций, при которых они являются осложнением у 4,5–21,0% пациентов [1, 5]. Однако нередко уточнить этиологию ХСГ не представляется возможным.
Главными причинами учащения ХСГ за последние годы являются распространение черепно-мозговых травм и цереброваскулярных заболеваний. Существенную роль играет постарение населения, что в связи с возрастной атрофией мозга, изменениями сосудистой системы, реологических свойств крови создает дополнительные предпосылки для формирования ХСГ. Аналогичное значение приобретают краниоцеребральные аномалии у детей. Определенное место в учащении ХСГ занимает алкоголизм, а также ряд других неблагоприятных воздействий на головной мозг и другие органы.
Весьма существенно, что если раньше ХСГ выявлялись почти исключительно у лиц пожилого и старческого возраста, то в настоящее время они значительно «помолодели» и встречаются достаточно часто в молодом и среднем возрасте, а также у детей [1, 6].
Экстраполируя данные по эпидемиологии ХСГ на японском острове Авадзи на всю Японию с учетом роста ее популяции к 2020 г. до 135 304 (где лица старше 65 лет составят 23,6%), K. Kawamura и соавт. [7] приходят к выводу, что частота ХСГ возрастет до 16,3 на 100 тыс. населения в год (в том числе из этого показателя на долю лиц старше 65 лет придется 13,7, а на долю лиц до 65 лет – 2,6). Исходя из этих расчетов, операции по поводу ХСГ станут одними из наиболее частых нейрохирургических вмешательств в Японии. Подобная динамика ожидает и другие страны.
I. Фаза клинической компенсации. Общемозговая симптоматика отсутствует. Очаговая симптоматика отсутствует, либо резидуальна и обусловлена перенесенной черепно-мозговой травмой или преморбидной патологией.
II. Фаза клинической субкомпенсации. Общее состояние больного удовлетворительное. Сознание ясное. Могут выявляться различные очаговые неврологические или психические симптомы, обычно мягко выраженные. Дислокационная симптоматика отсутствует.
III. Фаза умеренной клинической декомпенсации. Общее состояние больного обычно средней тяжести. Нередки сонливость, элементы оглушения, признаки внутричерепной гипертензии. Нарастают очаговые симптомы поражения, в основном со стороны двигательной сферы. Могут улавливаться отдельные вторичные стволовые признаки.
IV. Фаза грубой клинической декомпенсации. Общее состояние больного тяжелое. Сознание нарушено, нередко до глубокого оглушения. Выражены признаки внутричерепной гипертензии. Развиваются синдромы дислокации ствола мозга, чаще на тенториальном уровне. Становятся очевидными расстройства жизненно важных функций.
V. Терминальная фаза. Необратимая кома.
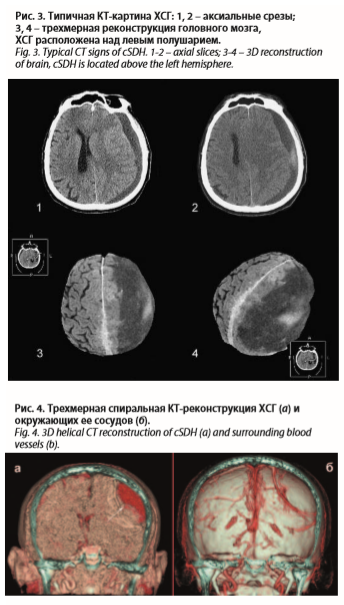 Распределение 558 больных с ХСГ по клиническим фазам при поступлении их в НМИЦ нейрохирургии им. ак. Н.Н. Бурденко представлено на рис. 2.
Распределение 558 больных с ХСГ по клиническим фазам при поступлении их в НМИЦ нейрохирургии им. ак. Н.Н. Бурденко представлено на рис. 2.
В фазе клинической компенсации находились 8,7% больных, в фазе субкомпенсации – 49,8%, в фазе умеренной декомпенсации – 34,9% и в фазе грубой клинической декомпенсации – 6,6% больных.
Таким образом, при поступлении в стационар преобладали пациенты в фазах субкомпенсации и умеренной декомпенсации.
По нашим данным [8], при ХСГ чаще наблюдается постепенный (недели, месяцы) темп углубления клинической декомпенсации (у 51,6% больных); быстрый (дни) темп отмечен у 25,1% больных, лавинообразный (часы) – у 3,2%, ундулирующее течение – у 6,4%. Последние три варианта преобладают у пожилых и стариков. Клиническая фаза ХСГ была стабильна на протяжении многих месяцев и даже лет у 4,6% больных; у 9,1% наблюдалась только положительная динамика в смене клинических фаз.
При повозрастном анализе вариабельной клинической картины ХСГ нами установлены следующие основные закономерности:
1) частое преобладание общемозговой симптоматики над очаговой во всех возрастных группах;
2) по мере увеличения возраста больных изменяется структура общемозговых симптомов – от гипертензионных в детском, молодом и среднем возрасте до гипотензионных в пожилом и старческом возрасте, что связано с преобладанием в младших возрастных группах отека мозга и внутричерепной гипертензии, а в старших возрастных группах – коллапса мозга и внутричерепной гипотензии;
3) повышение с возрастом больных роли сосудистого слагаемого в генезе симптоматики при ХСГ, что вместе с инволюционными факторами обусловливает бóльшую частоту нарушений психики у лиц старческого и пожилого возраста по сравнению с младшими возрастными группами;
4) при доминировании среди очаговой симптоматики двигательных нарушений степень их выраженности и устойчивости обычно усугубляется с возрастом;
5) наблюдается повозрастное смещение соотношения клинических фаз заболевания в сторону их утяжеления; иными словами, чем старше больной с ХСГ, тем чаще у него выявляется грубая декомпенсация. Это связано как с истощающимися с возрастом компенсаторными возможностями, так и с нарастанием инволюционной и приобретенной патологии;
6) фазовые переходы многообразны и во многом связаны с возрастными анатомо-физиологическими особенностями черепа, головного мозга и организма в целом. Если наступает клиническая декомпенсация, то наиболее быстро в фазу грубой декомпенсации входят больные пожилого и старческого возраста, что объясняется тем, что у этой категории больных компримирующее воздействие ХСГ на мозг сопровождается выраженными сосудистыми нарушениями;
7) декомпенсация при ХСГ развивается по пяти ведущим параметрам: общемозговому, стволовому, очаговому, соматическому и инструментальному. При этом для ХСГ во всех возрастных группах характерны диссоциации между различными показателями, что необходимо учитывать при установлении клинической фазы заболевания.
Соматический статус играет особую роль в оценке клинической фазы ХСГ у пожилых и стариков.
При ХСГ, в отличие от острых гематом, во всех возрастных группах могут не срабатывать привычные критические инструментальные показатели, имея в виду как их параллелизм с развертыванием общемозговой, очаговой и стволовой симптоматики, так и прогностическое значение. Например, при смещении срединных структур, достигающем критических цифр – 15 мм и более, пациент может находиться в фазе субкомпенсации и даже клинической компенсации.
Как показали исследования, возрастной и фазовый подходы весьма перспективны для оценки состояния больного, анализа данных инструментальных методов диагностики и выбора адекватной тактики лечения ХСГ.
Надо отметить, что близкое количественное распределение больных с ХСГ по группам получено и при использовании стадий T. Markwalder [9]: I стадия (нет симптоматики) – 10,1%; II стадия (легкая симптоматика) – 50,8%; III стадия (умеренная симптоматика) – 32,3%; IV стадия (грубая симптоматика) – 6,8% больных. Это обстоятельство, как представляется, свидетельствует о достаточной объективности фазного подхода к анализу клинического течения ХСГ.
Светлый промежуток при ХСГ может длиться неделями, месяцами и даже годами. Симптоматика ХСГ полиморфна. Наблюдается резкое ухудшение состояния больного спонтанно или под влиянием разных дополнительных факторов (легкая повторная травма головы, перегревание на солнце, употребление алкоголя, повышение артериального давления, простудные заболевания и т.п.). Клиническая картина при этом может напоминать различные заболевания центральной нервной системы: доброкачественные и злокачественные опухоли мозга, инсульт, спонтанное субарахноидальное кровоизлияние, церебральный атеросклероз, энцефалит, эпилепсию и др.
В период развернутой клинической картины ХСГ часты изменения сознания в виде оглушения или аментивной спутанности с нарушением памяти, ориентировки.
Среди очаговых признаков ХСГ ведущая роль принадлежит пирамидному гемисиндрому. Встречаются также речевые нарушения, гемигипалгезия, гемианопсия и др. Большой удельный вес в клинической картине ХСГ имеет экстрапирамидная симптоматика (гипомимия, брадикинезия, общая скованность, повышение мышечного тонуса по пластическому типу, подкорковый тремор и др.), выходящая за пределы возрастных изменений. Нередки нарушения статики и походки. В фазах клинической декомпенсации проявляется вторичная дислокационная среднемозговая симптоматика (парез взора вверх, двусторонние стопные знаки, анизокория, спонтанный нистагм и др.).
Над зоной расположения гематомы может отмечаться притупление перкуторного звука.
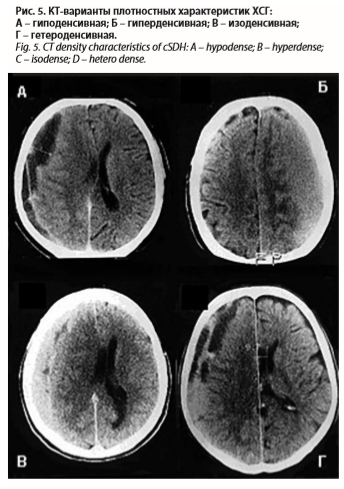 ХСГ представляет собой на КТ зону измененной плотности между костями черепа и веществом мозга, обычно серповидной формы с многодолевым распространением и преимущественно парасагиттально-конвекситальной локализацией; при этом наружная граница повторяет очертания внутренней поверхности костей черепа, а внутренняя граница – очертания полушария мозга (рис. 3, 4).
ХСГ представляет собой на КТ зону измененной плотности между костями черепа и веществом мозга, обычно серповидной формы с многодолевым распространением и преимущественно парасагиттально-конвекситальной локализацией; при этом наружная граница повторяет очертания внутренней поверхности костей черепа, а внутренняя граница – очертания полушария мозга (рис. 3, 4).
Семиотика. По плотности мы разделили ХСГ на гиподенсивные (28 и менее Ед. H), изоденсивные (29–45 Ед. Н), гиперденсивные (более 45 Ед. Н), а также гетероденсивные (рис. 5).
Гиподенсивные ХСГ встречаются наиболее часто. Снижение плотности содержимого гематомы колеблется от выраженного до незначительного (17–28 Ед. Н), однако всегда превышает плотность ликвора. Чаще гиподенсивная зона гомогенна, но порой улавливаются и разные по интенсивности участки снижения плотности. На этом фоне могут выявляться линейные повышения плотности за счет визуализации наружного или внутреннего листка капсулы либо перегородок при многокамерной ХСГ.
Сопоставление данных КТ с операционными находками показывает, что у большинства больных с гиподенсивными ХСГ в полости гематомы содержится ксантохромная либо коричневато-зеленоватая мутная жидкость, у некоторых – измененная разжиженная кровь, а также мелкие свертки крови.
При гиподенсивных ХСГ длительность анамнеза колеблется в широких пределах – от 25 сут до 5 лет, иногда от 14 сут. Феномен снижения плотности содержимого ХСГ преимущественно связан с деградацией фибрина в свертках крови.
Изоденсивные ХСГ встречаются реже. Плотность содержимого гематомы практически не отличается от вещества мозга. Вместе с тем на КТ обычно выражены признаки объемного процесса и, что характерно при ХСГ, отсутствуют конвекситальные субарахноидальные пространства на стороне поражения.
Сопоставление данных КТ с операционными находками показывает, что у половины больных с изоденсивными ХСГ в полости гематом содержится коричневато-зеленоватая жидкость, у других – разжиженная кровь и ее свертки.
Изоденсивные ХСГ отмечены при длительности анамнеза от 18 сут до 1 года. Феномен изоплотности может появляться и раньше: порой спустя 10–14 сут после черепно-мозговой травмы. Он определяется главным образом соотношением разжиженной крови и ее дериватов в полости ХСГ.
Гиперденсивные ХСГ встречаются редко. Повышение плотности содержимого гематом варьирует от нерезко выраженного до значительного.
 При гиперденсивных ХСГ в большинстве случаев в полости гематомы содержатся, наряду с разжиженной кровью, ее свертки. Отметим, что чем в большем объеме в гематоме преобладают свертки крови, тем выше ее плотность. Феномен повышения плотности связан с повторными кровоизлияниями в полость гематомы, которые могут наблюдаться спустя любое время после формирования ХСГ.
При гиперденсивных ХСГ в большинстве случаев в полости гематомы содержатся, наряду с разжиженной кровью, ее свертки. Отметим, что чем в большем объеме в гематоме преобладают свертки крови, тем выше ее плотность. Феномен повышения плотности связан с повторными кровоизлияниями в полость гематомы, которые могут наблюдаться спустя любое время после формирования ХСГ.
Гетероденсивные ХСГ встречаются часто. Представлены на КТ мозаичными картинами: в полости гематомы в различных соотношениях сочетаются участки повышенной и пониженной плотности, реже пониженной плотности и плотности, равной таковой вещества мозга, а в отдельных случаях наблюдаются все три варианта изменений плотности ХСГ.
Для гетерогенных ХСГ характерен феномен седиментации в виде четкого разграничения содержимого гематомы на низкоплотную верхнюю часть и высокоплотную нижнюю часть (при положении больного на спине).
При сопоставлении данных КТ с операционными находками установлено, что у 2/3 больных полость гематомы содержит свертки крови в смеси с зеленовато-коричневатой жидкостью, у остальных – темную жидкую кровь и мелкие сгустки фибрина.
Длительность анамнеза при гетероденсивных ХСГ колеблется от 16 сут до 5 лет. Неоднородная плотность связана как с повторными макро- и микрокровоизлияниями в полость гематомы, так и с деградацией ранее излившейся крови. Оседание высокоплотных, еще не распавшихся форменных элементов крови обусловливает появление КТ-феномена седиментации.
В структуре ХСГ на КТ могут также прослеживаться уплотненные листки капсулы, тяжи, межкамерные перегородки и некоторые другие образования. Капсула ХСГ выявляется при КТ примерно в 10-й части наблюдений, хотя на операциях наружную и внутреннюю мембрану (выраженные в различной степени) находят практически всегда. Эта диссоциация может быть объяснена малой контрастируемостью капсулы, нередко ее тонкостью, прилежанием к костям черепа и веществу мозга с повторением их очертаний. Возможно также, что в ряде случаев невыявление существующей капсулы ХСГ на КТ обусловлено тем, что не всегда используют контрастное усиление.
Применение трехмерной реконструкции ХСГ с помощью спиральной КТ расширило анатомо-топографические представления об осумкованных кровоизлияниях, показав их соотношение как с мозговыми структурами, так и с сосудами полушарий (феномен бессосудистой зоны); см. рис. 4.
Современные возможности перфузионных методик (КТ-перфузия) позволяют оценивать состояние объемного мозгового кровотока при ХСГ и его динамику в послеоперационном периоде.
Представим выделенный нами компьютерно-томографический синдром ХСГ. Наиболее часто он характеризуется:
– зоной измененной плотности (гиподенсивной, гиперденсивной, гетероденсивной) между костями черепа и веществом мозга, чаще серповидной формы и обычно имеющей многодолевое или плащевое распространение (одно- или двухстороннее) с преимущественно парасагиттально-конвекситальной локализацией;
– повторением очертаний внутренней поверхности костей черепа наружной границей патологической зоны измененной плотности и очертаний поверхности полушария головного мозга – ее внутренней границей;
– значительным преобладанием площади патологической зоны над ее толщиной;
– отсутствием субарахноидальных щелей на стороне расположения гематомы с одновременным дислокационным воздействием на гомолатеральный боковой желудочек.
При ХСГ редкой атипичной локализации (базальная, межполушарная, заднечерепная и др.) КТ-синдромы, наряду с общими чертами, имеют много существенных отличий от выделенного КТ-синдрома наиболее распространенной типичной полушарной локализации ХСГ.
При двусторонней ХСГ важными дополнительными компьютерно-томографическими признаками являются отсутствие изображения конвекситальных субарахноидальных щелей с обеих сторон и феномен сближения передних и задних рогов боковых желудочков, а также изменение их талии.
КТ-синдром ХСГ может дополняться и другими прямыми их признаками: феноменом седиментации, визуализацией наружного или внутреннего листков капсулы, многокамерного строения или интрагематомных трабекул (их выявлению часто может способствовать контрастное усиление).
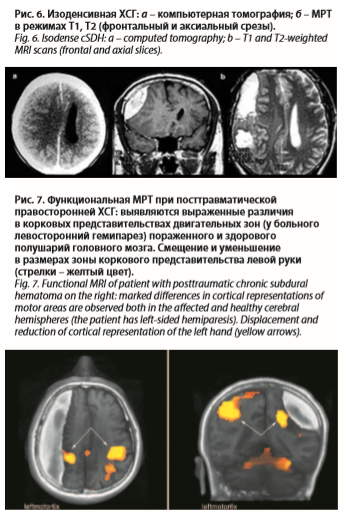
Для ХСГ характерна высокая контрастность изображения на МР-томограммах по сравнению с прилежащим веществом мозга. Зоны повышенного сигнала, соответствующие расположению и размерам ХСГ, имеют серповидную либо линзообразную форму с четкими контурами и примыкают к костям свода черепа (см. рис. 6). При этом определяются также выраженные в разной степени вторичные признаки объемного процесса – деформация и смещение желудочковой системы, сдавление конвекситальных субарахноидальных щелей на стороне поражения и др.
Сопоставление КТ и МРТ при распознавании ХСГ представлено на рис. 6. Высокая контрастность изображения ХСГ на МР-томограммах особенно существенна при изоденсивных гематомах, а также при распространенных плоскостных оболочечных гематомах толщиной до 10 мм, которые нередко плохо определяются при КТ. МРТ способна выявлять структуру гематомы, ее капсулу и другие особенности ХСГ. Четко визуализируется сопровождающая ХСГ различная очаговая патология мозга.
Высокая информативность МРТ при ХСГ объясняется изменением валентности железа при образовании метгемоглобина, приобретением им гидрофильных и парамагнитных свойств.
Примененная нами методика функционального МРТ-картирования при ХСГ позволяет уточнять локализацию и состояние функционально значимых зон больших полушарий (рис. 7).
Прикладным итогом проведенных нами исследований является выделение МРТ-синдрома ХСГ. Он характеризуется:
а – наличием контрастной зоны усиления сигнала, чаще гомогенной, над веществом головного мозга, имеющей многодолевое или плащевое распространение (одно- или двустороннее) с конвекситальной или парасагиттальной локализацией и наружными контурами, повторяющими рельеф костей свода черепа, четкими внутренними контурами, ровными или повторяющими очертания борозд и извилин мозга;
б – значительным преобладанием площади зоны патологического сигнала над ее толщиной при преимущественно серповидной форме на аксиальных срезах и преимущественно линзообразной – на фронтальных срезах;
в – удлинением времени спин-спинновой (Т2) при укорочении времени спин-решеточной (Т1) релаксации (не наблюдаемым при подавляющем большинстве других объемных внутричерепных образований), что выражается в высокой контрастности изображения на томограммах, полученных как в импульсной последовательности SE с сильной зависимостью от (Т2) релаксационного времени, так и положительной контрастности на томограммах, полученных в импульсном режиме IR.
Итак, МРТ является наиболее надежным полипроекционным методом неинвазивного распознавания хронических внутричерепных гематом независимо от их расположения, объема и характера содержимого.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах / Information about the authors
Лихтерман Леонид Болеславович – д-р мед. наук, проф., невролог, гл. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. ак. Н.Н. Бурденко». E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Leonid B. Likhterman – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Кравчук Александр Дмитриевич – д-р мед. наук, проф., нейрохирург, зав. 9-м нейрохирургическим отделением, ФГАУ «НМИЦ нейрохирургии им. ак. Н.Н. Бурденко». ORCID: 0000-0002-3112-8256
Aleksandr D. Kravchuk – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0002-3112-8256
Охлопков Владимир Александрович – канд. мед. наук, доцент, нейрохирург, ст. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. ак. Н.Н. Бурденко». ORCID: 0000-0001-8911-2372
Vladimir A. Okhlopkov – Cand. Sci. (Med.), Assoc. Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0001-8911-2372
Статья поступила в редакцию / The article received: 16.03.2021
Статья принята к печати / The article approved for publication: 19.03.2021
Клинический разбор в общей медицине №02 2021
Хронические субдуральные гематомы головного мозга: проблемы и решения. Часть 1. Клинические варианты и диагностика
Номера страниц в выпуске:21-27
Аннотация
Хроническая субдуральная гематома (ХСГ) представляет собой полиэтиологическое объемное внутричерепное кровоизлияние, вызывающее местную и/или общую компрессию головного мозга и имеющее отграничительную капсулу, определяющую все особенности церебральных патофизиологических реакций, клинического течения и лечебной тактики. В статье рассматриваются современные представления об этиологии и клиническом течении ХСГ, сделан акцент на диагностику. На основании анализа 558 верифицированных наблюдений ХСГ представлена фазность их клинического течения и нейровизуализационная диагностика. Выделены КТ- и МРТ-синдромы ХСГ.
Ключевые слова: хроническая субдуральная гематома, фазность клинического течения, КТ-распознавание, МРТ-распознавание.
Для цитирования: Лихтерман Л.Б., Кравчук А.Д., Охлопков В.А. Хронические субдуральные гематомы головного мозга: проблемы и решения. Часть 1. Клинические варианты и диагностика. Клинический разбор в общей медицине. 2021; 2: 21–27. DOI: 10.47407/ kr2021.2.2.00038
Хроническая субдуральная гематома (ХСГ) представляет собой полиэтиологическое объемное внутричерепное кровоизлияние, вызывающее местную и/или общую компрессию головного мозга и имеющее отграничительную капсулу, определяющую все особенности церебральных патофизиологических реакций, клинического течения и лечебной тактики. В статье рассматриваются современные представления об этиологии и клиническом течении ХСГ, сделан акцент на диагностику. На основании анализа 558 верифицированных наблюдений ХСГ представлена фазность их клинического течения и нейровизуализационная диагностика. Выделены КТ- и МРТ-синдромы ХСГ.
Ключевые слова: хроническая субдуральная гематома, фазность клинического течения, КТ-распознавание, МРТ-распознавание.
Для цитирования: Лихтерман Л.Б., Кравчук А.Д., Охлопков В.А. Хронические субдуральные гематомы головного мозга: проблемы и решения. Часть 1. Клинические варианты и диагностика. Клинический разбор в общей медицине. 2021; 2: 21–27. DOI: 10.47407/ kr2021.2.2.00038
Chronic subdural hematomas: challenges and solutions. Part I. Clinical variants and diagnosis
Leonid B. Likhterman, Aleksandr D. Kravchuk, Vladimir A. OkhlopkovBurdenko National Medical Research Center for Neurosurgery, Moscow, Russia
ova@nsi.ru
Abstract
Chronic subdural hematoma (cSDH) is a multifactorial extensive intracranial hemorrhage, causing the local and/or general brain compression. Hematoma has a delimiting capsule, which defines all pathophysiological features, clinical course and treatment tactics. The paper reports contemporary views on ethiology and clinical course of cSDH. Emphasis is placed on the diagnosis. Based on the analysis of 558 verified cSDH observations, the phasal course and brain imaging data are reported. CT and MRI signs of cSDH are defined.
Key words: chronic subdural hematoma, phasal course, CT recognition, MRI recognition.
For citation: Likhterman L.B., Kravchuk A.D., Okhlopkov V.A. Chronic subdural hematomas: challenges and solutions. Part I. Clinical variants and diagnosis. Clinical review for general practice. 2021; 2: 21–27. DOI: 10.47407/kr2021.2.2.00038
 Хроническая субдуральная гематома (ХСГ) – полиэтиологическое объемное внутричерепное кровоизлияние, располагающееся под твердой мозговой оболочкой, вызывающее местную и/или общую компрессию головного мозга и имеющее (в отличие от острых и подострых субдуральных гематом) отграничительную капсулу, определяющую все особенности церебральных патофизиологических реакций, клинического течения и лечебной тактики (рис. 1).
Хроническая субдуральная гематома (ХСГ) – полиэтиологическое объемное внутричерепное кровоизлияние, располагающееся под твердой мозговой оболочкой, вызывающее местную и/или общую компрессию головного мозга и имеющее (в отличие от острых и подострых субдуральных гематом) отграничительную капсулу, определяющую все особенности церебральных патофизиологических реакций, клинического течения и лечебной тактики (рис. 1).Формирование отграничительной капсулы имеет принципиальное значение, так как приводит к появлению во внутричерепном пространстве относительно независимого образования, во многом подчиняющегося собственным закономерностям развития [1].
Этиология
Наиболее частой причиной ХСГ является черепно-мозговая травма; по нашим данным в 73% [1].Следующим по частоте этиологическим фактором ХСГ являются сосудистые катастрофы: разрывы артериальных аневризм и артерио-венозных мальформаций, геморрагические инсульты, кровоизлияния из первичных и метастатических опухолей головного мозга [2, 3].
Другими причинами образования ХСГ могут быть коагулопатии на фоне длительного приема антикоагулянтов, гемофилии, геморрагического диатеза, поражений печени, сепсиса, а также хронический алкоголизм, инфекционные заболевания, токсические поражения, краниоцеребральные диспропорции и т.д. [4].
Следует указать, что все чаще ХСГ являются ятрогенными, особенно в связи с распространением шунтирующих операций, при которых они являются осложнением у 4,5–21,0% пациентов [1, 5]. Однако нередко уточнить этиологию ХСГ не представляется возможным.
Эпидемиология
Необходимость в корректном эпидемиологическом изучении ХСГ в связи с их распространенностью бесспорна.Главными причинами учащения ХСГ за последние годы являются распространение черепно-мозговых травм и цереброваскулярных заболеваний. Существенную роль играет постарение населения, что в связи с возрастной атрофией мозга, изменениями сосудистой системы, реологических свойств крови создает дополнительные предпосылки для формирования ХСГ. Аналогичное значение приобретают краниоцеребральные аномалии у детей. Определенное место в учащении ХСГ занимает алкоголизм, а также ряд других неблагоприятных воздействий на головной мозг и другие органы.
Весьма существенно, что если раньше ХСГ выявлялись почти исключительно у лиц пожилого и старческого возраста, то в настоящее время они значительно «помолодели» и встречаются достаточно часто в молодом и среднем возрасте, а также у детей [1, 6].
Экстраполируя данные по эпидемиологии ХСГ на японском острове Авадзи на всю Японию с учетом роста ее популяции к 2020 г. до 135 304 (где лица старше 65 лет составят 23,6%), K. Kawamura и соавт. [7] приходят к выводу, что частота ХСГ возрастет до 16,3 на 100 тыс. населения в год (в том числе из этого показателя на долю лиц старше 65 лет придется 13,7, а на долю лиц до 65 лет – 2,6). Исходя из этих расчетов, операции по поводу ХСГ станут одними из наиболее частых нейрохирургических вмешательств в Японии. Подобная динамика ожидает и другие страны.
Фазность клинического течения хронической субдуральной гематомы
Основываясь на концепции фазности развития синдрома компрессии головного мозга, в клиническом течении ХСГ нами прослежены и выделены пять фаз, каждая из которых характеризуется рядом свойственных ей особенностей [1, 2].I. Фаза клинической компенсации. Общемозговая симптоматика отсутствует. Очаговая симптоматика отсутствует, либо резидуальна и обусловлена перенесенной черепно-мозговой травмой или преморбидной патологией.
II. Фаза клинической субкомпенсации. Общее состояние больного удовлетворительное. Сознание ясное. Могут выявляться различные очаговые неврологические или психические симптомы, обычно мягко выраженные. Дислокационная симптоматика отсутствует.
III. Фаза умеренной клинической декомпенсации. Общее состояние больного обычно средней тяжести. Нередки сонливость, элементы оглушения, признаки внутричерепной гипертензии. Нарастают очаговые симптомы поражения, в основном со стороны двигательной сферы. Могут улавливаться отдельные вторичные стволовые признаки.
IV. Фаза грубой клинической декомпенсации. Общее состояние больного тяжелое. Сознание нарушено, нередко до глубокого оглушения. Выражены признаки внутричерепной гипертензии. Развиваются синдромы дислокации ствола мозга, чаще на тенториальном уровне. Становятся очевидными расстройства жизненно важных функций.
V. Терминальная фаза. Необратимая кома.
 Распределение 558 больных с ХСГ по клиническим фазам при поступлении их в НМИЦ нейрохирургии им. ак. Н.Н. Бурденко представлено на рис. 2.
Распределение 558 больных с ХСГ по клиническим фазам при поступлении их в НМИЦ нейрохирургии им. ак. Н.Н. Бурденко представлено на рис. 2.В фазе клинической компенсации находились 8,7% больных, в фазе субкомпенсации – 49,8%, в фазе умеренной декомпенсации – 34,9% и в фазе грубой клинической декомпенсации – 6,6% больных.
Таким образом, при поступлении в стационар преобладали пациенты в фазах субкомпенсации и умеренной декомпенсации.
По нашим данным [8], при ХСГ чаще наблюдается постепенный (недели, месяцы) темп углубления клинической декомпенсации (у 51,6% больных); быстрый (дни) темп отмечен у 25,1% больных, лавинообразный (часы) – у 3,2%, ундулирующее течение – у 6,4%. Последние три варианта преобладают у пожилых и стариков. Клиническая фаза ХСГ была стабильна на протяжении многих месяцев и даже лет у 4,6% больных; у 9,1% наблюдалась только положительная динамика в смене клинических фаз.
При повозрастном анализе вариабельной клинической картины ХСГ нами установлены следующие основные закономерности:
1) частое преобладание общемозговой симптоматики над очаговой во всех возрастных группах;
2) по мере увеличения возраста больных изменяется структура общемозговых симптомов – от гипертензионных в детском, молодом и среднем возрасте до гипотензионных в пожилом и старческом возрасте, что связано с преобладанием в младших возрастных группах отека мозга и внутричерепной гипертензии, а в старших возрастных группах – коллапса мозга и внутричерепной гипотензии;
3) повышение с возрастом больных роли сосудистого слагаемого в генезе симптоматики при ХСГ, что вместе с инволюционными факторами обусловливает бóльшую частоту нарушений психики у лиц старческого и пожилого возраста по сравнению с младшими возрастными группами;
4) при доминировании среди очаговой симптоматики двигательных нарушений степень их выраженности и устойчивости обычно усугубляется с возрастом;
5) наблюдается повозрастное смещение соотношения клинических фаз заболевания в сторону их утяжеления; иными словами, чем старше больной с ХСГ, тем чаще у него выявляется грубая декомпенсация. Это связано как с истощающимися с возрастом компенсаторными возможностями, так и с нарастанием инволюционной и приобретенной патологии;
6) фазовые переходы многообразны и во многом связаны с возрастными анатомо-физиологическими особенностями черепа, головного мозга и организма в целом. Если наступает клиническая декомпенсация, то наиболее быстро в фазу грубой декомпенсации входят больные пожилого и старческого возраста, что объясняется тем, что у этой категории больных компримирующее воздействие ХСГ на мозг сопровождается выраженными сосудистыми нарушениями;
7) декомпенсация при ХСГ развивается по пяти ведущим параметрам: общемозговому, стволовому, очаговому, соматическому и инструментальному. При этом для ХСГ во всех возрастных группах характерны диссоциации между различными показателями, что необходимо учитывать при установлении клинической фазы заболевания.
Соматический статус играет особую роль в оценке клинической фазы ХСГ у пожилых и стариков.
При ХСГ, в отличие от острых гематом, во всех возрастных группах могут не срабатывать привычные критические инструментальные показатели, имея в виду как их параллелизм с развертыванием общемозговой, очаговой и стволовой симптоматики, так и прогностическое значение. Например, при смещении срединных структур, достигающем критических цифр – 15 мм и более, пациент может находиться в фазе субкомпенсации и даже клинической компенсации.
Как показали исследования, возрастной и фазовый подходы весьма перспективны для оценки состояния больного, анализа данных инструментальных методов диагностики и выбора адекватной тактики лечения ХСГ.
Надо отметить, что близкое количественное распределение больных с ХСГ по группам получено и при использовании стадий T. Markwalder [9]: I стадия (нет симптоматики) – 10,1%; II стадия (легкая симптоматика) – 50,8%; III стадия (умеренная симптоматика) – 32,3%; IV стадия (грубая симптоматика) – 6,8% больных. Это обстоятельство, как представляется, свидетельствует о достаточной объективности фазного подхода к анализу клинического течения ХСГ.
Светлый промежуток при ХСГ может длиться неделями, месяцами и даже годами. Симптоматика ХСГ полиморфна. Наблюдается резкое ухудшение состояния больного спонтанно или под влиянием разных дополнительных факторов (легкая повторная травма головы, перегревание на солнце, употребление алкоголя, повышение артериального давления, простудные заболевания и т.п.). Клиническая картина при этом может напоминать различные заболевания центральной нервной системы: доброкачественные и злокачественные опухоли мозга, инсульт, спонтанное субарахноидальное кровоизлияние, церебральный атеросклероз, энцефалит, эпилепсию и др.
В период развернутой клинической картины ХСГ часты изменения сознания в виде оглушения или аментивной спутанности с нарушением памяти, ориентировки.
Среди очаговых признаков ХСГ ведущая роль принадлежит пирамидному гемисиндрому. Встречаются также речевые нарушения, гемигипалгезия, гемианопсия и др. Большой удельный вес в клинической картине ХСГ имеет экстрапирамидная симптоматика (гипомимия, брадикинезия, общая скованность, повышение мышечного тонуса по пластическому типу, подкорковый тремор и др.), выходящая за пределы возрастных изменений. Нередки нарушения статики и походки. В фазах клинической декомпенсации проявляется вторичная дислокационная среднемозговая симптоматика (парез взора вверх, двусторонние стопные знаки, анизокория, спонтанный нистагм и др.).
Над зоной расположения гематомы может отмечаться притупление перкуторного звука.
Диагностика
Наряду с клинической симптоматикой в разпознавании ХСГ велика роль инструментальных методов исследования, среди которых доминируют компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) [8, 10].Компьютерная томография
 ХСГ представляет собой на КТ зону измененной плотности между костями черепа и веществом мозга, обычно серповидной формы с многодолевым распространением и преимущественно парасагиттально-конвекситальной локализацией; при этом наружная граница повторяет очертания внутренней поверхности костей черепа, а внутренняя граница – очертания полушария мозга (рис. 3, 4).
ХСГ представляет собой на КТ зону измененной плотности между костями черепа и веществом мозга, обычно серповидной формы с многодолевым распространением и преимущественно парасагиттально-конвекситальной локализацией; при этом наружная граница повторяет очертания внутренней поверхности костей черепа, а внутренняя граница – очертания полушария мозга (рис. 3, 4).Семиотика. По плотности мы разделили ХСГ на гиподенсивные (28 и менее Ед. H), изоденсивные (29–45 Ед. Н), гиперденсивные (более 45 Ед. Н), а также гетероденсивные (рис. 5).
Гиподенсивные ХСГ встречаются наиболее часто. Снижение плотности содержимого гематомы колеблется от выраженного до незначительного (17–28 Ед. Н), однако всегда превышает плотность ликвора. Чаще гиподенсивная зона гомогенна, но порой улавливаются и разные по интенсивности участки снижения плотности. На этом фоне могут выявляться линейные повышения плотности за счет визуализации наружного или внутреннего листка капсулы либо перегородок при многокамерной ХСГ.
Сопоставление данных КТ с операционными находками показывает, что у большинства больных с гиподенсивными ХСГ в полости гематомы содержится ксантохромная либо коричневато-зеленоватая мутная жидкость, у некоторых – измененная разжиженная кровь, а также мелкие свертки крови.
При гиподенсивных ХСГ длительность анамнеза колеблется в широких пределах – от 25 сут до 5 лет, иногда от 14 сут. Феномен снижения плотности содержимого ХСГ преимущественно связан с деградацией фибрина в свертках крови.
Изоденсивные ХСГ встречаются реже. Плотность содержимого гематомы практически не отличается от вещества мозга. Вместе с тем на КТ обычно выражены признаки объемного процесса и, что характерно при ХСГ, отсутствуют конвекситальные субарахноидальные пространства на стороне поражения.
Сопоставление данных КТ с операционными находками показывает, что у половины больных с изоденсивными ХСГ в полости гематом содержится коричневато-зеленоватая жидкость, у других – разжиженная кровь и ее свертки.
Изоденсивные ХСГ отмечены при длительности анамнеза от 18 сут до 1 года. Феномен изоплотности может появляться и раньше: порой спустя 10–14 сут после черепно-мозговой травмы. Он определяется главным образом соотношением разжиженной крови и ее дериватов в полости ХСГ.
Гиперденсивные ХСГ встречаются редко. Повышение плотности содержимого гематом варьирует от нерезко выраженного до значительного.
 При гиперденсивных ХСГ в большинстве случаев в полости гематомы содержатся, наряду с разжиженной кровью, ее свертки. Отметим, что чем в большем объеме в гематоме преобладают свертки крови, тем выше ее плотность. Феномен повышения плотности связан с повторными кровоизлияниями в полость гематомы, которые могут наблюдаться спустя любое время после формирования ХСГ.
При гиперденсивных ХСГ в большинстве случаев в полости гематомы содержатся, наряду с разжиженной кровью, ее свертки. Отметим, что чем в большем объеме в гематоме преобладают свертки крови, тем выше ее плотность. Феномен повышения плотности связан с повторными кровоизлияниями в полость гематомы, которые могут наблюдаться спустя любое время после формирования ХСГ.Гетероденсивные ХСГ встречаются часто. Представлены на КТ мозаичными картинами: в полости гематомы в различных соотношениях сочетаются участки повышенной и пониженной плотности, реже пониженной плотности и плотности, равной таковой вещества мозга, а в отдельных случаях наблюдаются все три варианта изменений плотности ХСГ.
Для гетерогенных ХСГ характерен феномен седиментации в виде четкого разграничения содержимого гематомы на низкоплотную верхнюю часть и высокоплотную нижнюю часть (при положении больного на спине).
При сопоставлении данных КТ с операционными находками установлено, что у 2/3 больных полость гематомы содержит свертки крови в смеси с зеленовато-коричневатой жидкостью, у остальных – темную жидкую кровь и мелкие сгустки фибрина.
Длительность анамнеза при гетероденсивных ХСГ колеблется от 16 сут до 5 лет. Неоднородная плотность связана как с повторными макро- и микрокровоизлияниями в полость гематомы, так и с деградацией ранее излившейся крови. Оседание высокоплотных, еще не распавшихся форменных элементов крови обусловливает появление КТ-феномена седиментации.
В структуре ХСГ на КТ могут также прослеживаться уплотненные листки капсулы, тяжи, межкамерные перегородки и некоторые другие образования. Капсула ХСГ выявляется при КТ примерно в 10-й части наблюдений, хотя на операциях наружную и внутреннюю мембрану (выраженные в различной степени) находят практически всегда. Эта диссоциация может быть объяснена малой контрастируемостью капсулы, нередко ее тонкостью, прилежанием к костям черепа и веществу мозга с повторением их очертаний. Возможно также, что в ряде случаев невыявление существующей капсулы ХСГ на КТ обусловлено тем, что не всегда используют контрастное усиление.
Применение трехмерной реконструкции ХСГ с помощью спиральной КТ расширило анатомо-топографические представления об осумкованных кровоизлияниях, показав их соотношение как с мозговыми структурами, так и с сосудами полушарий (феномен бессосудистой зоны); см. рис. 4.
Современные возможности перфузионных методик (КТ-перфузия) позволяют оценивать состояние объемного мозгового кровотока при ХСГ и его динамику в послеоперационном периоде.
Представим выделенный нами компьютерно-томографический синдром ХСГ. Наиболее часто он характеризуется:
– зоной измененной плотности (гиподенсивной, гиперденсивной, гетероденсивной) между костями черепа и веществом мозга, чаще серповидной формы и обычно имеющей многодолевое или плащевое распространение (одно- или двухстороннее) с преимущественно парасагиттально-конвекситальной локализацией;
– повторением очертаний внутренней поверхности костей черепа наружной границей патологической зоны измененной плотности и очертаний поверхности полушария головного мозга – ее внутренней границей;
– значительным преобладанием площади патологической зоны над ее толщиной;
– отсутствием субарахноидальных щелей на стороне расположения гематомы с одновременным дислокационным воздействием на гомолатеральный боковой желудочек.
При ХСГ редкой атипичной локализации (базальная, межполушарная, заднечерепная и др.) КТ-синдромы, наряду с общими чертами, имеют много существенных отличий от выделенного КТ-синдрома наиболее распространенной типичной полушарной локализации ХСГ.
При двусторонней ХСГ важными дополнительными компьютерно-томографическими признаками являются отсутствие изображения конвекситальных субарахноидальных щелей с обеих сторон и феномен сближения передних и задних рогов боковых желудочков, а также изменение их талии.
КТ-синдром ХСГ может дополняться и другими прямыми их признаками: феноменом седиментации, визуализацией наружного или внутреннего листков капсулы, многокамерного строения или интрагематомных трабекул (их выявлению часто может способствовать контрастное усиление).
Магнитно-резонансная томография
Ведущим методом неинвазивного распознавания ХСГ, наряду с КТ, стала МРТ. Ее преимущества особенно очевидны при изоденсивных гематомах (рис. 6). Для МРТ не существует рентгеновского барьера изоденсивных тканей и вместе с тем исключительно широки пределы разграничения структур с различным содержанием воды и различными магнитными свойствами.Для ХСГ характерна высокая контрастность изображения на МР-томограммах по сравнению с прилежащим веществом мозга. Зоны повышенного сигнала, соответствующие расположению и размерам ХСГ, имеют серповидную либо линзообразную форму с четкими контурами и примыкают к костям свода черепа (см. рис. 6). При этом определяются также выраженные в разной степени вторичные признаки объемного процесса – деформация и смещение желудочковой системы, сдавление конвекситальных субарахноидальных щелей на стороне поражения и др.
Сопоставление КТ и МРТ при распознавании ХСГ представлено на рис. 6. Высокая контрастность изображения ХСГ на МР-томограммах особенно существенна при изоденсивных гематомах, а также при распространенных плоскостных оболочечных гематомах толщиной до 10 мм, которые нередко плохо определяются при КТ. МРТ способна выявлять структуру гематомы, ее капсулу и другие особенности ХСГ. Четко визуализируется сопровождающая ХСГ различная очаговая патология мозга.
Высокая информативность МРТ при ХСГ объясняется изменением валентности железа при образовании метгемоглобина, приобретением им гидрофильных и парамагнитных свойств.
Примененная нами методика функционального МРТ-картирования при ХСГ позволяет уточнять локализацию и состояние функционально значимых зон больших полушарий (рис. 7).
Прикладным итогом проведенных нами исследований является выделение МРТ-синдрома ХСГ. Он характеризуется:
а – наличием контрастной зоны усиления сигнала, чаще гомогенной, над веществом головного мозга, имеющей многодолевое или плащевое распространение (одно- или двустороннее) с конвекситальной или парасагиттальной локализацией и наружными контурами, повторяющими рельеф костей свода черепа, четкими внутренними контурами, ровными или повторяющими очертания борозд и извилин мозга;
б – значительным преобладанием площади зоны патологического сигнала над ее толщиной при преимущественно серповидной форме на аксиальных срезах и преимущественно линзообразной – на фронтальных срезах;
в – удлинением времени спин-спинновой (Т2) при укорочении времени спин-решеточной (Т1) релаксации (не наблюдаемым при подавляющем большинстве других объемных внутричерепных образований), что выражается в высокой контрастности изображения на томограммах, полученных как в импульсной последовательности SE с сильной зависимостью от (Т2) релаксационного времени, так и положительной контрастности на томограммах, полученных в импульсном режиме IR.
Итак, МРТ является наиболее надежным полипроекционным методом неинвазивного распознавания хронических внутричерепных гематом независимо от их расположения, объема и характера содержимого.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах / Information about the authors
Лихтерман Леонид Болеславович – д-р мед. наук, проф., невролог, гл. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. ак. Н.Н. Бурденко». E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Leonid B. Likhterman – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. E-mail: ova@nsi.ru; ORCID: 0000-0002-9948-9816
Кравчук Александр Дмитриевич – д-р мед. наук, проф., нейрохирург, зав. 9-м нейрохирургическим отделением, ФГАУ «НМИЦ нейрохирургии им. ак. Н.Н. Бурденко». ORCID: 0000-0002-3112-8256
Aleksandr D. Kravchuk – D. Sci. (Med.), Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0002-3112-8256
Охлопков Владимир Александрович – канд. мед. наук, доцент, нейрохирург, ст. науч. сотр. 9-го нейрохирургического отделения, ФГАУ «НМИЦ нейрохирургии им. ак. Н.Н. Бурденко». ORCID: 0000-0001-8911-2372
Vladimir A. Okhlopkov – Cand. Sci. (Med.), Assoc. Prof., Burdenko National Medical Research Center for Neurosurgery. ORCID: 0000-0001-8911-2372
Статья поступила в редакцию / The article received: 16.03.2021
Статья принята к печати / The article approved for publication: 19.03.2021
Список исп. литературыСкрыть список1. Потапов А.А., Лихтерман Л.Б., Кравчук А.Д. Хронические субдуральные гематомы. Москва, 1997.
[Potapov A.A., Likhterman L.B., Kravchuk A.D. Khronicheskie subdural'nye gematomy. Moscow, 1997 (in Russian).]
2. Коновалов А.Н., Кравчук А.Д., Потапов А.А. и др. Минимально инвазивная хирургия хронических субдуральных гематом. В кн.: Реконструктивная и минимально инвазивная хирургия последствий черепно-мозговой травмы. Москва, 2012. C. 226–83.
[Konovalov A.N., Kravchuk A.D., Potapov A.A. et al. Minimal'no invazivnaia khirurgiia khronicheskikh subdural'nykh gematom. In: Rekonstruktivnaia i minimal'no invazivnaia khirurgiia posledstvii cherepno-mozgovoi travmy. Moscow, 2012. P. 226–83 (in Russian).]
3. Loew F. Management of chronic subdural haematomas and hydromas. Adv Techn stand Neurosurgery 1982; 9: 113–31.
4. Rust T, Kiemer N, Albert Erasmus A. Chronic subdural haematomas and anticoagulation or antithrombotic therapy. J Clin Neuroscience 2006; 13 (8): 823–7.
5. Chen JCT, Levy ML. Causes, Epidemiology, and Risk Factors of Chronic Subdural Hematoma. Neurosurg Clin N Am 2000; 11 (3): 339–406.
6. Swift DM, McBride L. Chronic subdural hematoma in children. Neurosurg Clin N Am 2000; 11 (3): 439–46.
7. Kuwamura K et al. Epidemiologic aspect of chronic subdural hematoma. Recent Advances in Neurotraumatology. Tokyo: SpringerVerlag, 1993. P. 450–52.
8. Лихтерман Л.Б. Черепно-мозговая травма. Диагностика и лечение. ГЭОТАР-Медиа. Москва, 2014.
[Likhterman L.B. Cherepno-mozgovaia travma. Diagnostika i lechenie. GEOTAR-Media. Moscow, 2014 (in Russian).]
9. Markwalder T, Seilor R. Chronic subdural hematoma: to drain or not drain? Neurosurgery 1985; 16 (2): 185–8.
10. Коновалов А.Н., Лихтерман Л.Б., Эль-Кади Х. Дифференцированное лечение хронических субдуральных гематом. Вопросы нейрохирургии. 1990; 1: 29–33.
[Konovalov A.N., Likhterman L.B., El'-Kadi Kh. Differentsirovannoe lechenie khronicheskikh subdural'nykh gematom. Voprosy neirokhirurgii. 1990; 1: 29–33 (in Russian).]


