Клинический разбор в общей медицине №7 2024
Аннотация
В данном клиническом наблюдении и обзоре литературы представлены возможности диагностических исследований для изучения редкого патологического состояния – интравенозного лейомиоматоза. Правильная интерпретация данных инструментальной визуализации и морфологическая верификация интравенозного лейомиоматоза помогает выполнить своевременное и полноценное хирургическое лечение.
Ключевые слова: лейомиома, внутривенный лейомиоматоз, интравенозный лейомиоматоз, сосудистый тромб, магнитно-резонансная томография, компьютерная томография.
Для цитирования: Шеберова Е.В., Рябов А.Б., Агабабян Т.А., Гриневич В.Н., Афонин Г.В., Колобаев И.В., Цыгельников С.А., Терс-ких Д.С., Минаева Н.Г., Иванов С.А., Каприн А.Д. Лучевые методы в диагностике интравенозного лейомиоматоза: описание клинического случая и обзор литературы. Клинический разбор в общей медицине. 2024; 5 (7): 52–58. DOI: 10.47407/kr2024.5.7.00p426
Imaging of intravenous leiomyomatosis: a case report and literature review
Elizaveta V. Sheberova1, Andrey B. Ryabov2,3, Tatev A. Agababyan1, Vyacheslav N. Grinevich1,2, Grigory V. Afonin1, Ilya V. Kolobaev2, Stanislav A. Tsygelnikov2,4, Dmitry S. Terskikh5,
Natalia G. Minaeva1, Sergey A. Ivanov1,6, Andrey D. Kaprin2,6
1Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre, Obninsk, Russia;
2Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre, Moscow, Russia;
3National Medical Research Radiological Centre of the Ministry of Health of the Russian Federation, Moscow, Russia;
4Pirogov Russian National Research Medical University, Moscow, Russia;
5Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia;
6Patrice Lumumba People’s Friendship University of Russia (RUDN University), Moscow, Russia
lisa_iroshnikova@mail.ru
Abstract
This case report and literature review presents the imaging features of the rare pathological condition – intravenous leiomyomatosis. Correct interpretation of diagnostic imaging data and morphological verification of intravenous leiomyomatosis helps to perform timely and complete surgical treatment.
Keywords: leiomyoma, intravenous leiomyomatosis, vascular thrombus, magnetic resonance imaging, computed tomography.
For citation: Sheberova E.V., Ryabov A.B., Agababian T.A., Grinevich V.N., Afonin G.V., Kolobaev I.V., Tsygelnikov S.A., Terskih D.S., Minae-va N.G., Ivanov S.A., Kaprin A.D. Imaging of intravenous leiomyomatosis: a case report and literature review. Clinical review for general practice. 2024; 5 (7): 52–58. (In Russ.). DOI: 10.47407/kr2024.5.7.00p426
Лейомиомы – это моноклональные опухоли из гладкомышечных клеток миометрия [1]. Частота выявления лейомиомы матки зависит от метода диагностики, а «золотым стандартом» считается патоморфологическое исследование. Согласно литературным данным, большая часть случаев лейомиомы матки клинически проявляются в позднем репродуктивном и перименопаузальном периоде, и являются одной из самых частых причиной обращения к гинекологу [2]. Выявленные лейомиомы классифицируются как доброкачественные, однако иногда встречаются варианты лейомиом, при которых однозначно нельзя определить их характер, поскольку их морфологические признаки не противоречат доброкачественным новообразованиям, но они характеризуются злокачественными клиническими проявлениями. Согласно классификации Всемирной организации здравоохранения, эти образования классифицируются, как гладкомышечные опухоли неясного злокачественного потенциала. Именно к таким заболеваниям относят редко встречающуюся метастазирующую лейомиому и интравенозный лейомиоматоз (ИВЛ) [3].
Своевременная диагностика ИВЛ представляет собой огромную проблему, так как примерно у 30% пациентов на ранней стадии нет никаких симптомов и отсутствуют специфические онкомаркеры. В поздних стадиях диагностика затруднена тем, что состояние редко встречается и проявляется многообразием неспецифических симптомов [4, 5].
Целью статьи явилось описание редкого клинического случая пациентки с внетазовой ИВЛ и анализ возможностей различных методов визуализации для диагностики данного заболевания.
Клиническое наблюдение
Пациентка Ч., 1952 г., в анамнезе лапаротомия, надвлагалищная ампутация матки без придатков. Операционный материал не предоставлен. Спустя три года после операции появились жалобы на боли внизу живота, увеличение живота в объеме, одышку, отеки. По данным ультразвукового исследования (УЗИ) по месту жительства – объемное образование малого таза. Выполнена биопсия образования. Консультирована в НМИЦ радиологии. Выполнен пересмотр биопсийного материала в рамках телемедицинской консультации.
 Заключение по морфологическому исследованию: хронический цервицит, фрагменты опухоли, принадлежащей, вероятнее всего, к лейомиоме с отеком стромы узла. Рекомендовано исследование материала в большем объеме.
Заключение по морфологическому исследованию: хронический цервицит, фрагменты опухоли, принадлежащей, вероятнее всего, к лейомиоме с отеком стромы узла. Рекомендовано исследование материала в большем объеме.
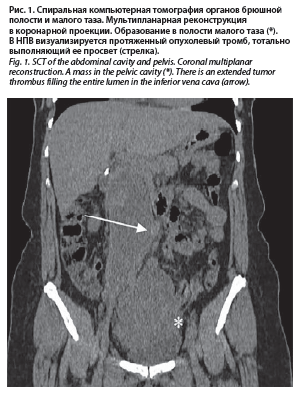
Представлены данные компьтерной томографии (КТ) органов грудной клетки, брюшной полости и малого таза без контрастного усиления. Визуализировано объемное образование малого таза, расширение нижней полой вены (НПВ), вероятно, за счет прорастания опухоли по ходу ее стенок. Косвенные КТ-признаки синдрома НПВ. Патологии со стороны органов грудной полости в условиях нативного исследования не получено (рис. 1).
На УЗИ сердца выявлено подвижное образование в полости правого предсердия (68×36 мм), стенозирующее транстрикуспидальный поток в фазу желудочковой диастолы, компрессирующее межпредсердную перегородку в фазу желудочковой систолы и, по-видимому, имеющее происхождение из субстрата, обтурирующего НПВ, в супраренальном отделе – более 60% по диаметру. В полости перикарда – до 40 мл экссудата.
Так как у пациентки аллергическая реакция на контрастное вещество в анамнезе, принято решение отказаться от проведения КТ с контрастным усилением. Назначена магнитно-резонансная томография (МРТ) органов брюшной полости и малого таза.
На МРТ органов малого таза с контрастированием (рис. 2) в полости малого таза, в ложе удаленного тела матки, смещая мочевой пузырь и шейку матки влево, определялось объемное опухолевое образование с гетерогенным сигналом на Т2ВИ, неравномерным накоплением контрастного вещества, размерами до 7,9×11,2×7,8 см. Образование прорастало в параметрий, культю шейки матки, плотно прилежало к правой стенке мочевого пузыря и, вероятно, правому яичнику. В просвете НПВ на уровне исследования, распространяясь на общую подвздошную вену справа, а также внутреннюю и наружную (в проксимальном отделе) подвздошные вены справа, визуализировалось опухолевое образование с аналогичными сигнальными характеристиками, местами прорастающее в окружающую клетчатку, расширяющее просвет вен до 1,5–5,0 см.
На МРТ органов брюшной полости с контрастированием (рис. 3) НПВ расширена до 6,2 см в диаметре, просвет субтотально выполнен неоднородным содержимым без достоверных признаков ограничения диффузии, с нижним полюсом изменений в области малого таза, верхним – в правом предсердии.
Таким образом, МР-картина соответствовала опухолевому образованию в ложе удаленного тела матки с вовлечением параметрия, шейки матки. Опухолевая эмболия НПВ, правых общей, наружной и внутренней подвздошных вен.
Поставлен предварительный диагноз: интравенозный леомиоматоз с дифференциальным диагнозом лейомиосаркомы. Повторная биопсия образования была не показана, так как результат не повлиял бы на тактику лечения. Рекомендовано удаление образования культи шейки матки.
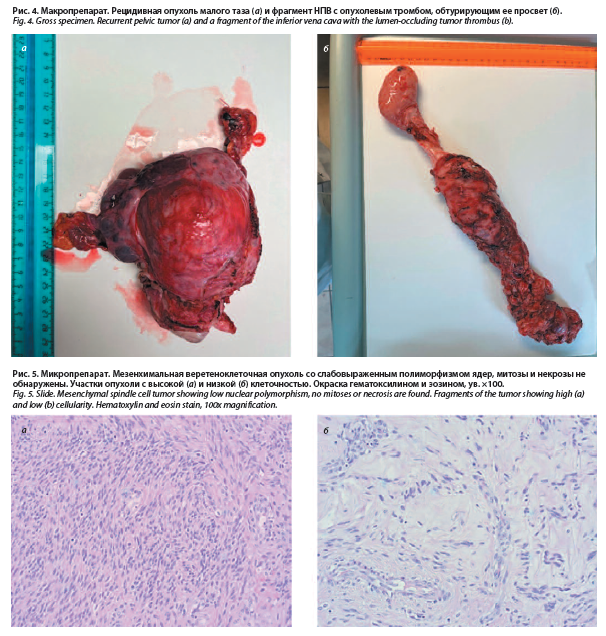
Пациентке было проведено хирургическое лечение в объеме стернотомии, лапаротомии, резекции НПВ, тромбэктомии из правого предсердия, удаления рецидивной опухоли в малом тазу с использованием аппарата искусственного кровообращения. Интраоперационно в малом тазу выявлено опухолевое образование размерами до 12 см, умеренно подвижное. НПВ расширена на всем протяжении, максимально до 7 см в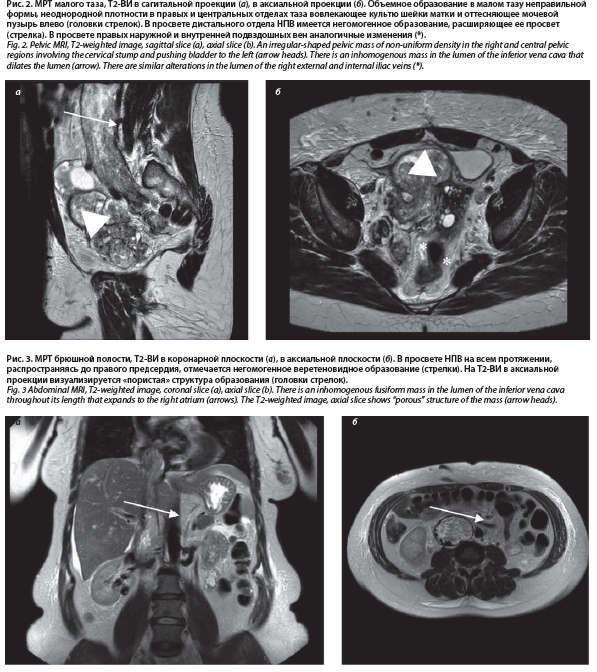 диаметре. Мобилизована НПВ в инфраренальном отделе, слева – до общей подвздошной вены, справа – до конфлюенса внутренней и наружной правых подвздошных вен. Наибольший опухолевый узел в малом тазу удален. При дальнейшей ревизии выявлено, что опухоль вовлекает внутреннюю подвздошную вену справа с образованием опухолевого тромба. В условиях искусственного кровообращения выполнено продольное рассечение правого предсердия с продлением на НПВ. Из полости правого предсердия извлечена верхушка тромба. Макроскопическое описание: рецидивная опухоль малого таза в виде узла максимальным размером 10 см и резецированная НПВ длиной 26 см, просвет ее расширен до 5 см и обтурирован опухолевым тромбом (рис. 4).
диаметре. Мобилизована НПВ в инфраренальном отделе, слева – до общей подвздошной вены, справа – до конфлюенса внутренней и наружной правых подвздошных вен. Наибольший опухолевый узел в малом тазу удален. При дальнейшей ревизии выявлено, что опухоль вовлекает внутреннюю подвздошную вену справа с образованием опухолевого тромба. В условиях искусственного кровообращения выполнено продольное рассечение правого предсердия с продлением на НПВ. Из полости правого предсердия извлечена верхушка тромба. Макроскопическое описание: рецидивная опухоль малого таза в виде узла максимальным размером 10 см и резецированная НПВ длиной 26 см, просвет ее расширен до 5 см и обтурирован опухолевым тромбом (рис. 4).
Микроскопическое описание: мезенхимальная веретеноклеточная опухоль со слабовыраженным полиморфизмом ядер, митозы и некрозы не обнаружены (рис. 5). Морфологическая картина соответствует ИВЛ, ассоциированному с лейомиомой матки.
Пациентка выписана на 17-е сутки в удовлетворительном состоянии.
Обсуждение
ИВЛ – редкая, но важная клиническая ситуация. Ранняя диагностика ИВЛ и своевременное хирургическое вмешательство имеют решающее значение, ведь зачастую интравенозный и внутрисердечный лейомиоматоз вызывают не только сердечные симптомы, в числе которых клинические проявления застойной сердечной недостаточности, но и способны привести к тромбоэмболии легочной артерии и внезапной смерти больного [5, 6].
Случай «метастазирования» доброкачественной опухоли матки в легкое был описан W. Minakowski. Еще в 1901 г. Штейнером был предложен термин «метастазирующая фибромиома матки» [3]. Р. Steiner упоминает также термин «доброкачественная метастазирующая лейомиома», которая характеризуется множественными доброкачественными метастатическими лейомиомами в органах и тканях у пациенток, имеющих
лейомиому матки при отсутствии данных о другом опухолевом процессе [3]. Наблюдение именно ИВЛ было описано в 1896 г., а первый представленный случай с расширением правого предсердия при вскрытии датирован 1907 г. [6]. Внутривенный лейомиоматоз чаще встречается у женщин в пременопаузе, у большинства этих женщин (90%) были роды [7]. Возраст пациенток обычно составляет 20–70 лет, в среднем – 45 лет. Частота встречаемости ИВЛ составляет 0,097% от всех лейомиом. К настоящему времени случаи ИВЛ с внутрисердечным распространением составляют около 10%, а в мировой литературе всего зарегистрировано около 300 случаев [8, 9].
Были предложены две основные теории возникновения внутривенного лейомиоматоза. Согласно теории O.K. Steinmetz и соавт. опухоль распространяется путем инвазии уже существующей лейомиомы матки в просветы венозных сосудов [10]. E. Knauer и соавт. полагают, что ИВЛ может развиваться путем метаплазии гладкомышечных клеток стенок вен матки [11]. Также возможно сочетание двух теорий.
ИВЛ может ограничиваться инвазией в маточные вены или распространяться по всей венозной системе, достигая сердца или легочных артерий. Прогноз у пациентов с внетазовой ИВЛ неблагоприятный. Когда ИВЛ распространяется в НПВ, частота рецидивов увеличивается до 30% [12]. При ограничении ИВЛ полостью таза частота рецидивов составляет 5,4% по данным исследования 166 случаев [13].
Таким образом, ранняя диагностика имеет решающее значение для благоприятного прогноза у пациентов с ИВЛ [14].
P.M. Lam и соавт. описали один из возможных путей распространения в системный венозный кровоток через маточную вену, которая может распространяться на внутренние подвздошные вены, общие подвздошные вены, а затем на НПВ [15].
Другие авторы подтверждают внеорганное распространение клеток миомы через вены широкой связки матки, вагинальные и
яичниковые вены. Около 25% клеток опухолей таким путем могут мигрировать гематогенным путем в бассейн полой вены, в сердце, легкие, тазовые лимфатические узлы [16, 17].
В представленном клиническом случае вероятнее всего имел место путь распространения через маточную, внутренние и общие подвздошные вены в НПВ.
ИВЛ клинически подразделяется на четыре стадии в зависимости от степени распространения опухоли [18]. Стадия I относится к инвазии опухолью стенки маточной вены, которая ограничена тазом. II стадия предполагает инвазию опухоли в брюшную полость без поражения почечной вены. III стадия характеризуется дальнейшим распространением опухоли в правое предсердие без поражения легочной артерии. Стадия IV характеризуется вовлечением опухоли в легочную артерию и/или метастазами в легкие. Это не официальная парадигма стадирования ИВЛ, а предложенная некоторыми авторами иерархия клинических стадий.
 Дифференциальный диагноз ИВЛ преимущественно включает: тромбы в системных венах, доброкачественную метастазирующую лейомиому, лейомиосаркому, возникающую из стенки НПВ, миксому правого предсердия и опухолевый тромбоз при карциноме, поскольку эти образования имеют сходные характеристики КТ или МРТ [19, 20].
Дифференциальный диагноз ИВЛ преимущественно включает: тромбы в системных венах, доброкачественную метастазирующую лейомиому, лейомиосаркому, возникающую из стенки НПВ, миксому правого предсердия и опухолевый тромбоз при карциноме, поскольку эти образования имеют сходные характеристики КТ или МРТ [19, 20].
Внутритазовый ИВЛ часто не имеет типичных особенностей при УЗИ и КТ, что затрудняет дифференциальную диагностику с лейомиомой, особенно при небольших интрамуральных поражениях. Поэтому своевременная и точная диагностика ИВЛ I стадии с помощью МРТ особенно важна для достижения благоприятных результатов лечения пациентов.
Характерная картина ИВЛ при МРТ включает в себя наличие крупного образования неправильной формы в матке и параметрии, часто с сопутствующей лейомиомой и поражением широкой связки матки, с изоинтенсивным сигналом на T1ВИ и слабо гиперинтенсивным сигналом на T2ВИ. Также ИВЛ могут быть представлены извитыми плотными образованиями неправильной формы в миометрии или параметрии, с наличием сосудистых структур в толще с множественными внутрисосудистыми дефектами заполнения, которые визуализируются при T2ВИ [21].
Другие исследователи отмечают, что на МР-изображении опухолевое поражение выглядело как растительная губка люффа на корональных изображениях FIESTA, а также как сетчатая и пористая структура на аксиальных изображениях в Т2ВИ [22]. Ряд авторов дает следующие характеристики опухоли при МР-
исследовании: трубчатая структура неоднородного сигнала, с активным накоплением препарата на основе гадоксетовой кислоты [22, 23]. Некоторые авторы описывают ИВЛ как «червеобразную» неоднородную опухоль, достигающую по сосудам камер сердца [23]. Внутри структуры опухоли ИВЛ нередко могут наблюдаться трубчатые структуры, которые отражают расширенные сосуды, что было подтверждено рядом ученых при выполнении операции [23].
Эхокардиография является предпочтительным методом первичной визуализации, использующимся для оценки внутрисердечных поражений. В качестве уточняющих методов проводятся КТ и МРТ, которые способны внести дополнительную информацию о протяженности и характере поражения, а также скорректировать план операционного вмешательства [26].
Пациентам с внетазовым ИВЛ рекомендуется проводить КТ в рамках комплексного
обследования перед операцией с целью определения распространения процесса [27].
В описанном R.J. Fornaris и соавт. наблюдении при КТ грудной клетки и брюшной полости с контрастным усилением визуализировался удлиненный дефект наполнения в правом предсердии и правом желудочке, распространяющийся на НПВ, левую почечную вену и левую гонадную вену за счет образования неоднородной структуры, неравномерно накапливающего контрастное вещество [28].
L. Kang и соавт. также отметили образование неоднородной структуры на постконтрастных сериях при КТ, с меньшей плотностью опухоли по сравнению с контрастным усилением кровотока в НПВ и правом предсердии [22].
Оперативное лечение при выявленной ИВЛ направлено на полную резекцию всей опухоли с доступом наиболее безопасным для пациента, чаще всего с помощью одно- или двухэтапной операции. Если в исходе операции достигается полная резекция, то рецидив возникает крайне редко [27]. У некоторых пациентов при не полностью удаленной внутривенной опухоли может наблюдаться постоянный или отсроченный продолженный рост с частотой рецидивов до 30% [23].
Заключение
Таким образом, методы лучевой диагностики играют важную роль в диагностике и наблюдении пациентов с диагнозом ИВЛ. Дифференциальный диагноз включает сосудистый тромб, а также первичные и метастатические опухоли. Междисциплинарный подход в изучении ИВЛ позволяет разработать необходимый алгоритм инструментальной диагностики столь редкого патологического состояния с целью оптимизации выбора тактики лечения.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Шеберова Елизавета Викторовна – врач-рентгенолог, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии».
E-mail: lisa_iroshnikova@mail.ru; ORCID: 0000-0001-7827-2741
Elizaveta V. Sheberova – Radiologist, Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. E-mail: lisa_iroshnikova@mail.ru;
ORCID: 0000-0001-7827-2741
Рябов Андрей Борисович – д-р мед. наук, зам. ген. директора по хирургии, ФГБУ «НМИЦ радиологии»; руководитель отдела торакоабдоминальной онкохирургии, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-1037-2364
Andrey B. Ryabov – Dr. Sci. (Med.), National Medical Research Radiological Centre, Moscow; Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-1037-2364
Агабабян Татев Артаковна – канд. мед. наук, зав. отд-нием лучевой диагностики, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-9971-3451
Tatev A. Agababyan – Cand. Sci. (Med.), Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-9971-3451
Гриневич Вячеслав Николаевич – канд. мед. наук, зав. отд-нием онкопатологии, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии»; зав. патологоанатомическим отделением МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0003-1908-2256
Vyacheslav N. Grinevich – Cand. Sci. (Med.), Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre; Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID:0000-0003-1908-2256
Афонин Григорий Владиславович – канд. мед. наук, и.о. зав. отд-нием лучевого и хирургического лечения заболеваний торакальной области, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-7128-2397
Grigory V. Afonin – Cand. Sci. (Med.), Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-7128-2397
Колобаев Илья Владимирович – канд. мед. наук, зав. торакоабдоминальным отделением, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-3573-6996
Ilya V. Kolobaev – Cand. Sci. (Med.), Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-3573-6996
Цыгельников Станислав Анатольевич – д-р мед. наук, проф. каф. факультетской хирургии, ФГАОУ ВО «РНИМУ
им. Н.И. Пирогова»; сердечно-сосудистый хирург, МНИОИ
им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии».
AuthorID: 470248
Stanislav A. Tsygelnikov – Dr. Sci. (Med.), Prof., Pirogov Russian National Research Medical University; Cardiovascular Surgeon, Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre. AuthorID: 470248
Терских Дмитрий Сергеевич – студент 6 курса лечебного факультета, ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет)
Dmitry S. Terskikh – 6th year student, Sechenov First Moscow State Medical University (Sechenov University)
Минаева Наталья Георгиевна – канд. биол. наук, вед. науч. сотр. научно-образовательного отдела, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0009-0004-9583-6501
Natalia G. Minaeva – Cand. Sci. (Biol.), Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID: 0009-0004-9583-6501
Иванов Сергей Анатольевич – чл.-корр. РАН, д-р мед. наук, проф. каф. онкологии и рентгенорадиологии им. В.П. Харченко медицинского института РУДН, директор МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0001-7689-6032
Sergey A. Ivanov – Corr. Memb. RAS, Dr. Sci. (Med.), Director of Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre, Prof., Patrice Lumumba People’s Friendship University of Russia (RUDN University). ORCID: 0000-0001-7689-6032
Каприн Андрей Дмитриевич – академик РАН, д-р мед. наук, проф., зав. каф. онкологии и рентгенорадиологии им.
В.П. Харченко медицинского института РУДН, дир. МНИОИ
им. П.А. Герцена (филиал ФГБУ «НМИЦ радиологии»), ген. дир. ФГБУ «НМИЦ радиологии». ORCID: 0000-0001-8784-8415
Andrey D. Kaprin – Acad. RAS, Dr. Sci. (Med.), Full Prof., Patrice Lumumba People’s Friendship University of Russia (RUDN University), Director Hertsen Moscow Oncology Research Institute, General Director National Medical Research Radiological Centre. ORCID: 0000-0001-8784-8415
Поступила в редакцию: 03.07.2024
Поступила после рецензирования: 11.07.2024
Принята к публикации: 11.07.2024
Revised: 11.07.2024
Revised: 11.07.2024
Accepted: 11.07.2024
Клинический разбор в общей медицине №7 2024
Лучевые методы в диагностике интравенозного лейомиоматоза: описание клинического случая и обзор литературы
Аннотация
В данном клиническом наблюдении и обзоре литературы представлены возможности диагностических исследований для изучения редкого патологического состояния – интравенозного лейомиоматоза. Правильная интерпретация данных инструментальной визуализации и морфологическая верификация интравенозного лейомиоматоза помогает выполнить своевременное и полноценное хирургическое лечение.
Ключевые слова: лейомиома, внутривенный лейомиоматоз, интравенозный лейомиоматоз, сосудистый тромб, магнитно-резонансная томография, компьютерная томография.
Для цитирования: Шеберова Е.В., Рябов А.Б., Агабабян Т.А., Гриневич В.Н., Афонин Г.В., Колобаев И.В., Цыгельников С.А., Терс-ких Д.С., Минаева Н.Г., Иванов С.А., Каприн А.Д. Лучевые методы в диагностике интравенозного лейомиоматоза: описание клинического случая и обзор литературы. Клинический разбор в общей медицине. 2024; 5 (7): 52–58. DOI: 10.47407/kr2024.5.7.00p426
Imaging of intravenous leiomyomatosis: a case report and literature review
Elizaveta V. Sheberova1, Andrey B. Ryabov2,3, Tatev A. Agababyan1, Vyacheslav N. Grinevich1,2, Grigory V. Afonin1, Ilya V. Kolobaev2, Stanislav A. Tsygelnikov2,4, Dmitry S. Terskikh5,
Natalia G. Minaeva1, Sergey A. Ivanov1,6, Andrey D. Kaprin2,6
1Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre, Obninsk, Russia;
2Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre, Moscow, Russia;
3National Medical Research Radiological Centre of the Ministry of Health of the Russian Federation, Moscow, Russia;
4Pirogov Russian National Research Medical University, Moscow, Russia;
5Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia;
6Patrice Lumumba People’s Friendship University of Russia (RUDN University), Moscow, Russia
lisa_iroshnikova@mail.ru
Abstract
This case report and literature review presents the imaging features of the rare pathological condition – intravenous leiomyomatosis. Correct interpretation of diagnostic imaging data and morphological verification of intravenous leiomyomatosis helps to perform timely and complete surgical treatment.
Keywords: leiomyoma, intravenous leiomyomatosis, vascular thrombus, magnetic resonance imaging, computed tomography.
For citation: Sheberova E.V., Ryabov A.B., Agababian T.A., Grinevich V.N., Afonin G.V., Kolobaev I.V., Tsygelnikov S.A., Terskih D.S., Minae-va N.G., Ivanov S.A., Kaprin A.D. Imaging of intravenous leiomyomatosis: a case report and literature review. Clinical review for general practice. 2024; 5 (7): 52–58. (In Russ.). DOI: 10.47407/kr2024.5.7.00p426
Лейомиомы – это моноклональные опухоли из гладкомышечных клеток миометрия [1]. Частота выявления лейомиомы матки зависит от метода диагностики, а «золотым стандартом» считается патоморфологическое исследование. Согласно литературным данным, большая часть случаев лейомиомы матки клинически проявляются в позднем репродуктивном и перименопаузальном периоде, и являются одной из самых частых причиной обращения к гинекологу [2]. Выявленные лейомиомы классифицируются как доброкачественные, однако иногда встречаются варианты лейомиом, при которых однозначно нельзя определить их характер, поскольку их морфологические признаки не противоречат доброкачественным новообразованиям, но они характеризуются злокачественными клиническими проявлениями. Согласно классификации Всемирной организации здравоохранения, эти образования классифицируются, как гладкомышечные опухоли неясного злокачественного потенциала. Именно к таким заболеваниям относят редко встречающуюся метастазирующую лейомиому и интравенозный лейомиоматоз (ИВЛ) [3].
Своевременная диагностика ИВЛ представляет собой огромную проблему, так как примерно у 30% пациентов на ранней стадии нет никаких симптомов и отсутствуют специфические онкомаркеры. В поздних стадиях диагностика затруднена тем, что состояние редко встречается и проявляется многообразием неспецифических симптомов [4, 5].
Целью статьи явилось описание редкого клинического случая пациентки с внетазовой ИВЛ и анализ возможностей различных методов визуализации для диагностики данного заболевания.
Клиническое наблюдение
Пациентка Ч., 1952 г., в анамнезе лапаротомия, надвлагалищная ампутация матки без придатков. Операционный материал не предоставлен. Спустя три года после операции появились жалобы на боли внизу живота, увеличение живота в объеме, одышку, отеки. По данным ультразвукового исследования (УЗИ) по месту жительства – объемное образование малого таза. Выполнена биопсия образования. Консультирована в НМИЦ радиологии. Выполнен пересмотр биопсийного материала в рамках телемедицинской консультации.
 Заключение по морфологическому исследованию: хронический цервицит, фрагменты опухоли, принадлежащей, вероятнее всего, к лейомиоме с отеком стромы узла. Рекомендовано исследование материала в большем объеме.
Заключение по морфологическому исследованию: хронический цервицит, фрагменты опухоли, принадлежащей, вероятнее всего, к лейомиоме с отеком стромы узла. Рекомендовано исследование материала в большем объеме. Представлены данные компьтерной томографии (КТ) органов грудной клетки, брюшной полости и малого таза без контрастного усиления. Визуализировано объемное образование малого таза, расширение нижней полой вены (НПВ), вероятно, за счет прорастания опухоли по ходу ее стенок. Косвенные КТ-признаки синдрома НПВ. Патологии со стороны органов грудной полости в условиях нативного исследования не получено (рис. 1).
На УЗИ сердца выявлено подвижное образование в полости правого предсердия (68×36 мм), стенозирующее транстрикуспидальный поток в фазу желудочковой диастолы, компрессирующее межпредсердную перегородку в фазу желудочковой систолы и, по-видимому, имеющее происхождение из субстрата, обтурирующего НПВ, в супраренальном отделе – более 60% по диаметру. В полости перикарда – до 40 мл экссудата.
Так как у пациентки аллергическая реакция на контрастное вещество в анамнезе, принято решение отказаться от проведения КТ с контрастным усилением. Назначена магнитно-резонансная томография (МРТ) органов брюшной полости и малого таза.
На МРТ органов малого таза с контрастированием (рис. 2) в полости малого таза, в ложе удаленного тела матки, смещая мочевой пузырь и шейку матки влево, определялось объемное опухолевое образование с гетерогенным сигналом на Т2ВИ, неравномерным накоплением контрастного вещества, размерами до 7,9×11,2×7,8 см. Образование прорастало в параметрий, культю шейки матки, плотно прилежало к правой стенке мочевого пузыря и, вероятно, правому яичнику. В просвете НПВ на уровне исследования, распространяясь на общую подвздошную вену справа, а также внутреннюю и наружную (в проксимальном отделе) подвздошные вены справа, визуализировалось опухолевое образование с аналогичными сигнальными характеристиками, местами прорастающее в окружающую клетчатку, расширяющее просвет вен до 1,5–5,0 см.
На МРТ органов брюшной полости с контрастированием (рис. 3) НПВ расширена до 6,2 см в диаметре, просвет субтотально выполнен неоднородным содержимым без достоверных признаков ограничения диффузии, с нижним полюсом изменений в области малого таза, верхним – в правом предсердии.
Таким образом, МР-картина соответствовала опухолевому образованию в ложе удаленного тела матки с вовлечением параметрия, шейки матки. Опухолевая эмболия НПВ, правых общей, наружной и внутренней подвздошных вен.
Поставлен предварительный диагноз: интравенозный леомиоматоз с дифференциальным диагнозом лейомиосаркомы. Повторная биопсия образования была не показана, так как результат не повлиял бы на тактику лечения. Рекомендовано удаление образования культи шейки матки.
Пациентке было проведено хирургическое лечение в объеме стернотомии, лапаротомии, резекции НПВ, тромбэктомии из правого предсердия, удаления рецидивной опухоли в малом тазу с использованием аппарата искусственного кровообращения. Интраоперационно в малом тазу выявлено опухолевое образование размерами до 12 см, умеренно подвижное. НПВ расширена на всем протяжении, максимально до 7 см в
 диаметре. Мобилизована НПВ в инфраренальном отделе, слева – до общей подвздошной вены, справа – до конфлюенса внутренней и наружной правых подвздошных вен. Наибольший опухолевый узел в малом тазу удален. При дальнейшей ревизии выявлено, что опухоль вовлекает внутреннюю подвздошную вену справа с образованием опухолевого тромба. В условиях искусственного кровообращения выполнено продольное рассечение правого предсердия с продлением на НПВ. Из полости правого предсердия извлечена верхушка тромба. Макроскопическое описание: рецидивная опухоль малого таза в виде узла максимальным размером 10 см и резецированная НПВ длиной 26 см, просвет ее расширен до 5 см и обтурирован опухолевым тромбом (рис. 4).
диаметре. Мобилизована НПВ в инфраренальном отделе, слева – до общей подвздошной вены, справа – до конфлюенса внутренней и наружной правых подвздошных вен. Наибольший опухолевый узел в малом тазу удален. При дальнейшей ревизии выявлено, что опухоль вовлекает внутреннюю подвздошную вену справа с образованием опухолевого тромба. В условиях искусственного кровообращения выполнено продольное рассечение правого предсердия с продлением на НПВ. Из полости правого предсердия извлечена верхушка тромба. Макроскопическое описание: рецидивная опухоль малого таза в виде узла максимальным размером 10 см и резецированная НПВ длиной 26 см, просвет ее расширен до 5 см и обтурирован опухолевым тромбом (рис. 4).Микроскопическое описание: мезенхимальная веретеноклеточная опухоль со слабовыраженным полиморфизмом ядер, митозы и некрозы не обнаружены (рис. 5). Морфологическая картина соответствует ИВЛ, ассоциированному с лейомиомой матки.
Пациентка выписана на 17-е сутки в удовлетворительном состоянии.
Обсуждение
ИВЛ – редкая, но важная клиническая ситуация. Ранняя диагностика ИВЛ и своевременное хирургическое вмешательство имеют решающее значение, ведь зачастую интравенозный и внутрисердечный лейомиоматоз вызывают не только сердечные симптомы, в числе которых клинические проявления застойной сердечной недостаточности, но и способны привести к тромбоэмболии легочной артерии и внезапной смерти больного [5, 6].
Случай «метастазирования» доброкачественной опухоли матки в легкое был описан W. Minakowski. Еще в 1901 г. Штейнером был предложен термин «метастазирующая фибромиома матки» [3]. Р. Steiner упоминает также термин «доброкачественная метастазирующая лейомиома», которая характеризуется множественными доброкачественными метастатическими лейомиомами в органах и тканях у пациенток, имеющих
лейомиому матки при отсутствии данных о другом опухолевом процессе [3]. Наблюдение именно ИВЛ было описано в 1896 г., а первый представленный случай с расширением правого предсердия при вскрытии датирован 1907 г. [6]. Внутривенный лейомиоматоз чаще встречается у женщин в пременопаузе, у большинства этих женщин (90%) были роды [7]. Возраст пациенток обычно составляет 20–70 лет, в среднем – 45 лет. Частота встречаемости ИВЛ составляет 0,097% от всех лейомиом. К настоящему времени случаи ИВЛ с внутрисердечным распространением составляют около 10%, а в мировой литературе всего зарегистрировано около 300 случаев [8, 9].
Были предложены две основные теории возникновения внутривенного лейомиоматоза. Согласно теории O.K. Steinmetz и соавт. опухоль распространяется путем инвазии уже существующей лейомиомы матки в просветы венозных сосудов [10]. E. Knauer и соавт. полагают, что ИВЛ может развиваться путем метаплазии гладкомышечных клеток стенок вен матки [11]. Также возможно сочетание двух теорий.
ИВЛ может ограничиваться инвазией в маточные вены или распространяться по всей венозной системе, достигая сердца или легочных артерий. Прогноз у пациентов с внетазовой ИВЛ неблагоприятный. Когда ИВЛ распространяется в НПВ, частота рецидивов увеличивается до 30% [12]. При ограничении ИВЛ полостью таза частота рецидивов составляет 5,4% по данным исследования 166 случаев [13].
Таким образом, ранняя диагностика имеет решающее значение для благоприятного прогноза у пациентов с ИВЛ [14].
P.M. Lam и соавт. описали один из возможных путей распространения в системный венозный кровоток через маточную вену, которая может распространяться на внутренние подвздошные вены, общие подвздошные вены, а затем на НПВ [15].
Другие авторы подтверждают внеорганное распространение клеток миомы через вены широкой связки матки, вагинальные и
яичниковые вены. Около 25% клеток опухолей таким путем могут мигрировать гематогенным путем в бассейн полой вены, в сердце, легкие, тазовые лимфатические узлы [16, 17].
В представленном клиническом случае вероятнее всего имел место путь распространения через маточную, внутренние и общие подвздошные вены в НПВ.
ИВЛ клинически подразделяется на четыре стадии в зависимости от степени распространения опухоли [18]. Стадия I относится к инвазии опухолью стенки маточной вены, которая ограничена тазом. II стадия предполагает инвазию опухоли в брюшную полость без поражения почечной вены. III стадия характеризуется дальнейшим распространением опухоли в правое предсердие без поражения легочной артерии. Стадия IV характеризуется вовлечением опухоли в легочную артерию и/или метастазами в легкие. Это не официальная парадигма стадирования ИВЛ, а предложенная некоторыми авторами иерархия клинических стадий.
 Дифференциальный диагноз ИВЛ преимущественно включает: тромбы в системных венах, доброкачественную метастазирующую лейомиому, лейомиосаркому, возникающую из стенки НПВ, миксому правого предсердия и опухолевый тромбоз при карциноме, поскольку эти образования имеют сходные характеристики КТ или МРТ [19, 20].
Дифференциальный диагноз ИВЛ преимущественно включает: тромбы в системных венах, доброкачественную метастазирующую лейомиому, лейомиосаркому, возникающую из стенки НПВ, миксому правого предсердия и опухолевый тромбоз при карциноме, поскольку эти образования имеют сходные характеристики КТ или МРТ [19, 20].Внутритазовый ИВЛ часто не имеет типичных особенностей при УЗИ и КТ, что затрудняет дифференциальную диагностику с лейомиомой, особенно при небольших интрамуральных поражениях. Поэтому своевременная и точная диагностика ИВЛ I стадии с помощью МРТ особенно важна для достижения благоприятных результатов лечения пациентов.
Характерная картина ИВЛ при МРТ включает в себя наличие крупного образования неправильной формы в матке и параметрии, часто с сопутствующей лейомиомой и поражением широкой связки матки, с изоинтенсивным сигналом на T1ВИ и слабо гиперинтенсивным сигналом на T2ВИ. Также ИВЛ могут быть представлены извитыми плотными образованиями неправильной формы в миометрии или параметрии, с наличием сосудистых структур в толще с множественными внутрисосудистыми дефектами заполнения, которые визуализируются при T2ВИ [21].
Другие исследователи отмечают, что на МР-изображении опухолевое поражение выглядело как растительная губка люффа на корональных изображениях FIESTA, а также как сетчатая и пористая структура на аксиальных изображениях в Т2ВИ [22]. Ряд авторов дает следующие характеристики опухоли при МР-
исследовании: трубчатая структура неоднородного сигнала, с активным накоплением препарата на основе гадоксетовой кислоты [22, 23]. Некоторые авторы описывают ИВЛ как «червеобразную» неоднородную опухоль, достигающую по сосудам камер сердца [23]. Внутри структуры опухоли ИВЛ нередко могут наблюдаться трубчатые структуры, которые отражают расширенные сосуды, что было подтверждено рядом ученых при выполнении операции [23].
Эхокардиография является предпочтительным методом первичной визуализации, использующимся для оценки внутрисердечных поражений. В качестве уточняющих методов проводятся КТ и МРТ, которые способны внести дополнительную информацию о протяженности и характере поражения, а также скорректировать план операционного вмешательства [26].
Пациентам с внетазовым ИВЛ рекомендуется проводить КТ в рамках комплексного
обследования перед операцией с целью определения распространения процесса [27].
В описанном R.J. Fornaris и соавт. наблюдении при КТ грудной клетки и брюшной полости с контрастным усилением визуализировался удлиненный дефект наполнения в правом предсердии и правом желудочке, распространяющийся на НПВ, левую почечную вену и левую гонадную вену за счет образования неоднородной структуры, неравномерно накапливающего контрастное вещество [28].
L. Kang и соавт. также отметили образование неоднородной структуры на постконтрастных сериях при КТ, с меньшей плотностью опухоли по сравнению с контрастным усилением кровотока в НПВ и правом предсердии [22].
Оперативное лечение при выявленной ИВЛ направлено на полную резекцию всей опухоли с доступом наиболее безопасным для пациента, чаще всего с помощью одно- или двухэтапной операции. Если в исходе операции достигается полная резекция, то рецидив возникает крайне редко [27]. У некоторых пациентов при не полностью удаленной внутривенной опухоли может наблюдаться постоянный или отсроченный продолженный рост с частотой рецидивов до 30% [23].
Заключение
Таким образом, методы лучевой диагностики играют важную роль в диагностике и наблюдении пациентов с диагнозом ИВЛ. Дифференциальный диагноз включает сосудистый тромб, а также первичные и метастатические опухоли. Междисциплинарный подход в изучении ИВЛ позволяет разработать необходимый алгоритм инструментальной диагностики столь редкого патологического состояния с целью оптимизации выбора тактики лечения.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Шеберова Елизавета Викторовна – врач-рентгенолог, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии».
E-mail: lisa_iroshnikova@mail.ru; ORCID: 0000-0001-7827-2741
Elizaveta V. Sheberova – Radiologist, Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. E-mail: lisa_iroshnikova@mail.ru;
ORCID: 0000-0001-7827-2741
Рябов Андрей Борисович – д-р мед. наук, зам. ген. директора по хирургии, ФГБУ «НМИЦ радиологии»; руководитель отдела торакоабдоминальной онкохирургии, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-1037-2364
Andrey B. Ryabov – Dr. Sci. (Med.), National Medical Research Radiological Centre, Moscow; Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-1037-2364
Агабабян Татев Артаковна – канд. мед. наук, зав. отд-нием лучевой диагностики, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-9971-3451
Tatev A. Agababyan – Cand. Sci. (Med.), Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-9971-3451
Гриневич Вячеслав Николаевич – канд. мед. наук, зав. отд-нием онкопатологии, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии»; зав. патологоанатомическим отделением МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0003-1908-2256
Vyacheslav N. Grinevich – Cand. Sci. (Med.), Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre; Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID:0000-0003-1908-2256
Афонин Григорий Владиславович – канд. мед. наук, и.о. зав. отд-нием лучевого и хирургического лечения заболеваний торакальной области, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-7128-2397
Grigory V. Afonin – Cand. Sci. (Med.), Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-7128-2397
Колобаев Илья Владимирович – канд. мед. наук, зав. торакоабдоминальным отделением, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0002-3573-6996
Ilya V. Kolobaev – Cand. Sci. (Med.), Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre. ORCID: 0000-0002-3573-6996
Цыгельников Станислав Анатольевич – д-р мед. наук, проф. каф. факультетской хирургии, ФГАОУ ВО «РНИМУ
им. Н.И. Пирогова»; сердечно-сосудистый хирург, МНИОИ
им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии».
AuthorID: 470248
Stanislav A. Tsygelnikov – Dr. Sci. (Med.), Prof., Pirogov Russian National Research Medical University; Cardiovascular Surgeon, Hertsen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre. AuthorID: 470248
Терских Дмитрий Сергеевич – студент 6 курса лечебного факультета, ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет)
Dmitry S. Terskikh – 6th year student, Sechenov First Moscow State Medical University (Sechenov University)
Минаева Наталья Георгиевна – канд. биол. наук, вед. науч. сотр. научно-образовательного отдела, МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0009-0004-9583-6501
Natalia G. Minaeva – Cand. Sci. (Biol.), Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre. ORCID: 0009-0004-9583-6501
Иванов Сергей Анатольевич – чл.-корр. РАН, д-р мед. наук, проф. каф. онкологии и рентгенорадиологии им. В.П. Харченко медицинского института РУДН, директор МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии». ORCID: 0000-0001-7689-6032
Sergey A. Ivanov – Corr. Memb. RAS, Dr. Sci. (Med.), Director of Tsyb Medical Radiological Research Centre – branch of the National Medical Research Radiological Centre, Prof., Patrice Lumumba People’s Friendship University of Russia (RUDN University). ORCID: 0000-0001-7689-6032
Каприн Андрей Дмитриевич – академик РАН, д-р мед. наук, проф., зав. каф. онкологии и рентгенорадиологии им.
В.П. Харченко медицинского института РУДН, дир. МНИОИ
им. П.А. Герцена (филиал ФГБУ «НМИЦ радиологии»), ген. дир. ФГБУ «НМИЦ радиологии». ORCID: 0000-0001-8784-8415
Andrey D. Kaprin – Acad. RAS, Dr. Sci. (Med.), Full Prof., Patrice Lumumba People’s Friendship University of Russia (RUDN University), Director Hertsen Moscow Oncology Research Institute, General Director National Medical Research Radiological Centre. ORCID: 0000-0001-8784-8415
Поступила в редакцию: 03.07.2024
Поступила после рецензирования: 11.07.2024
Принята к публикации: 11.07.2024
Revised: 11.07.2024
Revised: 11.07.2024
Accepted: 11.07.2024
20 августа 2024
Количество просмотров: 315


