Клинический разбор в общей медицине №1 2025
Tatyana M. Parfenova1, Daria A. Nadezhdina1
1 Voyno-Yasenetsky Krasnoyarsk State Medical University, Krasnoyarsk, Russia;
2 Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon, Krasnoyarsk, Russia
aks-n-v@yandex.ru
Abstract
Echinococcosis is a chronic parasitic disease caused by Echinococcus granulosus. Echinococcosis of the heart is a rather rare localization (0,01–3% of all cases of echinococcosis). The difficulty in diagnosing echinococcosis of the heart is that the clinical picture is erased and nonspecific, therefore, as a rule, more than one year passes from the first symptoms to clinical verification. The surgical method is the only effective method for treating intracardiac echinococcosis. The purpose of our work: to present a clinical case of echinococcosis with a rare localization. A clinical case of combined echinococcosis of the liver, lungs, brain with involvement of the heart (right ventricle and right atrium) in a 55-year-old patient with a history of extrapulmonary tuberculosis, destruction of the body of the sternum, resection of the sternum and chondral part of the ribs, postoperative recurrent fistula is presented. The severity of the patient's condition was due to decompensated pulmonary heart of combined genesis (bronchopulmonary and thoracodiaphragmatic forms), as well as direct damage to the right heart by echinococcus.
Key words: disseminated echinococcosis, echinococcosis of the right heart, treatment of echinococcosis.
For citation: Aksyutina N.V., Bolshakova T.Yu., Ibragimova K.T., Kononov E.N., Parfenova T.M., Nadezhdina D.A. Clinical case of multiple echinococcosis involving the right heart. Clinical review for general practice. 2025; 6 (1): 18–23 (In Russ.). DOI: 10.47407/kr2025.6.01.00p450
Эхинококкоз – хроническое паразитарное заболевание, причиной развития которого является Echinococcus granulosus, относящийся к ленточным червям. Промежуточным хозяином является человек, пораженный яйцами гельминта, попавшими в желудочно-кишечный тракт. Через слизистую оболочку кишечника личинки (онкосферы), попадая в систему портального кровообращения, проникают в печень, трансформируются в эхинококковые кисты. Часть же личинок, проходя через печеночный барьер, попадают в правые отделы сердца через нижнюю полую вену, затем через малый круг кровообращения возникает возможность проникновения онкосфер в легкие, где они также формируют кисты. Однако в ряде случаев, не задерживаясь в легких, личинки проникают в левые отделы сердца, затем через большой круг кровообращения они поражают различные органы, в том числе и сердце через коронарный кровоток [1]. Из личинки развивается материнская киста, представляющая собой пузырь, заполненный жидкостью. В случае разрыва материнской кисты могут образоваться вторичные эхинококковые кисты как в просвете материнской, так и за ее пределами [2, 3].
Учитывая маршрут движения личинки по кровеносному руслу человека, закономерно, что наиболее частая локализация эхинококковых кист в печени (70–85%), реже – в легких (15–35%), очень редко – в других зонах. Эхинококкоз сердца – довольно редкая локализация (0,01–3% от всех случаев эхинококкоза) [2, 4–6]. По данным литературы, поражение левого желудочка сердца наблюдается в 2–3 раза чаще правого, а предсердий – в 5 раз реже желудочков [1, 4, 7]. Изолированное первичное поражение перикарда встречается редко [8–10]. Чаще эхинококкоз сердца и перикарда сочетается с поражением эхинококком других органов [2, 3, 8–10]. В силу особенностей строения сердечной мышцы и ее функции материнская киста, не достигнув больших размеров, погибает, что сопровождается появлением дочерних пузырей. Даже при наличии небольших эхинококковых кист стенки сердца могут истончаться с формированием аневризматических образований. Около 75% летальных исходов возникает из-за разрыва кисты, септического шока, эмболических осложнений [11–16].
 Сложность в диагностике эхинококкоза сердца заключается в том, что клиническая картина достаточно стертая и неспецифичная, поэтому от первых симптомов до клинической верификации, как правило, проходит не один год. В литературе описаны случаи успешного хирургического лечения эхинококкоза сердца и перикарда благодаря внедрению в практическую медицину новых, высокоинформативных методов диагностики заболеваний сердца, таких как магнитно-резонансная томография (МРТ), компьютерная томография (КТ) с контрастированием, чреспищеводная и внутрисердечная эхокардиография (ЭхоКГ). Однако даже эти методы исследования не способны выявить мелкие отсевы эхинококка.
Сложность в диагностике эхинококкоза сердца заключается в том, что клиническая картина достаточно стертая и неспецифичная, поэтому от первых симптомов до клинической верификации, как правило, проходит не один год. В литературе описаны случаи успешного хирургического лечения эхинококкоза сердца и перикарда благодаря внедрению в практическую медицину новых, высокоинформативных методов диагностики заболеваний сердца, таких как магнитно-резонансная томография (МРТ), компьютерная томография (КТ) с контрастированием, чреспищеводная и внутрисердечная эхокардиография (ЭхоКГ). Однако даже эти методы исследования не способны выявить мелкие отсевы эхинококка.
Особенность лечения пациентов с эхинококкозом сердца заключается в том, что химиотерапия препаратами-гермицидами является смертельно опасной, так как приводит к гибели паразитов с деструкцией стенок кист с последующим их разрывом [15, 17], поэтому хирургический метод является единственным эффективным методом лечения внутрисердечного эхинококкоза. Окончательно не решен вопрос о тактике лечения при сочетании внутрисердечного и эхинококкоза других органов, хотя при этом оперативное лечение с рациональной химиотерапией дает хорошие результаты [18, 19]. Однако у каждого третьего пациента после операции имеет место рецидив заболевания, а после повторных операций – у каждого второго [20]. Так, например, С.И. Жуковым и соавт. был описан рецидив успешного хирургичского лечения эхинококкоза в области верхушки и передней стенки правого желудочка спустя 24 года после первичного хирургического лечения и длительной противогельминтной терапии [1].
Ю.Л. Шевченко и соавт. описали ряд случаев хирургического лечения эхинококкоза сердца в сочетании с поражением печени, легких и головного мозга у молодых пациентов без их дальнейшего наблюдения [21]. Цель нашей работы: представить и обсудить редкий случай сочетанного эхинококкоза печени, легких, головного мозга с вовлечением в процесс сердца (правого желудочка и правого предсердия).
В отделении торакальной хирургии находилась на лечении пациентка К., 55 лет, инвалид II группы, по профессии геолог.
Со слов пациентки и анализе предоставленных выписных эпикризов предыдущих госпитализаций в 2008 г. у нее была диагностирована внелегочная форма туберкулеза с локализацией в рукоятке грудины и ее деструкцией, по поводу чего получала специфическую терапию до 2011 г. В 2009 г. при контрольном обследовании выявлено округлое образование правой доли печени. Была выполнена гемигепатэктомия. При гистологическом исследовании обнаружен многокамерный эхинококк. Пациентке назначен пожизненный прием албендазола. Послеоперационный период осложнился эмпиемой плевры справа, выполнялось дренирование правой плевральной полости. При контрольном рентгенологическом исследовании легких выявлены множественные очаговые образования, которые расценивались как проявления туберкулеза легких. С 2011 г. у пациентки появились эпизоды головокружения. При МРТ выявлено новообразование правого полушария мозжечка, в связи с чем выполнена трепанация черепа и удаление образования эхинококкового генеза. В это же время открылся свищ с гнойным отделяемым в области грудины. При рентгенологическом исследовании – субтотальная деструкция тела грудины и хрящевых отрезков ребер справа. Неоднократно выполнялись фистулотомии со вскрытием абсцессов и дренированием грудины, а в 2012 г. была проведена резекция грудины, хондральной части ребер справа (II, IV, V), фистулотомия. Гистологически выявлено туберкулезное воспаление. Иммуноферментный анализ с эхинококковым антигеном положительный. С этого времени ежегодно рецидивировали абсцессы в области грудины с формированием свища. Выполнялись некрэктомии, фистулэктомии. За этот период при неоднократном исследовании мокроты и смывов бронхов микобактерии туберкулеза (МКТ) не выявлялись. Серологические реакции на туберкулез, ПЦР мокроты на МКТ отрицательные. Пациентка регулярно принимала албендазол.
Очередная госпитализация в хирургическое отделение в октябре 2022 г. Поступила с жалобами на боли в области грудной клетки, одышку в покое, отеки голеней, снижение массы тела. Ухудшение состояния прогрессировало в течение последних 6 мес, а около двух месяцев до поступления вновь открылся свищ в средней трети грудины.
При поступлении в отделение состояние пациентки тяжелое. Телосложение астеническое, пониженной массы тела (индекс массы тела 15,6 кг/м2). Кожные покровы бледные, цианоз носогубного треугольника. Грудная клетка деформирована вследствие удаленной грудины, выраженного кифоза грудного отдела позвоночника. Положение вынужденное, с опорой на локти, с участием в дыхании мышц плечевого пояса. На передней поверхности грудной клетки послеоперационный рубец 12,0×0,3 см, в средней трети – свищ 0,4 см. В легких дыхание жесткое, ослаблено в нижних отделах. Частота дыхательных движений – 24 в 1 мин. Сердечные тоны ритмичные, приглушены, частота сердечных сокращений (ЧСС) – 88 в 1 мин. Артериальное давление – 110/80 мм рт. ст. Живот мягкий, безболезненный. Печень на 2 см выступает из-под края реберной дуги, умеренно болезненная. Отеки нижней трети голеней.
За период нахождения в стационаре в развернутом анализе крови выявлены изменения: ускорение СОЭ до 45–54 мм/ч, умеренная лейкопения (5,4–3,7×109/л), тромбоцитопения (141–204×109/л), гипохромная анемия с уровнем гемоглобина 88–102 г/л. Биохимические показатели крови (билирубин и его фракции, глюкоза, креатинин, общий белок и белковые фракции, К+, Na+) в пределах нормальных значений.
Рентгенография органов грудной клетки: Мягкие ткани не изменены. Тело грудины не визуализируется. Определяется снижение пневматизации средней доли правого легкого, язычковых сегментов левого и нижних долей с обеих сторон. Корни не структурны, расширены. Уплотнена плевра по косой и горизонтальной междолевым щелям справа. В левом синусе не исключается наличие жидкости. Диафрагма расположена обычно. Контуры сердца не визуализируются.
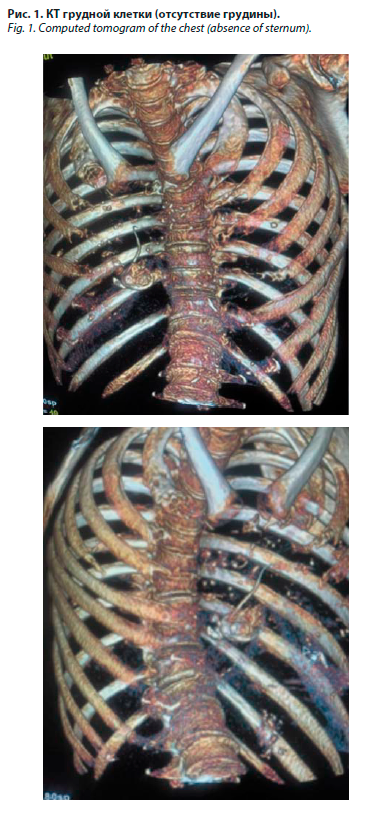
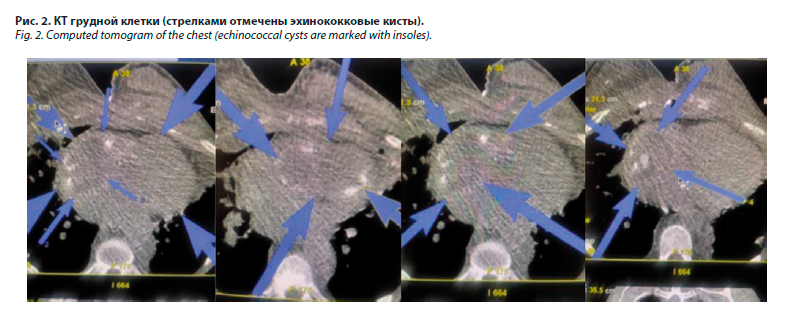
КТ грудной клетки: в связи с вынужденным положением пациентки исследование проводилось на правом боку; грудина отсутствует (рис. 1). При КТ-фистулографии по катетеру выполнена лежащая прекардиально полость неправильной формы размерами около 4–5 см (содержит контраст и воздух). По обоим легочным полям множественные участки пневмосклероза и, вероятно, кальцинировавшиеся паразитарные кисты. Одна из них в S6 справа содержит небольшое количество воздуха. В средостении и полости перикарда также множественные гетерогенные участки кальциноза, вероятнее всего посттуберкулезной этиологии. Несмотря на невысокое качество изображения КТ грудной клетки (вынужденное положение на боку, артефакты от рук), при более детальном рассмотрении в правых отделах сердца визуализировались изменения (плюс-ткань), которые можно интерпретировать как эхинококковые кисты (рис. 2).
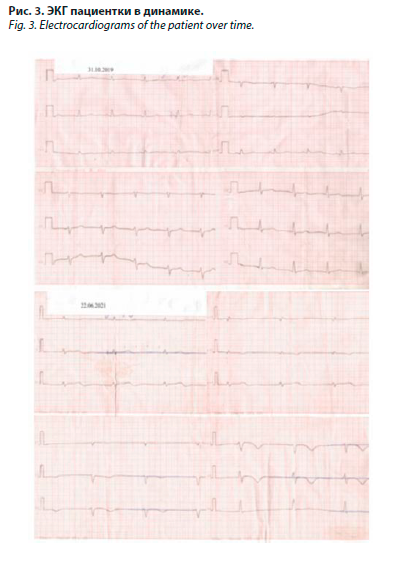
На электрокардиографии (ЭКГ) при поступлении (октябрь 2022 г.) синусовый ритм с ЧСС 75 уд/мин, rS с V1 по V4, (-) зубцы Т с V1 по V5. При ретроспективном анализе ЭКГ от октября 2019 г. выявлена синусовая тахикардия с ЧСС 108 уд/мин, нормальный прирост зубцов R и (+) зубцы Т во всех грудных отведениях. На ЭКГ от 22.06.2021 регистрировался а-в узловой ритм с ЧСС
67 уд/мин, появились (-) зубцы Т в грудных отведениях (рис. 3).
 По ЭхоКГ: левые отделы сердца не увеличены (левое предсердие – 3,5 см, конечно-диастолический размер – 5,1 см, конечный систолический размер – 3,6 см). Снижение глобальной сократимости миокарда левого желудочка (фракция выброса по Simpson 45%). Межжелудочковая перегородка и задняя стенка левого желудочка 1,0 см. Движение межжелудочковой перегородки парадоксальное. Выявлены зоны гипокинезии и акинезии в верхушечной части левого желудочка, переднеперегородочной и перегородочной области. Отмечалась дилатация правого предсердия (4,5–5,1 см), правого желудочка (3,0 см). Градиент давления на трикуспидальном клапане 50 мм рт. ст. Регургитация на трикуспидальном клапане II ст. Систолическое давление в легочной артерии – 65 мм рт. ст. Нижняя полая вена – 2,6 см (расширена), коллабирует слабо. В перикарде наличие свободного эхо-пространства в области задней стенки левого желудочка (13 мм), в области верхушки (12 мм), передней стенки правого желудочка и правого предсердия до 6 мм. В плевральной полости слева наличие свободного эхо-пространства до 4,5 см. Уплотнение аорты, створок аортального клапана с пристворчатой регургитацией. Митральная регургитация I ст.
По ЭхоКГ: левые отделы сердца не увеличены (левое предсердие – 3,5 см, конечно-диастолический размер – 5,1 см, конечный систолический размер – 3,6 см). Снижение глобальной сократимости миокарда левого желудочка (фракция выброса по Simpson 45%). Межжелудочковая перегородка и задняя стенка левого желудочка 1,0 см. Движение межжелудочковой перегородки парадоксальное. Выявлены зоны гипокинезии и акинезии в верхушечной части левого желудочка, переднеперегородочной и перегородочной области. Отмечалась дилатация правого предсердия (4,5–5,1 см), правого желудочка (3,0 см). Градиент давления на трикуспидальном клапане 50 мм рт. ст. Регургитация на трикуспидальном клапане II ст. Систолическое давление в легочной артерии – 65 мм рт. ст. Нижняя полая вена – 2,6 см (расширена), коллабирует слабо. В перикарде наличие свободного эхо-пространства в области задней стенки левого желудочка (13 мм), в области верхушки (12 мм), передней стенки правого желудочка и правого предсердия до 6 мм. В плевральной полости слева наличие свободного эхо-пространства до 4,5 см. Уплотнение аорты, створок аортального клапана с пристворчатой регургитацией. Митральная регургитация I ст.
Исследование функции внешнего дыхания: жизненная емкость легких (ЖЕЛ) – 28% д. ж.; объем форсированного выдоха за 1-ую секунду (ОФВ1) – 25% д. ж.; ОФВ1/форсированная ЖЕЛ (ФЖЕЛ) – 0,6; ОФВ1 после пробы с бронхолитиком – 29% д. ж. Заключение: резкое снижение ЖЕЛ. Нарушение функции вентиляции по обструктивному типу резкое. Проба с бронхолитиком отрицательная. Прирост ОФВ1 после пробы с бронхолитиком на 1,6%.
На 12-й день нахождения в стационаре пациентке выполнено оперативное вмешательство: вскрытие полости абсцесса размером 5×4×4 см, расположенного в переднем средостении, удалены секвестры хрящевой ткани, полость абсцесса санирована. В послеоперационном периоде рана очистилась, наблюдалась грануляция.
За время пребывания в стационаре пациентке проводилась антибактериальная терапия (Цефазолин), дезинтоксикационная терапия (Дисоль), получала растворы для энтерального и парентерального питания (Фрезубин, Альбумин), нестероидные противовоспалительные препараты (Кетопрофен). По поводу сердечной недостаточности были назначены ингибитор ангиотензинпревращающего фермента (Периндоприл), β-адреноблокатор (Карведилол), антагонист минералокортикоидных рецепторов (Верошпирон), блокатор натрий-глюкозного ко-транспортера 2-го типа (Дапаглифлозин), диуретики (Фуросемид, Торасемид), сердечные гликозиды (Дигоксин), препараты калия (Панангин). Продолжала прием противопротозойной терапии (Альбендозол 600 мг/сут).
Несмотря на проводимую терапию, у пациентки сохранялась одышка в покое, тахикардия, отеки стоп и голеней. На 40-й день госпитализации произошла остановка дыхания и сердечной деятельности. Реанимационные мероприятия оказались не эффективными.
При патолого-анатомическом вскрытии в области затылочной кости черепа закрытое фрезевое отверстие, твердая оболочка головного мозга сращена с краями фрезевого отверстия. При осмотре грудной клетки в проекции средней трети грудины справа виден свищевой ход, проникающий в грудную полость. Грудина и часть ребер справа резецированы. Сердце, сердечная сорочка сращены с грудной стенкой. В плевральных полостях по 150–250 мл жидкости. Полость перикарда облитерирована, листки перикарда утолщены, белесоватого цвета. Сердце увеличено за счет правых отделов (12,5×12,5×8 см). В области боковой стенки правого желудочка и правого предсердия разрастание в виде цветной капусты, распространяющееся на органы переднего средостения, охватывающие ствол легочной артерии, восходящий отдел дуги аорты с их сдавлением. Миокард дряблой консистенции, волокнистого строения, серовато-красный, с мелкими рассеянными белесоватыми рубчиками, неравномерного кровенаполнения. Толщина стенки левого желудочка 1,2–1,3 см.
В толще стенки правого желудочка и правого предсердия определяется полостное образование овальной формы 7,5×6,0×7,0 см с плотной стенкой, представленной волокнистой белесоватой тканью толщиной 2,5–3,0 см. Выстилка полостного образования гладкая.
В просвете полости выявлены замазкообразные гноевидные массы серо-желтого цвета. Полости правого предсердия и правого желудочка резко сужены за счет выбухания образования вовнутрь. Эндокард и клапанный аппарат не изменены, коронарные артерии интактны. Легочный ствол и обе легочные артерии содержат посмертные свертки крови. Легочная ткань на разрезе застойная, темно-красного цвета, влажная. В S6 и S3 справа определяются образования до 3,0 см в диаметре, представленные на разрезе плотной пористой белесоватой тканью. В просвете трахеи и бронхов в большом количестве пенистая розовая мокрота. На передней брюшной стенке по средней линии живота старый послеоперационный рубец. В брюшной полости расположение органов правильное. Листки брюшины гладкие, блестящие, в верхнем этаже массивные спайки в области печени. В брюшной полости наличие свободной жидкости 2,5 л. При осмотре органов пищеварения обращает на себя внимание деформированная печень, спаянная с диафрагмой, в размерах уменьшена (18,0×12,0×10,0 см). Селезенка увеличена (14,0×8,0×4,0 см).
При гистологическом исследовании стенка полостного образования, выявленного в сердце, представлена плотной соединительной тканью, в которой определяются очаговые скопления лимфоидных, эпителиоидных клеток и фибробластов, а также малочисленных гигантских многоядерных клеток наподобие клеток инородных тел, множественные очаги дистрофического обызвествления капсулы. С внутренней стороны капсулы определяются характерные сколексы, окруженные бесструктурными и некротическими массами. В окружающей ткани миокарда участки отека стромы и полнокровия сосудов с инфильтрацией полиморфно-ядерными лейкоцитами, лимфоцитами, макрофагами, плазматическими клетками. Во всех органах признаки острого венозного полнокровия.
Причиной столь массивной диссеминации эхинококковым процессом внутренних органов, несмотря на проводимую противопротозойную терапиию, может быть ятрогения из-за нарушения техники выполнения эхинококкэктомии, в результате чего происходит интраоперационная имплантация сколексов [21, 22]. Другой наиболее частой причиной диссеминации является самопроизвольный разрыв эхинококковых кист печени и легких с попаданием сколексов в кровоток с последующим распространением их в другие органы [23, 24]. У представленной пациентки мог быть как спонтанный, так и ятрогенный во время гемигепатэктомии разрыв кисты печени с последующей диссеминацией эхинококка в легкие, головной мозг и сердце. Особенностью данного случая является изолированное поражение правого желудочка и предсердия, без вовлечения левых отделов сердца. В стенке правого желудочка и правого предсердия имело место крупное полостное образование до 7,5 см в диаметре с характерными сколексами.
У пациентки поражение эхинококком правых отделов сердца наслоилось на хроническое легочное сердце смешанной этиологии (поражение легких в сочетании с деформацией грудной клетки). Это способствовало прогрессированию явлений сердечной недостаточности, что явилось причиной смерти больной.
При эхинококкозе сердца возможно оперативное лечение. В основном выполняют энуклеацию хитиновой оболочки с сохранением фиброзной капсулы с последующей обработкой антисептическим раствором, что позволяет снизить риск рецидива эхинококкоза.
В случае больших кист вариантом лечения является метод «пункция-аспирация-инъекция-повторная аспирация» (PAIR) [1, 4, 22]. В литературе описаны случаи успешного хирургического лечения эхинококкоза сердца при своевременной диагностике. Однако при множественном поражении миокарда очень высок риск повреждения важных структур сердца с развитием массивного кровотечения. В описанном нами клиническом случае отмечался диссеминированный процесс с поражением печени, легких, головного мозга, сердца, причем эхинококкоз сердца был заподозрен на поздней стадии заболевания. Хирургическое лечение данной пациентки было невозможно в связи с тяжестью состояния, обусловленного декомпенсированным легочным сердцем сочетанного генеза: торакодиафрагмального (деформация грудной клетки в виде выраженного грудного кифоза в результате резекции грудины, хондральной части ребер), бронхолегочного (в легких множественные участки пневмосклероза, кальцифицировавшиеся паразитарные кисты), васкулярного генеза (сдавление ствола легочной артерии множественными эхинококковыми кистами) в сочетании с эхинококковым поражением миокарда правых камер сердца.
Данный клинический случай интересен тем, что, несмотря на непрерывную терапию албендазолом, процесс принял диссеминированный характер с редкой локализацией эхинококковых кист в правых отделах сердца с распространением на органы переднего средостения, ствол легочной артерии, восходящий отдел дуги аорты с их сдавлением. От момента диагностики первичного эхинококкоза в печени и начала лечения пациентка прожила 12 лет.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare no conflict of interest.
Информация об авторах
Information about the authors
Аксютина Наталья Валерьевна – д-р мед. наук, доц., проф. каф. факультетской терапии ФГБОУ ВО «КрасГМУ им. проф.
В.Ф. Войно-Яснецкого», врач-кардиолог КГБУЗ «КМКБ №20 им. И.С. Берзона». E-mail: aks-n-v@yandex.ru; ОRCID: 0000-0002-4856-2729
Natalya V. Aksyutina – Dr. Sci. (Med.), Full Prof., Voyno-Yasenetsky Krasnoyarsk State Medical University, cardiologist, Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon. E-mail: aks-n-v@yandex.ru; ORCID: 0000-0002-4856-2729
Большакова Татьяна Юрьевна – канд. мед. наук., доц. каф. факультетской терапии ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого». ОRCID: 0000-0001-9653-6026
Tatyana Yu. Bolshakova – Cand. Sci. (Med.), Voyno-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0001-9653-6026
Ибрагимова Клара Талгатбековна – врач-терапевт, КГБУЗ «КМКБ №20 им. И.С. Берзона»
Klara T. Ibragimova – Therapist, Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon.
Кононов Евгений Николаевич – врач-кардиолог, зам. главного врача по клинико-экспертной работе, КГБУЗ «КМКБ №20 им. И.С. Берзона»
Evgeny N. Kononov – Cardiologist, Deputy Chief Physician for Clinical and Expert Work, Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon
Парфенова Татьяна Михайловна – канд. мед. наук., доц., доц. каф. факультетской терапии, ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0002-1140-6722
Tatyana M. Parfenova – Cand. Sci. (Med.), Voyno-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0002-1140-6722
Надеждина Дарья Аркадьевна – клин. ординатор каф. физической и реабилитационной медицины с курсом ПО, ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого»
Daria A. Nadezhdina – Clinical Resident, Voyno-Yasenetsky Krasnoyarsk State Medical University
Поступила в редакцию: 05.12.2024
Поступила после рецензирования: 26.12.2024
Принята к публикации: 16.01.2025
Received: 05.12.2024
Revised: 26.12.2024
Accepted: 16.01.2025
Клинический разбор в общей медицине №1 2025
Клинический случай множественного эхинококкоза с вовлечением в процесс правых отделов сердца
Номера страниц в выпуске:18-23
Аннотация
Эхинококкоз – хроническое паразитарное заболевание, причиной развития которого является Echinococcus granulosus. Эхинококкоз сердца – довольно редкая локализация (0,01–3% от всех случаев эхинококкоза). Сложность в диагностике эхинококкоза сердца заключается в том, что клиническая картина является стертой и неспецифичной, поэтому от первых симптомов до клинической верификации, как правило, проходит не один год. Хирургический метод является единственным эффективным методом лечения внутрисердечного эхинококкоза. Цель нашей работы: представить клинический случай эхинококкоза с редкой локализацией. Приведен клинический случай сочетанного эхинококкоза печени, легких, головного мозга с вовлечением в процесс сердца (правого желудочка и правого предсердия) у пациентки 55 лет, имеющей в анамнезе внелегочную форму туберкулеза, деструкцию тела грудины, резекцию грудины и хондральной части ребер, послеоперационный рецидивирующий свищ. Тяжесть состояния больной была обусловлена декомпенсированным легочным сердцем сочетанного генеза (бронхолегочная, торакодиафрагмальная и васкулярная формы), а также непосредственным поражением эхинококком правых отделов сердца.
Ключевые слова: диссеминированный эхинококкоз, эхинококкоз правых отделов сердца, лечение эхинококкоза.
Для цитирования: Аксютина Н.В., Большакова Т.Ю., Ибрагимова К.Т., Кононов Е.Н., Парфенова Т.М., Надеждина Д.А. Клинический случай множественного эхинококкоза с вовлечением в процесс правых отделов сердца. Клинический разбор в общей медицине. 2025; 6 (1): 18–23. DOI: 10.47407/kr2025.6.01.00p450
Эхинококкоз – хроническое паразитарное заболевание, причиной развития которого является Echinococcus granulosus. Эхинококкоз сердца – довольно редкая локализация (0,01–3% от всех случаев эхинококкоза). Сложность в диагностике эхинококкоза сердца заключается в том, что клиническая картина является стертой и неспецифичной, поэтому от первых симптомов до клинической верификации, как правило, проходит не один год. Хирургический метод является единственным эффективным методом лечения внутрисердечного эхинококкоза. Цель нашей работы: представить клинический случай эхинококкоза с редкой локализацией. Приведен клинический случай сочетанного эхинококкоза печени, легких, головного мозга с вовлечением в процесс сердца (правого желудочка и правого предсердия) у пациентки 55 лет, имеющей в анамнезе внелегочную форму туберкулеза, деструкцию тела грудины, резекцию грудины и хондральной части ребер, послеоперационный рецидивирующий свищ. Тяжесть состояния больной была обусловлена декомпенсированным легочным сердцем сочетанного генеза (бронхолегочная, торакодиафрагмальная и васкулярная формы), а также непосредственным поражением эхинококком правых отделов сердца.
Ключевые слова: диссеминированный эхинококкоз, эхинококкоз правых отделов сердца, лечение эхинококкоза.
Для цитирования: Аксютина Н.В., Большакова Т.Ю., Ибрагимова К.Т., Кононов Е.Н., Парфенова Т.М., Надеждина Д.А. Клинический случай множественного эхинококкоза с вовлечением в процесс правых отделов сердца. Клинический разбор в общей медицине. 2025; 6 (1): 18–23. DOI: 10.47407/kr2025.6.01.00p450
Clinical case of multiple echinococcosis involving the right heart
Natalya V. Aksyutina1,2, Tatyana Yu. Bolshakova1, Klara T. Ibragimova2, Evgeny N. Kononov2,Tatyana M. Parfenova1, Daria A. Nadezhdina1
1 Voyno-Yasenetsky Krasnoyarsk State Medical University, Krasnoyarsk, Russia;
2 Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon, Krasnoyarsk, Russia
aks-n-v@yandex.ru
Abstract
Echinococcosis is a chronic parasitic disease caused by Echinococcus granulosus. Echinococcosis of the heart is a rather rare localization (0,01–3% of all cases of echinococcosis). The difficulty in diagnosing echinococcosis of the heart is that the clinical picture is erased and nonspecific, therefore, as a rule, more than one year passes from the first symptoms to clinical verification. The surgical method is the only effective method for treating intracardiac echinococcosis. The purpose of our work: to present a clinical case of echinococcosis with a rare localization. A clinical case of combined echinococcosis of the liver, lungs, brain with involvement of the heart (right ventricle and right atrium) in a 55-year-old patient with a history of extrapulmonary tuberculosis, destruction of the body of the sternum, resection of the sternum and chondral part of the ribs, postoperative recurrent fistula is presented. The severity of the patient's condition was due to decompensated pulmonary heart of combined genesis (bronchopulmonary and thoracodiaphragmatic forms), as well as direct damage to the right heart by echinococcus.
Key words: disseminated echinococcosis, echinococcosis of the right heart, treatment of echinococcosis.
For citation: Aksyutina N.V., Bolshakova T.Yu., Ibragimova K.T., Kononov E.N., Parfenova T.M., Nadezhdina D.A. Clinical case of multiple echinococcosis involving the right heart. Clinical review for general practice. 2025; 6 (1): 18–23 (In Russ.). DOI: 10.47407/kr2025.6.01.00p450
Эхинококкоз – хроническое паразитарное заболевание, причиной развития которого является Echinococcus granulosus, относящийся к ленточным червям. Промежуточным хозяином является человек, пораженный яйцами гельминта, попавшими в желудочно-кишечный тракт. Через слизистую оболочку кишечника личинки (онкосферы), попадая в систему портального кровообращения, проникают в печень, трансформируются в эхинококковые кисты. Часть же личинок, проходя через печеночный барьер, попадают в правые отделы сердца через нижнюю полую вену, затем через малый круг кровообращения возникает возможность проникновения онкосфер в легкие, где они также формируют кисты. Однако в ряде случаев, не задерживаясь в легких, личинки проникают в левые отделы сердца, затем через большой круг кровообращения они поражают различные органы, в том числе и сердце через коронарный кровоток [1]. Из личинки развивается материнская киста, представляющая собой пузырь, заполненный жидкостью. В случае разрыва материнской кисты могут образоваться вторичные эхинококковые кисты как в просвете материнской, так и за ее пределами [2, 3].
Учитывая маршрут движения личинки по кровеносному руслу человека, закономерно, что наиболее частая локализация эхинококковых кист в печени (70–85%), реже – в легких (15–35%), очень редко – в других зонах. Эхинококкоз сердца – довольно редкая локализация (0,01–3% от всех случаев эхинококкоза) [2, 4–6]. По данным литературы, поражение левого желудочка сердца наблюдается в 2–3 раза чаще правого, а предсердий – в 5 раз реже желудочков [1, 4, 7]. Изолированное первичное поражение перикарда встречается редко [8–10]. Чаще эхинококкоз сердца и перикарда сочетается с поражением эхинококком других органов [2, 3, 8–10]. В силу особенностей строения сердечной мышцы и ее функции материнская киста, не достигнув больших размеров, погибает, что сопровождается появлением дочерних пузырей. Даже при наличии небольших эхинококковых кист стенки сердца могут истончаться с формированием аневризматических образований. Около 75% летальных исходов возникает из-за разрыва кисты, септического шока, эмболических осложнений [11–16].
 Сложность в диагностике эхинококкоза сердца заключается в том, что клиническая картина достаточно стертая и неспецифичная, поэтому от первых симптомов до клинической верификации, как правило, проходит не один год. В литературе описаны случаи успешного хирургического лечения эхинококкоза сердца и перикарда благодаря внедрению в практическую медицину новых, высокоинформативных методов диагностики заболеваний сердца, таких как магнитно-резонансная томография (МРТ), компьютерная томография (КТ) с контрастированием, чреспищеводная и внутрисердечная эхокардиография (ЭхоКГ). Однако даже эти методы исследования не способны выявить мелкие отсевы эхинококка.
Сложность в диагностике эхинококкоза сердца заключается в том, что клиническая картина достаточно стертая и неспецифичная, поэтому от первых симптомов до клинической верификации, как правило, проходит не один год. В литературе описаны случаи успешного хирургического лечения эхинококкоза сердца и перикарда благодаря внедрению в практическую медицину новых, высокоинформативных методов диагностики заболеваний сердца, таких как магнитно-резонансная томография (МРТ), компьютерная томография (КТ) с контрастированием, чреспищеводная и внутрисердечная эхокардиография (ЭхоКГ). Однако даже эти методы исследования не способны выявить мелкие отсевы эхинококка. Особенность лечения пациентов с эхинококкозом сердца заключается в том, что химиотерапия препаратами-гермицидами является смертельно опасной, так как приводит к гибели паразитов с деструкцией стенок кист с последующим их разрывом [15, 17], поэтому хирургический метод является единственным эффективным методом лечения внутрисердечного эхинококкоза. Окончательно не решен вопрос о тактике лечения при сочетании внутрисердечного и эхинококкоза других органов, хотя при этом оперативное лечение с рациональной химиотерапией дает хорошие результаты [18, 19]. Однако у каждого третьего пациента после операции имеет место рецидив заболевания, а после повторных операций – у каждого второго [20]. Так, например, С.И. Жуковым и соавт. был описан рецидив успешного хирургичского лечения эхинококкоза в области верхушки и передней стенки правого желудочка спустя 24 года после первичного хирургического лечения и длительной противогельминтной терапии [1].
Ю.Л. Шевченко и соавт. описали ряд случаев хирургического лечения эхинококкоза сердца в сочетании с поражением печени, легких и головного мозга у молодых пациентов без их дальнейшего наблюдения [21]. Цель нашей работы: представить и обсудить редкий случай сочетанного эхинококкоза печени, легких, головного мозга с вовлечением в процесс сердца (правого желудочка и правого предсердия).
В отделении торакальной хирургии находилась на лечении пациентка К., 55 лет, инвалид II группы, по профессии геолог.
Со слов пациентки и анализе предоставленных выписных эпикризов предыдущих госпитализаций в 2008 г. у нее была диагностирована внелегочная форма туберкулеза с локализацией в рукоятке грудины и ее деструкцией, по поводу чего получала специфическую терапию до 2011 г. В 2009 г. при контрольном обследовании выявлено округлое образование правой доли печени. Была выполнена гемигепатэктомия. При гистологическом исследовании обнаружен многокамерный эхинококк. Пациентке назначен пожизненный прием албендазола. Послеоперационный период осложнился эмпиемой плевры справа, выполнялось дренирование правой плевральной полости. При контрольном рентгенологическом исследовании легких выявлены множественные очаговые образования, которые расценивались как проявления туберкулеза легких. С 2011 г. у пациентки появились эпизоды головокружения. При МРТ выявлено новообразование правого полушария мозжечка, в связи с чем выполнена трепанация черепа и удаление образования эхинококкового генеза. В это же время открылся свищ с гнойным отделяемым в области грудины. При рентгенологическом исследовании – субтотальная деструкция тела грудины и хрящевых отрезков ребер справа. Неоднократно выполнялись фистулотомии со вскрытием абсцессов и дренированием грудины, а в 2012 г. была проведена резекция грудины, хондральной части ребер справа (II, IV, V), фистулотомия. Гистологически выявлено туберкулезное воспаление. Иммуноферментный анализ с эхинококковым антигеном положительный. С этого времени ежегодно рецидивировали абсцессы в области грудины с формированием свища. Выполнялись некрэктомии, фистулэктомии. За этот период при неоднократном исследовании мокроты и смывов бронхов микобактерии туберкулеза (МКТ) не выявлялись. Серологические реакции на туберкулез, ПЦР мокроты на МКТ отрицательные. Пациентка регулярно принимала албендазол.
Очередная госпитализация в хирургическое отделение в октябре 2022 г. Поступила с жалобами на боли в области грудной клетки, одышку в покое, отеки голеней, снижение массы тела. Ухудшение состояния прогрессировало в течение последних 6 мес, а около двух месяцев до поступления вновь открылся свищ в средней трети грудины.
При поступлении в отделение состояние пациентки тяжелое. Телосложение астеническое, пониженной массы тела (индекс массы тела 15,6 кг/м2). Кожные покровы бледные, цианоз носогубного треугольника. Грудная клетка деформирована вследствие удаленной грудины, выраженного кифоза грудного отдела позвоночника. Положение вынужденное, с опорой на локти, с участием в дыхании мышц плечевого пояса. На передней поверхности грудной клетки послеоперационный рубец 12,0×0,3 см, в средней трети – свищ 0,4 см. В легких дыхание жесткое, ослаблено в нижних отделах. Частота дыхательных движений – 24 в 1 мин. Сердечные тоны ритмичные, приглушены, частота сердечных сокращений (ЧСС) – 88 в 1 мин. Артериальное давление – 110/80 мм рт. ст. Живот мягкий, безболезненный. Печень на 2 см выступает из-под края реберной дуги, умеренно болезненная. Отеки нижней трети голеней.
За период нахождения в стационаре в развернутом анализе крови выявлены изменения: ускорение СОЭ до 45–54 мм/ч, умеренная лейкопения (5,4–3,7×109/л), тромбоцитопения (141–204×109/л), гипохромная анемия с уровнем гемоглобина 88–102 г/л. Биохимические показатели крови (билирубин и его фракции, глюкоза, креатинин, общий белок и белковые фракции, К+, Na+) в пределах нормальных значений.
Рентгенография органов грудной клетки: Мягкие ткани не изменены. Тело грудины не визуализируется. Определяется снижение пневматизации средней доли правого легкого, язычковых сегментов левого и нижних долей с обеих сторон. Корни не структурны, расширены. Уплотнена плевра по косой и горизонтальной междолевым щелям справа. В левом синусе не исключается наличие жидкости. Диафрагма расположена обычно. Контуры сердца не визуализируются.
КТ грудной клетки: в связи с вынужденным положением пациентки исследование проводилось на правом боку; грудина отсутствует (рис. 1). При КТ-фистулографии по катетеру выполнена лежащая прекардиально полость неправильной формы размерами около 4–5 см (содержит контраст и воздух). По обоим легочным полям множественные участки пневмосклероза и, вероятно, кальцинировавшиеся паразитарные кисты. Одна из них в S6 справа содержит небольшое количество воздуха. В средостении и полости перикарда также множественные гетерогенные участки кальциноза, вероятнее всего посттуберкулезной этиологии. Несмотря на невысокое качество изображения КТ грудной клетки (вынужденное положение на боку, артефакты от рук), при более детальном рассмотрении в правых отделах сердца визуализировались изменения (плюс-ткань), которые можно интерпретировать как эхинококковые кисты (рис. 2).

На электрокардиографии (ЭКГ) при поступлении (октябрь 2022 г.) синусовый ритм с ЧСС 75 уд/мин, rS с V1 по V4, (-) зубцы Т с V1 по V5. При ретроспективном анализе ЭКГ от октября 2019 г. выявлена синусовая тахикардия с ЧСС 108 уд/мин, нормальный прирост зубцов R и (+) зубцы Т во всех грудных отведениях. На ЭКГ от 22.06.2021 регистрировался а-в узловой ритм с ЧСС
67 уд/мин, появились (-) зубцы Т в грудных отведениях (рис. 3).
 По ЭхоКГ: левые отделы сердца не увеличены (левое предсердие – 3,5 см, конечно-диастолический размер – 5,1 см, конечный систолический размер – 3,6 см). Снижение глобальной сократимости миокарда левого желудочка (фракция выброса по Simpson 45%). Межжелудочковая перегородка и задняя стенка левого желудочка 1,0 см. Движение межжелудочковой перегородки парадоксальное. Выявлены зоны гипокинезии и акинезии в верхушечной части левого желудочка, переднеперегородочной и перегородочной области. Отмечалась дилатация правого предсердия (4,5–5,1 см), правого желудочка (3,0 см). Градиент давления на трикуспидальном клапане 50 мм рт. ст. Регургитация на трикуспидальном клапане II ст. Систолическое давление в легочной артерии – 65 мм рт. ст. Нижняя полая вена – 2,6 см (расширена), коллабирует слабо. В перикарде наличие свободного эхо-пространства в области задней стенки левого желудочка (13 мм), в области верхушки (12 мм), передней стенки правого желудочка и правого предсердия до 6 мм. В плевральной полости слева наличие свободного эхо-пространства до 4,5 см. Уплотнение аорты, створок аортального клапана с пристворчатой регургитацией. Митральная регургитация I ст.
По ЭхоКГ: левые отделы сердца не увеличены (левое предсердие – 3,5 см, конечно-диастолический размер – 5,1 см, конечный систолический размер – 3,6 см). Снижение глобальной сократимости миокарда левого желудочка (фракция выброса по Simpson 45%). Межжелудочковая перегородка и задняя стенка левого желудочка 1,0 см. Движение межжелудочковой перегородки парадоксальное. Выявлены зоны гипокинезии и акинезии в верхушечной части левого желудочка, переднеперегородочной и перегородочной области. Отмечалась дилатация правого предсердия (4,5–5,1 см), правого желудочка (3,0 см). Градиент давления на трикуспидальном клапане 50 мм рт. ст. Регургитация на трикуспидальном клапане II ст. Систолическое давление в легочной артерии – 65 мм рт. ст. Нижняя полая вена – 2,6 см (расширена), коллабирует слабо. В перикарде наличие свободного эхо-пространства в области задней стенки левого желудочка (13 мм), в области верхушки (12 мм), передней стенки правого желудочка и правого предсердия до 6 мм. В плевральной полости слева наличие свободного эхо-пространства до 4,5 см. Уплотнение аорты, створок аортального клапана с пристворчатой регургитацией. Митральная регургитация I ст.Исследование функции внешнего дыхания: жизненная емкость легких (ЖЕЛ) – 28% д. ж.; объем форсированного выдоха за 1-ую секунду (ОФВ1) – 25% д. ж.; ОФВ1/форсированная ЖЕЛ (ФЖЕЛ) – 0,6; ОФВ1 после пробы с бронхолитиком – 29% д. ж. Заключение: резкое снижение ЖЕЛ. Нарушение функции вентиляции по обструктивному типу резкое. Проба с бронхолитиком отрицательная. Прирост ОФВ1 после пробы с бронхолитиком на 1,6%.
На 12-й день нахождения в стационаре пациентке выполнено оперативное вмешательство: вскрытие полости абсцесса размером 5×4×4 см, расположенного в переднем средостении, удалены секвестры хрящевой ткани, полость абсцесса санирована. В послеоперационном периоде рана очистилась, наблюдалась грануляция.
За время пребывания в стационаре пациентке проводилась антибактериальная терапия (Цефазолин), дезинтоксикационная терапия (Дисоль), получала растворы для энтерального и парентерального питания (Фрезубин, Альбумин), нестероидные противовоспалительные препараты (Кетопрофен). По поводу сердечной недостаточности были назначены ингибитор ангиотензинпревращающего фермента (Периндоприл), β-адреноблокатор (Карведилол), антагонист минералокортикоидных рецепторов (Верошпирон), блокатор натрий-глюкозного ко-транспортера 2-го типа (Дапаглифлозин), диуретики (Фуросемид, Торасемид), сердечные гликозиды (Дигоксин), препараты калия (Панангин). Продолжала прием противопротозойной терапии (Альбендозол 600 мг/сут).
Несмотря на проводимую терапию, у пациентки сохранялась одышка в покое, тахикардия, отеки стоп и голеней. На 40-й день госпитализации произошла остановка дыхания и сердечной деятельности. Реанимационные мероприятия оказались не эффективными.
При патолого-анатомическом вскрытии в области затылочной кости черепа закрытое фрезевое отверстие, твердая оболочка головного мозга сращена с краями фрезевого отверстия. При осмотре грудной клетки в проекции средней трети грудины справа виден свищевой ход, проникающий в грудную полость. Грудина и часть ребер справа резецированы. Сердце, сердечная сорочка сращены с грудной стенкой. В плевральных полостях по 150–250 мл жидкости. Полость перикарда облитерирована, листки перикарда утолщены, белесоватого цвета. Сердце увеличено за счет правых отделов (12,5×12,5×8 см). В области боковой стенки правого желудочка и правого предсердия разрастание в виде цветной капусты, распространяющееся на органы переднего средостения, охватывающие ствол легочной артерии, восходящий отдел дуги аорты с их сдавлением. Миокард дряблой консистенции, волокнистого строения, серовато-красный, с мелкими рассеянными белесоватыми рубчиками, неравномерного кровенаполнения. Толщина стенки левого желудочка 1,2–1,3 см.
В толще стенки правого желудочка и правого предсердия определяется полостное образование овальной формы 7,5×6,0×7,0 см с плотной стенкой, представленной волокнистой белесоватой тканью толщиной 2,5–3,0 см. Выстилка полостного образования гладкая.
В просвете полости выявлены замазкообразные гноевидные массы серо-желтого цвета. Полости правого предсердия и правого желудочка резко сужены за счет выбухания образования вовнутрь. Эндокард и клапанный аппарат не изменены, коронарные артерии интактны. Легочный ствол и обе легочные артерии содержат посмертные свертки крови. Легочная ткань на разрезе застойная, темно-красного цвета, влажная. В S6 и S3 справа определяются образования до 3,0 см в диаметре, представленные на разрезе плотной пористой белесоватой тканью. В просвете трахеи и бронхов в большом количестве пенистая розовая мокрота. На передней брюшной стенке по средней линии живота старый послеоперационный рубец. В брюшной полости расположение органов правильное. Листки брюшины гладкие, блестящие, в верхнем этаже массивные спайки в области печени. В брюшной полости наличие свободной жидкости 2,5 л. При осмотре органов пищеварения обращает на себя внимание деформированная печень, спаянная с диафрагмой, в размерах уменьшена (18,0×12,0×10,0 см). Селезенка увеличена (14,0×8,0×4,0 см).
При гистологическом исследовании стенка полостного образования, выявленного в сердце, представлена плотной соединительной тканью, в которой определяются очаговые скопления лимфоидных, эпителиоидных клеток и фибробластов, а также малочисленных гигантских многоядерных клеток наподобие клеток инородных тел, множественные очаги дистрофического обызвествления капсулы. С внутренней стороны капсулы определяются характерные сколексы, окруженные бесструктурными и некротическими массами. В окружающей ткани миокарда участки отека стромы и полнокровия сосудов с инфильтрацией полиморфно-ядерными лейкоцитами, лимфоцитами, макрофагами, плазматическими клетками. Во всех органах признаки острого венозного полнокровия.
Причиной столь массивной диссеминации эхинококковым процессом внутренних органов, несмотря на проводимую противопротозойную терапиию, может быть ятрогения из-за нарушения техники выполнения эхинококкэктомии, в результате чего происходит интраоперационная имплантация сколексов [21, 22]. Другой наиболее частой причиной диссеминации является самопроизвольный разрыв эхинококковых кист печени и легких с попаданием сколексов в кровоток с последующим распространением их в другие органы [23, 24]. У представленной пациентки мог быть как спонтанный, так и ятрогенный во время гемигепатэктомии разрыв кисты печени с последующей диссеминацией эхинококка в легкие, головной мозг и сердце. Особенностью данного случая является изолированное поражение правого желудочка и предсердия, без вовлечения левых отделов сердца. В стенке правого желудочка и правого предсердия имело место крупное полостное образование до 7,5 см в диаметре с характерными сколексами.
У пациентки поражение эхинококком правых отделов сердца наслоилось на хроническое легочное сердце смешанной этиологии (поражение легких в сочетании с деформацией грудной клетки). Это способствовало прогрессированию явлений сердечной недостаточности, что явилось причиной смерти больной.
При эхинококкозе сердца возможно оперативное лечение. В основном выполняют энуклеацию хитиновой оболочки с сохранением фиброзной капсулы с последующей обработкой антисептическим раствором, что позволяет снизить риск рецидива эхинококкоза.
В случае больших кист вариантом лечения является метод «пункция-аспирация-инъекция-повторная аспирация» (PAIR) [1, 4, 22]. В литературе описаны случаи успешного хирургического лечения эхинококкоза сердца при своевременной диагностике. Однако при множественном поражении миокарда очень высок риск повреждения важных структур сердца с развитием массивного кровотечения. В описанном нами клиническом случае отмечался диссеминированный процесс с поражением печени, легких, головного мозга, сердца, причем эхинококкоз сердца был заподозрен на поздней стадии заболевания. Хирургическое лечение данной пациентки было невозможно в связи с тяжестью состояния, обусловленного декомпенсированным легочным сердцем сочетанного генеза: торакодиафрагмального (деформация грудной клетки в виде выраженного грудного кифоза в результате резекции грудины, хондральной части ребер), бронхолегочного (в легких множественные участки пневмосклероза, кальцифицировавшиеся паразитарные кисты), васкулярного генеза (сдавление ствола легочной артерии множественными эхинококковыми кистами) в сочетании с эхинококковым поражением миокарда правых камер сердца.
Данный клинический случай интересен тем, что, несмотря на непрерывную терапию албендазолом, процесс принял диссеминированный характер с редкой локализацией эхинококковых кист в правых отделах сердца с распространением на органы переднего средостения, ствол легочной артерии, восходящий отдел дуги аорты с их сдавлением. От момента диагностики первичного эхинококкоза в печени и начала лечения пациентка прожила 12 лет.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare no conflict of interest.
Информация об авторах
Information about the authors
Аксютина Наталья Валерьевна – д-р мед. наук, доц., проф. каф. факультетской терапии ФГБОУ ВО «КрасГМУ им. проф.
В.Ф. Войно-Яснецкого», врач-кардиолог КГБУЗ «КМКБ №20 им. И.С. Берзона». E-mail: aks-n-v@yandex.ru; ОRCID: 0000-0002-4856-2729
Natalya V. Aksyutina – Dr. Sci. (Med.), Full Prof., Voyno-Yasenetsky Krasnoyarsk State Medical University, cardiologist, Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon. E-mail: aks-n-v@yandex.ru; ORCID: 0000-0002-4856-2729
Большакова Татьяна Юрьевна – канд. мед. наук., доц. каф. факультетской терапии ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого». ОRCID: 0000-0001-9653-6026
Tatyana Yu. Bolshakova – Cand. Sci. (Med.), Voyno-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0001-9653-6026
Ибрагимова Клара Талгатбековна – врач-терапевт, КГБУЗ «КМКБ №20 им. И.С. Берзона»
Klara T. Ibragimova – Therapist, Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon.
Кононов Евгений Николаевич – врач-кардиолог, зам. главного врача по клинико-экспертной работе, КГБУЗ «КМКБ №20 им. И.С. Берзона»
Evgeny N. Kononov – Cardiologist, Deputy Chief Physician for Clinical and Expert Work, Krasnoyarsk Interdistrict Clinical Hospital No 20 named after I.S. Berzon
Парфенова Татьяна Михайловна – канд. мед. наук., доц., доц. каф. факультетской терапии, ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0002-1140-6722
Tatyana M. Parfenova – Cand. Sci. (Med.), Voyno-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0002-1140-6722
Надеждина Дарья Аркадьевна – клин. ординатор каф. физической и реабилитационной медицины с курсом ПО, ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого»
Daria A. Nadezhdina – Clinical Resident, Voyno-Yasenetsky Krasnoyarsk State Medical University
Поступила в редакцию: 05.12.2024
Поступила после рецензирования: 26.12.2024
Принята к публикации: 16.01.2025
Received: 05.12.2024
Revised: 26.12.2024
Accepted: 16.01.2025
Список исп. литературыСкрыть список1. Жукова С.И., Макаров И.А., Рыжкова Д.В. и др. Клинический случай эхинококкоза сердца. MEDLINE.RU. 2022;23:312-21.
Zhukova S.I., Makarov I.A., Ryzhkova D.V. et al. Case report of echinococcosis of the heart. MEDLINE.RU. 2022;23:312-21 (in Russian).
2. Гилевич М.Ю. Некоторые проблемы рецидивов эхинококковой болезни. Вестник хирургии. 1985;134(6):41-5.
Gilevich M.Yu. Some problems of recurrence of echinococcal disease. Bulletin of Surgery. 1985;134(6):41-5 (in Russian).
3. Гаибов А.Д., Неъматзода О., Рахмонов Д.А. и др. Случай диссеминированного эхинококкоза свободной брюшной полости. Оперативная хирургия и клиническая анатомия (Пироговский научный журнал). 2022;6(3):50-5. DOI: 10.17116/operhirurg2022603150
Gaibov A.D., Nematzoda O., Rakhmonov D.A. et al. A case of disseminated echinococcosis of the abdominal cavity. Russian Journal of Operative Surgery and Clinical Anatomy. 2022;6(3):50-5. DOI: 10.17116/operhirurg2022603150 (in Russian).
4. Иванов В.А., Подчасов Д.А., Евсеев Е.П. и др. Успешное хирургическое лечение эхинококкоза сердца. Кардиология и сердечно-сосудистая хирургия. 2011;4(4):89-92.
Ivanov V.A., Podchasov D.A., Evseev E.P. et al. Successful surgical treatment of cardiac echinococcosis. Russian Journal of Cardiology and Cardiovascular Surgery. 2011;4(4):89-92 (in Russian).
5. Miralles A, Bracamonte L, Pavie A et al. Cardiac echinococcosis. Surgical treatment and results. J Thorac Cardiovasc Surg 1994;107(1):184-90.
6. Uysalel A, Aral A, Atalay S, Akalin H. Cardiac echinococcsis with multivisceral involvement. Pediatr Cardiol 1996;17(4):268-70. DOI: 10.1007/BF02524808
7. Гаибов А.Д., Камолов А.Н., Мирзоев С.А. и др. Эмболия бифуркации аорты, вызванная разорвавшейся эхинококковой кистой сердца. Кардиология и сердечно-сосудистая хирургия. 2009;2(5):89-92.
Gaibov A.D., Kamolov A.N., Mirzoev S.A. et al. Embolism of aorta bifurcation caused by rupture of cardiac hydatid cyst. Russian Journal of Cardiology and Cardiovascular Surgery. 2009;2(5):89-92 (in Russian).
8. Di Bello R, Menendez H. Intracardiac rupture of hydatid cysts of the heart. A study based on three personal observations and 101 cases in the world literature. Circulation 1963;27:366-74. DOI: 10.1161/01.cir.27.3.366
9. Петровский Б.В., Милонов О.Б., Десничин П.П. Хирургия эхинококкоза. Москва: Медицина; София: Медицина и физкультура, 1985;216.
Petrovskiy B.V., Milonov O.B., Desnichin P.P. Moscow: Medicine; Sofia: Medicine and Physical Education, 1985;216 (in Russian).
10. Von Sinner WN. CT and MRI findings of cardiac echinococcosis. Eur Radiol 1995;5:66-73.
11. Miralles A, Bracamonte L, Pavie A et al. Cardiac echinococcosis. Surgical treatment and results. J Thorac Cardiovasc Surg 1994;107(1):184-90.
12. Birincioðlu CL, Bardakci H, Küçüker SA et al. A clinical dilemma: cardiac and pericardiac echinococcosis. Ann Thorac Surg 1999;68(4):1290-4. DOI: 10.1016/s0003-4975(99)00692-x
13. Uysalel A, Yazicioglu L, Aral A, Akalin H. A multivesicular cardiac hydatid cyst with hepatic involvement. Eur J Cardiothorac Surg 1998;14(3):335-7. DOI: 10.1016/s1010-7940(98)00169-9
14. Ahmed T, Al-Zaibag M, Allan A et al. Cardiac echinococcosis causing acute dissection of the left ventricular free wall. Echocardiography 2002;19(4):333-6. DOI: 10.1046/j.1540-8175.2002.00333.x
15. Unlü Y, Ceviz M, Karaoðlanoðlu N et al. Arterial embolism caused by a ruptured hydatid cyst in the heart: report of a case. Surg Today 2002;32(11):989-91. DOI: 10.1007/s005950200198
16. Kopp CW, Binder T, Grimm M et al. Images in cardiovascular medicine. Left ventricular echinococcosis with peripheral embolization. Circulation 2002;106(13):1741-2. DOI: 10.1161/01.cir.0000035274.48425.92
17. Giorgadze, Nadareishivili A, Goziridze M et al. Unusual recurrence of hydatid cysts of the heart: report of two cases and review of the clinical and surgical aspects of the disease. J Card Surg 2000;15(3):223-8. DOI: 10.1111/j.1540-8191.2000.tb00460.x
18. Odev K, Acikgözoglu S, Gormüs N et al. Pulmonary embolism due to cardiac hydatid disease: imaging findings of unusual complication of hydatid cyst. Eur Radiol 2002;12(3):627-33. DOI: 10.1007/s003300100988
19. Lahdhili H, Hachicha S, Ziadi M, Thameur H. Acute pulmonary embolism due to the rupture of a right ventricle hydatic cyst. Eur J Cardiothorac Surg 2002;22(3):462-4. DOI: 10.1016/s1010-7940(02)00360-3
20. Bolourian A.A. Total resection of interatrial septal echinococcosis. Asian Cardiovascular and Thoracic Annals 1998;6(1):54-6.
21. Курбонов К.М., Азиззода З.А., Ефанов М.Г., Рузибойзода К.Р. Результаты применения миниинвазивных технологий в хирургическом лечении эхинококкоза печени и его осложнений. Вестник Авиценны. 2020;22(3):448-54. DOI: 10.25005/2074-0581-2020-22-3-448-454
Kurbonov K.M., Azizzoda Z.A., Efanov M.G., Ruziboyzoda K.R. Results of the use of minimally invasive technologies in the surgical treatment of hepatic echinococcosis and its complications. Vestnik Avitsenny = Avicenna Bulletin. 2020;22(3):448-54. DOI: 10.25005/2074-0581-2020-22-3-448-454 (in Russian).
22. Гулов М.К., Салимов Д.С., Турсунов Р.А. и др. Классификация осложнений эхинококкоза печени. Вестник Авиценны. 2010;3(44):18-24.
Gulov M.K., Salimov D.C., Tursunov R.A. et al. Summary classification of liver echinococcosis complications. Vestnik Avitsenny = Avicenna Bulletin. 2010;3(44):18-24 (in Russian).
23. Tünger Ö. Dünyada Kistik Ekinokokkoz Epidemiyolojisi [Epidemiology of cystic echinococcosis in the world]. Turkiye Parazitol Derg 2013;37(1):47-52. DOI: 10.5152/tpd.2013.12
24. Mahmoudi S, Mamishi S, Banar M et al. Epidemiology of echinococcosis in Iran: a systematic review and meta-analysis. BMC Infect Dis 2019;19(1):929. DOI: 10.1186/s12879-019-4458-5


