Клинический разбор в общей медицине №3 2025
Irina Yu. Botvinko2, Ekaterina E. Nakonechnaya3
1 Omsk State Medical University, Omsk, Russia;
2 Omsk region Clinical medical and sanitary unit No. 7, Omsk, Russia;
3 Omsk region Clinical cardiology dispensary, Omsk, Russia
ElenaV.Usacheva@yandex.ru
Abstract
The importance of timely diagnosis of pulmonary hypertension in primary health care is difficult to overestimate, since this condition is characterized by a low five-year survival rate, is characterized by difficulty in establishing a diagnosis, low alertness and insufficient awareness of clinicians about this disease. The article presents the main methods of diagnosis of pulmonary hypertension, provides data typical for three hemodynamic types of pulmonary hypertension. Echocardiographic diagnosis of pulmonary hypertension is the most widely used instrumental method, since the method is accessible to a primary care physician and allows identifying patients who need to be referred for further examination using invasive technologies. The role and significance of measuring the rate of tricuspid regurgitation of 2.8 m/s in the diagnosis of this pathological condition is indicated. The advantages and place of transthoracic echocardiography in the noninvasive diagnosis of the hemodynamic variant of pulmonary hypertension are shown by determining the maximum rate of early diastolic filling of the left ventricle (E) and the maximum rate of early diastolic displacement of the lateral segment of the mitral valve ring (e') according to the Nagueh formula. The article presents clinical cases demonstrating the capabilities of transthoracic echocardiography in detecting pulmonary hypertension and determining its hemodynamic type. The determination of the hemodynamic type of pulmonary hypertension by noninvasive methods allows for further differential diagnostic search only among the causes of the established type of pulmonary hypertension, which shortens the diagnostic pathway, saves time and costs for diagnosis and allows timely treatment.
Keywords: pulmonary hypertension, chronic thromboembolic pulmonary hypertension, chronic thromboembolic lung disease, echocardiography, pulmonary artery jamming pressure, pulmonary vascular resistance, precapillary type, postcapillary type.
For citation: Usacheva E.V., Nadey E.V., Shkirinets A.V., Kanunnikova O.I., Botvinko I.U., Nakonechnaia E.E. Echocardiography in the
differential diagnosis of the causes of pulmonary hypertension on the example of clinical cases. Clinical review for general practice. 2025; 6 (3): 47–54 (In Russ.). DOI: 10.47407/kr2024.6.3.00581
5-летней выживаемости [3].
ЛГ может возникнуть как одно из отдаленных осложнений тромбоэмболии ЛА и в таком случае трактуется как хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) [4–6]. ХТЭЛГ – это прекапиллярная форма ЛГ, причиной которой является наличие организованных (хронических) окклюзирующих или неокклюзирующих тромботических масс в ЛА (главных, долевых, сегментарных, субсегментарных артериях) в течение не менее трех месяцев после эпизода тромбоэмболии и развитие дистальной легочной васкулопатии [1, 7]. Отличительной особенностью ХТЭЛГ является неравномерность поражения сосудистого легочного русла и в большинстве случаев наличие взаимосвязи с тромбозом периферических вен [8].
По разным данным, распространенность ХТЭЛГ составляет от 2 до 40 случаев на 1 млн человек [9, 1], но точных данных по эпидемиологии данного заболевания нет, при этом очевидно, что оно распространено гораздо шире, чем принято считать [10]. ХТЭЛГ следует подозревать у каждого пациента с симптомами и признаками ЛГ неясного генеза даже при отсутствии перенесенного эпизода тромбоэмболии ЛА (ТЭЛА). Сложности в установлении диагноза во многом связаны с самим заболеванием, а именно с неспецифической клинической картиной, однако, имеет значение и низкая настороженность врачей в отношении ХТЭЛГ [11], и недостаточная информированность клиницистов о данном заболевании [5, 6].
Принципы параклинической диагностики хронической тромбоэмболической легочной гипертензии
Лабораторные маркеры. Тактика лабораторного обследования при подозрении на ХТЭЛГ определяется тем, что в основе заболевания лежит тромбофилическое состояние. Для выявления тромбофилии и предрасполагающих к ней заболеваний, проводят как общеклиническое обследование (общий и биохимический общетерапевтический анализы крови), исследование кислотно-основного состояния и газов крови, так и оценку данных коагулограммы, в том числе D-димера. При выявлении в процессе скрининговых исследований изменений в системе гемостаза либо при наличии рецидивирующих тромботических событий проводится расширенное исследование системы гемостаза [12].
NT-proBNP – предшественник мозгового натрийуретического пептида – это биомаркер, рекомендуемый для оценки наличия правожелудочковой сердечной недостаточности, определения функционального статуса пациента с подтвержденной идиопатической ЛГ (ЛАГ) и для оценки прогноза и эффективности проводимой ЛАГ-специфической терапии [1, 8, 13].
Инструментальная диагностика при подозрении на ХТЭЛГ выполняется в несколько этапов и на первом этапе проводятся скрининговые методы исследования – электрокардиография (ЭКГ) и трансторакальная эхокардиография (ТТ-ЭхоКГ), прицельная рентгенография органов грудной клетки, исследование функции внешнего дыхания. Далее проводят мультиспиральную компьютерную томографию легких с контрастированием бассейна ЛА (МСКТ ОГК), вентиляционно-перфузионную сцинтиграфию и катетеризацию правых отделов сердца.
ЭКГ – обязательный метод диагностики у больных с подозрением на наличие ХТЭЛГ при первичном обследовании и в процессе динамического наблюдения [1]. Этот метод позволяет выявить признаки гипертрофии и перегрузки правого желудочка (ПЖ), дилатации и гипертрофии правого предсердия (р-pulmonale).
ЭКГ-признаки гипертрофии ПЖ, а именно увеличение амплитуды зубца R и соотношения R/S в правых отведениях, имеют недостаточную чувствительность (55%) и специфичность (70%), чтобы быть использованными в качестве скрининговых, тогда как признаки перегрузки ПЖ (преходящее смещение сегмента RS-T и сглаженность или инверсия Т в правых грудных отведениях) являются более чувствительными. Следует отметить, что такие ЭКГ-признаки, как расширение комплекса QRS и удлинение интервала QT свидетельствуют о тяжести ЛГ и ассоциированы с неблагоприятным прогнозом [14]. Неоспоримым преимуществом метода является его простота, доступность и низкая стоимость, но ЭКГ-признаки поражения правых отделов сердца определяются уже в развернутой стадии болезни, что снижает диагностическую ценность данного метода [15].
ТТ-ЭхоКГ – основной метод на этапе диагностического поиска, ценность которого обусловлена тем, что ТТ-ЭхоКГ позволяет не только оценить уровень давления в ЛА, но и установить наличие заболеваний, приводящих к развитию ЛГ, в первую очередь пороков сердца [15, 16].
МСКТ ОГК, а именно КТ-ангиопульмонография – наиболее информативный метод визуализации в диагностике ХТЭЛГ, позволяющий оценить структуру легочного русла, наличие тромботических масс и их локализацию. МСКТ-картина хронической тромбоэмболии может быть представлена окклюзиями и стенозами ЛА, а также эксцентрическими дефектами наполнения вследствие наличия тромбов, в том числе реканализованных [17]. По результатам МСКТ ОГК можно заподозрить наличие ЛГ, идентифицировать причину ЛГ (например, ХТЭЛГ или заболевание легких), выявить признаки ЛАГ-ассоциированных состояний (например, дилатация пищевода при системной склеродермии или наличие порока сердца) [18]. Поэтому проведение
КТ-ангиопульмонографии рекомендуется всем пациентам с ЛГ для выявления причины заболевания [19, 20].
Вентиляционно-перфузионная сцинтиграфия (ВПС) легких является одним из методов, позволяющих исключить тромбоэмболический генез ЛГ. При наличии подозрения на ХТЭЛГ и неинформативности
ТТ-ЭхоКГ, ВПС является исследованием выбора, она обладает 96–100% чувствительностью и 86–95% специфичностью для выявления признаков ХТЭЛГ и не обладает нефротоксичностью. Множественные дефекты перфузии с сохраненной вентиляционной функцией – характерные признаки ХТЭЛГ. Однако, учитывая стоимость и радиационную нагрузку, ВПС не может быть рекомендована в качестве скрининга ХТЭЛГ [21].
Чрезвенозная катетеризация сердца (ЧВКС). «Золотым стандартом» диагностики ЛГ считается выполнение малоинвазивного вмешательства – ЧВКС.
В соответствии с современными рекомендациями, диагноз ЛГ устанавливается при уровне среднего давления в ЛА (ДЛА) более 20 мм рт. ст., измеренного при ЧВКС в покое. По результатам ЧВКС можно определить гемодинамический вариант ЛГ – прекапиллярная или посткапиллярная, и определить дальнейшую тактику ведения пациента. Гемодинамическими критериями прекапиллярного варианта ЛГ служат: среднее ДЛА>20 мм рт. ст., давление заклинивания ЛА (ДЗЛА)≤15 мм рт. ст., легочное сосудистое сопротивление (ЛСС)>2 ед. Вуда при наличии множественных стенозирующих и/или окклюзирующих поражений ветвей ЛА различного калибра. ЧВКС является инвазивной процедурой, информативность и безопасность которой основывается на четырех принципах: рациональном выборе венозного доступа, тщательной калибровке датчика давления, соблюдении правил измерения ДЗЛА и расчете сердечного выброса [6, 12]. Недостатками метода являются необходимость введения больших объемов контрастного вещества, недостаточное контрастирование верхнедолевых ветвей, необходимость наличия специального оборудования и квалифицированных опытных специалистов.
Эхокардиографическая диагностика легочной гипертензии
На уровне первичного звена здравоохранения ТТ-ЭхоКГ является неинвазивным, информативным и доступным методом диагностики ЛГ. Доказана хорошая сопоставимость результатов ТТ-ЭхоКГ с данными ЧВКС. Учитывая, что ЧВКС является инвазивной процедурой, которая проводится на базе экспертного центра, ТТ-ЭхоКГ идеально подходит для динамического наблюдения пациента. Обнаружение пороков сердца (септальные дефекты, открытый артериальный проток, аномальный дренаж легочных вен, сложные врожденные пороки сердца), как наиболее частой причины ЛГ, является одной из важных задач в дифференциально-диагностическом алгоритме при проведении ТТ-ЭхоКГ.
ЭхоКГ-диагностика ЛГ включает расчет давления в ЛА, а также оценку дополнительных признаков, к которым относят размеры правых отделов сердца, дисфункцию ПЖ и диаметр ЛА [12]. Наиболее значимый вклад в оценку ЛГ вносят допплерографические методики, с измерением систолического, диастолического и среднего давления в ЛА с помощью непрерывно-волнового допплера по скорости регургитации на трикуспидальном и пульмональном клапанах [1].
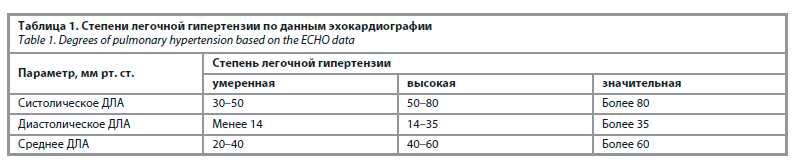
Определение систолического ДЛА при проведении ТТ-ЭхоКГ основано на оценке показателей трикуспидальной регургитации (ТР), обусловленной наличием градиента давления между ПЖ и правым предсердием (ПП) в фазу систолы. Следует отметить, что в рутинной практике определение среднего ДЛА и диастолического ДЛА по данным ТТ-ЭхоКГ практически не используется, однако их расчет может быть применен в случаях, когда в силу тех или иных причин расчет ДЛА затруднен. В зависимости от величин систолического, среднего и диастолического ДЛА, ЛГ подразделяют на умеренную, высокую и значительную. Выделение степеней тяжести ЛГ необходимо для определения тактики ведения пациента и скорости принятия решений в конкретный период времени. Пороговые значения выраженности ЛГ приведены в табл. 1 [22].
Измерение ДЛА по ТР и легочной регургитации может быть сопряжено с получением как завышенных, так и заниженных значений этого показателя в силу различных причин (несоблюдение правил допплерометрического исследования, выраженная дилатация правых отделов сердца, эмпирическая оценка давления в ПП и др.). В связи с этим современные согласительные документы вместо степеней ЛГ при проведении
ТТ-ЭхоКГ на начальном этапе обследования рекомендуют оценивать вероятность наличия ЛГ, которая может быть определена как низкая, средняя или высокая [1].
С этой целью экспертами был предложен диагностический алгоритм, в котором в качестве начального критерия оценки необходимо использовать скорость ТР.
Пограничным значением в диагностике ЛГ является скорость ТР 2,8 м/с, что соответствует градиенту давления 31 мм рт. ст. В силу того, что скорость ТР далеко не всегда отражает степень повышения давления в ЛА, при определении вероятности ЛГ необходимо также принимать во внимание ряд дополнительных признаков,
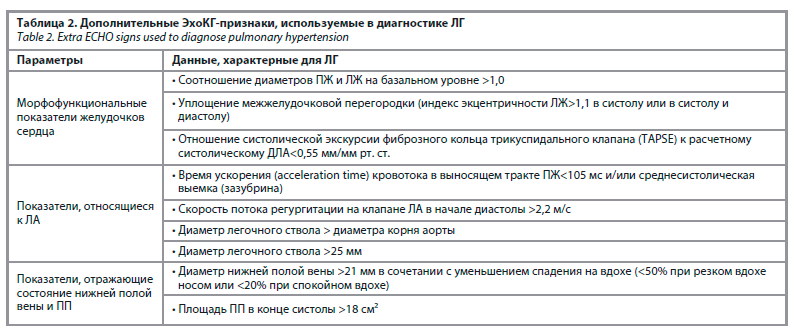
отражающих морфологические и функциональные показатели. В современных рекомендациях по диагностике и лечению ЛГ эти признаки разделены на 3 группы (табл. 2).
Во всех случаях, когда скорость ТР не превышает значения 2,8 м/с и нет дополнительных ЭхоКГ-признаков, вероятность ЛГ расценивается как низкая. О средней вероятности ЛГ свидетельствует увеличение скорости ТР в пределах 2,9–3,4 м/с при отсутствии дополнительных критериев ЛГ, а также нормальная скорость ТР при наличии дополнительных признаков, относящихся по меньшей мере к двум из трех групп, перечисленных выше. Если же скорость ТР превышает 3,4 м/с, вне зависимости от наличия или отсутствия дополнительных признаков вероятность ЛГ считают высокой, как и в случаях, когда скорость ТР имеет промежуточные значения (2,9–3,4 м/с) в сочетании с дополнительными признаками ЛГ. Предложенный диагностический алгоритм позволяет выделить категорию пациентов, которые нуждаются в дальнейшем детальном обследовании для верификации ЛГ с применением более сложных методов исследования, в том числе ЧВКС.
Несомненным преимуществом ТТ-ЭхоКГ является возможность неинвазивного определения гемодинамического варианта ЛГ. На сегодняшний день предложены формулы, позволяющие по данным допплерометрии рассчитать значения ДЗЛА и ЛСС.
Для расчета ДЗЛА используется формула Nagueh [23]: ДЗЛА = 1,24 × Е/е' + 1,9, где E – максимальная скорость раннего диастолического наполнения левого желудочка (ЛЖ), е' – максимальная скорость раннего диастолического смещения латерального сегмента кольца митрального клапана.
ЛСС рассчитывается по формуле: (среднее ДЛА – ДЗЛА)/сердечный выброс, и измеряется в единицах Вуда. Наиболее часто в эхокардиографической оценке ЛСС используется формула, которая была предложена A.E. Abbas и соавт. в 2003 г. [24]: ЛСС = (Vтр/VTIвтпж × ×10)+0,16, где Vтр – максимальная скорость ТР, а VTIвтпж – интеграл скорости кровотока в выносящем тракте ПЖ.
Место эхокардиографии в дифференциальной диагностике форм легочной гипертензии на примере клинических случаев
Клинический случай 1. Пациент Ф., 74 лет, обратился к врачу-пульмонологу в апреле 2024 г. после эпизода кровохарканья с жалобами на кашель с отхождением мокроты серого цвета с прожилками крови до 10 мл, инспираторную одышку при умеренных физических нагрузках. Из анамнеза известно, что первое кровохарканье было в январе 2022 г., когда был госпитализирован с острым флеботромбозом слева и инфаркт-пневмонией, затем в марте 2024 г. вновь госпитализация с острым флеботромбоз справа, рецидивирующим тромбозом слева с развитием инфаркт-пневмонии слева, кровохарканьем. После выписки осмотрен врачом-пульмонологом для решения вопроса о приеме антикоагулянтов. При физикальном исследовании тоны сердца приглушены, ритмичные, акцент II тона над ЛА, на верхушке короткий, систолический шум, иррадиирует вдоль левого края грудины вверх. Выставлен предварительный диагноз: состояние после рецидивирующей ТЭЛА мелких ветвей ЛА с развитием инфаркт-пневмонии (январь 2022 г., март 2024 г.), кровохарканье (январь 2022 г., март 2024 г.). С учетом наличия одышки, кровохарканья в анамнезе и акцента второго тона на ЛА была заподозрена ЛГ. Рекомендовано дообследование для исключения иных причин кровохарканья: ТТ-ЭхоКГ (исключение недостаточности левых отделов сердца), исследование мокроты на кислотоустойчивые микобактерии (КУМ) и атипичные клетки, фибробронхоскопия с исследованием бронхоальвеолярного лаважа на атипичные клетки, цитологию, КУМ и консультация фтизиатра (для исключения туберкулеза и новообразования как причины кровохарканья). По результатам проведенного обследования выявлены признаки митральной регургитации 1-й степени при нормальных размерах левых отделов сердца и сохранной фракции выброса ЛЖ, что исключало патологию левых отделов сердца как причину кровохарканья. Выявлены признаки ТР 2-й степени с уровнем систолического ДЛА 35 мм рт. ст., при нормальных размерах ПЖ и ПП, при отсутствии признаков дисфункции ПЖ (TAPSE 27 мм), что исключало наличие ЛГ у данного пациента. Туберкулез и новообразования органов дыхания также были исключены. С учетом тромботического анамнеза, наличия кровохарканья у пациента без признаков ЛГ, заподозрена хроническая тромбоэмболическая болезнь легких (ХТЭБЛ), в связи с чем пациент был направлен на МСКТ ОГК с контрастированием. 24.04.2024 по данным МСКТ ОГК: ствол ЛА – 27 мм, левая ветвь – 22 мм, правая ветвь – 23 мм, в просвете передней сегментарной ветви правой верхнедолевой ЛА и в устье нижнедолевой ветви левой ЛА определяются тромботические массы с зонами поствоспалительного пневмофиброза в нижних долях обоих легких. Таким образом, у пациента в возрасте старше 70 лет ЛГ при высокой ее вероятности была исключена по данным ТТ-ЭхоКГ. Наличие по данным МСКТ ОГК признаков ХТЭБЛ при отсутствии ЛГ свидетельствует о высоких компенсаторных возможностях организма, благодаря которым при наличии признаков обструкции ветвей ЛА ЛГ не развилась. Подтверждение ХЭТБЛ позволило принять решение о продолжении приема антикоагулянтов с целью профилактики рецидива ТЭЛА и необходимости проведения контрольной ТТ-ЭхоКГ не реже чем 1 раз в год в течение трех лет для оценки состояния правых отделов сердца и давления в ЛА.
Клинический случай 2. Пациентка С., 65 лет, в феврале 2024 г. обратилась к врачу-пульмонологу с жалобами на одышку, возникающую во время физической нагрузки по интенсивности несколько выше бытового уровня, сопровождается болью за грудиной давящей, жгучей, однократно в ответ на нитроглицерин возникло предобморочное состояние, при этом боль и одышка не купировались, в связи с чем более нитроглицерин не использовала. Считает себя больной с ноября 2020 г., когда после перенесенной новой коронавирусной инфекции с тяжелой пневмонией, в объеме 55% поражения легочной ткани, появилась одышка. В сентябре 2023 г. в связи с сохраняющейся одышкой обратилась к пульмонологу, предоставив МСКТ ОГК от 06.04.2023. Пульмонологом заболевание органов дыхания исключено, назначено проведение повторной консультации кардиолога. Четыре месяца пациентка за медицинской помощью не обращалась, получала лечение амбулаторно в объеме вторичной кардиоваскулярной профилактики. Во второй половине января 2024 г. стала отмечать появление загрудинных болей в ответ на физическую нагрузку, в силу чего появился страх выходить на улицу, 29.01.2024 в связи с интенсивными болями была по неотложной помощи госпитализирована в кардиологическое отделение, где были выявлены признаки ЛГ, высокий уровень Д-димера при интактных коронарных артериях, по результатам выписки амбулаторно направлена на дообследование для уточнения генеза ЛГ. В стационарных условиях были определены традиционные параметры ТТ-ЭХОКГ, не позволяющие рассчитать ДЗЛА и ЛСС, и, соответственно, определить тип ЛГ. С учетом высокого уровня Д-димера и наследственного отягощенного анамнеза по тромботическим событиям (мама пациентки в 55 лет умерла от массивной ТЭЛА) была заподозрена ХТЭЛГ, амбулаторно выполнена МСКТ ОГК с ангиографией легочных сосудов (апрель 2024 г.), по данным которой признаков тромбоза ветвей ЛА не выявлено, но подтверждены признаки ЛГ в виде увеличения диаметра легочного ствола до 38 мм (диаметр аорты 34 мм), признаки единичных очагов локального фиброза легких с обеих сторон по сравнению с МСКТ ОГК от 06.04.2023 без динамики. Поскольку при установлении причины ЛГ круг диагностического поиска определяется формой ЛГ (прекапиллярная/посткапиллярная), пациентка повторно была направлена на ТТ-ЭхоКГ с оценкой параметров, необходимых для расчета ДЗЛА и ЛСС, и на основании этого выбора пути диагностического поиска. Данные ТТ-ЭхоКГ пациентки С. представлены в табл. 3.
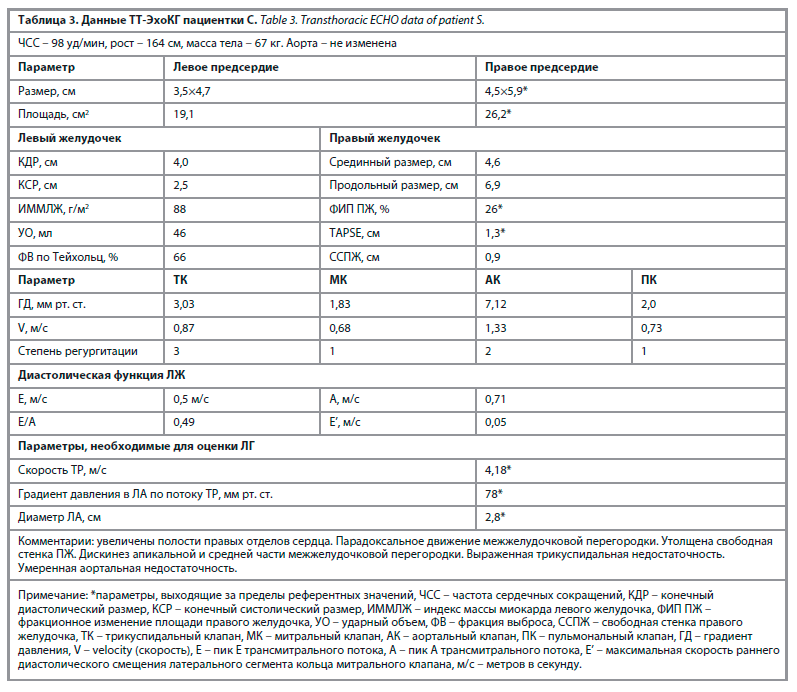
Известно, что для установления формы ЛГ в условиях первичного звена здравоохранения и отбора пациентов на проведение ЧВКС предлагается использование расчетных ДЗЛА и ЛСС, которые в допустимой степени эквивалентны данным ЧВКС. На основании результатов ТТ-ЭхоКГ нами рассчитаны ДЗЛА и ЛСС:
ДЗЛА = 1,24 × Е/е' + 1,9 = 1,24 × 0,5/0,05 + 1,9 = 14,3
ЛСС = (Среднее ДЛА – ДЗЛА)/сердечный выброс = (80 – 14,3)/4,5 = 14,6.
Рассчитанные ДЗЛА и ЛСС указывали на прекапиллярный генез ЛГ у данной пациентки. Установление прекапиллярного генеза ЛГ позволило исключить патологию левых отделов сердца как причину ЛГ и продолжить дифференциально-диагностический поиск среди причин прекапиллярной ЛГ. Пациентка повторно была приглашена на прием, во время которого выявлены признаки синдрома Рейно, поэтому приоритетным стало исключение системного заболевания соединительной ткани как причины ЛГ. При обследовании выявлена позитивность по антинуклеарному фактору – 5120 с типом свечения АС21 и АС3 (при норме до 160), антитела к центромере, в связи с чем пациентка была направлена к ревматологу, который по совокупности данных выставил диагноз «системная склеродермия». Таким образом, ТТ-ЭхоКГ, позволяя рассчитать ДЗЛА и ЛСС, помогает сузить круг исследований, необходимых для установления диагноза, сократить сроки диагностического поиска и своевременно приступить к патогенетическому лечению ЛГ.
Стойкая ЛГ всегда сопровождается необратимым ремоделированием сосудов с последующей их обструкцией и ригидностью. Без своевременно начатого лечения это приводит к гипертрофии и недостаточности ПЖ, что является основной причиной смерти. Регистры ЛГ сообщают о выживаемости от 68% до 93% через 1 год и от 39% до 77% через 3 года, 12-месячная смертность у пациентов с ЛГ, ассоциированной с патологией левых отделов сердца, достигает 32%, а предикторами худшего прогноза являются нарушение функции почек, анемия, пожилой возраст, дисфункция ПЖ и наличие комбинированного посткапиллярного и прекапиллярного варианта ЛГ, а не изолированного посткапиллярного [25].
Окончательному диагнозу предшествует поэтапное обследование пациента, которое при наличии показаний завершается ЧВКС. В связи с ограниченной доступностью ЧВКС на уровне первичного звена здравоохранения показания к этому исследованию должны быть определены на предварительном этапе обследования. Диагностическая тактика предварительного этапа определяется вариантом ЛГ – прекапиллярный или посткапиллярный. Представленные клинические случаи демонстрируют возможности применения расчетных показателей – ДЗЛА и/или ЛСС на основании параметров ТТ-ЭхоКГ для выбора диагностической тактики. ТТ-ЭхоКГ доступна на уровне первичного звена здравоохранения в каждом регионе. На сегодняшний день большинство протоколов ТТ-ЭхоКГ не содержат данных о скорости ТР и не позволяют рассчитать ДЗЛА и ЛСС. Поэтому необходимо совместное с врачами функциональной диагностики обсуждение и включение в протокол ТТ-ЭхоКГ измерения скорости ТР при ее наличии. При скорости ТР более 2,8 м/с – обязательное измерение размеров и оценка функции правых отделов сердца для раннего выявления ЛГ:
• соотношение ПЖ/ЛЖ на базальном уровне;
• TAPSE;
• скорость начальной диастолической легочной регургитации;
• время ускорения в выносящем тракте ПЖ;
• интеграл линейной скорости потока в выносящем тракте ПЖ;
• максимальная скорость раннего диастолического наполнения ЛЖ (Е);
• максимальная скорость раннего диастолического смещения латерального сегмента кольца митрального клапана (е');
• частота сердечных сокращений.
Использование такой технологии позволит осуществлять раннюю диагностику и лечение ЛГ, снизить инвалидизацию и смертность населения с данным патологическим состоянием.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Усачева Елена Владимировна – канд. мед. наук, доц., доц. каф. внутренних болезней и семейной медицины ДПО, ФГБОУ ВО ОмГМУ. E-mail: elenav.usacheva@yandex.ru; ORCID: 0000-0002-6134-1533: Researcher ID: I-4077-2017: Scopus Author ID: 56380398700
Elena V. Usacheva – Cand. Sci. (Med.), Assoc. Prof., Omsk State Medical University. E-mail: elenav.usacheva@yandex.ru; ORCID: 0000-0002-6134-1533; Researcher ID: I-4077-20174; Scopus Author ID: 56380398700
Надей Елена Витальевна – канд. мед. наук, доц., доц. каф. внутренних болезней и семейной медицины ДПО, ФГБОУ ВО
ОмГМУ. E-mail: nadeyelena@yandex.ru, ORCID: 0000-0003-0440-7118
Elena V. Nadey – Cand. Sci. (Med.), Assoc. Prof., Omsk State
Medical University. E-mail: nadeyelena@yandex.ru; ORCID: 0000-0003-0440-7118
Шкиринец (Нелидова) Анастасия Владимировна – канд. мед. наук, доц., доц. каф. пропедевтики внутренних болезней, ФГБОУ ВО ОмГМУ. E-mail: avnelidova@mail.ru; ORCID: 0000-0003-0149-6119; Researcher ID: B-8428-2017; SPIN-код: 1506-3007; Scopus Author ID: 631273
Anastasia V. Shkirinets (Nelidova) – Cand. Sci. (Med.), Assoc. Prof., Omsk State Medical University. E-mail: avnelidova@mail.ru; ORCID: 0000-0003-0149-6119; Researcher ID: B-8428-2017; SPIN-код: 1506-3007; Scopus Author ID: 631273
Канунникова Олеся Игорьевна – канд. мед. наук, ассистент каф. внутренних болезней и семейной медицины ДПО, ФГБОУ ВО ОмГМУ. E-mail: lesia.tch@yandex.ru; ORCID: 0009-0003-3721-4379; Researcher ID: LDF-2487-2024; Scopus Author ID: 56512463200
Olesya I. Kanunnikova – Cand. Sci. (Med.), Аssistant, Omsk State Medical University. E-mail: lesia.tch@yandex.ru; ORCID: 0009-0003-3721-4379; Researcher ID: LDF-2487-2024; Scopus Author ID: 56512463200
Ботвинко Ирина Юрьевна – врач функциональной диагностики, БУЗОО «КМСЧ №7». E-mail: irinabotvinko@mail.ru
Irina Yu. Botvinko – Doctor of functional diagnostics, Clinical medical and sanitary unit No. 7. E-mail: mail irinabotvinko@mail.ru
Наконечная Екатерина Эдуардовна – врач-ревматолог, зав. ревматологическим отделением, БУЗОО «Клинический кардиологический диспансер». E-mail: eka_giz@mail.ru
Ekaterina E. Nakonechnaya – Rheumatologist, Clinical Cardiological Dispensary. E-mail: eka_giz@mail.ru
Поступила в редакцию: 11.02.2025
Поступила после рецензирования: 19.02.2025
Принята к публикации: 27.02.2025
Received: 11.02.2025
Revised: 19.02.2025
Accepted: 27.02.2025
Клинический разбор в общей медицине №3 2025
Эхокардиография в дифференциальной диагностике причин легочной гипертензии на примере клинических случаев
Номера страниц в выпуске:47-54
Аннотация
Значимость своевременной диагностики легочной гипертензии в условиях первичного звена здравоохранения трудно переоценить, поскольку это состояние характеризуется низким уровнем 5-летней выживаемости, отличается сложностью установления диагноза, низкой настороженностью и недостаточной информированностью клиницистов о данном заболевании. В статье представлены основные методы диагностики легочной гипертензии, приведены данные, характерные для трех гемодинамических типов легочной гипертензии. Наиболее широко из инструментальных методов представлена эхокардиографическая диагностика легочной гипертензии, поскольку метод является доступным для врача первичного звена и позволяет выделить пациентов, нуждающихся в направлении на дообследование с помощью инвазивных технологий. Обозначена роль и значимость измерения скорости трикуспидальной регургитации 2,8 м/с в диагностике данного патологического состояния. Показаны преимущества и место трансторакальной эхокардиографии в неинвазивной диагностике гемодинамического варианта легочной гипертензии с помощью определения максимальной скорости раннего диастолического наполнения левого желудочка (Е) и максимальной скорости раннего диастолического смещения латерального сегмента кольца митрального клапана (е') по формуле Nagueh. В статье представлены клинические случаи, демонстрирующие возможности трансторакальной эхокардиографии в выявлении легочной гипертензии, определении ее гемодинамического типа. Определение гемодинамического типа легочной гипертензии неинвазивными методами позволяет проводить дальнейший дифференциально-диагностический поиск только среди причин установленного типа легочной гипертензии, что сокращает диагностический путь, экономит время и затраты на диагностику и позволяет своевременно приступить к лечению.
Ключевые слова: легочная гипертензия, хроническая тромбоэмболическая легочная гипертензия, хроническая тромбоэмболическая болезнь легких, эхокардиография, давление заклинивания легочной артерии, легочное сосудистое сопротивление, прекапиллярный тип, посткапиллярный тип.
Для цитирования: Усачева Е.В., Надей Е.В., Шкиринец А.В., Канунникова О.И., Ботвинко И.Ю., Наконечная Е.Э. Эхокардиография в дифференциальной диагностике причин легочной гипертензии на примере клинических случаев. Клинический разбор в общей медицине. 2025; 6 (3): 47–54. DOI: 10.47407/kr2024.6.3.00581
Значимость своевременной диагностики легочной гипертензии в условиях первичного звена здравоохранения трудно переоценить, поскольку это состояние характеризуется низким уровнем 5-летней выживаемости, отличается сложностью установления диагноза, низкой настороженностью и недостаточной информированностью клиницистов о данном заболевании. В статье представлены основные методы диагностики легочной гипертензии, приведены данные, характерные для трех гемодинамических типов легочной гипертензии. Наиболее широко из инструментальных методов представлена эхокардиографическая диагностика легочной гипертензии, поскольку метод является доступным для врача первичного звена и позволяет выделить пациентов, нуждающихся в направлении на дообследование с помощью инвазивных технологий. Обозначена роль и значимость измерения скорости трикуспидальной регургитации 2,8 м/с в диагностике данного патологического состояния. Показаны преимущества и место трансторакальной эхокардиографии в неинвазивной диагностике гемодинамического варианта легочной гипертензии с помощью определения максимальной скорости раннего диастолического наполнения левого желудочка (Е) и максимальной скорости раннего диастолического смещения латерального сегмента кольца митрального клапана (е') по формуле Nagueh. В статье представлены клинические случаи, демонстрирующие возможности трансторакальной эхокардиографии в выявлении легочной гипертензии, определении ее гемодинамического типа. Определение гемодинамического типа легочной гипертензии неинвазивными методами позволяет проводить дальнейший дифференциально-диагностический поиск только среди причин установленного типа легочной гипертензии, что сокращает диагностический путь, экономит время и затраты на диагностику и позволяет своевременно приступить к лечению.
Ключевые слова: легочная гипертензия, хроническая тромбоэмболическая легочная гипертензия, хроническая тромбоэмболическая болезнь легких, эхокардиография, давление заклинивания легочной артерии, легочное сосудистое сопротивление, прекапиллярный тип, посткапиллярный тип.
Для цитирования: Усачева Е.В., Надей Е.В., Шкиринец А.В., Канунникова О.И., Ботвинко И.Ю., Наконечная Е.Э. Эхокардиография в дифференциальной диагностике причин легочной гипертензии на примере клинических случаев. Клинический разбор в общей медицине. 2025; 6 (3): 47–54. DOI: 10.47407/kr2024.6.3.00581
Echocardiography in the differential diagnosis of the causes of pulmonary hypertension on the example of clinical cases
Elena V. Usacheva1, Elena V. Nadey1, Anastasia V. Shkirinets (Nelidova)1, Olesya I. Kanunnikova1,Irina Yu. Botvinko2, Ekaterina E. Nakonechnaya3
1 Omsk State Medical University, Omsk, Russia;
2 Omsk region Clinical medical and sanitary unit No. 7, Omsk, Russia;
3 Omsk region Clinical cardiology dispensary, Omsk, Russia
ElenaV.Usacheva@yandex.ru
Abstract
The importance of timely diagnosis of pulmonary hypertension in primary health care is difficult to overestimate, since this condition is characterized by a low five-year survival rate, is characterized by difficulty in establishing a diagnosis, low alertness and insufficient awareness of clinicians about this disease. The article presents the main methods of diagnosis of pulmonary hypertension, provides data typical for three hemodynamic types of pulmonary hypertension. Echocardiographic diagnosis of pulmonary hypertension is the most widely used instrumental method, since the method is accessible to a primary care physician and allows identifying patients who need to be referred for further examination using invasive technologies. The role and significance of measuring the rate of tricuspid regurgitation of 2.8 m/s in the diagnosis of this pathological condition is indicated. The advantages and place of transthoracic echocardiography in the noninvasive diagnosis of the hemodynamic variant of pulmonary hypertension are shown by determining the maximum rate of early diastolic filling of the left ventricle (E) and the maximum rate of early diastolic displacement of the lateral segment of the mitral valve ring (e') according to the Nagueh formula. The article presents clinical cases demonstrating the capabilities of transthoracic echocardiography in detecting pulmonary hypertension and determining its hemodynamic type. The determination of the hemodynamic type of pulmonary hypertension by noninvasive methods allows for further differential diagnostic search only among the causes of the established type of pulmonary hypertension, which shortens the diagnostic pathway, saves time and costs for diagnosis and allows timely treatment.
Keywords: pulmonary hypertension, chronic thromboembolic pulmonary hypertension, chronic thromboembolic lung disease, echocardiography, pulmonary artery jamming pressure, pulmonary vascular resistance, precapillary type, postcapillary type.
For citation: Usacheva E.V., Nadey E.V., Shkirinets A.V., Kanunnikova O.I., Botvinko I.U., Nakonechnaia E.E. Echocardiography in the
differential diagnosis of the causes of pulmonary hypertension on the example of clinical cases. Clinical review for general practice. 2025; 6 (3): 47–54 (In Russ.). DOI: 10.47407/kr2024.6.3.00581
Введение
Легочная гипертензия (ЛГ) – это термин, используемый для описания патологического состояния, характеризующегося аномально высоким давлением в легочной артерии (ЛА) [1, 2]. Значимость проблемы ЛГ и ее своевременной диагностики в условиях первичного звена здравоохранения трудно переоценить, поскольку ЛГ является состоянием с крайне низким уровнем5-летней выживаемости [3].
ЛГ может возникнуть как одно из отдаленных осложнений тромбоэмболии ЛА и в таком случае трактуется как хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) [4–6]. ХТЭЛГ – это прекапиллярная форма ЛГ, причиной которой является наличие организованных (хронических) окклюзирующих или неокклюзирующих тромботических масс в ЛА (главных, долевых, сегментарных, субсегментарных артериях) в течение не менее трех месяцев после эпизода тромбоэмболии и развитие дистальной легочной васкулопатии [1, 7]. Отличительной особенностью ХТЭЛГ является неравномерность поражения сосудистого легочного русла и в большинстве случаев наличие взаимосвязи с тромбозом периферических вен [8].
По разным данным, распространенность ХТЭЛГ составляет от 2 до 40 случаев на 1 млн человек [9, 1], но точных данных по эпидемиологии данного заболевания нет, при этом очевидно, что оно распространено гораздо шире, чем принято считать [10]. ХТЭЛГ следует подозревать у каждого пациента с симптомами и признаками ЛГ неясного генеза даже при отсутствии перенесенного эпизода тромбоэмболии ЛА (ТЭЛА). Сложности в установлении диагноза во многом связаны с самим заболеванием, а именно с неспецифической клинической картиной, однако, имеет значение и низкая настороженность врачей в отношении ХТЭЛГ [11], и недостаточная информированность клиницистов о данном заболевании [5, 6].
Принципы параклинической диагностики хронической тромбоэмболической легочной гипертензии
Лабораторные маркеры. Тактика лабораторного обследования при подозрении на ХТЭЛГ определяется тем, что в основе заболевания лежит тромбофилическое состояние. Для выявления тромбофилии и предрасполагающих к ней заболеваний, проводят как общеклиническое обследование (общий и биохимический общетерапевтический анализы крови), исследование кислотно-основного состояния и газов крови, так и оценку данных коагулограммы, в том числе D-димера. При выявлении в процессе скрининговых исследований изменений в системе гемостаза либо при наличии рецидивирующих тромботических событий проводится расширенное исследование системы гемостаза [12].
NT-proBNP – предшественник мозгового натрийуретического пептида – это биомаркер, рекомендуемый для оценки наличия правожелудочковой сердечной недостаточности, определения функционального статуса пациента с подтвержденной идиопатической ЛГ (ЛАГ) и для оценки прогноза и эффективности проводимой ЛАГ-специфической терапии [1, 8, 13].
Инструментальная диагностика при подозрении на ХТЭЛГ выполняется в несколько этапов и на первом этапе проводятся скрининговые методы исследования – электрокардиография (ЭКГ) и трансторакальная эхокардиография (ТТ-ЭхоКГ), прицельная рентгенография органов грудной клетки, исследование функции внешнего дыхания. Далее проводят мультиспиральную компьютерную томографию легких с контрастированием бассейна ЛА (МСКТ ОГК), вентиляционно-перфузионную сцинтиграфию и катетеризацию правых отделов сердца.
ЭКГ – обязательный метод диагностики у больных с подозрением на наличие ХТЭЛГ при первичном обследовании и в процессе динамического наблюдения [1]. Этот метод позволяет выявить признаки гипертрофии и перегрузки правого желудочка (ПЖ), дилатации и гипертрофии правого предсердия (р-pulmonale).
ЭКГ-признаки гипертрофии ПЖ, а именно увеличение амплитуды зубца R и соотношения R/S в правых отведениях, имеют недостаточную чувствительность (55%) и специфичность (70%), чтобы быть использованными в качестве скрининговых, тогда как признаки перегрузки ПЖ (преходящее смещение сегмента RS-T и сглаженность или инверсия Т в правых грудных отведениях) являются более чувствительными. Следует отметить, что такие ЭКГ-признаки, как расширение комплекса QRS и удлинение интервала QT свидетельствуют о тяжести ЛГ и ассоциированы с неблагоприятным прогнозом [14]. Неоспоримым преимуществом метода является его простота, доступность и низкая стоимость, но ЭКГ-признаки поражения правых отделов сердца определяются уже в развернутой стадии болезни, что снижает диагностическую ценность данного метода [15].
ТТ-ЭхоКГ – основной метод на этапе диагностического поиска, ценность которого обусловлена тем, что ТТ-ЭхоКГ позволяет не только оценить уровень давления в ЛА, но и установить наличие заболеваний, приводящих к развитию ЛГ, в первую очередь пороков сердца [15, 16].
МСКТ ОГК, а именно КТ-ангиопульмонография – наиболее информативный метод визуализации в диагностике ХТЭЛГ, позволяющий оценить структуру легочного русла, наличие тромботических масс и их локализацию. МСКТ-картина хронической тромбоэмболии может быть представлена окклюзиями и стенозами ЛА, а также эксцентрическими дефектами наполнения вследствие наличия тромбов, в том числе реканализованных [17]. По результатам МСКТ ОГК можно заподозрить наличие ЛГ, идентифицировать причину ЛГ (например, ХТЭЛГ или заболевание легких), выявить признаки ЛАГ-ассоциированных состояний (например, дилатация пищевода при системной склеродермии или наличие порока сердца) [18]. Поэтому проведение
КТ-ангиопульмонографии рекомендуется всем пациентам с ЛГ для выявления причины заболевания [19, 20].
Вентиляционно-перфузионная сцинтиграфия (ВПС) легких является одним из методов, позволяющих исключить тромбоэмболический генез ЛГ. При наличии подозрения на ХТЭЛГ и неинформативности
ТТ-ЭхоКГ, ВПС является исследованием выбора, она обладает 96–100% чувствительностью и 86–95% специфичностью для выявления признаков ХТЭЛГ и не обладает нефротоксичностью. Множественные дефекты перфузии с сохраненной вентиляционной функцией – характерные признаки ХТЭЛГ. Однако, учитывая стоимость и радиационную нагрузку, ВПС не может быть рекомендована в качестве скрининга ХТЭЛГ [21].
Чрезвенозная катетеризация сердца (ЧВКС). «Золотым стандартом» диагностики ЛГ считается выполнение малоинвазивного вмешательства – ЧВКС.
В соответствии с современными рекомендациями, диагноз ЛГ устанавливается при уровне среднего давления в ЛА (ДЛА) более 20 мм рт. ст., измеренного при ЧВКС в покое. По результатам ЧВКС можно определить гемодинамический вариант ЛГ – прекапиллярная или посткапиллярная, и определить дальнейшую тактику ведения пациента. Гемодинамическими критериями прекапиллярного варианта ЛГ служат: среднее ДЛА>20 мм рт. ст., давление заклинивания ЛА (ДЗЛА)≤15 мм рт. ст., легочное сосудистое сопротивление (ЛСС)>2 ед. Вуда при наличии множественных стенозирующих и/или окклюзирующих поражений ветвей ЛА различного калибра. ЧВКС является инвазивной процедурой, информативность и безопасность которой основывается на четырех принципах: рациональном выборе венозного доступа, тщательной калибровке датчика давления, соблюдении правил измерения ДЗЛА и расчете сердечного выброса [6, 12]. Недостатками метода являются необходимость введения больших объемов контрастного вещества, недостаточное контрастирование верхнедолевых ветвей, необходимость наличия специального оборудования и квалифицированных опытных специалистов.
Эхокардиографическая диагностика легочной гипертензии
На уровне первичного звена здравоохранения ТТ-ЭхоКГ является неинвазивным, информативным и доступным методом диагностики ЛГ. Доказана хорошая сопоставимость результатов ТТ-ЭхоКГ с данными ЧВКС. Учитывая, что ЧВКС является инвазивной процедурой, которая проводится на базе экспертного центра, ТТ-ЭхоКГ идеально подходит для динамического наблюдения пациента. Обнаружение пороков сердца (септальные дефекты, открытый артериальный проток, аномальный дренаж легочных вен, сложные врожденные пороки сердца), как наиболее частой причины ЛГ, является одной из важных задач в дифференциально-диагностическом алгоритме при проведении ТТ-ЭхоКГ.
ЭхоКГ-диагностика ЛГ включает расчет давления в ЛА, а также оценку дополнительных признаков, к которым относят размеры правых отделов сердца, дисфункцию ПЖ и диаметр ЛА [12]. Наиболее значимый вклад в оценку ЛГ вносят допплерографические методики, с измерением систолического, диастолического и среднего давления в ЛА с помощью непрерывно-волнового допплера по скорости регургитации на трикуспидальном и пульмональном клапанах [1].
Определение систолического ДЛА при проведении ТТ-ЭхоКГ основано на оценке показателей трикуспидальной регургитации (ТР), обусловленной наличием градиента давления между ПЖ и правым предсердием (ПП) в фазу систолы. Следует отметить, что в рутинной практике определение среднего ДЛА и диастолического ДЛА по данным ТТ-ЭхоКГ практически не используется, однако их расчет может быть применен в случаях, когда в силу тех или иных причин расчет ДЛА затруднен. В зависимости от величин систолического, среднего и диастолического ДЛА, ЛГ подразделяют на умеренную, высокую и значительную. Выделение степеней тяжести ЛГ необходимо для определения тактики ведения пациента и скорости принятия решений в конкретный период времени. Пороговые значения выраженности ЛГ приведены в табл. 1 [22].

Измерение ДЛА по ТР и легочной регургитации может быть сопряжено с получением как завышенных, так и заниженных значений этого показателя в силу различных причин (несоблюдение правил допплерометрического исследования, выраженная дилатация правых отделов сердца, эмпирическая оценка давления в ПП и др.). В связи с этим современные согласительные документы вместо степеней ЛГ при проведении
ТТ-ЭхоКГ на начальном этапе обследования рекомендуют оценивать вероятность наличия ЛГ, которая может быть определена как низкая, средняя или высокая [1].
С этой целью экспертами был предложен диагностический алгоритм, в котором в качестве начального критерия оценки необходимо использовать скорость ТР.
Пограничным значением в диагностике ЛГ является скорость ТР 2,8 м/с, что соответствует градиенту давления 31 мм рт. ст. В силу того, что скорость ТР далеко не всегда отражает степень повышения давления в ЛА, при определении вероятности ЛГ необходимо также принимать во внимание ряд дополнительных признаков,
отражающих морфологические и функциональные показатели. В современных рекомендациях по диагностике и лечению ЛГ эти признаки разделены на 3 группы (табл. 2).

Во всех случаях, когда скорость ТР не превышает значения 2,8 м/с и нет дополнительных ЭхоКГ-признаков, вероятность ЛГ расценивается как низкая. О средней вероятности ЛГ свидетельствует увеличение скорости ТР в пределах 2,9–3,4 м/с при отсутствии дополнительных критериев ЛГ, а также нормальная скорость ТР при наличии дополнительных признаков, относящихся по меньшей мере к двум из трех групп, перечисленных выше. Если же скорость ТР превышает 3,4 м/с, вне зависимости от наличия или отсутствия дополнительных признаков вероятность ЛГ считают высокой, как и в случаях, когда скорость ТР имеет промежуточные значения (2,9–3,4 м/с) в сочетании с дополнительными признаками ЛГ. Предложенный диагностический алгоритм позволяет выделить категорию пациентов, которые нуждаются в дальнейшем детальном обследовании для верификации ЛГ с применением более сложных методов исследования, в том числе ЧВКС.
Несомненным преимуществом ТТ-ЭхоКГ является возможность неинвазивного определения гемодинамического варианта ЛГ. На сегодняшний день предложены формулы, позволяющие по данным допплерометрии рассчитать значения ДЗЛА и ЛСС.
Для расчета ДЗЛА используется формула Nagueh [23]: ДЗЛА = 1,24 × Е/е' + 1,9, где E – максимальная скорость раннего диастолического наполнения левого желудочка (ЛЖ), е' – максимальная скорость раннего диастолического смещения латерального сегмента кольца митрального клапана.
ЛСС рассчитывается по формуле: (среднее ДЛА – ДЗЛА)/сердечный выброс, и измеряется в единицах Вуда. Наиболее часто в эхокардиографической оценке ЛСС используется формула, которая была предложена A.E. Abbas и соавт. в 2003 г. [24]: ЛСС = (Vтр/VTIвтпж × ×10)+0,16, где Vтр – максимальная скорость ТР, а VTIвтпж – интеграл скорости кровотока в выносящем тракте ПЖ.
Место эхокардиографии в дифференциальной диагностике форм легочной гипертензии на примере клинических случаев
Клинический случай 1. Пациент Ф., 74 лет, обратился к врачу-пульмонологу в апреле 2024 г. после эпизода кровохарканья с жалобами на кашель с отхождением мокроты серого цвета с прожилками крови до 10 мл, инспираторную одышку при умеренных физических нагрузках. Из анамнеза известно, что первое кровохарканье было в январе 2022 г., когда был госпитализирован с острым флеботромбозом слева и инфаркт-пневмонией, затем в марте 2024 г. вновь госпитализация с острым флеботромбоз справа, рецидивирующим тромбозом слева с развитием инфаркт-пневмонии слева, кровохарканьем. После выписки осмотрен врачом-пульмонологом для решения вопроса о приеме антикоагулянтов. При физикальном исследовании тоны сердца приглушены, ритмичные, акцент II тона над ЛА, на верхушке короткий, систолический шум, иррадиирует вдоль левого края грудины вверх. Выставлен предварительный диагноз: состояние после рецидивирующей ТЭЛА мелких ветвей ЛА с развитием инфаркт-пневмонии (январь 2022 г., март 2024 г.), кровохарканье (январь 2022 г., март 2024 г.). С учетом наличия одышки, кровохарканья в анамнезе и акцента второго тона на ЛА была заподозрена ЛГ. Рекомендовано дообследование для исключения иных причин кровохарканья: ТТ-ЭхоКГ (исключение недостаточности левых отделов сердца), исследование мокроты на кислотоустойчивые микобактерии (КУМ) и атипичные клетки, фибробронхоскопия с исследованием бронхоальвеолярного лаважа на атипичные клетки, цитологию, КУМ и консультация фтизиатра (для исключения туберкулеза и новообразования как причины кровохарканья). По результатам проведенного обследования выявлены признаки митральной регургитации 1-й степени при нормальных размерах левых отделов сердца и сохранной фракции выброса ЛЖ, что исключало патологию левых отделов сердца как причину кровохарканья. Выявлены признаки ТР 2-й степени с уровнем систолического ДЛА 35 мм рт. ст., при нормальных размерах ПЖ и ПП, при отсутствии признаков дисфункции ПЖ (TAPSE 27 мм), что исключало наличие ЛГ у данного пациента. Туберкулез и новообразования органов дыхания также были исключены. С учетом тромботического анамнеза, наличия кровохарканья у пациента без признаков ЛГ, заподозрена хроническая тромбоэмболическая болезнь легких (ХТЭБЛ), в связи с чем пациент был направлен на МСКТ ОГК с контрастированием. 24.04.2024 по данным МСКТ ОГК: ствол ЛА – 27 мм, левая ветвь – 22 мм, правая ветвь – 23 мм, в просвете передней сегментарной ветви правой верхнедолевой ЛА и в устье нижнедолевой ветви левой ЛА определяются тромботические массы с зонами поствоспалительного пневмофиброза в нижних долях обоих легких. Таким образом, у пациента в возрасте старше 70 лет ЛГ при высокой ее вероятности была исключена по данным ТТ-ЭхоКГ. Наличие по данным МСКТ ОГК признаков ХТЭБЛ при отсутствии ЛГ свидетельствует о высоких компенсаторных возможностях организма, благодаря которым при наличии признаков обструкции ветвей ЛА ЛГ не развилась. Подтверждение ХЭТБЛ позволило принять решение о продолжении приема антикоагулянтов с целью профилактики рецидива ТЭЛА и необходимости проведения контрольной ТТ-ЭхоКГ не реже чем 1 раз в год в течение трех лет для оценки состояния правых отделов сердца и давления в ЛА.
Клинический случай 2. Пациентка С., 65 лет, в феврале 2024 г. обратилась к врачу-пульмонологу с жалобами на одышку, возникающую во время физической нагрузки по интенсивности несколько выше бытового уровня, сопровождается болью за грудиной давящей, жгучей, однократно в ответ на нитроглицерин возникло предобморочное состояние, при этом боль и одышка не купировались, в связи с чем более нитроглицерин не использовала. Считает себя больной с ноября 2020 г., когда после перенесенной новой коронавирусной инфекции с тяжелой пневмонией, в объеме 55% поражения легочной ткани, появилась одышка. В сентябре 2023 г. в связи с сохраняющейся одышкой обратилась к пульмонологу, предоставив МСКТ ОГК от 06.04.2023. Пульмонологом заболевание органов дыхания исключено, назначено проведение повторной консультации кардиолога. Четыре месяца пациентка за медицинской помощью не обращалась, получала лечение амбулаторно в объеме вторичной кардиоваскулярной профилактики. Во второй половине января 2024 г. стала отмечать появление загрудинных болей в ответ на физическую нагрузку, в силу чего появился страх выходить на улицу, 29.01.2024 в связи с интенсивными болями была по неотложной помощи госпитализирована в кардиологическое отделение, где были выявлены признаки ЛГ, высокий уровень Д-димера при интактных коронарных артериях, по результатам выписки амбулаторно направлена на дообследование для уточнения генеза ЛГ. В стационарных условиях были определены традиционные параметры ТТ-ЭХОКГ, не позволяющие рассчитать ДЗЛА и ЛСС, и, соответственно, определить тип ЛГ. С учетом высокого уровня Д-димера и наследственного отягощенного анамнеза по тромботическим событиям (мама пациентки в 55 лет умерла от массивной ТЭЛА) была заподозрена ХТЭЛГ, амбулаторно выполнена МСКТ ОГК с ангиографией легочных сосудов (апрель 2024 г.), по данным которой признаков тромбоза ветвей ЛА не выявлено, но подтверждены признаки ЛГ в виде увеличения диаметра легочного ствола до 38 мм (диаметр аорты 34 мм), признаки единичных очагов локального фиброза легких с обеих сторон по сравнению с МСКТ ОГК от 06.04.2023 без динамики. Поскольку при установлении причины ЛГ круг диагностического поиска определяется формой ЛГ (прекапиллярная/посткапиллярная), пациентка повторно была направлена на ТТ-ЭхоКГ с оценкой параметров, необходимых для расчета ДЗЛА и ЛСС, и на основании этого выбора пути диагностического поиска. Данные ТТ-ЭхоКГ пациентки С. представлены в табл. 3.

Известно, что для установления формы ЛГ в условиях первичного звена здравоохранения и отбора пациентов на проведение ЧВКС предлагается использование расчетных ДЗЛА и ЛСС, которые в допустимой степени эквивалентны данным ЧВКС. На основании результатов ТТ-ЭхоКГ нами рассчитаны ДЗЛА и ЛСС:
ДЗЛА = 1,24 × Е/е' + 1,9 = 1,24 × 0,5/0,05 + 1,9 = 14,3
ЛСС = (Среднее ДЛА – ДЗЛА)/сердечный выброс = (80 – 14,3)/4,5 = 14,6.
Рассчитанные ДЗЛА и ЛСС указывали на прекапиллярный генез ЛГ у данной пациентки. Установление прекапиллярного генеза ЛГ позволило исключить патологию левых отделов сердца как причину ЛГ и продолжить дифференциально-диагностический поиск среди причин прекапиллярной ЛГ. Пациентка повторно была приглашена на прием, во время которого выявлены признаки синдрома Рейно, поэтому приоритетным стало исключение системного заболевания соединительной ткани как причины ЛГ. При обследовании выявлена позитивность по антинуклеарному фактору – 5120 с типом свечения АС21 и АС3 (при норме до 160), антитела к центромере, в связи с чем пациентка была направлена к ревматологу, который по совокупности данных выставил диагноз «системная склеродермия». Таким образом, ТТ-ЭхоКГ, позволяя рассчитать ДЗЛА и ЛСС, помогает сузить круг исследований, необходимых для установления диагноза, сократить сроки диагностического поиска и своевременно приступить к патогенетическому лечению ЛГ.
Заключение
Одышка – наиболее частый симптом, являющийся поводом обращения к врачу в условиях первичного звена здравоохранения. Несмотря на то что распространенность одышки выше у лиц пожилого возраста, дифференциальный ряд должен включать ЛГ, как причину длительно сохраняющейся и постепенно нарастающей одышки, независимо от возраста пациента.Стойкая ЛГ всегда сопровождается необратимым ремоделированием сосудов с последующей их обструкцией и ригидностью. Без своевременно начатого лечения это приводит к гипертрофии и недостаточности ПЖ, что является основной причиной смерти. Регистры ЛГ сообщают о выживаемости от 68% до 93% через 1 год и от 39% до 77% через 3 года, 12-месячная смертность у пациентов с ЛГ, ассоциированной с патологией левых отделов сердца, достигает 32%, а предикторами худшего прогноза являются нарушение функции почек, анемия, пожилой возраст, дисфункция ПЖ и наличие комбинированного посткапиллярного и прекапиллярного варианта ЛГ, а не изолированного посткапиллярного [25].
Окончательному диагнозу предшествует поэтапное обследование пациента, которое при наличии показаний завершается ЧВКС. В связи с ограниченной доступностью ЧВКС на уровне первичного звена здравоохранения показания к этому исследованию должны быть определены на предварительном этапе обследования. Диагностическая тактика предварительного этапа определяется вариантом ЛГ – прекапиллярный или посткапиллярный. Представленные клинические случаи демонстрируют возможности применения расчетных показателей – ДЗЛА и/или ЛСС на основании параметров ТТ-ЭхоКГ для выбора диагностической тактики. ТТ-ЭхоКГ доступна на уровне первичного звена здравоохранения в каждом регионе. На сегодняшний день большинство протоколов ТТ-ЭхоКГ не содержат данных о скорости ТР и не позволяют рассчитать ДЗЛА и ЛСС. Поэтому необходимо совместное с врачами функциональной диагностики обсуждение и включение в протокол ТТ-ЭхоКГ измерения скорости ТР при ее наличии. При скорости ТР более 2,8 м/с – обязательное измерение размеров и оценка функции правых отделов сердца для раннего выявления ЛГ:
• соотношение ПЖ/ЛЖ на базальном уровне;
• TAPSE;
• скорость начальной диастолической легочной регургитации;
• время ускорения в выносящем тракте ПЖ;
• интеграл линейной скорости потока в выносящем тракте ПЖ;
• максимальная скорость раннего диастолического наполнения ЛЖ (Е);
• максимальная скорость раннего диастолического смещения латерального сегмента кольца митрального клапана (е');
• частота сердечных сокращений.
Использование такой технологии позволит осуществлять раннюю диагностику и лечение ЛГ, снизить инвалидизацию и смертность населения с данным патологическим состоянием.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Усачева Елена Владимировна – канд. мед. наук, доц., доц. каф. внутренних болезней и семейной медицины ДПО, ФГБОУ ВО ОмГМУ. E-mail: elenav.usacheva@yandex.ru; ORCID: 0000-0002-6134-1533: Researcher ID: I-4077-2017: Scopus Author ID: 56380398700
Elena V. Usacheva – Cand. Sci. (Med.), Assoc. Prof., Omsk State Medical University. E-mail: elenav.usacheva@yandex.ru; ORCID: 0000-0002-6134-1533; Researcher ID: I-4077-20174; Scopus Author ID: 56380398700
Надей Елена Витальевна – канд. мед. наук, доц., доц. каф. внутренних болезней и семейной медицины ДПО, ФГБОУ ВО
ОмГМУ. E-mail: nadeyelena@yandex.ru, ORCID: 0000-0003-0440-7118
Elena V. Nadey – Cand. Sci. (Med.), Assoc. Prof., Omsk State
Medical University. E-mail: nadeyelena@yandex.ru; ORCID: 0000-0003-0440-7118
Шкиринец (Нелидова) Анастасия Владимировна – канд. мед. наук, доц., доц. каф. пропедевтики внутренних болезней, ФГБОУ ВО ОмГМУ. E-mail: avnelidova@mail.ru; ORCID: 0000-0003-0149-6119; Researcher ID: B-8428-2017; SPIN-код: 1506-3007; Scopus Author ID: 631273
Anastasia V. Shkirinets (Nelidova) – Cand. Sci. (Med.), Assoc. Prof., Omsk State Medical University. E-mail: avnelidova@mail.ru; ORCID: 0000-0003-0149-6119; Researcher ID: B-8428-2017; SPIN-код: 1506-3007; Scopus Author ID: 631273
Канунникова Олеся Игорьевна – канд. мед. наук, ассистент каф. внутренних болезней и семейной медицины ДПО, ФГБОУ ВО ОмГМУ. E-mail: lesia.tch@yandex.ru; ORCID: 0009-0003-3721-4379; Researcher ID: LDF-2487-2024; Scopus Author ID: 56512463200
Olesya I. Kanunnikova – Cand. Sci. (Med.), Аssistant, Omsk State Medical University. E-mail: lesia.tch@yandex.ru; ORCID: 0009-0003-3721-4379; Researcher ID: LDF-2487-2024; Scopus Author ID: 56512463200
Ботвинко Ирина Юрьевна – врач функциональной диагностики, БУЗОО «КМСЧ №7». E-mail: irinabotvinko@mail.ru
Irina Yu. Botvinko – Doctor of functional diagnostics, Clinical medical and sanitary unit No. 7. E-mail: mail irinabotvinko@mail.ru
Наконечная Екатерина Эдуардовна – врач-ревматолог, зав. ревматологическим отделением, БУЗОО «Клинический кардиологический диспансер». E-mail: eka_giz@mail.ru
Ekaterina E. Nakonechnaya – Rheumatologist, Clinical Cardiological Dispensary. E-mail: eka_giz@mail.ru
Поступила в редакцию: 11.02.2025
Поступила после рецензирования: 19.02.2025
Принята к публикации: 27.02.2025
Received: 11.02.2025
Revised: 19.02.2025
Accepted: 27.02.2025
Список исп. литературыСкрыть список1. Авдеев С.Н., Барбараш О.Л., Валиева З.С. и др. Легочная гипертензия, в том числе хроническая тромбоэмболическая легочная гипертензия. Клинические рекомендации 2024. Российский кардиологический журнал. 2024;29(11):6161. DOI: 10.15829/1560-4071-2024-6161
Avdeev S.N., Barbarash O.L., Valieva Z.S. et al. Pulmonary hypertension, including chronic thromboembolic pulmonary hypertension. Clinical guidelines 2024. Russian Journal of Cardiology. 2024;29(11):61. DOI: 10.15829/1560-4071-2024-61 (in Russian).
2. Poch D, Mandel J. Pulmonary Hypertension. Ann Intern Med 2021;174(4):ITC49-ITC64.
3. Johnson S, Sommer N, Cox-Flaherty K et al. Pulmonary Hypertension: A Contemporary Review. Am J Respir Crit Care Med 2023;208(5):528-48.
4. Opitz I, Ulrich S. Chronic thromboembolic pulmonary hypertension. Swiss Med Wkly 2018 Dec 21;148:w14702.
5. Чернявский А.М., Едемский А..Г, Васильцева О.Я. и др. Хроническая тромбоэмболическая легочная гипертензия: эпидемиология, диагностика, лечение – современное состояние проблемы. Вестник Российской академии медицинских наук. 2023;78(4):297-304.
Chernyavsky A.M., Edemsky A..G., Vasiltseva O.Ya. et al. Chronic thromboembolic pulmonary hypertension: epidemiology, diagnosis, treatment – the current state of the problem. Bulletin of the Russian Academy of Medical Sciences. 2023;78(4):297-304 (in Russian).
6. Чазова И.Е., Мартынюк Т.В. Клинические рекомендации по диагностике и лечению хронической тромбоэмболической легочной гипертензии (I часть). Терапевтический архив. 2016;88(9):90-101.
Chazova I.E., Martynyuk T.V. Clinical guidelines for the diagnosis and treatment of chronic thromboembolic pulmonary hypertension (Part I). Therapeutic Archive. 2016;88(9):90-101 (in Russian).
7. Simonneau G, Dorfmüller P, Guignabert C et al. Chronic thromboembolic pulmonary hypertension: the magic of pathophysiology. Ann Cardiothorac Surg 2022;11(2):106-19.
8. Gerges M, Yacoub M. Chronic thromboembolic pulmonary hypertension – still evolving. Glob Cardiol Sci Pract 2020;2020(1):e202011.
9. Чазова И.Е., Чернявский А.М., Мартынюк Т.В. и др. Актуальные вопросы хронической тромбоэмболической легочной гипертензии: мнение экспертов. Кардиологический вестник. 2015;10(1):78-9.
Chazova I.E., Chernyavsky A.M., Martynyuk T.V. et al. Topical issues of chronic thromboembolic pulmonary hypertension: expert opinion. Cardiological Bulletin. 2015;10(1):78-9 (in Russian).
10. Al-Qadi M, LeVarge B, Ford HJ. Epidemiology, Pathogenesis, and Clinical Approach in Group 5 Pulmonary Hypertension. Front Med (Lausanne). 2021;7:616720.
11. Чернявский А.М., Новикова Н.В., Едемский А.Г. и др. Хроническая тромбоэмболическая легочная гипертензия: сложные аспекты диагностики и лечения. Медицинский алфавит. 2015;2(10):5-9.
Chernyavsky A.M., Novikova N.V., Edemsky A.G. et al. Chronic thromboembolic pulmonary hypertension: complex aspects of diagnosis and treatment. Medical Alphabet. 2015;2(10):5-9 (in Russian).
12. Humbert M, Kovacs G, Hoeper MM et al. ESC/ERS Scientific Document Group. 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension Developed by the task force for the diagnosis and treatment of pulmonary hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS). Endorsed by the International Society for Heart and Lung Transplantation (ISHLT) and the European Reference Network on rare respiratory diseases (ERN-LUNG). Eur Heart J 2022;43(38):3618-731.
13. Шостак Н.А., Клименко А.А., Шеменкова В.С. и др. Современный алгоритм диагностики хронической тромбоэмболический легочной гипертензии. Терапия. 2019;4(30):113-20.
Shostak N.A., Klimenko A.A., Shemenkova V.S. et al. A modern algorithm for the diagnosis of chronic thromboembolic pulmonary hypertension. Therapy. 2019;4(30):113-20 (in Russian).
14. Ryan JJ, Archer SL. The right ventricle in pulmonary arterial hypertension: disorders of metabolism, angiogenesis and adrenergic signaling in right ventricular failure. Circ Res 2014;115(1):176-88.
15. Чазова И.Е. Хроническая тромбоэмболическая легочная гипертензия: современные возможности диагностики и лечения. Терапевтический архив. 2023;95(12):1017-21.
Chazova I.E. Chronic thromboembolic pulmonary hypertension: modern diagnostic and treatment options. Therapeutic Archive. 2023;95(12):1017-21 (in Russian).
16. Шостак НА, Kлименко АА, Демидова НА и др. Хроническая тромбоэмболическая легочная гипертензия – подходы к диагностике и лечению. Медицинский совет. 2013;9:10-6.
Shostak NA, Klimenko AA, Demidova NA et al. Chronic thromboembolic pulmonary hypertension – approaches to diagnosis and treatment. Medical advice. 2013;9:10-6 (in Russian).
17. He J, Fang W, Lev B et al. Diagnosis of chronic thromboembolic pulmonary hypertension: comparison of ventilation/perfusion scanning and multidetector computed tomography pulmonary angiography with pulmonary angiography. Nucl Med Commun 2012;33(5):459-63.
18. Rajaram S, Swift AJ, Condliffe R et al. CT features of pulmonary arterial hypertension and its major subtypes: a systematic CT evaluation of 292 patients from the ASPIRE Registry. Thorax 2015;70(4):382-7.
19. Frost A, Badesch D, Gibbs JSR et al. Diagnosis of pulmonary hypertension. Eur Respir J 2019;53(1):1801904.
20. Kim NH, Delcroix M, Jais X et al. Chronic thromboembolic pulmonary hypertension. Eur Respir J 2019;53(1):1801915.
21. Cosmi B, Nijkeuter M, Valentino M et al. Residual emboli on lung perfusion scan or multidetector computed tomography after a first episode of acute pulmonary embolism. Intern Emerg Med 2011;6(6):521-28.
22. Рыбакова М.К., Алехин М.Н., Митьков В.В. Практическое руководство по ультразвуковой диагностике. Эхокардиография. М.: Видар, 2008.
Rybakova M.K., Alyokhin M.N., Mitkov V.V. Practical guide to ultrasound diagnostics. Echocardiography. Moscow: Vidar, 2008 (in Russian).
23. Nagueh SF, Middleton KJ, Kopelen HA et al. Doppler tissue imaging: a noninvasive technique for evaluation of left ventricular relaxation and estimation of filling pressures. J Am Coll Cardiol 1997;30:1527-33.
24. Abbas AE, Fortuin FD, Schiller NB et al. A simple method for noninvasive estimation of pulmonary vascular resistance. J Am Coll Cardiol 2003;41:1021-7.
25. Mandras SA, Mehta HS, Vaidya A. Pulmonary Hypertension: A Brief Guide for Clinicians. Mayo Clin Proc. 2020;95(9):1978-88.


