Клинический разбор в общей медицине №6 2025
1 Russian University of Medicine (ROSUNIMED), Moscow, Russia;
2 Loginov Moscow Clinical Research Center, Moscow, Russia
lena@obsudim.ru
Abstract
Diabetes mellitus (DM) falls into the category of socially significant non-communicable diseases. When ineffectively treated, DM can considerably worsen the patients’ quality of life due to the development of systemic vascular complications leading to disability and early death. Reduction of the risk of diabetic complications and mortality can only be achieved through multifaceted disease management. It is emphasized that DM is a chronic disease, and DM treatment represents the long-term, lifelong process that should involve both the physician and the patient him/herself. Selection of individual treatment targets and methods of glycemic control are discussed. The paper presents current understanding of blood glucose self-monitoring (SMBG), discloses its benefits in terms of DM control. The use of SMBG allows the physician to objectively assess the efficacy of the treatment prescribed and allows patients to become active contributors to the treatment process. The data are provided of the clinical trials focused on assessing the SMBG effectiveness. The role of SMBG in prevention of hypoglycemia is considered. Thorough SMBG makes it possible to prevent sharp blood glucose level fluctuations and to timely detect hypoglycemia. Attention is paid to the recommended SMBG rate depending on hypoglycemic therapy. The issues of glucose meter selection are considered. An important criterion for choosing the glucose meter is compliance with accuracy standards, convenience and ease of use. With advancement in technology improving blood glucose level measurement, the SMBG procedure becomes easier, which contributes to improvement of the hypoglycemic therapy efficacy and adherence to treatment.
Keywords: diabetes mellitus, prevalence, hyperglycemia, hypoglycemia, self-monitoring of blood glucose, glucose meters.
For citation: For citation: Biryukova E.V., Solovyova I.V. Self-monitoring of blood glucose is an important component of effective diabetes mellitus control. Clinical review for general practice. 2025; 6 (6): 57–66 (In Russ.). DOI: 10.47407/kr2025.6.6.00631
Сахарный диабет (СД) занимает лидирующие позиции среди неинфекционных заболеваний, распространенных по всему миру. Согласно информации, предоставленной Международной федерацией диабета (МФД) в 2024 г., 589 млн взрослых людей в возрасте от 20 до 79 лет живут с диагнозом СД, что соответствует 11,1% от общей численности населения мира в указанной возрастной категории. По прогнозам, к 2050 г. это число может вырасти до 853 млн человек, что составит 13% населения планеты [1].
Доминирует численность пациентов, страдающих СД 2-го типа (СД 2) [2]. Причем 635 млн взрослых в возрасте 20–79 лет живут с нарушенной толерантностью к глюкозе (12%) [1]. Высокая распространенность предиабета создает предпосылки для дальнейшего роста заболеваемости СД 2, ежегодно от 5 до 10% случаев предиабета переходят в СД 2 [3]. Существенное увеличение числа пациентов, страдающих СД 2, главным образом обусловлено избыточной массой тела или ожирением, накоплением висцерального жира, а также недостаточной физической активностью [4]. Результаты исследования NATION показали, что число людей с предиабетом и СД 2 возрастает пропорционально увеличению индекса массы тела (ИМТ) [5]. В частности, среди лиц с ИМТ менее 25 кг/м2 распространенность СД 2 и предиабета составила 1,1 и 7,4% соответственно. У лиц с избыточной массой тела (ИМТ от 25 до 30 кг/м2) распространенность СД 2 достигла 3,9%, а предиабета – 18,6%.
В группе людей с ожирением (ИМТ 30 кг/м2 и выше) СД 2 был выявлен у 12% участников, а предиабет – у 33,1%. Важно отметить, что половые различия в распространенности нарушений углеводного обмена не наблюдались.
Наряду с избыточной массой тела / ожирением большое значение имеют и другие факторы риска развития СД 2, представленные в табл. 1 [6].
 При недостаточно эффективном лечении СД может существенно ухудшить качество жизни пациентов из-за развития системных сосудистых осложнений (нефропатия, ретинопатия, поражение магистральных сосудов сердца, головного мозга, артерий нижних конечностей), приводящих к инвалидизации и преждевременной смерти [6, 7]. СД является основной причиной слабовидения, слепоты, хронической болезни почек, инсульта, ампутаций нижних конечностей и смертности от ишемической болезни сердца и сердечной недостаточности [8, 9]. По данным МФД в 2024 г. более 3,4 млн человек скончались вследствие СД, что составляет 9,3% от общего числа смертей в мире [1]. Велик и экономический урон, наносимый хроническими диабетическими осложнениями: СД является причиной не менее 12% мировых расходов на здравоохранение [10]. Развитие диабетических системных осложнений в среднем увеличивает затраты на лечение в 3–10 раз, предотвращение данных осложнений представляет собой значимую цель современной медицины [11]. Хроническая гипергликемия является основной причиной развития и прогрессирования сосудистых осложнений при СД. Несмотря на наличие обширных научных данных, демонстрирующих важность тщательного контроля уровня глюкозы в крови, задача обеспечения адекватного метаболического контроля и предупреждения хронических осложнений диабета не теряет своей остроты и требует решения [2, 12]. Согласно крупному метаанализу 24 исследований (n=369,251) только 42,8% пациентов с СД 2 (95% доверительный интервал 38,1–47,5) имели целевой контроль гликемии [13].
При недостаточно эффективном лечении СД может существенно ухудшить качество жизни пациентов из-за развития системных сосудистых осложнений (нефропатия, ретинопатия, поражение магистральных сосудов сердца, головного мозга, артерий нижних конечностей), приводящих к инвалидизации и преждевременной смерти [6, 7]. СД является основной причиной слабовидения, слепоты, хронической болезни почек, инсульта, ампутаций нижних конечностей и смертности от ишемической болезни сердца и сердечной недостаточности [8, 9]. По данным МФД в 2024 г. более 3,4 млн человек скончались вследствие СД, что составляет 9,3% от общего числа смертей в мире [1]. Велик и экономический урон, наносимый хроническими диабетическими осложнениями: СД является причиной не менее 12% мировых расходов на здравоохранение [10]. Развитие диабетических системных осложнений в среднем увеличивает затраты на лечение в 3–10 раз, предотвращение данных осложнений представляет собой значимую цель современной медицины [11]. Хроническая гипергликемия является основной причиной развития и прогрессирования сосудистых осложнений при СД. Несмотря на наличие обширных научных данных, демонстрирующих важность тщательного контроля уровня глюкозы в крови, задача обеспечения адекватного метаболического контроля и предупреждения хронических осложнений диабета не теряет своей остроты и требует решения [2, 12]. Согласно крупному метаанализу 24 исследований (n=369,251) только 42,8% пациентов с СД 2 (95% доверительный интервал 38,1–47,5) имели целевой контроль гликемии [13].
Гипергликемия, как ключевой фактор в развитии диабетических осложнений, требует эффективного лечения с достижением целевых метаболических показателей сразу после выявления СД. Идея «метаболической памяти», также известная как «эффект наследия», свидетельствует о сохранении эффекта влияния предшествующего гликемического контроля (первичного хорошего или неудовлетворительного метаболического контроля) на развитие и прогрессирование сосудистых осложнений при СД [14]. Создание хорошей «метаболической памяти» предполагает раннее интенсивное лечение гипергликемии, направленное на нормализацию метаболического контроля, что помогает отсрочить развитие диабетических системных осложнений.
Феномен «эффекта наследия» был продемонстрирован в исследовании DCCT (Diabetes Complications and Control Trial): интенсивный контроль гликемии в течение 9 лет и снижение уровня HbA1c на каждый 1% сопровождались достоверным уменьшением риска развития микрососудистых осложнений на 44% у пациентов с СД 1-го типа (СД 1) [15]. Исследование UKPDS показало, что у пациентов с впервые выявленным СД 2 интенсивный контроль гликемии на протяжении 7,5 года и снижение на 1% уровня HbA1c статистически значимо уменьшили риск развития микрососудистых осложнений на 37%. Кроме того, наблюдалось снижение риска инфаркта миокарда на 14%, инсульта головного мозга на 12%, ампутаций нижних конечностей на 43% и летального исхода, обусловленного диабетом, на 21% [16]. Раннее интенсивное лечение СД, направленное на достижение целевых показателей гликемии, существенно превосходит эффекты позднего достижения компенсации углеводного обмена после длительного периода неудовлетворительных показателей гликемии [14, 17].
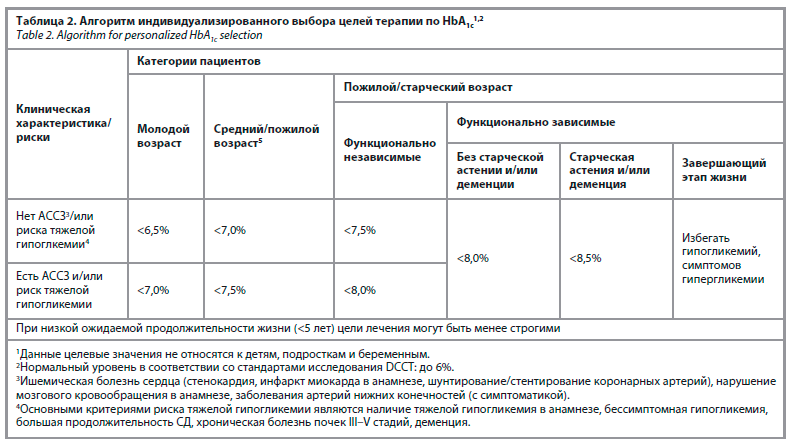
Все международные руководства акцентируют внимание на значимости поддержания оптимального уровня глюкозы в крови и регулярного СКГ у пациентов с СД. Это особенно актуально для пациентов, использующих инсулин и принимающих пероральные сахароснижающие средства, способные спровоцировать гипогликемию [6, 19, 20]. В выпуске 12 (2025 г.) «Алгоритмов специализированной медицинской помощи больных сахарным диабетом» подчеркивается важность выбора индивидуальных целей лечения в зависимости от возраста пациента, ожидаемой продолжительности жизни, функциональной зависимости, наличия атеросклеротических сердечно-сосудистых заболеваний (АССЗ) и риска тяжелой гипогликемии (табл. 2) [6]. Для большинства взрослых пациентов с СД адекватным является целевой уровень HbA1c менее 7,0%.
Методы контроля уровня гликемии включают СКГ и непрерывный мониторинг глюкозы (НМГ), которые не следует рассматривать как конкурирующие технологии. В реальной клинической практике необходимо использовать достоинства каждого метода для лучшего управления СД [21]. СКГ с помощью глюкометра продолжает оставаться необходимым при использовании НМГ [19].
Со времен открытия инсулина СКГ является одним из значимых достижений в области лечения СД [22]. Современное понимание СКГ подразумевает определенную кратность регулярных измерений концентрации глюкозы крови и представляет собой важный ориентир, используемый врачом и пациентом для оценки результата сахароснижающей терапии и внесения необходимых корректив в план лечения. Регулярное обучение пациентов с СД является неотъемлемой частью терапевтического процесса и необходимо для эффективного СКГ. В процессе обучения приобретаются практические навыки, которые имеют решающее значение для СКГ [23].
Результаты масштабных клинических исследований в области СД однозначно показывают: поддержание оптимального уровня глюкозы в крови играет ключевую роль в предотвращении или существенном замедлении развития и ухудшения хронических диабетических осложнений [15, 16, 24]. Достижение наилучшего гликемического контроля у пациентов с СД 1 возможно при использовании интенсифицированной (базис-болюсной) инсулинотерапии, предполагающей многократные инъекции или непрерывную подкожную инфузию инсулина. Для адекватной коррекции дозы инсулина до достижения индивидуальных целевых показателей гликемического контроля необходимо учитывать результаты СКГ или НМГ в течение дня, а также количество углеводов, потребляемых с пищей, и другие факторы, влияющие на уровень глюкозы в крови. Обратимся к итогам ключевого исследования DCCT – первого масштабного продолжительного рандомизированного исследования с участием больных СД 1 [15]. Это исследование заложило основу современных подходов к лечению СД 1, подчеркнув преимущества частого СКГ в сочетании с коррекцией доз инсулина в режиме многократных инъекций для достижения индивидуальных гликемических целей по сравнению с традиционной инсулинотерапией (1–2 инъекции в сутки) и измерением глюкозы 1 раз в день. Исследование убедительно показало, что интенсивная инсулинотерапия, основанная на регулярном СКГ и индивидуальной коррекции доз инсулина, позволяет достичь уровня глюкозы в крови, близкого к норме. Это, в свою очередь, привело к значительному снижению риска развития и прогрессирования диабетических осложнений.
Эффективность инсулинотерапии связана с обязательным СКГ при СД 2. В частности, в масштабном исследовании ORIGIN титрация дозы базального инсулина гларгин-100 осуществлялась с помощью доступного алгоритма на основании СКГ, что позволило достигнуть целевого гликемического контроля при высокой безопасности проводимой инсулинотерапии [26].
Согласно результатам других исследований, уровень HbA1c начинает значимо улучшаться, как только пациент увеличивает частоту СКГ независимо от типа СД или вида сахароснижающей терапии [27–31]. В ретроспективном исследовании ROSSO (Retrolective Study Self Monitoring of Blood Glucose and Outcome in people with Type 2 Diabetes) анализу были подвергнуты данные 3268 пациентов с СД 2 за период 6,5 года, предшествующих исследованию. Среди включенных 1479 пациентов проводили СКГ, в то время как остальные его не выполняли. Как оказалось, в группе СКГ снижался на 32% риск развития диабетических осложнений (острого инфаркта миокарда, инсульта, ампутаций, слепоты, необходимости гемодиализа), а риск смерти от СД 2 – на 51%. Результаты ROSSO также свидетельствуют, что СКГ способствует увеличению продолжительность жизни, и что немаловажно, улучшению качества жизни пациентов с СД 2, независимо от характера использованной фармакотерапии [32]. Именно поэтому врачи должны уделять особое внимание СКГ.
СКГ позволяет пациентам получать и использовать информацию о показателях гликемии в повседневной жизни. Регулярные занятия спортом и поддержание двигательной активности – важная составляющая здорового образа жизни, способствующая улучшению его качества. Пациентам с СД необходимо знать о вероятных изменениях глюкозы в крови во время занятий спортом и любой двигательной активности. Однако, особенно при СД 1, физическая активность может провоцировать гипогликемию в процессе и после тренировок, поэтому основная задача – профилактика гипогликемии, связанной с физической нагрузкой [19, 33]. Регулярный СКГ или НМГ позволяет пациентам с СД, владеющим методами профилактики гипогликемий, воплощать в повседневной жизни любые виды физической активности (ФА), в том числе занятия спортом, и избежать гипогликемий с учетом следующих противопоказаний и мер предосторожности [6] (табл. 3).

СКГ дает возможность оценить индивидуальную реакцию организма на различные типы физических нагрузок и повысить заинтересованность пациентов в регулярных занятиях. Для обеспечения безопасности при выполнении физических упражнений всем пациентам необходимо контролировать уровень глюкозы в крови, особенно тем, кто получает инсулин или пероральные препараты, стимулирующие выработку инсулина. Измерение уровня глюкозы обязательно перед тренировками, временным ограничением для которых служит уровень глюкозы в плазме крови выше 13,0 ммоль/л в сочетании с кетонами в моче или 16 ммоль/л (даже при отсутствии кетонов).
Хотя регулярная ФА не является методом сахароснижающей терапии при СД 1, при СД 2 физические нагрузки способствуют достижению целевых уровней гликемии, похудению, помогают улучшить чувствительность тканей к инсулину, показатели липидного профиля крови. В настоящее время модификация образа жизни рекомендуется в качестве 1-й линии лечения СД 2, что достигается повышением физической активности и ограничением калорийности рациона [33, 34].
Показано, что СКГ повышает результат программ модификации образа жизни по коррекции образа жизни. В ретроспективном исследовании, проведенном S. Tomah и соавт., были представлены интересные данные, полученные в результате анализа программы по изменению образа жизни (Why WAIT, продолжительность 12 нед). Участникам программы (средний возраст 57±9 лет, продолжительность СД 2 10±8 лет, ИМТ 36±6 кг/м2, уровень HbA1c 7,8±1,4%, 45% на инсулинотерапии) рекомендовалось ежедневно проводить СКГ с использованием глюкометра. Измерения глюкозы следовало выполнять перед каждым приемом пищи, перед отходом ко сну, до и после физических упражнений, через 2 ч после еды, а также при подозрении на гипо- или гипергликемию [35]. В зависимости от частоты СКГ, проводимого пациентами с СД 2 в течение периода наблюдения, участники были разделены на три группы (по тертилям частоты СКГ). Средняя частота СКГ составила 2,3 (1,1–2,9) раза в сутки в группе нижнего тертиля, 3,4 (3,0–3,9) раза в сутки в группе среднего тертиля и 5 (4,0–7,7) раз в сутки в группе верхнего тертиля. Исходные средние значения массы тела пациентов составили 107,6±20,3 кг в группе нижнего тертиля частоты СКГ, 107,4±19,2 кг в группе среднего тертиля и 107,4±24 кг в группе верхнего тертиля. Исходные значения HbA1c составили 7,5%±1,0%, 8,0%±1,5% и 8,0%±1,6% соответственно для тех же групп. Группы были сопоставимы по возрасту, полу, расе, продолжительности диабета, использованию инсулина, уровню HbA1c, ИМТ.
После 12 нед наблюдения лица, практиковавшие частый СКГ, продемонстрировали существенно большее снижение массы тела, чем участники с менее регулярным мониторингом гликемии. В частности, группа, находившаяся в верхнем тертиле по частоте СКГ, достигла среднего уменьшения массы тела на 10,4 кг (в диапазоне от -7,6 до -14,4 кг). Для сравнения, в среднем и нижнем тертилях этот показатель составил 8,3 кг (от
-5,2 до -12,2 кг) и 6,9 кг (от -4,2 до -8,9 кг) соответственно (p=0,018). Аналогичная тенденция наблюдалась и в динамике ИМТ. В зависимости от тертиля частоты СКГ, изменения ИМТ составили -3,9 кг/м2 (от
-2,8 до -4,9 кг/м2), -2,7 кг/м2 (от -1,6 до -3,9 кг/м2) и
-2,5 кг/м2 (от -1,5 до 3,3 кг/м2) (p=0,012). Более высокая частота тестирования уровня глюкозы была связана со значительно лучшей динамикой HbA1c, отмеченной в конце исследования. В группе с наиболее частым СКГ снижение HbA1c составило -1,25% (от -0,6 до -3,1%), тогда как в среднем и нижнем тертилях эти значения были равны -0,8% (от -0,3 до -2%) и -0,5% (от -0,2 до
-1,2%) соответственно (p=0,048) [35].
У многих пациентов с СД одной из ключевых причин отсутствия достижения целевых показателей гликемии является недостаточный контроль уровня глюкозы в крови. К сожалению, довольно часто пациенты не следуют предписаниям врача в полной мере. Это касается не только соблюдения диетических ограничений, необходимого уровня ФА, но и регулярного СКГ. Например, в исследовании, проведенном M.V. Hansen и соавт., было установлено, что только 39% больных СД 1 ежедневно проводили СКГ, 20% делали это несколько раз в неделю, 17% – один-два раза в неделю, а 24% – реже одного раза в неделю [36]. По данным S.A. Farhan и соавт. только каждый пятый пациент с СД 2 осуществлял измерение уровня глюкозы через 2 ч после приема пищи, 16% проводили СКГ только при плохом самочувствии, а 14% – при клинических симптомах гипогликемии [37].
У пациентов с СД уровень глюкозы крови подвержен колебаниям под воздействием различных факторов, которые могут приводить как к повышению, так и к снижению гликемии. Физические нагрузки, стрессовые ситуации, употребление алкоголя, вирусные заболевания, обострения хронических болезней, а также прием определенных лекарственных препаратов, таких как глюкокортикоиды, – лишь некоторые из них. Важно отметить, что проведение СКГ позволяет вовремя выявлять факторы, влияющие на изменение уровня глюкозы, и своевременно корректировать лечение.
Гипогликемические состояния – частое явление при СД 1; различные исследования показывают, что при
СД 1 в среднем наблюдается от 0,5 до 5 тяжелых гипогликемических событий ежегодно [15, 38]. Реже гипогликемии встречаются при СД 2. Вместе с тем частота гипогликемий при СД 2 возрастает с увеличением длительности заболевания [39, 40]. Проводя сахароснижающую терапию у пациентов с СД 2, всегда следует помнить о риске гипогликемий, который могут увеличивать некоторые препараты, вместе с тем есть группы препаратов, преимуществом которых является низкий риск гипогликемий (табл. 4).

Опаснейшим исходом гипогликемии являются негативные сердечно-сосудистые события, обусловленные множеством патофизиологических механизмов. В ответ на падение уровня глюкозы в крови происходит активация симпатической и контринсулярной системы, сопровождающаяся выбросом значительного количества катехоламинов и других гормонов, что провоцирует сбои в гемодинамике, электрической стабильности сердца и процессах реполяризации, вызывает вазоконстрикцию, прокоагулянтное состояние, ухудшает реологию крови, увеличивает потребность миокарда в кислороде. Эти процессы могут приводить к изменениям регионарного кровотока, провоцировать ишемию миокарда и мозга, вызывая острый инфаркт миокарда, сердечную недостаточность или инсульт; имеются данные, подтверждающие связь между гипогликемией и сердечными аритмиями, которые потенциально предрасполагают к внезапной смерти [41].
Разнообразные факторы и состояния способны спровоцировать гипогликемию. Как уже отмечалось, случаи гипогликемии чаще наблюдаются у больных на инсулинотерапии или получающих секретагоги. В их число входят также усиленные/продолжительные или нестандартные физические нагрузки, употребление алкоголя, несистематическое питание с пропусками еды или с малым количеством углеводов, а также рвота, синдром мальабсорбции. Дополнительными факторами риска выступают пожилой возраст и расстройства когнитивных функций, почечная и печеночная недостаточность, длительность СД, автономная нейропатия, ранее перенесенные эпизоды гипогликемии, ухудшение способности распознавать гипогликемию.
Частые эпизоды гипогликемии вызывают постепенное истощение контррегуляторных защитных механизмов, что приводит к утрате способности распознавать привычные симптомы этого опасного состояния и повышает риск тяжелой гипогликемии. Как показало исследование VADT (Veterans Affairs Diabetes Trial), перенесенная тяжелая гипогликемия в четыре раза увеличивает риск смерти от сердечно-сосудистых заболеваний, причем этот фактор оказывается более значимым, чем возраст, уровень гликированного гемоглобина, нарушение липидного обмена [41].
СКГ дает возможность оперативно обнаружить состояние гипогликемии и, как следствие, вовремя принять меры для его устранения. Систематическое самостоятельное измерение уровня глюкозы в крови помогает выявлять и скрытые случаи (бессимптомные) гипогликемии. Это особенно важно для пациентов, имеющих проблемы с ощущением гипогликемии, вызванные нарушениями в работе контррегуляторных механизмов и ослаблением симпатоадреналовой реакции в ответ на гипогликемию. Потеря чувствительности к гипогликемии встречается у 20–25% пациентов с СД 1 и у 10% с СД 2 на инсулинотерапии; причем нарушение распознавания гипогликемии у пациентов с СД связано с шестикратным увеличением риска тяжелой гипогликемии, страхом гипогликемии и когнитивной дисфункцией [42, 43].
Как было отмечено ранее, для создания благоприятной «метаболической памяти» и предотвращения развития сосудистых осложнений крайне важно поддерживать целевые уровни гликемии с момента диагностики; значение гликемического контроля на ранних стадиях СД для развития осложнений становится заметным лишь спустя продолжительное время [14]. Интересные данные представлены в ретроспективном исследовании H.K. Sia и соавт., которое вовлекло 4987 пациентов с впервые выявленным СД 2 (средний возраст 56,2±11,5 года, 51,9% – мужчины). Участники были разделены на две группы в зависимости от наличия или отсутствия регулярного СКГ с момента начала сахароснижающей терапии: группа с ранним СКГ («+») и группа без раннего СКГ («-»). Результаты показали, что в реальной клинической практике систематическое проведение измерений уровня глюкозы в крови с помощью глюкометра ассоциировалось с улучшением гликемического контроля. При этом данный эффект наблюдался вне зависимости от типа применяемой сахароснижающей терапии, будь то метформин, тиазолидиндионы, ингибиторы дипептидилпептидазы-4 или препараты, стимулирующие секрецию инсулина. У пациентов, регулярно выполнявших СКГ (группа СКГ «+»), наблюдался более низкий уровень HbA1c в сопоставлении с теми, кто не осуществлял подобный мониторинг глюкозы в крови. Наибольшее расхождение в значениях достигало 0,55% по прошествии 3 мес, что сохранялось и в дальнейшем: через 6 и 12 мес различие составляло 0,45% в обоих случаях [44]. Таким образом, регулярный СКГ помогает улучшить эффект сахароснижающей терапии с момента диагностики заболевания.
Рекомендуемая частота СКГ в зависимости от типа СД отражена в международных и национальных руководствах по лечению СД. В соответствии с Российскими клиническими рекомендациями, больным СД 1 без осложнений СКГ необходимо проводить не менее 4 раз ежедневно (до еды, через 2 ч после еды, на ночь, периодически ночью); при наличии признаков осложнений СД, присоединении сопутствующих заболеваний, появлении дополнительных факторов риска вопрос о частоте обследований решается индивидуально [6]. СКГ при СД 2 в дебюте заболевания, а также при недостижении целевых уровней гликемического контроля необходимо осуществлять ежедневно несколько раз; в дальнейшем его частота определяется видом сахаро-снижающей терапии (табл. 5).
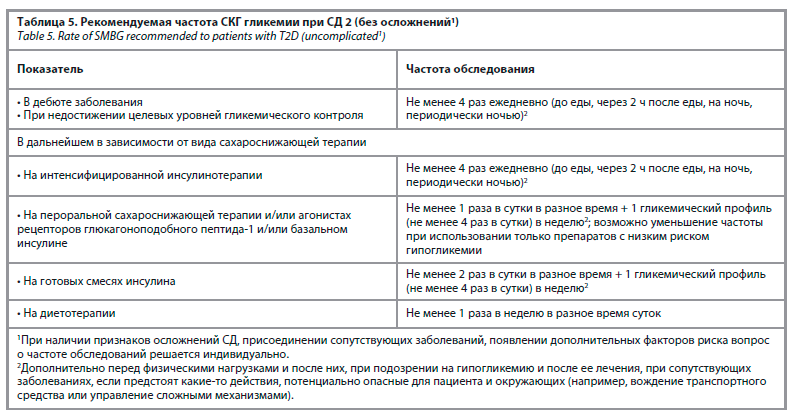
Надо сказать, что рекомендации по частоте СКГ при СД 2 могут быть распространены и на больных с другими специфическими типами СД.
Использование СКГ дает врачу возможность определить, насколько эффективна назначенная немедикаментозная и медикаментозная терапия. Пациенты, в свою очередь, получают возможность принимать активное участие в процессе своего лечения, что ведет к большей осознанности и приверженности плану лечения, предложенному врачом, а также повышает их личную ответственность за достигнутые результаты.
Не стоит думать, что сам по себе СКГ улучшит показатели гликемии. Положительный результат достигается, когда пациент с СД, обладающий необходимыми знаниями, использует данные СКГ для принятия обдуманных решений в своей повседневной жизни [46, 47]. Активное участие больного в этом процессе подразумевает способность сопоставлять собственные показатели уровня глюкозы в крови с индивидуальными целевыми значениями, находить взаимосвязи между образом жизни (повседневной активностью, физической нагрузкой, пищевым рационом), терапией и текущими показателями глюкозы. Это также требует тщательного анализа факторов, мешающих достижению оптимального контроля гликемии, и определения причин отклонений уровня глюкозы в крови от целевых значений.
Пациенты с СД часто сталкиваются с трудностями в соблюдении рекомендаций по изменению рациона питания. СКГ дает наглядное представление о том, как различные продукты влияют на уровень гликемии после еды. Это позволяет оперативно корректировать рацион, обеспечивая сбалансированное питание, что, несомненно, способствует более эффективному лечению. Однако, чтобы в полной мере использовать преимущества СКГ, пациентам с СД необходимо систематическое обучение, которое поможет им правильно применять методы СКГ и анализировать полученные данные для оптимизации терапии. Только так можно добиться значимых улучшений в управлении СД [47].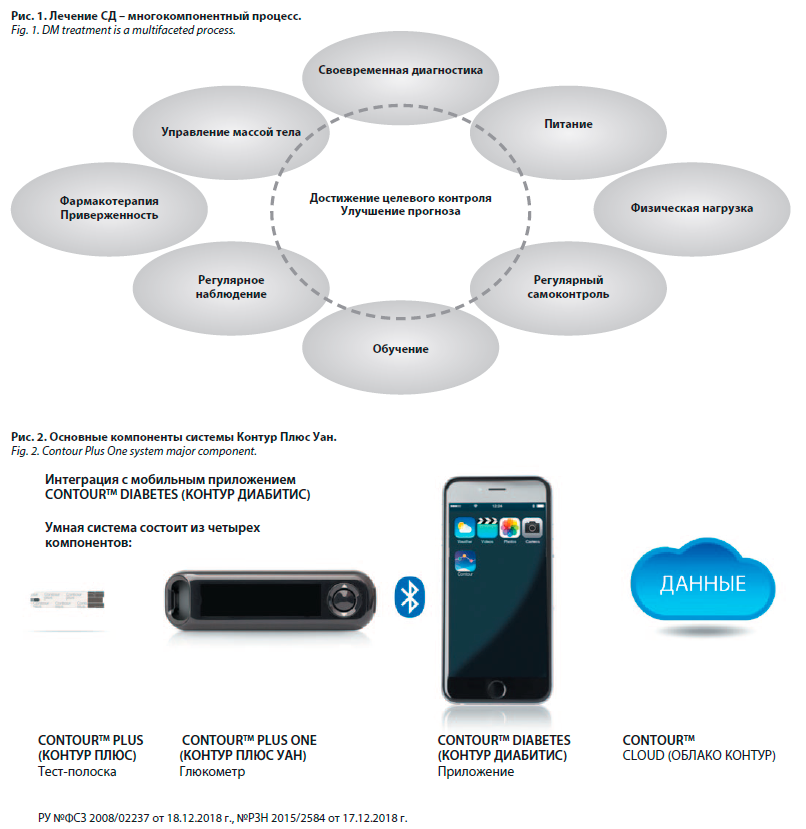
Один из современных глюкометров, соответствующий всем требованиям, предъявляемым к приборам индивидуального использования, – глюкометр Контур Плюс Уан (ContourTM Plus One), который показал высокую точность как в лабораторных, так и клинических условиях. Умная система ContourTM Plus One состоит из 4 компонентов: тест-полоска, глюкометр, мобильное приложение и облачное хранилище данных (рис. 2). Благодаря интеграции глюкометра с бесплатным мобильным приложением (доступно для скачивания в онлайн-магазинах приложений) значительно расширяются возможности управления СД со стороны пациента и взаимодействия с врачом.
Высокая точность определения концентрации глюкозы в крови в сочетании с удобством использования данного глюкометра и другими передовыми решениями способствует формированию позитивного отношения пациентов к СКГ. Это позволяет избежать ошибочных действий в терапии, например неверной дозировки инсулина, и, как следствие, достичь оптимальных показателей контроля гликемии.
При выборе глюкометра следует учитывать несколько ключевых аспектов: не только его соответствие современным требованиям к точности, но и интуитивно простой и понятный интерфейс, удобство применения, легкость получения результата пациентами, экономичность. Данные критерии гарантируют беспроблемное проведение измерения уровня глюкозы в крови пациентами всех возрастных групп.
Технология нанесения образца крови «Второй шанс» позволяет пациентам повторно наносить кровь на ту же самую тест-полоску, если первоначального образца было недостаточно, и измерить уровень глюкозы в крови. Повторное нанесение возможно в течение минуты, при этом нет необходимости дополнительного прокола пальца. Это особенно важно для лиц с СД, в частности для пациентов старшего возраста. Удобство использования прибора также заключается в быстром времени измерения уровня глюкозы в крови – всего 5 с, что является критически важным при развитии гипогликемии.
Глюкометр оборудован световым индикатором в области порта для тест-полосок, использующим цветовую схему, аналогичную светофору – функция «Умная подсветка», которая предоставляет мгновенную обратную связь, сигнализируя цветом об уровне глюкозы, и позволяет пользоваться глюкометром при различном освещении. Это помогает пользователю визуально оценивать результаты измерения: зеленый цвет указывает на то, что уровень глюкозы в крови находится в пределах нормы, желтый и красный цвета – о повышенном или пониженном уровне глюкозы соответственно.
Устройство способно автоматически устанавливать связь с бесплатным мобильным приложением Контур Диабитис (Contour Diabetes) и последующей загрузкой всех показателей измерений глюкозы в электронный дневник – расширенную цифровую версию дневника самоконтроля. Для пациентов с СД это открывает доступ к широким возможностям сбора и анализа информации, поскольку все важные для управления уровнем глюкозы данные фиксируются в электронном дневнике, позволяя пользователям более эффективно отслеживать уровень глюкозы в крови (например, указывая пометки «до еды» и «после еды»), регистрировать дозировку лекарств, потребление углеводов, добавлять комментарии и детализированные записи о приемах пищи, загружать фотографии еды, а также фиксировать изменения в своем образе жизни и другие важные факторы.
Функция «Мои тенденции» позволяет отслеживать динамику показателей глюкозы в крови и оповещает пользователя о потенциальных причинах, влияющих на эти колебания гликемии. Важно отметить, что фиксация положительных изменений уровня глюкозы в крови благодаря сбалансированному питанию и систематическим занятиям физическими упражнениями может стать мощным мотиватором для пациента, способствуя укреплению приверженности здоровому образу жизни и повышению качества жизни [48, 49].
С помощью функции отчетов, сгенерированных на основе всей информации, поступающей в мобильное приложение Контур Диабитис, появляется возможность внедрить современные цифровые решения в коммуникацию между пациентом и врачом, тем самым повышая эффективность лечения. Благодаря синхронизации мобильного приложения с облачным хранилищем данных (Российский сервер) пациенты могут оперативно передавать врачу полную информацию о результатах СКГ в крови в цифровом виде. Это обеспечивает возможность совместного анализа причин изменений уровня сахара, выявления критических ситуаций и своевременного обращения к специалисту.
Подводя итоги, следует отметить, что современная сахароснижающая терапия предусматривает обязательное проведение СКГ. Система Контур Плюс Уан характеризуется высокой степенью точности, интуитивно понятным способом измерения уровня глюкозы в крови, а также интеграцией информационных технологий для поддержания связи между пациентом и врачом. Эти возможности широко реализованы в различных функциях системы, что позволяет пациентам активно участвовать в процессе лечения СД и максимально эффективно использовать преимущества СКГ в повседневной жизни.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Бирюкова Елена Валерьевна – д-р мед. наук, проф. каф. эндокринологии и диабетологии, ФГБОУ ВО «Российский университет медицины». E-mail: lena@obsudim.ru; ORCID: 0000-0001-9007-4123
Elena V. Biryukova – Dr. Sci. (Med.), Prof., Russian University of Medicine (ROSUNIMED). E-mail: lena@obsudim.ru; ORCID: 0000-0001-9007-4123
Соловьева Инна Владимировна – ассистент каф. эндокринологии и диабетологии, ФГБОУ ВО «Российский университет медицины»; зав. отд-нием эндокринологии, ГБУЗ «МКНЦ им. А.С. Логинова». E-mail: Inna.dell.85@mail.ru; ORCID: 0000-0002-2125-622X
Inna V. Solovyova – Аssistant, Russian University of Medicine (ROSUNIMED); Head of the Department of Endocrinology, Loginov Moscow Clinical Research Center. E-mail: Inna.dell.85@mail.ru;
ORCID: 0000-0002-2125-622X
Поступила в редакцию: 18.06.2025
Поступила после рецензирования: 24.06.2025
Принята к публикации: 26.06.2025
Received: 18.06.2025
Revised: 24.06.2025
Accepted: 26.06.2025
Клинический разбор в общей медицине №6 2025
Самоконтроль гликемии – важный компонент эффективного управления сахарным диабетом
Номера страниц в выпуске:57-66
Аннотация
Сахарный диабет (СД) относится к категории социально значимых неинфекционных заболеваний. При недостаточно эффективном лечении СД может существенно ухудшить качество жизни пациентов из-за развития диабетических системных сосудистых осложнений, приводящих к инвалидизации и преждевременной смерти. Снижения риска развития диабетических осложнений и смертности можно добиться только многофакторным управлением заболеванием. Подчеркнуто, что СД является хроническим заболеванием, его лечение представляет длительный, пожизненный процесс, в котором должен участвовать не только врач, но и сам пациент. Обсуждается выбор индивидуальных целей лечения заболевания, методы контроля гликемии. В статье представлено современное понимание самоконтроля гликемии (СКГ), раскрыты его преимущества в управлении СД. Применение СКГ позволяет врачу объективно оценить эффективность назначенного лечения, а пациентам – быть активными участниками процесса терапии. Приведены данные клинических исследований по оценке эффективности СКГ. Рассматривается роль СКГ в профилактике гипогликемий. Тщательный СКГ позволяет избежать резких колебаний уровня глюкозы в крови, своевременно выявлять гипогликемии. Уделено внимание рекомендуемой частоте СКГ в зависимости от сахароснижающей терапии. Затронуты вопросы выбора глюкометра. Важным критерием для выбора глюкометра является соответствие стандартам точности, удобство и простота использования. Благодаря совершенствованию технологий, повышающих точность измерений глюкозы крови, процедура СКГ упрощается, что способствует повышению эффективности сахароснижающей терапии и приверженности к лечению.
Ключевые слова: сахарный диабет, распространенность, гипергликемия, гипогликемия, самоконтроль гликемии, глюкометры.
Для цитирования: Бирюкова Е.В, Соловьева И.В. Самоконтроль гликемии – важный компонент эффективного управления сахарным диабетом. Клинический разбор в общей медицине. 2025; 6 (6): 57–66. DOI: 10.47407/kr2025.6.6.00631
Сахарный диабет (СД) относится к категории социально значимых неинфекционных заболеваний. При недостаточно эффективном лечении СД может существенно ухудшить качество жизни пациентов из-за развития диабетических системных сосудистых осложнений, приводящих к инвалидизации и преждевременной смерти. Снижения риска развития диабетических осложнений и смертности можно добиться только многофакторным управлением заболеванием. Подчеркнуто, что СД является хроническим заболеванием, его лечение представляет длительный, пожизненный процесс, в котором должен участвовать не только врач, но и сам пациент. Обсуждается выбор индивидуальных целей лечения заболевания, методы контроля гликемии. В статье представлено современное понимание самоконтроля гликемии (СКГ), раскрыты его преимущества в управлении СД. Применение СКГ позволяет врачу объективно оценить эффективность назначенного лечения, а пациентам – быть активными участниками процесса терапии. Приведены данные клинических исследований по оценке эффективности СКГ. Рассматривается роль СКГ в профилактике гипогликемий. Тщательный СКГ позволяет избежать резких колебаний уровня глюкозы в крови, своевременно выявлять гипогликемии. Уделено внимание рекомендуемой частоте СКГ в зависимости от сахароснижающей терапии. Затронуты вопросы выбора глюкометра. Важным критерием для выбора глюкометра является соответствие стандартам точности, удобство и простота использования. Благодаря совершенствованию технологий, повышающих точность измерений глюкозы крови, процедура СКГ упрощается, что способствует повышению эффективности сахароснижающей терапии и приверженности к лечению.
Ключевые слова: сахарный диабет, распространенность, гипергликемия, гипогликемия, самоконтроль гликемии, глюкометры.
Для цитирования: Бирюкова Е.В, Соловьева И.В. Самоконтроль гликемии – важный компонент эффективного управления сахарным диабетом. Клинический разбор в общей медицине. 2025; 6 (6): 57–66. DOI: 10.47407/kr2025.6.6.00631
Self-monitoring of blood glucose is an important component of effective diabetes mellitus control
Elena V. Biryukova1, Inna V. Solovyova1,21 Russian University of Medicine (ROSUNIMED), Moscow, Russia;
2 Loginov Moscow Clinical Research Center, Moscow, Russia
lena@obsudim.ru
Abstract
Diabetes mellitus (DM) falls into the category of socially significant non-communicable diseases. When ineffectively treated, DM can considerably worsen the patients’ quality of life due to the development of systemic vascular complications leading to disability and early death. Reduction of the risk of diabetic complications and mortality can only be achieved through multifaceted disease management. It is emphasized that DM is a chronic disease, and DM treatment represents the long-term, lifelong process that should involve both the physician and the patient him/herself. Selection of individual treatment targets and methods of glycemic control are discussed. The paper presents current understanding of blood glucose self-monitoring (SMBG), discloses its benefits in terms of DM control. The use of SMBG allows the physician to objectively assess the efficacy of the treatment prescribed and allows patients to become active contributors to the treatment process. The data are provided of the clinical trials focused on assessing the SMBG effectiveness. The role of SMBG in prevention of hypoglycemia is considered. Thorough SMBG makes it possible to prevent sharp blood glucose level fluctuations and to timely detect hypoglycemia. Attention is paid to the recommended SMBG rate depending on hypoglycemic therapy. The issues of glucose meter selection are considered. An important criterion for choosing the glucose meter is compliance with accuracy standards, convenience and ease of use. With advancement in technology improving blood glucose level measurement, the SMBG procedure becomes easier, which contributes to improvement of the hypoglycemic therapy efficacy and adherence to treatment.
Keywords: diabetes mellitus, prevalence, hyperglycemia, hypoglycemia, self-monitoring of blood glucose, glucose meters.
For citation: For citation: Biryukova E.V., Solovyova I.V. Self-monitoring of blood glucose is an important component of effective diabetes mellitus control. Clinical review for general practice. 2025; 6 (6): 57–66 (In Russ.). DOI: 10.47407/kr2025.6.6.00631
Сахарный диабет (СД) занимает лидирующие позиции среди неинфекционных заболеваний, распространенных по всему миру. Согласно информации, предоставленной Международной федерацией диабета (МФД) в 2024 г., 589 млн взрослых людей в возрасте от 20 до 79 лет живут с диагнозом СД, что соответствует 11,1% от общей численности населения мира в указанной возрастной категории. По прогнозам, к 2050 г. это число может вырасти до 853 млн человек, что составит 13% населения планеты [1].
Доминирует численность пациентов, страдающих СД 2-го типа (СД 2) [2]. Причем 635 млн взрослых в возрасте 20–79 лет живут с нарушенной толерантностью к глюкозе (12%) [1]. Высокая распространенность предиабета создает предпосылки для дальнейшего роста заболеваемости СД 2, ежегодно от 5 до 10% случаев предиабета переходят в СД 2 [3]. Существенное увеличение числа пациентов, страдающих СД 2, главным образом обусловлено избыточной массой тела или ожирением, накоплением висцерального жира, а также недостаточной физической активностью [4]. Результаты исследования NATION показали, что число людей с предиабетом и СД 2 возрастает пропорционально увеличению индекса массы тела (ИМТ) [5]. В частности, среди лиц с ИМТ менее 25 кг/м2 распространенность СД 2 и предиабета составила 1,1 и 7,4% соответственно. У лиц с избыточной массой тела (ИМТ от 25 до 30 кг/м2) распространенность СД 2 достигла 3,9%, а предиабета – 18,6%.
В группе людей с ожирением (ИМТ 30 кг/м2 и выше) СД 2 был выявлен у 12% участников, а предиабет – у 33,1%. Важно отметить, что половые различия в распространенности нарушений углеводного обмена не наблюдались.
Наряду с избыточной массой тела / ожирением большое значение имеют и другие факторы риска развития СД 2, представленные в табл. 1 [6].
 При недостаточно эффективном лечении СД может существенно ухудшить качество жизни пациентов из-за развития системных сосудистых осложнений (нефропатия, ретинопатия, поражение магистральных сосудов сердца, головного мозга, артерий нижних конечностей), приводящих к инвалидизации и преждевременной смерти [6, 7]. СД является основной причиной слабовидения, слепоты, хронической болезни почек, инсульта, ампутаций нижних конечностей и смертности от ишемической болезни сердца и сердечной недостаточности [8, 9]. По данным МФД в 2024 г. более 3,4 млн человек скончались вследствие СД, что составляет 9,3% от общего числа смертей в мире [1]. Велик и экономический урон, наносимый хроническими диабетическими осложнениями: СД является причиной не менее 12% мировых расходов на здравоохранение [10]. Развитие диабетических системных осложнений в среднем увеличивает затраты на лечение в 3–10 раз, предотвращение данных осложнений представляет собой значимую цель современной медицины [11]. Хроническая гипергликемия является основной причиной развития и прогрессирования сосудистых осложнений при СД. Несмотря на наличие обширных научных данных, демонстрирующих важность тщательного контроля уровня глюкозы в крови, задача обеспечения адекватного метаболического контроля и предупреждения хронических осложнений диабета не теряет своей остроты и требует решения [2, 12]. Согласно крупному метаанализу 24 исследований (n=369,251) только 42,8% пациентов с СД 2 (95% доверительный интервал 38,1–47,5) имели целевой контроль гликемии [13].
При недостаточно эффективном лечении СД может существенно ухудшить качество жизни пациентов из-за развития системных сосудистых осложнений (нефропатия, ретинопатия, поражение магистральных сосудов сердца, головного мозга, артерий нижних конечностей), приводящих к инвалидизации и преждевременной смерти [6, 7]. СД является основной причиной слабовидения, слепоты, хронической болезни почек, инсульта, ампутаций нижних конечностей и смертности от ишемической болезни сердца и сердечной недостаточности [8, 9]. По данным МФД в 2024 г. более 3,4 млн человек скончались вследствие СД, что составляет 9,3% от общего числа смертей в мире [1]. Велик и экономический урон, наносимый хроническими диабетическими осложнениями: СД является причиной не менее 12% мировых расходов на здравоохранение [10]. Развитие диабетических системных осложнений в среднем увеличивает затраты на лечение в 3–10 раз, предотвращение данных осложнений представляет собой значимую цель современной медицины [11]. Хроническая гипергликемия является основной причиной развития и прогрессирования сосудистых осложнений при СД. Несмотря на наличие обширных научных данных, демонстрирующих важность тщательного контроля уровня глюкозы в крови, задача обеспечения адекватного метаболического контроля и предупреждения хронических осложнений диабета не теряет своей остроты и требует решения [2, 12]. Согласно крупному метаанализу 24 исследований (n=369,251) только 42,8% пациентов с СД 2 (95% доверительный интервал 38,1–47,5) имели целевой контроль гликемии [13].Гипергликемия, как ключевой фактор в развитии диабетических осложнений, требует эффективного лечения с достижением целевых метаболических показателей сразу после выявления СД. Идея «метаболической памяти», также известная как «эффект наследия», свидетельствует о сохранении эффекта влияния предшествующего гликемического контроля (первичного хорошего или неудовлетворительного метаболического контроля) на развитие и прогрессирование сосудистых осложнений при СД [14]. Создание хорошей «метаболической памяти» предполагает раннее интенсивное лечение гипергликемии, направленное на нормализацию метаболического контроля, что помогает отсрочить развитие диабетических системных осложнений.
Феномен «эффекта наследия» был продемонстрирован в исследовании DCCT (Diabetes Complications and Control Trial): интенсивный контроль гликемии в течение 9 лет и снижение уровня HbA1c на каждый 1% сопровождались достоверным уменьшением риска развития микрососудистых осложнений на 44% у пациентов с СД 1-го типа (СД 1) [15]. Исследование UKPDS показало, что у пациентов с впервые выявленным СД 2 интенсивный контроль гликемии на протяжении 7,5 года и снижение на 1% уровня HbA1c статистически значимо уменьшили риск развития микрососудистых осложнений на 37%. Кроме того, наблюдалось снижение риска инфаркта миокарда на 14%, инсульта головного мозга на 12%, ампутаций нижних конечностей на 43% и летального исхода, обусловленного диабетом, на 21% [16]. Раннее интенсивное лечение СД, направленное на достижение целевых показателей гликемии, существенно превосходит эффекты позднего достижения компенсации углеводного обмена после длительного периода неудовлетворительных показателей гликемии [14, 17].
Место самоконтроля гликемии в лечении сахарного диабета
Лечение СД – это многокомпонентный процесс, включающий несколько взаимосвязанных элементов и требующий постоянного сотрудничества врача и больного для достижения и удержания целевых показателей глюкозы в крови (рис. 1). СД является хроническим заболеванием, его лечение представляет длительный, пожизненный процесс, в котором должен участвовать не только врач, но и сам пациент. В процессе лечения заболевания ключевую роль играют не только немедикаментозные и медикаментозные подходы, но и терапевтическое обучение больных, самоконтроль гликемии (СКГ) как важные элементы лечения, сопровождающие пациента на протяжении всего периода заболевания [18]. Успех проводимого лечения всецело зависит от того, насколько больной СД может грамотно управлять своим заболеванием, что возможно при наличии медицинских знаний о нем и высоком уровне мотивации в достижении целевых показателей гликемии.Все международные руководства акцентируют внимание на значимости поддержания оптимального уровня глюкозы в крови и регулярного СКГ у пациентов с СД. Это особенно актуально для пациентов, использующих инсулин и принимающих пероральные сахароснижающие средства, способные спровоцировать гипогликемию [6, 19, 20]. В выпуске 12 (2025 г.) «Алгоритмов специализированной медицинской помощи больных сахарным диабетом» подчеркивается важность выбора индивидуальных целей лечения в зависимости от возраста пациента, ожидаемой продолжительности жизни, функциональной зависимости, наличия атеросклеротических сердечно-сосудистых заболеваний (АССЗ) и риска тяжелой гипогликемии (табл. 2) [6]. Для большинства взрослых пациентов с СД адекватным является целевой уровень HbA1c менее 7,0%.

Методы контроля уровня гликемии включают СКГ и непрерывный мониторинг глюкозы (НМГ), которые не следует рассматривать как конкурирующие технологии. В реальной клинической практике необходимо использовать достоинства каждого метода для лучшего управления СД [21]. СКГ с помощью глюкометра продолжает оставаться необходимым при использовании НМГ [19].
Со времен открытия инсулина СКГ является одним из значимых достижений в области лечения СД [22]. Современное понимание СКГ подразумевает определенную кратность регулярных измерений концентрации глюкозы крови и представляет собой важный ориентир, используемый врачом и пациентом для оценки результата сахароснижающей терапии и внесения необходимых корректив в план лечения. Регулярное обучение пациентов с СД является неотъемлемой частью терапевтического процесса и необходимо для эффективного СКГ. В процессе обучения приобретаются практические навыки, которые имеют решающее значение для СКГ [23].
Результаты масштабных клинических исследований в области СД однозначно показывают: поддержание оптимального уровня глюкозы в крови играет ключевую роль в предотвращении или существенном замедлении развития и ухудшения хронических диабетических осложнений [15, 16, 24]. Достижение наилучшего гликемического контроля у пациентов с СД 1 возможно при использовании интенсифицированной (базис-болюсной) инсулинотерапии, предполагающей многократные инъекции или непрерывную подкожную инфузию инсулина. Для адекватной коррекции дозы инсулина до достижения индивидуальных целевых показателей гликемического контроля необходимо учитывать результаты СКГ или НМГ в течение дня, а также количество углеводов, потребляемых с пищей, и другие факторы, влияющие на уровень глюкозы в крови. Обратимся к итогам ключевого исследования DCCT – первого масштабного продолжительного рандомизированного исследования с участием больных СД 1 [15]. Это исследование заложило основу современных подходов к лечению СД 1, подчеркнув преимущества частого СКГ в сочетании с коррекцией доз инсулина в режиме многократных инъекций для достижения индивидуальных гликемических целей по сравнению с традиционной инсулинотерапией (1–2 инъекции в сутки) и измерением глюкозы 1 раз в день. Исследование убедительно показало, что интенсивная инсулинотерапия, основанная на регулярном СКГ и индивидуальной коррекции доз инсулина, позволяет достичь уровня глюкозы в крови, близкого к норме. Это, в свою очередь, привело к значительному снижению риска развития и прогрессирования диабетических осложнений.
Эффективность инсулинотерапии связана с обязательным СКГ при СД 2. В частности, в масштабном исследовании ORIGIN титрация дозы базального инсулина гларгин-100 осуществлялась с помощью доступного алгоритма на основании СКГ, что позволило достигнуть целевого гликемического контроля при высокой безопасности проводимой инсулинотерапии [26].
Согласно результатам других исследований, уровень HbA1c начинает значимо улучшаться, как только пациент увеличивает частоту СКГ независимо от типа СД или вида сахароснижающей терапии [27–31]. В ретроспективном исследовании ROSSO (Retrolective Study Self Monitoring of Blood Glucose and Outcome in people with Type 2 Diabetes) анализу были подвергнуты данные 3268 пациентов с СД 2 за период 6,5 года, предшествующих исследованию. Среди включенных 1479 пациентов проводили СКГ, в то время как остальные его не выполняли. Как оказалось, в группе СКГ снижался на 32% риск развития диабетических осложнений (острого инфаркта миокарда, инсульта, ампутаций, слепоты, необходимости гемодиализа), а риск смерти от СД 2 – на 51%. Результаты ROSSO также свидетельствуют, что СКГ способствует увеличению продолжительность жизни, и что немаловажно, улучшению качества жизни пациентов с СД 2, независимо от характера использованной фармакотерапии [32]. Именно поэтому врачи должны уделять особое внимание СКГ.
СКГ позволяет пациентам получать и использовать информацию о показателях гликемии в повседневной жизни. Регулярные занятия спортом и поддержание двигательной активности – важная составляющая здорового образа жизни, способствующая улучшению его качества. Пациентам с СД необходимо знать о вероятных изменениях глюкозы в крови во время занятий спортом и любой двигательной активности. Однако, особенно при СД 1, физическая активность может провоцировать гипогликемию в процессе и после тренировок, поэтому основная задача – профилактика гипогликемии, связанной с физической нагрузкой [19, 33]. Регулярный СКГ или НМГ позволяет пациентам с СД, владеющим методами профилактики гипогликемий, воплощать в повседневной жизни любые виды физической активности (ФА), в том числе занятия спортом, и избежать гипогликемий с учетом следующих противопоказаний и мер предосторожности [6] (табл. 3).

СКГ дает возможность оценить индивидуальную реакцию организма на различные типы физических нагрузок и повысить заинтересованность пациентов в регулярных занятиях. Для обеспечения безопасности при выполнении физических упражнений всем пациентам необходимо контролировать уровень глюкозы в крови, особенно тем, кто получает инсулин или пероральные препараты, стимулирующие выработку инсулина. Измерение уровня глюкозы обязательно перед тренировками, временным ограничением для которых служит уровень глюкозы в плазме крови выше 13,0 ммоль/л в сочетании с кетонами в моче или 16 ммоль/л (даже при отсутствии кетонов).
Хотя регулярная ФА не является методом сахароснижающей терапии при СД 1, при СД 2 физические нагрузки способствуют достижению целевых уровней гликемии, похудению, помогают улучшить чувствительность тканей к инсулину, показатели липидного профиля крови. В настоящее время модификация образа жизни рекомендуется в качестве 1-й линии лечения СД 2, что достигается повышением физической активности и ограничением калорийности рациона [33, 34].
Показано, что СКГ повышает результат программ модификации образа жизни по коррекции образа жизни. В ретроспективном исследовании, проведенном S. Tomah и соавт., были представлены интересные данные, полученные в результате анализа программы по изменению образа жизни (Why WAIT, продолжительность 12 нед). Участникам программы (средний возраст 57±9 лет, продолжительность СД 2 10±8 лет, ИМТ 36±6 кг/м2, уровень HbA1c 7,8±1,4%, 45% на инсулинотерапии) рекомендовалось ежедневно проводить СКГ с использованием глюкометра. Измерения глюкозы следовало выполнять перед каждым приемом пищи, перед отходом ко сну, до и после физических упражнений, через 2 ч после еды, а также при подозрении на гипо- или гипергликемию [35]. В зависимости от частоты СКГ, проводимого пациентами с СД 2 в течение периода наблюдения, участники были разделены на три группы (по тертилям частоты СКГ). Средняя частота СКГ составила 2,3 (1,1–2,9) раза в сутки в группе нижнего тертиля, 3,4 (3,0–3,9) раза в сутки в группе среднего тертиля и 5 (4,0–7,7) раз в сутки в группе верхнего тертиля. Исходные средние значения массы тела пациентов составили 107,6±20,3 кг в группе нижнего тертиля частоты СКГ, 107,4±19,2 кг в группе среднего тертиля и 107,4±24 кг в группе верхнего тертиля. Исходные значения HbA1c составили 7,5%±1,0%, 8,0%±1,5% и 8,0%±1,6% соответственно для тех же групп. Группы были сопоставимы по возрасту, полу, расе, продолжительности диабета, использованию инсулина, уровню HbA1c, ИМТ.
После 12 нед наблюдения лица, практиковавшие частый СКГ, продемонстрировали существенно большее снижение массы тела, чем участники с менее регулярным мониторингом гликемии. В частности, группа, находившаяся в верхнем тертиле по частоте СКГ, достигла среднего уменьшения массы тела на 10,4 кг (в диапазоне от -7,6 до -14,4 кг). Для сравнения, в среднем и нижнем тертилях этот показатель составил 8,3 кг (от
-5,2 до -12,2 кг) и 6,9 кг (от -4,2 до -8,9 кг) соответственно (p=0,018). Аналогичная тенденция наблюдалась и в динамике ИМТ. В зависимости от тертиля частоты СКГ, изменения ИМТ составили -3,9 кг/м2 (от
-2,8 до -4,9 кг/м2), -2,7 кг/м2 (от -1,6 до -3,9 кг/м2) и
-2,5 кг/м2 (от -1,5 до 3,3 кг/м2) (p=0,012). Более высокая частота тестирования уровня глюкозы была связана со значительно лучшей динамикой HbA1c, отмеченной в конце исследования. В группе с наиболее частым СКГ снижение HbA1c составило -1,25% (от -0,6 до -3,1%), тогда как в среднем и нижнем тертилях эти значения были равны -0,8% (от -0,3 до -2%) и -0,5% (от -0,2 до
-1,2%) соответственно (p=0,048) [35].
У многих пациентов с СД одной из ключевых причин отсутствия достижения целевых показателей гликемии является недостаточный контроль уровня глюкозы в крови. К сожалению, довольно часто пациенты не следуют предписаниям врача в полной мере. Это касается не только соблюдения диетических ограничений, необходимого уровня ФА, но и регулярного СКГ. Например, в исследовании, проведенном M.V. Hansen и соавт., было установлено, что только 39% больных СД 1 ежедневно проводили СКГ, 20% делали это несколько раз в неделю, 17% – один-два раза в неделю, а 24% – реже одного раза в неделю [36]. По данным S.A. Farhan и соавт. только каждый пятый пациент с СД 2 осуществлял измерение уровня глюкозы через 2 ч после приема пищи, 16% проводили СКГ только при плохом самочувствии, а 14% – при клинических симптомах гипогликемии [37].
У пациентов с СД уровень глюкозы крови подвержен колебаниям под воздействием различных факторов, которые могут приводить как к повышению, так и к снижению гликемии. Физические нагрузки, стрессовые ситуации, употребление алкоголя, вирусные заболевания, обострения хронических болезней, а также прием определенных лекарственных препаратов, таких как глюкокортикоиды, – лишь некоторые из них. Важно отметить, что проведение СКГ позволяет вовремя выявлять факторы, влияющие на изменение уровня глюкозы, и своевременно корректировать лечение.
Гипогликемические состояния – частое явление при СД 1; различные исследования показывают, что при
СД 1 в среднем наблюдается от 0,5 до 5 тяжелых гипогликемических событий ежегодно [15, 38]. Реже гипогликемии встречаются при СД 2. Вместе с тем частота гипогликемий при СД 2 возрастает с увеличением длительности заболевания [39, 40]. Проводя сахароснижающую терапию у пациентов с СД 2, всегда следует помнить о риске гипогликемий, который могут увеличивать некоторые препараты, вместе с тем есть группы препаратов, преимуществом которых является низкий риск гипогликемий (табл. 4).

Опаснейшим исходом гипогликемии являются негативные сердечно-сосудистые события, обусловленные множеством патофизиологических механизмов. В ответ на падение уровня глюкозы в крови происходит активация симпатической и контринсулярной системы, сопровождающаяся выбросом значительного количества катехоламинов и других гормонов, что провоцирует сбои в гемодинамике, электрической стабильности сердца и процессах реполяризации, вызывает вазоконстрикцию, прокоагулянтное состояние, ухудшает реологию крови, увеличивает потребность миокарда в кислороде. Эти процессы могут приводить к изменениям регионарного кровотока, провоцировать ишемию миокарда и мозга, вызывая острый инфаркт миокарда, сердечную недостаточность или инсульт; имеются данные, подтверждающие связь между гипогликемией и сердечными аритмиями, которые потенциально предрасполагают к внезапной смерти [41].
Разнообразные факторы и состояния способны спровоцировать гипогликемию. Как уже отмечалось, случаи гипогликемии чаще наблюдаются у больных на инсулинотерапии или получающих секретагоги. В их число входят также усиленные/продолжительные или нестандартные физические нагрузки, употребление алкоголя, несистематическое питание с пропусками еды или с малым количеством углеводов, а также рвота, синдром мальабсорбции. Дополнительными факторами риска выступают пожилой возраст и расстройства когнитивных функций, почечная и печеночная недостаточность, длительность СД, автономная нейропатия, ранее перенесенные эпизоды гипогликемии, ухудшение способности распознавать гипогликемию.
Частые эпизоды гипогликемии вызывают постепенное истощение контррегуляторных защитных механизмов, что приводит к утрате способности распознавать привычные симптомы этого опасного состояния и повышает риск тяжелой гипогликемии. Как показало исследование VADT (Veterans Affairs Diabetes Trial), перенесенная тяжелая гипогликемия в четыре раза увеличивает риск смерти от сердечно-сосудистых заболеваний, причем этот фактор оказывается более значимым, чем возраст, уровень гликированного гемоглобина, нарушение липидного обмена [41].
СКГ дает возможность оперативно обнаружить состояние гипогликемии и, как следствие, вовремя принять меры для его устранения. Систематическое самостоятельное измерение уровня глюкозы в крови помогает выявлять и скрытые случаи (бессимптомные) гипогликемии. Это особенно важно для пациентов, имеющих проблемы с ощущением гипогликемии, вызванные нарушениями в работе контррегуляторных механизмов и ослаблением симпатоадреналовой реакции в ответ на гипогликемию. Потеря чувствительности к гипогликемии встречается у 20–25% пациентов с СД 1 и у 10% с СД 2 на инсулинотерапии; причем нарушение распознавания гипогликемии у пациентов с СД связано с шестикратным увеличением риска тяжелой гипогликемии, страхом гипогликемии и когнитивной дисфункцией [42, 43].
Как было отмечено ранее, для создания благоприятной «метаболической памяти» и предотвращения развития сосудистых осложнений крайне важно поддерживать целевые уровни гликемии с момента диагностики; значение гликемического контроля на ранних стадиях СД для развития осложнений становится заметным лишь спустя продолжительное время [14]. Интересные данные представлены в ретроспективном исследовании H.K. Sia и соавт., которое вовлекло 4987 пациентов с впервые выявленным СД 2 (средний возраст 56,2±11,5 года, 51,9% – мужчины). Участники были разделены на две группы в зависимости от наличия или отсутствия регулярного СКГ с момента начала сахароснижающей терапии: группа с ранним СКГ («+») и группа без раннего СКГ («-»). Результаты показали, что в реальной клинической практике систематическое проведение измерений уровня глюкозы в крови с помощью глюкометра ассоциировалось с улучшением гликемического контроля. При этом данный эффект наблюдался вне зависимости от типа применяемой сахароснижающей терапии, будь то метформин, тиазолидиндионы, ингибиторы дипептидилпептидазы-4 или препараты, стимулирующие секрецию инсулина. У пациентов, регулярно выполнявших СКГ (группа СКГ «+»), наблюдался более низкий уровень HbA1c в сопоставлении с теми, кто не осуществлял подобный мониторинг глюкозы в крови. Наибольшее расхождение в значениях достигало 0,55% по прошествии 3 мес, что сохранялось и в дальнейшем: через 6 и 12 мес различие составляло 0,45% в обоих случаях [44]. Таким образом, регулярный СКГ помогает улучшить эффект сахароснижающей терапии с момента диагностики заболевания.
Рекомендуемая частота самоконтроля гликемии
Важно обсудить с пациентом индивидуальные целевые значения основных показателей гликемического контроля и частоту проведения СКГ, что представлено в действующих рекомендациях. Однако на практике значительное число пациентов с СД нерегулярно отслеживают уровень глюкозы в крови, ограничиваясь, как правило, измерением показателя натощак. Исследование, проведенное Y. Qi и соавт., выявило, что более половины (54,1%) пациентов не осведомлены о рекомендуемой частоте СКГ, а большинство (67,62 и 95,08%) не имеют четкого представления о целевых значениях глюкозы натощак и через два часа после приема пищи [45].Рекомендуемая частота СКГ в зависимости от типа СД отражена в международных и национальных руководствах по лечению СД. В соответствии с Российскими клиническими рекомендациями, больным СД 1 без осложнений СКГ необходимо проводить не менее 4 раз ежедневно (до еды, через 2 ч после еды, на ночь, периодически ночью); при наличии признаков осложнений СД, присоединении сопутствующих заболеваний, появлении дополнительных факторов риска вопрос о частоте обследований решается индивидуально [6]. СКГ при СД 2 в дебюте заболевания, а также при недостижении целевых уровней гликемического контроля необходимо осуществлять ежедневно несколько раз; в дальнейшем его частота определяется видом сахаро-снижающей терапии (табл. 5).

Надо сказать, что рекомендации по частоте СКГ при СД 2 могут быть распространены и на больных с другими специфическими типами СД.
Использование СКГ дает врачу возможность определить, насколько эффективна назначенная немедикаментозная и медикаментозная терапия. Пациенты, в свою очередь, получают возможность принимать активное участие в процессе своего лечения, что ведет к большей осознанности и приверженности плану лечения, предложенному врачом, а также повышает их личную ответственность за достигнутые результаты.
Не стоит думать, что сам по себе СКГ улучшит показатели гликемии. Положительный результат достигается, когда пациент с СД, обладающий необходимыми знаниями, использует данные СКГ для принятия обдуманных решений в своей повседневной жизни [46, 47]. Активное участие больного в этом процессе подразумевает способность сопоставлять собственные показатели уровня глюкозы в крови с индивидуальными целевыми значениями, находить взаимосвязи между образом жизни (повседневной активностью, физической нагрузкой, пищевым рационом), терапией и текущими показателями глюкозы. Это также требует тщательного анализа факторов, мешающих достижению оптимального контроля гликемии, и определения причин отклонений уровня глюкозы в крови от целевых значений.
Пациенты с СД часто сталкиваются с трудностями в соблюдении рекомендаций по изменению рациона питания. СКГ дает наглядное представление о том, как различные продукты влияют на уровень гликемии после еды. Это позволяет оперативно корректировать рацион, обеспечивая сбалансированное питание, что, несомненно, способствует более эффективному лечению. Однако, чтобы в полной мере использовать преимущества СКГ, пациентам с СД необходимо систематическое обучение, которое поможет им правильно применять методы СКГ и анализировать полученные данные для оптимизации терапии. Только так можно добиться значимых улучшений в управлении СД [47].

Возможности и преимущества современных глюкометров
Со временем подходы к мониторингу глюкозы в крови заметно изменились, обогатившись передовыми технологиями. Появление современных глюкометров для индивидуального пользования, характеризующихся простотой и удобством применения, значительно увеличили число пациентов с СД, способных самостоятельно отслеживать концентрацию глюкозы в крови. В настоящее время для СКГ рекомендуется применять персональные глюкометры, в том числе с настройкой индивидуального целевого диапазона гликемии, с функцией беспроводной передачи данных об уровне глюкозы крови медицинским специалистам, родственникам или в установленное на смартфон пациента специальное приложение для использования при дистанционном наблюдении. Индивидуальные глюкометры должны соответствовать ГОСТ Р ИСО 15197–2015 по аналитической и клинической точности, что позволяет повысить эффективность и безопасность сахароснижающей терапии [6].Один из современных глюкометров, соответствующий всем требованиям, предъявляемым к приборам индивидуального использования, – глюкометр Контур Плюс Уан (ContourTM Plus One), который показал высокую точность как в лабораторных, так и клинических условиях. Умная система ContourTM Plus One состоит из 4 компонентов: тест-полоска, глюкометр, мобильное приложение и облачное хранилище данных (рис. 2). Благодаря интеграции глюкометра с бесплатным мобильным приложением (доступно для скачивания в онлайн-магазинах приложений) значительно расширяются возможности управления СД со стороны пациента и взаимодействия с врачом.
Высокая точность определения концентрации глюкозы в крови в сочетании с удобством использования данного глюкометра и другими передовыми решениями способствует формированию позитивного отношения пациентов к СКГ. Это позволяет избежать ошибочных действий в терапии, например неверной дозировки инсулина, и, как следствие, достичь оптимальных показателей контроля гликемии.
При выборе глюкометра следует учитывать несколько ключевых аспектов: не только его соответствие современным требованиям к точности, но и интуитивно простой и понятный интерфейс, удобство применения, легкость получения результата пациентами, экономичность. Данные критерии гарантируют беспроблемное проведение измерения уровня глюкозы в крови пациентами всех возрастных групп.
Технология нанесения образца крови «Второй шанс» позволяет пациентам повторно наносить кровь на ту же самую тест-полоску, если первоначального образца было недостаточно, и измерить уровень глюкозы в крови. Повторное нанесение возможно в течение минуты, при этом нет необходимости дополнительного прокола пальца. Это особенно важно для лиц с СД, в частности для пациентов старшего возраста. Удобство использования прибора также заключается в быстром времени измерения уровня глюкозы в крови – всего 5 с, что является критически важным при развитии гипогликемии.
Глюкометр оборудован световым индикатором в области порта для тест-полосок, использующим цветовую схему, аналогичную светофору – функция «Умная подсветка», которая предоставляет мгновенную обратную связь, сигнализируя цветом об уровне глюкозы, и позволяет пользоваться глюкометром при различном освещении. Это помогает пользователю визуально оценивать результаты измерения: зеленый цвет указывает на то, что уровень глюкозы в крови находится в пределах нормы, желтый и красный цвета – о повышенном или пониженном уровне глюкозы соответственно.
Устройство способно автоматически устанавливать связь с бесплатным мобильным приложением Контур Диабитис (Contour Diabetes) и последующей загрузкой всех показателей измерений глюкозы в электронный дневник – расширенную цифровую версию дневника самоконтроля. Для пациентов с СД это открывает доступ к широким возможностям сбора и анализа информации, поскольку все важные для управления уровнем глюкозы данные фиксируются в электронном дневнике, позволяя пользователям более эффективно отслеживать уровень глюкозы в крови (например, указывая пометки «до еды» и «после еды»), регистрировать дозировку лекарств, потребление углеводов, добавлять комментарии и детализированные записи о приемах пищи, загружать фотографии еды, а также фиксировать изменения в своем образе жизни и другие важные факторы.
Функция «Мои тенденции» позволяет отслеживать динамику показателей глюкозы в крови и оповещает пользователя о потенциальных причинах, влияющих на эти колебания гликемии. Важно отметить, что фиксация положительных изменений уровня глюкозы в крови благодаря сбалансированному питанию и систематическим занятиям физическими упражнениями может стать мощным мотиватором для пациента, способствуя укреплению приверженности здоровому образу жизни и повышению качества жизни [48, 49].
С помощью функции отчетов, сгенерированных на основе всей информации, поступающей в мобильное приложение Контур Диабитис, появляется возможность внедрить современные цифровые решения в коммуникацию между пациентом и врачом, тем самым повышая эффективность лечения. Благодаря синхронизации мобильного приложения с облачным хранилищем данных (Российский сервер) пациенты могут оперативно передавать врачу полную информацию о результатах СКГ в крови в цифровом виде. Это обеспечивает возможность совместного анализа причин изменений уровня сахара, выявления критических ситуаций и своевременного обращения к специалисту.
Подводя итоги, следует отметить, что современная сахароснижающая терапия предусматривает обязательное проведение СКГ. Система Контур Плюс Уан характеризуется высокой степенью точности, интуитивно понятным способом измерения уровня глюкозы в крови, а также интеграцией информационных технологий для поддержания связи между пациентом и врачом. Эти возможности широко реализованы в различных функциях системы, что позволяет пациентам активно участвовать в процессе лечения СД и максимально эффективно использовать преимущества СКГ в повседневной жизни.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Бирюкова Елена Валерьевна – д-р мед. наук, проф. каф. эндокринологии и диабетологии, ФГБОУ ВО «Российский университет медицины». E-mail: lena@obsudim.ru; ORCID: 0000-0001-9007-4123
Elena V. Biryukova – Dr. Sci. (Med.), Prof., Russian University of Medicine (ROSUNIMED). E-mail: lena@obsudim.ru; ORCID: 0000-0001-9007-4123
Соловьева Инна Владимировна – ассистент каф. эндокринологии и диабетологии, ФГБОУ ВО «Российский университет медицины»; зав. отд-нием эндокринологии, ГБУЗ «МКНЦ им. А.С. Логинова». E-mail: Inna.dell.85@mail.ru; ORCID: 0000-0002-2125-622X
Inna V. Solovyova – Аssistant, Russian University of Medicine (ROSUNIMED); Head of the Department of Endocrinology, Loginov Moscow Clinical Research Center. E-mail: Inna.dell.85@mail.ru;
ORCID: 0000-0002-2125-622X
Поступила в редакцию: 18.06.2025
Поступила после рецензирования: 24.06.2025
Принята к публикации: 26.06.2025
Received: 18.06.2025
Revised: 24.06.2025
Accepted: 26.06.2025
Список исп. литературыСкрыть список1. International Diabetes Federation – 2025. IDF Diabetes Atlas 11th Edition. URL: https://diabetesatlas.org/resources/idf-diabetes-atlas-2025/
2. Khan MAB, Hashim MJ, King JK et al. Epidemiology of type 2 diabetes – global burden of disease and forecasted trends. J Epidemiol Glob Health 2020;10:107-11. DOI: 10.2991/jegh.k.191028.001
3. Gerstein HC, Santaguida P, Raina P et al. Annual incidence and relative risk of diabetes in people with various categories of dysglycemia: a systematic overview and meta-analysis of prospective studies. Diabetes Res Clin Pract 2007;78:305-12. DOI: 10.1016/j.diabres.2007.05.004
4. Mainous AG, Tanner RJ, Jo A, Anton SD. Prevalence of Prediabetes and Abdominal Obesity Among Healthy-Weight Adults: 18-Year Trend. Ann Fam Med 2016;14(4):304-10. DOI: 10.1370/afm.1946
5. Dedov II, Shestakova MV, Benedetti MM et al. Prevalence of Type 2 diabetes mellitus (T2DM) in the adult Russian population (NATION study). Diabetes Research and Clinical Practice 2016;115:90-5. DOI: 10.1016/j.diabres.2016.02.010
6. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. Под редакцией И.И. Дедова, М.В. Шестаковой, О.Ю. Сухаревой. 12-й выпуск, М., 2025.
Standards of specialized diabetes care. Edited by I.I. Dedov, M.V. Shestakova, O.Yu. Sukhareva. 12 Edition (revised). Moscow, 2025 (in Russian).
7. Kolarić V, Svirčević V, Bijuk R, Zupančič V. Chronic complicationof diabetes and qualitu of life. Acta Clin Croat 2022;61(3):520-27. DOI: 10.20471/acc.2022.61.03.18
8. Harding JL, Pavkov ME, Magliano DJ et al. Global trends in diabetes complications: a review of current evidence. Diabetologia 2019;62:3-16. DOI: 10.1007/s00125-018-4711-2
9. Maranta F, Cianfanelli L, Cianflone D. Glycaemic control and vascular complications in diabetes mellitus type 2. Adv Exp Med Biol 2021;1307:129-52. DOI: 10.1007/5584_2020_514
10. Bommer C, Sagalova V, Heesemann E et al. Global economic burden of diabetes in adults: projections from 2015 to 2030. Diabetes Care 2018;41(5):963-70. DOI: 10.2337/dc17-1962
11. Дедов И.И., Шестакова М.В. Проблемы контроля качества диабетологической службы в России по данным на январь 2007 г. Сахарный диабет. 2008;11(3):55-7.
Dedov I.I., Shestakova M.V. Problems of quality control of diabetological services in Russia as of January 2007. Diabetes Mellitus. 2008;11(3):55-7 (in Russian).
12. Lu X, Xie Q, Pan X et al. Type 2 diabetes mellitus in adults: pathogenesis, prevention and therapy. Signal Transduct Target Ther 2024;9(1):262. DOI: 10.1038/s41392-024-01951-9
13. Khunti K, Ceriello A, Cos X, De Block C. Achievement of guideline targets for blood pressure, lipid, and glycaemic control in type 2 diabetes: A meta-analysis. Diabetes Res Clin Pract 2018 Mar;137:137-48. DOI: 10.1016/j.diabres.2017.12.004
14. Черников А.А., Северина А.С., Шамхалова М.Ш., Шестакова М.В. Роль механизмов «метаболической памяти» в развитии и прогрессировании сосудистых осложнений сахарного диабета. Сахарный диабет. 2017;20(2):126-34. DOI: 10.14341/7674
Chernikov A.A., Severina A.S., Shamkhalova M.Sh., Shestakova M.V. The role of "metabolic memory" mechanisms in the development and progression of vascular complications of diabetes mellitus. Diabetes Mellitus. 2017;20(2):126-34. DOI: 10.14341/7674 (in Russian).
15. Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications (DCCT/EDIC) Research Group, Nathan D.M., Zinman B et al. Modern-day clinical course of type 1 diabetes mellitus after 30 years' duration: the diabetes control and complications trial/epidemiology of diabetes interventions and complications and Pittsburgh epidemiology of diabetes complications experience (1983–2005). Arch Intern Med 2009;169(14);1307-16. DOI: 10.1001/archinternmed.2009.193
16. Stratton IM, Adler AI, Neil HA et al. Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study. BMJ 2000;321(7258): 405-12. DOI: 10.1136/bmj.321.7258.405
17. Roberto T, Rita BA, Prattichizzo F et al. The “Metabolic Memory” theory and the early treatment of hyperglycemia in prevention
of diabetic complications. Nutrients 2017;9(5):437. DOI: 10.3390/nu9050437
18. Pleus S, Freckmann G, Schauer S et al. Self-Monitoring of Blood Glucose as an Integral Part in the Management of People with Type 2 Diabetes Mellitus. Diabetes Ther 2022;13(5):829-46. DOI: 10.1007/ s13300-022-01254-8
19. Phillips PJ, Leow S. HbA1c, blood glucose monitoring and insulin therapy. Aust Fam Physician 2014;43(9):611-5.
20. American Diabetes Association Professional Practice Committee. 7. Diabetes technology: Standards of Care in Diabetes – 2025. Diabetes Care 2025;48(Suppl.1):S146-S166. URL: https://ntag.nhs.uk/wp-content/uploads/2025/02/NENC-Guidelines-Self-Monitoring-of-Blood-Glucose-and-Ketones-in-Diabetes-update-Jan-2025-approved.pdf
21. Аметов А.С., Камынина Л.Л. Современный подход к управлению диабетом: фокус на терапевтическом обучении и инновационных технологиях. Эндокринология: новости, мнения, обучение. 2013;(1):37-42.
Ametov A.S., Kamynina L.L. Modern approach to diabetes management: focus on therapeutic training and innovative technologies. Endocrinology: news, opinions, training. 2013;(1):37-42 (in Russian).
22. Benjamin EM. Self-Monitoring of Blood Glucose: The Basics. Clin Diabetes 2002;20(1): 45-7. DOI: 10.2337/diaclin.20.1.45
23. Майоров А.Ю., Мельникова О.Г., Филиппов Ю.И. Вопросы самоконтроля гликемии в практике лечения сахарного диабета. Справочник поликлинического врача. 2012;(12):32-6.
Mayorov A.Yu., Melnikova O.G., Filippov Yu.I. Issues of self-control of glycemia in the practice of diabetes mellitus treatment. Polyclinic doctor's Handbook. 2012;(12):32-6 (in Russian).
24. Casanova F, Adingupu DD, Adams F et al. The impact of cardiovascular co-morbidities and duration of diabetes on the association between microvascular function and glycaemic control. Cardiovasc Diabetol 2017;16:114.
25. Schnell O, Hanefeld M, Monnier L. Self-monitoring of blood glucose: a prerequisite for diabetes management in outcome trials. J Diabetes Sci Technol 2014;8(3):609-14. DOI: 10.1177/1932296814528134
26. ORIGIN Trial Investigators, Gerstein H, Yusuf S et al. Rationale, design, and baseline characteristics for a large international trial of cardiovascular disease prevention in people with dysglycemia: the
ORIGIN Trial (Outcome Reduction with an Initial Glargine Intervention). Am Heart J 2008;155(1):26-32. DOI: 10.1016/j.ahj.2007.09.009
27. Rao PV, Makkar BM, Kumar A et al. RSSDI consensus on self-monitoring of blood glucose in types 1 and 2 diabetes mellitus in India. Int J Diabetes Dev Ctries 2018;38:260-79. DOI: 10.1007/s13410-018-0677-3
28. Clar C, Barnard K, Cummins E, Royle P et al. Self-monitoring of blood glucose in type 2 diabetes: systematic review. Health Technol Assess 2010;14(12):1-140. DOI: 10.3310/hta14120
29. Hou YY, Li W, Qiu JB, Wang XH. Efficacy of blood glucose self-monitoring on glycemic control in patients with non-insulin-treated type 2 diabetes: a meta-analysis. Int J Nurs Sci 2014;1(2):191-5. DOI: 10.1016/j.ijnss.2014.05.003
30. Poolsup N, Suksomboon N, Rattanasookchit S. Meta-analysis of the benefits of self-monitoring of blood glucose on glycemic control in type 2 diabetes patients: an update. Diabetes Technol Ther 2009;11(12):775-84. DOI: 10.1089/dia.2009.0091
31. Sia HK, Kor CT, Tu ST et al. Self-monitoring of blood glucose in association with glycemic control in newly diagnosed non-insulin-treated diabetes patients: a retrospective cohort study. Sci Rep 2021;11(1):1176. DOI: 10.1038/s41598-021-81024-x
32. Schneider B, Martin S, Heinemann L et al. Interrelations between diabetes therapy, self-monitoring of blood glucose, blood glucose and non-fatal or fatal endpoints in patients with type 2 diabetes / results of a longitudinal cohort study (ROSSO 5). Arzneimittelforschung 2007;57(12):762-9. DOI: 10.1055/s-0031-1296677
33. Colberg SR, Sigal RJ,Yardley JE et al. Physical Activity/Exercise and Diabetes: A Position Statement of the American Diabetes Association. Diabetes Care 2016;39(11):2065-79. DOI: 10.2337/dc16-1728
34. Shah SZA, Karam JA, Zeb A et al. Movement is improvement: the therapeutic effects of exercise and general physical activity on glycemic control in patients with type 2 diabetes mellitus: a systematic review and meta-analysis of randomized controlled trials. Diabetes Therapy 2021;12(3):707-32. DOI: 10.1007/s13300-021-01005-1
35. Tomah S, Mahmoud N, Mottalib A et al. Frequency of self-monitoring of blood glucose in relation to weight loss and A1C during intensive multidisciplinary weight management in patients with type 2 diabetes and obesity. BMJ Open Diabetes Res Care 2019;7(1):e000659. DOI: 10.1136/bmjdrc-2019-000659
36. Hansen MV, Pedersen-Bjergaard U, Heller SR et al. Frequency and motives of blood glucose self-monitoring in type 1 diabetes. Diabetes Res Clin Pract 2009;85:183-8. DOI: 10.1016/j.diabres.2009.04.022
37. Farhan SA, Shaikh AT, Ziaet M et al. Prevalence and Predictors of Home Use of Glucometers in Diabetic Patients. Cureus 2017;9(6):e1330. DOI: 10.7759/cureus.1330
38. Khunti K, Alsifri S, Aronson R. Rates and predictors of hypoglycaemia in 27 585 people from 24 countries with insulin-treated type 1 and type 2 diabetes: the global HAT study. Diabet Obes Metab 2016;18(9):907-15. DOI: 10.1111/dom.12689
39. Seaquist ER, Miller ME, Bonds DE et al. The Impact of Frequent and Unrecognized Hypoglycemia on Mortality in the ACCORD Study. Diabetes Care 2012;35(2):409-14. DOI: 10.2337/dc11-0996
40. Katsiki N, Kotsa K, Stoian AP, Mikhailidis DP. Hypoglycaemia and Cardiovascular Disease Risk in Patients with Diabetes. Curr Pharm Des 2020;26(43):5637-49. DOI: 10.2174/1381612826666200909142658
41. Duckworth WC, McCarren M, Abraira С. Glucose Control and Cardiovascular Complications: The VA Diabetes Trial. Diabetes Care 2001;24(5):942-5 DOI: 10.2337/diacare.24.5.942
42. McNeilly AD, Rory J McCrimmon Impaired hypoglycaemia awareness in type 1 diabetes: lessons from the lab. Diabetologia 2018;61(4):743-50. DOI: 10.1007/s00125-018-4548-8
43. Graveling AJ, Frier BM. Impaired awareness of hypoglycaemia: a review. Diabetes Metab 2010;36(Suppl 3):S64-74. DOI: 10.1016/S1262-3636(10)70470-5
44. Sia HK, Kor CT, Tu ST. Self-monitoring of blood glucose in association with glycemic control in newly diagnosed non-insulin-treated diabetes patients: a retrospective cohort study. Scientific Reports 2021;11(1):1176. DOI: 10.1038/s41598-021-81024-x
45. Qi Y, Feng W. Cause analysis and nursing countermeasures of self-monitoring of blood glucose in diabetic patients. Electronic J Pract Clin Nurs 2017;16:44-5. DOI: 10.3969/j.issn.2096-2479.2017.16.034
46. Chrvala CA, Sherr D, Lipman RD. Diabetes self-management education for adults with type 2 diabetes mellitus: A systematic review of the effect on glycemic control. Patient Educ Couns 2016;99(6):926-43. DOI: 10.1016/j.pec.2015.11.003
47. Pleus S, Freckmann G, Schauer S et al. Self-Monitoring of Blood Glucose as an Integral Part in the Management of People with Type 2 Diabetes Mellitus. Diabetes Ther 2022;13(5):829-46. DOI: 10.1007/ s13300-022-01254-8
48. Parkin CG, Davidson JA. Value of self-monitoring blood glucose pattern analysis in improving diabetes outcomes. J Diabetes Sci Technol 2009;3(3):500-8. DOI: 10.1177/193229680900300314
49. Li Z, Hu Y, Yan R, Li H et al. Twenty Minute Moderate-Intensity Post-Dinner Exercise Reduces the Postprandial Glucose Response in Chinese Patients with Type 2 Diabetes. Med Sci Monit 2018; 24:7170-7. DOI: 10.12659/MSM.910827.
16 июля 2025
Количество просмотров: 297


