Клинический разбор в общей медицине №8 2025
Клинический разбор в общей медицине №8 2025
Негормональная коррекция стресс-ассоциированных нарушений менструального цикла: данные исследования МОНАРХ о применении комплекса Мабелль Цикл
Номера страниц в выпуске:86-94
Аннотация
Цель. Оценить эффективность и безопасность использования препарата Мабелль Цикл в коррекции стресс-зависимых расстройств менструального цикла (МЦ).
Материалы и методы. Проведено исследование с участием 80 пациенток в возрасте 18–31 года (средний возраст 24,41±2,95 года) со стресс-зависимыми расстройствами МЦ (по Международной классификации болезней 10-го пересмотра: N91.1 Вторичная аменорея, N91.2 Аменорея неуточненная). Участницы были разделены на две статистически гомогенные группы в соотношении 1:1. Первая, основная, группа (40 пациенток) получала Мабелль Цикл (активные компоненты: экстракт клевера лугового, экстракт плодов витекса священного, экстракт корня дудника китайского, экстракт семян гриффонии простолистной, D,L-фенилаланин, железо) 3 мес по 2 таблетки в сутки, вторая, контрольная (40 пациенток), – немедикаментозную терапию (консультацию психолога, физиотерапию). Длительность терапии составила 3 мес. Эффективность оценивалась по восстановлению МЦ, динамике менструальных симптомов и показателям опросника MEDI-Q, безопасность – по частоте возникновения нежелательных реакций. Дизайн исследования – открытое независимое неинтервенционное проспективное.
Результаты. После применения фитокомплекса Мабелль Цикл наблюдалось восстановление МЦ у 22,5% пациенток в 1-м месяце, 50,0% – во 2-м и 62,5% – в 3-м по сравнению с 7,5%, 17,5% и 27,5% в группе контроля, соответственно. Статистически значимые различия выявлены со 2-го месяца терапии (p=0,008). Помимо восстановления МЦ отмечены значимое снижение лабильности настроения (с 45,0% до 7,5%, p=0,015), масталгии (с 40,0% до 10,0%, p=0,008), полное купирование депрессивных симптомов (p<0,001) в группе
Мабелль Цикл. Также было показано статистически значимое улучшение по симптому «отечность» уже ко 2-му визиту (р=0,005). Общий балл MEDI-Q в группе, получавшей фитокомплекс, снизился с 58,00 до 33,00 (p=0,001) с достижением значимых межгрупповых различий к концу исследования (p=0,001).
Заключение. Мабелль Цикл демонстрирует высокую эффективность и безопасность в восстановлении МЦ при стресс-зависимых расстройствах. Применение фитокомплекса в течение 3 мес обеспечивает достоверное улучшение регулярности цикла, снижение выраженности психоэмоциональных и соматических симптомов, повышение качества жизни пациенток. Полученные результаты позволяют рекомендовать комплекс Мабелль Цикл для включения в клинические протоколы ведения пациенток со стресс-зависимыми расстройствами МЦ.
Ключевые слова: стресс-зависимая аменорея, нарушения менструального цикла, фитотерапия.
Для цитирования: Радзинский В.Е., Оразов М.Р., Хамошина М.Б., Орехов Р.Е., Муллина И.А., Лесная О.А. Негормональная коррекция стресс-ассоциированных нарушений менструального цикла: данные исследования МОНАРХ о применении комплекса Мабелль Цикл. Клинический разбор в общей медицине. 2025; 6 (8): 86–94. DOI: 10.47407/kr2025.6.8.00663
Цель. Оценить эффективность и безопасность использования препарата Мабелль Цикл в коррекции стресс-зависимых расстройств менструального цикла (МЦ).
Материалы и методы. Проведено исследование с участием 80 пациенток в возрасте 18–31 года (средний возраст 24,41±2,95 года) со стресс-зависимыми расстройствами МЦ (по Международной классификации болезней 10-го пересмотра: N91.1 Вторичная аменорея, N91.2 Аменорея неуточненная). Участницы были разделены на две статистически гомогенные группы в соотношении 1:1. Первая, основная, группа (40 пациенток) получала Мабелль Цикл (активные компоненты: экстракт клевера лугового, экстракт плодов витекса священного, экстракт корня дудника китайского, экстракт семян гриффонии простолистной, D,L-фенилаланин, железо) 3 мес по 2 таблетки в сутки, вторая, контрольная (40 пациенток), – немедикаментозную терапию (консультацию психолога, физиотерапию). Длительность терапии составила 3 мес. Эффективность оценивалась по восстановлению МЦ, динамике менструальных симптомов и показателям опросника MEDI-Q, безопасность – по частоте возникновения нежелательных реакций. Дизайн исследования – открытое независимое неинтервенционное проспективное.
Результаты. После применения фитокомплекса Мабелль Цикл наблюдалось восстановление МЦ у 22,5% пациенток в 1-м месяце, 50,0% – во 2-м и 62,5% – в 3-м по сравнению с 7,5%, 17,5% и 27,5% в группе контроля, соответственно. Статистически значимые различия выявлены со 2-го месяца терапии (p=0,008). Помимо восстановления МЦ отмечены значимое снижение лабильности настроения (с 45,0% до 7,5%, p=0,015), масталгии (с 40,0% до 10,0%, p=0,008), полное купирование депрессивных симптомов (p<0,001) в группе
Мабелль Цикл. Также было показано статистически значимое улучшение по симптому «отечность» уже ко 2-му визиту (р=0,005). Общий балл MEDI-Q в группе, получавшей фитокомплекс, снизился с 58,00 до 33,00 (p=0,001) с достижением значимых межгрупповых различий к концу исследования (p=0,001).
Заключение. Мабелль Цикл демонстрирует высокую эффективность и безопасность в восстановлении МЦ при стресс-зависимых расстройствах. Применение фитокомплекса в течение 3 мес обеспечивает достоверное улучшение регулярности цикла, снижение выраженности психоэмоциональных и соматических симптомов, повышение качества жизни пациенток. Полученные результаты позволяют рекомендовать комплекс Мабелль Цикл для включения в клинические протоколы ведения пациенток со стресс-зависимыми расстройствами МЦ.
Ключевые слова: стресс-зависимая аменорея, нарушения менструального цикла, фитотерапия.
Для цитирования: Радзинский В.Е., Оразов М.Р., Хамошина М.Б., Орехов Р.Е., Муллина И.А., Лесная О.А. Негормональная коррекция стресс-ассоциированных нарушений менструального цикла: данные исследования МОНАРХ о применении комплекса Мабелль Цикл. Клинический разбор в общей медицине. 2025; 6 (8): 86–94. DOI: 10.47407/kr2025.6.8.00663
Original Article
Irina A. Mullina2, Olesia A. Lesnaya1
1Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2Semashko Clinical Hospital “Russian Railways-Medicine”, Moscow, Russia
omekan@mail.ru
Abstract
Aim. To evaluate the efficacy and safety of using the complex herbal preparation Mabell Cycle in the treatment of stress-dependent menstrual disorders.
Materials and methods. Prospective, open-label, non-interventional study was conducted with 80 patients aged 18–31 years (mean age 24.41±2.95 years) with stress-dependent menstrual disorders. The participants were ratio into two groups: the main group (n=40) received
Mabelle Cycle (active ingredients: Trifolium pratense (red clover) extract, Vitex agnus-castus extract, Angelica sinensis root extract, Griffonia simplicifolia extract, D,L-phenylalanine, iron) at a dose of 2 tablets daily for 3 months, while the control group (n=40) received non-drug therapy (consultation with a psychologist, physiotherapy) following the same regimen. The duration of therapy was 3 months. Efficacy was assessed by menstrual cycle restoration, dynamics of premenstrual syndrome symptoms, and MEDI-Q questionnaire indicators. Safety assessent was based on the incidence of adverse reactions. Study design: prospective, open-label, non-interventional.
Results. The Mabell Cycle group showed progressive restoration of the menstrual cycle: 22.5%, 50.0%, and 62.5% of patients over three months of therapy compared to 7.5%, 17.5%, and 27.5% in the control group, respectively. Statistically significant differences were detected from the second month of therapy (p=0.008). The Mabell Cycle group showed significant reduction in mood lability (from 45.0% to 7.5%, p=0.015), mastalgia (from 40.0% to 10.0%, p=0.008), complete resolution of depressive symptoms (p<0.001), and improvement in five out of six evaluated psycho-emotional parameters versus three in the control group. The total MEDI-Q score in the Mabell Cycle group decreased from 58.00 to 33.00 (p=0.001), achieving significant intergroup differences by the end of the study (p=0.001).
Conclusion. The multitarget phytocomplex Mabell Сycle demonstrates high efficacy and safety in restoring the menstrual cycle in stress-dependent disorders. The use of a phytocomplex for 3 months provides significant improvement in cycle regularity, reduction in the severity of psycho-emotional and somatic symptoms, and enhancement of patients' quality of life. The results obtained allow recommending the phytocomplex
Mabell Cycle for inclusion in clinical protocols for managing patients with stress-dependent menstrual disorders.
Keywords: stress-dependent amenorrhea, menstrual disorders, phytotherapy.
For citation: Radzinskiy V.E., Orazov M.R., Khamoshina M.B., Orekhov R.E., Mullina I.A., Lesnaya O.A. Clinical review for general practice. 2025; 6 (8): 86–94 (In Russ.). DOI: 10.47407/kr2025.6.8.00663
1) расстройства, связанные с МЦ, где функция яичников, как правило, не изменена, а патогенетической основой служат нарушения центральной нервной системы или заболевания органов-мишеней;
2) расстройства ритма менструаций, при которых патогенетической основой, как правило, служат различные варианты яичниковой недостаточности или овариальной дисфункции [1].
Несмотря на высокую распространенность стресса и его научно доказанное негативное влияние на здоровье, прямые механизмы его воздействия на расстройства МЦ до сих пор неясны и остаются на уровне гипотез.
Стресс-зависимые нарушения МЦ (СНМЦ) представляют собой комплексную группу патологических состояний, этиологически связанных с воздействием стрессогенных факторов и клинически проявляющихся нарушениями ритма менструаций или специфическими симптомами, сопряженными с МЦ [1–5]. В соответствии с Международной классификацией болезней 10-го пересмотра (МКБ-10) не существует легитимного диагноза «стресс-индуцированные нарушения ритма менструаций», их можно классифицировать преимущественно в рамках рубрики N91, охватывающей отсутствие, скудость и редкость менструальных кровотечений. Современный научный дискурс характеризуется терминологическим разнообразием: «стресс-провоцированная», «стресс-зависимая» и «гипоталамическая аменорея» часто употребляются как равнозначные понятия, причем термин «гипоталамическая» в ряде исследований замещается определением «психогенная», что подчеркивает первостепенную роль дисфункции центральной нервной системы в патогенезе данного состояния [1, 4–6].
Патогенетическая взаимосвязь между стрессовым фактором и нарушениями МЦ реализуется через сложный каскад нейроэндокринных изменений [6]. Для СНМЦ характерен дисбаланс гонадотропных гормонов, проявляющийся в снижении уровня лютеинизирующего гормона (ЛГ) при относительно сохранной секреции фолликулостимулирующего гормона (ФСГ). Клинические варианты определяются как «нормогонадотропная» или «гипогонадотропная» аменорея в зависимости от концентрации ЛГ (выше или ниже 3 мЕд/мл соответственно) [7]. В действующих клинических рекомендациях («Аменорея и олигоменорея», 2024 г.) вторичную аменорею, связанную с дисфункцией гипоталамуса, определяют как функциональную гипоталамическую (ФГА), для которой характерно прекращение менструаций на фоне стресса, чрезмерных физических нагрузок и/или снижения массы тела [8]. Стрессовое воздействие на гипоталамо-гипофизарно-яичниковую ось может нарушать процесс формирования доминантного фолликула, приводя к развитию синдрома хронической ановуляции [1].
Клинический спектр СНМЦ включает разнообразные проявления: вторичную аменорею, частота которой у женщин репродуктивного возраста достигает 3–5%
[2, 9]; первичную аменорею, составляющую примерно 3% от всех случаев ФГА [1]; аномальные маточные кровотечения; а также соматические и эмоциональные циклические расстройства, в том числе предменструальный синдром (ПМС) и предменструальное дисфорическое расстройство. Важно отметить, что стрессовые факторы, провоцирующие СНМЦ, не обязательно носят экстремальный характер – дистресс может быть обусловлен повседневными психосоциальными обстоятельствами, связанными с бытовой, учебной, профессиональной или семейной сферами жизни [1]. В условиях урбанизации и возрастающих психоэмоциональных нагрузок современного общества наблюдается тенденция к увеличению распространенности СНМЦ среди женского населения.
В настоящее время в рутинной практике врача акушера-гинеколога особую актуальность приобретает поиск эффективных методов коррекции нарушений МЦ, в частности стресс-зависимой аменореи, с использованием фитотерапевтических средств. Анализ современной научной литературы свидетельствует о значительном интересе исследователей к использованию фитокомплексов в регуляции МЦ, что подтверждается множеством систематических обзоров и метаанализов [10–14].
Особый интерес представляет изучение эффективности комплексной фитотерапии, каждый компонент которой обладает определенным терапевтическим потенциалом в регуляции разных уровней репродуктивной системы.
В рамках проведенного исследования изучалось влияние комплекса Мабелль Цикл, который в своем составе содержит: экстракт плодов витекса священного, экстракт клевера лугового, экстракт корня дудника китайского, экстракт семян гриффонии простолистной (источник 5-гидрокситриптофана – 5-НТР), D,L-фенилаланин, железо.
Витекс священный способствует нормализации уровня пролактина, что приводит к регуляции МЦ и уменьшению выраженности клинических проявлений ПМС [10, 12]. Систематические обзоры демонстрируют неоднородность доказательной базы различных фитотерапевтических средств в коррекции расстройств МЦ. Наиболее изученным является витекс священный, эффективность которого подтверждена в 17 рандомизированных контролируемых исследованиях. Метаанализ показал значительный суммарный размер эффекта (g=-1.21) в отношении купирования выраженности ПМС, хотя высокий показатель гетерогенности (I²=91%) указывает на существенные различия между исследованиями [10, 12]. Также в ряде исследований отмечается потенциал влияния витекса священного на регулярность МЦ [15].
Клевер луговой содержит фитоэстрогены, обладает мочегонным эффектом, способствуя уменьшению предменструального отечного синдрома. Высокое содержание магния в нем оказывает положительное влияние на психоэмоциональное состояние пациенток [16]. Современные исследования традиционной китайской медицины также подтверждают потенциал фитоэстрогенов в регуляции женской репродуктивной системы [17].
Дудник китайский богат фитоэстрогенами и витамином Е, в систематическом обзоре традиционной китайской медицины отмечается его эффективность при различных нарушениях репродуктивной системы [11–13].
Гриффония простолистная, являющаяся источником 5-НТР, представляет особый интерес в контексте коррекции психоэмоциональных нарушений. Исследования показывают, что 5-НТР эффективно способствует нормализации уровня серотонина, что особенно важно при СНМЦ [18].
Включение в состав комплексного средства D,L-фенилаланина и железа обосновано их ролью в нормализации психоэмоционального состояния и восполнении физиологических потерь железа соответственно.
Фенилаланин, являясь незаменимой аминокислотой, участвует в биохимических процессах головного мозга, способствуя улучшению настроения и снижению болевой чувствительности [19, 20].
Растущий интерес к фитотерапевтическим средствам обосновывает необходимость в дополнительных исследованиях их эффективности и безопасности с использованием современных методологических подходов. Особенно актуальным является изучение комплексных составов, которые содержат несколько активных фитокомпонентов, их синергетического действия и безопасности применения при СНМЦ. Проблема методологического качества существующих исследований, включая небольшие размеры выборок и различные подходы к оценке эффективности, подчеркивает необходимость крупномасштабных рандомизированных контролируемых исследований с четкими стандартизированными протоколами [10, 13].
Открытое независимое неинтервенционное проспективное исследование МОНАРХ (MONARCH) с целью оценки эффективности и безопасности использования Мабелль Цикл в коррекции стресс-зависимых расстройств МЦ выполнено на клинической базе кафедры акушерства и гинекологии с курсом перинатологии
Медицинского института РУДН в ЧУЗ «Клиническая больница "РЖД-Медицина" им. Н.А. Семашко». Все женщины предоставили письменное информированное согласие на участие в исследовании и использование персональных клинических, инструментальных и лабораторных показателей в отчетах и научных публикациях.
Критерии включения:
• возраст 18–45 лет;
• наличие СНМЦ по типу олигоменореи или аменореи без симптомов ПМС или с симптомами ПМС легкой и умеренной степени;
• отсутствие морфологического субстрата СНМЦ и тяжелой экстрагенитальной патологии так же являлись обязательным условием;
• наличие подписанного информированного согласия.
Критерии невключения:
• другие причины нарушения МЦ;
• отсутствие стресс-зависимых причин;
• тяжелая степень ПМС;
• прием в период исследования гормональных контрацептивов, гормонов гипоталамуса, гипофиза, нейролептиков и антидепрессантов, ингибиторов обратного захвата серотонина, ингибиторов пролактина;
• недавно проведенное психиатрическое, хирургическое и другое лечение ПМС;
• хронические заболевания почек, печени, язва желудка в активной стадии, синдром мальабсорбции, гиперсекреция желчных кислот;
• кормление грудью, беременность в настоящее время или планирование беременности;
• наличие у пациентки гиперчувствительности к любому компоненту биологически активной добавки.
При соответствии всем критериям включения и отсутствии критериев невключения пациентки знакомились со всеми аспектами исследования и подписывали информированное согласие. Всем пациенткам изучаемой когорты в рамках действующих клинических рекомендаций («Аменорея и олигоменорея», 2024 г.) была рекомендована консультация медицинского психолога с целью выявления и лечения психоэмоциональных расстройств, а также эндокринолога – для коррекции рациона питания и восстановления массы тела (при верифицированном дефиците индекса массы тела).
• сбор анамнеза, демографических данных;
• антропометрические измерения (рост, масса тела), физикальный осмотр;
• ультразвуковое исследование органов малого таза;
• лабораторные исследования: общий анализ крови, оценка уровней половых гормонов методами электрохемилюминесцентного иммуноанализа и иммуноферментного анализа на биохимическом и иммунохимическом анализаторе Cobas 8000 (Roche) с определением уровней ФСГ, ЛГ, пролактина, тиреотропного гормона, β-хорионического гонадотропина человека);
• анкетирование на основании опросника менструального дистресса (Menstrual Distress Questionnaire, MEDI-Q) – валидированного инструмента оценки менструальных симптомов, включающего 25 пунктов по следующим областям: боль, дискомфорт, психические и когнитивные изменения, гастроинтестинальные симптомы и изменения физиологических функций (опросник позволяет оценить общий балл – MEDI-Q Total Score и три подшкалы: менструальные симптомы – MS, дистресс, связанный с менструальными симптомами, – MSD, и индекс менструальной специфичности – MESI);
• выдача менструального календаря для заполнения.
При визите завершения оценивались:
• жалобы пациенток;
• эффективность терапии на основе анализа менструального календаря;
• безопасность терапии по частоте возникновения нежелательных реакций;
• оценка качества жизни согласно модифицированному опроснику MEDI-Q (общий балл и три подшкалы: MS, MSD, MESI) в динамике.
Оценка эффективности
Первичной конечной точкой являлась оценка эффективности использования фитокомплекса Мабелль Цикл в регуляции ритма МЦ в сравнении с группой с немедикаментозной терапией.
Вторичными конечными точками служили:
• оценка качества жизни пациенток согласно модифицированному опроснику MEDI-Q;
• оценка частоты возникновения нежелательных реакций.
Статистический анализ
Статистическая обработка данных проводилась с учетом характера распределения показателей. Проверка на нормальность распределения осуществлялась с помощью критерия Шапиро–Уилка (при n<50) или критерия Колмогорова–Смирнова (при n>50).
Для количественных показателей с нормальным распределением рассчитывались:
• средние арифметические величины (M);
• стандартные отклонения (SD);
• границы 95% ДИ.
Для количественных показателей с распределением, отличным от нормального, определялись:
• медиана (Me);
• нижний и верхний квартили (Q1–Q3).
Для сравнительного анализа использовались:
• U-критерий Манна–Уитни для сравнения двух независимых групп по показателям с распределением, отличным от нормального;
• парный t-критерий Стьюдента для сравнения связанных выборок с нормально распределенными показателями;
• критерий Уилкоксона для сравнения связанных выборок с показателями, имеющими распределение, отличное от нормального.
Различия считались статистически значимыми при p<0,05.
Версия SPSS 11.0.1 для Windows (SPSS Inc., США) использовалась для управления данными и статистического анализа.
В исследование были включены сопоставимые группы пациенток репродуктивного возраста (средний возраст 24,41±2,95 года; 95% ДИ 23,76–25,07; диапазон 18,00–31,00 года) с нормальным или сниженным индексом массы тела. Исходные/базовые параметры менструальной функции до возникновения СНМЦ у участниц были в пределах физиологической нормы по длительности цикла и продолжительности менструации.
В обеих группах преобладали пациентки с нормальным объемом кровопотери (67,5–75%). Отсутствие статистически значимых различий между группами по анализируемым клинико-анамнестическим параметрам (p>0,05) свидетельствует об однородности групп и позволяет в дальнейшем объективизировать полученные данные.
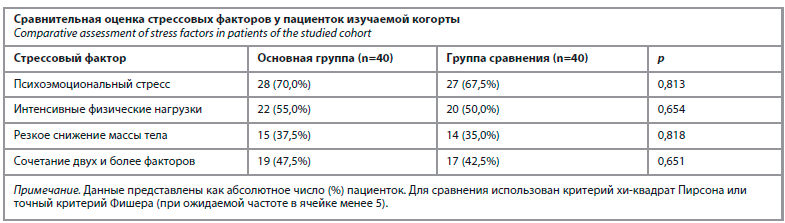
До включения пациенток в настоящее исследование был проведен анализ перенесенных стрессовых факторов у пациенток изучаемой когорты (см. таблицу).
Сравнительный анализ этиологических факторов ФГА не выявил статистически значимых различий между исследуемыми группами (p>0,05), что подтверждает сопоставимую однородность групп. Психоэмоциональный стресс был ведущим триггером реализации аменореи у пациенток изучаемой когорты, на втором месте – интенсивные физические нагрузки, реже встречалось резкое снижение массы тела. Примерно у половины пациенток наблюдалось сочетание нескольких стрессовых факторов.
По данным сонографического исследования, у пациенток изучаемой когорты отмечались характерные для ФГА изменения: уменьшение объема яичников и толщины эндометрия. У 62,5–65,0% пациенток изучаемой популяции визуализировались мелкие антральные фолликулы диаметром до 4–6 мм, что свидетельствовало о подавлении фолликулогенеза.
Исходные лабораторные показатели в обеих группах были в пределах референсных значений и оказались сопоставимы между группами (p>0,05). Это касается как показателей общего анализа крови (эритроцитарные, лейкоцитарные и тромбоцитарные), так и стероидного профиля (ФСГ, ЛГ, пролактин, тиреотропный гормон). Отсутствие значимых различий между группами подтверждает их однородность по лабораторным параметрам на момент включения в исследование. В ходе исследования установлено, что уровень ЛГ в сыворотке крови составил 1,95 (1,50–2,30) мМЕ/мл в основной группе и 2,05 (1,60–7,10) мМЕ/мл в группе контроля (p=0,300), что соответствует диагностическим критериям ФГА.
Анализ эффективности применения Мабелль Цикл к концу 1-го месяца показал незначительные статистические различия между изученными группами (22,5% vs 7,5% соответственно, p=0,115). Следует отметить, что начиная со 2-го месяца применения фитокомплекса и немедикаментозных методов наблюдались статистически значимые различия: среди пациенток, получивших Мабелль Цикл, МЦ восстановился у 47,5% против 17,5% в контрольной группе (p=0,008), а к концу 3-го месяца – у 62,5% против 27,5% соответственно (p=0,003). Полученные результаты свидетельствуют о более высокой эффективности применения препарата Мабелль Цикл в сравнении с группой контроля в восстановлении МЦ пациенток со стресс-зависимыми расстройствами МЦ.
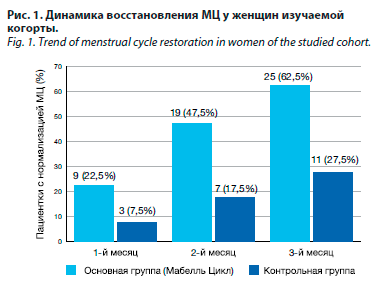 Сравнительный анализ динамики восстановления МЦ у пациенток изучаемой когорты представлен на рис. 1.
Сравнительный анализ динамики восстановления МЦ у пациенток изучаемой когорты представлен на рис. 1.
Анализ эффективности купирования симптомов менструального дистресса продемонстрировал статистически значимое улучшение в обеих группах по таким ключевым показателям, как лабильность настроения, отечность и масталгия.
У пациенток, получивших Мабелль Цикл, отмечено более значительное снижение выраженности ментальных симптомов (лабильность настроения: с 45,0 до 7,5% соответственно, p=0,015) и масталгии (с 40,0 до 10,0%, p=0,008) по сравнению с группой немедикаментозной терапии. Для симптома «отечность» было показано статистически значимое улучшение уже ко 2-му визиту в основной группе пациенток (р=0,005).
В ходе исследования проанализирована эффективность купирования психоэмоциональных симптомов на фоне приема препарата Мабелль Цикл или проведения немедикаментозной терапии (рис. 2).
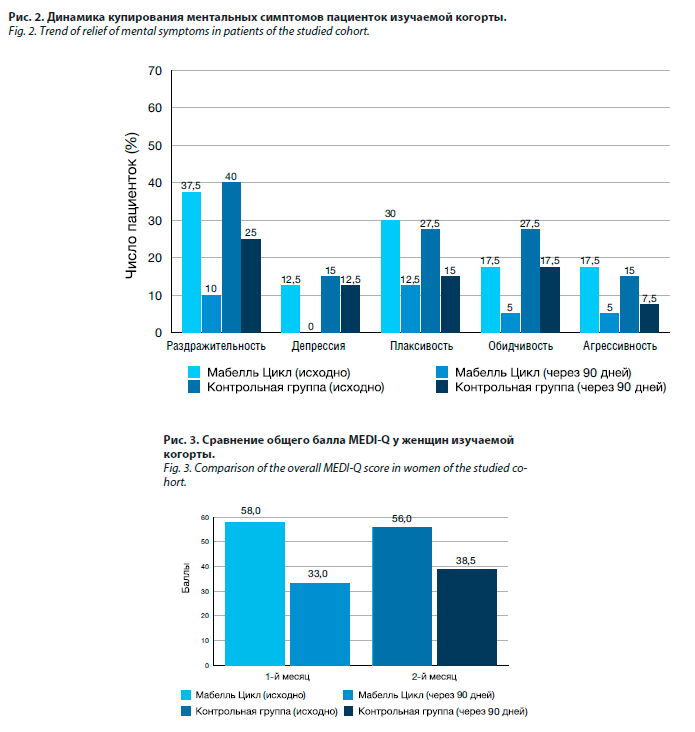
Статистически значимое улучшение было зафиксировано у пациенток, получивших Мабелль Цикл: снижение раздражительности (с 37,5 до 10,0%, p=0,005), плаксивости (с 30,0 до 12,5%, p=0,001), обидчивости
(с 17,5 до 5,0%, p<0,001) и агрессивности (с 17,5 до 5,0%, p<0.001) и полное купирование симптома депрессии (p<0,001).
Между тем в контрольной группе значимое улучшение наблюдалось только по трем симптомам: плаксивость, агрессивность и обидчивость. Особенно заметна разница в динамике снижения выраженности депрессивных симптомов, которые полностью купировались у пациенток основной группы, но сохранялись у 12,5% пациенток группы сравнения.
Шкала, получившая название «Опросник менструального стресса» (MEDI-Q), была разработана S. Vannuccini и соавт. (2021 г.) [21], это инструмент, который всесторонне оценивает проблемы с МЦ. MEDI-Q оценивает влияние менструальных симптомов на качество жизни по фазам МЦ. Шкала дает общий балл и баллы по трем субшкалам: МС определяет количество симптомов дистресса во время менструации, MSD – их выраженность, а MESI – индекс менструальной специфичности – оценивается от 0 до 1, где 0 означает, что менструальные симптомы преобладают в предменструальной фазе, а 1 – что все симптомы вызывают больший дистресс в менструальной фазе.
В ходе настоящего исследования у пациенток, получивших Мабелль Цикл, установлено более выраженное снижение общего балла MEDI-Q (с 58,00 до 33,00, p<0,001): достоверные различия с группой сравнения (с 56,00 до 38,50, p<0,001) к концу исследования достигли между группами статистической достоверности; p=0,001 (рис. 3).
Аналогичная динамика прослеживалась по эффективности уменьшения количества менструальных симптомов (МС), где также продемонстрировано более существенное улучшение у пациенток, получивших Мабелль Цикл (снижение с 20,00 до 13,00 балла), относительно группы сравнения (с 19,50 до 15,00 баллов), хотя межгрупповые различия не достигли статистической значимости (p=0,211). Динамика снижения выраженности симптомов менструального дистресса (MSD) была достоверно более значима в основной группе (0,68) по сравнению с контрольной (0,27); p=0,010. Индекс менструальной специфичности показал тенденцию к повышению, более выраженную в группе Мабелль Цикл (с 0,6–0,8 до 0,8–0,9), чем в группе сравнения (с 0,7–0,83 до 0,8–0,9), что может свидетельствовать о большем влиянии на уменьшение проявлений симптомов в предменструальный период.
Прогрессивное восстановление МЦ в когорте пациенток, получивших Мабелль Цикл (22,5%, 50,0% и 62,5% за 3 мес применения) значительно превосходило результаты в группе сравнения (7,5%, 17,5% и 27,5% соответственно). Статистически значимые различия, выявленные уже на 2-м месяце приема (p=0,008), указывают на значимый потенциал изучаемого фитокомплекса. Полученные данные согласуются с современными представлениями о патофизиологии стресс-индуцированных нарушений МЦ, которые характеризуются нарушениями в гипоталамо-гипофизарно-гонадной оси вследствие психологического стресса, избыточных физических нагрузок и нарушений пищевого поведения [22, 23].
Наблюдаемая эффективность может быть объяснена комплексным воздействием биоактивных компонентов на различные уровни регуляции МЦ. Витекс священный, входящий в состав комплекса, оказывает регулирующее влияние на уровень пролактина [10, 12], что объясняет положительную динамику восстановления цикла, особенно учитывая, что исходные значения пролактина у пациенток были на верхних границах нормы.
Значимое улучшение психоэмоционального статуса пациенток, получивших фитокомплекс, выразившееся в снижении частоты лабильности настроения (с 45,0 до 7,5%, p=0,015), депрессии (полное купирование симптома, p<0,001), раздражительности, плаксивости, обидчивости и агрессивности, можно объяснить синергетическим действием его компонентов. Эти результаты хорошо коррелируют с данными метаанализа Т. Reilly и соавт. [24], которые подчеркивают важность серотонинергической модуляции в коррекции эмоциональных нарушений, ассоциированных с МЦ.
Гриффония простолистная, как источник 5-НТР, и D,L-фенилаланин оказывают положительное влияние на серотонинергическую систему, что коррелирует с улучшением настроения [18, 19]. Эти эффекты особенно важны в коррекции стресс-зависимой аменореи, так как психологический фактор является одним из ключевых патогенетических факторов ФГА [22, 23].
Статистически значимое снижение общего балла MEDI-Q в когорте пациенток, получивших Мабелль Цикл (с 58,00 до 33,00, p<0,001), с достижением значимых межгрупповых различий к концу исследования (p=0,001) свидетельствует об улучшении качества жизни, связанного с менструальной функцией. Уменьшение выраженности менструальных симптомов и снижение уровня дистресса согласуются с результатами систематического обзора J. Robinson и соавт. [25], который подчеркивает важность комплексного подхода к коррекции предменструальной симптоматики.
Наблюдаемая положительная динамика симптомов ПМС может быть обусловлена комплексным воздействием фитоэстрогенов клевера лугового и дудника китайского, а также мочегонным эффектом клевера, способствующим уменьшению отечного синдрома [16, 17, 26]. Эти результаты перекликаются с данными систематических обзоров, указывающих на эффективность фитотерапевтических средств в облегчении симптомов ПМС [13, 17].
Полученные результаты подтверждают важность многофакторного подхода к лечению стресс-индуцированной олиго- и аменореи, который подчеркивается в современной литературе [22, 23, 27]. А. Mohamed и соавт. [27] и N. Naderpoor и соавт. [28] отмечают эффективность комплексных интервенций, включающих модификацию образа жизни и нефармакологические стратегии, что соответствует дизайну нашего исследования, где фитокомплекс применялся совместно с рекомендациями по режиму питания и физической активности.
Учитывая многофакторную природу данной нозологии, использование фитокомплекса, воздействующего одновременно на гормональные, психоэмоциональные и соматические проявления, представляется патогенетически обоснованным подходом. Значимых нежелательных реакций, в том числе аллергических, в ходе применения препарата Мабелль Цикл не было отмечено. Отказов от приема не было зарегистрировано.
Высокий комплаенс фитокомплекса обусловлен не только доказанной клинической эффективностью, но и исключительной безопасностью, хорошей переносимостью и удобством применения.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Материал подготовлен при поддержке АО «Нижфарм». Мнение автора может
не совпадать с мнением компании.
Информация об авторах
Information about the authors
Радзинский Виктор Евсеевич – акад. РАН, д-р мед. наук, проф., зав. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: radzinsky@mail.ru; ORCID: 0000-0002-7428-0469
Viktor E. Radzinskiy – Acad. RAS, Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: radzinsky@mail.ru; ORCID: 0000-0002-7428-0469
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Хамошина Марина Борисовна – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Marina B. Khamoshina – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Орехов Роман Евгеньевич – канд. мед. наук, ассистент каф. акушерства и гинекологии с курсом перинатологии ФГАОУ ВО РУДН. E-mail: romanorekhovv@ya.ru
Roman E. Orekhov – Cand. Sci. (Med.), Assistant, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: romanorekhovv@ya.ru
Муллина Ирина Александровна – канд. мед. наук, врач акушер-гинеколог гинекологического отд-ния ЧУЗ «КБ "РЖД-Медицина" им. Н.А. Семашко». E-mail: 211irina2111@gmail.com
Irina A. Mullina – Cand. Sci. (Med.), Semashko Clinical Hospital “Russian Railways-Medicine”. E-mail: 211irina2111@gmail.com
Лесная Олеся Анатольевна – ассистент каф. общей врачебной практики ФГАОУ ВО РУДН. E-mail: lesnaya-oa@rudn.ru
Olesia A. Lesnaya – Assistant, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: lesnaya-oa@rudn.ru
Поступила в редакцию: 30.06.2025
Поступила после рецензирования: 14.07.2025
Принята к публикации: 17.07.2025
Received: 30.06.2025
Revised: 14.07.2025
Accepted: 17.07.2025
Nonhormonal adjustment of stress-associated menstrual cycle disorders: data of MONARCH trial on the use of Mabelle Cycle complex
Viktor E. Radzinskiy1, Mekan R. Orazov1, Marina B. Khamoshina1, Roman E. Orekhov1,Irina A. Mullina2, Olesia A. Lesnaya1
1Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2Semashko Clinical Hospital “Russian Railways-Medicine”, Moscow, Russia
omekan@mail.ru
Abstract
Aim. To evaluate the efficacy and safety of using the complex herbal preparation Mabell Cycle in the treatment of stress-dependent menstrual disorders.
Materials and methods. Prospective, open-label, non-interventional study was conducted with 80 patients aged 18–31 years (mean age 24.41±2.95 years) with stress-dependent menstrual disorders. The participants were ratio into two groups: the main group (n=40) received
Mabelle Cycle (active ingredients: Trifolium pratense (red clover) extract, Vitex agnus-castus extract, Angelica sinensis root extract, Griffonia simplicifolia extract, D,L-phenylalanine, iron) at a dose of 2 tablets daily for 3 months, while the control group (n=40) received non-drug therapy (consultation with a psychologist, physiotherapy) following the same regimen. The duration of therapy was 3 months. Efficacy was assessed by menstrual cycle restoration, dynamics of premenstrual syndrome symptoms, and MEDI-Q questionnaire indicators. Safety assessent was based on the incidence of adverse reactions. Study design: prospective, open-label, non-interventional.
Results. The Mabell Cycle group showed progressive restoration of the menstrual cycle: 22.5%, 50.0%, and 62.5% of patients over three months of therapy compared to 7.5%, 17.5%, and 27.5% in the control group, respectively. Statistically significant differences were detected from the second month of therapy (p=0.008). The Mabell Cycle group showed significant reduction in mood lability (from 45.0% to 7.5%, p=0.015), mastalgia (from 40.0% to 10.0%, p=0.008), complete resolution of depressive symptoms (p<0.001), and improvement in five out of six evaluated psycho-emotional parameters versus three in the control group. The total MEDI-Q score in the Mabell Cycle group decreased from 58.00 to 33.00 (p=0.001), achieving significant intergroup differences by the end of the study (p=0.001).
Conclusion. The multitarget phytocomplex Mabell Сycle demonstrates high efficacy and safety in restoring the menstrual cycle in stress-dependent disorders. The use of a phytocomplex for 3 months provides significant improvement in cycle regularity, reduction in the severity of psycho-emotional and somatic symptoms, and enhancement of patients' quality of life. The results obtained allow recommending the phytocomplex
Mabell Cycle for inclusion in clinical protocols for managing patients with stress-dependent menstrual disorders.
Keywords: stress-dependent amenorrhea, menstrual disorders, phytotherapy.
For citation: Radzinskiy V.E., Orazov M.R., Khamoshina M.B., Orekhov R.E., Mullina I.A., Lesnaya O.A. Clinical review for general practice. 2025; 6 (8): 86–94 (In Russ.). DOI: 10.47407/kr2025.6.8.00663
Актуальность проблемы
В течение жизни женская репродуктивная система претерпевает ряд ежемесячных циклических морфофункциональных изменений, называемых менструальным циклом (МЦ), направленных на подготовку женского организма к беременности. Регулярность МЦ – один из важнейших показателей репродуктивного здоровья. Вместе с тем любые дисфункции репродуктивной регуляции негативно отражаются на менструальной функции. С клинической точки зрения все нарушения МЦ следует стратифицировать на две большие группы:1) расстройства, связанные с МЦ, где функция яичников, как правило, не изменена, а патогенетической основой служат нарушения центральной нервной системы или заболевания органов-мишеней;
2) расстройства ритма менструаций, при которых патогенетической основой, как правило, служат различные варианты яичниковой недостаточности или овариальной дисфункции [1].
Несмотря на высокую распространенность стресса и его научно доказанное негативное влияние на здоровье, прямые механизмы его воздействия на расстройства МЦ до сих пор неясны и остаются на уровне гипотез.
Стресс-зависимые нарушения МЦ (СНМЦ) представляют собой комплексную группу патологических состояний, этиологически связанных с воздействием стрессогенных факторов и клинически проявляющихся нарушениями ритма менструаций или специфическими симптомами, сопряженными с МЦ [1–5]. В соответствии с Международной классификацией болезней 10-го пересмотра (МКБ-10) не существует легитимного диагноза «стресс-индуцированные нарушения ритма менструаций», их можно классифицировать преимущественно в рамках рубрики N91, охватывающей отсутствие, скудость и редкость менструальных кровотечений. Современный научный дискурс характеризуется терминологическим разнообразием: «стресс-провоцированная», «стресс-зависимая» и «гипоталамическая аменорея» часто употребляются как равнозначные понятия, причем термин «гипоталамическая» в ряде исследований замещается определением «психогенная», что подчеркивает первостепенную роль дисфункции центральной нервной системы в патогенезе данного состояния [1, 4–6].
Патогенетическая взаимосвязь между стрессовым фактором и нарушениями МЦ реализуется через сложный каскад нейроэндокринных изменений [6]. Для СНМЦ характерен дисбаланс гонадотропных гормонов, проявляющийся в снижении уровня лютеинизирующего гормона (ЛГ) при относительно сохранной секреции фолликулостимулирующего гормона (ФСГ). Клинические варианты определяются как «нормогонадотропная» или «гипогонадотропная» аменорея в зависимости от концентрации ЛГ (выше или ниже 3 мЕд/мл соответственно) [7]. В действующих клинических рекомендациях («Аменорея и олигоменорея», 2024 г.) вторичную аменорею, связанную с дисфункцией гипоталамуса, определяют как функциональную гипоталамическую (ФГА), для которой характерно прекращение менструаций на фоне стресса, чрезмерных физических нагрузок и/или снижения массы тела [8]. Стрессовое воздействие на гипоталамо-гипофизарно-яичниковую ось может нарушать процесс формирования доминантного фолликула, приводя к развитию синдрома хронической ановуляции [1].
Клинический спектр СНМЦ включает разнообразные проявления: вторичную аменорею, частота которой у женщин репродуктивного возраста достигает 3–5%
[2, 9]; первичную аменорею, составляющую примерно 3% от всех случаев ФГА [1]; аномальные маточные кровотечения; а также соматические и эмоциональные циклические расстройства, в том числе предменструальный синдром (ПМС) и предменструальное дисфорическое расстройство. Важно отметить, что стрессовые факторы, провоцирующие СНМЦ, не обязательно носят экстремальный характер – дистресс может быть обусловлен повседневными психосоциальными обстоятельствами, связанными с бытовой, учебной, профессиональной или семейной сферами жизни [1]. В условиях урбанизации и возрастающих психоэмоциональных нагрузок современного общества наблюдается тенденция к увеличению распространенности СНМЦ среди женского населения.
В настоящее время в рутинной практике врача акушера-гинеколога особую актуальность приобретает поиск эффективных методов коррекции нарушений МЦ, в частности стресс-зависимой аменореи, с использованием фитотерапевтических средств. Анализ современной научной литературы свидетельствует о значительном интересе исследователей к использованию фитокомплексов в регуляции МЦ, что подтверждается множеством систематических обзоров и метаанализов [10–14].
Особый интерес представляет изучение эффективности комплексной фитотерапии, каждый компонент которой обладает определенным терапевтическим потенциалом в регуляции разных уровней репродуктивной системы.
В рамках проведенного исследования изучалось влияние комплекса Мабелль Цикл, который в своем составе содержит: экстракт плодов витекса священного, экстракт клевера лугового, экстракт корня дудника китайского, экстракт семян гриффонии простолистной (источник 5-гидрокситриптофана – 5-НТР), D,L-фенилаланин, железо.
Витекс священный способствует нормализации уровня пролактина, что приводит к регуляции МЦ и уменьшению выраженности клинических проявлений ПМС [10, 12]. Систематические обзоры демонстрируют неоднородность доказательной базы различных фитотерапевтических средств в коррекции расстройств МЦ. Наиболее изученным является витекс священный, эффективность которого подтверждена в 17 рандомизированных контролируемых исследованиях. Метаанализ показал значительный суммарный размер эффекта (g=-1.21) в отношении купирования выраженности ПМС, хотя высокий показатель гетерогенности (I²=91%) указывает на существенные различия между исследованиями [10, 12]. Также в ряде исследований отмечается потенциал влияния витекса священного на регулярность МЦ [15].
Клевер луговой содержит фитоэстрогены, обладает мочегонным эффектом, способствуя уменьшению предменструального отечного синдрома. Высокое содержание магния в нем оказывает положительное влияние на психоэмоциональное состояние пациенток [16]. Современные исследования традиционной китайской медицины также подтверждают потенциал фитоэстрогенов в регуляции женской репродуктивной системы [17].
Дудник китайский богат фитоэстрогенами и витамином Е, в систематическом обзоре традиционной китайской медицины отмечается его эффективность при различных нарушениях репродуктивной системы [11–13].
Гриффония простолистная, являющаяся источником 5-НТР, представляет особый интерес в контексте коррекции психоэмоциональных нарушений. Исследования показывают, что 5-НТР эффективно способствует нормализации уровня серотонина, что особенно важно при СНМЦ [18].
Включение в состав комплексного средства D,L-фенилаланина и железа обосновано их ролью в нормализации психоэмоционального состояния и восполнении физиологических потерь железа соответственно.
Фенилаланин, являясь незаменимой аминокислотой, участвует в биохимических процессах головного мозга, способствуя улучшению настроения и снижению болевой чувствительности [19, 20].
Растущий интерес к фитотерапевтическим средствам обосновывает необходимость в дополнительных исследованиях их эффективности и безопасности с использованием современных методологических подходов. Особенно актуальным является изучение комплексных составов, которые содержат несколько активных фитокомпонентов, их синергетического действия и безопасности применения при СНМЦ. Проблема методологического качества существующих исследований, включая небольшие размеры выборок и различные подходы к оценке эффективности, подчеркивает необходимость крупномасштабных рандомизированных контролируемых исследований с четкими стандартизированными протоколами [10, 13].
Материалы и методы
Цель исследования – оценить эффективность и безопасность использования Мабелль Цикл в коррекции стресс-зависимых расстройств МЦ.Открытое независимое неинтервенционное проспективное исследование МОНАРХ (MONARCH) с целью оценки эффективности и безопасности использования Мабелль Цикл в коррекции стресс-зависимых расстройств МЦ выполнено на клинической базе кафедры акушерства и гинекологии с курсом перинатологии
Медицинского института РУДН в ЧУЗ «Клиническая больница "РЖД-Медицина" им. Н.А. Семашко». Все женщины предоставили письменное информированное согласие на участие в исследовании и использование персональных клинических, инструментальных и лабораторных показателей в отчетах и научных публикациях.
Дизайн исследования
В исследование были включены 80 пациенток со стресс-зависимыми расстройствами МЦ по типу аменореи или олигоменореи (N91 по МКБ-10). Средний возраст участниц составил 24,41±2,95 года (95% доверительный интервал – ДИ 23,76–25,07; диапазон 18,00–31,00 года). Пациентки были разделены на две группы в соотношении 1:1: 1-я группа (40 пациенток) получала Мабелль Цикл (активные компоненты: экстракт клевера лугового, экстракт плодов витекса священного, экстракт корня дудника китайского, экстракт семян гриффонии простолистной, D,L-фенилаланин, железо) 3 мес по 2 таблетки в сутки, 2-я (40 пациенток) – немедикаментозную терапию (консультацию психолога, физиотерапию).Критерии включения:
• возраст 18–45 лет;
• наличие СНМЦ по типу олигоменореи или аменореи без симптомов ПМС или с симптомами ПМС легкой и умеренной степени;
• отсутствие морфологического субстрата СНМЦ и тяжелой экстрагенитальной патологии так же являлись обязательным условием;
• наличие подписанного информированного согласия.
Критерии невключения:
• другие причины нарушения МЦ;
• отсутствие стресс-зависимых причин;
• тяжелая степень ПМС;
• прием в период исследования гормональных контрацептивов, гормонов гипоталамуса, гипофиза, нейролептиков и антидепрессантов, ингибиторов обратного захвата серотонина, ингибиторов пролактина;
• недавно проведенное психиатрическое, хирургическое и другое лечение ПМС;
• хронические заболевания почек, печени, язва желудка в активной стадии, синдром мальабсорбции, гиперсекреция желчных кислот;
• кормление грудью, беременность в настоящее время или планирование беременности;
• наличие у пациентки гиперчувствительности к любому компоненту биологически активной добавки.
При соответствии всем критериям включения и отсутствии критериев невключения пациентки знакомились со всеми аспектами исследования и подписывали информированное согласие. Всем пациенткам изучаемой когорты в рамках действующих клинических рекомендаций («Аменорея и олигоменорея», 2024 г.) была рекомендована консультация медицинского психолога с целью выявления и лечения психоэмоциональных расстройств, а также эндокринолога – для коррекции рациона питания и восстановления массы тела (при верифицированном дефиците индекса массы тела).
Методы обследования
При первичном визите проводились:• сбор анамнеза, демографических данных;
• антропометрические измерения (рост, масса тела), физикальный осмотр;
• ультразвуковое исследование органов малого таза;
• лабораторные исследования: общий анализ крови, оценка уровней половых гормонов методами электрохемилюминесцентного иммуноанализа и иммуноферментного анализа на биохимическом и иммунохимическом анализаторе Cobas 8000 (Roche) с определением уровней ФСГ, ЛГ, пролактина, тиреотропного гормона, β-хорионического гонадотропина человека);
• анкетирование на основании опросника менструального дистресса (Menstrual Distress Questionnaire, MEDI-Q) – валидированного инструмента оценки менструальных симптомов, включающего 25 пунктов по следующим областям: боль, дискомфорт, психические и когнитивные изменения, гастроинтестинальные симптомы и изменения физиологических функций (опросник позволяет оценить общий балл – MEDI-Q Total Score и три подшкалы: менструальные симптомы – MS, дистресс, связанный с менструальными симптомами, – MSD, и индекс менструальной специфичности – MESI);
• выдача менструального календаря для заполнения.
При визите завершения оценивались:
• жалобы пациенток;
• эффективность терапии на основе анализа менструального календаря;
• безопасность терапии по частоте возникновения нежелательных реакций;
• оценка качества жизни согласно модифицированному опроснику MEDI-Q (общий балл и три подшкалы: MS, MSD, MESI) в динамике.
Оценка эффективности
Первичной конечной точкой являлась оценка эффективности использования фитокомплекса Мабелль Цикл в регуляции ритма МЦ в сравнении с группой с немедикаментозной терапией.
Вторичными конечными точками служили:
• оценка качества жизни пациенток согласно модифицированному опроснику MEDI-Q;
• оценка частоты возникновения нежелательных реакций.
Статистический анализ
Статистическая обработка данных проводилась с учетом характера распределения показателей. Проверка на нормальность распределения осуществлялась с помощью критерия Шапиро–Уилка (при n<50) или критерия Колмогорова–Смирнова (при n>50).
Для количественных показателей с нормальным распределением рассчитывались:
• средние арифметические величины (M);
• стандартные отклонения (SD);
• границы 95% ДИ.
Для количественных показателей с распределением, отличным от нормального, определялись:
• медиана (Me);
• нижний и верхний квартили (Q1–Q3).
Для сравнительного анализа использовались:
• U-критерий Манна–Уитни для сравнения двух независимых групп по показателям с распределением, отличным от нормального;
• парный t-критерий Стьюдента для сравнения связанных выборок с нормально распределенными показателями;
• критерий Уилкоксона для сравнения связанных выборок с показателями, имеющими распределение, отличное от нормального.
Различия считались статистически значимыми при p<0,05.
Версия SPSS 11.0.1 для Windows (SPSS Inc., США) использовалась для управления данными и статистического анализа.
Результаты

В исследование были включены сопоставимые группы пациенток репродуктивного возраста (средний возраст 24,41±2,95 года; 95% ДИ 23,76–25,07; диапазон 18,00–31,00 года) с нормальным или сниженным индексом массы тела. Исходные/базовые параметры менструальной функции до возникновения СНМЦ у участниц были в пределах физиологической нормы по длительности цикла и продолжительности менструации.
В обеих группах преобладали пациентки с нормальным объемом кровопотери (67,5–75%). Отсутствие статистически значимых различий между группами по анализируемым клинико-анамнестическим параметрам (p>0,05) свидетельствует об однородности групп и позволяет в дальнейшем объективизировать полученные данные.
До включения пациенток в настоящее исследование был проведен анализ перенесенных стрессовых факторов у пациенток изучаемой когорты (см. таблицу).
Сравнительный анализ этиологических факторов ФГА не выявил статистически значимых различий между исследуемыми группами (p>0,05), что подтверждает сопоставимую однородность групп. Психоэмоциональный стресс был ведущим триггером реализации аменореи у пациенток изучаемой когорты, на втором месте – интенсивные физические нагрузки, реже встречалось резкое снижение массы тела. Примерно у половины пациенток наблюдалось сочетание нескольких стрессовых факторов.
По данным сонографического исследования, у пациенток изучаемой когорты отмечались характерные для ФГА изменения: уменьшение объема яичников и толщины эндометрия. У 62,5–65,0% пациенток изучаемой популяции визуализировались мелкие антральные фолликулы диаметром до 4–6 мм, что свидетельствовало о подавлении фолликулогенеза.
Исходные лабораторные показатели в обеих группах были в пределах референсных значений и оказались сопоставимы между группами (p>0,05). Это касается как показателей общего анализа крови (эритроцитарные, лейкоцитарные и тромбоцитарные), так и стероидного профиля (ФСГ, ЛГ, пролактин, тиреотропный гормон). Отсутствие значимых различий между группами подтверждает их однородность по лабораторным параметрам на момент включения в исследование. В ходе исследования установлено, что уровень ЛГ в сыворотке крови составил 1,95 (1,50–2,30) мМЕ/мл в основной группе и 2,05 (1,60–7,10) мМЕ/мл в группе контроля (p=0,300), что соответствует диагностическим критериям ФГА.
Анализ эффективности применения Мабелль Цикл к концу 1-го месяца показал незначительные статистические различия между изученными группами (22,5% vs 7,5% соответственно, p=0,115). Следует отметить, что начиная со 2-го месяца применения фитокомплекса и немедикаментозных методов наблюдались статистически значимые различия: среди пациенток, получивших Мабелль Цикл, МЦ восстановился у 47,5% против 17,5% в контрольной группе (p=0,008), а к концу 3-го месяца – у 62,5% против 27,5% соответственно (p=0,003). Полученные результаты свидетельствуют о более высокой эффективности применения препарата Мабелль Цикл в сравнении с группой контроля в восстановлении МЦ пациенток со стресс-зависимыми расстройствами МЦ.
 Сравнительный анализ динамики восстановления МЦ у пациенток изучаемой когорты представлен на рис. 1.
Сравнительный анализ динамики восстановления МЦ у пациенток изучаемой когорты представлен на рис. 1.Анализ эффективности купирования симптомов менструального дистресса продемонстрировал статистически значимое улучшение в обеих группах по таким ключевым показателям, как лабильность настроения, отечность и масталгия.
У пациенток, получивших Мабелль Цикл, отмечено более значительное снижение выраженности ментальных симптомов (лабильность настроения: с 45,0 до 7,5% соответственно, p=0,015) и масталгии (с 40,0 до 10,0%, p=0,008) по сравнению с группой немедикаментозной терапии. Для симптома «отечность» было показано статистически значимое улучшение уже ко 2-му визиту в основной группе пациенток (р=0,005).
В ходе исследования проанализирована эффективность купирования психоэмоциональных симптомов на фоне приема препарата Мабелль Цикл или проведения немедикаментозной терапии (рис. 2).

Статистически значимое улучшение было зафиксировано у пациенток, получивших Мабелль Цикл: снижение раздражительности (с 37,5 до 10,0%, p=0,005), плаксивости (с 30,0 до 12,5%, p=0,001), обидчивости
(с 17,5 до 5,0%, p<0,001) и агрессивности (с 17,5 до 5,0%, p<0.001) и полное купирование симптома депрессии (p<0,001).
Между тем в контрольной группе значимое улучшение наблюдалось только по трем симптомам: плаксивость, агрессивность и обидчивость. Особенно заметна разница в динамике снижения выраженности депрессивных симптомов, которые полностью купировались у пациенток основной группы, но сохранялись у 12,5% пациенток группы сравнения.
Шкала, получившая название «Опросник менструального стресса» (MEDI-Q), была разработана S. Vannuccini и соавт. (2021 г.) [21], это инструмент, который всесторонне оценивает проблемы с МЦ. MEDI-Q оценивает влияние менструальных симптомов на качество жизни по фазам МЦ. Шкала дает общий балл и баллы по трем субшкалам: МС определяет количество симптомов дистресса во время менструации, MSD – их выраженность, а MESI – индекс менструальной специфичности – оценивается от 0 до 1, где 0 означает, что менструальные симптомы преобладают в предменструальной фазе, а 1 – что все симптомы вызывают больший дистресс в менструальной фазе.
В ходе настоящего исследования у пациенток, получивших Мабелль Цикл, установлено более выраженное снижение общего балла MEDI-Q (с 58,00 до 33,00, p<0,001): достоверные различия с группой сравнения (с 56,00 до 38,50, p<0,001) к концу исследования достигли между группами статистической достоверности; p=0,001 (рис. 3).
Аналогичная динамика прослеживалась по эффективности уменьшения количества менструальных симптомов (МС), где также продемонстрировано более существенное улучшение у пациенток, получивших Мабелль Цикл (снижение с 20,00 до 13,00 балла), относительно группы сравнения (с 19,50 до 15,00 баллов), хотя межгрупповые различия не достигли статистической значимости (p=0,211). Динамика снижения выраженности симптомов менструального дистресса (MSD) была достоверно более значима в основной группе (0,68) по сравнению с контрольной (0,27); p=0,010. Индекс менструальной специфичности показал тенденцию к повышению, более выраженную в группе Мабелль Цикл (с 0,6–0,8 до 0,8–0,9), чем в группе сравнения (с 0,7–0,83 до 0,8–0,9), что может свидетельствовать о большем влиянии на уменьшение проявлений симптомов в предменструальный период.
Обсуждение
Исследование продемонстрировало эффективность негормонального многокомпонетного фитокомплекса Мабелль Цикл в восстановлении МЦ при СНМЦ. Полученные результаты позволяют рассматривать данный комплекс как перспективную альтернативу в коррекции стресс-зависимых расстройств МЦ.Прогрессивное восстановление МЦ в когорте пациенток, получивших Мабелль Цикл (22,5%, 50,0% и 62,5% за 3 мес применения) значительно превосходило результаты в группе сравнения (7,5%, 17,5% и 27,5% соответственно). Статистически значимые различия, выявленные уже на 2-м месяце приема (p=0,008), указывают на значимый потенциал изучаемого фитокомплекса. Полученные данные согласуются с современными представлениями о патофизиологии стресс-индуцированных нарушений МЦ, которые характеризуются нарушениями в гипоталамо-гипофизарно-гонадной оси вследствие психологического стресса, избыточных физических нагрузок и нарушений пищевого поведения [22, 23].
Наблюдаемая эффективность может быть объяснена комплексным воздействием биоактивных компонентов на различные уровни регуляции МЦ. Витекс священный, входящий в состав комплекса, оказывает регулирующее влияние на уровень пролактина [10, 12], что объясняет положительную динамику восстановления цикла, особенно учитывая, что исходные значения пролактина у пациенток были на верхних границах нормы.
Значимое улучшение психоэмоционального статуса пациенток, получивших фитокомплекс, выразившееся в снижении частоты лабильности настроения (с 45,0 до 7,5%, p=0,015), депрессии (полное купирование симптома, p<0,001), раздражительности, плаксивости, обидчивости и агрессивности, можно объяснить синергетическим действием его компонентов. Эти результаты хорошо коррелируют с данными метаанализа Т. Reilly и соавт. [24], которые подчеркивают важность серотонинергической модуляции в коррекции эмоциональных нарушений, ассоциированных с МЦ.
Гриффония простолистная, как источник 5-НТР, и D,L-фенилаланин оказывают положительное влияние на серотонинергическую систему, что коррелирует с улучшением настроения [18, 19]. Эти эффекты особенно важны в коррекции стресс-зависимой аменореи, так как психологический фактор является одним из ключевых патогенетических факторов ФГА [22, 23].
Статистически значимое снижение общего балла MEDI-Q в когорте пациенток, получивших Мабелль Цикл (с 58,00 до 33,00, p<0,001), с достижением значимых межгрупповых различий к концу исследования (p=0,001) свидетельствует об улучшении качества жизни, связанного с менструальной функцией. Уменьшение выраженности менструальных симптомов и снижение уровня дистресса согласуются с результатами систематического обзора J. Robinson и соавт. [25], который подчеркивает важность комплексного подхода к коррекции предменструальной симптоматики.
Наблюдаемая положительная динамика симптомов ПМС может быть обусловлена комплексным воздействием фитоэстрогенов клевера лугового и дудника китайского, а также мочегонным эффектом клевера, способствующим уменьшению отечного синдрома [16, 17, 26]. Эти результаты перекликаются с данными систематических обзоров, указывающих на эффективность фитотерапевтических средств в облегчении симптомов ПМС [13, 17].
Полученные результаты подтверждают важность многофакторного подхода к лечению стресс-индуцированной олиго- и аменореи, который подчеркивается в современной литературе [22, 23, 27]. А. Mohamed и соавт. [27] и N. Naderpoor и соавт. [28] отмечают эффективность комплексных интервенций, включающих модификацию образа жизни и нефармакологические стратегии, что соответствует дизайну нашего исследования, где фитокомплекс применялся совместно с рекомендациями по режиму питания и физической активности.
Учитывая многофакторную природу данной нозологии, использование фитокомплекса, воздействующего одновременно на гормональные, психоэмоциональные и соматические проявления, представляется патогенетически обоснованным подходом. Значимых нежелательных реакций, в том числе аллергических, в ходе применения препарата Мабелль Цикл не было отмечено. Отказов от приема не было зарегистрировано.
Заключение
Установлены эффективность и безопасность использования мультитаргетного негормонального комплекса Мабелль Цикл в коррекции стресс-зависимых расстройств МЦ у женщин репродуктивного возраста.Высокий комплаенс фитокомплекса обусловлен не только доказанной клинической эффективностью, но и исключительной безопасностью, хорошей переносимостью и удобством применения.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Материал подготовлен при поддержке АО «Нижфарм». Мнение автора может
не совпадать с мнением компании.
Информация об авторах
Information about the authors
Радзинский Виктор Евсеевич – акад. РАН, д-р мед. наук, проф., зав. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: radzinsky@mail.ru; ORCID: 0000-0002-7428-0469
Viktor E. Radzinskiy – Acad. RAS, Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: radzinsky@mail.ru; ORCID: 0000-0002-7428-0469
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Хамошина Марина Борисовна – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Marina B. Khamoshina – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Орехов Роман Евгеньевич – канд. мед. наук, ассистент каф. акушерства и гинекологии с курсом перинатологии ФГАОУ ВО РУДН. E-mail: romanorekhovv@ya.ru
Roman E. Orekhov – Cand. Sci. (Med.), Assistant, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: romanorekhovv@ya.ru
Муллина Ирина Александровна – канд. мед. наук, врач акушер-гинеколог гинекологического отд-ния ЧУЗ «КБ "РЖД-Медицина" им. Н.А. Семашко». E-mail: 211irina2111@gmail.com
Irina A. Mullina – Cand. Sci. (Med.), Semashko Clinical Hospital “Russian Railways-Medicine”. E-mail: 211irina2111@gmail.com
Лесная Олеся Анатольевна – ассистент каф. общей врачебной практики ФГАОУ ВО РУДН. E-mail: lesnaya-oa@rudn.ru
Olesia A. Lesnaya – Assistant, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: lesnaya-oa@rudn.ru
Поступила в редакцию: 30.06.2025
Поступила после рецензирования: 14.07.2025
Принята к публикации: 17.07.2025
Received: 30.06.2025
Revised: 14.07.2025
Accepted: 17.07.2025
Список исп. литературыСкрыть список1. Волель Б.А., Рагимова А.А., Кузнецова И.В., Бурчаков Д.И. Современные представления о стресс-зависимых нарушениях менструального цикла. Акушерство и гинекология. 2016;(12):34-40.
Volel B.A., Ragimova A.A., Kuznetsova I.V., Burchakov D.I. Modern concepts of stress-dependent menstrual cycle disorders. Obstetrics and Gynecology. 2016;(12):34-40. (in Russian).
2. Агарков В.А., Бронфман С.А., Кудаева Л.М., Уварова Е.В. Психологические аспекты патогенеза функциональной аменореи. Психическое здоровье. 2012;7(74):70-8.
Agarkov V.A., Bronfman S.A., Kudayeva L.M., Uvarova E.V. Psychological aspects of the pathogenesis of functional amenorrhea. Mental health. 2012;7(74):70-8 (in Russian).
3. Practice Committee of the American Society for Reproductive Medicine. Current evaluation of amenorrhea. Fertil Steril 2006;(86):S148.
4. Андреева Е.Н., Шереметьева Е.В. Нерегулярный менструальный цикл у женщин репродуктивного возраста как часть синдрома мегаполиса. Гинекология. 2020;22(6):6-10. DOI: 10.26442/20795696. 2020.6.200487
Andreeva E.N., Sheremetyeva E.V. Irregular menstrual cycle in women of reproductive age as part of the metropolis syndrome. Gynecology. 2020;22(6):6-10. DOI: 10.26442/20795696.2020.6.200487 (in Russian).
5. Андреева Е.Н., Шереметьева Е.В., Адамян Л.В. Этиологические и патогенетические факторы дисфункции яичников у женщин репродуктивного периода. Проблемы репродукции. 2020;26(6):34-43. DOI: 10.17116/repro20202606134
Andreeva E.N., Sheremetyeva E.V., Adamyan L.V. Etiological and pathogenetic factors of ovarian dysfunction in women of reproductive age. Problems of reproduction. 2020;26(6):34-43. DOI: 10.17116/repro20202606134 (in Russian).
6. Pauli SA, Berga SL. Athletic amenorrhea: energy deficit or psychogenic challenge? Ann N Y Acad Sci 2010;(1205):33-8. DOI: 10.1111/j.1749-6632.2010.05663.x
7. Lania A, Gianotti L, Gagliardi I et al. Functional hypothalamic and drug-induced amenorrhea: an overview. J Endocrin Invest 2019;42(9):1001-10. DOI: 10.1007/s40618-019-01013-w
8. Клинические рекомендации. Аменорея и олигоменорея. 2024.
Clinical guidelines. Amenorrhea and oligomenorrhea. 2024 (in Russian).
9. Palm-Fischbacher S, Ehlert J. Dispositional resilience as a moderator of the relationship between chronic stress and irregular menstrual cycle. J Psychosomatic Obstet Gynaecol 2014;35(2):42-50.
10. Van Die MD, Burger HG, Teede HJ, Bone KM. Vitex agnus-castus extracts for female reproductive disorders: a systematic review of clinical trials. Planta Med 2013;79(7):562-75.
11. Карпович О.В., Гуменюк Р.Л., Ордиянц И.М. и др. Перспективы применения фитоэстрогенов. Вестн. РУДН. 2005;4.
Karpovich O.V., Gumenyuk R.L., Ordiyants I.M. et al. Prospects for the use of phytoestrogens. Vestn. RUDN. 2005;4 (in Russian).
12. Verkaik S, Kamperman AM, van Westrhenen R, Schulte PFJ. The treatment of premenstrual syndrome with preparations of Vitex agnus castus: a systematic review and meta-analysis. Am J Obstet Gynecol. 2017;217(2):150-66.
13. Arentz S, Smith CA, Abbott J, Bensoussan A. Nutritional supplements and herbal medicines for women with polycystic ovary syndrome. BMC Complement Altern Med 2017;17(1):500.
14. Lakshmi JN, Babu AN, Kiran SSM et al. Herbs as a Source for the Treatment of Polycystic Ovarian Syndrome: A Systematic Review. BioTech 2023.
15. Höller M, Steindl H, Abramov-Sommariva D et al. Use of Vitex agnus-castus in patients with menstrual cycle disorders: a single-center retrospective longitudinal cohort study. Arch Gynecol Obstet 2024.
16. Кароматов И.Д., Абдулхаков И.У. Клевер луговой применение в медицине (обзор литературы). Биология и интегративная медицина. 2016;(5).
Karomatova I.D., Abdulhakov I.U. Red clover application in medicine (literature review). Biology and integrative medicine. 2016;(5) (in Russian).
17. Jang SH, Kim DI, Choi MS. Effects and treatment methods of acupuncture and herbal medicine for premenstrual syndrome/premenstrual dysphoric disorder: systematic review. BMC Complement Altern Med 2014;14:11.
18. Якушевская О.В. Негормональная коррекция климактерических расстройств. Медицинский совет. 2021;(21-1).
Yakushevskaya O.V. Non-hormonal correction of climacteric disorders. Medical Council. 2021; (21-1) (in Russian).
19. Колбасова Е.А., Киселева Н.И., Дорошенко Е.М. и др. Содержание свободных аминокислот в сыворотке крови у женщин с хирургической и естественной менопаузой. Вестник ВГМУ. 2013;(3).
Kolbasova E.A., Kiseleva N.I., Doroshenko E.M. et al. Content of free amino acids in blood serum in women with surgical and natural menopause. Bulletin of VSMU. 2013; (3) (in Russian).
20. Proctor ML, Murphy PA. Herbal and dietary therapies for primary and secondary dysmenorrhoea. Cochrane Database Syst Rev 2001.
21. Vannuccini S, Rossi E, Cassioli E et al. Menstrual Distress Questionnaire(MEDI-Q): a new tool to assess menstruation-related distress. Reprod Biomed Online 2021;43(6):1107-16.
22. Shufelt CL et al. Hypothalamic Amenorrhea and the Long-Term Health Consequences. Semin Reprod Med 2017. DOI: 10.1055/s-0037-1603581
23. Morrison AE et al. A review of the pathophysiology of functional hypothalamic amenorrhoea in women subject to psychological stress, disordered eating, excessive exercise or a combination of these factors. Clin Endocrinol (Oxf) 2021. DOI: 10.1111/cen.14399
24. Reilly TJ et al. Intermittent selective serotonin reuptake inhibitors for premenstrual syndromes: A systematic review and meta-analysis of randomised trials. J Psychopharmacol 2023. DOI: 10.1177/026988 11221099645
25. Robinson J et al. Effect of nutritional interventions on the psychological symptoms of premenstrual syndrome in women of reproductive age: a systematic review of randomized controlled trials. Nutr Rev 2025. DOI: 10.1093/nutrit/nuae043
26. Ried K, Stuart K. Efficacy of Traditional Chinese Herbal Medicine in the management of female infertility: a systematic review. Complement Ther Med 2011;19(6):319-31.
27. Mohamed AH et al. Impact of lifestyle interventions on reproductive and psychological outcomes in women with polycystic ovary syndrome: A systematic review. Medicine (Baltimore) 2025. DOI: 10.1097/MD. 0000000000041178
28. Naderpoor N et al. Metformin and lifestyle modification in polycystic ovary syndrome: systematic review and meta-analysis. Hum Reprod Update 2015. DOI: 10.1093/humupd/dmv025
29. Hassanzadeh R, Shabani F, Montazeri M, Mirghafourvand M. The Effect of Fenugreek on the Severity of Dysmenorrhea: A Systematic Review and Meta-analysis. Curr Drug Res Rev 2024.


