Клинический разбор в общей медицине №9 2025
1 Martinex International Research Center for Innovative Technologies, Moscow, Russia
2 Multidisciplinary Medical Center «CHAO», Perm, Russia;
3 Perm State Medical University named after Academician E.A. Wagner (PSMU), Perm, Russia;
4 «Donni Clinic» of Aesthetic Medicine, Gynecology and Cosmetology, Moscow, Russia;
5 Patrice Lumumba People's Friendship University of Russia (RUDN University), Moscow, Russia
mikhailova@martinex.ru
Abstract
Aesthetic gynecology is a constantly evolving area that is gradually being recognized as a full-fledged area of regenerative medicine, in which the issue of control over biological processes at the tissue level is central. In this context, hyaluronic acid (HA), that occupied the niche of a biomechanical filler over a long time, has undergone a fundamental perceptual shift: from an inert intracellular matrix component to a highly active signaling molecule. Such a paradigm shift from passive substitution to active control over regeneration dictates the need for critical reconsideration of the therapeutic arsenal. In terms of biochemistry, the classical HA-based cross-linked fillers solving the volume adjustment problems demonstrate severe limitations when there is a need for subtle modulation of the cellular microenvironment. Thus, the development of platforms that can not only prolong the HA tissue residence, but also ensure the receptor-specific delivery and controlled release of bioactive ligands, becomes a challenge of modern biomedicine. The review is focused on the evolutionary transition from standard fillers to the fundamentally new class of drugs, biorepair agents, as well as on the scientific substantiation of the targeted conjugation technology as a tool to overcome the existing therapeutic limitations.
Keywords: hyaluronic acid, aesthetic gynecology, regenerative medicine, biorepair agents, conjugation, CD44 receptor.
For citation: Mikhaylova N.P., Chazova O.A., Znatdinov D.I., Avetisyan D.G. Hyaluronic acid evolution in gynecological practice: from biomechanical properties to receptor-mediated regeneration control. Clinical review for general practice. 2025; 6 (9): 49–54 (In Russ.). DOI: 10.47407/kr2025.6.9.00672
Важно отметить, что одним из ключевых аспектов внедрения любых методик в эстетической и реконструктивной гинекологии является их доказанное влияние и на качество жизни пациентов. Проведенные исследования демонстрируют, что подобные вмешательства оказывают значимое положительное влияние на психологическое благополучие, что проявляется в достоверном улучшении субъективной оценки тела и повышении самооценки в послеоперационном периоде, при этом возраст пациенток является значимым дифференцирующим фактором [4].
ГК, длительное время рассматривавшаяся преимущественно как структурный компонент внеклеточного матрикса (ВКМ) кожи, суставов, глаз и других тканей, в последние десятилетия кардинально переосмыслена в своей биологической роли. Открытие ее сложных функций, опосредованных специфическими клеточными рецепторами (такими как CD44 и RHAMM), выявило ключевое значение ГК в регуляции фундаментальных клеточных процессов: пролиферации, миграции, адгезии и дифференцировки. Молекулярная масса ГК является критическим параметром при разработке биоматериалов для регенеративной медицины, определяя их взаимодействие с CD44 и, как следствие, клиническую эффективность [5]. Высокомолекулярные формы обладают преимущественно противовоспалительным, протективным и пространственно-организующим действием, в то время как низкомолекулярные фрагменты часто проявляют провоспалительные и ангиогенные свойства, играя роль в ремоделировании тканей, например при заживлении ран [6]. Благодаря уникальным физико-химическим свойствам (биосовместимость, биодеградируемость, высокая гидрофильность, вязкоэластичность) и возможности направленной химической модификации, ГК и ее производные нашли широчайшее применение в медицине. Они активно используются не только в офтальмологии и лечении остеоартрита, но и являются основой для создания современных биоматериалов в тканевой инженерии. В дерматологии, косметологии и регенеративной медицине производные ГК применяются в качестве раневых покрытий, каркасов (скаффолдов) для выращивания кожных эквивалентов (включая дерму и микроциркуляторную сеть), систем доставки биологически активных молекул, существенно улучшая процессы регенерации кожи, а также в рамках эстетического и антивозрастного направления. Особое значение применение ГК и ее производных приобретает в гинекологии, где они используются как для структурной коррекции, так и для стимуляции регенеративных процессов в тканях репродуктивной системы. Физиологическая роль гиалуронана в женской репродуктивной системе фундаментальна: ГК является ключевым компонентом ВКМ эндометрия, цервикальной слизи и яичников, регулируя гидратацию тканей, клеточную миграцию, пролиферацию, воспалительный ответ и процессы ремоделирования во время менструального цикла, имплантации и регенерации [7]. Таким образом, ГК трансформировалась из пассивного компонента ВКМ в активную сигнальную молекулу с огромным мультидисциплинарным терапевтическим потенциалом [8].
Актуальность и принципиальные отличия различных форм гиалуроновой кислоты
Нативная ГК обладает линейной полимерной структурой с выраженной гидрофильно-гидрофобной организацией, формирующей жесткие цепи в растворе. Ее третичная структура и сетчатая организация остаются предметом дискуссий, однако доказано влияние противоионов (Na⁺, Ca²⁺) на конформацию цепи (2- или 3-спираль) и физико-химические свойства. Введение препаратов нативной ГК (биоревитализация) представляет собой минимально инвазивную методику, применяемую с целью восстановления тканевого гомеостаза и коррекции инволюционных изменений кожи. Клинически это проявляется в улучшении гидратации, тургора тканей, уменьшении выраженности атрофических изменений слизистых оболочек и кожи генитальной области [9]. Несмотря на биосовместимость, нативная ГК быстро деградирует in vivo под действием гиалуронидаз и активного кислорода, что ограничивает ее применение – короткий период полувыведения требует разработки стратегий стабилизации (например, сшивания) [10].
Сшитая ГК (кросс-линк) создается для повышения механической прочности, вязкоэластичности и пролонгации действия in vivo за счет образования сетки между цепями с помощью бифункциональных агентов [11]:
– сшивка по ОН-группам: использование бисэпоксидов (BDDE, PEGDE), дивинилсульфона (DVS), ангидридов (этерификация) или альдегидов (образование полуацеталей). Однако, стоит отметить, что BDDE – золотой стандарт и наиболее распространенный сшиватель;
– сшивка по СООН-группам. Например, диамины или бис-карбодиимиды (образование бис-N-ацилмочевин);
– перспективные методы: фотосшивание, ферментативное сшивание и двойное сшивание (ионное и ковалентное), позволяющие тонко настраивать свойства материалов для тканевой инженерии и доставки лекарств. Безопасность и стабильность сшитого продукта критически зависят от типа сшивателя и степени очистки.
Филлеры на основе сшитой ГК имеют относительно широкие показания и активно используются для реставрации объема, тонуса больших половых губ и зияния вульварного кольца у женщин репродуктивного, а также перименопаузального возраста, что является безопасной и эффективной малоинвазивной альтернативой [12, 13]. Однако классические филлеры на основе сшитой ГК выполняют исключительно пространственно-механическую функцию коррекции объема, что является их фундаментальным ограничением, несмотря на потенциальную трансдукцию [14]. Контурную пластику также комбинируют с радиочастотным воздействием у пациенток с урогенитальной атрофией и синдромом вагинальной релаксации [15]. В общем и целом активное развитие и внедрение в клиническую практику неинвазивных аппаратных методик в комбинации с филлерами продемонстрировали значительную эффективность в коррекции состояний, ассоциированных с дефицитом соединительной ткани: урогенитальной атрофии, синдромом вагинальной релаксации, стрессового недержания мочи и гиперактивного мочевого пузыря и т.п. [16–18]. Однако эти методы, будучи эффективными для ремоделирования существующего матрикса, также имеют ограниченный потенциал для управления более сложными процессами физиологической регенерации. К тому же следует учитывать, что та же IPL-технология обладает дегидратирующим эффектом, так как вода – один из хромофоров для интенсивного импульсного света. Чтобы компенсировать потерю влаги, перед процедурой IPL и сразу после интрадермально вводят нативную ГК (процедура биоревитализации). Это помогает поддерживать водный баланс кожи и усиливает терапевтический эффект широкополосного импульсного света [19, 20]. Это закономерно актуализировало разработку следующего поколения вмешательств – инъекционных платформ, способных не только обеспечивать структурную поддержку и биоревитализацию, но и осуществлять адресную доставку эффекторов регенерации. Параллельно наметился принципиально иной вектор – переход от преимущественно механической коррекции объема к активному биологическому воздействию на тканевые процессы.
Метод представляет собой стратегию направленной доставки, основанную на формировании ковалентных связей (сложноэфирных, амидных) между функциональными группами ГК (-COOH, -OH) и лигандами [25]. Данная технология позволяет создавать препараты ГК нового класса с улучшенной фармакокинетикой: повышается растворимость гидрофобных агентов, обеспечивается пролонгированное высвобождение и рецептор-специфичный транспорт [26]. К тому же это приводит к ограничению подвижности полимерной цепи и стерическому затруднению доступа гиалуронидаз к субстрату, что значительно пролонгирует время нахождения модифицированного геля в тканях по сравнению с нативной ГК [27]. Перспективность решения подтверждается разработкой адресных систем для лечения даже онкологических заболеваний, где конъюгаты ГК выступают платформой для таргетной терапии [28]. Результаты других исследований демонстрируют, что конъюгация белкового антигена с ГК формирует перспективную вакцинную платформу для клинического применения [29].
Важнейшим механизмом, обеспечивающим целенаправленную интраклеточную доставку активных компонентов в рамках стратегии биорепарации, является рецептор-опосредованный транспорт, ключевым игроком в котором выступает трансмембранный гликопротеин CD44. Будучи основным рецептором гиалуронана, CD44 экспрессируется на поверхности широкого спектра клеток, включая фибробласты, кератиноциты, эндотелиальные и иммунокомпетентные клетки, играя ключевую роль в клеточной адгезии, миграции, пролиферации и передаче сигналов [30]. Таргетинг CD44 с помощью конъюгированных с ГК комплексов позволяет реализовать механизм активного рецептор-опосредованного эндоцитоза. Данный процесс не только обеспечивает селективное накопление терапевтической конструкции в клетках-мишенях, но и защищает биологически активные молекулы от преждевременной деградации в межклеточном пространстве. Последующая интрацеллюлярная обработка в эндосомально-лизосомальном компартменте приводит к контролируемому высвобождению активных лигандов, что в совокупности значительно повышает биодоступность и терапевтическую эффективность доставляемых компонентов и открывает новые перспективы для управления регенеративными процессами на тканевом уровне [31–33].
Достижения в области конъюгации ГК, демонстрирующие столь впечатляющие результаты в дерматологии, косметологии, регенеративной медицине и даже онкотерапии, закономерно открывают перспективы для гинекологии. Применение конъюгированных форм ГК, полученных преимущественно методом твердофазной модификации, знаменует качественно новый этап в гинекологической практике, преодолевая ключевые ограничения нативной ГК и стандартных коктейлей. Пример коммерческой реализации – технология Hyalrepair [34]. Принципиальное значение имеет персонализация состава терапевтического комплекса, основанная на тщательном анализе анамнеза пациента. Именно анамнез диктует выбор оптимальных агентов (витаминов C, B2, B9, глутатиона, микроэлементов Mg/Zn и т.п.), необходимых для:
– стимуляции регенеративных процессов (ремоделирования экстрацеллюлярного матрикса, ангиогенеза, клеточной пролиферации и дифференцировки) в зонах повреждения или локальной недостаточности;
– эффективной таргетной доставки противовоспалительных или иммунорегуляторных молекул непосредственно к клеткам-мишеням в очаге хронического воспаления;
– точной модуляции локального клеточного и гуморального ответа, исходя из индивидуальных особенностей патогенеза.
К примеру, проведенный анализ мультифакторного физиологического воздействия витамина С позволяет констатировать, что данный микронутриент обладает существенным регуляторным потенциалом в отношении морфофункционального состояния тканей репродуктивного тракта. Его роль не ограничивается классическим кофакторным участием в гидроксилировании пролина и лизина, обеспечивающем конформационную стабильность и прочность коллагенов базальных мембран и стромы, но и включает модуляцию процессов аутофагии, ингибирование тирозиназы и эпигенетическую регуляцию через активацию TET-диоксигеназ. Однако высокая лабильность молекулы и возраст-ассоциированное снижение экспрессии натрий-зависимых переносчиков SVCT1/SVCT2 лимитируют ее биодоступность при системном введении (пероральный прием). В свете изложенного стратегия интрадермальной доставки стабильных производных аскорбата (таких как аскорбил-2-фосфат), ковалентно конъюгированных с гиалуронаном, представляет собой патогенетически обоснованный метод преодоления фармакокинетических ограничений. Данный подход обеспечивает создание пролонгированного депо в целевой ткани, что является необходимым условием для реализации плейотропных эффектов витамина С и потенцирования процессов репарации и ремоделирования ВКМ [35]. Данный комплекс позволяет достичь клинически значимых эффектов: устойчивой стимуляции неоколлагенеза и эластогенеза, коррекции локальной гиперпигментации, оптимизации клеточного обновления и потенцирования противоопухолевого иммунного надзора на тканевом уровне, что в совокупности повышает эффективность терапии состояний, ассоциированных с дистрофией и инволюцией тканей вульвовагинальной области.
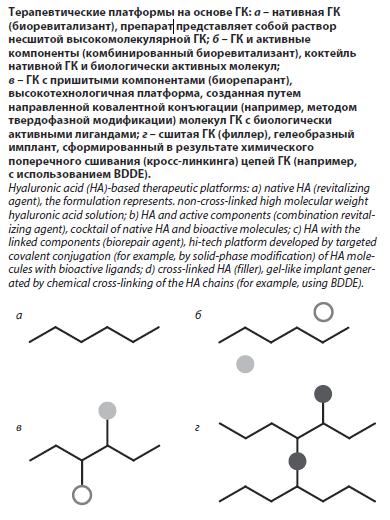 Класс препаратов с конъюгированными формами ГК был назван биорепарантами, подчеркивая их репаративный потенциал, достигнутый за счет инженерного решения по контролируемой доставке и высвобождению активных компонентов. Однако на практике существует терминологическая путаница: врачи часто ошибочно приравнивают биорепаранты к комбинированным или комплексным биоревитализантам или коктейлям (см. рисунок). Критически важно понимать, что термин «биорепарация» отражает именно технологический принцип создания препарата (модификация носителя для пролонгированного и таргетного действия), а не просто факт наличия в его составе нескольких биологически активных веществ.
Класс препаратов с конъюгированными формами ГК был назван биорепарантами, подчеркивая их репаративный потенциал, достигнутый за счет инженерного решения по контролируемой доставке и высвобождению активных компонентов. Однако на практике существует терминологическая путаница: врачи часто ошибочно приравнивают биорепаранты к комбинированным или комплексным биоревитализантам или коктейлям (см. рисунок). Критически важно понимать, что термин «биорепарация» отражает именно технологический принцип создания препарата (модификация носителя для пролонгированного и таргетного действия), а не просто факт наличия в его составе нескольких биологически активных веществ.
Важным аспектом является дифференцированный подход к выбору техники введения. Введение биорепарантов может осуществляться как с использованием иглы, так и канюли. Однако применение канюли является предпочтительным, поскольку обеспечивает более гомогенное, малотравматичное и стандартизированное распределение препарата за счет использования меньшего количества точек входа. Это особенно актуально в контексте использования современных решений, поскольку безопасность и атравматичность техник напрямую влияет на реализацию их репаративного потенциала и эффективность рецептор-опосредованного управления регенерацией [36].
конъюгированной ГК являются стратегически перспективным направлением, требующим дальнейших рандомизированных исследований для формализации протоколов и оценки отдаленных результатов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare that there is no conflict of interest.
Информация об авторах
Information about the authors
Михайлова Наталья Павловна – канд. мед. наук., ст. науч. сотр., АНО «Международный научно-исследовательский центр инновационных технологий Мартинекс». Е-mail: mikhailova@martinex.ru; ORCID: 0009-0005-4494-0170
Natalia P. Mikhaylova – Cand. Sci. (Med.), Senior Res. Officer, Martinex International Research Center for Innovative Technologies. Е-mail: mikhailova@martinex.ru; ORCID: 0009-0005-4494-0170
Чазова Ольга Алексеевна — глав. врач многопрофильного медицинского центра «ЧАО»; аспирант каф. акушерства и гинекологии ФГБОУ ВО «ПГМУ им. академика Е.А. Вагнера» Минздрава России. E-mail: olyachazova@yandex.ru; ORCID: 0009-0001-0183-095X
Olga A. Chazova – Head Physician, Multidisciplinary Medical Center "CHAO"; Postgraduate student, Perm State Medical University named after Academician E.A. Wagner (PSMU). E-mail: olyachazova@yandex.ru; ORCID: 0009-0001-0183-095X
Знатдинов Дамир Ильдусович – науч. сотр., АНО «Международный научно-исследовательский центр инновационных технологий Мартинекс». E-mail: znatdinov@martinex.ru; ORCID: 0009-0001-3227-4415
Damir I. Znatdinov – Res. Officer, Martinex International Research Center for Innovative Technologies. E-mail: znatdinov@martinex.ru; ORCID: 0009-0001-3227-4415
Аветисян Донара Григоровна – глав. врач клиники эстетической медицины, гинекологии и косметологии «Донни клиник»; аспирант каф. акушерства и гинекологии, ФГАОУ ВО «РУДН им. Патриса Лумумбы». E-mail: Doc.donara@gmail.com; ORCID: 0009-0008-6561-8289
Donara G. Avetisyan – Head Physician, "Donni Clinic" of Aesthetic Medicine, Gynecology and Cosmetology; Postgraduate student, Patrice Lumumba People’s Friendship University of Russia (RUDN University).
E-mail: Doc.donara@gmail.com; ORCID: 0009-0008-6561-8289
Поступила в редакцию: 02.09.2025
Поступила после рецензирования: 08.09.2025
Принята к публикации: 11.09.2025
Received: 02.09.2025
Revised: 08.09.2025
Accepted: 11.09.2025
Клинический разбор в общей медицине №9 2025
Эволюция гиалуроновой кислоты в гинекологической практике: от биомеханических свойств к рецептор-опосредованному управлению регенерацией
Номера страниц в выпуске:49-54
Аннотация
Эстетическая гинекология – динамично развивающаяся область, которая постепенно утверждается в качестве полноценной отрасли регенеративной медицины, где центральным становится вопрос управления биологическими процессами на тканевом уровне. В этом контексте гиалуроновая кислота (ГК), длительное время занимавшая нишу биомеханического филлера, претерпела фундаментальную трансформацию восприятия – от инертного компонента внеклеточного матрикса до высокоактивной сигнальной молекулы. Данный парадигмальный сдвиг от пассивного замещения к активному управлению регенерацией диктует необходимость критического переосмысления терапевтического арсенала. Биохимически сложилось, что классические сшитые филлеры на основе ГК, решающие задачи объемной коррекции, демонстрируют выраженную ограниченность при необходимости тонкой модуляции клеточного микроокружения. Таким образом, вызовом для современной биомедицины становится разработка платформ, способных не только пролонгировать резидентность ГК в тканях, но и обеспечить рецептор-специфичную доставку и контролируемое высвобождение биологически активных лигандов. Настоящий обзор посвящен анализу эволюционного перехода от стандартных филлеров к принципиально новому классу препаратов – биорепарантам и научному обоснованию технологий направленной конъюгации как инструменту преодоления существующих терапевтических ограничений.
Ключевые слова: гиалуроновая кислота, эстетическая гинекология, регенеративная медицина, биорепаранты, конъюгация,
рецептор CD44.
Для цитирования: Михайлова Н.П., Чазова О.А., Знатдинов Д.И., Аветисян Д.Г. Эволюция гиалуроновой кислоты в гинекологической практике: от биомеханических свойств к рецептор-опосредованному управлению регенерацией. Клинический разбор в общей медицине. 2025; 6 (9): 49–54. DOI: 10.47407/kr2025.6.9.00672
Эстетическая гинекология – динамично развивающаяся область, которая постепенно утверждается в качестве полноценной отрасли регенеративной медицины, где центральным становится вопрос управления биологическими процессами на тканевом уровне. В этом контексте гиалуроновая кислота (ГК), длительное время занимавшая нишу биомеханического филлера, претерпела фундаментальную трансформацию восприятия – от инертного компонента внеклеточного матрикса до высокоактивной сигнальной молекулы. Данный парадигмальный сдвиг от пассивного замещения к активному управлению регенерацией диктует необходимость критического переосмысления терапевтического арсенала. Биохимически сложилось, что классические сшитые филлеры на основе ГК, решающие задачи объемной коррекции, демонстрируют выраженную ограниченность при необходимости тонкой модуляции клеточного микроокружения. Таким образом, вызовом для современной биомедицины становится разработка платформ, способных не только пролонгировать резидентность ГК в тканях, но и обеспечить рецептор-специфичную доставку и контролируемое высвобождение биологически активных лигандов. Настоящий обзор посвящен анализу эволюционного перехода от стандартных филлеров к принципиально новому классу препаратов – биорепарантам и научному обоснованию технологий направленной конъюгации как инструменту преодоления существующих терапевтических ограничений.
Ключевые слова: гиалуроновая кислота, эстетическая гинекология, регенеративная медицина, биорепаранты, конъюгация,
рецептор CD44.
Для цитирования: Михайлова Н.П., Чазова О.А., Знатдинов Д.И., Аветисян Д.Г. Эволюция гиалуроновой кислоты в гинекологической практике: от биомеханических свойств к рецептор-опосредованному управлению регенерацией. Клинический разбор в общей медицине. 2025; 6 (9): 49–54. DOI: 10.47407/kr2025.6.9.00672
Hyaluronic acid evolution in gynecological practice: from biomechanical properties to receptor-mediated regeneration control
Natalia P. Mikhaylova1, Olga A. Chazova2,3, Damir I. Znatdinov1, Donara G. Avetisyan4,51 Martinex International Research Center for Innovative Technologies, Moscow, Russia
2 Multidisciplinary Medical Center «CHAO», Perm, Russia;
3 Perm State Medical University named after Academician E.A. Wagner (PSMU), Perm, Russia;
4 «Donni Clinic» of Aesthetic Medicine, Gynecology and Cosmetology, Moscow, Russia;
5 Patrice Lumumba People's Friendship University of Russia (RUDN University), Moscow, Russia
mikhailova@martinex.ru
Abstract
Aesthetic gynecology is a constantly evolving area that is gradually being recognized as a full-fledged area of regenerative medicine, in which the issue of control over biological processes at the tissue level is central. In this context, hyaluronic acid (HA), that occupied the niche of a biomechanical filler over a long time, has undergone a fundamental perceptual shift: from an inert intracellular matrix component to a highly active signaling molecule. Such a paradigm shift from passive substitution to active control over regeneration dictates the need for critical reconsideration of the therapeutic arsenal. In terms of biochemistry, the classical HA-based cross-linked fillers solving the volume adjustment problems demonstrate severe limitations when there is a need for subtle modulation of the cellular microenvironment. Thus, the development of platforms that can not only prolong the HA tissue residence, but also ensure the receptor-specific delivery and controlled release of bioactive ligands, becomes a challenge of modern biomedicine. The review is focused on the evolutionary transition from standard fillers to the fundamentally new class of drugs, biorepair agents, as well as on the scientific substantiation of the targeted conjugation technology as a tool to overcome the existing therapeutic limitations.
Keywords: hyaluronic acid, aesthetic gynecology, regenerative medicine, biorepair agents, conjugation, CD44 receptor.
For citation: Mikhaylova N.P., Chazova O.A., Znatdinov D.I., Avetisyan D.G. Hyaluronic acid evolution in gynecological practice: from biomechanical properties to receptor-mediated regeneration control. Clinical review for general practice. 2025; 6 (9): 49–54 (In Russ.). DOI: 10.47407/kr2025.6.9.00672
Введение
Эстетическая и регенеративная гинекология представляет собой динамично развивающуюся междисциплинарную область, интегрирующую достижения дерматологии, гинекологии и пластической хирургии для коррекции косметологических и функциональных нарушений вульвовагинальной области. В арсенале специалиста присутствует широкий спектр методик, включающий как инвазивные хирургические вмешательства, так и неинвазивные подходы с применением аппаратных и инъекционных методов, среди которых ключевое место занимают препараты на основе гиалуроновой кислоты (ГК). Современный подход к здоровью данной области требует комплексного понимания ее анатомо-физиологических особенностей, микробиоценоза и защитных механизмов, и несмотря на растущий спрос, обусловленный социокультурными факторами и стремлением к улучшению качества жизни, область характеризуется выраженным дефицитом доказательных данных относительно отдаленной эффективности и безопасности многих вмешательств, что актуализирует необходимость тщательного информирования пациенток, разработки стандартизированных протоколов и проведения дальнейших проспективных исследований [1–3].Важно отметить, что одним из ключевых аспектов внедрения любых методик в эстетической и реконструктивной гинекологии является их доказанное влияние и на качество жизни пациентов. Проведенные исследования демонстрируют, что подобные вмешательства оказывают значимое положительное влияние на психологическое благополучие, что проявляется в достоверном улучшении субъективной оценки тела и повышении самооценки в послеоперационном периоде, при этом возраст пациенток является значимым дифференцирующим фактором [4].
ГК, длительное время рассматривавшаяся преимущественно как структурный компонент внеклеточного матрикса (ВКМ) кожи, суставов, глаз и других тканей, в последние десятилетия кардинально переосмыслена в своей биологической роли. Открытие ее сложных функций, опосредованных специфическими клеточными рецепторами (такими как CD44 и RHAMM), выявило ключевое значение ГК в регуляции фундаментальных клеточных процессов: пролиферации, миграции, адгезии и дифференцировки. Молекулярная масса ГК является критическим параметром при разработке биоматериалов для регенеративной медицины, определяя их взаимодействие с CD44 и, как следствие, клиническую эффективность [5]. Высокомолекулярные формы обладают преимущественно противовоспалительным, протективным и пространственно-организующим действием, в то время как низкомолекулярные фрагменты часто проявляют провоспалительные и ангиогенные свойства, играя роль в ремоделировании тканей, например при заживлении ран [6]. Благодаря уникальным физико-химическим свойствам (биосовместимость, биодеградируемость, высокая гидрофильность, вязкоэластичность) и возможности направленной химической модификации, ГК и ее производные нашли широчайшее применение в медицине. Они активно используются не только в офтальмологии и лечении остеоартрита, но и являются основой для создания современных биоматериалов в тканевой инженерии. В дерматологии, косметологии и регенеративной медицине производные ГК применяются в качестве раневых покрытий, каркасов (скаффолдов) для выращивания кожных эквивалентов (включая дерму и микроциркуляторную сеть), систем доставки биологически активных молекул, существенно улучшая процессы регенерации кожи, а также в рамках эстетического и антивозрастного направления. Особое значение применение ГК и ее производных приобретает в гинекологии, где они используются как для структурной коррекции, так и для стимуляции регенеративных процессов в тканях репродуктивной системы. Физиологическая роль гиалуронана в женской репродуктивной системе фундаментальна: ГК является ключевым компонентом ВКМ эндометрия, цервикальной слизи и яичников, регулируя гидратацию тканей, клеточную миграцию, пролиферацию, воспалительный ответ и процессы ремоделирования во время менструального цикла, имплантации и регенерации [7]. Таким образом, ГК трансформировалась из пассивного компонента ВКМ в активную сигнальную молекулу с огромным мультидисциплинарным терапевтическим потенциалом [8].
Актуальность и принципиальные отличия различных форм гиалуроновой кислоты
Нативная ГК обладает линейной полимерной структурой с выраженной гидрофильно-гидрофобной организацией, формирующей жесткие цепи в растворе. Ее третичная структура и сетчатая организация остаются предметом дискуссий, однако доказано влияние противоионов (Na⁺, Ca²⁺) на конформацию цепи (2- или 3-спираль) и физико-химические свойства. Введение препаратов нативной ГК (биоревитализация) представляет собой минимально инвазивную методику, применяемую с целью восстановления тканевого гомеостаза и коррекции инволюционных изменений кожи. Клинически это проявляется в улучшении гидратации, тургора тканей, уменьшении выраженности атрофических изменений слизистых оболочек и кожи генитальной области [9]. Несмотря на биосовместимость, нативная ГК быстро деградирует in vivo под действием гиалуронидаз и активного кислорода, что ограничивает ее применение – короткий период полувыведения требует разработки стратегий стабилизации (например, сшивания) [10].
Сшитая ГК (кросс-линк) создается для повышения механической прочности, вязкоэластичности и пролонгации действия in vivo за счет образования сетки между цепями с помощью бифункциональных агентов [11]:
– сшивка по ОН-группам: использование бисэпоксидов (BDDE, PEGDE), дивинилсульфона (DVS), ангидридов (этерификация) или альдегидов (образование полуацеталей). Однако, стоит отметить, что BDDE – золотой стандарт и наиболее распространенный сшиватель;
– сшивка по СООН-группам. Например, диамины или бис-карбодиимиды (образование бис-N-ацилмочевин);
– перспективные методы: фотосшивание, ферментативное сшивание и двойное сшивание (ионное и ковалентное), позволяющие тонко настраивать свойства материалов для тканевой инженерии и доставки лекарств. Безопасность и стабильность сшитого продукта критически зависят от типа сшивателя и степени очистки.
Филлеры на основе сшитой ГК имеют относительно широкие показания и активно используются для реставрации объема, тонуса больших половых губ и зияния вульварного кольца у женщин репродуктивного, а также перименопаузального возраста, что является безопасной и эффективной малоинвазивной альтернативой [12, 13]. Однако классические филлеры на основе сшитой ГК выполняют исключительно пространственно-механическую функцию коррекции объема, что является их фундаментальным ограничением, несмотря на потенциальную трансдукцию [14]. Контурную пластику также комбинируют с радиочастотным воздействием у пациенток с урогенитальной атрофией и синдромом вагинальной релаксации [15]. В общем и целом активное развитие и внедрение в клиническую практику неинвазивных аппаратных методик в комбинации с филлерами продемонстрировали значительную эффективность в коррекции состояний, ассоциированных с дефицитом соединительной ткани: урогенитальной атрофии, синдромом вагинальной релаксации, стрессового недержания мочи и гиперактивного мочевого пузыря и т.п. [16–18]. Однако эти методы, будучи эффективными для ремоделирования существующего матрикса, также имеют ограниченный потенциал для управления более сложными процессами физиологической регенерации. К тому же следует учитывать, что та же IPL-технология обладает дегидратирующим эффектом, так как вода – один из хромофоров для интенсивного импульсного света. Чтобы компенсировать потерю влаги, перед процедурой IPL и сразу после интрадермально вводят нативную ГК (процедура биоревитализации). Это помогает поддерживать водный баланс кожи и усиливает терапевтический эффект широкополосного импульсного света [19, 20]. Это закономерно актуализировало разработку следующего поколения вмешательств – инъекционных платформ, способных не только обеспечивать структурную поддержку и биоревитализацию, но и осуществлять адресную доставку эффекторов регенерации. Параллельно наметился принципиально иной вектор – переход от преимущественно механической коррекции объема к активному биологическому воздействию на тканевые процессы.
Принципы использования и перспективы конъюгированных форм гиалуроновой кислоты в гинекологии
Синергия данных международных клинических испытаний за последние 15 лет указывает на значительные преимущества комбинации ГК и биологически активных компонентов (витаминов, аминокислот, микроэлементов, пептидов). Данная комбинация, в отличие от применения нативной ГК, обеспечивает достоверное увеличение эффективности вмешательств. Ключевые механизмы включают стимуляцию пролиферации клеточного пула, ускоренную реэпителизацию, формирование сети коллагеновых волокон и улучшение качества регенеративной ткани и т.п. Полученные данные подтверждают, что данные композиции воздействуют на фундаментальные механизмы клеточного старения [21–23]. Логичным продолжением работы подобных коктейлей является принципиально новый подход к пролонгации резидентного времени нахождения ГК в тканях – конъюгация ГК с биологически активными молекулами под воздействием ультравысокого давления и сдвиговой деформации без использования химических сшивающих агентов [24].Метод представляет собой стратегию направленной доставки, основанную на формировании ковалентных связей (сложноэфирных, амидных) между функциональными группами ГК (-COOH, -OH) и лигандами [25]. Данная технология позволяет создавать препараты ГК нового класса с улучшенной фармакокинетикой: повышается растворимость гидрофобных агентов, обеспечивается пролонгированное высвобождение и рецептор-специфичный транспорт [26]. К тому же это приводит к ограничению подвижности полимерной цепи и стерическому затруднению доступа гиалуронидаз к субстрату, что значительно пролонгирует время нахождения модифицированного геля в тканях по сравнению с нативной ГК [27]. Перспективность решения подтверждается разработкой адресных систем для лечения даже онкологических заболеваний, где конъюгаты ГК выступают платформой для таргетной терапии [28]. Результаты других исследований демонстрируют, что конъюгация белкового антигена с ГК формирует перспективную вакцинную платформу для клинического применения [29].
Важнейшим механизмом, обеспечивающим целенаправленную интраклеточную доставку активных компонентов в рамках стратегии биорепарации, является рецептор-опосредованный транспорт, ключевым игроком в котором выступает трансмембранный гликопротеин CD44. Будучи основным рецептором гиалуронана, CD44 экспрессируется на поверхности широкого спектра клеток, включая фибробласты, кератиноциты, эндотелиальные и иммунокомпетентные клетки, играя ключевую роль в клеточной адгезии, миграции, пролиферации и передаче сигналов [30]. Таргетинг CD44 с помощью конъюгированных с ГК комплексов позволяет реализовать механизм активного рецептор-опосредованного эндоцитоза. Данный процесс не только обеспечивает селективное накопление терапевтической конструкции в клетках-мишенях, но и защищает биологически активные молекулы от преждевременной деградации в межклеточном пространстве. Последующая интрацеллюлярная обработка в эндосомально-лизосомальном компартменте приводит к контролируемому высвобождению активных лигандов, что в совокупности значительно повышает биодоступность и терапевтическую эффективность доставляемых компонентов и открывает новые перспективы для управления регенеративными процессами на тканевом уровне [31–33].
Достижения в области конъюгации ГК, демонстрирующие столь впечатляющие результаты в дерматологии, косметологии, регенеративной медицине и даже онкотерапии, закономерно открывают перспективы для гинекологии. Применение конъюгированных форм ГК, полученных преимущественно методом твердофазной модификации, знаменует качественно новый этап в гинекологической практике, преодолевая ключевые ограничения нативной ГК и стандартных коктейлей. Пример коммерческой реализации – технология Hyalrepair [34]. Принципиальное значение имеет персонализация состава терапевтического комплекса, основанная на тщательном анализе анамнеза пациента. Именно анамнез диктует выбор оптимальных агентов (витаминов C, B2, B9, глутатиона, микроэлементов Mg/Zn и т.п.), необходимых для:
– стимуляции регенеративных процессов (ремоделирования экстрацеллюлярного матрикса, ангиогенеза, клеточной пролиферации и дифференцировки) в зонах повреждения или локальной недостаточности;
– эффективной таргетной доставки противовоспалительных или иммунорегуляторных молекул непосредственно к клеткам-мишеням в очаге хронического воспаления;
– точной модуляции локального клеточного и гуморального ответа, исходя из индивидуальных особенностей патогенеза.
К примеру, проведенный анализ мультифакторного физиологического воздействия витамина С позволяет констатировать, что данный микронутриент обладает существенным регуляторным потенциалом в отношении морфофункционального состояния тканей репродуктивного тракта. Его роль не ограничивается классическим кофакторным участием в гидроксилировании пролина и лизина, обеспечивающем конформационную стабильность и прочность коллагенов базальных мембран и стромы, но и включает модуляцию процессов аутофагии, ингибирование тирозиназы и эпигенетическую регуляцию через активацию TET-диоксигеназ. Однако высокая лабильность молекулы и возраст-ассоциированное снижение экспрессии натрий-зависимых переносчиков SVCT1/SVCT2 лимитируют ее биодоступность при системном введении (пероральный прием). В свете изложенного стратегия интрадермальной доставки стабильных производных аскорбата (таких как аскорбил-2-фосфат), ковалентно конъюгированных с гиалуронаном, представляет собой патогенетически обоснованный метод преодоления фармакокинетических ограничений. Данный подход обеспечивает создание пролонгированного депо в целевой ткани, что является необходимым условием для реализации плейотропных эффектов витамина С и потенцирования процессов репарации и ремоделирования ВКМ [35]. Данный комплекс позволяет достичь клинически значимых эффектов: устойчивой стимуляции неоколлагенеза и эластогенеза, коррекции локальной гиперпигментации, оптимизации клеточного обновления и потенцирования противоопухолевого иммунного надзора на тканевом уровне, что в совокупности повышает эффективность терапии состояний, ассоциированных с дистрофией и инволюцией тканей вульвовагинальной области.
 Класс препаратов с конъюгированными формами ГК был назван биорепарантами, подчеркивая их репаративный потенциал, достигнутый за счет инженерного решения по контролируемой доставке и высвобождению активных компонентов. Однако на практике существует терминологическая путаница: врачи часто ошибочно приравнивают биорепаранты к комбинированным или комплексным биоревитализантам или коктейлям (см. рисунок). Критически важно понимать, что термин «биорепарация» отражает именно технологический принцип создания препарата (модификация носителя для пролонгированного и таргетного действия), а не просто факт наличия в его составе нескольких биологически активных веществ.
Класс препаратов с конъюгированными формами ГК был назван биорепарантами, подчеркивая их репаративный потенциал, достигнутый за счет инженерного решения по контролируемой доставке и высвобождению активных компонентов. Однако на практике существует терминологическая путаница: врачи часто ошибочно приравнивают биорепаранты к комбинированным или комплексным биоревитализантам или коктейлям (см. рисунок). Критически важно понимать, что термин «биорепарация» отражает именно технологический принцип создания препарата (модификация носителя для пролонгированного и таргетного действия), а не просто факт наличия в его составе нескольких биологически активных веществ.Важным аспектом является дифференцированный подход к выбору техники введения. Введение биорепарантов может осуществляться как с использованием иглы, так и канюли. Однако применение канюли является предпочтительным, поскольку обеспечивает более гомогенное, малотравматичное и стандартизированное распределение препарата за счет использования меньшего количества точек входа. Это особенно актуально в контексте использования современных решений, поскольку безопасность и атравматичность техник напрямую влияет на реализацию их репаративного потенциала и эффективность рецептор-опосредованного управления регенерацией [36].
Заключение
Таким образом, эволюция терапевтического применения ГК в гинекологической практике преодолела принципиальный рубеж, трансформировавшись от биомеханической коррекции объемного дефицита на основе сшитых гелей к стратегии активного, рецептор-опосредованного управления тканевой регенерацией с использованием конъюгированных форм. Установлено, что сшитый гиалуронан, выполняя исключительно объемно-структурные функции, исчерпал свой терапевтический потенциал в контексте решения сложных задач реконструктивной и эстетической гинекологии, требующих модуляции клеточного микроокружения. Ключом к преодолению этих ограничений является использование технологий направленного конъюгирования, в частности метода твердофазной модификации под воздействием ультравысокого давления и сдвиговой деформации, который позволяет создавать стабильные ковалентные комплексы ГК с биологически активными лигандами без применения токсичных сшивающих агентов. Такие конъюгаты, репрезентирующие класс биорепарантов, обеспечивают не только пролонгированную резидентность в тканях за счет стерического затруднения доступа гиалуронидаз, но и осуществляют рецептор-специфичный (CD44-опосредованный) транспорт и контролируемое высвобождение активных компонентов, что позволяет целенаправленно влиять на фундаментальные процессы пролиферации, дифференцировки, неоангиогенеза и ремоделирования ВКМ. Персонализированный подбор активных компонентов конъюгата, детерминированный индивидуальным патогенезом, открывает новые перспективы для таргетной терапии хронического воспаления, урогенитальной атрофии и последствий инволютивных изменений, что знаменует становление нового парадигмального подхода – от коррекции к управляемой регенерации в гинекологической практике. Таким образом, разработка и внедрение биорепарантов на основеконъюгированной ГК являются стратегически перспективным направлением, требующим дальнейших рандомизированных исследований для формализации протоколов и оценки отдаленных результатов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare that there is no conflict of interest.
Информация об авторах
Information about the authors
Михайлова Наталья Павловна – канд. мед. наук., ст. науч. сотр., АНО «Международный научно-исследовательский центр инновационных технологий Мартинекс». Е-mail: mikhailova@martinex.ru; ORCID: 0009-0005-4494-0170
Natalia P. Mikhaylova – Cand. Sci. (Med.), Senior Res. Officer, Martinex International Research Center for Innovative Technologies. Е-mail: mikhailova@martinex.ru; ORCID: 0009-0005-4494-0170
Чазова Ольга Алексеевна — глав. врач многопрофильного медицинского центра «ЧАО»; аспирант каф. акушерства и гинекологии ФГБОУ ВО «ПГМУ им. академика Е.А. Вагнера» Минздрава России. E-mail: olyachazova@yandex.ru; ORCID: 0009-0001-0183-095X
Olga A. Chazova – Head Physician, Multidisciplinary Medical Center "CHAO"; Postgraduate student, Perm State Medical University named after Academician E.A. Wagner (PSMU). E-mail: olyachazova@yandex.ru; ORCID: 0009-0001-0183-095X
Знатдинов Дамир Ильдусович – науч. сотр., АНО «Международный научно-исследовательский центр инновационных технологий Мартинекс». E-mail: znatdinov@martinex.ru; ORCID: 0009-0001-3227-4415
Damir I. Znatdinov – Res. Officer, Martinex International Research Center for Innovative Technologies. E-mail: znatdinov@martinex.ru; ORCID: 0009-0001-3227-4415
Аветисян Донара Григоровна – глав. врач клиники эстетической медицины, гинекологии и косметологии «Донни клиник»; аспирант каф. акушерства и гинекологии, ФГАОУ ВО «РУДН им. Патриса Лумумбы». E-mail: Doc.donara@gmail.com; ORCID: 0009-0008-6561-8289
Donara G. Avetisyan – Head Physician, "Donni Clinic" of Aesthetic Medicine, Gynecology and Cosmetology; Postgraduate student, Patrice Lumumba People’s Friendship University of Russia (RUDN University).
E-mail: Doc.donara@gmail.com; ORCID: 0009-0008-6561-8289
Поступила в редакцию: 02.09.2025
Поступила после рецензирования: 08.09.2025
Принята к публикации: 11.09.2025
Received: 02.09.2025
Revised: 08.09.2025
Accepted: 11.09.2025
Список исп. литературыСкрыть список1. Graziottin A. Maintaining vulvar, vaginal and perineal health: Clinical considerations. Womens Health (Lond) 2024;20:17455057231223716. DOI: 10.1177/17455057231223716
2. Jindal A, Mysore V, Mysore JV. Cosmetic gynecology-An emerging field for the dermatologist. J Cosmet Dermatol 2023;22(1):111-8. DOI: 10.1111/ jocd.15484
3. Mohammad S, Joshi KS, Mohammad S, Acharya N. Aesthetic Gynaecology: What Women Want? Cureus 2023;15(8):e44251. DOI: 10.7759/cureus.44251
4. Skwirczyńska E, Piotrowiak M, Ostrowski M et al. Welfare and Self-Assessment in Patients after Aesthetic and Reconstructive Treatments. Int J Environ Res Public Health 2022;19(18):11238. DOI: 10.3390/ ijerph191811238
5. Karam J, Singer BJ, Miwa H et al. Molecular weight of hyaluronic acid crosslinked into biomaterial scaffolds affects angiogenic potential. Acta Biomater 2023;169:228-42. DOI: 10.1016/j.actbio.2023.08.001
6. Abatangelo G, Vindigni V, Avruscio G et al. Hyaluronic Acid: Redefining Its Role. Cells 2020;9(7):1743. DOI: 10.3390/cells9071743
7. Ye H, Zhang R, Zhang C et al. Advances in hyaluronic acid: Bioactivity, complexed biomaterials and biological application: A review. Asian J Surg 2024. Published online August 30, 2024. DOI: 10.1016/j.asjsur. 2024.08.100
8. Iaconisi GN, Lunetti P, Gallo N et al. Hyaluronic Acid: A Powerful Biomolecule with Wide-Ranging Applications-A Comprehensive Review. Int J Mol Sci 2023;24(12):10296. DOI: 10.3390/ijms241210296. PMID: 37373443; PMCID: PMC10299688.
9. Соколова А.В., Аполихина И.А. Гиалуроновая кислота: перспективы использования в гинекологии. Доктор.Ру. 2021;20(8):36-40. DOI: 10.31550/1727-2378-2021-20-8-36-40
Sokolova A.V., Apolikhina I.A. Hyaluronic Acid: Prospective Use in Gynaecology. Doctor.Ru. 2021;20(8):36-40. DOI: 10.31550/1727-2378-2021-20-8-36-40 (in Russian).
10. Marinho A, Nunes C, Reis S. Hyaluronic Acid: A Key Ingredient in the Therapy of Inflammation. Biomolecules 2021;11(10):1518. DOI: 10.3390/biom11101518. PMID: 34680150; PMCID: PMC8533685.
11. Wu Y, Zhao S, Wang J et al. Methods for determining the structure and physicochemical properties of hyaluronic acid and its derivatives: A review. Int J Biol Macromol 2024;282(Pt 6):137603. DOI: 10.1016/ j.ijbiomac.2024.137603
12. Tarabini F, Rozemberg L, Zapata-Sudo G, Braz A. A Novel Hyaluronic Acid Filling Technique for Restoring Volume of the Labia Majora. Cureus 2023;15(9):e45728. DOI: 10.7759/cureus.45728
13. Тетерина Т.А., Аполихина И.А., Казакова С.Н., Михайлова Н.П. Современные возможности интимной контурной пластики у женщин репродуктивного и перименопаузального возраста. Акушерство и гинекология. 2024;10:173-82. DOI: 10.18565/aig.2024.247
Teterina T.A., Apolikhina I.A., Kazakova S.N., Mikhaylova N.P. Modern possibilities for intimate contour correction in reproductive-aged and perimenopausal women. Obstetrics and Gynecology. 2024;(10):139149. DOI: 10.18565/aig.2024.247 (in Russian).
14. Greene JJ, Sidle DM. The Hyaluronic Acid Fillers: Current Understanding of the Tissue Device Interface. Facial Plast Surg Clin North Am 2015;23(4):423-32. DOI: 10.1016/j.fsc.2015.07.002
15. Kolczewski P, Parafiniuk M, Zawodny P et al. Hyaluronic Acid and Radiofrequency in Patients with Urogenital Atrophy and Vaginal Laxity. Pharmaceuticals (Basel) 2022;15(12):1571. DOI: 10.3390/ph15121571
16. Kolczewski P, Kozłowski M, Cymbaluk-Płoska A. Micro-Focused Ultrasound Therapy in Patients with Urogenital Atrophy and Vaginal Laxity. J Clin Med 2022;11(23):6980. DOI: 10.3390/jcm11236980. PMID: 36498554; PMCID: PMC9739894.
17. Mishra VV, Solanki SB, Mishra NV, Alinsod RM. Transcutaneous Temperature Controlled Radiofrequency: Groundbreaking Technology - Female Stress Urinary Incontinence and Overactive Bladder Can Be Treated Noninvasively and with Vulvovaginal Rejuvenation? J Midlife Health 2023;14(2):69-72. DOI: 10.4103/jmh.jmh_19_23. PMID: 38029027;
PMCID: PMC10664049.
18. Solanki SB, Mishra V, Mishra N et al. Transcutaneous Temperature-controlled Radiofrequency for Vaginal Rejuvenation. J Midlife Health 2024;15(4):250-57. DOI: 10.4103/jmh.jmh_32_24. PMID: 39959723; PMCID: PMC11824938.
19. Yi J, Hong T, Zeng H et al. A Meta-analysis-Based Assessment of Intense Pulsed Light for Treatment of Melasma. Aesthetic Plast Surg 2020;44(3):947-52. DOI: 10.1007/s00266-020-01637-x
20. Сапон А.М., Гутоп Е.О., Ахмедбаева И.А. и др. Рандомизированое исследование эффективности и безопасности сочетанного применения дермальных имплантатов на основе гиалуроновой кислоты, технологии IPL и неаблятивной лазерной фракционной шлифовки для коррекции возрастных изменений. Клиническая дерматология и венерология. 2025;24(1):94-101. DOI: 10.17116/klinderma20252401194
Sapon A.M., Gutop E.O., Akhmedbaeva I.A. et al. Randomized study of efficacy and safety of combined application of hyaluronic acid-based dermal implants, IPL technology and non-ablative laser fractional resurfacing for age-related changes correction. Russian Journal of Clinical Dermatology and Venereology. 2025;24(1):94-101. DOI: 10.17116/klinderma20252 401194 (in Russian).
21. Romanelli M. Unique combination of hyaluronic acid and amino acids in the management of patients with a range of moderate-to-severe chronic wounds: Evidence from international clinical trials. Int Wound J 2024;21(Suppl 1):4-8. DOI: 10.1111/iwj.14617. PMID: 38392947; PMCID: PMC10886430.
22. Scarano A, Qorri E, Sbarbati A et al. The efficacy of hyaluronic acid fragments with amino acid in combating facial skin aging: an ultrasound and histological study. J Ultrasound 2024;27(3):689-97. DOI: 10.1007/s40477-024-00925-5. PMID: 38913131; PMCID: PMC11333785.
23. Bogdanowicz P, Bensadoun P, Noizet M et al. Senomorphic activity of a combination of niacinamide and hyaluronic acid: correlation with clinical improvement of skin aging. Sci Rep 2024;14(1):16321. DOI: 10.1038/s41598-024-66624-7. PMID: 39009698; PMCID: PMC11251187.
24. Petit N, Chang YJ, Lobianco FA et al. Hyaluronic acid as a versatile building block for the development of biofunctional hydrogels: In vitro models and preclinical innovations. Mater Today Bio 2025;31:101596. DOI: 10.1016/j.mtbio.2025.101596
25. Grabowski M, Gmyrek D, Żurawska M, Trusek A. Hyaluronic Acid: Production Strategies, Gel-Forming Properties, and Advances in Drug Delivery Systems. Gels 2025;11(6):424. DOI: 10.3390/gels11060424
26. Di Mola A, Landi MR, Massa A et al. Hyaluronic Acid in Biomedical Fields: New Trends from Chemistry to Biomaterial Applications. Int J Mol Sci 2022;23(22):14372. DOI: 10.3390/ijms232214372. PMID: 36430855; PMCID: PMC9695447.
27. Khabarov VN, Mikhailova NP. Hyaluronic acid. Application in cosmetology and medicine. LAP LAMBERT Academic Publishing, 2012.
28. Zaboronok A, Yamamoto T, Nakai K et al. Hyaluronic acid as a potential boron carrier for BNCT: Preliminary evaluation. Appl Radiat Isot 2015;106:181-4. DOI: 10.1016/j.apradiso.2015.08.020
29. Dalla Pietà A, Genova B, Penna A et al. On the adjuvanticity of hyaluronan: The case of a SARS-CoV-2 vaccine. J Control Release 2025;382:113674. DOI: 10.1016/j.jconrel.2025.113674
30. Weng X, Maxwell-Warburton S, Hasib A et al. The membrane receptor CD44: novel insights into metabolism. Trends Endocrinol Metab 2022;33(5):318-32. DOI: 10.1016/j.tem.2022.02.002
31. Kotla NG, Bonam SR, Rasala S et al. Recent advances and prospects of hyaluronan as a multifunctional therapeutic system. J Control Release 2021;336:598-620. DOI: 10.1016/j.jconrel.2021.07.002
32. Fu CP, Cai XY, Chen SL et al. Hyaluronic Acid-Based Nanocarriers for Anticancer Drug Delivery. Polymers (Basel) 2023;15(10):2317. DOI: 10.3390/polym15102317
33. Salathia S, Gigliobianco MR, Casadidio C et al. Hyaluronic Acid-Based Nanosystems for CD44 Mediated Anti-Inflammatory and Antinociceptive Activity. Int J Mol Sci 2023;24(8):7286. DOI: 10.3390/ijms24087286
34. Saravanakumar K, Park S, Santosh SS et al. Application of hyaluronic acid in tissue engineering, regenerative medicine, and nanomedicine: A review. Int J Biol Macromol 2022;222(Pt B):2744-2760. DOI: 10.1016/j.ijbiomac. 2022.10.055
35. Михайлова Н.П., Знатдинов Д.И., Борзова И.В., Селянин М.А. Витамин С в модуляции старения кожи: молекулярные механизмы и инновационные стратегии доставки. Успехи геронтологии. 2025;38(3):427-34. DOI: 10.34922/AE.2025.38.3.015
Mikhailova N.P., Znatdinov D.I., Borzova I.V., Selyanin M.A. Vitamin C in the modulation of skin aging: molecular mechanisms and innovative delivery strategies. The successes of gerontology. 2025;38(3):427-34. DOI: 10.34922/AE.2025.38.3.015 (in Russian).
36. Leylek O, Peker BH, Demircivi E, Peker H. Cannulated intravaginal injection technique (CIVIT) A Novel Vaginal Injection Technique. Sci Rep 2025;15(1):7651. Published 2025 Mar 5. DOI: 10.1038/s41598-025-91069-x


