Клинический разбор в общей медицине №10 2025
1 Smolensk State Medical University, Smolensk, Russia;
2 Clinical Emergency Hospital, Smolensk, Russia
billy_boss@mail.ru
Abstract
Numerous studies have shown that cardiovascular diseases of atherosclerotic genesis, including acute myocardial infarction, are closely associated with an osteoporosis and a low-energy fractures. A commonality of risk factors and pathogenesis of coronary heart disease and osteoporosis was revealed.
Aim. To examine the risk of osteoporosis and major pathological fractures in men with acute myocardial infarction.
Materials and methods. Patients with acute MI treated at the Emergency Cardiology Department of the Smolensk Clinical Emergency Hospital were assessed. Examination and treatment were prescribed in accordance with the standards established. All the patients were through the questionnaire survey conducted using a unified questionnaire for determination of the OP risk factors with the 10-year fracture risk assessment (FRAX score). The data obtained for each patient were inserted in the Excel spreadsheet; statistical analysis was conducted using the SPSS 20.0 software package.
Results. 53 men with acute myocardial infarction were examined, with an average age of 55.6±4.8 years. A direct correlation was found between coronary stenosis and total cholesterol level (correlation coefficient 0.39), low-density lipoprotein cholesterol level (correlation coefficient 0.35). A high risk of fracture was detected in 49.1% of patients, an average risk of 30.2% and a low risk of 20%. A significant difference in coronary stenosis was obtained between the group at high risk of osteoporosis and fractures and the group at low risk (p=0.02). Total cholesterol and low-density lipoprotein cholesterol in patients at high fracture risk were different from the low-risk group (p=0.011 and p=0.0007 respectively). A low probability of a 10-year probability of developing the main pathological fractures according to the FRAX-method was revealed. Also, the point of therapeutic intervention at which osteoporosis therapy should be initiated was not reached.
Conclusion. 49.1% of male patients under 65 years of age with acute myocardial infarction have a high risk of osteoporosis and major fractures. A reliable relationship was revealed between the risk of osteoporosis and atherogenesis processes. According to the obtained results, osteoporosis may be part of the cardiovascular continuum. Therapy with beta-blockers and lipid-lowering drugs can prevent the development and progression of osteoporosis.
Keywords: atherosclerosis, myocardial infarction, osteoporosis, spontaneous fractures.
For citation: Bazina I.B., Kozyrev O.A., Dekhnich N.A., Silkina Yu.A., Polonik A.S., Akaev D.I., Sinitskiy A.V., Pavlova M.V. Risk of osteoporosis in men with acute myocardial infarction. Clinical review for general practice. 2025; 6 (10): 88–92 (In Russ.). DOI: 10.47407/kr2025.6.10.00p4542
Введение
Сердечно-сосудистые заболевания являются одной из самых актуальных социально-экономических проблем современной медицины. Инфаркт миокарда (ИМ) – основная причина высокой смертности во всех странах мира, особенно среди трудоспособного населения [1]. Остеопороз (ОП) также занимает лидирующее место в структуре заболеваемости и смертности, является социально значимой патологией, связанной с переломами позвонков и периферических костей, инвалидностью, большими материальными затратами на лечение и реабилитацию пациентов [2]. Атеросклероз и ОП вначале могут протекать бессимптомно, поэтому не привлекают внимание врачей. Фатальными клиническими проявлениями выступают ИМ и проксимальные низкоэнергетические переломы (перелом шейки бедра).
В последние годы доказана взаимосвязь между ишемической болезнью сердца (ИБС) и ОП, выявлены общие патогенетические механизмы и факторы риска развития атеросклероза и резорбции костной ткани с потерей ее минеральной плотности независимо от возраста. По данным современной литературы, низкая минеральная плотность кости (МПК) является независимым фактором риска развития коронарного атеросклероза [3]. Единство механизмов ОП и атеросклероза заключается в том, что моноциты сосудистой стенки могут дифференцироваться в «пенистые клетки» с последующим развитием атеросклеротической бляшки или в остеокласты, которые способствуют резорбции костной ткани [4]. Зная взаимосвязь этих заболеваний, можно проводить одновременное их лечение и профилактику.
Цель исследования – изучить риск развития ОП и основных патологических переломов у мужчин с острым ИМ.
Материалы и методы
Обследованы пациенты с острым ИМ, находящиеся на лечении в отделении неотложной кардиологии ОГБУЗ «Клиническая больница скорой медицинской помощи» г. Смоленска. Все участники исследования подписали информированное добровольное согласие.
Обследование и лечение назначались в соответствии с установленными стандартами. Всем пациентам проводилась эхокардиография (ЭхоКГ) на аппарате AFFINITI 70 (Philips, Нидерланды), коронароангиография, ультразвуковое дуплексное сканирование брахиоцефальных артерий на аппарате AFFINITI 50 (Philips, Нидерланды). Биохимический анализ крови и липидограмма выполнены по стандартным методикам. Все пациенты были анкетированы с помощью унифицированного опросника [5] для определения факторов риска ОП, проведена оценка риска перелома по шкале FRAX [6]. Сердечно-сосудистый риск определяли с использованием шкал SCORЕ2 и SCORE2-OP. Полученные данные на каждого пациента внесены в таблицу Excel, и в последующем проведен статистический анализ с помощью программы SPSS 20.0. Проведено вычисление частот встречаемости признаков, 95% доверительных интервалов; определение средних значений (М) и стандартной ошибки среднего (m) для количественных признаков. Сравнение частот выполнено с помощью критерия χ2, сравнение количественных показателей – с помощью критерия Стьюдента для независимых выборок (в случае нормального распределения показателя).
Результаты
Обследованы 53 пациента мужского пола с острым ИМ в возрасте до 65 лет, средний возраст – 55,6±4,8 года. Индекс массы тела составил 28,5±3,7 кг/м2. Повторный ИМ наблюдался у 9 (16,9%) пациентов. Передний ИМ был у 31 пациента (58,5%), нижний – у 17 (32,0%), циркулярный – у 3 (5,7%), боковой – у 2 (3,8%). Сахарный диабет (СД) выявлен у 6 (11,3%) пациентов. Гиподинамию как фактор риска атеросклероза отметили 36 (67,9%) обследованных. Курили 35 (66%) пациентов. Артериальная гипертензия отмечалась у 100% пациентов, дислипидемия – у 47 (88,7%).
Определялись повышенный средний уровень общего холестерина (ОХС), холестерина липопротеинов низкой плотности (ХС ЛПНП), повышение коэффициента атерогенности, снижение скорости клубочковой фильтрации (СКФ) (табл. 1). Учитывая, что у всех исследуемых пациентов с ИМ отмечается очень высокий сердечно-сосудистый риск, целевой уровень ХС ЛПНП должен быть менее 1,4 ммоль/л [7].
 Несмотря на трудоспособный возраст наших пациентов (до 65 лет), средние показатели фракции выброса (ФВ) левого желудочка (ЛЖ) снижены до 48%, левое предсердие (ЛП) расширено до 4,5 см (табл. 2). Признаками артериальной гипертензии служат увеличение толщины межжелудочковой перегородки (ТМЖП), толщины задней стенки левого желудочка (ТЗСЛЖ) и толщины комплекса «интима–медиа» (ТКИМ).
Несмотря на трудоспособный возраст наших пациентов (до 65 лет), средние показатели фракции выброса (ФВ) левого желудочка (ЛЖ) снижены до 48%, левое предсердие (ЛП) расширено до 4,5 см (табл. 2). Признаками артериальной гипертензии служат увеличение толщины межжелудочковой перегородки (ТМЖП), толщины задней стенки левого желудочка (ТЗСЛЖ) и толщины комплекса «интима–медиа» (ТКИМ).
При проведении коронароангиографии преобладал правый тип кровоснабжения (n=38; 71,7%), левый тип был у 10 (18,9%) обследованных, сбалансированный тип – у 5 (9,4%). У 22 (41,5%) пациентов выявлен стеноз в бассейне левой коронарной артерии, у 20 (37,7%) – в бассейне правой коронарной артерии, у 11 (20,7%) пациентов выявлен стеноз коронарных артерий в обоих бассейнах. У 12 (22,6%) обследованных отмечалось сочетание стеноза и тромбоза коронарных артерий. Стеноз коронарных артерий составил 47,9±23,3%. У 26 (49,0%) пациентов выявлен коронарный стеноз более 50% просвета сосуда, что является гемодинамически значимым состоянием.
Выявлена прямая корреляционная зависимость между выраженностью коронарного стеноза и уровнем ОХС (коэффициент корреляции 0,39), а также уровнем ХС ЛПНП (коэффициент корреляции 0,35). ФВ ЛЖ имеет обратную корреляцию с уровнем ХС ЛПНП (коэффициент корреляции 0,34), уровнем триглицеридов (коэффициент корреляции 0,29) и прямую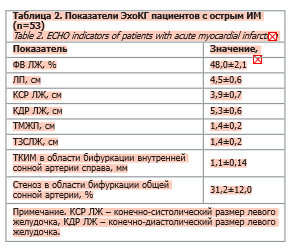 корреляцию с ХС ЛПВП (коэффициент корреляции 0,28).
корреляцию с ХС ЛПВП (коэффициент корреляции 0,28).
У пациентов с ИМ были исследованы факторы риска ОП по результатам анкетирования. Имеется общность факторов риска атеросклероза (например, гиподинамия, СД, курение) и ОП. Кроме того, недостаточное употребление молочной пищи отметили 20 (37,7%) обследованных, предшествующие переломы – 23 (43,4%), снижение СКФ <90 мл/мин выявлено у 51 пациента (96,2%). Снижение СКФ <60 мл/мин отмечено у 7 (13,2%) обследованных.
С учетом результатов анкетирования, высокий риск развития переломов выявлен у 26 (49,1%) пациентов, средний риск – у 16 (30,2%), низкий риск – у 11 (20,7%). У пациентов с высоким риском развития ОП коронарный стеноз составил 56,4±23,2%, со средним риском – 42,7±19,5%, с низким риском – 37,7±23,8%. Выявлены достоверные различия коронарного стенозирования между группой высокого риска развития ОП и группой низкого риска (p=0,02). Уровень ОХС у пациентов с высоким риском развития переломов (по данным анкетирования) составил 7,35±0,94 ммоль/л и достоверно отличался от группы с низким риском – 6,40±0,89 ммоль/л (p=0,011). ХС ЛПНП в группе высокого и низкого риска развития переломов также имел достоверные различия: 5,58±0,84 и 4,34±0,92 ммоль/л соответственно (p=0,0007).
Для выявления лиц с высокой вероятностью переломов, в том числе среди мужчин старше 50 лет, рекомендуется скрининг с использованием FRAX®-алгоритма. Всем пациентам с ИМ проводили персональную оценку вероятности развития основных патологических переломов в ближайшие 10 лет по результатам FRAX®-метода. Выявлена низкая 10-летняя вероятность развития основных патологических переломов – в среднем 6,0±2,9%, без данных о МПК. Только у 7 (13,2%) пациентов диагностирована средняя вероятность развития переломов – от 11 до 14%. Также не была достигнута точка терапевтического вмешательства, при которой следует начинать терапию ОП. Однако, по данным современной литературы, считается, что FRAX®-метод имеет ряд несовершенств. Так, не учитываются влияние вторичных причин на развитие ОП, наличие СД, дозы принимаемых глюкокортикоидов и других препаратов, а также многие другие факторы риска развития ОП [6].
Обсуждение
Проблема сердечно-сосудистых заболеваний, развития и профилактики острого ИМ имеет такое же важное значение, как и профилактика ОП. Эти заболевания объединяют такие факторы риска, как снижение СКФ, гиподинамия, курение, наличие СД, возраст старше 65 лет. Кроме того, костная ткань и сосуды имеют общие молекулярно-морфологические свойства. Кальцинаты сосудистой стенки по своему составу напоминают строение кости (соли кальция, остеонектин, остеокальцин). Интересно, что бета-блокаторы – основные антиангинальные и антигипертензивные препараты, которые активно используются при лечении ИМ, – могут угнетать активность остеокластов и тормозить развитие ОП [4]. В отличие от минерализации костей, сосудистая кальцификация является патологическим процессом, который формируется в результате появления в сосудистой стенке клеток с остеогенными свойствами. Это ведет к отложению кальция в интиме, появлению атероматозных бляшек с плотной покрышкой, увеличению жесткости сосудистой стенки [8, 9]. Эти процессы считаются независимым предиктором кардиоваскулярных событий [10].
У больных ИМ были выявлены такие важные факторы риска ОП, как недостаточное употребление молочной пищи (37,7%), предшествующие переломы после 50 лет (43,4%), снижение СКФ <90 мл/мин (96,2%), гиподинамия (67,9%), СД (11,3%). Мы установили, что, по данным анкетирования, высокий риск развития переломов имеют 49,1% пациентов с ИМ. Это требует проведения более тщательной диагностики ОП с использованием биохимических маркеров костной резорбции и костеобразования, денситометрии. В нашем исследовании показана взаимосвязь между коронарным стенозом и риском развития ОП и костных переломов. Так, при высоком риске переломов стеноз коронарных артерий составил 56,4±23,2%, при низком риске – 37,7±23,8% (p=0,02). Значения ОХС и ХС ЛПНП были достоверно выше при высоком риске развития переломов, чем при низком (p=0,011 и p=0,0007 соответственно). Это объясняется тем, что дислипидемия является одним из ведущих факторов риска кальцификации сосудистой стенки. Модифицированные ЛПНП подавляют дифференцировку остеобластов в ткани сосудов, понижают их активность, таким образом снижается МПК. ХС ЛПНП, приводя к атероматозу и стенозу сосудов, питающих кости и надкостницу, также снижают процессы остеогенеза [11, 12].
Известно, что ОП встречается у мужчин реже и в более позднем возрасте, чем у женщин, и в 40% случаев имеет вторичные причины. Диагностика ОП у мужчин старше 50 лет основывается не только на результатах денситометрии, но и на сведениях о перенесенных ранее низкоэнергетических переломах [13]. Более низкая частота ОП и переломов у мужчин по сравнению с женщинами объясняется особенностями строения костной ткани, менее интенсивными процессами костной резорбции (нет резкого снижения уровня половых гормонов), более развитой мышечной массой [14]. В нашем исследовании выявлена преимущественно низкая вероятность развития основных патологических переломов в ближайшие 10 лет по результатам FRAX®-метода (6,0%). Только 9,4% пациентов имели средний риск. Такое отличие от результатов анкетирования может быть связано с тем, что при использовании FRAX®-алгоритма не учитываются многие факторы риска ОП (доза глюкокортикоидов, количество сигарет и алкоголя, влияние СД2 на риск переломов), т.е. алгоритм имеет ограничения, требующие клинического суждения врача; при наличии у пациента множественных переломов риск последующих переломов будет занижен [6, 15].
Выводы
1. У 49,1% пациентов мужского пола в возрасте до 65 лет с острым ИМ доказан высокий риск развития ОП и основных патологических переломов.
2. Выявлена достоверная взаимосвязь между риском развития ОП и процессами атерогенеза: стенозом коронарных артерий, уровнем ОХС и ХС ЛПНП. ОП, наряду с дислипидемией и снижением СКФ, может входить в состав сердечно-сосудистого континуума.
3. У мужчин в возрасте до 65 лет для оценки риска развития низкоэнергетических переломов необходимо учитывать все факторы и вторичные причины формирования ОП. При выявлении высокого риска переломов необходимо исследование маркеров костеобразования и костной резорбции, проведение денситометрии для решения вопроса о назначении терапии ОП.
4. Терапия бета-блокаторами и гиполипидемическими препаратами может предупреждать развитие и прогрессирование ОП.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Базина Ирина Борисовна – канд. мед. наук, доц. каф. госпитальной терапии ФГБОУ ВО СГМУ. E-mail: billy_boss@mail.ru; ORCID 0000-0002-3886-8943
Irina B. Bazina – Cand. Sci. (Med.), Smolensk State Medical University. E-mail: billy_boss@mail.ru; ORCID 0000-0002-3886-8943
Козырев Олег Анатольевич – д-р мед. наук, проф., зав. каф. госпитальной терапии ФГБОУ ВО СГМУ. E-mail: oak02@yandex.ru; ORCID 0000-0001-9715-5532
Oleg A. Kozyrev – Dr. Sci. (Med.), Full Prof., Smolensk State Medical University. E-mail: oak02@yandex.ru; ORCID 0000-0001-9715-5532
Дехнич Наталья Николаевна – д-р мед. наук, проф. каф. факультетской терапии, проректор по дополнительному профессиональному образованию и развитию регионального здравоохранения ФГБОУ ВО СГМУ. E-mail: n.dekhnich@mail.ru; ORCID 0000-0002-6144-3919
Natalya N. Dekhnich – Dr. Sci. (Med.), Prof., Vice-Rector for Additional Professional Education and Development of Regional Health, Smolensk State Medical University. E-mail: n.dekhnich@mail.ru;
ORCID 0000-0002-6144-3919
Силкина Юлия Алексеевна – студентка 6-го курса ФГБОУ ВО СГМУ. E-mail: juliasolzzz@yandex.ru; ORCID 0009-0006-1485-9256
Yulia A. Silkina – 6th year Student, Smolensk State Medical University. E-mail: juliasolzzz@yandex.ru; ORCID 0009-0006-1485-9256
Полоник Алена Сергеевна – студентка 6-го курса ФГБОУ ВО СГМУ. E-mail: alien_poloniyaug@mail.ru; ORCID 0009-0005-1897-6698
Alena S. Polonik – 6th year Student, Smolensk State Medical University. E-mail: alien_poloniyaug@mail.ru; ORCID 0009-0005-1897-6698
Акаев Денис Игоревич – студент 6-го курса ФГБОУ ВО СГМУ. E-mail: denakaev4729@yandex.ru; ORCID 0000-0002-7065-1613
Denis I. Akaev – 6th year Student, Smolensk State Medical University. E-mail: denakaev4729@yandex.ru; ORCID 0000-0002-7065-1613
Синицкий Алексей Викторович – зав. отд-нием неотложной кардиологии № 2 ОГБУЗ «Клиническая больница скорой медицинской помощи». E-mail: Avs1991@mail.ru
Aleksey V. Sinitskiy – Head of the Emergency Cardiology Department No. 2, Clinical Emergency Hospital. E-mail: Avs1991@mail.ru
Павлова Марина Владимировна – ассистент каф. госпитальной терапии ФГБОУ ВО СГМУ. E-mail: wedmashka007@rambler.ru; ORCID 0009-0000-4485-1964
Marina V. Pavlova – Assistant, Smolensk State Medical University. E-mail: wedmashka007@rambler.ru; ORCID 0009-0000-4485-1964
Поступила в редакцию: 22.04.2025
Поступила после рецензирования: 11.05.2025
Принята к публикации: 05.06.2025
Received: 22.04.2025
Revised: 11.05.2025
Accepted: 05.06.2025
Клинический разбор в общей медицине №10 2025
Риск развития остеопороза у мужчин с острым инфарктом миокарда
Номера страниц в выпуске:88-92
Аннотация
Многочисленные исследования показали, что сердечно-сосудистые заболевания атеросклеротического генеза, в том числе острый инфаркт миокарда (ИМ), тесно связаны с остеопорозом (ОП) и низкоэнергетическими переломами. Выявлены общность факторов риска и патогенеза атеросклеротической болезни сердца и ОП.
Цель. Изучить риск развития ОП и основных патологических переломов у мужчин с острым ИМ.
Материалы и методы. Обследованы пациенты с острым ИМ, находящиеся на лечении в отделении неотложной кардиологии
ОГБУЗ «Клиническая больница скорой медицинской помощи» г. Смоленска. Обследование и лечение назначались в соответствии с установленными стандартами. Все пациенты были анкетированы с помощью унифицированного опросника для определения факторов риска ОП с оценкой 10-летнего риска перелома по шкале FRAX. Полученные данные на каждого пациента внесены в таблицу Excel, проведен статистический анализ с помощью программы SPSS 20.0.
Результаты. Обследованы 53 мужчины с острым ИМ (средний возраст – 55,6±4,8 года). Выявлена прямая корреляция между коронарным стенозом и уровнем общего холестерина (коэффициент корреляции 0,39), уровнем холестерина липопротеинов низкой плотности (коэффициент корреляции 0,35). Высокий риск развития переломов выявлен у 49,1% пациентов, средний риск – у 30,2%, низкий риск – у 20,0%. Получено достоверное отличие коронарного стенозирования между группой высокого риска развития ОП и группой низкого риска (p=0,02). Уровни общего холестерина и холестерина липопротеинов низкой плотности у пациентов с высоким риском переломов отличались от таковых в группе с низким риском (p=0,011 и p=0,0007 соответственно). Выявлена низкая 10-летняя вероятность развития основных патологических переломов по FRAX®-методу. Также не была достигнута точка терапевтического вмешательства, при которой следует начинать терапию ОП.
Выводы. У 49,1% пациентов мужского пола в возрасте до 65 лет с острым ИМ доказан высокий риск развития ОП и основных патологических переломов. Выявлена достоверная взаимосвязь между риском развития ОП и процессами атерогенеза. Учитывая полученные результаты, ОП может быть включен в состав сердечно-сосудистого континуума. Терапия бета-блокаторами и гиполипидемическими препаратами может предупреждать развитие и прогрессирование ОП.
Ключевые слова: атеросклероз, инфаркт миокарда, остеопороз, патологические переломы.
Для цитирования: Базина И.Б., Козырев О.А., Дехнич Н.Н., Силкина Ю.А., Полоник А.С., Акаев Д.И., Синицкий А.В., Павлова М.В. Риск развития остеопороза у мужчин с острым инфарктом миокарда. Клинический разбор в общей медицине. 2025; 6 (10): 88–92. DOI: 10.47407/kr2025.6.10.00p4542
Многочисленные исследования показали, что сердечно-сосудистые заболевания атеросклеротического генеза, в том числе острый инфаркт миокарда (ИМ), тесно связаны с остеопорозом (ОП) и низкоэнергетическими переломами. Выявлены общность факторов риска и патогенеза атеросклеротической болезни сердца и ОП.
Цель. Изучить риск развития ОП и основных патологических переломов у мужчин с острым ИМ.
Материалы и методы. Обследованы пациенты с острым ИМ, находящиеся на лечении в отделении неотложной кардиологии
ОГБУЗ «Клиническая больница скорой медицинской помощи» г. Смоленска. Обследование и лечение назначались в соответствии с установленными стандартами. Все пациенты были анкетированы с помощью унифицированного опросника для определения факторов риска ОП с оценкой 10-летнего риска перелома по шкале FRAX. Полученные данные на каждого пациента внесены в таблицу Excel, проведен статистический анализ с помощью программы SPSS 20.0.
Результаты. Обследованы 53 мужчины с острым ИМ (средний возраст – 55,6±4,8 года). Выявлена прямая корреляция между коронарным стенозом и уровнем общего холестерина (коэффициент корреляции 0,39), уровнем холестерина липопротеинов низкой плотности (коэффициент корреляции 0,35). Высокий риск развития переломов выявлен у 49,1% пациентов, средний риск – у 30,2%, низкий риск – у 20,0%. Получено достоверное отличие коронарного стенозирования между группой высокого риска развития ОП и группой низкого риска (p=0,02). Уровни общего холестерина и холестерина липопротеинов низкой плотности у пациентов с высоким риском переломов отличались от таковых в группе с низким риском (p=0,011 и p=0,0007 соответственно). Выявлена низкая 10-летняя вероятность развития основных патологических переломов по FRAX®-методу. Также не была достигнута точка терапевтического вмешательства, при которой следует начинать терапию ОП.
Выводы. У 49,1% пациентов мужского пола в возрасте до 65 лет с острым ИМ доказан высокий риск развития ОП и основных патологических переломов. Выявлена достоверная взаимосвязь между риском развития ОП и процессами атерогенеза. Учитывая полученные результаты, ОП может быть включен в состав сердечно-сосудистого континуума. Терапия бета-блокаторами и гиполипидемическими препаратами может предупреждать развитие и прогрессирование ОП.
Ключевые слова: атеросклероз, инфаркт миокарда, остеопороз, патологические переломы.
Для цитирования: Базина И.Б., Козырев О.А., Дехнич Н.Н., Силкина Ю.А., Полоник А.С., Акаев Д.И., Синицкий А.В., Павлова М.В. Риск развития остеопороза у мужчин с острым инфарктом миокарда. Клинический разбор в общей медицине. 2025; 6 (10): 88–92. DOI: 10.47407/kr2025.6.10.00p4542
Risk of osteoporosis in men with acute myocardial infarction
Irina B. Bazina1, Oleg A. Kozyrev1, Natalya N. Dekhnich1, Yulia A. Silkina1, Alena S. Polonik1, Denis I. Akaev1, Aleksey V. Sinitskiy2, Marina V. Pavlova11 Smolensk State Medical University, Smolensk, Russia;
2 Clinical Emergency Hospital, Smolensk, Russia
billy_boss@mail.ru
Abstract
Numerous studies have shown that cardiovascular diseases of atherosclerotic genesis, including acute myocardial infarction, are closely associated with an osteoporosis and a low-energy fractures. A commonality of risk factors and pathogenesis of coronary heart disease and osteoporosis was revealed.
Aim. To examine the risk of osteoporosis and major pathological fractures in men with acute myocardial infarction.
Materials and methods. Patients with acute MI treated at the Emergency Cardiology Department of the Smolensk Clinical Emergency Hospital were assessed. Examination and treatment were prescribed in accordance with the standards established. All the patients were through the questionnaire survey conducted using a unified questionnaire for determination of the OP risk factors with the 10-year fracture risk assessment (FRAX score). The data obtained for each patient were inserted in the Excel spreadsheet; statistical analysis was conducted using the SPSS 20.0 software package.
Results. 53 men with acute myocardial infarction were examined, with an average age of 55.6±4.8 years. A direct correlation was found between coronary stenosis and total cholesterol level (correlation coefficient 0.39), low-density lipoprotein cholesterol level (correlation coefficient 0.35). A high risk of fracture was detected in 49.1% of patients, an average risk of 30.2% and a low risk of 20%. A significant difference in coronary stenosis was obtained between the group at high risk of osteoporosis and fractures and the group at low risk (p=0.02). Total cholesterol and low-density lipoprotein cholesterol in patients at high fracture risk were different from the low-risk group (p=0.011 and p=0.0007 respectively). A low probability of a 10-year probability of developing the main pathological fractures according to the FRAX-method was revealed. Also, the point of therapeutic intervention at which osteoporosis therapy should be initiated was not reached.
Conclusion. 49.1% of male patients under 65 years of age with acute myocardial infarction have a high risk of osteoporosis and major fractures. A reliable relationship was revealed between the risk of osteoporosis and atherogenesis processes. According to the obtained results, osteoporosis may be part of the cardiovascular continuum. Therapy with beta-blockers and lipid-lowering drugs can prevent the development and progression of osteoporosis.
Keywords: atherosclerosis, myocardial infarction, osteoporosis, spontaneous fractures.
For citation: Bazina I.B., Kozyrev O.A., Dekhnich N.A., Silkina Yu.A., Polonik A.S., Akaev D.I., Sinitskiy A.V., Pavlova M.V. Risk of osteoporosis in men with acute myocardial infarction. Clinical review for general practice. 2025; 6 (10): 88–92 (In Russ.). DOI: 10.47407/kr2025.6.10.00p4542
Введение
Сердечно-сосудистые заболевания являются одной из самых актуальных социально-экономических проблем современной медицины. Инфаркт миокарда (ИМ) – основная причина высокой смертности во всех странах мира, особенно среди трудоспособного населения [1]. Остеопороз (ОП) также занимает лидирующее место в структуре заболеваемости и смертности, является социально значимой патологией, связанной с переломами позвонков и периферических костей, инвалидностью, большими материальными затратами на лечение и реабилитацию пациентов [2]. Атеросклероз и ОП вначале могут протекать бессимптомно, поэтому не привлекают внимание врачей. Фатальными клиническими проявлениями выступают ИМ и проксимальные низкоэнергетические переломы (перелом шейки бедра).
В последние годы доказана взаимосвязь между ишемической болезнью сердца (ИБС) и ОП, выявлены общие патогенетические механизмы и факторы риска развития атеросклероза и резорбции костной ткани с потерей ее минеральной плотности независимо от возраста. По данным современной литературы, низкая минеральная плотность кости (МПК) является независимым фактором риска развития коронарного атеросклероза [3]. Единство механизмов ОП и атеросклероза заключается в том, что моноциты сосудистой стенки могут дифференцироваться в «пенистые клетки» с последующим развитием атеросклеротической бляшки или в остеокласты, которые способствуют резорбции костной ткани [4]. Зная взаимосвязь этих заболеваний, можно проводить одновременное их лечение и профилактику.
Цель исследования – изучить риск развития ОП и основных патологических переломов у мужчин с острым ИМ.
Материалы и методы
Обследованы пациенты с острым ИМ, находящиеся на лечении в отделении неотложной кардиологии ОГБУЗ «Клиническая больница скорой медицинской помощи» г. Смоленска. Все участники исследования подписали информированное добровольное согласие.
Обследование и лечение назначались в соответствии с установленными стандартами. Всем пациентам проводилась эхокардиография (ЭхоКГ) на аппарате AFFINITI 70 (Philips, Нидерланды), коронароангиография, ультразвуковое дуплексное сканирование брахиоцефальных артерий на аппарате AFFINITI 50 (Philips, Нидерланды). Биохимический анализ крови и липидограмма выполнены по стандартным методикам. Все пациенты были анкетированы с помощью унифицированного опросника [5] для определения факторов риска ОП, проведена оценка риска перелома по шкале FRAX [6]. Сердечно-сосудистый риск определяли с использованием шкал SCORЕ2 и SCORE2-OP. Полученные данные на каждого пациента внесены в таблицу Excel, и в последующем проведен статистический анализ с помощью программы SPSS 20.0. Проведено вычисление частот встречаемости признаков, 95% доверительных интервалов; определение средних значений (М) и стандартной ошибки среднего (m) для количественных признаков. Сравнение частот выполнено с помощью критерия χ2, сравнение количественных показателей – с помощью критерия Стьюдента для независимых выборок (в случае нормального распределения показателя).
Результаты
Обследованы 53 пациента мужского пола с острым ИМ в возрасте до 65 лет, средний возраст – 55,6±4,8 года. Индекс массы тела составил 28,5±3,7 кг/м2. Повторный ИМ наблюдался у 9 (16,9%) пациентов. Передний ИМ был у 31 пациента (58,5%), нижний – у 17 (32,0%), циркулярный – у 3 (5,7%), боковой – у 2 (3,8%). Сахарный диабет (СД) выявлен у 6 (11,3%) пациентов. Гиподинамию как фактор риска атеросклероза отметили 36 (67,9%) обследованных. Курили 35 (66%) пациентов. Артериальная гипертензия отмечалась у 100% пациентов, дислипидемия – у 47 (88,7%).
Определялись повышенный средний уровень общего холестерина (ОХС), холестерина липопротеинов низкой плотности (ХС ЛПНП), повышение коэффициента атерогенности, снижение скорости клубочковой фильтрации (СКФ) (табл. 1). Учитывая, что у всех исследуемых пациентов с ИМ отмечается очень высокий сердечно-сосудистый риск, целевой уровень ХС ЛПНП должен быть менее 1,4 ммоль/л [7].
 Несмотря на трудоспособный возраст наших пациентов (до 65 лет), средние показатели фракции выброса (ФВ) левого желудочка (ЛЖ) снижены до 48%, левое предсердие (ЛП) расширено до 4,5 см (табл. 2). Признаками артериальной гипертензии служат увеличение толщины межжелудочковой перегородки (ТМЖП), толщины задней стенки левого желудочка (ТЗСЛЖ) и толщины комплекса «интима–медиа» (ТКИМ).
Несмотря на трудоспособный возраст наших пациентов (до 65 лет), средние показатели фракции выброса (ФВ) левого желудочка (ЛЖ) снижены до 48%, левое предсердие (ЛП) расширено до 4,5 см (табл. 2). Признаками артериальной гипертензии служат увеличение толщины межжелудочковой перегородки (ТМЖП), толщины задней стенки левого желудочка (ТЗСЛЖ) и толщины комплекса «интима–медиа» (ТКИМ).При проведении коронароангиографии преобладал правый тип кровоснабжения (n=38; 71,7%), левый тип был у 10 (18,9%) обследованных, сбалансированный тип – у 5 (9,4%). У 22 (41,5%) пациентов выявлен стеноз в бассейне левой коронарной артерии, у 20 (37,7%) – в бассейне правой коронарной артерии, у 11 (20,7%) пациентов выявлен стеноз коронарных артерий в обоих бассейнах. У 12 (22,6%) обследованных отмечалось сочетание стеноза и тромбоза коронарных артерий. Стеноз коронарных артерий составил 47,9±23,3%. У 26 (49,0%) пациентов выявлен коронарный стеноз более 50% просвета сосуда, что является гемодинамически значимым состоянием.
Выявлена прямая корреляционная зависимость между выраженностью коронарного стеноза и уровнем ОХС (коэффициент корреляции 0,39), а также уровнем ХС ЛПНП (коэффициент корреляции 0,35). ФВ ЛЖ имеет обратную корреляцию с уровнем ХС ЛПНП (коэффициент корреляции 0,34), уровнем триглицеридов (коэффициент корреляции 0,29) и прямую
 корреляцию с ХС ЛПВП (коэффициент корреляции 0,28).
корреляцию с ХС ЛПВП (коэффициент корреляции 0,28). У пациентов с ИМ были исследованы факторы риска ОП по результатам анкетирования. Имеется общность факторов риска атеросклероза (например, гиподинамия, СД, курение) и ОП. Кроме того, недостаточное употребление молочной пищи отметили 20 (37,7%) обследованных, предшествующие переломы – 23 (43,4%), снижение СКФ <90 мл/мин выявлено у 51 пациента (96,2%). Снижение СКФ <60 мл/мин отмечено у 7 (13,2%) обследованных.
С учетом результатов анкетирования, высокий риск развития переломов выявлен у 26 (49,1%) пациентов, средний риск – у 16 (30,2%), низкий риск – у 11 (20,7%). У пациентов с высоким риском развития ОП коронарный стеноз составил 56,4±23,2%, со средним риском – 42,7±19,5%, с низким риском – 37,7±23,8%. Выявлены достоверные различия коронарного стенозирования между группой высокого риска развития ОП и группой низкого риска (p=0,02). Уровень ОХС у пациентов с высоким риском развития переломов (по данным анкетирования) составил 7,35±0,94 ммоль/л и достоверно отличался от группы с низким риском – 6,40±0,89 ммоль/л (p=0,011). ХС ЛПНП в группе высокого и низкого риска развития переломов также имел достоверные различия: 5,58±0,84 и 4,34±0,92 ммоль/л соответственно (p=0,0007).
Для выявления лиц с высокой вероятностью переломов, в том числе среди мужчин старше 50 лет, рекомендуется скрининг с использованием FRAX®-алгоритма. Всем пациентам с ИМ проводили персональную оценку вероятности развития основных патологических переломов в ближайшие 10 лет по результатам FRAX®-метода. Выявлена низкая 10-летняя вероятность развития основных патологических переломов – в среднем 6,0±2,9%, без данных о МПК. Только у 7 (13,2%) пациентов диагностирована средняя вероятность развития переломов – от 11 до 14%. Также не была достигнута точка терапевтического вмешательства, при которой следует начинать терапию ОП. Однако, по данным современной литературы, считается, что FRAX®-метод имеет ряд несовершенств. Так, не учитываются влияние вторичных причин на развитие ОП, наличие СД, дозы принимаемых глюкокортикоидов и других препаратов, а также многие другие факторы риска развития ОП [6].
Обсуждение
Проблема сердечно-сосудистых заболеваний, развития и профилактики острого ИМ имеет такое же важное значение, как и профилактика ОП. Эти заболевания объединяют такие факторы риска, как снижение СКФ, гиподинамия, курение, наличие СД, возраст старше 65 лет. Кроме того, костная ткань и сосуды имеют общие молекулярно-морфологические свойства. Кальцинаты сосудистой стенки по своему составу напоминают строение кости (соли кальция, остеонектин, остеокальцин). Интересно, что бета-блокаторы – основные антиангинальные и антигипертензивные препараты, которые активно используются при лечении ИМ, – могут угнетать активность остеокластов и тормозить развитие ОП [4]. В отличие от минерализации костей, сосудистая кальцификация является патологическим процессом, который формируется в результате появления в сосудистой стенке клеток с остеогенными свойствами. Это ведет к отложению кальция в интиме, появлению атероматозных бляшек с плотной покрышкой, увеличению жесткости сосудистой стенки [8, 9]. Эти процессы считаются независимым предиктором кардиоваскулярных событий [10].
У больных ИМ были выявлены такие важные факторы риска ОП, как недостаточное употребление молочной пищи (37,7%), предшествующие переломы после 50 лет (43,4%), снижение СКФ <90 мл/мин (96,2%), гиподинамия (67,9%), СД (11,3%). Мы установили, что, по данным анкетирования, высокий риск развития переломов имеют 49,1% пациентов с ИМ. Это требует проведения более тщательной диагностики ОП с использованием биохимических маркеров костной резорбции и костеобразования, денситометрии. В нашем исследовании показана взаимосвязь между коронарным стенозом и риском развития ОП и костных переломов. Так, при высоком риске переломов стеноз коронарных артерий составил 56,4±23,2%, при низком риске – 37,7±23,8% (p=0,02). Значения ОХС и ХС ЛПНП были достоверно выше при высоком риске развития переломов, чем при низком (p=0,011 и p=0,0007 соответственно). Это объясняется тем, что дислипидемия является одним из ведущих факторов риска кальцификации сосудистой стенки. Модифицированные ЛПНП подавляют дифференцировку остеобластов в ткани сосудов, понижают их активность, таким образом снижается МПК. ХС ЛПНП, приводя к атероматозу и стенозу сосудов, питающих кости и надкостницу, также снижают процессы остеогенеза [11, 12].
Известно, что ОП встречается у мужчин реже и в более позднем возрасте, чем у женщин, и в 40% случаев имеет вторичные причины. Диагностика ОП у мужчин старше 50 лет основывается не только на результатах денситометрии, но и на сведениях о перенесенных ранее низкоэнергетических переломах [13]. Более низкая частота ОП и переломов у мужчин по сравнению с женщинами объясняется особенностями строения костной ткани, менее интенсивными процессами костной резорбции (нет резкого снижения уровня половых гормонов), более развитой мышечной массой [14]. В нашем исследовании выявлена преимущественно низкая вероятность развития основных патологических переломов в ближайшие 10 лет по результатам FRAX®-метода (6,0%). Только 9,4% пациентов имели средний риск. Такое отличие от результатов анкетирования может быть связано с тем, что при использовании FRAX®-алгоритма не учитываются многие факторы риска ОП (доза глюкокортикоидов, количество сигарет и алкоголя, влияние СД2 на риск переломов), т.е. алгоритм имеет ограничения, требующие клинического суждения врача; при наличии у пациента множественных переломов риск последующих переломов будет занижен [6, 15].
Выводы
1. У 49,1% пациентов мужского пола в возрасте до 65 лет с острым ИМ доказан высокий риск развития ОП и основных патологических переломов.
2. Выявлена достоверная взаимосвязь между риском развития ОП и процессами атерогенеза: стенозом коронарных артерий, уровнем ОХС и ХС ЛПНП. ОП, наряду с дислипидемией и снижением СКФ, может входить в состав сердечно-сосудистого континуума.
3. У мужчин в возрасте до 65 лет для оценки риска развития низкоэнергетических переломов необходимо учитывать все факторы и вторичные причины формирования ОП. При выявлении высокого риска переломов необходимо исследование маркеров костеобразования и костной резорбции, проведение денситометрии для решения вопроса о назначении терапии ОП.
4. Терапия бета-блокаторами и гиполипидемическими препаратами может предупреждать развитие и прогрессирование ОП.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах
Information about the authors
Базина Ирина Борисовна – канд. мед. наук, доц. каф. госпитальной терапии ФГБОУ ВО СГМУ. E-mail: billy_boss@mail.ru; ORCID 0000-0002-3886-8943
Irina B. Bazina – Cand. Sci. (Med.), Smolensk State Medical University. E-mail: billy_boss@mail.ru; ORCID 0000-0002-3886-8943
Козырев Олег Анатольевич – д-р мед. наук, проф., зав. каф. госпитальной терапии ФГБОУ ВО СГМУ. E-mail: oak02@yandex.ru; ORCID 0000-0001-9715-5532
Oleg A. Kozyrev – Dr. Sci. (Med.), Full Prof., Smolensk State Medical University. E-mail: oak02@yandex.ru; ORCID 0000-0001-9715-5532
Дехнич Наталья Николаевна – д-р мед. наук, проф. каф. факультетской терапии, проректор по дополнительному профессиональному образованию и развитию регионального здравоохранения ФГБОУ ВО СГМУ. E-mail: n.dekhnich@mail.ru; ORCID 0000-0002-6144-3919
Natalya N. Dekhnich – Dr. Sci. (Med.), Prof., Vice-Rector for Additional Professional Education and Development of Regional Health, Smolensk State Medical University. E-mail: n.dekhnich@mail.ru;
ORCID 0000-0002-6144-3919
Силкина Юлия Алексеевна – студентка 6-го курса ФГБОУ ВО СГМУ. E-mail: juliasolzzz@yandex.ru; ORCID 0009-0006-1485-9256
Yulia A. Silkina – 6th year Student, Smolensk State Medical University. E-mail: juliasolzzz@yandex.ru; ORCID 0009-0006-1485-9256
Полоник Алена Сергеевна – студентка 6-го курса ФГБОУ ВО СГМУ. E-mail: alien_poloniyaug@mail.ru; ORCID 0009-0005-1897-6698
Alena S. Polonik – 6th year Student, Smolensk State Medical University. E-mail: alien_poloniyaug@mail.ru; ORCID 0009-0005-1897-6698
Акаев Денис Игоревич – студент 6-го курса ФГБОУ ВО СГМУ. E-mail: denakaev4729@yandex.ru; ORCID 0000-0002-7065-1613
Denis I. Akaev – 6th year Student, Smolensk State Medical University. E-mail: denakaev4729@yandex.ru; ORCID 0000-0002-7065-1613
Синицкий Алексей Викторович – зав. отд-нием неотложной кардиологии № 2 ОГБУЗ «Клиническая больница скорой медицинской помощи». E-mail: Avs1991@mail.ru
Aleksey V. Sinitskiy – Head of the Emergency Cardiology Department No. 2, Clinical Emergency Hospital. E-mail: Avs1991@mail.ru
Павлова Марина Владимировна – ассистент каф. госпитальной терапии ФГБОУ ВО СГМУ. E-mail: wedmashka007@rambler.ru; ORCID 0009-0000-4485-1964
Marina V. Pavlova – Assistant, Smolensk State Medical University. E-mail: wedmashka007@rambler.ru; ORCID 0009-0000-4485-1964
Поступила в редакцию: 22.04.2025
Поступила после рецензирования: 11.05.2025
Принята к публикации: 05.06.2025
Received: 22.04.2025
Revised: 11.05.2025
Accepted: 05.06.2025
Список исп. литературыСкрыть список1. Бойцов С.А., Шахнович Р.М., Эрлих А.Д. и др. Регистр острого инфаркта миокарда. РЕГИОН–ИМ – Российский рЕГИстр Острого иНфаркта миокарда. Кардиология. 2021;61(6):41-51. DOI: 10.18087/cardio.2021.6.n1595
Boytsov S.A., Shakhnovich R.M., Erlikh A.D. et al. Registry of Acute Myocardial Infarction. REGION-MI – Russian Registry of Acute Myocardial Infarction. Kardiologia. 2021;61(6):41-51. DOI: 10.18087/cardio.2021.6.n1595 (in Russian).
2. Лесняк О.М., Торопцова Н.В., ред. Федеральные клинические рекомендации по диагностике и лечению остеопороза. М.: ГЭОТАР-Медиа; 2014. 25 с.
Lesnyak O.M., Toroptsova N.V., eds. Federal clinical recommendations for the diagnosis and treatment of osteoporosis. Moscow: GEOTAR-Media; 2014. 25 p. (in Russian).
3. Marcovitz PA, Tran HH, Franklin BA et al. Usefulness of bone mineral density to predict significant coronary artery disease. Am J Cardiol 2005;96(8):1059-63.
4. Федорченко И.Л., Небиеридзе Д.В., Сафарян А.С. и др. Сердечно-сосудистые заболевания и остеопороз: что общего? Терапевтический архив. 2014;86(5):116-9.
Fedorchenko I.L., Nebieridze D.V., Safarian A.S. et al. Cardiovascular diseases and osteoporosis: What is common? Therapeutic Archive. 2014;86(5):116-9 (in Russian).
5. Кукес В.Г., Аникин Г.С., Минина Е.С. Остеопороз в практике врача-терапевта: роль альфакальцидола. Справочник поликлинического врача. 2015;(3):47-51.
Kukes V.G., Anikin G.S., Minina E.S. Osteoporosis in the practice of a therapist: the role of alphacalcidol. Spravochnik poliklinicheskogo vracha. 2015;(3):47-51 (in Russian).
6. Белая Ж.Е., Белова К.Ю., Бирюкова Е.В. и др. Федеральные клинические рекомендации по диагностике и лечению остеопороза. Остеопороз и остеопатии. 2021;24(2):4-47. DOI: 10.14341/osteo12930
Belaya Zh.E., Belova K.Yu., Biryukova E.V. et al. Federal clinical guidelines for diagnosis, treatment and prevention of osteoporosis. Osteoporosis and Bone Diseases. 2021;24(2):4-47. DOI: 10.14341/osteo 12930 (in Russian).
7. Ежов М.В., Кухарчук В.В., Сергиенко И.В. и др. Нарушения липидного обмена. Клинические рекомендации. Российский кардиологический журнал. 2023;28(5):250-97. DOI: 10.15829/1560-4071-2023-5471
Ezhov M.V., Kukharchuk V.V., Sergienko I.V. et al. Disorders of lipid metabolism. Clinical Guidelines 2023. Russian Journal of Cardiology. 2023;28(5):250-97. DOI: 10.15829/1560-4071-2023-5471 (in Russian).
8. Angelovich TA, Hearps AC, Jaworowski A. Inflammation-induced foam cell formation in chronic inflammatory disease. Immunol Cell Biol 2015;93(7):683-93.
9. Buckley ML, Ramji DP. The influence of dysfunctional signaling and lipid homeostasis in mediating the inflammatory responses during atherosclerosis. Biochim Biophys Acta. 2015;1857(7):1498-510.
10. Kanwar SS, Stone GW, Singh M et al. Acute coronary syndromes without coronary plaque rupture. Nat Rev Cardiol 2016;13(5):257-65.
11. Parhamy F, Tintut Y, Beamer WG et al. Atherogenic high-fat diet reduces bone mineralization in mice. J Bone Miner Res 2001;16(2):182-8.
12. Parhamy F, Morrow FD, Balucan J et al. Lipid oxidation products have opposite effects on calcifying vascular cell and bone cell differentiation. A possible explanation for the paradox of arterial calcification in osteoporotic patients. Arterioscler Thromb Vasc Biol 1997;17(4):680-7.
13. Лесняк О.М., Беневоленская Л.И., ред. Остеопороз. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа; 2011. 272 с.
Lesnyak O.M., Benevolenskaya L.I., eds. Osteoporosis. 2nd ed., rev. and add. Moscow: GEOTAR-Media; 2011. 272 p. (in Russian).
14. Лесняк О.М. Актуальные вопросы диагностики и лечения остеопороза у мужчин в амбулаторной практике. Российский семейный врач. 2017;21(4):39-44. DOI: 10.17816/RFD2017139-44
Lesnyak O.M. Current issues of diagnosis and treatment of osteoporosis in men in general practice. Russian Family Doctor. 2017;21(4):39-44. DOI: 10.17816/RFD2017139-44 (in Russian).
15. Kanis JA, Johnell O, Oden A et al. FRAXô and the assessment of fracture probability in men and women from the UK. Osteoporos Int 2008;19(4):385-97.


