Клинический разбор в общей медицине №01 2026
Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University, Simferopol, Russia
bubley.99@mail.ru
Abstract
Uric acid is the end product of purine metabolism in humans. The concentration of uric acid can depend on many factors, for example: diet, alcohol consumption, gender, age, and concomitant pathologies. The level of uric acid is maintained at a level that allows it to have a maximum degree of solubility in blood plasma. Studies have shown that uric acid is a powerful antioxidant at physiological concentrations. At high intracellular concentrations, uric acid has been shown to act as a pro-oxidant molecule. During the study, we focused on the pro-oxidant properties of uric acid at its non-physiological concentrations in gout patients. According to previous studies, an increased concentration of uric acid can affect the tone of the vascular wall, thereby damaging the vascular wall and causing endothelial dysfunction during prolonged exposure. The study involved
40 patients with gout. The levels of endothelin-1 (ET1), nitric oxide synthase (NOS-3), VEGF-A and C-reactive protein were measured. A correlation analysis was performed, and the strongest and most statistically significant correlation (ρ=0.515; p=0.001) was found between uric acid and ET1. The level of endothelin 1 increases markedly with increasing uric acid. In order to identify the relationship between ET1 (the dependent variable) and uric acid, a multiple linear regression was constructed. In the final model, uric acid turned out to be a significant independent predictor of ET1 levels (β=0.162; p=0.002): an increase of 1 mmol/L is associated with an increase in ET1 of about 0.162 mmol/L.
Keywords: gout, hyperuricemia, endothelial dysfunction, metabolic syndrome, systemic inflammation, endothelin-1.
For citation: Bubley K.V., Beloglazov V.A., Yatskov I.A., Ageeva E.A. The effect of hyperuricemia on markers of endothelial dysfunction in patients with gout. Clinical review for general practice. 2026; 7 (1): 46–49 (In Russ.). DOI: 10.47407/kr2026.7.1.00752
Введение
Подагра представляет собой метаболическое нарушение, которое характеризуется хронической гиперурикемией и отложением кристаллов моноурата натрия в тканях и вызывает как локальный иммунный ответ, так и системное хроническое воспаление [1]. Гиперурикемия определяется как уровень мочевой кислоты в сыворотке крови >7 мг/дл (210–420 мкмоль/л) у мужчин и >6 мг/дл (150–350 мкмоль/л) у женщин [1]. Важно отметить, что не у всех пациентов с гиперурикемией развивается подагра, однако риск ее возникновения увеличивается с ростом концентрации мочевой кислоты [1].
По данным на 2020 г., 55,8 млн человек во всем мире страдали подагрой, при этом стандартизированная по возрасту распространенность составила 659,3 (525,4–822,3) на 100 тыс. населения, что на 22,5% (20,9–24,2%) выше, чем в 1990 г. [2, 3]. По оценкам, общее число распространенных случаев подагры достигнет к 2050 г. 95,8 млн (81,1–116 млн) [2, 3].
Некоторые исследования указывают, что более низкие пороговые значения мочевой кислоты относительно нормы могут быть значимы для оценки сердечно-сосудистого риска [4]. Гиперурикемия может быть результатом как повышенного образования мочевой кислоты, так и снижения ее выведения либо сочетания обоих факторов [5]. На уровень мочевой кислоты влияют диетические факторы (продукты, богатые пуринами, алкоголь, фруктоза) и сопутствующие заболевания (злокачественные новообразования, хроническая почечная недостаточность и др.) [1].
Сложное взаимодействие процессов образования и выведения мочевой кислоты, подверженное влиянию образа жизни и генетических факторов, предполагает, что воздействие гиперурикемии может существенно различаться у пациентов с подагрой в зависимости от индивидуальных особенностей метаболизма [6]. Например, если гиперурикемия у одного пациента в основном обусловлена избыточным образованием мочевой кислоты, а у другого – нарушением ее выведения, то последующие эффекты на эндотелиальные маркеры могут различаться из-за разных уровней сопутствующих биологически активных веществ или компенсаторных механизмов.
Гиперурикемия, как в качестве самостоятельного фактора, так и совместно с системным воспалением, может повышать сердечно-сосудистый риск и провоцировать эндотелиальную дисфункцию через генерацию активных форм кислорода (ROS) и последующее повреждение эндотелия и на сегодняшний день может рассматриваться как одно из проявлений метаболического синдрома [1, 7]. Повышение уровня мочевой кислоты наблюдается у пациентов при гипертонии, неалкогольной жировой болезни печени, хронической болезни почек и сердечно-сосудистых заболеваниях [2]. Постоянное присутствие высокого уровня мочевой кислоты в крови может прямо или косвенно воздействовать на эндотелиальные клетки даже при отсутствии отложения кристаллов в сосудах, что выражается в феномене, известном как «сосудистая подагра» [8]. Вместе с тем взаимосвязь уровня мочевой кислоты у больных подагрой с маркерами эндотелиальной дисфункции до сегодняшнего дня остается малоизученным.
Цель исследования – оценить влияние концентрации мочевой кислоты на уровни вазоактивных маркеров (ET1, VEGF-A, NOS-3) у пациентов с подагрой вне обострения.
Материалы и методы
В исследовании приняли участие 38 пациентов (23 мужчины и 15 женщин, средний возраст – 47±8 лет) с подтвержденным диагнозом подагры вне обострения. По уровню в крови мочевой кислоты больные были распределены на две группы: 1-я группа – 26 человек, уровень мочевой кислоты >360 мкмоль/л; 2-я группа – 12 человек, уровень мочевой кислоты <360 мкмоль/л.
В качестве маркера активности воспаления использовался уровень С-реактивного белка (СРБ) в плазме крови.
Уровни СРБ, эндотелина-1 (ET1), NOS-3, VEGF-A в плазме крови измеряли с помощью иммуноферментного анализа с применением наборов производства Cloud Clone Corp. (Хубей, Китай), а концентрацию мочевой кислоты в сыворотке определяли колориметрическим методом с использованием автоматического анализатора.
Критериями исключения пациентов из исследования были: отказ пациента, системные заболевания соединительной ткани, беременность, онкологические заболевания, первичная гиперурикемия.
Статистический анализ проводился с помощью программного обеспечения IBM SPSS Statistics 28. Тип распределения параметров в вариационном ряду устанавливали по критерию Шапиро–Уилка. Значимость различий между несвязанными выборками определяли при помощи непараметрических критериев для независимых выборок (U-критерий Манна–Уитни). Корреляционный анализ проводился с использованием метода ранговой корреляции Спирмена. Построена линейная регрессионная модель.
Результаты
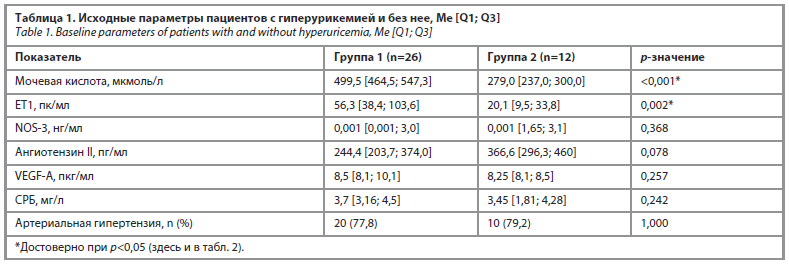
Как следует из данных, приведенных в табл. 1, статистически значимые различия между клиническими группами зарегистрированы только для ET1 и мочевой кислоты. При анализе маркеров эндотелиальной дисфункции выявлено достоверное повышение уровня ET1 у группы с гиперурикемией по сравнению с группой с нормальным уровнем мочевой кислоты (p<0,001), что может свидетельствовать о нарушении вазорегуляторной функции эндотелия и смещении состояния сосудистой стенки в сторону вазоконстрикции.
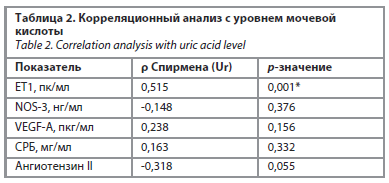
Проведенный корреляционный анализ (табл. 2) показал, что наиболее сильная и статистически значимая корреляция (ρ=0,515; p=0,001) обнаружена между мочевой кислотой и ET1. Остальные рассматриваемые параметры (NOS-3, VEGF-A, СРБ, ангиотензин II) не продемонстрировали статистически значимых корреляций с мочевой кислотой.
Таким образом, уровень мочевой кислоты положительно связан только с уровнем ET1, который, как известно, обладает вазоконстрикторными свойствами и не влияет на другие маркеры. Отсутствие влияния концентрации мочевой кислоты в крови на уровень NO-синтетазы (NOS-3) свидетельствует о том, что что гиперурикемия сдвигает баланс в сторону вазоконстрикции.
Построена множественная линейная регрессия уровня ET1 (зависимая переменная) от мочевой кислоты. В итоговой модели значимым независимым предиктором уровня ET1 оказалась мочевая кислота (β=0,162; p=0,002): повышение на 1 мкмоль/л связано с ростом ET1 примерно на 0,162 мкмоль/л. Полученная модель объясняет 24,2% дисперсии.
Результаты регрессионного анализа подтверждают значимую положительную связь между уровнем мочевой кислоты и концентрацией ET1.
Обсуждение
Результаты исследования демонстрируют значимую связь между повышенной концентрацией мочевой кислоты и увеличением содержания ET1 в плазме крови у пациентов с подагрой вне обострения. Полученные данные подтверждают концепцию, согласно которой гиперурикемия способствует развитию эндотелиальной дисфункции за счет смещения баланса между вазодилатирующими и вазоконстрикторными эффектами в сторону сужения сосудов. Механизмы данного взаимодействия могут включать повышение продукции реактивных форм кислорода (ROS) и последующего гиперокисления как внутриклеточной, так и внеклеточной среды, что приводит к снижению биодоступности окиси азота (NO) и продукции ET1 в эндотелиальных клетках [6, 9–11]. Совокупность множественных механизмов, посредством которых гиперурикемия подавляет продукцию NO, подчеркивает критическую роль этого пути в развитии эндотелиальной дисфункции, связанной с гиперурикемией. Например, увеличение продукции ксантиноксидазой активных форм кислорода, которые реагируют с NO, дополнительно снижает доступность NO [12]. Также при повышении активности аргиназы она конкурирует с eNOS за субстрат L-аргинин, что в свою очередь дополнительно снижает содержание NO посредством активации сигнального пути протеинкиназы С, приводя к фосфорилированию NOS-3 в ингибирующих сайтах [13, 14].
Наше исследование дополняет существующие данные о роли мочевой кислоты как прооксидантного агента, подчерчивая, что даже при отсутствии клинически выраженного воспаления и вне зависимости от наличия сопутствующего повреждающего фактора эндотелия (артериальная гипертензия) гиперурикемия способна вызвать повреждение эндотелия через гиперпродукцию ET1, а впоследствии – длительную вазоконстрикцию [15].
Отсутствие значимых изменений уровней NOS-3, VEGF-A и ангиотензина II указывает на избирательное влияние гиперурикемии на эндотелиальный баланс: повышение уровня ET1 не сопровождается компенсаторным повышением содержания NO-синтетазы или васкулогенеза, что может свидетельствовать о подавлении механизма защитной вазодилатации при хронической гиперурикемии. Эти результаты частично расходятся с данными некоторых исследований, где гиперурикемия ассоциировалась со снижением экспрессии NOS-3 и повышением маркеров вазодилатации. Вероятно, различия объясняются гетерогенностью когорты по сопутствующим метаболическим факторам и методическим особенностям определения маркеров [16, 17].
Множественная линейная регрессия показала, что мочевая кислота является независимым предиктором уровня ET1 (β=0,162; p=0,002), объясняя около 24,2% дисперсии показателя ET1. Это подчеркивает вклад гиперурикемии в патогенез эндотелиальной дисфункции и актуализирует необходимость контроля уровня мочевой кислоты для профилактики не только подагрических артритов, но и сердечно-сосудистых осложнений.
Заключение
Результаты исследования свидетельствуют о необходимости ранней диагностики и целенаправленной коррекции гиперурикемии у пациентов с подагрой вне обострения. Использование ингибиторов ксантиноксидазы может способствовать снижению уровня ET1 и уменьшению риска развития артериальной гипертензии и других сосудистых осложнений [18, 19].
Гиперурикемия у пациентов с подагрой является значимым фактором развития эндотелиальной дисфункции, главным образом через механизмы, включающие снижение биодоступности NO и, возможно, повышение уровня ET1. Влияние на VEGF-A представляется более сложным и требует дальнейшего изучения, что подтверждается изменением ключевых маркеров (ET1, NOS-3, VEGF-A). Полученные данные подчеркивают необходимость контроля уровня мочевой кислоты не только для профилактики подагрических атак, но и для снижения сердечно-сосудистого риска.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация о спонсорстве. Исследование не имело спонсорской поддержки.
Information about sponsorship. The study had no sponsorship.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Бублей Константин Викторович – ассистент каф. внутренней медицины №2 Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского». E-mail: bubley.99@mail.ru
Konstantin V. Bubley – аssistant, Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University.
E-mail: bubley.99@mail.ru
Белоглазов Владимир Алексеевич – д-р мед. наук, проф., зав. каф. внутренней медицины №2 Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского»
Vladimir A. Beloglazov – Dr. Sci. (Med.), Prof., Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University
Яцков Игорь Анатольевич – канд. мед. наук, доц. каф. внутренней медицины №2 Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского»
Igor A. Yatskov – Cand. Sci. (Med.), Assoc. Prof., Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University
Агеева Елизавета Сергеевна – д-р мед. наук, доц., зав. каф. медицинской биологии Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского»
Elizaveta S. Ageeva – Dr. Sci. (Med.), Assoc. Prof., Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University
Поступила в редакцию: 07.07.2025
Поступила после рецензирования: 31.07.2025
Принята к публикации: 14.08.2025
Received: 07.07.2025
Revised: 31.07.2025
Accepted: 14.08.2025
Клинический разбор в общей медицине №01 2026
Влияние гиперурикемии на маркеры эндотелиальной дисфункции у пациентов с подагрой
Номера страниц в выпуске:46-49
Аннотация
Мочевая кислота является конечным продуктом пуринового обмена у человека. Концентрация мочевой кислоты может зависеть от множества факторов, таких как диета, употребление алкоголя, пол, возраст и сопутствующие патологии. Уровень мочевой кислоты поддерживается на уровне, позволяющем ей иметь максимальную степень растворимости в плазме крови. В исследованиях было показано, что при физиологических концентрациях мочевая кислота является мощным антиоксидантом. При высокой внутриклеточной концентрации мочевая кислота, как было показано, действует как прооксидантная молекула. При проведении исследования мы сосредоточились на прооксидантных свойствах мочевой кислоты при ее нефизиологических концентрациях у пациентов с подагрой. По данным ранее проведенных исследований, повышенная концентрация мочевой кислоты способна воздействовать на тонус сосудистой стенки, при длительном воздействии повреждая сосудистую стенку и вызывая эндотелиальную дисфункцию. В исследовании приняли участие
40 пациентов с подагрой. Были измерены уровни эндотелина-1 (ET1), синтазы оксида азота (NOS-3), VEGF-A и С-реактивного белка. Проведен корреляционный анализ, наиболее сильная и статистически значимая корреляция (ρ=0,515; p=0,001) обнаружена между мочевой кислотой и ET1. Уровень ET1 заметно растет с увеличением концентрации мочевой кислоты. С целью выявления зависимости между ET1 (зависимая переменная) и мочевой кислотой была построена множественная линейная регрессия. В итоговой модели значимым независимым предиктором уровня ET1 оказалась мочевая кислота (β=0,162; p=0,002): повышение на 1 мкмоль/л связано с ростом ET1 примерно на 0,162 мкмоль/л.
Ключевые слова: подагра, гиперурикемия, эндотелиальная дисфункция, метаболический синдром, системное воспаление, эндотелин-1.
Для цитирования: Бублей К.В., Белоглазов В.А., Агеева Е.С., Яцков И.А. Влияние гиперурикемии на маркеры эндотелиальной дисфункции у пациентов с подагрой. Клинический разбор в общей медицине. 2026; 7 (1): 46–49. DOI: 10.47407/kr2026.7.1.00752
Мочевая кислота является конечным продуктом пуринового обмена у человека. Концентрация мочевой кислоты может зависеть от множества факторов, таких как диета, употребление алкоголя, пол, возраст и сопутствующие патологии. Уровень мочевой кислоты поддерживается на уровне, позволяющем ей иметь максимальную степень растворимости в плазме крови. В исследованиях было показано, что при физиологических концентрациях мочевая кислота является мощным антиоксидантом. При высокой внутриклеточной концентрации мочевая кислота, как было показано, действует как прооксидантная молекула. При проведении исследования мы сосредоточились на прооксидантных свойствах мочевой кислоты при ее нефизиологических концентрациях у пациентов с подагрой. По данным ранее проведенных исследований, повышенная концентрация мочевой кислоты способна воздействовать на тонус сосудистой стенки, при длительном воздействии повреждая сосудистую стенку и вызывая эндотелиальную дисфункцию. В исследовании приняли участие
40 пациентов с подагрой. Были измерены уровни эндотелина-1 (ET1), синтазы оксида азота (NOS-3), VEGF-A и С-реактивного белка. Проведен корреляционный анализ, наиболее сильная и статистически значимая корреляция (ρ=0,515; p=0,001) обнаружена между мочевой кислотой и ET1. Уровень ET1 заметно растет с увеличением концентрации мочевой кислоты. С целью выявления зависимости между ET1 (зависимая переменная) и мочевой кислотой была построена множественная линейная регрессия. В итоговой модели значимым независимым предиктором уровня ET1 оказалась мочевая кислота (β=0,162; p=0,002): повышение на 1 мкмоль/л связано с ростом ET1 примерно на 0,162 мкмоль/л.
Ключевые слова: подагра, гиперурикемия, эндотелиальная дисфункция, метаболический синдром, системное воспаление, эндотелин-1.
Для цитирования: Бублей К.В., Белоглазов В.А., Агеева Е.С., Яцков И.А. Влияние гиперурикемии на маркеры эндотелиальной дисфункции у пациентов с подагрой. Клинический разбор в общей медицине. 2026; 7 (1): 46–49. DOI: 10.47407/kr2026.7.1.00752
The effect of hyperuricemia on markers of endothelial dysfunction in patients with gout
Konstantin V. Bubley, Vladimir A. Beloglazov, Igor A. Yatskov, Elizaveta S. AgeevaGeorgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University, Simferopol, Russia
bubley.99@mail.ru
Abstract
Uric acid is the end product of purine metabolism in humans. The concentration of uric acid can depend on many factors, for example: diet, alcohol consumption, gender, age, and concomitant pathologies. The level of uric acid is maintained at a level that allows it to have a maximum degree of solubility in blood plasma. Studies have shown that uric acid is a powerful antioxidant at physiological concentrations. At high intracellular concentrations, uric acid has been shown to act as a pro-oxidant molecule. During the study, we focused on the pro-oxidant properties of uric acid at its non-physiological concentrations in gout patients. According to previous studies, an increased concentration of uric acid can affect the tone of the vascular wall, thereby damaging the vascular wall and causing endothelial dysfunction during prolonged exposure. The study involved
40 patients with gout. The levels of endothelin-1 (ET1), nitric oxide synthase (NOS-3), VEGF-A and C-reactive protein were measured. A correlation analysis was performed, and the strongest and most statistically significant correlation (ρ=0.515; p=0.001) was found between uric acid and ET1. The level of endothelin 1 increases markedly with increasing uric acid. In order to identify the relationship between ET1 (the dependent variable) and uric acid, a multiple linear regression was constructed. In the final model, uric acid turned out to be a significant independent predictor of ET1 levels (β=0.162; p=0.002): an increase of 1 mmol/L is associated with an increase in ET1 of about 0.162 mmol/L.
Keywords: gout, hyperuricemia, endothelial dysfunction, metabolic syndrome, systemic inflammation, endothelin-1.
For citation: Bubley K.V., Beloglazov V.A., Yatskov I.A., Ageeva E.A. The effect of hyperuricemia on markers of endothelial dysfunction in patients with gout. Clinical review for general practice. 2026; 7 (1): 46–49 (In Russ.). DOI: 10.47407/kr2026.7.1.00752
Введение
Подагра представляет собой метаболическое нарушение, которое характеризуется хронической гиперурикемией и отложением кристаллов моноурата натрия в тканях и вызывает как локальный иммунный ответ, так и системное хроническое воспаление [1]. Гиперурикемия определяется как уровень мочевой кислоты в сыворотке крови >7 мг/дл (210–420 мкмоль/л) у мужчин и >6 мг/дл (150–350 мкмоль/л) у женщин [1]. Важно отметить, что не у всех пациентов с гиперурикемией развивается подагра, однако риск ее возникновения увеличивается с ростом концентрации мочевой кислоты [1].

По данным на 2020 г., 55,8 млн человек во всем мире страдали подагрой, при этом стандартизированная по возрасту распространенность составила 659,3 (525,4–822,3) на 100 тыс. населения, что на 22,5% (20,9–24,2%) выше, чем в 1990 г. [2, 3]. По оценкам, общее число распространенных случаев подагры достигнет к 2050 г. 95,8 млн (81,1–116 млн) [2, 3].
Некоторые исследования указывают, что более низкие пороговые значения мочевой кислоты относительно нормы могут быть значимы для оценки сердечно-сосудистого риска [4]. Гиперурикемия может быть результатом как повышенного образования мочевой кислоты, так и снижения ее выведения либо сочетания обоих факторов [5]. На уровень мочевой кислоты влияют диетические факторы (продукты, богатые пуринами, алкоголь, фруктоза) и сопутствующие заболевания (злокачественные новообразования, хроническая почечная недостаточность и др.) [1].
Сложное взаимодействие процессов образования и выведения мочевой кислоты, подверженное влиянию образа жизни и генетических факторов, предполагает, что воздействие гиперурикемии может существенно различаться у пациентов с подагрой в зависимости от индивидуальных особенностей метаболизма [6]. Например, если гиперурикемия у одного пациента в основном обусловлена избыточным образованием мочевой кислоты, а у другого – нарушением ее выведения, то последующие эффекты на эндотелиальные маркеры могут различаться из-за разных уровней сопутствующих биологически активных веществ или компенсаторных механизмов.
Гиперурикемия, как в качестве самостоятельного фактора, так и совместно с системным воспалением, может повышать сердечно-сосудистый риск и провоцировать эндотелиальную дисфункцию через генерацию активных форм кислорода (ROS) и последующее повреждение эндотелия и на сегодняшний день может рассматриваться как одно из проявлений метаболического синдрома [1, 7]. Повышение уровня мочевой кислоты наблюдается у пациентов при гипертонии, неалкогольной жировой болезни печени, хронической болезни почек и сердечно-сосудистых заболеваниях [2]. Постоянное присутствие высокого уровня мочевой кислоты в крови может прямо или косвенно воздействовать на эндотелиальные клетки даже при отсутствии отложения кристаллов в сосудах, что выражается в феномене, известном как «сосудистая подагра» [8]. Вместе с тем взаимосвязь уровня мочевой кислоты у больных подагрой с маркерами эндотелиальной дисфункции до сегодняшнего дня остается малоизученным.
Цель исследования – оценить влияние концентрации мочевой кислоты на уровни вазоактивных маркеров (ET1, VEGF-A, NOS-3) у пациентов с подагрой вне обострения.
Материалы и методы
В исследовании приняли участие 38 пациентов (23 мужчины и 15 женщин, средний возраст – 47±8 лет) с подтвержденным диагнозом подагры вне обострения. По уровню в крови мочевой кислоты больные были распределены на две группы: 1-я группа – 26 человек, уровень мочевой кислоты >360 мкмоль/л; 2-я группа – 12 человек, уровень мочевой кислоты <360 мкмоль/л.
В качестве маркера активности воспаления использовался уровень С-реактивного белка (СРБ) в плазме крови.
Уровни СРБ, эндотелина-1 (ET1), NOS-3, VEGF-A в плазме крови измеряли с помощью иммуноферментного анализа с применением наборов производства Cloud Clone Corp. (Хубей, Китай), а концентрацию мочевой кислоты в сыворотке определяли колориметрическим методом с использованием автоматического анализатора.
Критериями исключения пациентов из исследования были: отказ пациента, системные заболевания соединительной ткани, беременность, онкологические заболевания, первичная гиперурикемия.
Статистический анализ проводился с помощью программного обеспечения IBM SPSS Statistics 28. Тип распределения параметров в вариационном ряду устанавливали по критерию Шапиро–Уилка. Значимость различий между несвязанными выборками определяли при помощи непараметрических критериев для независимых выборок (U-критерий Манна–Уитни). Корреляционный анализ проводился с использованием метода ранговой корреляции Спирмена. Построена линейная регрессионная модель.

Результаты
Как следует из данных, приведенных в табл. 1, статистически значимые различия между клиническими группами зарегистрированы только для ET1 и мочевой кислоты. При анализе маркеров эндотелиальной дисфункции выявлено достоверное повышение уровня ET1 у группы с гиперурикемией по сравнению с группой с нормальным уровнем мочевой кислоты (p<0,001), что может свидетельствовать о нарушении вазорегуляторной функции эндотелия и смещении состояния сосудистой стенки в сторону вазоконстрикции.
Проведенный корреляционный анализ (табл. 2) показал, что наиболее сильная и статистически значимая корреляция (ρ=0,515; p=0,001) обнаружена между мочевой кислотой и ET1. Остальные рассматриваемые параметры (NOS-3, VEGF-A, СРБ, ангиотензин II) не продемонстрировали статистически значимых корреляций с мочевой кислотой.
Таким образом, уровень мочевой кислоты положительно связан только с уровнем ET1, который, как известно, обладает вазоконстрикторными свойствами и не влияет на другие маркеры. Отсутствие влияния концентрации мочевой кислоты в крови на уровень NO-синтетазы (NOS-3) свидетельствует о том, что что гиперурикемия сдвигает баланс в сторону вазоконстрикции.
Построена множественная линейная регрессия уровня ET1 (зависимая переменная) от мочевой кислоты. В итоговой модели значимым независимым предиктором уровня ET1 оказалась мочевая кислота (β=0,162; p=0,002): повышение на 1 мкмоль/л связано с ростом ET1 примерно на 0,162 мкмоль/л. Полученная модель объясняет 24,2% дисперсии.
Результаты регрессионного анализа подтверждают значимую положительную связь между уровнем мочевой кислоты и концентрацией ET1.
Обсуждение
Результаты исследования демонстрируют значимую связь между повышенной концентрацией мочевой кислоты и увеличением содержания ET1 в плазме крови у пациентов с подагрой вне обострения. Полученные данные подтверждают концепцию, согласно которой гиперурикемия способствует развитию эндотелиальной дисфункции за счет смещения баланса между вазодилатирующими и вазоконстрикторными эффектами в сторону сужения сосудов. Механизмы данного взаимодействия могут включать повышение продукции реактивных форм кислорода (ROS) и последующего гиперокисления как внутриклеточной, так и внеклеточной среды, что приводит к снижению биодоступности окиси азота (NO) и продукции ET1 в эндотелиальных клетках [6, 9–11]. Совокупность множественных механизмов, посредством которых гиперурикемия подавляет продукцию NO, подчеркивает критическую роль этого пути в развитии эндотелиальной дисфункции, связанной с гиперурикемией. Например, увеличение продукции ксантиноксидазой активных форм кислорода, которые реагируют с NO, дополнительно снижает доступность NO [12]. Также при повышении активности аргиназы она конкурирует с eNOS за субстрат L-аргинин, что в свою очередь дополнительно снижает содержание NO посредством активации сигнального пути протеинкиназы С, приводя к фосфорилированию NOS-3 в ингибирующих сайтах [13, 14].
Наше исследование дополняет существующие данные о роли мочевой кислоты как прооксидантного агента, подчерчивая, что даже при отсутствии клинически выраженного воспаления и вне зависимости от наличия сопутствующего повреждающего фактора эндотелия (артериальная гипертензия) гиперурикемия способна вызвать повреждение эндотелия через гиперпродукцию ET1, а впоследствии – длительную вазоконстрикцию [15].
Отсутствие значимых изменений уровней NOS-3, VEGF-A и ангиотензина II указывает на избирательное влияние гиперурикемии на эндотелиальный баланс: повышение уровня ET1 не сопровождается компенсаторным повышением содержания NO-синтетазы или васкулогенеза, что может свидетельствовать о подавлении механизма защитной вазодилатации при хронической гиперурикемии. Эти результаты частично расходятся с данными некоторых исследований, где гиперурикемия ассоциировалась со снижением экспрессии NOS-3 и повышением маркеров вазодилатации. Вероятно, различия объясняются гетерогенностью когорты по сопутствующим метаболическим факторам и методическим особенностям определения маркеров [16, 17].
Множественная линейная регрессия показала, что мочевая кислота является независимым предиктором уровня ET1 (β=0,162; p=0,002), объясняя около 24,2% дисперсии показателя ET1. Это подчеркивает вклад гиперурикемии в патогенез эндотелиальной дисфункции и актуализирует необходимость контроля уровня мочевой кислоты для профилактики не только подагрических артритов, но и сердечно-сосудистых осложнений.
Заключение
Результаты исследования свидетельствуют о необходимости ранней диагностики и целенаправленной коррекции гиперурикемии у пациентов с подагрой вне обострения. Использование ингибиторов ксантиноксидазы может способствовать снижению уровня ET1 и уменьшению риска развития артериальной гипертензии и других сосудистых осложнений [18, 19].
Гиперурикемия у пациентов с подагрой является значимым фактором развития эндотелиальной дисфункции, главным образом через механизмы, включающие снижение биодоступности NO и, возможно, повышение уровня ET1. Влияние на VEGF-A представляется более сложным и требует дальнейшего изучения, что подтверждается изменением ключевых маркеров (ET1, NOS-3, VEGF-A). Полученные данные подчеркивают необходимость контроля уровня мочевой кислоты не только для профилактики подагрических атак, но и для снижения сердечно-сосудистого риска.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация о спонсорстве. Исследование не имело спонсорской поддержки.
Information about sponsorship. The study had no sponsorship.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Бублей Константин Викторович – ассистент каф. внутренней медицины №2 Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского». E-mail: bubley.99@mail.ru
Konstantin V. Bubley – аssistant, Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University.
E-mail: bubley.99@mail.ru
Белоглазов Владимир Алексеевич – д-р мед. наук, проф., зав. каф. внутренней медицины №2 Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского»
Vladimir A. Beloglazov – Dr. Sci. (Med.), Prof., Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University
Яцков Игорь Анатольевич – канд. мед. наук, доц. каф. внутренней медицины №2 Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского»
Igor A. Yatskov – Cand. Sci. (Med.), Assoc. Prof., Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University
Агеева Елизавета Сергеевна – д-р мед. наук, доц., зав. каф. медицинской биологии Ордена Трудового Красного Знамени Медицинского института им. С.И. Георгиевского ФГАОУ ВО «КФУ им. В.И. Вернадского»
Elizaveta S. Ageeva – Dr. Sci. (Med.), Assoc. Prof., Georgievsky Order of the Red Banner Medical Institute, Vernadsky Crimean Federal University
Поступила в редакцию: 07.07.2025
Поступила после рецензирования: 31.07.2025
Принята к публикации: 14.08.2025
Received: 07.07.2025
Revised: 31.07.2025
Accepted: 14.08.2025
Список исп. литературыСкрыть список1. Timsans J, Palomäki A, Kauppi M. Gout and Hyperuricemia: A Narrative Review of Their Comorbidities and Clinical Implications. J Clin Med 2024;13(24):7616. DOI: 10.3390/jcm13247616
2. Cross M, Smith E, Hoy D et al. Global, regional, and national burden of gout, 1990–2020, and projections to 2050: a systematic analysis of the Global Burden of Disease Study 2021. Lancet Rheumatol 2024 Aug;6(8):e507-e517. DOI: 10.1016/S2665-9913(24)00117-6
3. Choi HK, Ford ES. Prevalence of the metabolic syndrome in individuals with hyperuricemia. Am J Med 2007 May;120(5):442-7. DOI: 10.1016/j.amjmed.2006.06.040
4. Yu W, Cheng JD. Uric Acid and Cardiovascular Disease: An Update From Molecular Mechanism to Clinical Perspective. Front Pharmacol 2020;11:582680. DOI: 10.3389/fphar.2020.582680
5. Yu S, Hong Q, Wang Y et al. High Concentrations of Uric Acid Inhibit Angiogenesis via Regulation of the Krüppel-Like Factor 2-Vascular Endothelial Growth Factor-A Axis by miR-92a. Circ J 2015;79(11):2487-98. DOI: 10.1253/circj.CJ-15-0283
6. Borghi C, Agnoletti D, Cicero AFG. Uric Acid and Hypertension: a Review of Evidence and Future Perspectives for the Management of Cardiovascular Risk. Hypertension 2022 Sep;79(9):1927-36. DOI: 10.1161/HYPERTENSIONAHA.122.17956
7. Khosla UM, Zharikov S, Finch JL et al. Hyperuricemia induces endothelial dysfunction. Kidney Int 2005 May;67(5):1739-42. DOI: 10.1111/j.1523-1755.2005.00273.x
8. Qi X, Zhang Z, Jia M et al. Evolving multimorbidity patterns among ageing adults with cardiovascular disease continuum in Southwest China: A longitudinal cohort study. Int J Cardiol Cardiovasc Risk Prev 2025;25:200417. DOI: 10.1016/j.ijcrp.2025.200417
9. Mann GE, Rowlands DJ, Li FY et al. Activation of endothelial nitric oxide synthase by dietary isoflavones: Role of NO in Nrf2-mediated antioxidant gene expression. Cardiovasc Res 2007 Jul 15;75(2):261-74. DOI: 10.1016/j.cardiores.2007.04.004
10. Johnson RJ, Kang DH, Feig D et al. Is there a pathogenetic role for uric acid in hypertension and cardiovascular and renal disease? Hypertension 2003 Jun;41(6):1183-90. DOI: 10.1161/01.HYP.0000069700. 62727.C5
11. Mazzali M, Hughes J, Kim YG et al. Elevated uric acid increases blood pressure in the rat by a novel crystal-independent mechanism. Hypertension 2001;38(5):1101-6. DOI: 10.1161/hy1101.092839
12. Ciarambino T, Crispino P, Giordano M. Hyperuricemia and Endothelial Function: Is It a Simple Association or Do Gender Differences Play a Role in This Binomial? Biomedicines 2022;10(12):3067. DOI: 10.3390/biomedicines10123067
13. Papežíková I, Pekarová M, Kolářová H et al. Uric acid modulates vascular endothelial function through the down regulation of nitric oxide production. Free Radic Res 2013 Feb;47(2):82-8. DOI: 10.3109/10715762.2012.747677
14. Miricescu D, Totan A, Stefani C et al. Hyperuricemia, endothelial dysfunction and hypertension. Rom J Med Pract 2020;15(2):178-82. DOI: 10.37897/RJMP.2020.2.10
15. Tejero J, Shiva S, Gladwin MT. Sources of Vascular Nitric Oxide and Reactive Oxygen Species and Their Regulation. Physiol Rev 2019 Jan 1;99(1):311-79. DOI: 10.1152/physrev.00036.2017
16. Kanellis J, Watanabe S, Li JH et al. Uric acid stimulates monocyte chemoattractant protein-1 production in vascular smooth muscle cells via mitogen-activated protein kinase and cyclooxygenase-2. Hypertension 2003 Jun;41(6):1287-93. DOI: 10.1161/01.HYP.0000072820. 07472.3B
17. Choi YJ, Yoon Y, Lee KY et al. Uric acid induces endothelial dysfunction by vascular insulin resistance associated with the impairment of nitric oxide synthesis. FASEB J 2014 Jul;28(7):3197-204. DOI: 10.1096/fj.13-247148
18. Acharya C, Sharma A, Kantharia N. Involvement of oxidative stress in patients of gout and antioxidant effect of allopurinol. Int J Med Sci Public Health 2015;4(1):1-4. DOI: 10.5455/ijmsph.2015.0310201435
19. Tie N, Bai L, Li H et al. Effects of febuxostat in different doses on uric acid, inflammatory factors of serum and knee articular cavity, endothelin-1, and oxidative stress in patients with a gout-a comparative study. Afr Health Sci 2024;24(4):313-24. DOI: 10.4314/ahs.v24i4.40
18 февраля 2026
Количество просмотров: 110


