Клинический разбор в общей медицине №01 2026
Yulia A. Zgura
Professor V.F. Voino-Yasenetsky Krasnoyarsk State Medical University, Krasnoyarsk, Russia
urstalla@gmail.com
Abstract
Predictors of the development of contrast-induced acute kidney injury in patients with acute myocardial infarction who underwent coronary angiography and percutaneous coronary intervention have been identified. The regression analysis performed allowed us to identify three statistically significant risk factors for the development of contrast-induced acute kidney injury: anemia, age, and the volume of contrast agent administered per unit of body weight. The assessment of these simple indicators is performed at the patient's bedside and allows for the implementation of a comprehensive set of urgent therapeutic and preventive measures.
Aim. Identify predictors of contrast-induced acute kidney injury in patients with acute myocardial infarction.
Materials and methods. Clinical and epidemiological data obtained from 501 patients with acute myocardial infarction were analyzed by contemporary statistical methods of investigation.
Results. Significant risk factors of contrast-induced acute kidney injury in patients with acute myocardial infarction were detected. The ease of identifying these factors helps to predict the possibility of developing a serious complication of acute myocardial infarction.
Conclusion. We identified risk factors of contrast-induced acute kidney injury in the working condition of emergency cardiology hospital that will help carry out timely therapeutic and preventive measures.
Keywords: contrast-induced acute kidney injury, acute myocardial infarction, coronary angiography, percutaneous coronary intervention, predictors, risk factors.
For citation: Ursta A.A., Kotikov A.R., Ursta O.V., Kharkov E.I., Filimonova L.A., Zgura Yu.A. Detection of risk factors of acute contrast-induced kidney injury in patients with acute myocardial infarction. Clinical review for general practice. 2026; 7 (1): 50–54 (In Russ.).
DOI: 10.47407/kr2026.7.1.00753
Введение
Контраст-индуцированное острое повреждение почек (КИОПП) рассматривается как ухудшение фильтрационной функции почек в ответ на интравазальную инъекцию йодсодержащего рентгеноконтрастного препарата при обязательном исключении других возможных причин острого почечного повреждения (нефротоксины, гипотензия, экстраренальная обструкция и др.) [1, 2]. С момента появления транскатетерной диагностики и малоинвазивных лечебных процедур повышение уровня их безопасности для пациентов является приоритетной задачей [3, 4]. Риск развития КИОПП существенно возрастает у пожилых пациентов, у пациентов с изначально скомпрометированной функцией почек, при сахарном диабете и во многих других случаях [1, 5–9]. Отмечена взаимосвязь между развитием КИОПП и неблагоприятными клиническими исходами, среди которых можно выделить формирование хронической почечной недостаточности и кардиоваскулярные осложнения [1, 10–13].
Цель исследования – выявление факторов риска снижения фильтрационной функции почек в ответ на введение контрастсодержащих препаратов у пациентов с острым инфарктом миокарда (ОИМ), которые были подвергнуты коронароангиографии (КАГ) и чрескожному коронарному вмешательству (ЧКВ).
Материалы и методы
Клиническое исследование выполнено на кафедре пропедевтики внутренних болезней и терапии с курсом ПО ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого» Минздрава России (ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого»), клиническая база – кардиологическое отделение КГБУЗ «Красноярская межрайонная клиническая больница скорой медицинской помощи им. Н.С. Карповича» (КГБУЗ «КМКБСМП им. Н.С. Карповича»).
Идентификация кандидатов на включение в исследуемую группу выполнялась на основании письменного информированного согласия каждого пациента на участие в проведении исследования и дополнительных методов диагностики в соответствии со ст. 20 Федерального закона от 22.11.2011 №323-Ф3 (ред. 02.07.2021) «Об основах охраны здоровья граждан в Российской Федерации». Постановление локального этического комитета ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого» (протокол №62/2015 от 27.05.2015) подтвердило соответствие настоящего исследования этическим принципам.
Исследуемая группа представлена пациентами с диагностированным ОИМ (n=501), которые в 2014–2017 гг. проходили лечение в кардиологическом отделении КГБУЗ «КМКБСМП им. Н.С. Карповича» (табл. 1). Всем пациентам в обязательном порядке проводилась срочная КАГ с решением вопроса о дальнейшем ЧКВ.
Критерии исключения пациентов из исследуемой группы: диагностированный кардиогенный шок, ФВ ЛЖ ниже 40%, уровень центрального венозного давления выше 120 мм вод. ст., наличие хронической болезни почек V стадии, проведение заместительной почечной терапии, проведение рентгеноконтрастного исследования, не связанного с ЧКВ, отказ от участия в исследовании, тяжелые психические расстройства, поведенческие нарушения.
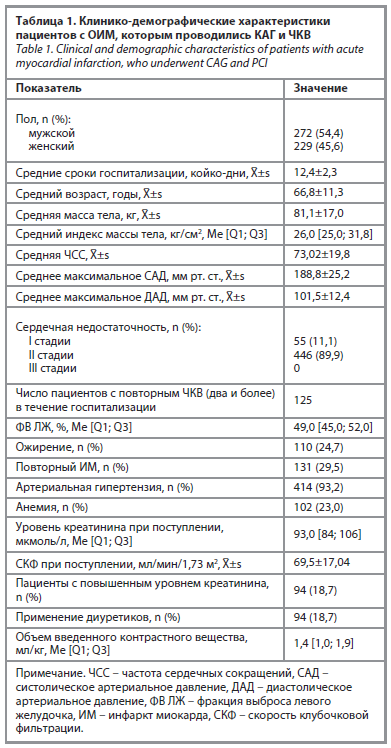 Верификация КИОПП осуществлялась на основании увеличения показателей креатинина сыворотки крови относительно базовых значений на 26 мкмоль/л и более в интервале 48 ч после проведения ЧКВ с использованием рентгеноконтрастных препаратов, другим основанием для верификации КИОПП было повышение уровня креатинина сыворотки крови более чем в 1,5 раза в течение недели после ЧКВ.
Верификация КИОПП осуществлялась на основании увеличения показателей креатинина сыворотки крови относительно базовых значений на 26 мкмоль/л и более в интервале 48 ч после проведения ЧКВ с использованием рентгеноконтрастных препаратов, другим основанием для верификации КИОПП было повышение уровня креатинина сыворотки крови более чем в 1,5 раза в течение недели после ЧКВ.
Характер распределения подавляющего большинства полученных количественных (дискретных и непрерывных) переменных в группах отличался от нормального, в отношении них использовали непараметрические методы исследования: дисперсионный анализ повторных измерений с критерием Фридмана, для парных сравнений независимых переменных применялся U-критерий Манна–Уитни. Переменные, имеющие распределение, отклоняющееся от нормального, отображались в виде медианы и квартилей (Me [Q1; Q3]). Корреляционный анализ осуществлялся посредством коэффициента корреляции Спирмена. В отношении переменных, подчинявшихся закону нормального распределения при попарных сравнениях, использовался критерий t Стьюдента, а в случае множественных сравнений применялся однофакторный дисперсионный анализ. Переменные с нормальным распределением отображались в виде арифметического среднего и стандартного отклонения (—X ±s). В отношении категориальных переменных применялся критерий χ2 Пирсона.
Статистический анализ полученных данных выполнялся с использованием параметрических и непараметрических методов, включая нелинейную логистическую регрессию. Все статистические операции выполнены в среде программирования R (Rversion 4.2.1).
Для поиска предикторов отобранные пациенты были случайным образом разделены на две группы: обучаемая и тестируемая (соотношение 4:1). В обучаемую группу отбирались переменные на основании однофакторных статистических методов, из нее в свою очередь осуществлялась случайная генерация 100 выборок с последующим проведением логистической регрессии. Каждая из генерируемых выборок пошагово оценивалась с целью отбора предикторов в итоговую модель. Таким образом были выявлены три переменные, которые были статистически значимы (p<0,001) более чем в 90% генерируемых выборок. Было рассчитано отношение шансов (ОШ) с 95% доверительными интервалами (ДИ) для каждого предиктора.
Адекватность полученных регрессионных моделей подтверждена критерием согласия Хосмера–Лемешева (p>0,2) в условиях генераций рандомизированных выборок. Объем выборки для представленных логистических регрессионных моделей можно считать приемлемым, основываясь на многочисленных публикациях, посвященных данной проблеме [14].
Результаты и обсуждение
Используя клинические данные (см. табл. 1), мы отобрали следующие переменные как предполагаемые факторы риска развития КИОПП: возраст (число лет), анемия (есть или нет), гемоглобин крови (г/л), ФВ ЛЖ (%), объем введенного контрастного вещества (мл/кг).
 Статистический анализ частотных распределений по возрастным диапазонам показал статистически значимые различия (χ2=23,9; p=0,003). Также отмечены статистически значимые различия распределения числовых значений показателей возраста в исследуемых группах (p=0,008).
Статистический анализ частотных распределений по возрастным диапазонам показал статистически значимые различия (χ2=23,9; p=0,003). Также отмечены статистически значимые различия распределения числовых значений показателей возраста в исследуемых группах (p=0,008).
В группе пациентов с КИОПП более 95% всех случаев приходятся на возрастной диапазон 61–90 лет, в то время как у пациентов без КИОПП доля рассматриваемого интервала составляла 70%. В группе пациентов с КИОПП возрастной диапазон составил 52–89 лет, в группе пациентов без КИОПП – 33–92 года.
Корреляционный анализ между исследуемыми переменными не выявил средних и сильных корреляционных связей.
Логистический регрессионный анализ переменной «возраст» с зависимой дихотомической переменной «КИОПП» позволил получить логистическую регрессионную модель:
1
pКИОПП = 1+e-(7,1503-0,072Возраст), где pКИОПП – вероятность развития КИОПП, e – основание натурального логарифма (2,7183).
В полученном уравнении регрессии присутствуют следующие коэффициенты: «-7,1503» – коэффициент сдвига (α), p<0,001, с 95% ДИ от -10,14 до -4,50, соответствующий на графике значению оси y при x=0; «0,072» – коэффициент наклона (β), p<0,001, с 95% ДИ 0,036–0,112. ОШ для представленного уравнения регрессии составило 4,06 (95% ДИ 3,625–4,372; p=0,024).
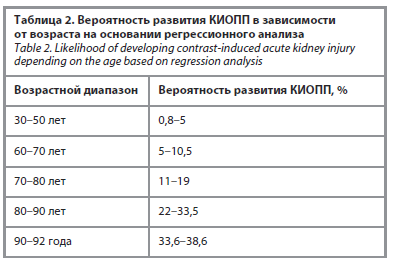
В табл. 2 отображены значения вероятностей развития КИОПП у исследуемых пациентов в выделенных возрастных диапазонах на основании полученного уравнения регрессии.
 Вероятность развития КИОПП значительно повышается у пациентов старше 80 лет с ИМ (выше 22%), а группа пациентов старше 90 лет с ИМ условно может быть расценена как группа очень высокого риска развития КИОПП.
Вероятность развития КИОПП значительно повышается у пациентов старше 80 лет с ИМ (выше 22%), а группа пациентов старше 90 лет с ИМ условно может быть расценена как группа очень высокого риска развития КИОПП.
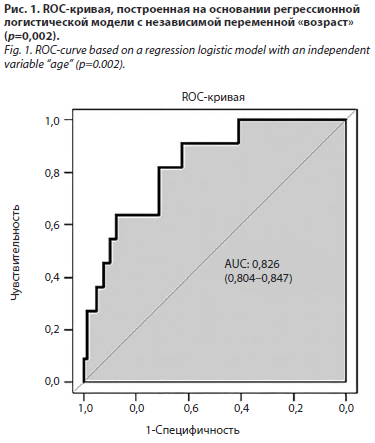
На основании полученного уравнения регрессии построена ROC-кривая (рис. 1) – графическая оценка качества бинарной классификации, количественным выражением которой является площадь под представленной кривой (AUC). Значение 0,83 в данном случае можно интерпретировать как способность данной модели в 83% случаев правильно определять наличие или отсутствие КИОПП на основании непрерывной переменной «возраст», что может считаться оптимистичным прогностическим показателем (p=0,002).
На основании критериев, предложенных Всемирной организацией здравоохранения, анемия определяется как снижение уровня гемоглобина ниже 120 г/л у женщин и ниже 130 г/л у мужчин. В группе пациентов с КИОПП анемия встречалась в 44,4% случаев (26 пациентов), в группе пациентов с нескомпрометированной функцией почек – в 23% случаев (102 пациента), что на основании использованных статистических методов оказалось статистически значимо различным (χ2=14,3; р<0,001).
Среднее значение уровня гемоглобина при поступлении в группе с КИОПП составило 129,1±17,8 г/л, у пациентов без КИОПП – 136,4±17,6 г/л. Между показателями уровня гемоглобина (г/л) в исследуемых группах на основании критерия Стьюдента были выявлены статистически значимые различия (t=2,32; p=0,018).
С целью оценки характера зависимости развития острого повреждения почек от анемии выполнено три варианта регрессионного анализа. В первом случае зависимой переменной явился показатель уровня гемоглобина (г/л), во втором – наличие или отсутствие анемии, в третьем – анемия представлена в формате степеней тяжести (три номинальных значения). Из трех представленных вариантов статистически значимое (p=0,009) регрессионное уравнение получилось только в отношении независимой дихотомической переменной «анемия» («есть» и «нет»), которое имело следующий вид:
1
pКИОПП = 1+e-(2.3026-0,9008Анемия), где pКИОПП – вероятность развития КИОПП, e – основание натурального логарифма (2,7183).
В полученном уравнении регрессии присутствуют следующие коэффициенты: «-2,3026» – коэффициент сдвига (α), p=0,016, с 95% ДИ от -2,793 до -1,869, соответствующий на графике значению оси y при x=0; «0,9008» – коэффициент наклона (β), p=0,009, с 95% ДИ 0,175–1,614. ОШ для представленного уравнения регрессии составило 4,231 (95% ДИ 3,532–5,087; p=0,021).
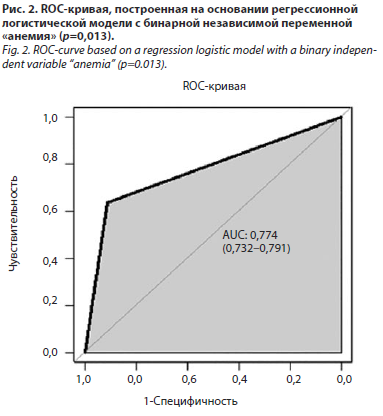 Вероятность развития КИОПП у пациентов с ОИМ при отсутствии анемии составила 9%, а при наличии анемии – 19%, что может быть расценено как категория умеренного риска. Результаты, полученные после построения ROC-кривой (рис. 2), можно интерпретировать как способность регрессионной модели в 77% случаев правильно определять наличие или отсутствие КИОПП на основании бинарной переменной «анемия», что может считаться оптимистичным прогностическим показателем.
Вероятность развития КИОПП у пациентов с ОИМ при отсутствии анемии составила 9%, а при наличии анемии – 19%, что может быть расценено как категория умеренного риска. Результаты, полученные после построения ROC-кривой (рис. 2), можно интерпретировать как способность регрессионной модели в 77% случаев правильно определять наличие или отсутствие КИОПП на основании бинарной переменной «анемия», что может считаться оптимистичным прогностическим показателем.
Медиана объема контрастного вещества на единицу массы тела у пациентов с КИОПП составила 1,7 [1,2; 2,6] мл/кг, а у пациентов без КИОПП – 1,4 [1,0; 1,9] мл/кг, при этом различия между показателями были статистически значимыми (W=919; p=0,039). После преобразования исследуемых переменных методом Tukey's ladder of powers для получения нормального распределения произведено сравнение данных с использованием критерия Стьюдента, который показал еще более значимые различия (t=-3,9677; p=0,008).
Регрессионное уравнение, построенное на основании логистического регрессионного анализа данных с зависимой дихотомической переменной КИОПП и независимой переменной «объем контраста» (мл/кг), имело следующий вид:
1
pКИОПП = 1+e-(2,9004+0,5200Vконтраста), где pКИОПП – вероятность развития КИОПП, e – основание натурального логарифма (2,7183).
В полученном уравнении регрессии присутствуют следующие коэффициенты: «-2,9004» – коэффициент сдвига (α), p=0,014, с 95% ДИ от -3,76 до 4,101, соответствующий на графике значению оси y при x=0; «0,5200» – коэффициент наклона (β), p=0,009, с 95% ДИ 0,112–0,921. ОШ для представленного уравнения регрессии составило 3,431 (95% ДИ 2,956–3,851; p=0,003).
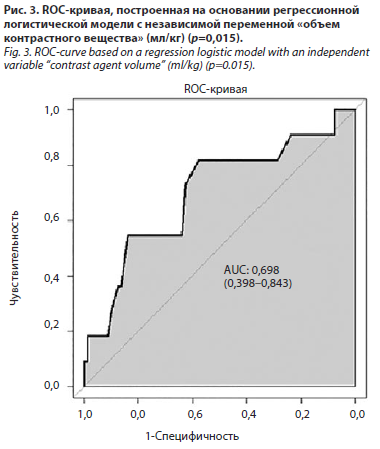 Полученное уравнение регрессии позволило построить ROC-кривую (рис. 3). Значение 0,7 в данном случае можно интерпретировать как способность данной модели в 70% случаев правильно определять наличие или отсутствие КИОПП на основании интервальной переменной «объем контрастного вещества» (мл/кг), что может считаться оптимистичным прогностическим показателем.
Полученное уравнение регрессии позволило построить ROC-кривую (рис. 3). Значение 0,7 в данном случае можно интерпретировать как способность данной модели в 70% случаев правильно определять наличие или отсутствие КИОПП на основании интервальной переменной «объем контрастного вещества» (мл/кг), что может считаться оптимистичным прогностическим показателем.
Медиана ФВ ЛЖ в группе пациентов с КИОПП имела значение 48,5 [46,0; 52,6] %, а в группе пациентов без КИОПП – 49,0 [46,0; 48,0] %, при этом различия были статистически значимы (W=5590; p=0,044).
Выполненный логистический регрессионный анализ установил недостоверную значимость коэффициентов уравнения регрессии: коэффициент сдвига α – p=0,7, коэффициент наклона β – p=0,0504. ОШ в полученном уравнении регрессии составило 1,24 (95% ДИ 0,837–1,692; p=0,873).
Заключение
Среди отбираемых в выборку пациентов исключались случаи с признаками кардиогенного шока вследствие ОИМ. Хорошо известно, что любой шок, в том числе кардиогенный, очень часто проявляется острым почечным повреждением в результате глобальных гемодинамических нарушений в организме. Учитывая то, что ОИМ является ургентным состоянием, достоверная дифференцировка этиологии нарушения почечной функции зачастую затруднительна. На этом основании изначально было принято решение об исключении из формируемой выборки пациентов с изначально повышенным уровнем креатинина. В противном случае достоверность верификации патогенеза острого почечного повреждения после проведения рентгеноконтрастного исследования была бы под большим сомнением. Несомненно, представленный факт может считаться недостатком формируемой модели прогнозирования развития КИОПП у пациентов с ОИМ, которым проводилось ЧКВ.
Проведенный анализ клинических и лабораторных факторов у пациентов исследуемых групп позволил предварительно выделить три статистически значимых фактора риска развития КИОПП: наличие анемии, возраст и объем вводимого контрастного вещества в пересчете на единицу массы тела.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare that there is no conflict of interest.
Информация о спонсорстве. Исследование не имело спонсорской поддержки.
Information about sponsorship. The study had no sponsorship.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Урста Алла Александровна – канд. мед. наук, ассистент, ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого».
E-mail: urstalla@gmail.com; ORCID: 0000-0002-9986-3097
Alla A. Ursta – Cand. Sci. (Med.), Assistant, V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. E-mail: urstalla@gmail.com; ORCID: 0000-0002-9986-3097
Котиков Алихан Русланович – канд. мед. наук, ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0002-4082-3162
Alikhan R. Kotikov – Cand. Sci. (Med.), V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0002-4082-3162
Урста Олег Васильевич – канд. мед. наук, ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0003-1463-2642
Oleg V. Ursta – Cand. Sci. (Med.), V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0003-1463-2642
Харьков Евгений Иванович – д-р мед. наук, проф., ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0002-8208-0926
Evgeny I. Kharkov – Dr. Sci. (Med.), Prof., V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0002-8208-0926
Филимонова Людмила Анатольевна – канд. мед. наук, доц., ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0009-0000-8341-6068
Ludmila A. Filimonova – Cand. Sci. (Med.), Assoc. Prof.,
V.F. Voino-Yasenetsky Krasnoyarsk State Medical University.
ORCID: 0009-0000-8341-6068
Згура Юлия Александровна – канд. мед. наук, доц., ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0009-0008-7239-4324
Yulia A. Zgura – Cand. Sci. (Med.), Assoc. Prof., V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0009-0008-7239-4324
Поступила в редакцию: 19.08.2025
Поступила после рецензирования: 01.10.2025
Принята к публикации: 02.10.2025
Received: 19.08.2025
Revised: 01.10.2025
Accepted: 02.10.2025
Клинический разбор в общей медицине №01 2026
Выявление факторов риска развития контраст-индуцированного острого повреждения почек у пациентов с острым инфарктом миокарда
Номера страниц в выпуске:50-54
Аннотация
Определены предикторы развития контраст-индуцированного острого повреждения почек (КИОПП) у пациентов с острым инфарктом миокарда (ОИМ), которым проводились коронароангиография и чрескожное коронарное вмешательство. Выполненный регрессионный анализ позволил определить три статистически достоверных фактора риска развития КИОПП: анемия, возраст и объем вводимого контрастного вещества в пересчете на единицу массы тела. Оценка этих простых показателей проводится у постели больного и позволяет обеспечить комплекс неотложных лечебных и профилактических мер.
Цель. Определить предикторы КИОПП у пациентов с ОИМ.
Материалы и методы. Клинические и эпидемиологические данные, полученные от 501 пациента с ОИМ, были проанализированы при помощи современных статистических методов исследования.
Результаты. Найдены статистически достоверные факторы риска развития КИОПП у пациентов с ОИМ. Простота определения этих факторов позволяет быстро прогнозировать возможность развития грозного осложнения ОИМ.
Заключение. Выявленные факторы риска развития КИОПП в условиях работы неотложного кардиологического стационара позволят вовремя провести лечебные и профилактические мероприятия.
Ключевые слова: контраст-индуцированное острое повреждение почек, острый инфаркт миокарда, коронароангиография, чрескожное коронарное вмешательство, предикторы, факторы риска.
Для цитирования: Урста А.А., Котиков А.Р., Урста О.В., Харьков Е.И., Филимонова Л.А., Згура Ю.А. Выявление факторов риска развития контраст-индуцированного острого повреждения почек у пациентов с острым инфарктом миокарда. Клинический разбор в общей медицине. 2026; 7 (1): 50–54. DOI: 10.47407/kr2026.7.1.00753
Определены предикторы развития контраст-индуцированного острого повреждения почек (КИОПП) у пациентов с острым инфарктом миокарда (ОИМ), которым проводились коронароангиография и чрескожное коронарное вмешательство. Выполненный регрессионный анализ позволил определить три статистически достоверных фактора риска развития КИОПП: анемия, возраст и объем вводимого контрастного вещества в пересчете на единицу массы тела. Оценка этих простых показателей проводится у постели больного и позволяет обеспечить комплекс неотложных лечебных и профилактических мер.
Цель. Определить предикторы КИОПП у пациентов с ОИМ.
Материалы и методы. Клинические и эпидемиологические данные, полученные от 501 пациента с ОИМ, были проанализированы при помощи современных статистических методов исследования.
Результаты. Найдены статистически достоверные факторы риска развития КИОПП у пациентов с ОИМ. Простота определения этих факторов позволяет быстро прогнозировать возможность развития грозного осложнения ОИМ.
Заключение. Выявленные факторы риска развития КИОПП в условиях работы неотложного кардиологического стационара позволят вовремя провести лечебные и профилактические мероприятия.
Ключевые слова: контраст-индуцированное острое повреждение почек, острый инфаркт миокарда, коронароангиография, чрескожное коронарное вмешательство, предикторы, факторы риска.
Для цитирования: Урста А.А., Котиков А.Р., Урста О.В., Харьков Е.И., Филимонова Л.А., Згура Ю.А. Выявление факторов риска развития контраст-индуцированного острого повреждения почек у пациентов с острым инфарктом миокарда. Клинический разбор в общей медицине. 2026; 7 (1): 50–54. DOI: 10.47407/kr2026.7.1.00753
Detection of risk factors of acute contrast-induced kidney injury in patients with acute myocardial infarction
Alla A. Ursta, Alichan R. Kotikov, Oleg V. Ursta, Evgeny I. Kharkov, Ludmila A. Filimonova,Yulia A. Zgura
Professor V.F. Voino-Yasenetsky Krasnoyarsk State Medical University, Krasnoyarsk, Russia
urstalla@gmail.com
Abstract
Predictors of the development of contrast-induced acute kidney injury in patients with acute myocardial infarction who underwent coronary angiography and percutaneous coronary intervention have been identified. The regression analysis performed allowed us to identify three statistically significant risk factors for the development of contrast-induced acute kidney injury: anemia, age, and the volume of contrast agent administered per unit of body weight. The assessment of these simple indicators is performed at the patient's bedside and allows for the implementation of a comprehensive set of urgent therapeutic and preventive measures.
Aim. Identify predictors of contrast-induced acute kidney injury in patients with acute myocardial infarction.
Materials and methods. Clinical and epidemiological data obtained from 501 patients with acute myocardial infarction were analyzed by contemporary statistical methods of investigation.
Results. Significant risk factors of contrast-induced acute kidney injury in patients with acute myocardial infarction were detected. The ease of identifying these factors helps to predict the possibility of developing a serious complication of acute myocardial infarction.
Conclusion. We identified risk factors of contrast-induced acute kidney injury in the working condition of emergency cardiology hospital that will help carry out timely therapeutic and preventive measures.
Keywords: contrast-induced acute kidney injury, acute myocardial infarction, coronary angiography, percutaneous coronary intervention, predictors, risk factors.
For citation: Ursta A.A., Kotikov A.R., Ursta O.V., Kharkov E.I., Filimonova L.A., Zgura Yu.A. Detection of risk factors of acute contrast-induced kidney injury in patients with acute myocardial infarction. Clinical review for general practice. 2026; 7 (1): 50–54 (In Russ.).
DOI: 10.47407/kr2026.7.1.00753
Введение
Контраст-индуцированное острое повреждение почек (КИОПП) рассматривается как ухудшение фильтрационной функции почек в ответ на интравазальную инъекцию йодсодержащего рентгеноконтрастного препарата при обязательном исключении других возможных причин острого почечного повреждения (нефротоксины, гипотензия, экстраренальная обструкция и др.) [1, 2]. С момента появления транскатетерной диагностики и малоинвазивных лечебных процедур повышение уровня их безопасности для пациентов является приоритетной задачей [3, 4]. Риск развития КИОПП существенно возрастает у пожилых пациентов, у пациентов с изначально скомпрометированной функцией почек, при сахарном диабете и во многих других случаях [1, 5–9]. Отмечена взаимосвязь между развитием КИОПП и неблагоприятными клиническими исходами, среди которых можно выделить формирование хронической почечной недостаточности и кардиоваскулярные осложнения [1, 10–13].
Цель исследования – выявление факторов риска снижения фильтрационной функции почек в ответ на введение контрастсодержащих препаратов у пациентов с острым инфарктом миокарда (ОИМ), которые были подвергнуты коронароангиографии (КАГ) и чрескожному коронарному вмешательству (ЧКВ).
Материалы и методы
Клиническое исследование выполнено на кафедре пропедевтики внутренних болезней и терапии с курсом ПО ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого» Минздрава России (ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого»), клиническая база – кардиологическое отделение КГБУЗ «Красноярская межрайонная клиническая больница скорой медицинской помощи им. Н.С. Карповича» (КГБУЗ «КМКБСМП им. Н.С. Карповича»).
Идентификация кандидатов на включение в исследуемую группу выполнялась на основании письменного информированного согласия каждого пациента на участие в проведении исследования и дополнительных методов диагностики в соответствии со ст. 20 Федерального закона от 22.11.2011 №323-Ф3 (ред. 02.07.2021) «Об основах охраны здоровья граждан в Российской Федерации». Постановление локального этического комитета ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого» (протокол №62/2015 от 27.05.2015) подтвердило соответствие настоящего исследования этическим принципам.
Исследуемая группа представлена пациентами с диагностированным ОИМ (n=501), которые в 2014–2017 гг. проходили лечение в кардиологическом отделении КГБУЗ «КМКБСМП им. Н.С. Карповича» (табл. 1). Всем пациентам в обязательном порядке проводилась срочная КАГ с решением вопроса о дальнейшем ЧКВ.
Критерии исключения пациентов из исследуемой группы: диагностированный кардиогенный шок, ФВ ЛЖ ниже 40%, уровень центрального венозного давления выше 120 мм вод. ст., наличие хронической болезни почек V стадии, проведение заместительной почечной терапии, проведение рентгеноконтрастного исследования, не связанного с ЧКВ, отказ от участия в исследовании, тяжелые психические расстройства, поведенческие нарушения.
 Верификация КИОПП осуществлялась на основании увеличения показателей креатинина сыворотки крови относительно базовых значений на 26 мкмоль/л и более в интервале 48 ч после проведения ЧКВ с использованием рентгеноконтрастных препаратов, другим основанием для верификации КИОПП было повышение уровня креатинина сыворотки крови более чем в 1,5 раза в течение недели после ЧКВ.
Верификация КИОПП осуществлялась на основании увеличения показателей креатинина сыворотки крови относительно базовых значений на 26 мкмоль/л и более в интервале 48 ч после проведения ЧКВ с использованием рентгеноконтрастных препаратов, другим основанием для верификации КИОПП было повышение уровня креатинина сыворотки крови более чем в 1,5 раза в течение недели после ЧКВ.Характер распределения подавляющего большинства полученных количественных (дискретных и непрерывных) переменных в группах отличался от нормального, в отношении них использовали непараметрические методы исследования: дисперсионный анализ повторных измерений с критерием Фридмана, для парных сравнений независимых переменных применялся U-критерий Манна–Уитни. Переменные, имеющие распределение, отклоняющееся от нормального, отображались в виде медианы и квартилей (Me [Q1; Q3]). Корреляционный анализ осуществлялся посредством коэффициента корреляции Спирмена. В отношении переменных, подчинявшихся закону нормального распределения при попарных сравнениях, использовался критерий t Стьюдента, а в случае множественных сравнений применялся однофакторный дисперсионный анализ. Переменные с нормальным распределением отображались в виде арифметического среднего и стандартного отклонения (—X ±s). В отношении категориальных переменных применялся критерий χ2 Пирсона.
Статистический анализ полученных данных выполнялся с использованием параметрических и непараметрических методов, включая нелинейную логистическую регрессию. Все статистические операции выполнены в среде программирования R (Rversion 4.2.1).
Для поиска предикторов отобранные пациенты были случайным образом разделены на две группы: обучаемая и тестируемая (соотношение 4:1). В обучаемую группу отбирались переменные на основании однофакторных статистических методов, из нее в свою очередь осуществлялась случайная генерация 100 выборок с последующим проведением логистической регрессии. Каждая из генерируемых выборок пошагово оценивалась с целью отбора предикторов в итоговую модель. Таким образом были выявлены три переменные, которые были статистически значимы (p<0,001) более чем в 90% генерируемых выборок. Было рассчитано отношение шансов (ОШ) с 95% доверительными интервалами (ДИ) для каждого предиктора.
Адекватность полученных регрессионных моделей подтверждена критерием согласия Хосмера–Лемешева (p>0,2) в условиях генераций рандомизированных выборок. Объем выборки для представленных логистических регрессионных моделей можно считать приемлемым, основываясь на многочисленных публикациях, посвященных данной проблеме [14].
Результаты и обсуждение
Используя клинические данные (см. табл. 1), мы отобрали следующие переменные как предполагаемые факторы риска развития КИОПП: возраст (число лет), анемия (есть или нет), гемоглобин крови (г/л), ФВ ЛЖ (%), объем введенного контрастного вещества (мл/кг).
 Статистический анализ частотных распределений по возрастным диапазонам показал статистически значимые различия (χ2=23,9; p=0,003). Также отмечены статистически значимые различия распределения числовых значений показателей возраста в исследуемых группах (p=0,008).
Статистический анализ частотных распределений по возрастным диапазонам показал статистически значимые различия (χ2=23,9; p=0,003). Также отмечены статистически значимые различия распределения числовых значений показателей возраста в исследуемых группах (p=0,008).В группе пациентов с КИОПП более 95% всех случаев приходятся на возрастной диапазон 61–90 лет, в то время как у пациентов без КИОПП доля рассматриваемого интервала составляла 70%. В группе пациентов с КИОПП возрастной диапазон составил 52–89 лет, в группе пациентов без КИОПП – 33–92 года.
Корреляционный анализ между исследуемыми переменными не выявил средних и сильных корреляционных связей.
Логистический регрессионный анализ переменной «возраст» с зависимой дихотомической переменной «КИОПП» позволил получить логистическую регрессионную модель:
1
pКИОПП = 1+e-(7,1503-0,072Возраст), где pКИОПП – вероятность развития КИОПП, e – основание натурального логарифма (2,7183).
В полученном уравнении регрессии присутствуют следующие коэффициенты: «-7,1503» – коэффициент сдвига (α), p<0,001, с 95% ДИ от -10,14 до -4,50, соответствующий на графике значению оси y при x=0; «0,072» – коэффициент наклона (β), p<0,001, с 95% ДИ 0,036–0,112. ОШ для представленного уравнения регрессии составило 4,06 (95% ДИ 3,625–4,372; p=0,024).
В табл. 2 отображены значения вероятностей развития КИОПП у исследуемых пациентов в выделенных возрастных диапазонах на основании полученного уравнения регрессии.
 Вероятность развития КИОПП значительно повышается у пациентов старше 80 лет с ИМ (выше 22%), а группа пациентов старше 90 лет с ИМ условно может быть расценена как группа очень высокого риска развития КИОПП.
Вероятность развития КИОПП значительно повышается у пациентов старше 80 лет с ИМ (выше 22%), а группа пациентов старше 90 лет с ИМ условно может быть расценена как группа очень высокого риска развития КИОПП.На основании полученного уравнения регрессии построена ROC-кривая (рис. 1) – графическая оценка качества бинарной классификации, количественным выражением которой является площадь под представленной кривой (AUC). Значение 0,83 в данном случае можно интерпретировать как способность данной модели в 83% случаев правильно определять наличие или отсутствие КИОПП на основании непрерывной переменной «возраст», что может считаться оптимистичным прогностическим показателем (p=0,002).
На основании критериев, предложенных Всемирной организацией здравоохранения, анемия определяется как снижение уровня гемоглобина ниже 120 г/л у женщин и ниже 130 г/л у мужчин. В группе пациентов с КИОПП анемия встречалась в 44,4% случаев (26 пациентов), в группе пациентов с нескомпрометированной функцией почек – в 23% случаев (102 пациента), что на основании использованных статистических методов оказалось статистически значимо различным (χ2=14,3; р<0,001).
Среднее значение уровня гемоглобина при поступлении в группе с КИОПП составило 129,1±17,8 г/л, у пациентов без КИОПП – 136,4±17,6 г/л. Между показателями уровня гемоглобина (г/л) в исследуемых группах на основании критерия Стьюдента были выявлены статистически значимые различия (t=2,32; p=0,018).
С целью оценки характера зависимости развития острого повреждения почек от анемии выполнено три варианта регрессионного анализа. В первом случае зависимой переменной явился показатель уровня гемоглобина (г/л), во втором – наличие или отсутствие анемии, в третьем – анемия представлена в формате степеней тяжести (три номинальных значения). Из трех представленных вариантов статистически значимое (p=0,009) регрессионное уравнение получилось только в отношении независимой дихотомической переменной «анемия» («есть» и «нет»), которое имело следующий вид:
1
pКИОПП = 1+e-(2.3026-0,9008Анемия), где pКИОПП – вероятность развития КИОПП, e – основание натурального логарифма (2,7183).
В полученном уравнении регрессии присутствуют следующие коэффициенты: «-2,3026» – коэффициент сдвига (α), p=0,016, с 95% ДИ от -2,793 до -1,869, соответствующий на графике значению оси y при x=0; «0,9008» – коэффициент наклона (β), p=0,009, с 95% ДИ 0,175–1,614. ОШ для представленного уравнения регрессии составило 4,231 (95% ДИ 3,532–5,087; p=0,021).
 Вероятность развития КИОПП у пациентов с ОИМ при отсутствии анемии составила 9%, а при наличии анемии – 19%, что может быть расценено как категория умеренного риска. Результаты, полученные после построения ROC-кривой (рис. 2), можно интерпретировать как способность регрессионной модели в 77% случаев правильно определять наличие или отсутствие КИОПП на основании бинарной переменной «анемия», что может считаться оптимистичным прогностическим показателем.
Вероятность развития КИОПП у пациентов с ОИМ при отсутствии анемии составила 9%, а при наличии анемии – 19%, что может быть расценено как категория умеренного риска. Результаты, полученные после построения ROC-кривой (рис. 2), можно интерпретировать как способность регрессионной модели в 77% случаев правильно определять наличие или отсутствие КИОПП на основании бинарной переменной «анемия», что может считаться оптимистичным прогностическим показателем.Медиана объема контрастного вещества на единицу массы тела у пациентов с КИОПП составила 1,7 [1,2; 2,6] мл/кг, а у пациентов без КИОПП – 1,4 [1,0; 1,9] мл/кг, при этом различия между показателями были статистически значимыми (W=919; p=0,039). После преобразования исследуемых переменных методом Tukey's ladder of powers для получения нормального распределения произведено сравнение данных с использованием критерия Стьюдента, который показал еще более значимые различия (t=-3,9677; p=0,008).
Регрессионное уравнение, построенное на основании логистического регрессионного анализа данных с зависимой дихотомической переменной КИОПП и независимой переменной «объем контраста» (мл/кг), имело следующий вид:
1
pКИОПП = 1+e-(2,9004+0,5200Vконтраста), где pКИОПП – вероятность развития КИОПП, e – основание натурального логарифма (2,7183).
В полученном уравнении регрессии присутствуют следующие коэффициенты: «-2,9004» – коэффициент сдвига (α), p=0,014, с 95% ДИ от -3,76 до 4,101, соответствующий на графике значению оси y при x=0; «0,5200» – коэффициент наклона (β), p=0,009, с 95% ДИ 0,112–0,921. ОШ для представленного уравнения регрессии составило 3,431 (95% ДИ 2,956–3,851; p=0,003).
 Полученное уравнение регрессии позволило построить ROC-кривую (рис. 3). Значение 0,7 в данном случае можно интерпретировать как способность данной модели в 70% случаев правильно определять наличие или отсутствие КИОПП на основании интервальной переменной «объем контрастного вещества» (мл/кг), что может считаться оптимистичным прогностическим показателем.
Полученное уравнение регрессии позволило построить ROC-кривую (рис. 3). Значение 0,7 в данном случае можно интерпретировать как способность данной модели в 70% случаев правильно определять наличие или отсутствие КИОПП на основании интервальной переменной «объем контрастного вещества» (мл/кг), что может считаться оптимистичным прогностическим показателем.Медиана ФВ ЛЖ в группе пациентов с КИОПП имела значение 48,5 [46,0; 52,6] %, а в группе пациентов без КИОПП – 49,0 [46,0; 48,0] %, при этом различия были статистически значимы (W=5590; p=0,044).
Выполненный логистический регрессионный анализ установил недостоверную значимость коэффициентов уравнения регрессии: коэффициент сдвига α – p=0,7, коэффициент наклона β – p=0,0504. ОШ в полученном уравнении регрессии составило 1,24 (95% ДИ 0,837–1,692; p=0,873).
Заключение
Среди отбираемых в выборку пациентов исключались случаи с признаками кардиогенного шока вследствие ОИМ. Хорошо известно, что любой шок, в том числе кардиогенный, очень часто проявляется острым почечным повреждением в результате глобальных гемодинамических нарушений в организме. Учитывая то, что ОИМ является ургентным состоянием, достоверная дифференцировка этиологии нарушения почечной функции зачастую затруднительна. На этом основании изначально было принято решение об исключении из формируемой выборки пациентов с изначально повышенным уровнем креатинина. В противном случае достоверность верификации патогенеза острого почечного повреждения после проведения рентгеноконтрастного исследования была бы под большим сомнением. Несомненно, представленный факт может считаться недостатком формируемой модели прогнозирования развития КИОПП у пациентов с ОИМ, которым проводилось ЧКВ.
Проведенный анализ клинических и лабораторных факторов у пациентов исследуемых групп позволил предварительно выделить три статистически значимых фактора риска развития КИОПП: наличие анемии, возраст и объем вводимого контрастного вещества в пересчете на единицу массы тела.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare that there is no conflict of interest.
Информация о спонсорстве. Исследование не имело спонсорской поддержки.
Information about sponsorship. The study had no sponsorship.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Урста Алла Александровна – канд. мед. наук, ассистент, ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого».
E-mail: urstalla@gmail.com; ORCID: 0000-0002-9986-3097
Alla A. Ursta – Cand. Sci. (Med.), Assistant, V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. E-mail: urstalla@gmail.com; ORCID: 0000-0002-9986-3097
Котиков Алихан Русланович – канд. мед. наук, ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0002-4082-3162
Alikhan R. Kotikov – Cand. Sci. (Med.), V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0002-4082-3162
Урста Олег Васильевич – канд. мед. наук, ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0003-1463-2642
Oleg V. Ursta – Cand. Sci. (Med.), V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0003-1463-2642
Харьков Евгений Иванович – д-р мед. наук, проф., ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0000-0002-8208-0926
Evgeny I. Kharkov – Dr. Sci. (Med.), Prof., V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0000-0002-8208-0926
Филимонова Людмила Анатольевна – канд. мед. наук, доц., ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0009-0000-8341-6068
Ludmila A. Filimonova – Cand. Sci. (Med.), Assoc. Prof.,
V.F. Voino-Yasenetsky Krasnoyarsk State Medical University.
ORCID: 0009-0000-8341-6068
Згура Юлия Александровна – канд. мед. наук, доц., ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого». ORCID: 0009-0008-7239-4324
Yulia A. Zgura – Cand. Sci. (Med.), Assoc. Prof., V.F. Voino-Yasenetsky Krasnoyarsk State Medical University. ORCID: 0009-0008-7239-4324
Поступила в редакцию: 19.08.2025
Поступила после рецензирования: 01.10.2025
Принята к публикации: 02.10.2025
Received: 19.08.2025
Revised: 01.10.2025
Accepted: 02.10.2025
Список исп. литературыСкрыть список1. Урста А.А., Харьков Е.И., Петрова М.М. и др. Вероятность развития контраст-индуцированного острого почечного повреждения у пациентов с острым инфарктом миокарда после коронароангиографии и чрескожного коронарного вмешательства. Российский кардиологический журнал. 2021;26(8):27-32. DOI: 10.15829/1560-4071-2021-4424
Ursta A.A., Kharkov E.I., Petrova M.M. et al. Risk assessment of contrast-induced acute kidney injury in patients with acute myocardial infarction after coronary angiography and percutaneous coronary intervention. Russian Journal of Cardiology. 2021;26(8):27-32. DOI: 10.15829/1560-4071-2021-4424 (in Russian).
2. Арсеничева О.В., Щапова Н.Н. Контрастиндуцированная нефропатия у больных с острым коронарным синдромом с подъемом сегмента ST: факторы риска и прогноз. Клиницист. 2019;13(3-4):36-42. DOI: 10.17650/1818-8338-2019-13-3-4-36-42
Arsenicheva O.V., Shchapova N.N. Contrast-induced nephropathy in patients with acute coronary syndrome with ST-segment elevation: risk factors and prognosis. Klinitsist. 2019;13(3-4):36-42. DOI: 10.17650/1818-8338-2019-13-3-4-36-42 (in Russian).
3. Acute Kidney Injury (AKI) – KDIGO. URL: http://kdigo.org/guidelines/acute-kidney-injury/ (date of access 02.10.2017).
4. Mehran R, Dangas GD, Steven D, Weisbord, SD. Contrast-Associated Acute Kidney Injury. N Engl J Med 2019;380:2146-55. DOI: 10.1056/NEJMra1805256
5. Morcos R, Kucharik M, Bansal P et al. Contrast-Induced Acute Kidney Injury: Review and Practical Update. Clin Med Insights Cardiol 2019;13:1179546819878680. DOI: 10.1177/1179546819878680
6. Denegri A, Mehran R, Holy E, Taramasso M. Post procedural risk assessment in patients undergoing trans aortic valve implantation according to the age, creatinine, and ejection fraction-7 score: Advantages of age, creatinine, and ejection fraction-7 in stratification of post-procedural outcome. Catheter Cardiovasc Interv 2019;93:141-8. DOI:
7. Демчук О.В., Сукманова И.А., Пономаренко И.В., Елыкомов В.А. Контрастиндуцированная нефропатия у пациентов с острым коронарным синдромом: клиническое значение, диагностика, методы профилактики. Кардиоваскулярная терапия и профилактика. 2020;19(2):82-8. DOI: 10.15829/1728-8800-2019-2255
Demchuk O.V., Sukmanova I.A., Ponomarenko I.V., Elykomov V.A. Contrast-induced nephropathy in patients with acute coronary syndrome: clinical significance, diagnosis, prophylaxis. Kardiovaskulyarnaya terapiya i profilaktika. 2020;19(2):82-8. DOI: 10.15829/1728-8800-2019-2255 (in Russian).
8. Кобзева Н.Д., Терентьев В.П., Батюшин М.М. Прогнозирование риска формирования постконтрастного острого повреждения почек у больных острым коронарным синдромом. Терапия. 2020;(4):124-30. DOI: 10.18565/therapy.2020.4.124-130
Kobzeva N.D., Terent'ev V.P., Batyushin M.M. Forecasting the risk of forming postcontrast acute kidney injury in patients with acute coronary syndrome. Terapiya. 2020;(4):124-30. DOI: 10.18565/therapy.2020.4.124-130 (in Russian).
9. Хильчук А.А., Абугов С.А., Щербак С.Г. и др. Ранняя диагностика контраст-индуцированного острого почечного повреждения у пациентов с острым коронарным синдромом без элевации сегмента ST. Эндоваскулярная хирургия. 2021;8(2):154-68. DOI: 10.24183/2409-4080-2021-8-2-154-168
Khil'chuk A.A., Abugov S.A., Shcherbak S.G. et al. Early diagnosis of contrast-induced acute kidney injury in patients with non-ST-elevation acute coronary syndrome Endovaskulyarnaya khirurgiya. 2021;8(2):154-68. DOI: 10.24183/2409-4080-2021-8-2-154-168 (in Russian).
10. Davenport MS, Perazella MA, Yee J et al. Use of intravenous iodinated contrast media in patients with kidney disease: consensus Statements from the American College of Radiology and the National Kidney Foundation. Kidney Med. 2020;2(1):85-93. DOI: 10.1016/j.xkme. 2020.01.001
11. Mehran R, Aymong ED, Nikolsky E et al. A simple risk score for prediction of contrast-induced nephropathy after percutaneous coronary intervention: development and initial validation. J Am Coll Cardiol 2004;44:1393-9. DOI: 10.1016/j.jacc.2004.06.068
12. Ronco F, Tarantini G, McCullough PA. Contrast induced acute kidney injury in interventional cardiology: an update and key guidance for clinicians. Rev Cardiovasc Med 2020;21(1):9-23. DOI: 10.31083/j.rcm.2020.01.44
13. Ribitsch W, Horina JH, Quehenberger F et al. Contrast Induced Acute Kidney Injury and its Impact on MidTerm Kidney Function, Cardiovascular Events and Mortality. Sci Rep 2019;9:16896. DOI: 10.1038/s41598-019-53040-5
14. Bujang MA, Sa'at N, Sidik TMITAB, Joo LC. Sample Size Guidelines for Logistic Regression from Observational Studies with Large Population: Emphasis on the Accuracy Between Statistics and Parameters Based on Real Life Clinical Data. Malays J Med Sci 2018;25:122-30. DOI: 10.21315/mjms2018.25.4.12
18 февраля 2026
Количество просмотров: 97


