Клинический разбор в общей медицине №01 2026
Aziza A. Shodmonova3, Nargiza I. Qarshiboyeva4, Ravshan O. Palvanov1
1 Urgench branch of Tashkent Medical Academy, Urgench, Uzbekistan;
2 Mamun University, Urgench, Uzbekistan;
3 Abu Ali ibn Sino Bukhara State Medical Institute, Bukhara, Uzbekistan;
4 Tashkent State Medical Institute, Urgench, Uzbekistan
ortiqovakbar1977@gmail.com
Abstract
Post-stroke Broca’s aphasia is a common and disabling condition, often resistant to conventional speech and language therapy (SLT). Intermittent theta burst stimulation (iTBS) is a neuromodulation technique with potential to promote neuroplasticity and improve language outcomes.
Aim. To assess the clinical efficacy and neurophysiological effects of iTBS combined with SLT in patients with subacute post-stroke Broca’s aphasia.
Materials and methods. In this randomized double-blind sham-controlled trial, 60 patients with subacute post-stroke Broca’s aphasia received active iTBS over the left inferior frontal gyrus (IFG) or sham stimulation alongside two weeks of standardized SLT. Language outcomes were assessed using the Western Aphasia Battery (WAB), alongside neuroimaging markers of cortical activation, EEG connectivity indices, functional independence (Barthel Index), and quality-of-life scales. Assessments were conducted at baseline, post-treatment, and at 1, 3, and 6 months.
Results. The iTBS group showed significantly greater gains in WAB Aphasia Quotient (p<0.001; d=1.63). fMRI revealed increased BOLD activity in the left IFG, and EEG indicated enhanced alpha coherence and reduced interhemispheric asymmetry. Functional and quality of life scores improved significantly in the iTBS group compared to sham.
Conclusions. iTBS combined with SLT significantly improves language recovery and cortical excitability in subacute post-stroke Broca’s aphasia.
Keywords: Broca’s aphasia, intermittent theta burst stimulation, post-stroke rehabilitation, neuroplasticity, randomized controlled trial.
For citation: Ortikov A.P., Kilichev I.A., Yusupov A.U., Shamuratova G.B., Shodmonova A.A., Qarshiboyeva N.I., Palvanov R.O. Efficacy of intermittent theta burst stimulation in post-stroke Broca’s aphasia: a randomized controlled trial with multimodal neurophysiological assessment. Clinical review for general practice. 2026; 7 (1): 63–71 (In Russ.). DOI: 10.47407/kr2026.7.1.00756
Афазия является распространенным и тяжелым последствием ишемического инсульта, встречающимся приблизительно у 30–40% пациентов, выживших после инсульта [1]. Среди них около 20% продолжают испытывать умеренные или выраженные речевые нарушения через год после дебюта заболевания, что приводит к стойким коммуникативным ограничениям и социальной изоляции [2, 3]. В странах с низким и средним уровнем дохода, включая государства Центральной Азии, распространенность данного состояния, вероятно, выше вследствие ограниченного доступа к ранней реабилитации и специализированным нейрореабилитационным центрам [4].
Постинсультная афазия обычно развивается вследствие инфаркта или геморрагического поражения речедоминантных корковых областей, преимущественно в левой перисильвиевой зоне [5]. Среди различных типов афазии афазия Брока характеризуется нарушением беглости речи при сохраненном понимании и нарушении грамматического построения высказываний [6]. Эти речевые дефициты не только существенно ограничивают коммуникативные возможности пациентов, но и ассоциируются с неблагоприятным функциональным восстановлением, снижением качества жизни и увеличением потребности в медицинской помощи [7]. Несмотря на то что логопедическая и речевая терапия остается основным методом лечения постинсультной афазии, ее эффективность зачастую ограничивается выраженностью речевых нарушений, утомляемостью пациентов и сниженным нейропластическим потенциалом в хронической фазе заболевания [8].
В последние годы методы нейромодуляции рассматриваются как перспективное дополнение к речевой терапии, направленное на усиление восстановления путем содействия корковой реорганизации. Транскраниальная магнитная стимуляция (TMC) – неинвазивная методика стимуляции мозга, использующая электромагнитные импульсы для временной модуляции нейронной активности в целевых зонах коры [9]. В зависимости от частоты и параметров стимуляции TMC может оказывать как возбуждающее, так и тормозящее воздействие на корковую возбудимость. Показано, что низкочастотная ТМС (≤1 Гц), применяемая к правому полушарию, способна подавлять дезадаптивное межполушарное торможение, тогда как высокочастотные протоколы (≥5 Гц), направленные на левую перилезионную кору, могут способствовать функциональной активации [10, 11].
Среди современных парадигм TMC особое внимание привлекает интермиттирующая тета-вспышками стимуляция (intermittent theta burst stimulation, iTBS) благодаря своей способности вызывать эффекты, сходные с долговременной потенциацией (ДВП), в сжатые временные интервалы [12]. Благодаря эффективности в модуляции корковой возбудимости iTBS рассматривается как целенаправленное вмешательство при постинсультной афазии, особенно при воздействии на левую нижнюю лобную извилину (НЛИ). Данная область, соответствующая зоне Брока, играет ключевую роль в инициации речи, артикуляции и синтаксической обработке и часто поражается при нефлюентных формах афазии. Ранее проведенные исследования показали, что возбуждающая iTBS или высокочастотная ритмическая транскраниальная магнитная стимуляция (рТМС), применяемая к левой НЛИ, способствует значительным улучшениям в назывании, беглости речи и понимании языка [13, 14].
Данные нейровизуализации дополнительно подтверждают значение НЛИ в процессах восстановления, поскольку повышение активности этой области положительно коррелирует с улучшением речевых показателей. Методика iTBS включает короткие серии высокочастотных стимулов (50 Гц), подаваемых с тета-диапазонными интервалами (5 Гц), что имитирует эндогенные тета-ритмы гиппокампа, ассоциированные с обучением и синаптической пластичностью [15]. Такая паттернированная стимуляция, как предполагается, усиливает синаптическую эффективность и модулирует функциональную связность как локальных, так и распределенных языковых сетей. В отличие от традиционной рТМС, протоколы iTBS имеют меньшую продолжительность (обычно 3–5 мин на сеанс) и лучше переносятся пациентами с постинсультной утомляемостью или когнитивными ограничениями.
Несмотря на теоретические преимущества iTBS, число клинических исследований, оценивающих ее эффективность при афазии, остается ограниченным и они характеризуются значительной вариабельностью в дизайне, отборе пациентов и используемых критериях исходов. Хотя некоторые работы демонстрируют выраженные улучшения речевых функций после применения iTBS, другие авторы сообщают лишь об умеренных либо несущественных результатах, что подчеркивает необходимость стандартизации протоколов и применения мультимодальных методов оценки [14, 16]. Кроме того, нейрофизиологические механизмы, лежащие в основе наблюдаемых улучшений, такие как изменения паттернов корковой активации или межполушарной функциональной связности, остаются недостаточно изученными и требуют дальнейших исследований с использованием методов функциональной магнитно-резонансной томографии (фМРТ) и электроэнцефалографии (ЭЭГ).
Цель исследования – оценить эффективность iTBS в сочетании с речевой терапией для улучшения речевых функций и нейрофизиологических показателей у пациентов с постинсультной афазией Брока.
Материалы и методы
Настоящее исследование было выполнено в формате рандомизированного двойного слепого плацебо-контролируемого клинического испытания с параллельным распределением групп. Исследование проводилось на кафедре неврологии Ургенчского филиала Ташкентской медицинской академии в период с 2022 по 2024 г. В исследование были включены 60 пациентов (мужчины и женщины) в возрасте от 30 до 70 лет с нефлюентной афазией, развившейся после ишемического инсульта. Участники были случайным образом распределены в соотношении 1:1 в группу активной iTBS или группу имитационной стимуляции с использованием сгенерированной компьютером последовательности рандомизации. Все пациенты проходили сеансы речевой терапии, проводимые сертифицированными логопедами. Терапия была стандартизирована на основе структурированного протокола, разработанного в соответствии с доказательными методами реабилитации афазии, включая фонологическое подсказывание, тренинг повторения и семантический анализ признаков. Сеансы речевой терапии проводились пять раз в неделю по 45 мин в течение 2 нед. Соблюдение протокола терапии контролировалось посредством ведения ежедневных журналов и контрольных листов терапевтов.
Критериями включения пациентов в исследование были: 1) кортикальный или подкорковый инфаркт левого полушария, подтвержденный данными МРТ или компьютерной томографии головного мозга; 2) афазия вследствие первого ишемического инсульта; 3) праворукость; 4) срок после инсульта от 2 нед до 6 мес; 5) сохраненная когнитивная функция – оценка по Краткой шкале оценки психического статуса (Mini-mental State Examination, MMSE) ≥24; 6) свободная речь до инсульта; 7) клинический диагноз постинсультной афазии, преимущественно афазии Брока, подтвержденный сертифицированным неврологом и логопедом; 8) отсутствие подтвержденных нейродегенеративных или тяжелых соматических заболеваний; 9) возраст от 30 до 70 лет.
Критериями исключения были: 1) афазия, вызванная другими заболеваниями (энцефалит, травма, отравление); 2) тяжелая депрессия; 3) беременность; 4) аллергическая реакция на мемантин; 5) тяжелые соматические заболевания: сердечная недостаточность III–IV класса по NYHA, неконтролируемый сахарный диабет, хроническая болезнь почек стадии IV и выше, тяжелая хроническая обструктивная болезнь легких или активное злокачественное новообразование, по поводу которого пациент получает системное лечение; 6) противопоказания к iTBS (кардиостимуляторы, металлические объекты, имплантированные в голову); 7) эпилепсия; 8) прием трициклических антидепрессантов или нейролептиков в течение последних 3 мес; 9) выраженная апраксия речи; 10) тяжелое нарушение понимания речи – оценка по шкале Western Aphasia Battery (WAB) ниже 4.
Этическое одобрение (№ 329/2022) было получено от институционального этического комитета, и все участники предоставили письменное информированное согласие перед включением в исследование. Исследование проводилось в соответствии с Хельсинкской декларацией.
Рандомизация и ослепление. Участники были случайным образом распределены в соотношении 1:1 в группу активной iTBS или группу имитационной стимуляции с использованием компьютерно-сгенерированной последовательности рандомизации. Сокрытие распределения обеспечивалось с помощью непрозрачных запечатанных конвертов. Все участники и специалисты, оценивавшие результаты, оставались ослепленными в отношении группового распределения на протяжении всего исследования.
Определение порога двигательной возбудимости в состоянии покоя
Порог двигательной возбудимости в состоянии покоя определялся индивидуально для каждого участника до начала первой сессии стимуляции. Поверхностные электроды электромиографии устанавливались над мышцей abductor pollicis brevis доминирующей руки. Порог двигательной возбудимости определялся с этой руки путем регистрации моторных вызванных потенциалов (МВП) в соответствии со стандартными процедурами TMC [12, 13, 17]. Такой подход был выбран из-за возможной вариабельности и ненадежности регистрации МВП с пораженного полушария у пациентов после инсульта. Одноимпульсная ТМС применялась над первичной моторной корой с использованием стимулятора DuoMAG XT (Deymed, Чешская Республика), оснащенного 70-миллиметровой катушкой в форме восьмерки. «Двигательная горячая точка» определялась как участок кожи головы, при стимуляции которого вызывались наибольшие и наиболее стабильные МВП в целевой мышце. Порог моторного ответа определялся как минимальная интенсивность стимуляции, вызывавшая МВП амплитудой не менее 50 мкВ в 5 из 10 последовательных испытаний при полном расслаблении мышцы. Этот порог использовался в качестве эталонного значения для определения индивидуальной интенсивности стимуляции на протяжении всего курса лечения.
Протокол стимуляции
Активная группа iTBS. Участники группы активной стимуляции получали iTBS, направленную на левую НЛИ, соответствующую области Брока. Место стимуляции определялось в соответствии с международной системой ЭЭГ 10–20, с ориентацией на позицию электрода F7. Стимуляция проводилась с использованием устройства DuoMAG XT (Deymed, Чешская Республика) с катушкой в форме восьмерки диаметром 70 мм, расположенной тангенциально к поверхности головы под углом 45° к сагиттальной плоскости. Протокол iTBS соответствовал стандартной схеме: тройные серии импульсов с частотой 50 Гц повторялись каждые 200 мс (т.е. 5 Гц) и подавались в виде двухсекундных поездов каждые 10 с. Каждая сессия включала в общей сложности 600 импульсов. Интенсивность стимуляции устанавливалась на уровне 80% от индивидуального порога двигательной возбудимости. Продолжительность одной сессии составляла около 3 мин, процедуры проводились один раз в день, пять раз в неделю, на протяжении 2 нед (всего 10 сессий). Все участники одновременно проходили курс речевой терапии в течение того же двухнедельного периода вмешательства.
Имитационная группа. Участники группы имитационной стимуляции проходили аналогичные процедуры, включая позиционирование катушки и продолжительность сеанса, с использованием той же системы DuoMAG XT. Однако применялась либо имитационная катушка, либо неэффективная ориентация активной катушки, что предотвращало корковую стимуляцию при сохранении слуховых и тактильных ощущений. Это обеспечивало эффективное ослепление участников и исследователей на протяжении всего периода исследования. Участники имитационной группы также проходили курс речевой терапии с той же частотой и по тому же протоколу, что и в группе активной стимуляции, для обеспечения сопоставимости данных.
Нейрофизиологическая оценка
ЭЭГ в состоянии покоя регистрировалась с использованием 64-канальной системы BrainAmp (монтаж 10–20, частота дискретизации 500 Гц, глаза закрыты, продолжительность записи – 5 мин). Данные проходили полосовую фильтрацию (1–45 Гц), очистку с помощью независимого компонентного анализа (ICA) и повторное приведение к среднему референтному электроду. Рассчитывалась когерентность в альфа-диапазоне (8–12 Гц) между левыми фронтотемпоральными областями (например, F7–T3), а также индексы межполушарной асимметрии. фМРТ в состоянии покоя выполнялась на сканере 3T GE Discovery MR750 (последовательность EPI; TR=2000 мс; TE=30 мс; размер вокселя = 3×3×3 мм³; 210 томов; 7 мин). Во время сканирования участники фиксировали взгляд на центральном кресте при открытых глазах. Предобработка и анализ данных выполнялись с использованием пакета CONN toolbox (v20b) и SPM12. Этапы включали коррекцию движений, нормализацию в пространстве MNI, сглаживание (6 мм FWHM) и временную фильтрацию (0,008–0,09 Гц). Возмущающие переменные (белое вещество, спинномозговая жидкость, движения) регрессировались. Функциональная связность анализировалась по корреляциям ROI–ROI между языковыми областями: левой НЛИ, задней верхней височной извилиной и дополнительной моторной зоной. Корреляции, преобразованные методом Фишера в z-показатели, сравнивались до и после вмешательства между группами; различия считались статистически значимыми при p<0,05 с поправкой FDR.
Показатели эффективности
Основным исходом являлось улучшение речевой функции, оцениваемое с помощью шкалы WAB. Сводные показатели, включая коэффициент афазии и его субкомпоненты (спонтанная речь, слуховое восприятие, повторение и называние), регистрировались на исходном уровне, после вмешательства, а также во время последующих контрольных оценок через 1, 3 и 6 мес. Вторичные исходы включали изменения нейрофизиологической активности, измеренные с помощью фМРТ и ЭЭГ в состоянии покоя. Эти методы использовались для оценки корковой реорганизации и межполушарной связности. Дополнительно проводилась оценка индекса Бартел для повседневной активности, опросника SF-36 для общей оценки состояния здоровья и SAQOL-39 (Stroke and Aphasia Quality of Life Scale) для оценки качества жизни, связанного с коммуникативной функцией, на исходном уровне и через 3 мес наблюдения. Шкала SF-36 использовалась для оценки общего качества жизни, связанного со здоровьем. Она включает восемь субдоменов (например, физическое функционирование, эмоциональное благополучие, жизненная активность), каждый из которых оценивается по шкале от 0 до 100. Более высокие баллы отражают лучшее субъективное состояние здоровья и функциональные возможности. Опросник SAQOL-39 является валидированным инструментом, специально разработанным для лиц с афазией. Он включает пункты, охватывающие коммуникативные навыки, психосоциальное благополучие, уровень энергии и повседневное функционирование. Ответы оцениваются по шкале типа Лайкерта, при этом более высокие суммарные и субшкальные баллы указывают на лучшее качество жизни и более высокую степень функциональной коммуникации.
Статистический анализ
Размер выборки был рассчитан с использованием программы G*Power 3.1 для двухвыборочного t-теста при допущении большого размера эффекта (d=0,8), уровне значимости α=0,05, статистической мощности 0,80 и стандартном отклонении 9,5 на основании данных предыдущих исследований. Минимально необходимое количество участников составляло 52, а целевое значение было увеличено до 60 для учета возможных потерь выборки. Исходные демографические и клинические данные были обобщены с помощью описательной статистики. Внутригрупповые сравнения между временными точками проводились с использованием дисперсионного анализа с повторными измерениями (ANOVA). Межгрупповые различия оценивались с помощью t-критерия Стьюдента или критерия Манна–Уитни в зависимости от распределения данных. Корреляционные связи между поведенческими и нейрофизиологическими показателями анализировались с использованием коэффициентов корреляции Пирсона или Спирмена. Статистическая значимость определялась при уровне p<0,05, а размер эффекта указывался по показателю d Коэна, где это было возможно. Все анализы выполнялись с использованием программного обеспечения SPSS версии 26.0 или R версии 4.2.2.
Результаты
Из 75 обследованных пациентов 60 соответствовали критериям включения и были рандомизированы поровну в группу активной iTBS (n=30) и группу имитационной стимуляции (n=30). Все участники завершили курс из 10 сеансов вмешательства. Контрольные оценки через 1, 3 и 6 мес были выполнены у 27 участников в каждой группе (уровень удержания – 90%). Серьезных нежелательных явлений зафиксировано не было. Анализ проводился по принципу намерения лечить; отсутствующие значения последующих наблюдений обрабатывались методом переноса последнего наблюдения.
Исходные характеристики
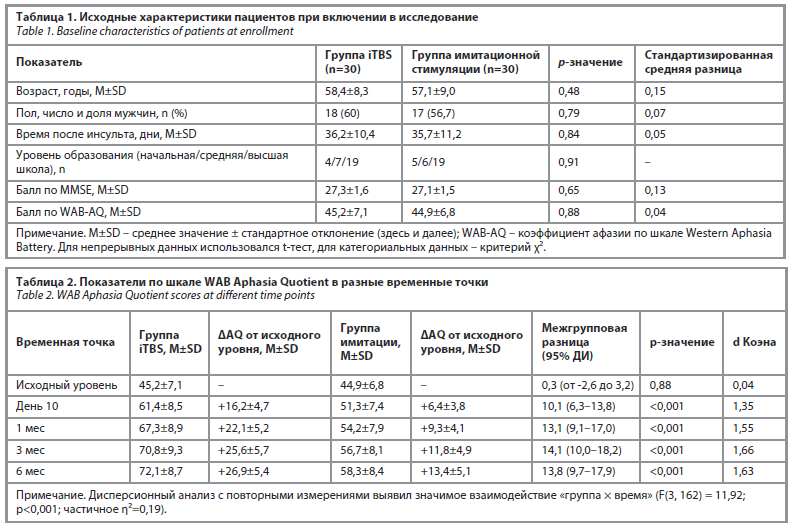
Демографические и клинические показатели были хорошо сбалансированы между группами (табл. 1). Статистически значимых различий по возрасту, полу, уровню образования, баллам по шкале MMSE или коэффициенту афазии (Aphasia Quotient, AQ) по WAB не выявлено (все p>0,05). Среднее время, прошедшее с момента инсульта, составило 36,0±10,8 дня в обеих группах. Всего 49 (81,7%) пациентов были включены в исследование в ранний подострый период (<90 дней), а 11 (18,3%) пациентов – в поздний подострый период. Стандартизированные средние различия для всех переменных составляли <0,2, что указывает на отсутствие исходного дисбаланса. Предпосылки нормальности и гомоскедастичности были проверены с использованием критериев Шапиро–Уилка и Левена соответственно (p>0,1 для всех случаев). Радиологический анализ данных визуализации показал, что локализация очагов поражения была сопоставима между группами. В обеих группах – iTBS и имитационной – большинство поражений затрагивали левую перисильвиеву кору, преимущественно НЛИ, островковую кору и переднюю часть верхней височной извилины. Объем поражений варьировал, но, как правило, не затрагивал задние речевые области, что соответствует диагностике нефлюентной формы афазии (афазии Брока).
Речевая продуктивность
Показатели коэффициента афазии (AQ) по шкале WAB значительно улучшались в обеих группах с течением времени, однако прирост был достоверно выше в группе iTBS на всех этапах после исходного измерения (табл. 2). В группе iTBS средний балл AQ увеличился с 45,2±7,1 на исходном уровне до 61,4±8,5 на 10-й день (d=1,98), с последующим повышением через 1 мес (67,3±8,9; d=2,49), 3 мес (70,8±9,3; d=2,81) и 6 мес (72,1±8,7; d=2,88). В группе имитационной стимуляции улучшения были менее выраженными: с 44,9±6,8 на исходном уровне до 51,3±7,4 на 10-й день (d=0,91) и 58,3±8,4 через 6 мес (d=1,54). Дисперсионный анализ с повторными измерениями (с поправкой Гринхауса–Гейссера, ε=0,84) выявил значимое взаимодействие «группа × время» (F(2,52, 151,3) = 11,92; p<0,001; η²=0,19). Межгрупповые различия превышали минимально клинически значимую разницу в 5 баллов AQ во всех временных точках.
Нейрофизиологические изменения
Анализ функциональной МРТ в состоянии покоя показал увеличение корреляций BOLD-сигнала между ROI-областями в группе iTBS после вмешательства, особенно в левой НЛИ. Функциональная связность дополнительно исследовалась с использованием анализа ROI-to-ROI корреляций между ключевыми левополушарными речевыми областями, включая НЛИ, дополнительную моторную зону и верхнюю височную извилину. Среднее процентное изменение сигнала в области НЛИ увеличилось с исходного уровня до значений в постлечебном периоде на 1,83±0,42% в группе iTBS по сравнению с увеличением на 0,94±0,35% в группе имитации (межгрупповая разница – 0,89%; 95% ДИ 0,65–1,13; p<0,001; d Коэна=2,18).
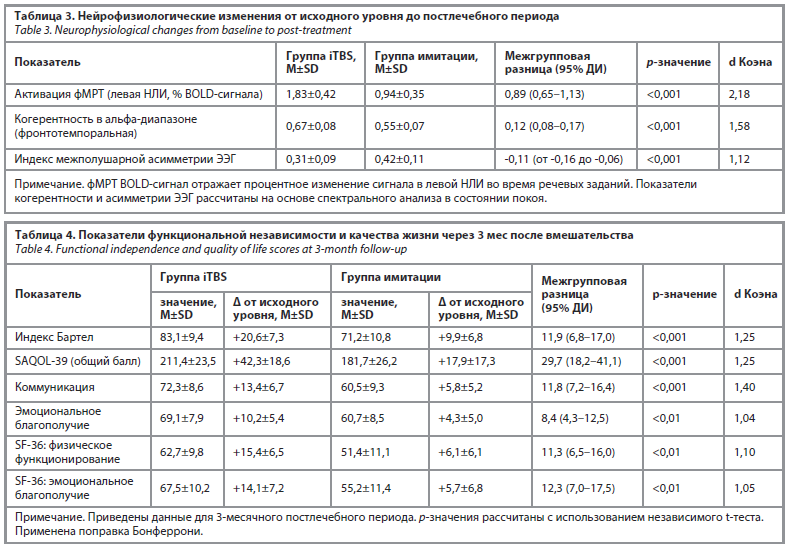
Анализ ЭЭГ в состоянии покоя выявил значительное повышение когерентности в альфа-диапазоне между фронтотемпоральными областями в группе iTBS (0,67±0,08) по сравнению с группой имитации (0,55±0,07; p<0,001; d=1,58). Кроме того, индексы межполушарной асимметрии значительно снизились в группе iTBS (0,31±0,09 против 0,42±0,11; p<0,001; d=1,12; табл. 3).
Функциональный статус и качество жизни
Через 3 мес после вмешательства участники группы iTBS продемонстрировали значительно более высокие показатели функциональной независимости и качества жизни по всем шкалам (табл. 4). Баллы по индексу Бартел увеличились в среднем на 20,6 пункта (83,1±9,4 против 62,5±10,2 на исходном уровне; p<0,001; d=2,09). Общий балл по шкале SAQOL-39 повысился на 42,3 пункта (211,4±23,5 против 169,1±21,8; p<0,001), при этом наибольшие улучшения отмечались в доменах «Коммуникация» (72,3±8,6) и «Эмоциональное благополучие» (69,1±7,9; в обоих случаях p<0,001). Показатели по субшкалам SF-36, отражающим физическое (62,7±9,8) и эмоциональное благополучие (67,5±10,2), также были достоверно выше в группе iTBS по сравнению с контрольной группой (p<0,01; d>1,0 для всех доменов; см. табл. 4). Вмешательство iTBS в целом хорошо переносилось. Легкие преходящие головные боли отмечались у четырех участников группы iTBS и у двух участников группы имитации, как правило, проходя самостоятельно без медицинского вмешательства. Серьезных нежелательных явлений не наблюдалось ни в одной из групп, и ни один участник не прекратил участие в исследовании из-за побочных эффектов.
Обсуждение
Настоящее рандомизированное двойное слепое плацебо-контролируемое исследование демонстрирует, что применение iTBS к левой НЛИ в сочетании с речевой терапией приводит к значительным и устойчивым улучшениям речевой функции, корковой активации и качества жизни у пациентов с постинсультной афазией Брока. Полученные результаты убедительно подтверждают эффективность нейромодулирующих методов как средства усиления восстановления речевых функций, особенно в подостром периоде реабилитации афазии.
Масштаб и устойчивость улучшения речевых функций, наблюдаемые в группе iTBS, согласуются с предыдущими исследованиями, указывающими на то, что возбуждающие протоколы TMC способны усиливать речевые способности за счет активации перилезионных областей. В исследовании J. Kindler и соавт. (2012) было показано, что применение iTBS к левой НЛИ значительно улучшало результаты называния у пациентов с хронической афазией [13]. Аналогично, J.B. Allendorfer и соавт. (2021) сообщили о поведенческих и нейровизуализационных улучшениях после применения самостоятельного протокола iTBS [14]. Наше исследование расширяет эти выводы благодаря использованию более крупной выборки, наличию контрольной группы с имитацией стимуляции и оценке долгосрочных эффектов до 6 мес после вмешательства. Кроме того, в отличие от многих предыдущих работ, в нашем исследовании применялась мультимодальная нейрофизиологическая оценка, что позволило подтвердить поведенческие улучшения объективными изменениями корковой активности.
Наблюдаемое увеличение показателей по шкале WAB Aphasia Quotient в группе iTBS было как статистически, так и клинически значимым. Средний прирост AQ примерно на 27 баллов через 6 мес превышает минимально клинически значимую разницу, описанную в литературе [18], и почти вдвое превышает улучшения, зафиксированные в группе имитации. Это подтверждает дополнительное преимущество iTBS по сравнению с одной лишь стандартной речевой терапией. В то время как N. Weiduschat и соавт. (2011) сообщили о положительных эффектах низкочастотной рТМС, применяемой к правой НЛИ [19], наше исследование показывает, что возбуждающая стимуляция левого полушария может быть еще более эффективной при применении на ранних этапах восстановления.
Результаты фМРТ, полученные в данном исследовании, показали повышение активации BOLD-сигнала в левой НЛИ и прилежащей перилезионной коре после применения iTBS. Это подтверждает гипотезу о том, что iTBS усиливает корковую возбудимость и способствует повторному вовлечению поврежденных языковых сетей. Кроме того, данные ЭЭГ в состоянии покоя продемонстрировали увеличение когерентности в альфа-диапазоне во фронтотемпоральных цепях и снижение межполушарной асимметрии – биомаркеров, часто связанных с функциональным восстановлением и синаптической реорганизацией. Эти эффекты согласуются с концепцией активность-зависимой нейропластичности, согласно которой стимуляционно-индуцированные механизмы, аналогичные ДВП, способствуют укреплению синаптических связей в перилезионных областях.
Предполагается, что стимуляция тета-вспышками, имитируя эндогенные тета-ритмы гиппокампа, более эффективно способствует пластическим процессам, чем традиционная рТМС [17]. Более того, доклинические исследования указывают, что iTBS может повышать экспрессию мозгового нейротрофического фактора (МНТФ) – ключевого модулятора синаптического восстановления и нейрогенеза [20]. Хотя уровень МНТФ напрямую не измерялся в данном исследовании, полученные нейрофизиологические данные косвенно подтверждают эту модель. Улучшенные поведенческие и нейрофизиологические результаты также свидетельствуют о том, что iTBS может способствовать восстановлению баланса при дезадаптивном межполушарном торможении – феномене, при котором интактное правое полушарие подавляет активность поврежденного левого через транскаллозальные пути [10]. Повышая возбудимость левой НЛИ, iTBS, вероятно, противодействует этому ингибирующему влиянию, облегчая более эффективную обработку речи.
Помимо языковых улучшений, участники группы iTBS продемонстрировали более высокие показатели по шкалам Бартел, SAQOL-39 и SF-36. Это указывает на то, что нейромодуляция способствует не только восстановлению речевых функций, но и повышению общей функциональной независимости и психосоциального благополучия. Данный эффект особенно важен в условиях ограниченных ресурсов, когда возможностей для длительной речевой терапии может быть недостаточно. Полученные результаты подтверждают целесообразность интеграции нейромодуляционных методов в протоколы ранней реабилитации афазии с целью ускорения функционального восстановления.
Время проведения нейромодуляции после инсульта все чаще рассматривается как критически важный фактор, определяющий эффективность лечения. В настоящем исследовании, хотя все участники были включены в подострый период (от 2 нед до 6 мес после инсульта), большинство из них получили лечение в первые 8 нед – промежуток, соответствующий ранней подострой фазе. Этот период характеризуется повышенной нейропластичностью, увеличенной синаптической восприимчивостью и динамической перестройкой нейронных сетей, что может повышать чувствительность к вмешательствам, таким как iTBS. Авторы предыдущих исследований (например, C. Grefkes и G.R. Fink, 2014) указывали, что стимуляция, проводимая на ранних этапах восстановления, может более эффективно использовать эндогенные механизмы реорганизации по сравнению с вмешательствами, начатыми на поздних стадиях [21]. Более того, мишени стимуляции могут требовать адаптации со временем: если на раннем этапе модуляция левой НЛИ способствует прямой реактивации основных языковых сетей, то на более поздних этапах может оказаться более эффективной стратегия, направленная на активацию компенсаторных сетей. Благоприятные результаты, полученные в настоящем исследовании, согласуются с этой концепцией; это позволяет предположить, что раннее применение iTBS после инсульта может представлять собой оптимальное терапевтическое окно для стимулирования восстановления речи. Эти выводы подчеркивают важность стратифицированного дизайна клинических исследований и персонализированных протоколов стимуляции, основанных на данных нейровизуализации и исходных профилях функциональной связности.
Нейромодулирующие эффекты iTBS, наблюдаемые в данном исследовании, также согласуются с результатами, полученными при использовании других методов неинвазивной стимуляции мозга. Например, высокочастотная рТМС, направленная на лобные области левого полушария, продемонстрировала способность улучшать речевые функции за счет реактивации корковых зон, тогда как анодная транскраниальная стимуляция постоянным током (tDCS), воздействующая на аналогичные нейронные сети, приводила к повышению эффективности называния и модуляции функциональной связности в состоянии покоя [11, 22, 23]. Эти параллельные данные подтверждают существование общего механизма пластичности, сходного с ДВП, и дополнительно обосновывают целесообразность применения возбуждающих стратегий стимуляции в реабилитации афазии.
Несмотря на свои сильные стороны, данное исследование имеет несколько ограничений. Во-первых, размер выборки, хотя и достаточный для выявления статистически значимых эффектов, остается относительно небольшим и ограничен рамками одного центра. В будущем необходимы многоцентровые исследования с участием более крупных и разнородных популяций для повышения обобщаемости результатов. Во-вторых, исследование было сосредоточено исключительно на афазии Брока, поэтому полученные данные не могут быть напрямую экстраполированы на другие подтипы, такие как афазия Вернике или глобальная афазия.
В-третьих, хотя в исследовании для оценки корковых механизмов использовались методы нейровизуализации и ЭЭГ, прямые биомаркеры, такие как уровень МНТФ в сыворотке крови или трактография, могли бы предоставить более детализированную информацию о состоянии белого вещества и процессах синаптической перестройки. Кроме того, пациенты не были стратифицированы по локализации, размеру очага поражения или времени, прошедшему с момента инсульта в пределах допустимого диапазона. Эти переменные могут существенно влиять на ответ на нейромодуляцию и должны быть изучены в будущих исследованиях. Наконец, хотя протокол имитационной стимуляции обеспечивал сохранение слуховых и тактильных ощущений, нельзя полностью исключить возможность влияния эффекта плацебо на поведенческие результаты.
Опираясь на полученные результаты, будущие исследования должны быть направлены на определение оптимальных стратегий дозирования, включая количество сеансов, частоту применения и временные рамки после инсульта. Сочетание iTBS с интенсивной речевой терапией или фармакологическими средствами (например, холинергическими модуляторами, миметиками МНТФ) может дополнительно способствовать восстановлению функций. Кроме того, изучение предиктивных биомаркеров, таких как исходная функциональная связность по данным ЭЭГ или объем поражения, может помочь выявить пациентов, которые с наибольшей вероятностью получат пользу от iTBS. Расширение протоколов для включения других вариантов афазии и пациентов в хронической фазе также представляется перспективным направлением.
Заключение
Настоящее рандомизированное плацебо-контролируемое исследование демонстрирует, что iTBS, применяемая в сочетании с речевой терапией, способствует улучшению восстановления речевых функций у пациентов с подострой постинсультной афазией Брока. Вмешательство привело к стойким улучшениям речевой продуктивности, функциональной независимости и качества жизни, которые сопровождаются изменениями корковой активности и связности, подтвержденными данными фМРТ и ЭЭГ. Полученные результаты подтверждают эффективность и хорошую переносимость iTBS как нейромодулирующего метода реабилитации афазии. Исследование также подчеркивает важность раннего вмешательства и комплексной мультимодальной оценки для оптимизации терапевтических исходов. Необходимы дальнейшие крупномасштабные многоцентровые исследования для подтверждения данных результатов, уточнения протоколов стимуляции и оценки их применимости при различных подтипах афазии и стадиях восстановления.
Конфликт интересов. Авторы заявляют об отсутствии потенциального конфликта интересов.
Conflict of interest. The authors have no potential conflicts of interest to disclose.
Финансирование. Авторы не получали целевого финансирования для проведения данного исследования.
Funding. The authors received no specific funding for this work.
Благодарности. Авторы выражают искреннюю признательность сотрудникам кафедры неврологии Ургенчского филиала Ташкентской медицинской академии за постоянную поддержку и помощь в ходе реализации данного исследования. Особая благодарность выражается логопедам и специалистам по клинической нейрофизиологии, чьи компетентность и преданность делу были решающими для успешного проведения вмешательства и сбора данных. Авторы также благодарны всем участникам исследования и их семьям за проявленное терпение, сотрудничество и доверие.
Acknowledgements. The authors would like to express their sincere gratitude to the staff of the Department of Neurology at the Urgench Branch of the Tashkent Medical Academy for their continuous support and assistance during the implementation of this study. Special thanks go to the speech-language therapists and clinical neurophysiology technicians whose expertise and dedication were essential to the successful completion of the intervention and data collection. We are also grateful to all study participants and their families for their time, cooperation, and trust.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Ортиков Акбар Пирнапаcович — ассистент каф. патологической анатомии, Ургенчский филиал Ташкентской медицинской академии. E-mail: ortiqovakbar1977@gmail.com; ORCID: 0009-0004-4658-2189
Akbar P. Ortikov – Assistant, Urgench branch of Tashkent Medical Academy. E-mail: ortiqovakbar1977@gmail.com; ORCID: 0009-0004-4658-2189
Киличев Ибодулла Абдуллаевич – д-р мед. наук, проф. каф. неврологии, медицинской психологии и психотерапии,
Ургенчский филиал Ташкентской медицинской академии. E-mail: qlichev@mail.ru; ORCID: 0009-0009-3219-5539
Ibodulla A. Kilichev – Dr. Sci. (Med.), Prof., Urgench branch of Tashkent Medical Academy. E-mail: qlichev@mail.ru; ORCID: 0009-0009-3219-5539
Юсупов Адхам Улугбекович – ассистент каф. неврологии, медицинской психологии и психотерапии, Ургенчский филиал Ташкентской медицинской академии.
E-mail: adham.yusupov.95@mail.ru; ORCID: 0009-0009-9675-5419
Adkham U. Yusupov – Assistant, Urgench branch of Tashkent Medical Academy. E-mail: adham.yusupov.95@mail.ru; ORCID: 0009-0009-9675-5419
Шамуратова Гульнора Бахтияровна – канд. мед. наук, доц. каф. естественных наук, Университет Мамуна. E-mail: gulnorashаmurаtovа8@gmail.com; ORCID: 0009-0002-8557-040X
Gulnora B. Shamuratova – Cand. Sci. (Med.), Assoc. Prof., Mamun University. E-mail: gulnorashаmurаtovа8@gmail.com; ORCID: 0009-0002-8557-040X
Шодмонова Азиза Адизовна – ассистент каф. гематологии и клинической лабораторной диагностики, Бухарский государственный медицинский институт им. Абу Али ибн Сино. E-mail: aziza.shodmonova@icloud.com; ORCID: 0009-0005-7544-3214
Aziza A. Shodmonova – Assistant, Abu Ali ibn Sino Bukhara State Medical Institute. E-mail: aziza.shodmonova@icloud.com; ORCID: 0009-0005-7544-3214
Каршибоева Наргиза Иброхимовна – аспирант каф. неврологии и медицинской психологии, Ташкентский государственный медицинский институт. E-mail: doc.ibrohimovanargiza@gmail.com; ORCID: 0009-0007-5488-893X
Nargiza I. Qarshiboyeva – Graduate Student, Tashkent State Medical Institute. E-mail: doc.ibrohimovanargiza@gmail.com;
ORCID: 009-007-5488-893X
Палванов Равшан Отамуратович – ассистент каф. неврологии, медицинской психологии и психотерапии, Ургенчский филиал Ташкентской медицинской академии. E-mail: ravshanpolvanov@gmail.com; ORCID: 0000-0002-6491-208X
Ravshan O. Palvanov – Assistant, Urgench branch of Tashkent Medical Academy. E-mail: ravshanpolvanov@gmail.com; ORCID: 0000-0002-6491-208X
Поступила в редакцию: 20.10.2025
Поступила после рецензирования: 01.11.2025
Принята к публикации: 06.11.2025
Received: 20.10.2025
Revised: 01.11.2025
Accepted: 06.11.2025
Клинический разбор в общей медицине №01 2026
Эффективность интермиттирующей тета-вспышками стимуляции при афазии Брока после инсульта: рандомизированное контролируемое исследование с мультимодальной нейрофизиологической оценкой
Номера страниц в выпуске:63-71
Аннотация
Афазия Брока – частое и тяжелое состояние после инсульта, нередко резистентное к логопедической терапии (ЛТ); при этом интермиттирующая тета-вспышками стимуляция (iTBS) рассматривается как перспективный нейромодуляционный подход, направленный на усиление нейропластичности и восстановление языковых функций.
Цель. Оценить клиническую эффективность и нейрофизиологические эффекты iTBS в сочетании с ЛТ у пациентов с подострой постинсультной афазией Брока.
Материалы и методы. В этом рандомизированном двойном слепом плацебо-контролируемом исследовании приняли участие
60 пациентов с афазией Брока, которые получали активную iTBS над левой нижнелобной извилиной (НЛИ) или псевдостимуляцию в сочетании с двухнедельным стандартным курсом ЛТ. Языковые функции оценивали по шкале Western Aphasia Battery (WAB) в сочетании с нейровизуализационными и электроэнцефалографическими показателями, показателями функциональной независимости и шкалами качества жизни на исходном уровне, после лечения, а также через 1, 3 и 6 мес.
Результаты. Группа iTBS продемонстрировала значительно больший прирост по индексу афазии WAB (p<0,001; d=1,63). По данным функциональной магнитно-резонансной томографии наблюдалось повышение BOLD-активности в левой НЛИ, а электроэнцефалография выявила усиление альфа-согласованности и снижение межполушарной асимметрии. Показатели функциональной независимости и качества жизни в группе iTBS значительно повысились по сравнению с группой плацебо.
Заключение. iTBS в сочетании с ЛТ существенно улучшает восстановление языковых функций и корковую возбудимость при подострой постинсультной афазии Брока.
Ключевые слова: афазия Брока, интермиттирующая тета-вспышками стимуляция, постинсультная реабилитация, нейропластичность, рандомизированное контролируемое исследование.
Для цитирования: Ортиков А.П., Киличев И.А., Юсупов А.У., Шамуратова Г.Б., Шодмонова А.А., Каршибоева Н.И., Палванов Р.О. Эффективность интермиттирующей тета-вспышками стимуляции при афазии Брока после инсульта: рандомизированное контролируемое исследование с мультимодальной нейрофизиологической оценкой. Клинический разбор в общей медицине. 2026; 7 (1): 63–71.
DOI: 10.47407/kr2026.7.1.00756
Афазия Брока – частое и тяжелое состояние после инсульта, нередко резистентное к логопедической терапии (ЛТ); при этом интермиттирующая тета-вспышками стимуляция (iTBS) рассматривается как перспективный нейромодуляционный подход, направленный на усиление нейропластичности и восстановление языковых функций.
Цель. Оценить клиническую эффективность и нейрофизиологические эффекты iTBS в сочетании с ЛТ у пациентов с подострой постинсультной афазией Брока.
Материалы и методы. В этом рандомизированном двойном слепом плацебо-контролируемом исследовании приняли участие
60 пациентов с афазией Брока, которые получали активную iTBS над левой нижнелобной извилиной (НЛИ) или псевдостимуляцию в сочетании с двухнедельным стандартным курсом ЛТ. Языковые функции оценивали по шкале Western Aphasia Battery (WAB) в сочетании с нейровизуализационными и электроэнцефалографическими показателями, показателями функциональной независимости и шкалами качества жизни на исходном уровне, после лечения, а также через 1, 3 и 6 мес.
Результаты. Группа iTBS продемонстрировала значительно больший прирост по индексу афазии WAB (p<0,001; d=1,63). По данным функциональной магнитно-резонансной томографии наблюдалось повышение BOLD-активности в левой НЛИ, а электроэнцефалография выявила усиление альфа-согласованности и снижение межполушарной асимметрии. Показатели функциональной независимости и качества жизни в группе iTBS значительно повысились по сравнению с группой плацебо.
Заключение. iTBS в сочетании с ЛТ существенно улучшает восстановление языковых функций и корковую возбудимость при подострой постинсультной афазии Брока.
Ключевые слова: афазия Брока, интермиттирующая тета-вспышками стимуляция, постинсультная реабилитация, нейропластичность, рандомизированное контролируемое исследование.
Для цитирования: Ортиков А.П., Киличев И.А., Юсупов А.У., Шамуратова Г.Б., Шодмонова А.А., Каршибоева Н.И., Палванов Р.О. Эффективность интермиттирующей тета-вспышками стимуляции при афазии Брока после инсульта: рандомизированное контролируемое исследование с мультимодальной нейрофизиологической оценкой. Клинический разбор в общей медицине. 2026; 7 (1): 63–71.
DOI: 10.47407/kr2026.7.1.00756
Efficacy of intermittent theta burst stimulation in post-stroke Broca’s aphasia: a randomized controlled trial with multimodal neurophysiological assessmentt
Akbar P. Ortikov1, Ibodulla A. Kilichev1, Adkham U. Yusupov1, Gulnora B. Shamuratova2,Aziza A. Shodmonova3, Nargiza I. Qarshiboyeva4, Ravshan O. Palvanov1
1 Urgench branch of Tashkent Medical Academy, Urgench, Uzbekistan;
2 Mamun University, Urgench, Uzbekistan;
3 Abu Ali ibn Sino Bukhara State Medical Institute, Bukhara, Uzbekistan;
4 Tashkent State Medical Institute, Urgench, Uzbekistan
ortiqovakbar1977@gmail.com
Abstract
Post-stroke Broca’s aphasia is a common and disabling condition, often resistant to conventional speech and language therapy (SLT). Intermittent theta burst stimulation (iTBS) is a neuromodulation technique with potential to promote neuroplasticity and improve language outcomes.
Aim. To assess the clinical efficacy and neurophysiological effects of iTBS combined with SLT in patients with subacute post-stroke Broca’s aphasia.
Materials and methods. In this randomized double-blind sham-controlled trial, 60 patients with subacute post-stroke Broca’s aphasia received active iTBS over the left inferior frontal gyrus (IFG) or sham stimulation alongside two weeks of standardized SLT. Language outcomes were assessed using the Western Aphasia Battery (WAB), alongside neuroimaging markers of cortical activation, EEG connectivity indices, functional independence (Barthel Index), and quality-of-life scales. Assessments were conducted at baseline, post-treatment, and at 1, 3, and 6 months.
Results. The iTBS group showed significantly greater gains in WAB Aphasia Quotient (p<0.001; d=1.63). fMRI revealed increased BOLD activity in the left IFG, and EEG indicated enhanced alpha coherence and reduced interhemispheric asymmetry. Functional and quality of life scores improved significantly in the iTBS group compared to sham.
Conclusions. iTBS combined with SLT significantly improves language recovery and cortical excitability in subacute post-stroke Broca’s aphasia.
Keywords: Broca’s aphasia, intermittent theta burst stimulation, post-stroke rehabilitation, neuroplasticity, randomized controlled trial.
For citation: Ortikov A.P., Kilichev I.A., Yusupov A.U., Shamuratova G.B., Shodmonova A.A., Qarshiboyeva N.I., Palvanov R.O. Efficacy of intermittent theta burst stimulation in post-stroke Broca’s aphasia: a randomized controlled trial with multimodal neurophysiological assessment. Clinical review for general practice. 2026; 7 (1): 63–71 (In Russ.). DOI: 10.47407/kr2026.7.1.00756
Афазия является распространенным и тяжелым последствием ишемического инсульта, встречающимся приблизительно у 30–40% пациентов, выживших после инсульта [1]. Среди них около 20% продолжают испытывать умеренные или выраженные речевые нарушения через год после дебюта заболевания, что приводит к стойким коммуникативным ограничениям и социальной изоляции [2, 3]. В странах с низким и средним уровнем дохода, включая государства Центральной Азии, распространенность данного состояния, вероятно, выше вследствие ограниченного доступа к ранней реабилитации и специализированным нейрореабилитационным центрам [4].
Постинсультная афазия обычно развивается вследствие инфаркта или геморрагического поражения речедоминантных корковых областей, преимущественно в левой перисильвиевой зоне [5]. Среди различных типов афазии афазия Брока характеризуется нарушением беглости речи при сохраненном понимании и нарушении грамматического построения высказываний [6]. Эти речевые дефициты не только существенно ограничивают коммуникативные возможности пациентов, но и ассоциируются с неблагоприятным функциональным восстановлением, снижением качества жизни и увеличением потребности в медицинской помощи [7]. Несмотря на то что логопедическая и речевая терапия остается основным методом лечения постинсультной афазии, ее эффективность зачастую ограничивается выраженностью речевых нарушений, утомляемостью пациентов и сниженным нейропластическим потенциалом в хронической фазе заболевания [8].
В последние годы методы нейромодуляции рассматриваются как перспективное дополнение к речевой терапии, направленное на усиление восстановления путем содействия корковой реорганизации. Транскраниальная магнитная стимуляция (TMC) – неинвазивная методика стимуляции мозга, использующая электромагнитные импульсы для временной модуляции нейронной активности в целевых зонах коры [9]. В зависимости от частоты и параметров стимуляции TMC может оказывать как возбуждающее, так и тормозящее воздействие на корковую возбудимость. Показано, что низкочастотная ТМС (≤1 Гц), применяемая к правому полушарию, способна подавлять дезадаптивное межполушарное торможение, тогда как высокочастотные протоколы (≥5 Гц), направленные на левую перилезионную кору, могут способствовать функциональной активации [10, 11].
Среди современных парадигм TMC особое внимание привлекает интермиттирующая тета-вспышками стимуляция (intermittent theta burst stimulation, iTBS) благодаря своей способности вызывать эффекты, сходные с долговременной потенциацией (ДВП), в сжатые временные интервалы [12]. Благодаря эффективности в модуляции корковой возбудимости iTBS рассматривается как целенаправленное вмешательство при постинсультной афазии, особенно при воздействии на левую нижнюю лобную извилину (НЛИ). Данная область, соответствующая зоне Брока, играет ключевую роль в инициации речи, артикуляции и синтаксической обработке и часто поражается при нефлюентных формах афазии. Ранее проведенные исследования показали, что возбуждающая iTBS или высокочастотная ритмическая транскраниальная магнитная стимуляция (рТМС), применяемая к левой НЛИ, способствует значительным улучшениям в назывании, беглости речи и понимании языка [13, 14].
Данные нейровизуализации дополнительно подтверждают значение НЛИ в процессах восстановления, поскольку повышение активности этой области положительно коррелирует с улучшением речевых показателей. Методика iTBS включает короткие серии высокочастотных стимулов (50 Гц), подаваемых с тета-диапазонными интервалами (5 Гц), что имитирует эндогенные тета-ритмы гиппокампа, ассоциированные с обучением и синаптической пластичностью [15]. Такая паттернированная стимуляция, как предполагается, усиливает синаптическую эффективность и модулирует функциональную связность как локальных, так и распределенных языковых сетей. В отличие от традиционной рТМС, протоколы iTBS имеют меньшую продолжительность (обычно 3–5 мин на сеанс) и лучше переносятся пациентами с постинсультной утомляемостью или когнитивными ограничениями.
Несмотря на теоретические преимущества iTBS, число клинических исследований, оценивающих ее эффективность при афазии, остается ограниченным и они характеризуются значительной вариабельностью в дизайне, отборе пациентов и используемых критериях исходов. Хотя некоторые работы демонстрируют выраженные улучшения речевых функций после применения iTBS, другие авторы сообщают лишь об умеренных либо несущественных результатах, что подчеркивает необходимость стандартизации протоколов и применения мультимодальных методов оценки [14, 16]. Кроме того, нейрофизиологические механизмы, лежащие в основе наблюдаемых улучшений, такие как изменения паттернов корковой активации или межполушарной функциональной связности, остаются недостаточно изученными и требуют дальнейших исследований с использованием методов функциональной магнитно-резонансной томографии (фМРТ) и электроэнцефалографии (ЭЭГ).
Цель исследования – оценить эффективность iTBS в сочетании с речевой терапией для улучшения речевых функций и нейрофизиологических показателей у пациентов с постинсультной афазией Брока.
Материалы и методы
Настоящее исследование было выполнено в формате рандомизированного двойного слепого плацебо-контролируемого клинического испытания с параллельным распределением групп. Исследование проводилось на кафедре неврологии Ургенчского филиала Ташкентской медицинской академии в период с 2022 по 2024 г. В исследование были включены 60 пациентов (мужчины и женщины) в возрасте от 30 до 70 лет с нефлюентной афазией, развившейся после ишемического инсульта. Участники были случайным образом распределены в соотношении 1:1 в группу активной iTBS или группу имитационной стимуляции с использованием сгенерированной компьютером последовательности рандомизации. Все пациенты проходили сеансы речевой терапии, проводимые сертифицированными логопедами. Терапия была стандартизирована на основе структурированного протокола, разработанного в соответствии с доказательными методами реабилитации афазии, включая фонологическое подсказывание, тренинг повторения и семантический анализ признаков. Сеансы речевой терапии проводились пять раз в неделю по 45 мин в течение 2 нед. Соблюдение протокола терапии контролировалось посредством ведения ежедневных журналов и контрольных листов терапевтов.
Критериями включения пациентов в исследование были: 1) кортикальный или подкорковый инфаркт левого полушария, подтвержденный данными МРТ или компьютерной томографии головного мозга; 2) афазия вследствие первого ишемического инсульта; 3) праворукость; 4) срок после инсульта от 2 нед до 6 мес; 5) сохраненная когнитивная функция – оценка по Краткой шкале оценки психического статуса (Mini-mental State Examination, MMSE) ≥24; 6) свободная речь до инсульта; 7) клинический диагноз постинсультной афазии, преимущественно афазии Брока, подтвержденный сертифицированным неврологом и логопедом; 8) отсутствие подтвержденных нейродегенеративных или тяжелых соматических заболеваний; 9) возраст от 30 до 70 лет.
Критериями исключения были: 1) афазия, вызванная другими заболеваниями (энцефалит, травма, отравление); 2) тяжелая депрессия; 3) беременность; 4) аллергическая реакция на мемантин; 5) тяжелые соматические заболевания: сердечная недостаточность III–IV класса по NYHA, неконтролируемый сахарный диабет, хроническая болезнь почек стадии IV и выше, тяжелая хроническая обструктивная болезнь легких или активное злокачественное новообразование, по поводу которого пациент получает системное лечение; 6) противопоказания к iTBS (кардиостимуляторы, металлические объекты, имплантированные в голову); 7) эпилепсия; 8) прием трициклических антидепрессантов или нейролептиков в течение последних 3 мес; 9) выраженная апраксия речи; 10) тяжелое нарушение понимания речи – оценка по шкале Western Aphasia Battery (WAB) ниже 4.
Этическое одобрение (№ 329/2022) было получено от институционального этического комитета, и все участники предоставили письменное информированное согласие перед включением в исследование. Исследование проводилось в соответствии с Хельсинкской декларацией.
Рандомизация и ослепление. Участники были случайным образом распределены в соотношении 1:1 в группу активной iTBS или группу имитационной стимуляции с использованием компьютерно-сгенерированной последовательности рандомизации. Сокрытие распределения обеспечивалось с помощью непрозрачных запечатанных конвертов. Все участники и специалисты, оценивавшие результаты, оставались ослепленными в отношении группового распределения на протяжении всего исследования.
Определение порога двигательной возбудимости в состоянии покоя
Порог двигательной возбудимости в состоянии покоя определялся индивидуально для каждого участника до начала первой сессии стимуляции. Поверхностные электроды электромиографии устанавливались над мышцей abductor pollicis brevis доминирующей руки. Порог двигательной возбудимости определялся с этой руки путем регистрации моторных вызванных потенциалов (МВП) в соответствии со стандартными процедурами TMC [12, 13, 17]. Такой подход был выбран из-за возможной вариабельности и ненадежности регистрации МВП с пораженного полушария у пациентов после инсульта. Одноимпульсная ТМС применялась над первичной моторной корой с использованием стимулятора DuoMAG XT (Deymed, Чешская Республика), оснащенного 70-миллиметровой катушкой в форме восьмерки. «Двигательная горячая точка» определялась как участок кожи головы, при стимуляции которого вызывались наибольшие и наиболее стабильные МВП в целевой мышце. Порог моторного ответа определялся как минимальная интенсивность стимуляции, вызывавшая МВП амплитудой не менее 50 мкВ в 5 из 10 последовательных испытаний при полном расслаблении мышцы. Этот порог использовался в качестве эталонного значения для определения индивидуальной интенсивности стимуляции на протяжении всего курса лечения.
Протокол стимуляции
Активная группа iTBS. Участники группы активной стимуляции получали iTBS, направленную на левую НЛИ, соответствующую области Брока. Место стимуляции определялось в соответствии с международной системой ЭЭГ 10–20, с ориентацией на позицию электрода F7. Стимуляция проводилась с использованием устройства DuoMAG XT (Deymed, Чешская Республика) с катушкой в форме восьмерки диаметром 70 мм, расположенной тангенциально к поверхности головы под углом 45° к сагиттальной плоскости. Протокол iTBS соответствовал стандартной схеме: тройные серии импульсов с частотой 50 Гц повторялись каждые 200 мс (т.е. 5 Гц) и подавались в виде двухсекундных поездов каждые 10 с. Каждая сессия включала в общей сложности 600 импульсов. Интенсивность стимуляции устанавливалась на уровне 80% от индивидуального порога двигательной возбудимости. Продолжительность одной сессии составляла около 3 мин, процедуры проводились один раз в день, пять раз в неделю, на протяжении 2 нед (всего 10 сессий). Все участники одновременно проходили курс речевой терапии в течение того же двухнедельного периода вмешательства.
Имитационная группа. Участники группы имитационной стимуляции проходили аналогичные процедуры, включая позиционирование катушки и продолжительность сеанса, с использованием той же системы DuoMAG XT. Однако применялась либо имитационная катушка, либо неэффективная ориентация активной катушки, что предотвращало корковую стимуляцию при сохранении слуховых и тактильных ощущений. Это обеспечивало эффективное ослепление участников и исследователей на протяжении всего периода исследования. Участники имитационной группы также проходили курс речевой терапии с той же частотой и по тому же протоколу, что и в группе активной стимуляции, для обеспечения сопоставимости данных.
Нейрофизиологическая оценка
ЭЭГ в состоянии покоя регистрировалась с использованием 64-канальной системы BrainAmp (монтаж 10–20, частота дискретизации 500 Гц, глаза закрыты, продолжительность записи – 5 мин). Данные проходили полосовую фильтрацию (1–45 Гц), очистку с помощью независимого компонентного анализа (ICA) и повторное приведение к среднему референтному электроду. Рассчитывалась когерентность в альфа-диапазоне (8–12 Гц) между левыми фронтотемпоральными областями (например, F7–T3), а также индексы межполушарной асимметрии. фМРТ в состоянии покоя выполнялась на сканере 3T GE Discovery MR750 (последовательность EPI; TR=2000 мс; TE=30 мс; размер вокселя = 3×3×3 мм³; 210 томов; 7 мин). Во время сканирования участники фиксировали взгляд на центральном кресте при открытых глазах. Предобработка и анализ данных выполнялись с использованием пакета CONN toolbox (v20b) и SPM12. Этапы включали коррекцию движений, нормализацию в пространстве MNI, сглаживание (6 мм FWHM) и временную фильтрацию (0,008–0,09 Гц). Возмущающие переменные (белое вещество, спинномозговая жидкость, движения) регрессировались. Функциональная связность анализировалась по корреляциям ROI–ROI между языковыми областями: левой НЛИ, задней верхней височной извилиной и дополнительной моторной зоной. Корреляции, преобразованные методом Фишера в z-показатели, сравнивались до и после вмешательства между группами; различия считались статистически значимыми при p<0,05 с поправкой FDR.
Показатели эффективности
Основным исходом являлось улучшение речевой функции, оцениваемое с помощью шкалы WAB. Сводные показатели, включая коэффициент афазии и его субкомпоненты (спонтанная речь, слуховое восприятие, повторение и называние), регистрировались на исходном уровне, после вмешательства, а также во время последующих контрольных оценок через 1, 3 и 6 мес. Вторичные исходы включали изменения нейрофизиологической активности, измеренные с помощью фМРТ и ЭЭГ в состоянии покоя. Эти методы использовались для оценки корковой реорганизации и межполушарной связности. Дополнительно проводилась оценка индекса Бартел для повседневной активности, опросника SF-36 для общей оценки состояния здоровья и SAQOL-39 (Stroke and Aphasia Quality of Life Scale) для оценки качества жизни, связанного с коммуникативной функцией, на исходном уровне и через 3 мес наблюдения. Шкала SF-36 использовалась для оценки общего качества жизни, связанного со здоровьем. Она включает восемь субдоменов (например, физическое функционирование, эмоциональное благополучие, жизненная активность), каждый из которых оценивается по шкале от 0 до 100. Более высокие баллы отражают лучшее субъективное состояние здоровья и функциональные возможности. Опросник SAQOL-39 является валидированным инструментом, специально разработанным для лиц с афазией. Он включает пункты, охватывающие коммуникативные навыки, психосоциальное благополучие, уровень энергии и повседневное функционирование. Ответы оцениваются по шкале типа Лайкерта, при этом более высокие суммарные и субшкальные баллы указывают на лучшее качество жизни и более высокую степень функциональной коммуникации.
Статистический анализ
Размер выборки был рассчитан с использованием программы G*Power 3.1 для двухвыборочного t-теста при допущении большого размера эффекта (d=0,8), уровне значимости α=0,05, статистической мощности 0,80 и стандартном отклонении 9,5 на основании данных предыдущих исследований. Минимально необходимое количество участников составляло 52, а целевое значение было увеличено до 60 для учета возможных потерь выборки. Исходные демографические и клинические данные были обобщены с помощью описательной статистики. Внутригрупповые сравнения между временными точками проводились с использованием дисперсионного анализа с повторными измерениями (ANOVA). Межгрупповые различия оценивались с помощью t-критерия Стьюдента или критерия Манна–Уитни в зависимости от распределения данных. Корреляционные связи между поведенческими и нейрофизиологическими показателями анализировались с использованием коэффициентов корреляции Пирсона или Спирмена. Статистическая значимость определялась при уровне p<0,05, а размер эффекта указывался по показателю d Коэна, где это было возможно. Все анализы выполнялись с использованием программного обеспечения SPSS версии 26.0 или R версии 4.2.2.
Результаты
Из 75 обследованных пациентов 60 соответствовали критериям включения и были рандомизированы поровну в группу активной iTBS (n=30) и группу имитационной стимуляции (n=30). Все участники завершили курс из 10 сеансов вмешательства. Контрольные оценки через 1, 3 и 6 мес были выполнены у 27 участников в каждой группе (уровень удержания – 90%). Серьезных нежелательных явлений зафиксировано не было. Анализ проводился по принципу намерения лечить; отсутствующие значения последующих наблюдений обрабатывались методом переноса последнего наблюдения.

Исходные характеристики
Демографические и клинические показатели были хорошо сбалансированы между группами (табл. 1). Статистически значимых различий по возрасту, полу, уровню образования, баллам по шкале MMSE или коэффициенту афазии (Aphasia Quotient, AQ) по WAB не выявлено (все p>0,05). Среднее время, прошедшее с момента инсульта, составило 36,0±10,8 дня в обеих группах. Всего 49 (81,7%) пациентов были включены в исследование в ранний подострый период (<90 дней), а 11 (18,3%) пациентов – в поздний подострый период. Стандартизированные средние различия для всех переменных составляли <0,2, что указывает на отсутствие исходного дисбаланса. Предпосылки нормальности и гомоскедастичности были проверены с использованием критериев Шапиро–Уилка и Левена соответственно (p>0,1 для всех случаев). Радиологический анализ данных визуализации показал, что локализация очагов поражения была сопоставима между группами. В обеих группах – iTBS и имитационной – большинство поражений затрагивали левую перисильвиеву кору, преимущественно НЛИ, островковую кору и переднюю часть верхней височной извилины. Объем поражений варьировал, но, как правило, не затрагивал задние речевые области, что соответствует диагностике нефлюентной формы афазии (афазии Брока).
Речевая продуктивность
Показатели коэффициента афазии (AQ) по шкале WAB значительно улучшались в обеих группах с течением времени, однако прирост был достоверно выше в группе iTBS на всех этапах после исходного измерения (табл. 2). В группе iTBS средний балл AQ увеличился с 45,2±7,1 на исходном уровне до 61,4±8,5 на 10-й день (d=1,98), с последующим повышением через 1 мес (67,3±8,9; d=2,49), 3 мес (70,8±9,3; d=2,81) и 6 мес (72,1±8,7; d=2,88). В группе имитационной стимуляции улучшения были менее выраженными: с 44,9±6,8 на исходном уровне до 51,3±7,4 на 10-й день (d=0,91) и 58,3±8,4 через 6 мес (d=1,54). Дисперсионный анализ с повторными измерениями (с поправкой Гринхауса–Гейссера, ε=0,84) выявил значимое взаимодействие «группа × время» (F(2,52, 151,3) = 11,92; p<0,001; η²=0,19). Межгрупповые различия превышали минимально клинически значимую разницу в 5 баллов AQ во всех временных точках.
Нейрофизиологические изменения
Анализ функциональной МРТ в состоянии покоя показал увеличение корреляций BOLD-сигнала между ROI-областями в группе iTBS после вмешательства, особенно в левой НЛИ. Функциональная связность дополнительно исследовалась с использованием анализа ROI-to-ROI корреляций между ключевыми левополушарными речевыми областями, включая НЛИ, дополнительную моторную зону и верхнюю височную извилину. Среднее процентное изменение сигнала в области НЛИ увеличилось с исходного уровня до значений в постлечебном периоде на 1,83±0,42% в группе iTBS по сравнению с увеличением на 0,94±0,35% в группе имитации (межгрупповая разница – 0,89%; 95% ДИ 0,65–1,13; p<0,001; d Коэна=2,18).

Анализ ЭЭГ в состоянии покоя выявил значительное повышение когерентности в альфа-диапазоне между фронтотемпоральными областями в группе iTBS (0,67±0,08) по сравнению с группой имитации (0,55±0,07; p<0,001; d=1,58). Кроме того, индексы межполушарной асимметрии значительно снизились в группе iTBS (0,31±0,09 против 0,42±0,11; p<0,001; d=1,12; табл. 3).
Функциональный статус и качество жизни
Через 3 мес после вмешательства участники группы iTBS продемонстрировали значительно более высокие показатели функциональной независимости и качества жизни по всем шкалам (табл. 4). Баллы по индексу Бартел увеличились в среднем на 20,6 пункта (83,1±9,4 против 62,5±10,2 на исходном уровне; p<0,001; d=2,09). Общий балл по шкале SAQOL-39 повысился на 42,3 пункта (211,4±23,5 против 169,1±21,8; p<0,001), при этом наибольшие улучшения отмечались в доменах «Коммуникация» (72,3±8,6) и «Эмоциональное благополучие» (69,1±7,9; в обоих случаях p<0,001). Показатели по субшкалам SF-36, отражающим физическое (62,7±9,8) и эмоциональное благополучие (67,5±10,2), также были достоверно выше в группе iTBS по сравнению с контрольной группой (p<0,01; d>1,0 для всех доменов; см. табл. 4). Вмешательство iTBS в целом хорошо переносилось. Легкие преходящие головные боли отмечались у четырех участников группы iTBS и у двух участников группы имитации, как правило, проходя самостоятельно без медицинского вмешательства. Серьезных нежелательных явлений не наблюдалось ни в одной из групп, и ни один участник не прекратил участие в исследовании из-за побочных эффектов.
Обсуждение
Настоящее рандомизированное двойное слепое плацебо-контролируемое исследование демонстрирует, что применение iTBS к левой НЛИ в сочетании с речевой терапией приводит к значительным и устойчивым улучшениям речевой функции, корковой активации и качества жизни у пациентов с постинсультной афазией Брока. Полученные результаты убедительно подтверждают эффективность нейромодулирующих методов как средства усиления восстановления речевых функций, особенно в подостром периоде реабилитации афазии.
Масштаб и устойчивость улучшения речевых функций, наблюдаемые в группе iTBS, согласуются с предыдущими исследованиями, указывающими на то, что возбуждающие протоколы TMC способны усиливать речевые способности за счет активации перилезионных областей. В исследовании J. Kindler и соавт. (2012) было показано, что применение iTBS к левой НЛИ значительно улучшало результаты называния у пациентов с хронической афазией [13]. Аналогично, J.B. Allendorfer и соавт. (2021) сообщили о поведенческих и нейровизуализационных улучшениях после применения самостоятельного протокола iTBS [14]. Наше исследование расширяет эти выводы благодаря использованию более крупной выборки, наличию контрольной группы с имитацией стимуляции и оценке долгосрочных эффектов до 6 мес после вмешательства. Кроме того, в отличие от многих предыдущих работ, в нашем исследовании применялась мультимодальная нейрофизиологическая оценка, что позволило подтвердить поведенческие улучшения объективными изменениями корковой активности.
Наблюдаемое увеличение показателей по шкале WAB Aphasia Quotient в группе iTBS было как статистически, так и клинически значимым. Средний прирост AQ примерно на 27 баллов через 6 мес превышает минимально клинически значимую разницу, описанную в литературе [18], и почти вдвое превышает улучшения, зафиксированные в группе имитации. Это подтверждает дополнительное преимущество iTBS по сравнению с одной лишь стандартной речевой терапией. В то время как N. Weiduschat и соавт. (2011) сообщили о положительных эффектах низкочастотной рТМС, применяемой к правой НЛИ [19], наше исследование показывает, что возбуждающая стимуляция левого полушария может быть еще более эффективной при применении на ранних этапах восстановления.
Результаты фМРТ, полученные в данном исследовании, показали повышение активации BOLD-сигнала в левой НЛИ и прилежащей перилезионной коре после применения iTBS. Это подтверждает гипотезу о том, что iTBS усиливает корковую возбудимость и способствует повторному вовлечению поврежденных языковых сетей. Кроме того, данные ЭЭГ в состоянии покоя продемонстрировали увеличение когерентности в альфа-диапазоне во фронтотемпоральных цепях и снижение межполушарной асимметрии – биомаркеров, часто связанных с функциональным восстановлением и синаптической реорганизацией. Эти эффекты согласуются с концепцией активность-зависимой нейропластичности, согласно которой стимуляционно-индуцированные механизмы, аналогичные ДВП, способствуют укреплению синаптических связей в перилезионных областях.
Предполагается, что стимуляция тета-вспышками, имитируя эндогенные тета-ритмы гиппокампа, более эффективно способствует пластическим процессам, чем традиционная рТМС [17]. Более того, доклинические исследования указывают, что iTBS может повышать экспрессию мозгового нейротрофического фактора (МНТФ) – ключевого модулятора синаптического восстановления и нейрогенеза [20]. Хотя уровень МНТФ напрямую не измерялся в данном исследовании, полученные нейрофизиологические данные косвенно подтверждают эту модель. Улучшенные поведенческие и нейрофизиологические результаты также свидетельствуют о том, что iTBS может способствовать восстановлению баланса при дезадаптивном межполушарном торможении – феномене, при котором интактное правое полушарие подавляет активность поврежденного левого через транскаллозальные пути [10]. Повышая возбудимость левой НЛИ, iTBS, вероятно, противодействует этому ингибирующему влиянию, облегчая более эффективную обработку речи.
Помимо языковых улучшений, участники группы iTBS продемонстрировали более высокие показатели по шкалам Бартел, SAQOL-39 и SF-36. Это указывает на то, что нейромодуляция способствует не только восстановлению речевых функций, но и повышению общей функциональной независимости и психосоциального благополучия. Данный эффект особенно важен в условиях ограниченных ресурсов, когда возможностей для длительной речевой терапии может быть недостаточно. Полученные результаты подтверждают целесообразность интеграции нейромодуляционных методов в протоколы ранней реабилитации афазии с целью ускорения функционального восстановления.
Время проведения нейромодуляции после инсульта все чаще рассматривается как критически важный фактор, определяющий эффективность лечения. В настоящем исследовании, хотя все участники были включены в подострый период (от 2 нед до 6 мес после инсульта), большинство из них получили лечение в первые 8 нед – промежуток, соответствующий ранней подострой фазе. Этот период характеризуется повышенной нейропластичностью, увеличенной синаптической восприимчивостью и динамической перестройкой нейронных сетей, что может повышать чувствительность к вмешательствам, таким как iTBS. Авторы предыдущих исследований (например, C. Grefkes и G.R. Fink, 2014) указывали, что стимуляция, проводимая на ранних этапах восстановления, может более эффективно использовать эндогенные механизмы реорганизации по сравнению с вмешательствами, начатыми на поздних стадиях [21]. Более того, мишени стимуляции могут требовать адаптации со временем: если на раннем этапе модуляция левой НЛИ способствует прямой реактивации основных языковых сетей, то на более поздних этапах может оказаться более эффективной стратегия, направленная на активацию компенсаторных сетей. Благоприятные результаты, полученные в настоящем исследовании, согласуются с этой концепцией; это позволяет предположить, что раннее применение iTBS после инсульта может представлять собой оптимальное терапевтическое окно для стимулирования восстановления речи. Эти выводы подчеркивают важность стратифицированного дизайна клинических исследований и персонализированных протоколов стимуляции, основанных на данных нейровизуализации и исходных профилях функциональной связности.
Нейромодулирующие эффекты iTBS, наблюдаемые в данном исследовании, также согласуются с результатами, полученными при использовании других методов неинвазивной стимуляции мозга. Например, высокочастотная рТМС, направленная на лобные области левого полушария, продемонстрировала способность улучшать речевые функции за счет реактивации корковых зон, тогда как анодная транскраниальная стимуляция постоянным током (tDCS), воздействующая на аналогичные нейронные сети, приводила к повышению эффективности называния и модуляции функциональной связности в состоянии покоя [11, 22, 23]. Эти параллельные данные подтверждают существование общего механизма пластичности, сходного с ДВП, и дополнительно обосновывают целесообразность применения возбуждающих стратегий стимуляции в реабилитации афазии.
Несмотря на свои сильные стороны, данное исследование имеет несколько ограничений. Во-первых, размер выборки, хотя и достаточный для выявления статистически значимых эффектов, остается относительно небольшим и ограничен рамками одного центра. В будущем необходимы многоцентровые исследования с участием более крупных и разнородных популяций для повышения обобщаемости результатов. Во-вторых, исследование было сосредоточено исключительно на афазии Брока, поэтому полученные данные не могут быть напрямую экстраполированы на другие подтипы, такие как афазия Вернике или глобальная афазия.
В-третьих, хотя в исследовании для оценки корковых механизмов использовались методы нейровизуализации и ЭЭГ, прямые биомаркеры, такие как уровень МНТФ в сыворотке крови или трактография, могли бы предоставить более детализированную информацию о состоянии белого вещества и процессах синаптической перестройки. Кроме того, пациенты не были стратифицированы по локализации, размеру очага поражения или времени, прошедшему с момента инсульта в пределах допустимого диапазона. Эти переменные могут существенно влиять на ответ на нейромодуляцию и должны быть изучены в будущих исследованиях. Наконец, хотя протокол имитационной стимуляции обеспечивал сохранение слуховых и тактильных ощущений, нельзя полностью исключить возможность влияния эффекта плацебо на поведенческие результаты.
Опираясь на полученные результаты, будущие исследования должны быть направлены на определение оптимальных стратегий дозирования, включая количество сеансов, частоту применения и временные рамки после инсульта. Сочетание iTBS с интенсивной речевой терапией или фармакологическими средствами (например, холинергическими модуляторами, миметиками МНТФ) может дополнительно способствовать восстановлению функций. Кроме того, изучение предиктивных биомаркеров, таких как исходная функциональная связность по данным ЭЭГ или объем поражения, может помочь выявить пациентов, которые с наибольшей вероятностью получат пользу от iTBS. Расширение протоколов для включения других вариантов афазии и пациентов в хронической фазе также представляется перспективным направлением.
Заключение
Настоящее рандомизированное плацебо-контролируемое исследование демонстрирует, что iTBS, применяемая в сочетании с речевой терапией, способствует улучшению восстановления речевых функций у пациентов с подострой постинсультной афазией Брока. Вмешательство привело к стойким улучшениям речевой продуктивности, функциональной независимости и качества жизни, которые сопровождаются изменениями корковой активности и связности, подтвержденными данными фМРТ и ЭЭГ. Полученные результаты подтверждают эффективность и хорошую переносимость iTBS как нейромодулирующего метода реабилитации афазии. Исследование также подчеркивает важность раннего вмешательства и комплексной мультимодальной оценки для оптимизации терапевтических исходов. Необходимы дальнейшие крупномасштабные многоцентровые исследования для подтверждения данных результатов, уточнения протоколов стимуляции и оценки их применимости при различных подтипах афазии и стадиях восстановления.
Конфликт интересов. Авторы заявляют об отсутствии потенциального конфликта интересов.
Conflict of interest. The authors have no potential conflicts of interest to disclose.
Финансирование. Авторы не получали целевого финансирования для проведения данного исследования.
Funding. The authors received no specific funding for this work.
Благодарности. Авторы выражают искреннюю признательность сотрудникам кафедры неврологии Ургенчского филиала Ташкентской медицинской академии за постоянную поддержку и помощь в ходе реализации данного исследования. Особая благодарность выражается логопедам и специалистам по клинической нейрофизиологии, чьи компетентность и преданность делу были решающими для успешного проведения вмешательства и сбора данных. Авторы также благодарны всем участникам исследования и их семьям за проявленное терпение, сотрудничество и доверие.
Acknowledgements. The authors would like to express their sincere gratitude to the staff of the Department of Neurology at the Urgench Branch of the Tashkent Medical Academy for their continuous support and assistance during the implementation of this study. Special thanks go to the speech-language therapists and clinical neurophysiology technicians whose expertise and dedication were essential to the successful completion of the intervention and data collection. We are also grateful to all study participants and their families for their time, cooperation, and trust.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Ортиков Акбар Пирнапаcович — ассистент каф. патологической анатомии, Ургенчский филиал Ташкентской медицинской академии. E-mail: ortiqovakbar1977@gmail.com; ORCID: 0009-0004-4658-2189
Akbar P. Ortikov – Assistant, Urgench branch of Tashkent Medical Academy. E-mail: ortiqovakbar1977@gmail.com; ORCID: 0009-0004-4658-2189
Киличев Ибодулла Абдуллаевич – д-р мед. наук, проф. каф. неврологии, медицинской психологии и психотерапии,
Ургенчский филиал Ташкентской медицинской академии. E-mail: qlichev@mail.ru; ORCID: 0009-0009-3219-5539
Ibodulla A. Kilichev – Dr. Sci. (Med.), Prof., Urgench branch of Tashkent Medical Academy. E-mail: qlichev@mail.ru; ORCID: 0009-0009-3219-5539
Юсупов Адхам Улугбекович – ассистент каф. неврологии, медицинской психологии и психотерапии, Ургенчский филиал Ташкентской медицинской академии.
E-mail: adham.yusupov.95@mail.ru; ORCID: 0009-0009-9675-5419
Adkham U. Yusupov – Assistant, Urgench branch of Tashkent Medical Academy. E-mail: adham.yusupov.95@mail.ru; ORCID: 0009-0009-9675-5419
Шамуратова Гульнора Бахтияровна – канд. мед. наук, доц. каф. естественных наук, Университет Мамуна. E-mail: gulnorashаmurаtovа8@gmail.com; ORCID: 0009-0002-8557-040X
Gulnora B. Shamuratova – Cand. Sci. (Med.), Assoc. Prof., Mamun University. E-mail: gulnorashаmurаtovа8@gmail.com; ORCID: 0009-0002-8557-040X
Шодмонова Азиза Адизовна – ассистент каф. гематологии и клинической лабораторной диагностики, Бухарский государственный медицинский институт им. Абу Али ибн Сино. E-mail: aziza.shodmonova@icloud.com; ORCID: 0009-0005-7544-3214
Aziza A. Shodmonova – Assistant, Abu Ali ibn Sino Bukhara State Medical Institute. E-mail: aziza.shodmonova@icloud.com; ORCID: 0009-0005-7544-3214
Каршибоева Наргиза Иброхимовна – аспирант каф. неврологии и медицинской психологии, Ташкентский государственный медицинский институт. E-mail: doc.ibrohimovanargiza@gmail.com; ORCID: 0009-0007-5488-893X
Nargiza I. Qarshiboyeva – Graduate Student, Tashkent State Medical Institute. E-mail: doc.ibrohimovanargiza@gmail.com;
ORCID: 009-007-5488-893X
Палванов Равшан Отамуратович – ассистент каф. неврологии, медицинской психологии и психотерапии, Ургенчский филиал Ташкентской медицинской академии. E-mail: ravshanpolvanov@gmail.com; ORCID: 0000-0002-6491-208X
Ravshan O. Palvanov – Assistant, Urgench branch of Tashkent Medical Academy. E-mail: ravshanpolvanov@gmail.com; ORCID: 0000-0002-6491-208X
Поступила в редакцию: 20.10.2025
Поступила после рецензирования: 01.11.2025
Принята к публикации: 06.11.2025
Received: 20.10.2025
Revised: 01.11.2025
Accepted: 06.11.2025
Список исп. литературыСкрыть список1. Engelter ST, Gostynski M, Papa S et al. Epidemiology of aphasia attributable to first ischemic stroke: incidence, severity, fluency, etiology, and thrombolysis. Stroke 2006;37(6):1379-84. DOI: 10.1161/01.STR. 0000221815.64093.8c
2. Flowers HL, Silver FL, Fang J et al. The incidence, co-occurrence, and predictors of dysphagia and aphasia after first-ever acute ischemic stroke. J Commun Disord 2013;46(3):238-48. DOI: 10.1016/j.jcomdis. 2013.04.001
3. Ellis C, Simpson AN, Bonilha H et al. The one-year attributable cost of poststroke aphasia. Stroke 2012;43(5):1429-31. DOI: 10.1161/STROKEAHA.111.647339
4. World Health Organization. Rehabilitation in health systems: guide for action. Geneva: World Health Organization; 2020.
5. Hillis AE. Aphasia: progress in the last quarter of a century. Neurology 2007;69(2):200-13. DOI: 10.1212/01.wnl.0000265600.69385.6f
6. Goodglass H, Kaplan E. The assessment of aphasia and related disorders. 2nd ed. Philadelphia: Lea & Febiger; 1983.
7. Hilari K, Byng S, Lamping DL, Smith SC. Stroke and Aphasia Quality of Life Scale-39 (SAQOL-39). Stroke 2003;34(8):1944-50. DOI: 10.1161/01.STR.0000081987.46660.ED
8. Brady MC, Kelly H, Godwin J, Enderby P. Speech and language therapy for aphasia following stroke. Cochrane Database Syst Rev 2016;(6):CD000425. DOI: 10.1002/14651858.CD000425.pub4
9. Pascual-Leone A, Walsh V, Rothwell J. Transcranial magnetic stimulation in cognitive neuroscience: virtual lesion, chronometry, and functional connectivity. Curr Opin Neurobiol 2000;10(2):232-7. DOI: 10.1016/s0959-4388(00)00081-7
10. Hamilton RH, Chrysikou EG, Coslett B. Mechanisms of aphasia recovery after stroke and the role of noninvasive brain stimulation. Brain Lang 2011;118(1-2):40-50. DOI: 10.1016/j.bandl.2011.02.005
11. Wang X, Zhang M, Zhang J, Hu J. Repetitive transcranial magnetic stimulation for the treatment of post-stroke aphasia: a systematic review and meta-analysis of randomized controlled trials. PLoS One 2014;9(3):e91133.
12. Oberman L, Edwards D, Eldaief M, Pascual-Leone A. Safety of theta burst transcranial magnetic stimulation: a systematic review of the literature. J Clin Neurophysiol 2011;28(1):67-74. DOI: 10.1097/WNP. 0b013e318205135f
13. Kindler J, Schumacher R, Cazzoli D et al. Theta burst stimulation over the left inferior frontal gyrus enhances naming performance in aphasic patients. Restor Neurol Neurosci 2012;30(3):255-66.
14. Allendorfer JB, Nenert R, Vannest J, Szaflarski JP. A pilot randomized controlled trial of intermittent theta burst stimulation as stand-alone treatment for post-stroke aphasia: effects on language and verbal functional magnetic resonance imaging. Med Sci Monit 2021;27:e934818. DOI: 10.12659/MSM.934818
15. Chung SW, Hoy KE, Fitzgerald PB. Theta-burst stimulation: a new form of TMS treatment for depression? Depress Anxiety 2015;32(3):182-92. DOI: 10.1002/da.22335
16. Meinzer M, Rodriguez AD, Gonzalez Rothi LJ. Neural biomarkers of functional improvement in chronic aphasia following intensive language therapy: a review of the literature. Restor Neurol Neurosci 2012;30(4):567-82.
17. Huang YZ, Edwards MJ, Rounis E et al. Theta burst stimulation of the human motor cortex. Neuron 2005;45(2):201-6. DOI: 10.1016/j.neuron.2004.12.033
18. Breitenstein C, Grewe T, Flöel A et al. Intensive speech and language therapy in patients with chronic aphasia after stroke: a randomized, open-label, blinded-endpoint, controlled trial in a health-care setting. Lancet 2017;389(10078):1528-38. DOI: 10.1016/S0140-6736(17)30067-3
19. Weiduschat N, Thiel A, Rubi-Fessen I et al. Effects of repetitive transcranial magnetic stimulation in aphasic stroke: a randomized controlled pilot study. Stroke 2011;42(2):409-15. DOI: 10.1161/STROKEAHA.110.597864
20. Wang HY, Crupi D, Liu J et al. Repetitive transcranial magnetic stimulation enhances BDNF-TrkB signaling in the prefrontal cortex of adult rats. Brain Stimul 2011;4(2):132-40.
21. Grefkes C, Fink GR. Connectivity-based approaches in stroke and recovery of function. Lancet Neurol 2014;13(2):206-16. DOI: 10.1016/S1474-4422(13)70264-3
22. Monti A, Ferrucci R, Fumagalli M et al. Transcranial direct current stimulation and language. J Neurol Neurosurg Psychiatry 2013;84(8):832-42. DOI: 10.1136/jnnp-2012-302825
23. Fridriksson J, Richardson JD, Baker JM, Rorden C. Transcranial direct current stimulation improves naming reaction time in fluent aphasia: a double-blind, sham-controlled study. Stroke 2011;42(3):819-21. DOI: 10.1161/STROKEAHA.110.600288


