Клинический разбор в общей медицине №01 2026
VOKA-SERVIS LLC, Renovatio Aesthetic Medicine Clinic, Krasnoyarsk, Russia
raginene@mail.ru
Abstract
Sleep disorders and back pain often co-exist and mutually reinforce each other, forming a vicious cycle of “pain – insomnia – increased pain”. A pathogenetically based approach for the musculotonic component of dorsalgia is a combination of NSAIDs and a central muscle relaxant. The aim of this study was to describe the clinical effect of a seven-day evening intake of ketoprofen 100 mg and tizanidine 2 mg in a patient with chronic vertebrogenic lumbalgia and secondary insomnia.
Clinical case: 43-year-old woman, dorsopathy of the lumbar spine with severe musculotonic syndrome, chronic insomnia. Intervention: ketoprofen 100 mg + tizanidine 2 mg once a night for 7 days; basic recommendations for sleep hygiene and a gentle motor regime. Effectiveness assessment: numerical rating scale (CRS) of pain, insomnia severity index (ISI), sleep diary (sleep efficiency, %).
Already on the 2nd day of therapy, pain decreased from 7/10 to 3/10 at rest and from 9/10 to 5/10 when moving; by day 7, to 2–3/10. Sleep quality according to HRH increased from 3/10 to 7–8/10; ISI decreased from 20 (initially) to 14 on day 4 and up to 8 on the 7th day. Sleep efficiency increased from 65% (baseline) to 79% (day 4) and 89% (day 7). Tolerability is good; mild desirable drowsiness was observed in the evening, no clinically significant adverse events were reported.
A short-term evening combination of ketoprofen 100 mg and tizanidine 2 mg in a patient with dorsalgia and secondary insomnia provided rapid pain reduction and improved sleep, indicating the possibility of breaking the vicious cycle of “pain-sleep” by combining analgesia and muscle relaxation/sedation. Controlled studies are needed to confirm the effectiveness and safety of the approach in wide samples.
Keywords: dorsalgia, vertebrogenic lumbalgia, insomnia, ketoprofen, tizanidine, NSAIDs, muscle relaxants.
For citation: Raginene I.G. Importance of pain jugulation in patients with dorsalgia and the associated sleep disorders. Case report. Clinical review for general practice. 2026; 7 (1): 72–76 (In Russ.). DOI: 10.47407/kr2026.7.1.00757
Всовременном обществе нарушения сна и боль в спине являются распространенными проблемами, которые угрожают здоровью [1]. Бессонница считается фактором риска для повышения частоты приступов боли. Также некоторыми исследователями выводится гипотеза об общих механизмах формирования центральной сенсибилизации и хронической бессонницы [2]. Распространенность нарушений сна как болезни в популяции достигает 15% [3], при этом эпизодические инсомнии встречаются у 85% населения [4]. Распространенность нарушений сна при хроническом болевом синдроме, согласно последним данным, достигает 45% [5].
Данные многочисленных исследований свидетельствуют о существовании корреляции между нарушениями сна и хронической болью в спине, при этом фундаментальные механизмы связи между нарушениями сна и хронической болью в спине все еще изучаются [6].
Исследования показывают наличие причинно-следственной связи между нарушением сна и болью в нижней части спины [7]. Проведенный в 2019 г. метаанализ (PubMed, Scopus и Embase; включено 21 исследование) подтверждает достоверную связь нарушений сна с болью в спине [отношение шансов (ОШ) 1,52; 95% доверительный интервал (ДИ) 1,37–1,68; p<0,001]. У мужчин ОШ составило 1,49 (95% ДИ 1,34–1,65; p<0,001), у женщин – 1,56 (95% ДИ 1,33–1,81; p<0,001). Связь между нарушениями сна и болью в спине может быть двусторонней: боль в спине может приводить к нарушениям сна, а улучшение сна может быть сдерживающим фактором против боли в спине [8].
Нестероидные противовоспалительные препараты (НПВП) являются препаратами первой линии и наиболее часто используются для терапии неспецифической скелетно-мышечной боли [9]. Очевидно, что оптимальные НПВП должны быть высокоэффективными (устранять боль, воспаление), безопасными (оказывать минимальное влияние на желудочно-кишечный тракт, печень и т.д.), быстродействующими (минимизация времени контакта препарата со слизистой оболочкой желудочно-кишечного тракта и снижение риска кумуляции), а также оказывать эффект продолжительно (удобство в применении) [10]. Одним из наиболее часто используемых препаратов группы НПВП является кетопрофен [9]. Противовоспалительное, аналгезирующее и жаропонижающее действие кетопрофена обусловлено блокированием ферментов циклооксигеназы-1 и -2 и, частично, липоксигеназы, что приводит к подавлению синтеза провоспалительных цитокинов, в том числе в центральной нервной системе [11]. Высокая анальгетическая эффективность кетопрофена была продемонстрирована в работе итальянских ученых P. Sarzi-Puttini и соавт.: был проведен метаанализ 13 рандомизированных клинических исследований (n=898), в которых сравнивалось действие кетопрофена 50–200 мг/сут с ибупрофеном 600–1800 мг/сут или диклофенаком 75–100 мг/сут у больных с различными ревматическими заболеваниями. Кетопрофен показал достоверное превосходство над препаратами сравнения в 9 из 13 рандомизированных клинических исследований. При этом вероятность достижения благоприятного эффекта при назначении кетопрофена была почти в 2 раза выше (ОШ 0,459; 95% ДИ 0,33–0,58; p=0,01) [12].
В другом метаанализе этих же авторов [13] исследовалась безопасность перорального приема кетопрофена в сравнении с ибупрофеном и диклофенаком с оценкой соотношения риск/польза при их применении. Полученные результаты показали, что кетопрофен хорошо переносится, а его профиль безопасности сопоставим с таковым ибупрофена и диклофенака. В свете высокой эффективности, продемонстрированной в предыдущем метаанализе, результаты изучения безопасности подтверждают вывод, что кетопрофен имеет наилучший профиль риск/польза по сравнению как с ибупрофеном, так и с диклофенаком. Преимуществом кетопрофена является также наличие большого разнообразия лекарственных форм. Это обеспечивает возможность индивидуализированного, удобного для каждого отдельного пациента лечения болевого синдрома любой локализации и различной интенсивности [14].
При наличии признаков выраженного мышечного спазма и неэффективности монотерапии НПВП при острой боли в спине рекомендованы также миорелаксанты. Тизанидин – миорелаксант, прекрасно подходящий в данной ситуации [14], так как наряду с центральным миорелаксирующим и аналгезирующим действием он обладает доказанным гастропротективным эффектом [15]. Это свойство тизанидина нивелирует возможные желудочно-кишечные нарушения, которые вероятны при назначении НПВП [14–16]. Механизм гастропротективного действия объясняется стимуляцией желудочных и центральных α2-адренергических рецепторов, что приводит к снижению секреции желудочной кислоты и повышению концентрации желудочного гликопротеина [14, 15].
Проводились многоцентровые двойные слепые плацебо-контролируемые исследования применения тизанидина с ибупрофеном [14], аспирином [17] и диклофенаком [16]. Более быстрый (на 3-й день лечения) статистически достоверный результат достигался в группе тизанидина. Серьезных побочных эффектов не наблюдалось ни в одной из групп. Сделан вывод, что при лечении острой боли в спине тизанидин снижает потребность в анальгетиках и предупреждает развитие гастропатии. Возможная сонливость (у 22% пациентов) при приеме тизанидина при постельном режиме лечения острой боли в спине может быть желательной и полезной, особенно в случаях нарушений сна.
Известно, что не только миорелаксирующий эффект, но и побочные действия тизанидина (снижение частоты сердечных сокращений и артериального давления) зависят от его концентрации в плазме крови. Тизанидин обладает узким терапевтическим индексом, поэтому необходим тщательный индивидуальный подбор дозы в зависимости от потребностей пациента [18, 19]. Согласно данным научной литературы, в случае болезненного мышечного спазма или спастичности тизанидин может применяться в различных дозах, начиная с 2 мг в день [19–23]. Для умеренного болевого синдрома может быть достаточно назначения тизанидина в дозе 2–4 мг на ночь на протяжении 5–7 дней [24].
Приведенные выше данные позволяют сделать вывод, что кетопрофен является высокоэффективным представителем НПВП, одним из препаратов выбора для стартового лечения как острой, так и хронической ноцицептивной боли. При этом вероятность развития побочных эффектов кетопрофена не выше, чем у других хорошо известных в клинической практике НПВП. Тизанидин в комбинации с НПВП снижает риск возникновения возможных гастропатий и повышает эффективность лечения острой боли в спине [14].
 Клинический случай
Клинический случай
Женщина 43 лет, бухгалтер по профессии (преимущественно сидячая работа), обратилась с жалобами на хроническую боль в поясничной области, усиливающуюся при физической нагрузке и в ночное время, ухудшение качества сна на фоне болевого синдрома. Диагноз: дорсопатия поясничного отдела позвоночника с выраженным мышечно-тоническим синдромом. Синдром инсомнии, вторичный. Пациентке назначена комбинированная терапия: кетопрофен 100 мг и тизанидин 2 мг однократно вечером перед сном в течение 7 дней. На фоне терапии уже в первые дни приема препаратов отмечено значительное уменьшение интенсивности боли по субъективной числовой рейтинговой шкале (ЧРШ; от 0 до 10 баллов, где 0–3 – выраженные нарушения сна, 4–6 – удовлетворительный сон, 7–10 баллов – хороший сон) и улучшение качества сна, оцениваемого с помощью анкеты сна, или индекса тяжести инсомнии (Insomnia Severity Index, ISI; опросник, используемый для оценки выраженности бессонницы у взрослых, где 0–7 баллов – нет клинически значимой бессонницы; 8–14 баллов – подпороговая бессонница; 15–21 балл – бессонница; 22–28 баллов – тяжелая бессонница), с устойчивым положительным эффектом по данным дневника сна. Представленный клинический случай демонстрирует эффективность и быстродействие данной комбинации в разрыве порочного круга «боль – нарушение сна – усиление боли».
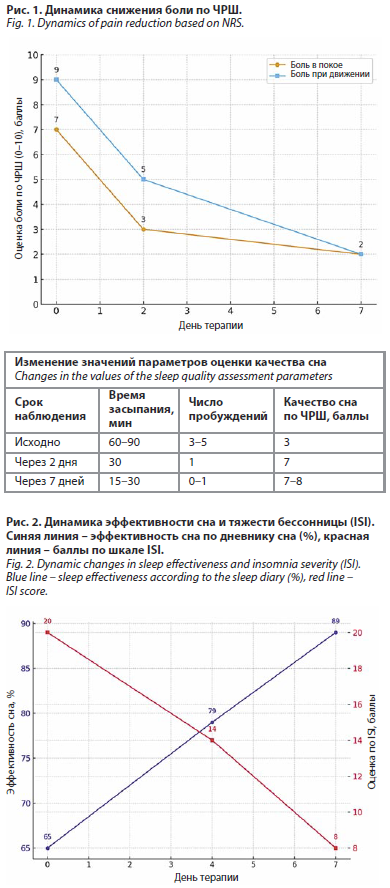
Основные жалобы при обращении: ноющая, тянущая боль в поясничной области, преимущественно справа. Интенсивность по ЧРШ: 7/10 в покое, до 9/10 при движении/наклонах (рис. 1). Усиление боли в ночное время, особенно при перемене положения тела в постели. Значительное ухудшение качества сна в последний месяц, совпавшее с усилением болей в спине. Пациентка отмечала эпизодические трудности с засыпанием и ранее, однако на момент обращения они стали постоянными: время засыпания – 60–90 мин, частые ночные пробуждения (3–5 раз за ночь) из-за дискомфорта и боли в спине, ощущение «разбитости» по утрам (см. таблицу). Общая удовлетворенность сном оценивалась как 3/10 (по субъективной ЧРШ; см. таблицу). По анкете сна ISI – 20 баллов (рис. 2).
Анамнез заболевания: боль в пояснице периодически беспокоила в течение 2–3 лет, последнее обострение – около 1 мес назад после подъема тяжести. Нарастание интенсивности боли, появление ночных болей и прогрессирующее ухудшение сна связывает с этим эпизодом. Самостоятельно принимала ибупрофен с незначительным и кратковременным эффектом в отношении боли, в отношении сна – без влияния.
Анамнез жизни: хронических заболеваний не отмечает. Аллергоанамнез не отягощен. Не курит, алкоголь употребляет редко. Наследственность по неврологическим и сомнологическим заболеваниям не отягощена.
Объективное обследование. Общий статус: состояние удовлетворительное. Сознание ясное.
 Неврологический статус. Позвоночник: пальпация паравертебральных точек LIV–V, LV–SI справа болезненна, напряжение паравертебральных мышц и квадратной мышцы поясницы справа. Объем движений в поясничном отделе ограничен: сгибание – 70% от нормы (боль), разгибание и боковые наклоны – умеренно ограничены из-за боли и мышечного напряжения. Симптом натяжения Ласега справа слабоположительный (70°). Мышечная сила, рефлексы (коленные, ахилловы), чувствительность в ногах – без особенностей. Патологических стопных знаков нет. Функции тазовых органов не нарушены.
Неврологический статус. Позвоночник: пальпация паравертебральных точек LIV–V, LV–SI справа болезненна, напряжение паравертебральных мышц и квадратной мышцы поясницы справа. Объем движений в поясничном отделе ограничен: сгибание – 70% от нормы (боль), разгибание и боковые наклоны – умеренно ограничены из-за боли и мышечного напряжения. Симптом натяжения Ласега справа слабоположительный (70°). Мышечная сила, рефлексы (коленные, ахилловы), чувствительность в ногах – без особенностей. Патологических стопных знаков нет. Функции тазовых органов не нарушены.
Оценка боли: интенсивность по ЧРШ на момент осмотра в покое – 8/10.
Оценка сна: клиническое интервью выявило соответствие критериям хронической инсомнии (трудности засыпания, поддержания сна, неудовлетворенность качеством сна, дневные нарушения – усталость, раздражительность) длительностью >3 мес. Субъективная оценка качества сна (по ЧРШ сна) – 3/10 (см. таблицу). По анкете сна ISI – 20 баллов (см. рис. 2). По данным дневника сна, эффективность сна за неделю составляла в среднем 65% (эффективность сна рассчитывается как отношение времени, проведенного во сне, ко времени, проведенному в постели, и выражается в процентах; см. рис. 2). Дневник сна пациентка заполняла ежедневно по утрам.
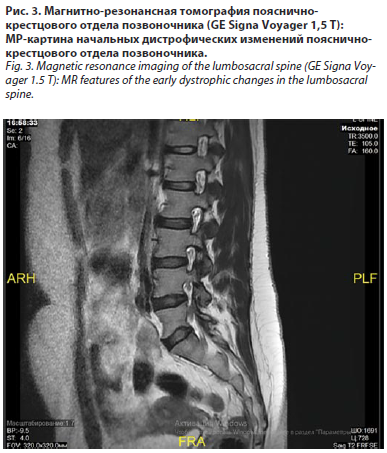
Инструментальная и лабораторная диагностика. Магнитно-резонансная томография поясничного отдела позвоночника: умеренные признаки остеохондроза LIV–SI, субхондральный склероз замыкательных пластин, краевые остеофиты тел позвонков. Спондилолистез не выявлен (рис. 3).
Общий анализ крови, мочи – без патологии.
Диагноз. Основной: дорсопатия поясничного отдела позвоночника с выраженным мышечно-тоническим синдромом. Хроническая вертеброгенная люмбалгия. Сопутствующий: синдром инсомнии (хронический, вторичный по отношению к болевому синдрому). Коды по МКБ-10: М42.1; G 47.0.
Лечение. Назначена комбинированная терапия:
• кетопрофен (Кетонал®) 100 мг перорально 1 раз в день вечером – 7 дней;
• тизанидин (Сирдалуд®) 2 мг перорально 1 раз в день вечером – 7 дней.
Режим приема – однократно вечером, за 30–60 мин до сна.
Немедикаментозные рекомендации: соблюдение гигиены сна, кратковременное ограничение подъема тяжестей и резких наклонов, умеренная двигательная активность в безболевом диапазоне.
Результаты терапии и наблюдение. Через 2 дня терапии пациентка отметила отчетливое уменьшение интенсивности боли в спине. Оценка боли по ЧРШ в покое составила 3/10, при движении – 5/10 (до терапии: в покое – 7/10, при движении – 9/10; см. рис. 1). Мышечное напряжение в пояснице субъективно уменьшилось.
Качество сна улучшилось уже через 2 дня от начала терапии: время засыпания сократилось до 30 мин, число ночных пробуждений – 1 раз (связывает с необходимостью посетить туалет, а не с болью; см. таблицу). Общая продолжительность сна – 6,5 ч. Утреннее самочувствие: нет чувства «разбитости» в утренние часы, уменьшение утренней скованности в спине. Оценка качества сна по ЧРШ – 7/10 (до начала терапии – 3/10; см. таблицу). По анкете ISI на фоне терапии качество сна оценивалось пациенткой на 14 баллов через 4 дня от начала терапии, что соответствует уровню подпороговой бессонницы. Эффективность сна на 4-й день терапии по дневнику сна составила 79%, в то время как до начала терапии она составляла 65% (см. рис. 2).
Последующее течение (наблюдение в течение 7 дней): пациентка продолжала прием препаратов в указанной дозе ежевечерне. Интенсивность дневной боли к 7-му дню терапии стабильно снижена (оценка по ЧРШ – 2–3/10), эпизоды значительного усиления при неловких движениях купировались самостоятельно или требовали единичного дополнительного приема НПВП днем (см. рис. 1). Ночная боль практически не беспокоила.
Через неделю от начала терапии качество сна улучшилось: засыпание в течение 15–30 мин, 0–1 пробуждение за ночь, оценка по ЧРШ – 7–8/10 (см. таблицу). Качество сна по анкете ISI – 8 баллов, эффективность сна по дневнику сна через 7 дней терапии – 89% (см. рис. 2).
Переносимость: побочных эффектов (диспепсия, головокружение, выраженная гипотония, избыточная седация днем) пациентка не отмечала. Легкая сонливость после приема препаратов перед сном расценена как желательный эффект.
Обсуждение
Представленный клинический случай наглядно демонстрирует типичный порочный круг «боль в спине – нарушение сна – усиление восприятия боли». Мышечно-тонический синдром при дорсопатии является ключевым фактором, поддерживающим как болевой синдром, так и нарушение сна, особенно из-за ночного усиления дискомфорта [25].
Выбор комбинации кетопрофена (НПВП) и тизанидина (миорелаксант центрального действия) был патогенетически обоснован:
1. Кетопрофен: препарат обладает мощным анальгетическим и противовоспалительным действием, превосходя по эффективности некоторые другие НПВП [12, 13]. Действие кетопрофена наступает быстро, что критически важно для купирования боли перед сном.
2. Тизанидин: оказывает центральное миорелаксирующее действие, уменьшая патологическое мышечное напряжение – основную причину боли в описанном клиническом случае [14]. Не менее важен его седативный эффект, развивающийся в течение 30–60 мин [18, 24]. Этот эффект, часто рассматриваемый как побочный, в контексте инсомнии, вторичной по отношению к боли, становится терапевтическим преимуществом, способствуя быстрому засыпанию и углублению сна [17]. Гастропротективные свойства тизанидина [15] также потенциально снижают риск НПВП-ассоциированных осложнений при комбинированной терапии.
Данный клинический случай представляет интерес в связи с демонстрацией быстрого двойного эффекта (анальгетического и снотворного) уже на 2-й день приема назначенной комбинации. Терапия привела к улучшению качества сна уже в первые дни и к стойкому положительному результату в последующем. Низкая доза тизанидина (2 мг) оказалась достаточной для достижения терапевтического эффекта без значимых побочных действий, что соответствует данным о возможности применения низких доз при болевых синдромах [24].
Заключение
Представленный клинический случай подтверждает эффективность и хорошую переносимость комбинации кетопрофена (100 мг) и тизанидина (2 мг), назначаемой однократно вечером, для лечения пациентов с болью в спине (дорсопатией с мышечно-тоническим синдромом) и сопутствующей вторичной инсомнией.
Ключевыми преимуществами комбинированной терапии (кетопрофен 100 мг и тизанидин 2 мг на ночь) являются:
1. Двойной терапевтический эффект: аналгезия (кетопрофен) + миорелаксация и седация / улучшение засыпания (тизанидин).
2. Благоприятный профиль безопасности при краткосрочном применении в указанных дозах.
3. Быстрое действие, позволяющее купировать боль и облегчить засыпание непосредственно перед сном.
4. Разрыв порочного круга «боль – нарушение сна».
Такой подход может быть рекомендован в качестве эффективной стратегии стартовой терапии для пациентов с сочетанной скелетно-мышечной болью в спине и инсомнией.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Информированное согласие. Пациентка предоставила письменное информированное согласие на публикацию данного клинического случая в анонимном виде.
Informed consent. The patient submitted the informed consent to publication of the anonymized case report.
Информация об авторе
Information about the author
Рагинене Ирина Геннадьевна – канд. мед. наук, врач невролог-сомнолог, ООО «ВОКА-СЕРВИС» Клиника эстетической медицины «Реновацио». E-mail: raginene@mail.ru; ORCID: 0009-0009-2091-1294
Irina G. Raginene – Cand. Sci. (Med.), neurologist-somnologist, VOKA-SERVIS LLC, Renovatio Aesthetic Medicine Clinic. E-mail: raginene@mail.ru; ORCID: 0009-0009-2091-1294
Поступила в редакцию: 14.11.2025
Поступила после рецензирования: 17.11.2025
Принята к публикации: 20.11.2025
Received: 14.11.2025
Revised: 17.11.2025
Accepted: 20.11.2025
Клинический разбор в общей медицине №01 2026
Значение купирования боли у пациентов с дорсалгией и сопутствующими нарушениями сна. Клинический случай
Номера страниц в выпуске:72-76
Аннотация
Нарушения сна и боль в спине часто сосуществуют и взаимно усиливают друг друга, формируя порочный круг «боль – инсомния – усиление боли». Патогенетически обоснованным подходом при мышечно-тоническом компоненте дорсалгии является сочетание нестероидного противовоспалительного препарата и центрального миорелаксанта.
Цель данной работы – описать клинический эффект семидневного вечернего приема кетопрофена 100 мг и тизанидина 2 мг у пациентки с хронической вертеброгенной люмбалгией и вторичной инсомнией.
Представлен клинический случай: женщина 43 лет с дорсопатией поясничного отдела с выраженным мышечно-тоническим синдромом, хронической инсомнией. Назначены кетопрофен 100 мг + тизанидин 2 мг однократно на ночь – 7 дней; даны базовые рекомендации по гигиене сна и щадящему двигательному режиму. Для оценки эффективности использовались числовая рейтинговая шкала (ЧРШ) боли, индекс тяжести инсомнии (ISI), дневник сна (эффективность сна, %).
Уже на 2-й день терапии боль снизилась с 7/10 до 3/10 в покое и с 9/10 до 5/10 при движении; к 7-му дню — до 2–3/10. Качество сна по ЧРШ повысилось с 3/10 до 7–8/10; ISI уменьшился с 20 (исходно) до 14 на 4-й день и до 8 на 7-й день. Эффективность сна выросла с 65% (исходно) до 79% (4-й день) и 89% (7-й день). Переносимость хорошая; отмечалась легкая желательная сонливость вечером, клинически значимых нежелательных явлений не зарегистрировано.
Таким образом, краткосрочная вечерняя комбинация кетопрофена 100 мг и тизанидина 2 мг у пациентки с дорсалгией и вторичной инсомнией обеспечила быстрое снижение боли и улучшение сна, что указывает на возможность разрыва порочного круга «боль–сон» за счет совмещения аналгезии и миорелаксации/седации. Необходимы контролируемые исследования для подтверждения эффективности и безопасности подхода в широких выборках.
Ключевые слова: дорсалгия, вертеброгенная люмбалгия, инсомния, кетопрофен, тизанидин, НПВП, миорелаксанты.
Для цитирования: Рагинене И.Г. Значение купирования боли у пациентов с дорсалгией и сопутствующими нарушениями сна. Клинический случай. Клинический разбор в общей медицине. 2026; 7 (1): 72–76. DOI: 10.47407/kr2026.7.1.00757
Нарушения сна и боль в спине часто сосуществуют и взаимно усиливают друг друга, формируя порочный круг «боль – инсомния – усиление боли». Патогенетически обоснованным подходом при мышечно-тоническом компоненте дорсалгии является сочетание нестероидного противовоспалительного препарата и центрального миорелаксанта.
Цель данной работы – описать клинический эффект семидневного вечернего приема кетопрофена 100 мг и тизанидина 2 мг у пациентки с хронической вертеброгенной люмбалгией и вторичной инсомнией.
Представлен клинический случай: женщина 43 лет с дорсопатией поясничного отдела с выраженным мышечно-тоническим синдромом, хронической инсомнией. Назначены кетопрофен 100 мг + тизанидин 2 мг однократно на ночь – 7 дней; даны базовые рекомендации по гигиене сна и щадящему двигательному режиму. Для оценки эффективности использовались числовая рейтинговая шкала (ЧРШ) боли, индекс тяжести инсомнии (ISI), дневник сна (эффективность сна, %).
Уже на 2-й день терапии боль снизилась с 7/10 до 3/10 в покое и с 9/10 до 5/10 при движении; к 7-му дню — до 2–3/10. Качество сна по ЧРШ повысилось с 3/10 до 7–8/10; ISI уменьшился с 20 (исходно) до 14 на 4-й день и до 8 на 7-й день. Эффективность сна выросла с 65% (исходно) до 79% (4-й день) и 89% (7-й день). Переносимость хорошая; отмечалась легкая желательная сонливость вечером, клинически значимых нежелательных явлений не зарегистрировано.
Таким образом, краткосрочная вечерняя комбинация кетопрофена 100 мг и тизанидина 2 мг у пациентки с дорсалгией и вторичной инсомнией обеспечила быстрое снижение боли и улучшение сна, что указывает на возможность разрыва порочного круга «боль–сон» за счет совмещения аналгезии и миорелаксации/седации. Необходимы контролируемые исследования для подтверждения эффективности и безопасности подхода в широких выборках.
Ключевые слова: дорсалгия, вертеброгенная люмбалгия, инсомния, кетопрофен, тизанидин, НПВП, миорелаксанты.
Для цитирования: Рагинене И.Г. Значение купирования боли у пациентов с дорсалгией и сопутствующими нарушениями сна. Клинический случай. Клинический разбор в общей медицине. 2026; 7 (1): 72–76. DOI: 10.47407/kr2026.7.1.00757
Importance of pain jugulation in patients with dorsalgia and the associated sleep disorders. Case report
Irina G. RagineneVOKA-SERVIS LLC, Renovatio Aesthetic Medicine Clinic, Krasnoyarsk, Russia
raginene@mail.ru
Abstract
Sleep disorders and back pain often co-exist and mutually reinforce each other, forming a vicious cycle of “pain – insomnia – increased pain”. A pathogenetically based approach for the musculotonic component of dorsalgia is a combination of NSAIDs and a central muscle relaxant. The aim of this study was to describe the clinical effect of a seven-day evening intake of ketoprofen 100 mg and tizanidine 2 mg in a patient with chronic vertebrogenic lumbalgia and secondary insomnia.
Clinical case: 43-year-old woman, dorsopathy of the lumbar spine with severe musculotonic syndrome, chronic insomnia. Intervention: ketoprofen 100 mg + tizanidine 2 mg once a night for 7 days; basic recommendations for sleep hygiene and a gentle motor regime. Effectiveness assessment: numerical rating scale (CRS) of pain, insomnia severity index (ISI), sleep diary (sleep efficiency, %).
Already on the 2nd day of therapy, pain decreased from 7/10 to 3/10 at rest and from 9/10 to 5/10 when moving; by day 7, to 2–3/10. Sleep quality according to HRH increased from 3/10 to 7–8/10; ISI decreased from 20 (initially) to 14 on day 4 and up to 8 on the 7th day. Sleep efficiency increased from 65% (baseline) to 79% (day 4) and 89% (day 7). Tolerability is good; mild desirable drowsiness was observed in the evening, no clinically significant adverse events were reported.
A short-term evening combination of ketoprofen 100 mg and tizanidine 2 mg in a patient with dorsalgia and secondary insomnia provided rapid pain reduction and improved sleep, indicating the possibility of breaking the vicious cycle of “pain-sleep” by combining analgesia and muscle relaxation/sedation. Controlled studies are needed to confirm the effectiveness and safety of the approach in wide samples.
Keywords: dorsalgia, vertebrogenic lumbalgia, insomnia, ketoprofen, tizanidine, NSAIDs, muscle relaxants.
For citation: Raginene I.G. Importance of pain jugulation in patients with dorsalgia and the associated sleep disorders. Case report. Clinical review for general practice. 2026; 7 (1): 72–76 (In Russ.). DOI: 10.47407/kr2026.7.1.00757
Всовременном обществе нарушения сна и боль в спине являются распространенными проблемами, которые угрожают здоровью [1]. Бессонница считается фактором риска для повышения частоты приступов боли. Также некоторыми исследователями выводится гипотеза об общих механизмах формирования центральной сенсибилизации и хронической бессонницы [2]. Распространенность нарушений сна как болезни в популяции достигает 15% [3], при этом эпизодические инсомнии встречаются у 85% населения [4]. Распространенность нарушений сна при хроническом болевом синдроме, согласно последним данным, достигает 45% [5].
Данные многочисленных исследований свидетельствуют о существовании корреляции между нарушениями сна и хронической болью в спине, при этом фундаментальные механизмы связи между нарушениями сна и хронической болью в спине все еще изучаются [6].
Исследования показывают наличие причинно-следственной связи между нарушением сна и болью в нижней части спины [7]. Проведенный в 2019 г. метаанализ (PubMed, Scopus и Embase; включено 21 исследование) подтверждает достоверную связь нарушений сна с болью в спине [отношение шансов (ОШ) 1,52; 95% доверительный интервал (ДИ) 1,37–1,68; p<0,001]. У мужчин ОШ составило 1,49 (95% ДИ 1,34–1,65; p<0,001), у женщин – 1,56 (95% ДИ 1,33–1,81; p<0,001). Связь между нарушениями сна и болью в спине может быть двусторонней: боль в спине может приводить к нарушениям сна, а улучшение сна может быть сдерживающим фактором против боли в спине [8].
Нестероидные противовоспалительные препараты (НПВП) являются препаратами первой линии и наиболее часто используются для терапии неспецифической скелетно-мышечной боли [9]. Очевидно, что оптимальные НПВП должны быть высокоэффективными (устранять боль, воспаление), безопасными (оказывать минимальное влияние на желудочно-кишечный тракт, печень и т.д.), быстродействующими (минимизация времени контакта препарата со слизистой оболочкой желудочно-кишечного тракта и снижение риска кумуляции), а также оказывать эффект продолжительно (удобство в применении) [10]. Одним из наиболее часто используемых препаратов группы НПВП является кетопрофен [9]. Противовоспалительное, аналгезирующее и жаропонижающее действие кетопрофена обусловлено блокированием ферментов циклооксигеназы-1 и -2 и, частично, липоксигеназы, что приводит к подавлению синтеза провоспалительных цитокинов, в том числе в центральной нервной системе [11]. Высокая анальгетическая эффективность кетопрофена была продемонстрирована в работе итальянских ученых P. Sarzi-Puttini и соавт.: был проведен метаанализ 13 рандомизированных клинических исследований (n=898), в которых сравнивалось действие кетопрофена 50–200 мг/сут с ибупрофеном 600–1800 мг/сут или диклофенаком 75–100 мг/сут у больных с различными ревматическими заболеваниями. Кетопрофен показал достоверное превосходство над препаратами сравнения в 9 из 13 рандомизированных клинических исследований. При этом вероятность достижения благоприятного эффекта при назначении кетопрофена была почти в 2 раза выше (ОШ 0,459; 95% ДИ 0,33–0,58; p=0,01) [12].
В другом метаанализе этих же авторов [13] исследовалась безопасность перорального приема кетопрофена в сравнении с ибупрофеном и диклофенаком с оценкой соотношения риск/польза при их применении. Полученные результаты показали, что кетопрофен хорошо переносится, а его профиль безопасности сопоставим с таковым ибупрофена и диклофенака. В свете высокой эффективности, продемонстрированной в предыдущем метаанализе, результаты изучения безопасности подтверждают вывод, что кетопрофен имеет наилучший профиль риск/польза по сравнению как с ибупрофеном, так и с диклофенаком. Преимуществом кетопрофена является также наличие большого разнообразия лекарственных форм. Это обеспечивает возможность индивидуализированного, удобного для каждого отдельного пациента лечения болевого синдрома любой локализации и различной интенсивности [14].
При наличии признаков выраженного мышечного спазма и неэффективности монотерапии НПВП при острой боли в спине рекомендованы также миорелаксанты. Тизанидин – миорелаксант, прекрасно подходящий в данной ситуации [14], так как наряду с центральным миорелаксирующим и аналгезирующим действием он обладает доказанным гастропротективным эффектом [15]. Это свойство тизанидина нивелирует возможные желудочно-кишечные нарушения, которые вероятны при назначении НПВП [14–16]. Механизм гастропротективного действия объясняется стимуляцией желудочных и центральных α2-адренергических рецепторов, что приводит к снижению секреции желудочной кислоты и повышению концентрации желудочного гликопротеина [14, 15].
Проводились многоцентровые двойные слепые плацебо-контролируемые исследования применения тизанидина с ибупрофеном [14], аспирином [17] и диклофенаком [16]. Более быстрый (на 3-й день лечения) статистически достоверный результат достигался в группе тизанидина. Серьезных побочных эффектов не наблюдалось ни в одной из групп. Сделан вывод, что при лечении острой боли в спине тизанидин снижает потребность в анальгетиках и предупреждает развитие гастропатии. Возможная сонливость (у 22% пациентов) при приеме тизанидина при постельном режиме лечения острой боли в спине может быть желательной и полезной, особенно в случаях нарушений сна.
Известно, что не только миорелаксирующий эффект, но и побочные действия тизанидина (снижение частоты сердечных сокращений и артериального давления) зависят от его концентрации в плазме крови. Тизанидин обладает узким терапевтическим индексом, поэтому необходим тщательный индивидуальный подбор дозы в зависимости от потребностей пациента [18, 19]. Согласно данным научной литературы, в случае болезненного мышечного спазма или спастичности тизанидин может применяться в различных дозах, начиная с 2 мг в день [19–23]. Для умеренного болевого синдрома может быть достаточно назначения тизанидина в дозе 2–4 мг на ночь на протяжении 5–7 дней [24].
Приведенные выше данные позволяют сделать вывод, что кетопрофен является высокоэффективным представителем НПВП, одним из препаратов выбора для стартового лечения как острой, так и хронической ноцицептивной боли. При этом вероятность развития побочных эффектов кетопрофена не выше, чем у других хорошо известных в клинической практике НПВП. Тизанидин в комбинации с НПВП снижает риск возникновения возможных гастропатий и повышает эффективность лечения острой боли в спине [14].
 Клинический случай
Клинический случайЖенщина 43 лет, бухгалтер по профессии (преимущественно сидячая работа), обратилась с жалобами на хроническую боль в поясничной области, усиливающуюся при физической нагрузке и в ночное время, ухудшение качества сна на фоне болевого синдрома. Диагноз: дорсопатия поясничного отдела позвоночника с выраженным мышечно-тоническим синдромом. Синдром инсомнии, вторичный. Пациентке назначена комбинированная терапия: кетопрофен 100 мг и тизанидин 2 мг однократно вечером перед сном в течение 7 дней. На фоне терапии уже в первые дни приема препаратов отмечено значительное уменьшение интенсивности боли по субъективной числовой рейтинговой шкале (ЧРШ; от 0 до 10 баллов, где 0–3 – выраженные нарушения сна, 4–6 – удовлетворительный сон, 7–10 баллов – хороший сон) и улучшение качества сна, оцениваемого с помощью анкеты сна, или индекса тяжести инсомнии (Insomnia Severity Index, ISI; опросник, используемый для оценки выраженности бессонницы у взрослых, где 0–7 баллов – нет клинически значимой бессонницы; 8–14 баллов – подпороговая бессонница; 15–21 балл – бессонница; 22–28 баллов – тяжелая бессонница), с устойчивым положительным эффектом по данным дневника сна. Представленный клинический случай демонстрирует эффективность и быстродействие данной комбинации в разрыве порочного круга «боль – нарушение сна – усиление боли».
Основные жалобы при обращении: ноющая, тянущая боль в поясничной области, преимущественно справа. Интенсивность по ЧРШ: 7/10 в покое, до 9/10 при движении/наклонах (рис. 1). Усиление боли в ночное время, особенно при перемене положения тела в постели. Значительное ухудшение качества сна в последний месяц, совпавшее с усилением болей в спине. Пациентка отмечала эпизодические трудности с засыпанием и ранее, однако на момент обращения они стали постоянными: время засыпания – 60–90 мин, частые ночные пробуждения (3–5 раз за ночь) из-за дискомфорта и боли в спине, ощущение «разбитости» по утрам (см. таблицу). Общая удовлетворенность сном оценивалась как 3/10 (по субъективной ЧРШ; см. таблицу). По анкете сна ISI – 20 баллов (рис. 2).
Анамнез заболевания: боль в пояснице периодически беспокоила в течение 2–3 лет, последнее обострение – около 1 мес назад после подъема тяжести. Нарастание интенсивности боли, появление ночных болей и прогрессирующее ухудшение сна связывает с этим эпизодом. Самостоятельно принимала ибупрофен с незначительным и кратковременным эффектом в отношении боли, в отношении сна – без влияния.
Анамнез жизни: хронических заболеваний не отмечает. Аллергоанамнез не отягощен. Не курит, алкоголь употребляет редко. Наследственность по неврологическим и сомнологическим заболеваниям не отягощена.
Объективное обследование. Общий статус: состояние удовлетворительное. Сознание ясное.
 Неврологический статус. Позвоночник: пальпация паравертебральных точек LIV–V, LV–SI справа болезненна, напряжение паравертебральных мышц и квадратной мышцы поясницы справа. Объем движений в поясничном отделе ограничен: сгибание – 70% от нормы (боль), разгибание и боковые наклоны – умеренно ограничены из-за боли и мышечного напряжения. Симптом натяжения Ласега справа слабоположительный (70°). Мышечная сила, рефлексы (коленные, ахилловы), чувствительность в ногах – без особенностей. Патологических стопных знаков нет. Функции тазовых органов не нарушены.
Неврологический статус. Позвоночник: пальпация паравертебральных точек LIV–V, LV–SI справа болезненна, напряжение паравертебральных мышц и квадратной мышцы поясницы справа. Объем движений в поясничном отделе ограничен: сгибание – 70% от нормы (боль), разгибание и боковые наклоны – умеренно ограничены из-за боли и мышечного напряжения. Симптом натяжения Ласега справа слабоположительный (70°). Мышечная сила, рефлексы (коленные, ахилловы), чувствительность в ногах – без особенностей. Патологических стопных знаков нет. Функции тазовых органов не нарушены.Оценка боли: интенсивность по ЧРШ на момент осмотра в покое – 8/10.
Оценка сна: клиническое интервью выявило соответствие критериям хронической инсомнии (трудности засыпания, поддержания сна, неудовлетворенность качеством сна, дневные нарушения – усталость, раздражительность) длительностью >3 мес. Субъективная оценка качества сна (по ЧРШ сна) – 3/10 (см. таблицу). По анкете сна ISI – 20 баллов (см. рис. 2). По данным дневника сна, эффективность сна за неделю составляла в среднем 65% (эффективность сна рассчитывается как отношение времени, проведенного во сне, ко времени, проведенному в постели, и выражается в процентах; см. рис. 2). Дневник сна пациентка заполняла ежедневно по утрам.
Инструментальная и лабораторная диагностика. Магнитно-резонансная томография поясничного отдела позвоночника: умеренные признаки остеохондроза LIV–SI, субхондральный склероз замыкательных пластин, краевые остеофиты тел позвонков. Спондилолистез не выявлен (рис. 3).
Общий анализ крови, мочи – без патологии.
Диагноз. Основной: дорсопатия поясничного отдела позвоночника с выраженным мышечно-тоническим синдромом. Хроническая вертеброгенная люмбалгия. Сопутствующий: синдром инсомнии (хронический, вторичный по отношению к болевому синдрому). Коды по МКБ-10: М42.1; G 47.0.
Лечение. Назначена комбинированная терапия:
• кетопрофен (Кетонал®) 100 мг перорально 1 раз в день вечером – 7 дней;
• тизанидин (Сирдалуд®) 2 мг перорально 1 раз в день вечером – 7 дней.
Режим приема – однократно вечером, за 30–60 мин до сна.
Немедикаментозные рекомендации: соблюдение гигиены сна, кратковременное ограничение подъема тяжестей и резких наклонов, умеренная двигательная активность в безболевом диапазоне.
Результаты терапии и наблюдение. Через 2 дня терапии пациентка отметила отчетливое уменьшение интенсивности боли в спине. Оценка боли по ЧРШ в покое составила 3/10, при движении – 5/10 (до терапии: в покое – 7/10, при движении – 9/10; см. рис. 1). Мышечное напряжение в пояснице субъективно уменьшилось.
Качество сна улучшилось уже через 2 дня от начала терапии: время засыпания сократилось до 30 мин, число ночных пробуждений – 1 раз (связывает с необходимостью посетить туалет, а не с болью; см. таблицу). Общая продолжительность сна – 6,5 ч. Утреннее самочувствие: нет чувства «разбитости» в утренние часы, уменьшение утренней скованности в спине. Оценка качества сна по ЧРШ – 7/10 (до начала терапии – 3/10; см. таблицу). По анкете ISI на фоне терапии качество сна оценивалось пациенткой на 14 баллов через 4 дня от начала терапии, что соответствует уровню подпороговой бессонницы. Эффективность сна на 4-й день терапии по дневнику сна составила 79%, в то время как до начала терапии она составляла 65% (см. рис. 2).
Последующее течение (наблюдение в течение 7 дней): пациентка продолжала прием препаратов в указанной дозе ежевечерне. Интенсивность дневной боли к 7-му дню терапии стабильно снижена (оценка по ЧРШ – 2–3/10), эпизоды значительного усиления при неловких движениях купировались самостоятельно или требовали единичного дополнительного приема НПВП днем (см. рис. 1). Ночная боль практически не беспокоила.
Через неделю от начала терапии качество сна улучшилось: засыпание в течение 15–30 мин, 0–1 пробуждение за ночь, оценка по ЧРШ – 7–8/10 (см. таблицу). Качество сна по анкете ISI – 8 баллов, эффективность сна по дневнику сна через 7 дней терапии – 89% (см. рис. 2).
Переносимость: побочных эффектов (диспепсия, головокружение, выраженная гипотония, избыточная седация днем) пациентка не отмечала. Легкая сонливость после приема препаратов перед сном расценена как желательный эффект.
Обсуждение
Представленный клинический случай наглядно демонстрирует типичный порочный круг «боль в спине – нарушение сна – усиление восприятия боли». Мышечно-тонический синдром при дорсопатии является ключевым фактором, поддерживающим как болевой синдром, так и нарушение сна, особенно из-за ночного усиления дискомфорта [25].
Выбор комбинации кетопрофена (НПВП) и тизанидина (миорелаксант центрального действия) был патогенетически обоснован:
1. Кетопрофен: препарат обладает мощным анальгетическим и противовоспалительным действием, превосходя по эффективности некоторые другие НПВП [12, 13]. Действие кетопрофена наступает быстро, что критически важно для купирования боли перед сном.
2. Тизанидин: оказывает центральное миорелаксирующее действие, уменьшая патологическое мышечное напряжение – основную причину боли в описанном клиническом случае [14]. Не менее важен его седативный эффект, развивающийся в течение 30–60 мин [18, 24]. Этот эффект, часто рассматриваемый как побочный, в контексте инсомнии, вторичной по отношению к боли, становится терапевтическим преимуществом, способствуя быстрому засыпанию и углублению сна [17]. Гастропротективные свойства тизанидина [15] также потенциально снижают риск НПВП-ассоциированных осложнений при комбинированной терапии.
Данный клинический случай представляет интерес в связи с демонстрацией быстрого двойного эффекта (анальгетического и снотворного) уже на 2-й день приема назначенной комбинации. Терапия привела к улучшению качества сна уже в первые дни и к стойкому положительному результату в последующем. Низкая доза тизанидина (2 мг) оказалась достаточной для достижения терапевтического эффекта без значимых побочных действий, что соответствует данным о возможности применения низких доз при болевых синдромах [24].
Заключение
Представленный клинический случай подтверждает эффективность и хорошую переносимость комбинации кетопрофена (100 мг) и тизанидина (2 мг), назначаемой однократно вечером, для лечения пациентов с болью в спине (дорсопатией с мышечно-тоническим синдромом) и сопутствующей вторичной инсомнией.
Ключевыми преимуществами комбинированной терапии (кетопрофен 100 мг и тизанидин 2 мг на ночь) являются:
1. Двойной терапевтический эффект: аналгезия (кетопрофен) + миорелаксация и седация / улучшение засыпания (тизанидин).
2. Благоприятный профиль безопасности при краткосрочном применении в указанных дозах.
3. Быстрое действие, позволяющее купировать боль и облегчить засыпание непосредственно перед сном.
4. Разрыв порочного круга «боль – нарушение сна».
Такой подход может быть рекомендован в качестве эффективной стратегии стартовой терапии для пациентов с сочетанной скелетно-мышечной болью в спине и инсомнией.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Conflict of interests. The author declares that there is not conflict of interests.
Информированное согласие. Пациентка предоставила письменное информированное согласие на публикацию данного клинического случая в анонимном виде.
Informed consent. The patient submitted the informed consent to publication of the anonymized case report.
Информация об авторе
Information about the author
Рагинене Ирина Геннадьевна – канд. мед. наук, врач невролог-сомнолог, ООО «ВОКА-СЕРВИС» Клиника эстетической медицины «Реновацио». E-mail: raginene@mail.ru; ORCID: 0009-0009-2091-1294
Irina G. Raginene – Cand. Sci. (Med.), neurologist-somnologist, VOKA-SERVIS LLC, Renovatio Aesthetic Medicine Clinic. E-mail: raginene@mail.ru; ORCID: 0009-0009-2091-1294
Поступила в редакцию: 14.11.2025
Поступила после рецензирования: 17.11.2025
Принята к публикации: 20.11.2025
Received: 14.11.2025
Revised: 17.11.2025
Accepted: 20.11.2025
Список исп. литературыСкрыть список1. Morphy H, Dunn KM, Lewis M et al. Epidemiology of insomnia: a longitudinal study in a UK population. Sleep 2007;30:274-80. DOI: 10.1093/sleep/30.3.274
2. de Tommaso M, Delussi M, Vecchio E et al. Sleep features and central sensitization symptoms in primary headache patients. J Headache Pain 2014;15:64. DOI: 10.1186/1129-2377-15-64
3. Lichstein KL, Taylor DJ, McCrae CS, Petrov ME. Insomnia: epidemiology and risk factors. Principles and Practice of Sleep Medicine. 6th ed. Philadelphia: Elsevier; 2016. P. 761-8. DOI: 10.1016/B978-1-4160-6645-3.00076-1
4. Курушина О.В., Барулин А.Е., Багирова Д.Я. Современные подходы к лечению инсомнии в общетерапевтической практике. Медицинский совет. 2019;(6):20-6. DOI: 10.21518/2079-701X-2019-6-20-26
Kurushina O.V., Barulin A.E., Bagirowa D.Ya. Modern approaches to the treatment of insomnia in general therapeutic practice. Medical Council 2019;(6):20-6. DOI: 10.21518/2079-701X-2019-6-20-26 (in Russian).
5. Виноградов Д.К., Доронина О.Б. Особенности нарушений сна у пациентов с хронической болью в спине. Клиническая практика. 2019;10(2):46-52. DOI: 10.17816/clinpract10246-52. EDN JKDLDN
Vinogradov D.K., Doronina O.B. Features of sleep disorders in patients with chronic back pain. Clinical Practice 2019;10(2):46-52. DOI: 10.17816/clinpract10246-52. EDN JKDLDN (in Russian).
6. Mertimo T, Heikkala E, Niinim‰ki J et al. The role of co-occurring insomnia and mental distress in the association between lumbar disc degeneration and low back pain related disability. BMC Musculoskelet Disord 2023;24:293. DOI: 10.1186/s12891-023-06365-2
7. Morelh„o PK, Gobbi C, Christofaro DGD et al. Bidirectional association between sleep quality and low back pain in older adults: a longitudinal observational study. Arch Phys Med Rehabil 2022;103:1558-64. DOI: 10.1016/j.apmr.2021.11.009
8. Amiri S, Behnezhad S. Sleep disturbances and back pain : Systematic review and meta-analysis. Neuropsychiatry 2020 Jun;34(2):74-84. DOI: 10.1007/s40211-020-00339-9
9. Супонева Н.А., Юсупова Д.Г. Скелетно-мышечная боль: современные подходы к диагностике и терапии. РМЖ. 2024;(4):46-50. EDN: OJMVNV
Suponeva N.A., Yusupova D.G. Musculoskeletal pain: modern approaches to diagnostics and therapy. RMJ. 2024;(4):46-50. EDN: OJMVNV (in Russian).
10. Страчунский Л.С., Козлов С.Н. Нестероидные противовоспалительные средства. М.; 1997. С. 11-21. Режим доступа: http://old.antibiotic.ru/rus/all/metod/npvs/npvs.shtml
Strachunsky L.S., Kozlov S.N. Nonsteroidal anti-inflammatory drugs. Moscow; 1997. P. 11-21. Available at: http://old.antibiotic.ru/rus/all/ metod/npvs/npvs.shtml (in Russian).
11. Инструкция по медицинскому применению препарата Кетонал (кетопрофен) ЛП-№(005253)-(РГ-RU) Государственный реестр лекарственных средств. Режим доступа: https://grls.minzdrav. gov.ru/Grls_View_v2.aspx?routingGuid=507dd697-648c-4916-8ead-3000eb3bfee6
Instructions for medical use of the drug Ketonal (ketoprofen) LP-No. (005253)-(RG-RU) State Register of Medicines. Available at: https://grls.minzdrav.gov.ru/Grls_View_v2.aspx?routingGuid=507dd697-648c-4916-8ead-3000eb3bfee6 (in Russian).
12. Sarzi-Puttini P, Atzeni F, Lanata L, Bagnasco M. Efficacy of ketoprofen vs. ibuprofen and diclofenac: a systematic review of the literature and meta-analysis. Clin Exp Rheumatol 2013;31(5):731-8. DOI: 10.1136/annrheumdis-2015-eular.4009
13. Sarzi-Puttini P, Atzeni F, Lanata L et al. A New Meta-Analysis on Safety of Ketoprofen Vs Ibuprofen and Diclofenac: Risk and Benefit of Nsaids Beyond Efficacy Meta-Analysis. 2014 ACR/ARHP Annual Meeting. Abstract number: 2443. Arthritis Rheum 2014;(Abstract Suppl):S1066. DOI: 10.1002/art.38914
14. Вдовиченко В.П., Борисенок О.А., Коршак Т.А. и др. Кетопрофен и тизанидин в лечении болевого синдрома. Медицинские новости. 2020;3(306):51-5. EDN: OGMKYL
Vdovichenko V.P., Borisenok O.A., Korshak T.A. et al. Ketoprofen and tizanidine in treatment of pain syndrome. Medical News 2020;3(306):51-5. EDN: OGMKYL (in Russian).
15. Emre M. The gastroprotective effects of tizanidine: an overview. Curr Ther Res 1998;59(1):2-12. DOI: 10.1016/S0011-393X(98)85018-2
16. Sirdalud Ternelin Asia-Pacific Study Group. Curr Ther Res 1998;59(1):13-22. DOI: 10.1016/s0011-393x(98)85019-4
17. Berry H, Hutchinson DR. A multicentre placebo-controlled study in general practice to evaluate the efficacy and safety of tizanidine in acute low-back pain. J Int Med Res 1988 Mar-Apr;16(2):75-82. DOI: 10.1177/030006058801600201
18. Инструкция по медицинскому применению препарата Сирдалуд (тизанидин) П N012947/01 Государственный реестр лекарственных средств. Режим доступа: https://grls.minzdrav.gov.ru/Grls_ View_v2.aspx?routingGuid=1bc9436b-67d3-4467-aa99-79385a10944b
Instructions for medical use of the drug Sirdalud (tizanidine) P N012947/01 State Register of Medicines. Available at: https://grls.minzdrav.gov.ru/Grls_View_v2.aspx?routingGuid=1bc9436b-67d3-4467-aa99-79385a10944b (in Russian).
19. Saper JR, Winner PK, Lake AE 3rd. An open-label dose-titration study of the efficacy and tolerability of tizanidine hydrochloride tablets in the prophylaxis of chronic daily headache. Headache 2001 Apr;41(4):357-68. DOI: 10.1046/j.1526-4610.2001.111006357.x
20. Fryda-Kaurimsky Z, M¸ller-Fassbender H. Tizanidine (DS 103-282) in the treatment of acute paravertebral muscle spasm: a controlled trial comparing tizanidine and diazepam. J Int Med Res 1981;9(6):501-5. DOI: 10.1177/030006058100900613
21. Pareek A, Chandurkar N, Chandanwale AS et al. Aceclofenac-tizanidine in the treatment of acute low back pain: a double-blind, double-dummy, randomized, multicentric, comparative study against aceclofenac alone. Eur Spine J 2009 Dec;18(12):1836-42. DOI: 10.1007/s00586-009-1019-4
22. Bass B, Weinshenker B, Rice GP et al. Tizanidine versus baclofen in the treatment of spasticity in patients with multiple sclerosis. Can J Neurol Sci 1988 Feb;15(1):15-9. DOI: 10.1017/s0317167100027104
23. Zhu LL, Wang YH, Zhou Q. Tizanidine: Advances in Pharmacology & Therapeutics and Drug Formulations. J Pain Res 2024 Mar 21;17:1257-71. DOI: 10.2147/JPR.S461032
24. Данилов А.Б. Применение тизанидина (Сирдалуда) в лечении боли и спазма. РМЖ. 2012;31:1543-7. EDN: RMJ_31_ Nevrologiya_Psihiatriya_Layout 1
Danilov A.B. The use of tizanidine (Sirdalud) in the treatment of pain and spasm. RMJ 2012;31:1543-7. EDN: RMJ_31_Nevrologiya_Psihiatriya_Layout 1 (in Russian).
25. Дубинина Т.В., Елисеев М.С. Боль в нижней части спины: распространенность, причины, диагностика, лечениею Неврология, нейропсихиатрия, психосоматика. 2011;(1):22-6. DOI: 10.14412/2074-2711-2011-129
Dubinina T.V., Eliseyev M.S. Low back pain: prevalence, causes, diagnosis, treatment. Neurology, Neuropsychiatry, Psychosomatics 2011;(1):22-6. DOI: 10.14412/2074-2711-2011-129 (in Russian).


