Клинический разбор в общей медицине №01 2026
1 War Veterans Hospital No. 3, Moscow, Russia;
2 Sechenov Moscow State Medical University (Sechenov University), Moscow, Russia;
3 Russian Medical Academy of Continuous Professional Education, Moscow, Russia
sshekshina@yandex.ru
Abstract
Aim. To evaluate the nature and outcomes of acute kidney injury in patients with combat trauma.
Materials and methods. The prospective observational study enrolled 54 patients who had suffered from combat trauma within 2 to 101 days (median 10.5 days; Q1–Q3: 5–21 days) before admission to hospital. All study participants were men. The mean age of patients was 38.9±9.9 years, ranging from 21 to 65 years. All wounded underwent clinical, laboratory and instrumental examination using standard methods for examining patients with combat injuries. Glomerular filtration rate (GFR) was calculated using two equations – CKD-EPI and MDRD.
Results. The mean creatinine concentration at the time of hospitalization was 296.6±174.5 μmol/l, urea – 20.9±9.6 mmol/l, GFR (MDRD) – 33.8±24.2 ml/min, GFR (CKD-EPI) – 37.8±27.8 ml/min. At the previous stages of evacuation, the mean creatinine concentration reached 396.7±203.2 μmol/l, urea – 23.0±11.3 mmol/l, GFR (MDRD) – 22.8±17.7 ml/min, GFR (CKD-EPI) – 24.1±19.7 ml/min. Significant correlations were established between the blood creatinine level and: urea (r=0.73; p<0.000001), total protein (r= -0.33; p=0.01), hemoglobin (r= -0.43; p=0.001). The blood concentration of urea correlated with albumin (r= -0.32; p=0.02), platelet count (r= -0.31; p=0.02) and the percentage of neutrophils (r=0.33; p=0.01). The mean duration of follow-up in the hospital was 58.2±35.6 days. During the observation, 9 patients (16.7%) died, 37 patients (68.5%) were discharged or transferred to other hospitals, 8 wounded continue treatment in the hospital (14.8%). During the observation period, the creatinine level decreased from 408.8 to 92.0 μmol/l (p<0.000001), urea – from 18.9 to 6.5 mmol/l (p=0.000001). Creatinine levels normalized in 62% of patients; out of 19 patients with persistently elevated creatinine levels, 6 cases ended in death. Blood urea concentration remained elevated in 32% of cases (5 of them with a fatal outcome). Renal replacement therapy was required in 55.6% of patients.
Conclusion. Patients with severe combat trauma often develop acute kidney injury – prerenal (caused mainly by traumatic shock) or renal. In most cases, this kidney injury is reversible.
Keywords: acute kidney injury, combat trauma, creatinine, glomerular filtration rate (GFR), shock.
For citation: Topolyanskaya S.V., Kostoeva Kh.Ya., Pilyarova M.Kh., Bubman L.I., Buriev I.M., Lytkina K.A., Ratchina S.A., Melkonyan G.G. Renal injury in patients with combat trauma: a single center experience. Clinical review for general practice. 2026; 7 (1): 105–111 (In Russ.). DOI: 10.47407/kr2026.7.1.00762
Введение
Полиорганная недостаточность, включая острое почечное повреждение (ОПП), является третьей по значимости причиной смерти после кровотечения и черепно-мозговой травмы у пациентов с различными видами травм [1]. При этом частота развития ОПП у пациентов с небоевыми травмами может доходить до 50% [2, 3]. ОПП независимо связано с увеличением продолжительности госпитализации пациентов с травмами и смертностью, которая может достигать 14,9–57% [3, 4]. Тяжелая травма запускает факторы риска повреждения почек, включая кровотечение, рабдомиолиз, воспалительные реакции, усугубляющиеся инфекционными осложнениями или экстренными оперативными вмешательствами, которые могут вызвать дополнительное повреждение почек и нарушение их функций [2].
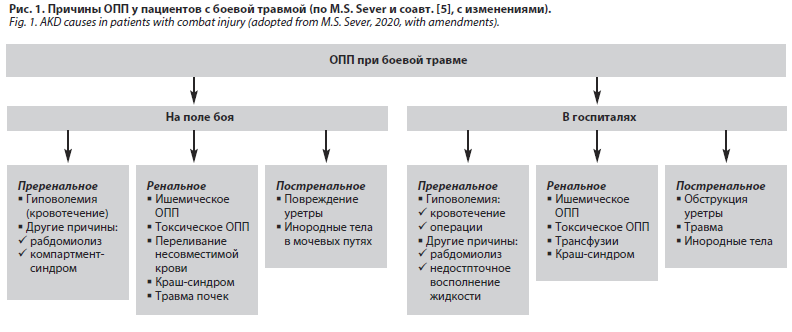
ОПП часто встречается и во время военных конфликтов и вносит значительный вклад в общее число погибших [5]. ОПП как осложнение боевой травмы нередко возникало в каждом крупном военном конфликте, начиная с момента его первоначального описания во время Второй мировой войны и до наших дней [6, 7]. Почечное повреждение у пациентов с боевыми травмами может развиться в результате самой травмы с повреждением различных органов и систем, кровотечения и гиповолемии, воздействия химических веществ и токсичных аэрозолей, а также синдрома сдавления [5]. В целом патофизиология преренального, ренального и постренального ОПП в условиях военных конфликтов такая же, как и у других вариантов повреждения почек [8]. Особое значение в условиях активных боевых действий может иметь большая распространенность синдрома сдавления [9]. Преренальное, ренальное или постренальное ОПП может возникать как на поле боя, так и на всех последующих этапах эвакуации [5] (рис. 1).
Данные о частоте ОПП в ходе различных военных конфликтов крайне немногочисленны и противоречивы [5, 6]. Так, во время Второй мировой войны ОПП регистрировалось у 18% тяжелораненых [6].
В ходе военных конфликтов в Ираке и Афганистане распространенность ОПП варьировала от 13 до 34% [3, 6, 7, 9–11]. По данным американских исследователей, острое почечное повреждение возникает у 34,3% тяжелораненых, находящихся в отделениях интенсивной терапии; в подавляющем большинстве случаев (80,5%) – в течение первых двух дней после госпитализации [11, 12]. Однако ни одно из этих исследований не отражает истинную частоту ОПП во время военных конфликтов из-за неточной регистрации, проблем диагностики и логистических препятствий. Частота встречаемости ОПП может значительно варьировать в зависимости от изучаемой популяции и применяемых критериев диагностики. [3, 5, 6]. Кроме того, на риск возникновения ОПП оказывают влияние тип используемого оружия, время с момента ранения, эффективность первоначальной помощи и скорость эвакуации. Важное значение имеют при этом тяжесть боевой травмы и ее тип (обусловливающий либо гиповолемический шок, вызванный кровотечением, либо синдром сдавления, связанный с тупой травмой; см. рис. 1), воздействие нефротоксичных веществ, а также иные осложнения, связанные с ранением [5].
Развитие ОПП ожидаемо связано с увеличением смертности как среди гражданских лиц, так и среди военных [2, 6]. По данным американских исследователей, зарегистрированная смертность от ОПП среди боевых потерь варьировала от 13 до 22% [10]. Тяжелое ОПП (определяемое как 3-кратное повышение уровня креатинина, абсолютное значение уровня креатинина ≥4 мг/дл или необходимость в заместительной почечной терапии – ЗПТ), хотя и встречается относительно редко (1–5%), ассоциируется с еще большим увеличением смертности (до 65%) [3, 10, 11, 13, 14]. А среди пострадавших, которым требуется проведение ЗПТ, смертность, связанная с посттравматическим ОПП, может достигать 63–75% [12, 15]. Однако благодаря более широкому применению ЗПТ в последнее время показатели смертности от ОПП среди раненых существенно снизились [5]. Немаловажное значение может иметь и долгосрочный прогноз у раненых и пострадавших, перенесших ОПП. Поскольку даже единственный эпизод ОПП может повысить риск развития хронической болезни почек (ХБП) в будущем, пациенты с посттравматическим ОПП, которым требуется проведение ЗПТ, даже после восстановления нормальной функции почек могут подвергаться в дальнейшем риску развития ХБП, ассоциирующейся с увеличением смертности в долгосрочной перспективе [16]. По данным I.J. Stewart и соавт., в когорте из 3846 тяжелораненых военнослужащих США острое повреждение почек в дальнейшем было связано почти с 5-кратным увеличением заболеваемости ХБП [17].
Учитывая крайне немногочисленные и противоречивые данные литературы, посвященной ОПП у пациентов с боевыми травмами, мы предприняли свое исследование по изучению почечного повреждения у раненых в ходе текущего военного конфликта.
Цель исследования – оценить характер и исходы ОПП у пациентов с боевыми ранениями.
Материалы и методы
Проспективное наблюдательное исследование выполнено на клинической базе Госпиталя для ветеранов войн №3 Департамента здравоохранения г. Москвы (ГВВ №3). В исследование включали раненых с ОПП, находящихся на стационарном лечении в ГВВ №3 в период с 01.09.2024 по 01.06.2025.
В рамках данного исследования всем раненым проводилось клиническое, лабораторное и инструментальное обследование с использованием стандартных методов обследования пациентов с боевыми травмами, включая общий и биохимический анализы крови. Наряду с этим проводился расчет скорости клубочковой фильтрации (СКФ) с использованием двух уравнений – CKD-EPI и MDRD.
Полученные данные анализировали с использованием программного обеспечения Statistica (версия 13). Количественные переменные исследовали на нормальность распределения с помощью критерия Шапиро–Уилка. При нормальном распределении описание количественных переменных представляли в виде минимального, максимального, среднего значений и стандартного отклонения (M±SD), качественных – в виде n (%), при ненормальном распределении – в виде медианы и квартилей (Me [Q1; Q3]). При сравнении групп использовали непараметрические методы (критерий Манна–Уитни). Проводили корреляционный анализ с помощью критерия Спирмена.
 Результаты
Результаты
В исследование включены 54 пациента, перенесших боевое ранение в сроки от 2 до 101 дня (10,5 [5,0; 21,0] дня) до поступления в стационар. Все участники исследования были мужчинами. Средний возраст пациентов составлял 38,9±9,9 года, варьируя от 21 года до 65 лет.
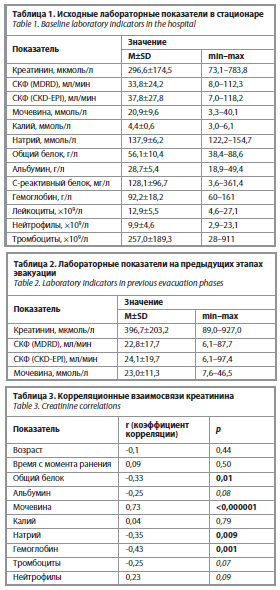
Исходные лабораторные показатели на момент включения пациентов в исследование представлены в табл. 1, известные показатели на предыдущих этапах эвакуации – в табл. 2.
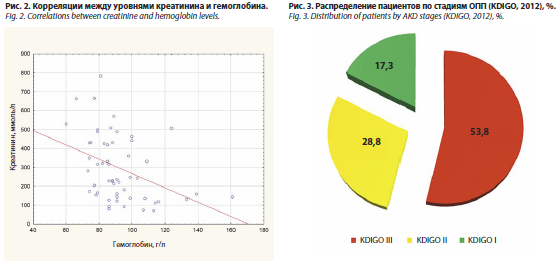
Корреляционные взаимосвязи уровня креатинина при поступлении представлены в табл. 3 и на рис. 2. Концентрация мочевины в крови на момент поступления в стационар достоверно коррелировала с показателями альбумина (r= -0,32; p=0,02), числом тромбоцитов (r= -0,31; p=0,02) и процентной долей нейтрофилов (r=0,33; p=0,01).
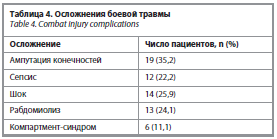
Распределение пациентов по стадиям ОПП (KDIGO, 2012) представлено на рис. 3.
Частота встречаемости некоторых осложнений боевой травмы в изученной группе пациентов представлена в табл. 4.
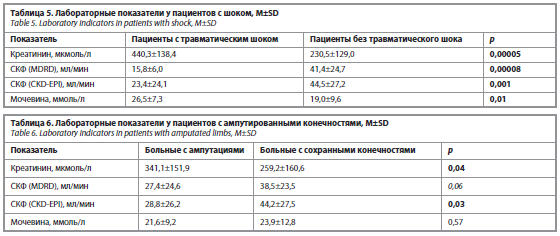
Показатели почечной функции у раненых с диагностированным шоком представлены в табл. 5, с ампутированными конечностями – в табл. 6.
В наблюдаемой группе пациентов достоверных различий по изучаемым показателям почечной функции у раненых с сепсисом и без септических осложнений не обнаружено.
Диагноз рабдомиолиза на предыдущих этапах эвакуации был поставлен 13 из 54 пациентов (24,1%). На момент поступления в стационар пациенты с рабдомиолизом имели достоверно меньший уровень общего белка (52,0±8,9 и 57,3±10,7 г/л соответственно; p=0,03) и более высокий уровень аланинаминотрансферазы (160,1 и 62,3 Ед/л соответственно; p=0,07). Других значимых различий, включая показатели почечной функции, не обнаружено. По данным медицинской документации, медиана показателя креатинфосфокиназы на предшествующих этапах эвакуации составила 6767 [729; 22 671] Ед/л.
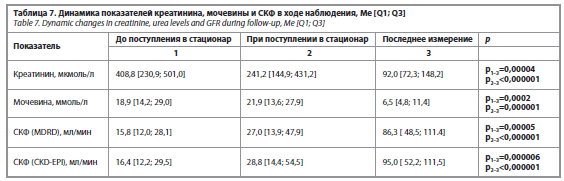
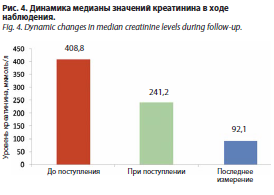
 Средняя продолжительность наблюдения в стационаре составила 58,2±35,6 дня (от 1 до 203 дней). Медиана наблюдения – 56,0 [38,0; 74,5] дня. За время наблюдения умерли 9 (16,7%) пациентов, выписаны или переведены в другие стационары – 37 (68,5%); 8 (14,8%) раненых продолжают лечение в стационаре. Динамика показателей креатинина, мочевины и СКФ представлена в табл. 7 и на рис. 4.
Средняя продолжительность наблюдения в стационаре составила 58,2±35,6 дня (от 1 до 203 дней). Медиана наблюдения – 56,0 [38,0; 74,5] дня. За время наблюдения умерли 9 (16,7%) пациентов, выписаны или переведены в другие стационары – 37 (68,5%); 8 (14,8%) раненых продолжают лечение в стационаре. Динамика показателей креатинина, мочевины и СКФ представлена в табл. 7 и на рис. 4.
За время наблюдения показатели креатинина нормализовались у 62% пациентов, оставались повышенными – у 48% (19 пациентов). Из 19 раненых с повышенным уровнем креатинина 6 умерли, однако во всех случаях патология почек не являлась непосредственной причиной смертельного исхода. У 10 из 19 пациентов с сохранявшимся повышением концентрации креатинина в крови его последний уровень был менее 200 мкмоль/л, у 4 – в диапазоне от 203 до 280 мкмоль/л, еще у 4 – от 329 до 392 мкмоль/л, у оставшегося раненого – 517 мкмоль/л. Уровень мочевины нормализовался у 34 (68%) пациентов, у 9 пациентов он сохранялся повышенным в диапазоне от 9,1 до 19,4 ммоль/л, еще у 6 – от 22,4 до 29,2 ммоль/л, у последнего (умершего) пациента на момент смерти концентрация мочевины достигала 46,3 ммоль/л.
По данным медицинской документации, сеансы ЗПТ на различных этапах эвакуации проводились у 30 (55,6%) пациентов. В группе раненых, которым были проведены сеансы ЗПТ, уровень креатинина снизился с 520,3±175,2 до 106,6±73,5 мкмоль/л (p=0,0000004), у пациентов без экстракорпоральных процедур – с 239,3±102,5 до 119,2±60,9 мкмоль/л (p=0,02).
Обсуждение
Наша серия случаев описывает пациентов с боевой травмой, у которых развилось ОПП. На момент поступления в стационар медиана уровня креатинина у наших пациентов составляла 241,2 мкмоль/л. В исследовании D. Zonies и соавт. у военнослужащих США с ОПП пиковый уровень креатинина в плазме крови варьировал от 123,8 до 371,3 мкмоль/л, составляя в среднем 291,7 мкмоль/л [14]. В этом исследовании 88,8% пациентов пострадали от минно-взрывного ранения [14]; в нашей серии случаев минно-взрывные ранения наблюдались у 80% раненых, у оставшихся пациентов ранения были осколочными. Еще в одной, ретроспективной, серии из 51 случая посттравматического ОПП, требующего проведения ЗПТ, 88% ранений были минно-взрывными или осколочными [13].
В изученной группе пациентов при поступлении в стационар уровень креатинина был ниже, чем на предыдущих этапах эвакуации, где медиана его значений достигала 408,8 мкмоль/л. Это согласуется с предшествующими данными американских исследователей, свидетельствующими о том, что у абсолютного большинства раненых ОПП возникает в первые дни после ранения [11, 12]. По данным K.D. Heegard и соавт., у 80,5% раненых ОПП возникало в первые 2 дня после госпитализации [11]. В когортном исследовании A. Harrois и соавт. у пациентов с небоевыми травмами острое почечное повреждение развивалось в первые 5 дней [2], тогда как в нашей серии медиана поступления в стационар составила 10,5 дня.
Ожидаемо, что ОПП регистрируется в основном у тяжелораненых; до 34,3% в этой группе раненых могут иметь ОПП [11, 12]. Среди наших пациентов 72,3% находились на лечении в отделении реанимации и интенсивной терапии.
В нашей группе пациентов лишь у одного при поступлении регистрировалась небольшая гиперкалиемия (6,06 ммоль/л). Напротив, данные других авторов свидетельствуют о том, что до ⅓ раненых с почечной недостаточностью имеют тяжелую гиперкалиемию в течение первых 4 дней после ранения [12]. В уже упомянутом выше исследовании D. Zonies и соавт. у всех 9 военнослужащих с ОПП развилась критическая гиперкалиемия со средними показателями калия в крови 6,4 ммоль/л [14]. Одним из возможных объяснений низкой встречаемости гиперкалиемии в нашей серии случаев могут быть большие сроки, прошедшие с момента ранения, а также проведение ЗПТ на предшествующих этапах эвакуации у 55,6% пациентов. Следует отметить, что в абсолютном большинстве случаев данные об уровне калия на предшествующих этапах эвакуации были недоступны.
В течение 56 дней наблюдения у 62% наших пациентов нормализовался уровень креатинина, у 68% – мочевины. В ретроспективном исследовании с участием 73 тяжелораненых военнослужащих США восстановление функции почек произошло в 86% случаев [7]. В американской работе только 15% пациентов с острым почечным повреждением потребовалась ЗПТ [7], тогда как в нашей серии случаев она проводилась у 55,6% пациентов. В исследовании D. Zonies и соавт. всем 9 военнослужащим с ОПП потребовалась ЗПТ [14].
В нашей серии случаев смертельный исход зарегистрирован у 9 (16,7%) пациентов, однако во всех случаях патология почек не являлась непосредственной причиной смерти. В исследовании J.A. Bolanos и соавт. в течение 60 дней наблюдения смертность от всех причин в группе из 51 раненого с ОПП, потребовавшим проведения ЗПТ, составила 22% [13]. У остальных раненых к концу периода наблюдения, составившего 1158 дней, средний уровень креатинина снизился до 75,1 мкмоль/л, а расчетная СКФ повысилась до 118 мл/мин, при этом ни у одного из пациентов СКФ не была ниже 60 мл/мин [13]. В нашей серии случаев к концу наблюдения у 14 пациентов СКФ составляла менее 60 мл/мин (шестеро из этих раненых умерли), однако период наблюдения у нас был намного меньше – 56 дней по сравнению с 1158 днями. Медиана последнего значения СКФ среди наших раненых составила 86,3 мл/мин, креатинина – 92,0 мкмоль/л. Стоит отметить, что расчетная СКФ может быть несколько завышена в нашей группе раненых в связи с тем, что 35,2% из них перенесли ампутации с нередкой утратой достаточно больших сегментов конечностей.
В изученной группе пациентов обращала на себя внимание высокая частота таких осложнений, как сепсис (22,2%), рабдомиолиз (24,1%), травматический шок (25,9%) и ампутации (35,2%). Аналогично нашим данным, в исследовании B. Muñoz и соавт. также часто встречалась бактериемия, диагностированная у 53% раненых с посттравматическим ОПП, и пациенты с ОПП в целом имели существенно большую частоту внутрибольничных инфекций по сравнению с ранеными без ОПП [7].
У наших раненых с травматическим шоком регистрировались значительно более высокие значения креатинина (440,3 и 230,5 мкмоль/л соответственно) и мочевины (26,5 и 19,0 ммоль/л соответственно) наряду с более низкими показателями СКФ (15,8 и 41,4 мл/мин соответственно) по сравнению с пациентами, у которых в медицинской документации не было упоминания про шок. В крупном исследовании A. Harrois и соавт. с участием 3111 пациентов с небоевой травмой частота ОПП составляла 13%, а у пациентов с геморрагическим шоком этот показатель возрастал до 42,5% [2]. При проведении многофакторного анализа геморрагический шок оказался независимым фактором риска ОПП [2]. В этой работе дополнительным фактором риска возникновения ОПП была тяжесть рабдомиолиза [2].
Взаимосвязь между рабдомиолизом и ОПП хорошо известна в контексте небоевой травмы. Что касается боевых ранений, то в ряде работ также подтверждена связь между тяжестью рабдомиолиза и развитием ОПП [9, 13, 18]. Так, в исследовании J.A. Bolanos и соавт. рабдомиолиз был предполагаемой причиной ОПП у 72% военнослужащих, которым потребовалось проведение ЗПТ [13]. В работе J. Elterman и соавт. рабдомиолиз (определяемый как уровень креатинфосфокиназы >5000 МЕ/л) развился в 24,8% случаев, а ОПП – в 20,7% [9]. Наиболее частым (у 71% пациентов) механизмом травмы в этом исследовании, как и в нашем, был минно-взрывной. Авторы упомянутой работы пришли к выводу о том, что повышенные пиковые уровни креатинфосфокиназы у раненых слабо связаны с развитием ОПП, но тем не менее не являются прогностическими [9]. В этой работе медиана максимального значения креатинфосфокиназы составила 4178 Ед/л, тогда как в нашей – 6767 Ед/л. Вместе с тем I.J. Stewart и соавт. продемонстрировали, что у пострадавших в боевых действиях при возникновении рабдомиолиза наблюдается более чем двукратное увеличение риска развития ОПП, а влияние рабдомиолиза на смертность может быть опосредовано именно ОПП [18].
Среди наших раненых диагноз рабдомиолиза на предыдущих этапах эвакуации был поставлен в 24,1% случаев, что намного превышает встречаемость данного осложнения в других группах наблюдаемых нами раненых. Однако при поступлении к нам в стационар клинические проявления рабдомиолиза уже стихали, что было обусловлено прежде всего давностью ранения, а также применением экстракорпоральных методов лечения.
Еще одним фактором, способным повлиять на возникновение и течение ОПП в нашей группе пациентов, могли быть ампутации конечностей, наблюдавшиеся в 35,1% случаев. Немаловажно, что среди наших пациентов с ОПП частота ампутаций была выше (35,1%), чем в других группах наблюдаемых нами раненых (25–27%). Так, в исследовании I.J. Stewart и соавт. с участием 3807 военнослужащих, тяжело раненных в Ираке и Афганистане, ампутации были одним из значимых предикторов острого почечного повреждения, повышающим риск его возникновения в 1,46 раза [3]. Другим предиктором ОПП в этой работе было низкое артериальное давление, повышающее риск развития ОПП в 1,6 раза [3], что нашло подтверждение и в наших данных о взаимосвязи ОПП и шока.
И, наконец, определенное значение в возникновении почечного повреждения у наших пациентов могло иметь и проникающее ранение органов брюшной полости и таза, наблюдавшееся у 15 из 54 раненых (27,8%). По данным T. Ząbkowski и соавт., в среднем около 8–10% травм живота, как тупых, так и проникающих, затрагивают почки [19]. Проникающие и даже тупые ранения не только способствуют прямому повреждению паренхиматозных органов, включая почки, но и могут вызвать повреждение сосудов с последующей массивной кровопотерей и даже шоком [19].
Заключение
Результаты исследования свидетельствуют о том, что у пациентов с тяжелыми боевыми ранениями нередко развивается ОПП – преренальное (обусловленное, главным образом, травматическим шоком) или ренальное. В большинстве случаев это почечное повреждение обратимо. Необходимо продолжение исследований по изучению ОПП и его исходов у пациентов с боевыми травмами.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare no conflict of interest.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Тополянская Светлана Викторовна – д-р мед. наук, проф. каф. госпитальной терапии №2 ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет), врач-терапевт Госпиталя для ветеранов войн №3 ДЗМ. E-mail: sshekshina@yahoo.com; ORCID: 0000-0002-4131-8432
Svetlana V. Topolyanskaya – Dr. Sci. (Med.), Prof., Sechenov First Moscow State Medical University (Sechenov University), therapist, War Veterans Hospital No. 3. E-mail: sshekshina@yahoo.com; ORCID: 0000-0002-4131-8432
Костоева Хава Якуповна – студентка ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет). E-mail: e.kostoeva02@mail.ru
Khava Ya. Kostoeva – Student, Sechenov First Moscow State Medical University (Sechenov University). E-mail: e.kostoeva02@mail.ru
Пилярова Медина Халитовна – врач-терапевт Госпиталя для ветеранов войн №3 ДЗМ. E-mail: pilyarovamk@zdrav.mos.ru
Medina Kh. Pilyarova – therapist, War Veterans Hospital No. 3. E-mail: pilyarovamk@zdrav.mos.ru
Бубман Леонид Игоревич – врач-хирург Госпиталя для ветеранов войн №3. E-mail: bubmanli@zdrav.mos.ru; ORCID: 0000-0002-4195-3188
Leonid I. Bubman – surgeon, War Veterans Hospital No. 3. E-mail: bubmanli@zdrav.mos.ru; ORCID: 0000-0002-4195-3188
Буриев Илья Михайлович – д-р мед. наук, проф., советник глав. врача по хирургии Госпиталя для ветеранов войн №3.
E-mail: burievim@zdrav.mos.ru
Ilya M. Buriev – Dr. Sci. (Med.), Full Prof., Advisor to the Chief Doctor for Surgery War Veterans Hospital No. 3. E-mail: burievim@zdrav.mos.ru
Лыткина Каринэ Арнольдовна – канд. мед. наук, зам. глав. врача по терапии Госпиталя для ветеранов войн №3. E-mail: lytkinaka@zdrav.mos.ru; ORCID: 0000-0001-9647-7492
Karine A. Lytkina – Cand. Sci. (Med.), Deputy Chief Doctor for Therapeutic Care, War Veterans Hospital No. 3. E-mail: lytkinaka@zdrav.mos.ru; ORCID: 0000-0001-9647-7492
Рачина Светлана Александровна – д-р мед. наук, проф., зав. каф. госпитальной терапии №2 ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет). E-mail: svetlana.ratchina@antibiotic.ru; ORCID: 0000-0002-3329-7846
Svetlana A. Rachina – Dr. Sci. (Med.), Full Prof., Sechenov First Moscow State Medical University (Sechenov University). E-mail: svetlana.ratchina@antibiotic.ru; ORCID: 0000-0002-3329-7846
Мелконян Георгий Геннадьевич – д-р мед. наук, проф., глав. врач Госпиталя для ветеранов войн №3, проф. каф. хирургии ФГБОУ ДПО «Российская медицинская академия непрерывного медицинского образования». E-mail: gvv3@zdrav.mos.ru; ORCID: 0000-0002-4021-5044
Georgiy G. Melkonyan – Dr. Sci. (Med.), Full Prof., Russian Medical Academy of Continuous Professional Education, Chief Doctor, War Veterans Hospital No. 3. E-mail: gvv3@zdrav.mos.ru; ORCID: 0000-0002-4021-5044
Поступила в редакцию: 14.08.2025
Поступила после рецензирования: 22.08.2025
Принята к публикации: 28.08.2025
Received: 14.08.2025
Revised: 22.08.2025
Accepted: 28.08.2025
Клинический разбор в общей медицине №01 2026
Почечное повреждение у пациентов с боевыми травмами: опыт одного центра
Номера страниц в выпуске:105-111
Аннотация
Цель. Оценить характер и исходы острого почечного повреждения у пациентов с боевыми ранениями.
Материалы и методы. В проспективное наблюдательное исследование включены 54 пациента, перенесших боевое ранение в сроки от 2 до 101 дня (10,5 [5,0; 21,0] дня) до поступления в стационар. Все участники исследования были мужчинами. Средний возраст пациентов составлял 38,9±9,9 года, варьируя от 21 года до 65 лет. Всем раненым проводилось клиническое, лабораторное и инструментальное обследование с использованием стандартных методов обследования пациентов с боевыми травмами. Скорость клубочковой фильтрации (СКФ) рассчитывали с использованием двух уравнений – CKD-EPI и MDRD.
Результаты. Средняя концентрация креатинина на момент госпитализации в стационар составила 296,6±174,5 мкмоль/л, мочевины – 20,9±9,6 ммоль/л, СКФ (MDRD) – 33,8±24,2 мл/мин, СКФ (CKD-EPI) – 37,8±27,8 мл/мин. На предыдущих этапах эвакуации средняя концентрация креатинина достигала 396,7±203,2 мкмоль/л, мочевины – 23,0±11,3 ммоль/л, СКФ (MDRD) – 22,8±17,7 мл/мин, СКФ (CKD-EPI) – 24,1±19,7 мл/мин. Установлены достоверные корреляции между уровнем креатинина крови и мочевины (r=0,73; p<0,000001), общего белка (r= -0,33; p=0,01), гемоглобина (r= -0,43; p=0,001). Концентрация мочевины в крови коррелировала с уровнем альбумина (r= -0,32; p=0,02), числом тромбоцитов (r= -0,31; p=0,02) и процентной долей нейтрофилов (r=0,33; p=0,01). Средняя продолжительность наблюдения в стационаре составила 58,2±35,6 дня. За время наблюдения умерли 9 (16,7%) пациентов, выписаны или переведены в другие стационары 37 (68,5%) пациентов, продолжают лечение в стационаре 8 (14,8%) раненых. За период наблюдения уровень креатинина снизился с 408,8 до 92,0 мкмоль/л (p<0,000001), мочевины – с 18,9 до 6,5 ммоль/л (p=0,000001). Показатели креатинина нормализовались у 62% пациентов; из 19 пациентов с сохранением повышенного уровня креатинина 6 случаев закончились смертельным исходом. Концентрация мочевины в крови оставалась повышенной в 32% случаев (5 из них – со смертельным исходом). Проведение заместительной почечной терапии потребовалось у 55,6% пациентов.
Заключение. У пациентов с тяжелыми боевыми ранениями нередко развивается острое почечное повреждение – преренальное (обусловленное, главным образом, травматическим шоком) или ренальное. В большинстве случаев это почечное повреждение обратимо.
Ключевые слова: острое почечное повреждение, боевая травма, креатинин, скорость клубочковой фильтрации (СКФ), шок.
Для цитирования: Тополянская С.В., Костоева Х.Я., Пилярова М.Х., Бубман Л.И., Буриев И.М., Лыткина К.А., Рачина С.А., Мелконян Г.Г. Почечное повреждение у пациентов с боевыми травмами: опыт одного центра. Клинический разбор в общей медицине. 2026; 7 (1): 105–111. DOI: 10.47407/kr2026.7.1.00762
Цель. Оценить характер и исходы острого почечного повреждения у пациентов с боевыми ранениями.
Материалы и методы. В проспективное наблюдательное исследование включены 54 пациента, перенесших боевое ранение в сроки от 2 до 101 дня (10,5 [5,0; 21,0] дня) до поступления в стационар. Все участники исследования были мужчинами. Средний возраст пациентов составлял 38,9±9,9 года, варьируя от 21 года до 65 лет. Всем раненым проводилось клиническое, лабораторное и инструментальное обследование с использованием стандартных методов обследования пациентов с боевыми травмами. Скорость клубочковой фильтрации (СКФ) рассчитывали с использованием двух уравнений – CKD-EPI и MDRD.
Результаты. Средняя концентрация креатинина на момент госпитализации в стационар составила 296,6±174,5 мкмоль/л, мочевины – 20,9±9,6 ммоль/л, СКФ (MDRD) – 33,8±24,2 мл/мин, СКФ (CKD-EPI) – 37,8±27,8 мл/мин. На предыдущих этапах эвакуации средняя концентрация креатинина достигала 396,7±203,2 мкмоль/л, мочевины – 23,0±11,3 ммоль/л, СКФ (MDRD) – 22,8±17,7 мл/мин, СКФ (CKD-EPI) – 24,1±19,7 мл/мин. Установлены достоверные корреляции между уровнем креатинина крови и мочевины (r=0,73; p<0,000001), общего белка (r= -0,33; p=0,01), гемоглобина (r= -0,43; p=0,001). Концентрация мочевины в крови коррелировала с уровнем альбумина (r= -0,32; p=0,02), числом тромбоцитов (r= -0,31; p=0,02) и процентной долей нейтрофилов (r=0,33; p=0,01). Средняя продолжительность наблюдения в стационаре составила 58,2±35,6 дня. За время наблюдения умерли 9 (16,7%) пациентов, выписаны или переведены в другие стационары 37 (68,5%) пациентов, продолжают лечение в стационаре 8 (14,8%) раненых. За период наблюдения уровень креатинина снизился с 408,8 до 92,0 мкмоль/л (p<0,000001), мочевины – с 18,9 до 6,5 ммоль/л (p=0,000001). Показатели креатинина нормализовались у 62% пациентов; из 19 пациентов с сохранением повышенного уровня креатинина 6 случаев закончились смертельным исходом. Концентрация мочевины в крови оставалась повышенной в 32% случаев (5 из них – со смертельным исходом). Проведение заместительной почечной терапии потребовалось у 55,6% пациентов.
Заключение. У пациентов с тяжелыми боевыми ранениями нередко развивается острое почечное повреждение – преренальное (обусловленное, главным образом, травматическим шоком) или ренальное. В большинстве случаев это почечное повреждение обратимо.
Ключевые слова: острое почечное повреждение, боевая травма, креатинин, скорость клубочковой фильтрации (СКФ), шок.
Для цитирования: Тополянская С.В., Костоева Х.Я., Пилярова М.Х., Бубман Л.И., Буриев И.М., Лыткина К.А., Рачина С.А., Мелконян Г.Г. Почечное повреждение у пациентов с боевыми травмами: опыт одного центра. Клинический разбор в общей медицине. 2026; 7 (1): 105–111. DOI: 10.47407/kr2026.7.1.00762
Renal injury in patients with combat trauma: a single center experience
Svetlana V. Topolyanskaya1,2, Khava Ya. Kostoeva2, Medina Kh. Pilyarova1, Leonid I. Bubman1, Ilya M. Buriev1, Karine A. Lytkina1, Svetlana A. Rachina2, Georgiy G. Melkonyan1,31 War Veterans Hospital No. 3, Moscow, Russia;
2 Sechenov Moscow State Medical University (Sechenov University), Moscow, Russia;
3 Russian Medical Academy of Continuous Professional Education, Moscow, Russia
sshekshina@yandex.ru
Abstract
Aim. To evaluate the nature and outcomes of acute kidney injury in patients with combat trauma.
Materials and methods. The prospective observational study enrolled 54 patients who had suffered from combat trauma within 2 to 101 days (median 10.5 days; Q1–Q3: 5–21 days) before admission to hospital. All study participants were men. The mean age of patients was 38.9±9.9 years, ranging from 21 to 65 years. All wounded underwent clinical, laboratory and instrumental examination using standard methods for examining patients with combat injuries. Glomerular filtration rate (GFR) was calculated using two equations – CKD-EPI and MDRD.
Results. The mean creatinine concentration at the time of hospitalization was 296.6±174.5 μmol/l, urea – 20.9±9.6 mmol/l, GFR (MDRD) – 33.8±24.2 ml/min, GFR (CKD-EPI) – 37.8±27.8 ml/min. At the previous stages of evacuation, the mean creatinine concentration reached 396.7±203.2 μmol/l, urea – 23.0±11.3 mmol/l, GFR (MDRD) – 22.8±17.7 ml/min, GFR (CKD-EPI) – 24.1±19.7 ml/min. Significant correlations were established between the blood creatinine level and: urea (r=0.73; p<0.000001), total protein (r= -0.33; p=0.01), hemoglobin (r= -0.43; p=0.001). The blood concentration of urea correlated with albumin (r= -0.32; p=0.02), platelet count (r= -0.31; p=0.02) and the percentage of neutrophils (r=0.33; p=0.01). The mean duration of follow-up in the hospital was 58.2±35.6 days. During the observation, 9 patients (16.7%) died, 37 patients (68.5%) were discharged or transferred to other hospitals, 8 wounded continue treatment in the hospital (14.8%). During the observation period, the creatinine level decreased from 408.8 to 92.0 μmol/l (p<0.000001), urea – from 18.9 to 6.5 mmol/l (p=0.000001). Creatinine levels normalized in 62% of patients; out of 19 patients with persistently elevated creatinine levels, 6 cases ended in death. Blood urea concentration remained elevated in 32% of cases (5 of them with a fatal outcome). Renal replacement therapy was required in 55.6% of patients.
Conclusion. Patients with severe combat trauma often develop acute kidney injury – prerenal (caused mainly by traumatic shock) or renal. In most cases, this kidney injury is reversible.
Keywords: acute kidney injury, combat trauma, creatinine, glomerular filtration rate (GFR), shock.
For citation: Topolyanskaya S.V., Kostoeva Kh.Ya., Pilyarova M.Kh., Bubman L.I., Buriev I.M., Lytkina K.A., Ratchina S.A., Melkonyan G.G. Renal injury in patients with combat trauma: a single center experience. Clinical review for general practice. 2026; 7 (1): 105–111 (In Russ.). DOI: 10.47407/kr2026.7.1.00762
Введение
Полиорганная недостаточность, включая острое почечное повреждение (ОПП), является третьей по значимости причиной смерти после кровотечения и черепно-мозговой травмы у пациентов с различными видами травм [1]. При этом частота развития ОПП у пациентов с небоевыми травмами может доходить до 50% [2, 3]. ОПП независимо связано с увеличением продолжительности госпитализации пациентов с травмами и смертностью, которая может достигать 14,9–57% [3, 4]. Тяжелая травма запускает факторы риска повреждения почек, включая кровотечение, рабдомиолиз, воспалительные реакции, усугубляющиеся инфекционными осложнениями или экстренными оперативными вмешательствами, которые могут вызвать дополнительное повреждение почек и нарушение их функций [2].

ОПП часто встречается и во время военных конфликтов и вносит значительный вклад в общее число погибших [5]. ОПП как осложнение боевой травмы нередко возникало в каждом крупном военном конфликте, начиная с момента его первоначального описания во время Второй мировой войны и до наших дней [6, 7]. Почечное повреждение у пациентов с боевыми травмами может развиться в результате самой травмы с повреждением различных органов и систем, кровотечения и гиповолемии, воздействия химических веществ и токсичных аэрозолей, а также синдрома сдавления [5]. В целом патофизиология преренального, ренального и постренального ОПП в условиях военных конфликтов такая же, как и у других вариантов повреждения почек [8]. Особое значение в условиях активных боевых действий может иметь большая распространенность синдрома сдавления [9]. Преренальное, ренальное или постренальное ОПП может возникать как на поле боя, так и на всех последующих этапах эвакуации [5] (рис. 1).
Данные о частоте ОПП в ходе различных военных конфликтов крайне немногочисленны и противоречивы [5, 6]. Так, во время Второй мировой войны ОПП регистрировалось у 18% тяжелораненых [6].
В ходе военных конфликтов в Ираке и Афганистане распространенность ОПП варьировала от 13 до 34% [3, 6, 7, 9–11]. По данным американских исследователей, острое почечное повреждение возникает у 34,3% тяжелораненых, находящихся в отделениях интенсивной терапии; в подавляющем большинстве случаев (80,5%) – в течение первых двух дней после госпитализации [11, 12]. Однако ни одно из этих исследований не отражает истинную частоту ОПП во время военных конфликтов из-за неточной регистрации, проблем диагностики и логистических препятствий. Частота встречаемости ОПП может значительно варьировать в зависимости от изучаемой популяции и применяемых критериев диагностики. [3, 5, 6]. Кроме того, на риск возникновения ОПП оказывают влияние тип используемого оружия, время с момента ранения, эффективность первоначальной помощи и скорость эвакуации. Важное значение имеют при этом тяжесть боевой травмы и ее тип (обусловливающий либо гиповолемический шок, вызванный кровотечением, либо синдром сдавления, связанный с тупой травмой; см. рис. 1), воздействие нефротоксичных веществ, а также иные осложнения, связанные с ранением [5].
Развитие ОПП ожидаемо связано с увеличением смертности как среди гражданских лиц, так и среди военных [2, 6]. По данным американских исследователей, зарегистрированная смертность от ОПП среди боевых потерь варьировала от 13 до 22% [10]. Тяжелое ОПП (определяемое как 3-кратное повышение уровня креатинина, абсолютное значение уровня креатинина ≥4 мг/дл или необходимость в заместительной почечной терапии – ЗПТ), хотя и встречается относительно редко (1–5%), ассоциируется с еще большим увеличением смертности (до 65%) [3, 10, 11, 13, 14]. А среди пострадавших, которым требуется проведение ЗПТ, смертность, связанная с посттравматическим ОПП, может достигать 63–75% [12, 15]. Однако благодаря более широкому применению ЗПТ в последнее время показатели смертности от ОПП среди раненых существенно снизились [5]. Немаловажное значение может иметь и долгосрочный прогноз у раненых и пострадавших, перенесших ОПП. Поскольку даже единственный эпизод ОПП может повысить риск развития хронической болезни почек (ХБП) в будущем, пациенты с посттравматическим ОПП, которым требуется проведение ЗПТ, даже после восстановления нормальной функции почек могут подвергаться в дальнейшем риску развития ХБП, ассоциирующейся с увеличением смертности в долгосрочной перспективе [16]. По данным I.J. Stewart и соавт., в когорте из 3846 тяжелораненых военнослужащих США острое повреждение почек в дальнейшем было связано почти с 5-кратным увеличением заболеваемости ХБП [17].
Учитывая крайне немногочисленные и противоречивые данные литературы, посвященной ОПП у пациентов с боевыми травмами, мы предприняли свое исследование по изучению почечного повреждения у раненых в ходе текущего военного конфликта.
Цель исследования – оценить характер и исходы ОПП у пациентов с боевыми ранениями.
Материалы и методы
Проспективное наблюдательное исследование выполнено на клинической базе Госпиталя для ветеранов войн №3 Департамента здравоохранения г. Москвы (ГВВ №3). В исследование включали раненых с ОПП, находящихся на стационарном лечении в ГВВ №3 в период с 01.09.2024 по 01.06.2025.
В рамках данного исследования всем раненым проводилось клиническое, лабораторное и инструментальное обследование с использованием стандартных методов обследования пациентов с боевыми травмами, включая общий и биохимический анализы крови. Наряду с этим проводился расчет скорости клубочковой фильтрации (СКФ) с использованием двух уравнений – CKD-EPI и MDRD.
Полученные данные анализировали с использованием программного обеспечения Statistica (версия 13). Количественные переменные исследовали на нормальность распределения с помощью критерия Шапиро–Уилка. При нормальном распределении описание количественных переменных представляли в виде минимального, максимального, среднего значений и стандартного отклонения (M±SD), качественных – в виде n (%), при ненормальном распределении – в виде медианы и квартилей (Me [Q1; Q3]). При сравнении групп использовали непараметрические методы (критерий Манна–Уитни). Проводили корреляционный анализ с помощью критерия Спирмена.
 Результаты
РезультатыВ исследование включены 54 пациента, перенесших боевое ранение в сроки от 2 до 101 дня (10,5 [5,0; 21,0] дня) до поступления в стационар. Все участники исследования были мужчинами. Средний возраст пациентов составлял 38,9±9,9 года, варьируя от 21 года до 65 лет.
Исходные лабораторные показатели на момент включения пациентов в исследование представлены в табл. 1, известные показатели на предыдущих этапах эвакуации – в табл. 2.
Корреляционные взаимосвязи уровня креатинина при поступлении представлены в табл. 3 и на рис. 2. Концентрация мочевины в крови на момент поступления в стационар достоверно коррелировала с показателями альбумина (r= -0,32; p=0,02), числом тромбоцитов (r= -0,31; p=0,02) и процентной долей нейтрофилов (r=0,33; p=0,01).
Распределение пациентов по стадиям ОПП (KDIGO, 2012) представлено на рис. 3.
Частота встречаемости некоторых осложнений боевой травмы в изученной группе пациентов представлена в табл. 4.
Показатели почечной функции у раненых с диагностированным шоком представлены в табл. 5, с ампутированными конечностями – в табл. 6.
В наблюдаемой группе пациентов достоверных различий по изучаемым показателям почечной функции у раненых с сепсисом и без септических осложнений не обнаружено.
Диагноз рабдомиолиза на предыдущих этапах эвакуации был поставлен 13 из 54 пациентов (24,1%). На момент поступления в стационар пациенты с рабдомиолизом имели достоверно меньший уровень общего белка (52,0±8,9 и 57,3±10,7 г/л соответственно; p=0,03) и более высокий уровень аланинаминотрансферазы (160,1 и 62,3 Ед/л соответственно; p=0,07). Других значимых различий, включая показатели почечной функции, не обнаружено. По данным медицинской документации, медиана показателя креатинфосфокиназы на предшествующих этапах эвакуации составила 6767 [729; 22 671] Ед/л.

 Средняя продолжительность наблюдения в стационаре составила 58,2±35,6 дня (от 1 до 203 дней). Медиана наблюдения – 56,0 [38,0; 74,5] дня. За время наблюдения умерли 9 (16,7%) пациентов, выписаны или переведены в другие стационары – 37 (68,5%); 8 (14,8%) раненых продолжают лечение в стационаре. Динамика показателей креатинина, мочевины и СКФ представлена в табл. 7 и на рис. 4.
Средняя продолжительность наблюдения в стационаре составила 58,2±35,6 дня (от 1 до 203 дней). Медиана наблюдения – 56,0 [38,0; 74,5] дня. За время наблюдения умерли 9 (16,7%) пациентов, выписаны или переведены в другие стационары – 37 (68,5%); 8 (14,8%) раненых продолжают лечение в стационаре. Динамика показателей креатинина, мочевины и СКФ представлена в табл. 7 и на рис. 4.За время наблюдения показатели креатинина нормализовались у 62% пациентов, оставались повышенными – у 48% (19 пациентов). Из 19 раненых с повышенным уровнем креатинина 6 умерли, однако во всех случаях патология почек не являлась непосредственной причиной смертельного исхода. У 10 из 19 пациентов с сохранявшимся повышением концентрации креатинина в крови его последний уровень был менее 200 мкмоль/л, у 4 – в диапазоне от 203 до 280 мкмоль/л, еще у 4 – от 329 до 392 мкмоль/л, у оставшегося раненого – 517 мкмоль/л. Уровень мочевины нормализовался у 34 (68%) пациентов, у 9 пациентов он сохранялся повышенным в диапазоне от 9,1 до 19,4 ммоль/л, еще у 6 – от 22,4 до 29,2 ммоль/л, у последнего (умершего) пациента на момент смерти концентрация мочевины достигала 46,3 ммоль/л.
По данным медицинской документации, сеансы ЗПТ на различных этапах эвакуации проводились у 30 (55,6%) пациентов. В группе раненых, которым были проведены сеансы ЗПТ, уровень креатинина снизился с 520,3±175,2 до 106,6±73,5 мкмоль/л (p=0,0000004), у пациентов без экстракорпоральных процедур – с 239,3±102,5 до 119,2±60,9 мкмоль/л (p=0,02).



Обсуждение
Наша серия случаев описывает пациентов с боевой травмой, у которых развилось ОПП. На момент поступления в стационар медиана уровня креатинина у наших пациентов составляла 241,2 мкмоль/л. В исследовании D. Zonies и соавт. у военнослужащих США с ОПП пиковый уровень креатинина в плазме крови варьировал от 123,8 до 371,3 мкмоль/л, составляя в среднем 291,7 мкмоль/л [14]. В этом исследовании 88,8% пациентов пострадали от минно-взрывного ранения [14]; в нашей серии случаев минно-взрывные ранения наблюдались у 80% раненых, у оставшихся пациентов ранения были осколочными. Еще в одной, ретроспективной, серии из 51 случая посттравматического ОПП, требующего проведения ЗПТ, 88% ранений были минно-взрывными или осколочными [13].
В изученной группе пациентов при поступлении в стационар уровень креатинина был ниже, чем на предыдущих этапах эвакуации, где медиана его значений достигала 408,8 мкмоль/л. Это согласуется с предшествующими данными американских исследователей, свидетельствующими о том, что у абсолютного большинства раненых ОПП возникает в первые дни после ранения [11, 12]. По данным K.D. Heegard и соавт., у 80,5% раненых ОПП возникало в первые 2 дня после госпитализации [11]. В когортном исследовании A. Harrois и соавт. у пациентов с небоевыми травмами острое почечное повреждение развивалось в первые 5 дней [2], тогда как в нашей серии медиана поступления в стационар составила 10,5 дня.
Ожидаемо, что ОПП регистрируется в основном у тяжелораненых; до 34,3% в этой группе раненых могут иметь ОПП [11, 12]. Среди наших пациентов 72,3% находились на лечении в отделении реанимации и интенсивной терапии.
В нашей группе пациентов лишь у одного при поступлении регистрировалась небольшая гиперкалиемия (6,06 ммоль/л). Напротив, данные других авторов свидетельствуют о том, что до ⅓ раненых с почечной недостаточностью имеют тяжелую гиперкалиемию в течение первых 4 дней после ранения [12]. В уже упомянутом выше исследовании D. Zonies и соавт. у всех 9 военнослужащих с ОПП развилась критическая гиперкалиемия со средними показателями калия в крови 6,4 ммоль/л [14]. Одним из возможных объяснений низкой встречаемости гиперкалиемии в нашей серии случаев могут быть большие сроки, прошедшие с момента ранения, а также проведение ЗПТ на предшествующих этапах эвакуации у 55,6% пациентов. Следует отметить, что в абсолютном большинстве случаев данные об уровне калия на предшествующих этапах эвакуации были недоступны.
В течение 56 дней наблюдения у 62% наших пациентов нормализовался уровень креатинина, у 68% – мочевины. В ретроспективном исследовании с участием 73 тяжелораненых военнослужащих США восстановление функции почек произошло в 86% случаев [7]. В американской работе только 15% пациентов с острым почечным повреждением потребовалась ЗПТ [7], тогда как в нашей серии случаев она проводилась у 55,6% пациентов. В исследовании D. Zonies и соавт. всем 9 военнослужащим с ОПП потребовалась ЗПТ [14].
В нашей серии случаев смертельный исход зарегистрирован у 9 (16,7%) пациентов, однако во всех случаях патология почек не являлась непосредственной причиной смерти. В исследовании J.A. Bolanos и соавт. в течение 60 дней наблюдения смертность от всех причин в группе из 51 раненого с ОПП, потребовавшим проведения ЗПТ, составила 22% [13]. У остальных раненых к концу периода наблюдения, составившего 1158 дней, средний уровень креатинина снизился до 75,1 мкмоль/л, а расчетная СКФ повысилась до 118 мл/мин, при этом ни у одного из пациентов СКФ не была ниже 60 мл/мин [13]. В нашей серии случаев к концу наблюдения у 14 пациентов СКФ составляла менее 60 мл/мин (шестеро из этих раненых умерли), однако период наблюдения у нас был намного меньше – 56 дней по сравнению с 1158 днями. Медиана последнего значения СКФ среди наших раненых составила 86,3 мл/мин, креатинина – 92,0 мкмоль/л. Стоит отметить, что расчетная СКФ может быть несколько завышена в нашей группе раненых в связи с тем, что 35,2% из них перенесли ампутации с нередкой утратой достаточно больших сегментов конечностей.
В изученной группе пациентов обращала на себя внимание высокая частота таких осложнений, как сепсис (22,2%), рабдомиолиз (24,1%), травматический шок (25,9%) и ампутации (35,2%). Аналогично нашим данным, в исследовании B. Muñoz и соавт. также часто встречалась бактериемия, диагностированная у 53% раненых с посттравматическим ОПП, и пациенты с ОПП в целом имели существенно большую частоту внутрибольничных инфекций по сравнению с ранеными без ОПП [7].
У наших раненых с травматическим шоком регистрировались значительно более высокие значения креатинина (440,3 и 230,5 мкмоль/л соответственно) и мочевины (26,5 и 19,0 ммоль/л соответственно) наряду с более низкими показателями СКФ (15,8 и 41,4 мл/мин соответственно) по сравнению с пациентами, у которых в медицинской документации не было упоминания про шок. В крупном исследовании A. Harrois и соавт. с участием 3111 пациентов с небоевой травмой частота ОПП составляла 13%, а у пациентов с геморрагическим шоком этот показатель возрастал до 42,5% [2]. При проведении многофакторного анализа геморрагический шок оказался независимым фактором риска ОПП [2]. В этой работе дополнительным фактором риска возникновения ОПП была тяжесть рабдомиолиза [2].
Взаимосвязь между рабдомиолизом и ОПП хорошо известна в контексте небоевой травмы. Что касается боевых ранений, то в ряде работ также подтверждена связь между тяжестью рабдомиолиза и развитием ОПП [9, 13, 18]. Так, в исследовании J.A. Bolanos и соавт. рабдомиолиз был предполагаемой причиной ОПП у 72% военнослужащих, которым потребовалось проведение ЗПТ [13]. В работе J. Elterman и соавт. рабдомиолиз (определяемый как уровень креатинфосфокиназы >5000 МЕ/л) развился в 24,8% случаев, а ОПП – в 20,7% [9]. Наиболее частым (у 71% пациентов) механизмом травмы в этом исследовании, как и в нашем, был минно-взрывной. Авторы упомянутой работы пришли к выводу о том, что повышенные пиковые уровни креатинфосфокиназы у раненых слабо связаны с развитием ОПП, но тем не менее не являются прогностическими [9]. В этой работе медиана максимального значения креатинфосфокиназы составила 4178 Ед/л, тогда как в нашей – 6767 Ед/л. Вместе с тем I.J. Stewart и соавт. продемонстрировали, что у пострадавших в боевых действиях при возникновении рабдомиолиза наблюдается более чем двукратное увеличение риска развития ОПП, а влияние рабдомиолиза на смертность может быть опосредовано именно ОПП [18].
Среди наших раненых диагноз рабдомиолиза на предыдущих этапах эвакуации был поставлен в 24,1% случаев, что намного превышает встречаемость данного осложнения в других группах наблюдаемых нами раненых. Однако при поступлении к нам в стационар клинические проявления рабдомиолиза уже стихали, что было обусловлено прежде всего давностью ранения, а также применением экстракорпоральных методов лечения.
Еще одним фактором, способным повлиять на возникновение и течение ОПП в нашей группе пациентов, могли быть ампутации конечностей, наблюдавшиеся в 35,1% случаев. Немаловажно, что среди наших пациентов с ОПП частота ампутаций была выше (35,1%), чем в других группах наблюдаемых нами раненых (25–27%). Так, в исследовании I.J. Stewart и соавт. с участием 3807 военнослужащих, тяжело раненных в Ираке и Афганистане, ампутации были одним из значимых предикторов острого почечного повреждения, повышающим риск его возникновения в 1,46 раза [3]. Другим предиктором ОПП в этой работе было низкое артериальное давление, повышающее риск развития ОПП в 1,6 раза [3], что нашло подтверждение и в наших данных о взаимосвязи ОПП и шока.
И, наконец, определенное значение в возникновении почечного повреждения у наших пациентов могло иметь и проникающее ранение органов брюшной полости и таза, наблюдавшееся у 15 из 54 раненых (27,8%). По данным T. Ząbkowski и соавт., в среднем около 8–10% травм живота, как тупых, так и проникающих, затрагивают почки [19]. Проникающие и даже тупые ранения не только способствуют прямому повреждению паренхиматозных органов, включая почки, но и могут вызвать повреждение сосудов с последующей массивной кровопотерей и даже шоком [19].
Заключение
Результаты исследования свидетельствуют о том, что у пациентов с тяжелыми боевыми ранениями нередко развивается ОПП – преренальное (обусловленное, главным образом, травматическим шоком) или ренальное. В большинстве случаев это почечное повреждение обратимо. Необходимо продолжение исследований по изучению ОПП и его исходов у пациентов с боевыми травмами.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. The authors declare no conflict of interest.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Тополянская Светлана Викторовна – д-р мед. наук, проф. каф. госпитальной терапии №2 ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет), врач-терапевт Госпиталя для ветеранов войн №3 ДЗМ. E-mail: sshekshina@yahoo.com; ORCID: 0000-0002-4131-8432
Svetlana V. Topolyanskaya – Dr. Sci. (Med.), Prof., Sechenov First Moscow State Medical University (Sechenov University), therapist, War Veterans Hospital No. 3. E-mail: sshekshina@yahoo.com; ORCID: 0000-0002-4131-8432
Костоева Хава Якуповна – студентка ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет). E-mail: e.kostoeva02@mail.ru
Khava Ya. Kostoeva – Student, Sechenov First Moscow State Medical University (Sechenov University). E-mail: e.kostoeva02@mail.ru
Пилярова Медина Халитовна – врач-терапевт Госпиталя для ветеранов войн №3 ДЗМ. E-mail: pilyarovamk@zdrav.mos.ru
Medina Kh. Pilyarova – therapist, War Veterans Hospital No. 3. E-mail: pilyarovamk@zdrav.mos.ru
Бубман Леонид Игоревич – врач-хирург Госпиталя для ветеранов войн №3. E-mail: bubmanli@zdrav.mos.ru; ORCID: 0000-0002-4195-3188
Leonid I. Bubman – surgeon, War Veterans Hospital No. 3. E-mail: bubmanli@zdrav.mos.ru; ORCID: 0000-0002-4195-3188
Буриев Илья Михайлович – д-р мед. наук, проф., советник глав. врача по хирургии Госпиталя для ветеранов войн №3.
E-mail: burievim@zdrav.mos.ru
Ilya M. Buriev – Dr. Sci. (Med.), Full Prof., Advisor to the Chief Doctor for Surgery War Veterans Hospital No. 3. E-mail: burievim@zdrav.mos.ru
Лыткина Каринэ Арнольдовна – канд. мед. наук, зам. глав. врача по терапии Госпиталя для ветеранов войн №3. E-mail: lytkinaka@zdrav.mos.ru; ORCID: 0000-0001-9647-7492
Karine A. Lytkina – Cand. Sci. (Med.), Deputy Chief Doctor for Therapeutic Care, War Veterans Hospital No. 3. E-mail: lytkinaka@zdrav.mos.ru; ORCID: 0000-0001-9647-7492
Рачина Светлана Александровна – д-р мед. наук, проф., зав. каф. госпитальной терапии №2 ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет). E-mail: svetlana.ratchina@antibiotic.ru; ORCID: 0000-0002-3329-7846
Svetlana A. Rachina – Dr. Sci. (Med.), Full Prof., Sechenov First Moscow State Medical University (Sechenov University). E-mail: svetlana.ratchina@antibiotic.ru; ORCID: 0000-0002-3329-7846
Мелконян Георгий Геннадьевич – д-р мед. наук, проф., глав. врач Госпиталя для ветеранов войн №3, проф. каф. хирургии ФГБОУ ДПО «Российская медицинская академия непрерывного медицинского образования». E-mail: gvv3@zdrav.mos.ru; ORCID: 0000-0002-4021-5044
Georgiy G. Melkonyan – Dr. Sci. (Med.), Full Prof., Russian Medical Academy of Continuous Professional Education, Chief Doctor, War Veterans Hospital No. 3. E-mail: gvv3@zdrav.mos.ru; ORCID: 0000-0002-4021-5044
Поступила в редакцию: 14.08.2025
Поступила после рецензирования: 22.08.2025
Принята к публикации: 28.08.2025
Received: 14.08.2025
Revised: 22.08.2025
Accepted: 28.08.2025
Список исп. литературыСкрыть список1. Dutton RP, Stansbury LG, Leone S et al. Trauma mortality in mature trauma systems: are we doing better? An analysis of trauma mortality patterns, 1997–2008. J Trauma 2010;69:620-6. DOI: 10.1097/TA.0b013e3181bbfe2a
2. Harrois A, Soyer B, Gauss T et al; Traumabase® Group. Prevalence and risk factors for acute kidney injury among trauma patients: a multicenter cohort study. Crit Care 2018;22(1):344. DOI: 10.1186/s13054-018-2265-9
3. Stewart IJ, Sosnov JA, Howard JT, Chung KK. Acute Kidney Injury in Critically Injured Combat Veterans: A Retrospective Cohort Study. Am J Kidney Dis 2016;68(4):564-70. DOI: 10.1053/j.ajkd.2016.03.419
4. Bagshaw SM, George C, Gibney RT, Bellomo R. A multi-center evaluation of early acute kidney injury in critically ill trauma patients. Ren Fail 2008;30:581-9. DOI: 10.1080/08860220802134649
5. Sever MS, Vanholder R, Lameire N. Acute Kidney Injury in Active Wars and Other Man-Made Disasters. Semin Nephrol 2020;40(4):341-53. DOI: 10.1016/j.semnephrol.2020.06.001
6. Hoareau GL, Beyer CA, Walker LE et al. Renal Replacement Therapy Capability for the Treatment of Combat-Associated Acute Kidney Injury: A Historical Perspective to Plan for Future Conflicts. Mil Med 2019;184(3-4):81-3. DOI: 10.1093/milmed/usy221
7. Muñoz B, Schobel SA, Lisboa FA et al. Clinical risk factors and inflammatory biomarkers of post-traumatic acute kidney injury in combat patients. Surgery 2020;168(4):662-70. DOI: 10.1016/j.surg.2020.04.064
8. Lameire N, Van Biesen W, Vanholder R. Acute renal failure. Lancet 2005;365:417-30. DOI: 10.1016/S0140-6736(05)70238-5
9. Elterman J, Zonies D, Stewart I et al. Rhabdomyolysis and acute kidney injury in the injured war fighter. J Trauma Acute Care Surg 2015;79(4 Suppl 2):S171-4. DOI: 10.1097/TA.0000000000000572
10. Stewart IJ, Tilley MA, Cotant CL et al. Association of AKI with adverse outcomes in burned military casualties. Clin J Am Soc Nephrol 2012;7(2):199-206. DOI: 10.2215/CJN.04420511
11. Heegard KD, Stewart IJ, Cap AP et al. Early acute kidney injury in military casualties. J Trauma Acute Care Surg 2015;78(5):988-93. DOI: 10.1097/TA.0000000000000607
12. Stewart I, Bolanos J, Little D et al. Hyperkalemia and Dialysis in the Deployed Setting (CPG ID: 52). Joint Trauma System Clinical Practice Guideline (JTS CPG). Available at: https://learning-media.allogy.com/api/v1/pdf/22425834-ca98-4008-a68a-7ec23eda12ce/contents
13. Bolanos JA, Yuan CM, Little DJ et al. Outcomes After Post-Traumatic AKI Requiring RRT in United States Military Service Members. Clin J Am Soc Nephrol 2015;10(10):1732-9. DOI: 10.2215/CJN.00890115
14. Zonies D, DuBose J, Elterman J et al. Early implementation of continuous renal replacement therapy optimizes casualty evacuation for combat-related acute kidney injury. J Trauma Acute Care Surg 2013;75(2 Suppl 2):S210-4. DOI: 10.1097/TA.0b013e318299d97a
15. Teschan PE, Post RS, Smith LH, Jr et al. Post-traumatic renal insufficiency in military casualties. I. Clinical characteristics. Am J Med 1955;18:172-86.
16. Lo LJ, Go AS, Chertow GM et al. Dialysis-requiring acute renal failure increases the risk of progressive chronic kidney disease. Kidney Int 2009;76(8):893-99. DOI: 10.1038/ki.2009.289
17. Stewart IJ, Sosnov JA, Howard JT et al. Retrospective Analysis of Long-Term Outcomes After Combat Injury: A Hidden Cost of War. Circulation 2015;132(22):2126-33. DOI: 10.1161/CIRCULATIONAHA.115.016950
18. Stewart IJ, Faulk TI, Sosnov JA et al. Rhabdomyolysis among critically ill combat casualties: Associations with acute kidney injury and mortality. J Trauma Acute Care Surg 2016;80(3):492-8. DOI: 10.1097/TA.0000000000000933
19. Ząbkowski T, Brzozowski R, Durma AD. Renal injuries in conflict zones: a 6-year study of traumatic cases in Afghanistan. Confl Health 2024;18(1):6. DOI: 10.1186/s13031-023-00566-1
18 февраля 2026
Количество просмотров: 97


