Клинический разбор в общей медицине №02 2026
1 Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2 Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery, Moscow, Russia;
3 POLYCLINIC.RU, Moscow, Russia
omekan@mail.ru
Abstract
Aim. To assess the efficacy of a complex treatment and prevention method for recurrent intrauterine synechiae (IUS) in fertile age.
Methods. A prospective study included 101 patients with the verified diagnosis N85.6 “IUS (relapse within 3–6 months post hysteroscopic adhesiolysis)”. During the study the patients were stratified into two groups by blinded randomization: index group (n=50) and comparison group (n=51). The index group (n=50) received combination treatment based on the original method (patent RU 2830460 C1) that included hysteroscopic adhesiolysis with administration of 3.0 mL of the sodium hyaluronate-based anti-adhesive gel (Antiadgezin, manufacturer Genewel Co., Ltd., Korea, representative for the Russian Federation Nizhpharm OJSC), cyclic hormone therapy (transdermal estrogens and micronized progesterone), as well as exposure to physical factors (ultrasound therapy targeting the pelvic organ projection zone and dermatoparamic iodine electrophoresis with galvanic current targeting the abdominal-vaginal-sacral region performed using the BTL4000-Premium-G system, BTL Corporate, Czech Republic). The comparison group (n=51) received standard treatment in the form of hysteroscopic adhesiolysis and cyclic hormone therapy (transdermal estrogens and micronized progesterone). The treatment efficacy was assessed within 3 months during the follow-up office hysteroscopy performed using the Karl Storz endoscopic equipment.
Results. The average age of patients with recurrent IUS was 37.36 years (Q₁–Q₃: 32.54–38.84). The IUS recurrence rate in the group receiving combination treatment was 3.5 times lower compared to that in patients, who received conventional therapy (p<0.001).
Conclusions. The developed IUS complex treatment method involving hysteroscopic adhesiolysis with subsequent implantation of the anti-adhesive barrier gel (Antiadgezin 3.0 mL), cyclic hormone therapy, and exposure to physical factors (ultrasound therapy targeting the pelvic organ projection zone and dermatoparamic iodine electrophoresis with galvanic current targeting the abdominal-vaginal-sacral region) demonstrates significant (p<0.001) superiority over the traditional approach: lower recurrence rate within 3 months of follow-up (3.5 times lower, 14.0% vs. 49.0%).
Keywords: intrauterine synechiae, relapse, treatment, sodium hyaluronate.
For citation: Orazov M.R., Mikhaleva L.M., Ismayilzade S.Ya. Intrauterine adhesion recurrence treatment and prevention efficacy at fertile age. Clinical review for general practice. 2026; 7 (2): 62–66 (In Russ.). DOI: 10.47407/kr2026.7.2.00771
Актуальность проблемы
В настоящее время одной из нерешенных проблем репродуктивной медицины во всем мире остаются внутриматочные синехии (ВМС) – мультифакториальный полигенный синдром с различными формами клинических детерминант, от асимптомного течения до абсолютной инфертильности и осложнений имплантации и гестации [1, 2].
Распространенность ВМС в мире достигает 19,1% (95% доверительный интервал 12,8–27,5%). При этом частота рецидива ВМС после лечения варьирует от 21 до 41,9% (W. Lee и соавт., 2021; A. Richtárová и соавт., 2022), что указывает на недостаточную эффективность существующих методов профилактики повторного формирования синехий [3].
Клиническая значимость проблемы определяется также широким спектром симптомов, включая скудные менструации, аменорею, бесплодие и другие осложнения [4]. Многофакторность этиологии, низкая результативность лечения адгезивного процесса полости матки определяют приоритетность поиска новых методов не только терапии, но и прежде всего прогнозирования исходов и профилактики ВМС, при этом исследования по оценке эффективности того или иного метода должны отличаться высоким качеством [5].
Решение этих вопросов позволит оптимизировать тактику ведения пациенток с ВМС, снизить частоту рецидивов и улучшить их репродуктивные исходы. Все перечисленное выше определило цель настоящего исследования: оценить эффективность комплексного метода лечения и профилактики рецидивов ВМС в репродуктивном возрасте.
Материалы и методы
Исследование выполнено в период 2021–2025 гг. на клинической базе кафедры акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН (заведующий кафедрой – заслуженный деятель науки РФ академик РАН профессор В.Е. Радзинский). В проспективный лечебный этап настоящего исследования вошла 101 пациентка с верифицированным диагнозом N85.6 «ВМС (рецидив, возникший в течение 3–6 мес после гистероскопического адгезиолизиса)».
Критерии включения:
• фертильный возраст (15–49 лет);
• верифицированный на основании гистероскопического исследования диагноз ВМС (код Международной классификации болезней 10-го пересмотра N85.6), рецидив ВМС (для основной группы);
• наличие информированного согласия на участие в исследовании.
Критерии исключения:
• отказ пациентки от участия в исследовании;
• сопутствующие заболевания матки (подслизистая миома матки, полипы эндометрия, гиперплазия эндометрия, аденомиоз, врожденные аномалии развития матки);
• злокачественные новообразования матки и шейки матки;
• острые воспалительные заболевания органов малого таза, тяжелое течение ВМС Va и Vb по классификации ESGE (European Society of Gynecological Endoscopy, 1995);
• атрезия цервикального канала;
• беременность на момент исследования (включая эктопическую).
Рецидивом ВМС считали вновь возникшие адгезии, верифицированные в ходе контрольного гистероскопического исследования через 6 мес после адгезиолизиса.
Все участницы планировали в ближайшее время реализацию репродуктивной функции и дали информированное согласие на участие. В ходе исследования методом слепой рандомизации пациентки были стратифицированы на две группы: основную группу (n=50) и группу сравнения (n=51). Основная группа (n=50) получала комплексное лечение по оригинальному методу (патент RU 2830460 C1) [6], включающее гистероскопический адгезиолизис с введением противоспаечного геля на основе гиалуроната натрия в объеме 3,0 мл (Антиадгезин производства компании Genewel Co., Ltd., Корея), циклическую гормональную терапию (трансдермальные эстрогены и микронизированный прогестерон), а также воздействие физическими факторами (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально на аппарате BTL4000-Ppremium-G, BTL Corporate, Чехия). Группа сравнения (n=51) получала стандартное лечение в виде гистероскопического адгезиолизиса и циклической гормонотерапии (трансдермальные эстрогены и микронизированный прогестерон). Эффективность лечения оценивали через 3 мес в ходе контрольной офисной гистероскопии с использованием эндоскопического оборудования Karl Storz.
Статистический анализ массива данных производили с помощью программ IBM SPSS v. 23.0 (IBM Corporation, США) и StatTech («Статтех», Россия). Для проверки нормальности распределения количественных данных использовали тесты Шапиро–Уилка при n<50 и Колмогорова–Смирнова при n>50. Для выявления независимых предикторов рецидива проводился многофакторный логистический регрессионный анализ с пошаговым включением переменных. В модель включались факторы, продемонстрировавшие значимость p<0,1 при однофакторном анализе. Качество модели оценивалось с помощью критерия Хосмера–Лемешова и площади под ROC-кривой (AUC).
Результаты и обсуждение
В ходе исследования было установлено, что медианный возраст пациенток с рецидивами ВМС составил 37,36 года (Q₁–Q₃: 32,54–38,84), статистически значимых различий установлено не было (p=0,063). При анализе социально-демографических характеристик не выявлено значимых межгрупповых различий по уровню образования (p=0,998) и брачному статусу (p=0,800).
В ходе исследования выявлены ключевые гистероскопические предикторы риска рецидива ВМС:
• атрофия эндометрия (отношение шансов – ОШ 4,51; 95% ДИ 1,40–14,64);
• частичная либо полная облитерация истмического отдела (ОШ 3,90; 95% ДИ 1,52–10,01);
• микрополипоз эндометрия (ОШ 2,91; 95% ДИ 1,05–8,07);
• отсутствие визуализации устьев маточных труб (ОШ 2,72; 95% ДИ 1,26–5,88);
• диффузная гиперемия эндометрия (ОШ 2,39; 95% ДИ 1,06–5,35);
• тяжелая степень адгезивно-фиброзных поражений (ОШ 2,15; 95% ДИ 1,15–4,31).
Вышеуказанные эндоскопические маркеры свидетельствуют о прогрессирующем характере фиброзирующих изменений при рецидивах заболевания и имеют важное значение для прогнозирования риска рецидива [7].
Анализ распределения степени тяжести ВМС в исследуемых группах продемонстрировал преобладание пациенток с легкой степенью адгезивного процесса как в основной группе, так и в группе сравнения. Меньшую долю составили пациентки со средней степенью тяжести, и наименьшая часть участниц исследования имели тяжелую степень патологического процесса. Статистический анализ с применением критерия хи-квадрат подтвердил отсутствие значимых межгрупповых различий (p=0,852), что свидетельствует об однородности, статистической гомогенности выборки и корректности проведенной рандомизации. Таким образом, группы были сопоставимы по исходной тяжести заболевания, что позволяет провести объективную оценку эффективности предложенного комплексного метода лечения в сравнении с традиционным подходом.
Контрольная офисная гистероскопия, проведенная через 3 мес после окончания лечения в рамках second look, позволила объективно оценить эффективность используемых терапевтических подходов (рис. 1).
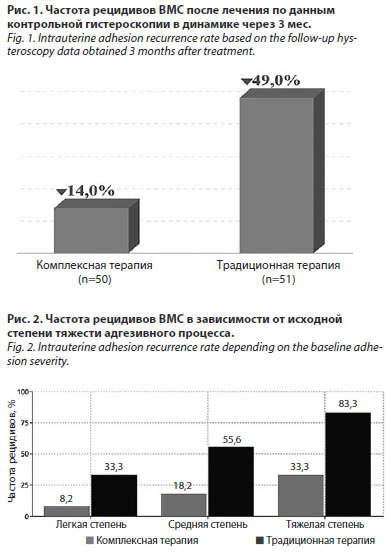 Согласно результатам, частота рецидивирования ВМС в группе традиционной терапии была в 3,5 раза выше, чем в группе комплексного лечения. Полученные данные убедительно демонстрируют преимущества разработанного комплексного подхода в профилактике рецидивов ВМС. Корреляционный анализ с использованием метода ранговой корреляции Спирмена выявил наличие статистически значимой положительной связи между исходной степенью тяжести внутриматочного адгезивного процесса и частотой развития рецидивов заболевания (ρ=0,642, p<0,001), что свидетельствует о значимом влиянии исходной тяжести патологического процесса на прогноз заболевания.
Согласно результатам, частота рецидивирования ВМС в группе традиционной терапии была в 3,5 раза выше, чем в группе комплексного лечения. Полученные данные убедительно демонстрируют преимущества разработанного комплексного подхода в профилактике рецидивов ВМС. Корреляционный анализ с использованием метода ранговой корреляции Спирмена выявил наличие статистически значимой положительной связи между исходной степенью тяжести внутриматочного адгезивного процесса и частотой развития рецидивов заболевания (ρ=0,642, p<0,001), что свидетельствует о значимом влиянии исходной тяжести патологического процесса на прогноз заболевания.
При стратификационном анализе частоты рецидивов в зависимости от исходной степени тяжести синехий установлена отчетливая градация эффективности лечения в обеих исследуемых группах (рис. 2).
В группе комплексной терапии наблюдалась прямая связь между тяжестью процесса и частотой рецидивов ВМС, однако сила этой корреляции была существенно ниже, чем в группе традиционного лечения.
Сравнительный анализ эффективности терапевтических подходов позволил установить достоверное преимущество разработанного комплексного метода лечения независимо от степени выраженности адгезивного процесса (p<0,001). Наиболее выраженный профилактический эффект комплексной терапии наблюдался у пациенток с легкой степенью адгезивного процесса, где частота рецидивов была ниже в 4,1 раза по сравнению с группой традиционного лечения. При средней степени тяжести синехий использование комплексного подхода обеспечивало снижение частоты рецидивов в 3,1 раза. Особого внимания заслуживает тот факт, что даже при тяжелой степени адгезивного процесса предложенный метод позволил добиться значимого терапевтического эффекта, снижая частоту рецидивов в 2,5 раза.
Проблема ВМС остается одним из наиболее сложных вызовов современной репродуктивной медицины, что обусловлено не только высокой частотой встречаемости данной нозологии, варьирующей от 3 до 13% в структуре внутриматочных заболеваний, но и значительным риском рецидивирования после лечения. Особую актуальность приобретают поиск предикторов рецидивирования и разработка эффективных методов профилактики повторного формирования синехий, учитывая, что частота рецидивов может достигать 21–41,9% в зависимости от распространенности первичного адгезивного процесса [8].
Механизм действия комплексного метода может быть объяснен с позиций современных представлений о патогенезе заболевания: персистирующее аномальное воспаление является основным драйвером/коунфандером эндометриального фиброза. Использование физических факторов, противоспаечного барьера на основе гиалуроната натрия (Антиадгезин в объеме 3,0 мл) в сочетании с циклической гормонотерапией позволяет воздействовать на различные звенья патогенеза, включая подавление экспрессии NF-κB-опосредованных механизмов воспаления [9].
Полученные результаты свидетельствуют о том, что:
• риск рецидива ВМС прямо пропорционален исходной степени тяжести адгезивного процесса;
• предложенный комплексный метод лечения эффективен при всех степенях тяжести адгезий;
• наибольшее клиническое преимущество метода наблюдается у пациенток с тяжелой степенью адгезивного процесса;
• раннее начало лечения при легкой степени адгезий позволяет достичь наилучших результатов (частота рецидивов менее 10%).
В современной гинекологической хирургии ключевым методом профилактики послеоперационных спаек является применение биорезорбируемых барьеров на основе гиалуроновой кислоты (ГК) в гелевой форме. Важным преимуществом таких гелевых форм является их способность за счет уникальной реологии обеспечивать формирование непрерывного равномерного покрытия всей площади операционной раны, включая анатомически сложные зоны (например, полость матки, поверхности яичников, интерстициальные отделы маточных труб).
ГК – эндогенный линейный гликозаминогликан, структурная единица внеклеточного матрикса, отвечающая в том числе за пролиферацию и миграцию различных клеток. Ее противоспаечный эффект реализуется за счет мультимодального действия, которое включает как механическое разделение серозных поверхностей, так и влияние на фибринолиз, ремезотелиализацию и модуляцию воспалительного каскада.
Принцип использования механических барьеров в современной хирургии заключается в размещении в операционной области барьера, который изолирует ее от окружающих тканей, предотвращая прикрепление фибриновых сгустков и дальнейшее формирование спаек. Таким образом, подходящий механический барьер должен быть биоразлагаемым, сохраняться в течение всего процесса заживления и быть инертным к иммунному ответу [10].
Ключевыми фармакологическими преимуществами ГК являются ее эндогенное происхождение, биосовместимость, биоразлагаемость и отсутствие антигенности. Эти свойства обеспечивают высокий профиль безопасности и неограниченные возможности для клинического применения.
ГК, как правило, применяется в противоспаечных барьерах в комбинации с другими компонентами, например с карбоксиметилцеллюлозой (КМЦ), образуя полимерный комплекс, который кинетически стабилизирует молекулу ГК, ингибируя ее ферментативный гидролиз, что приводит к увеличению периода биологической активности и, как следствие, к пролонгированному барьерному и противовоспалительному действию в зоне хирургического вмешательства [11, 12].
В настоящее время в Российской Федерации зарегистрирован и разрешен к применению противоспаечный барьер в виде геля на основе ГК Антиадгезин (производитель Genewel Co., Ltd., Корея, представитель в РФ АО «Нижфарм»). Гель Антиадгезин представляет собой комбинацию высокоочищенной натриевой соли ГК и КМЦ, разрешен к применению при различных оперативных вмешательствах, в том числе внутриматочных.
Антиадгезин механически разделяет серозные поверхности в течение критического периода заживления (до 7 сут), что предотвращает контакт и последующее слипание поврежденных тканей, сводя к минимуму риск развития фиброзных адгезий, не влияя при этом на нормально протекающие процессы регенерации. Гель прост в использовании, безопасен и инертен.
Послеоперационные внутриматочные спайки представляют собой важную клиническую проблему, поскольку могут привести к бесплодию, повторным выкидышам, нерегулярным циклам с дисменореей и тазовым болям [13].
Внутриматочное введение барьеров на основе ГК после внутриматочных вмешательств позволяет улучшить репродуктивные исходы, повышая частоту наступления беременности. Так, по данным проспективного рандомизированного исследования V. Tsapanos и соавт., внутриматочное введение противоспаечного барьерного средства, содержащего ГК и КМЦ, не только позволяет предотвратить формирование или уменьшить выраженность внутриматочного спаечного процесса, но и способствует сохранению репродуктивной функции. Внутриматочное введение геля с ГК и КМЦ после раздельного диагностического выскабливания повысило частоту наступления беременности в течение 8 мес до 100% против 54% в контроле. При этом у небеременных пациенток после раздельного диагностического выскабливания внутриматочное введение геля с ГК и КМЦ снизило частоту формирования синехий по данным гистеросальпингографии до 10% против 50% в контроле [14].
В проспективном рандомизированном клиническом исследовании (J. Do и соавт.) применение геля с ГК и КМЦ после внутриматочных вмешательств снизило частоту синехий через 4 нед до 13% против 26% в контроле [15].
Согласно данным систематического обзора и метаанализа, проведенного Л.В. Адамян и соавт., применение геля на основе ГК для профилактики спаек после гинекологических операций достоверно снижает частоту формирования умеренных и тяжелых послеоперационных спаек у женщин репродуктивного возраста (p=0,0010). При этом доля участков со спайками была статистически значимо выше в контрольной группе по сравнению с экспериментальной группой (p<0,00001) [11].
Современные исследования методов, направленных на профилактику образования спаек, сосредоточены на использовании механических барьеров и противоспаечных адъювантов. Использование комбинированных стратегий, включающих механические барьеры, адъюванты (например, гормоны) и др., представляется многообещающим вариантом [10].
Заключение
Предложенный оригинальный комплексный метод лечения, включающий гистероскопический адгезиолизис, имплантацию противоспаечного барьерного геля на основе гиалуроната натрия (Антиадгезин в объеме 3,0 мл), циклическую гормонотерапию и физиотерапевтическое воздействие (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально), продемонстрировал значительное превосходство над традиционным подходом, что выразилось в достоверном снижении частоты рецидивов в 3,5 раза (14,0% против 49,0%, p<0,05).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru;
ORCID: 0000-0002-1767-5536
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-1767-5536
Михалева Людмила Михайловна – чл.-кор. РАН, д-р мед. наук, проф., дир. НИИМЧ им.
акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского», засл. деят. науки РФ.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Liudmila M. Mikhaleva – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director of Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Исмаилзаде Севиндж Ядулла кызы – канд. мед. наук, врач акушер-гинеколог ООО «КДЦ «ПОЛИКЛИНИКА.РУ». E-mail: sevka_monika@mail.ru; ORCID: 0000-0002-7428-0469
Sevinc Ya. Ismayilzade – Cand. Sci. (Med.), gynecologist, POLYCLINIC.RU.
E-mail: sevka_monika@mail.ru; ORCID: 0000-0002-7428-0469
Поступила в редакцию: 13.01.2026
Поступила после рецензирования: 19.01.2026
Принята к публикации: 22.01.2026
Received: 13.01.2026
Revised: 19.01.2026
Accepted: 22.01.2026
Клинический разбор в общей медицине №02 2026
Эффективность лечения и профилактика рецидивов внутриматочных синехий в репродуктивном возрасте
Номера страниц в выпуске:62-66
Аннотация
Цель. Оценить эффективность комплексного метода лечения и профилактики рецидивов внутриматочных синехий (ВМС) в репродуктивном возрасте.
Материалы и методы. В проспективное исследование вошла 101 пациентка с верифицированным диагнозом N85.6 «ВМС (рецидив, возникший в течение 3–6 мес после гистероскопического адгезиолизиса)». В ходе исследования методом слепой рандомизации пациентки были стратифицированы на две группы: основную группу (n=50) и группу сравнения (n=51). Основная группа (n=50) получала комплексное лечение по оригинальному методу (патент RU 2830460 C1), включающее гистероскопический адгезиолизис с введением противоспаечного геля на основе гиалуроната натрия в объеме 3,0 мл (Антиадгезин, производитель Genewel Co., Ltd., Корея, представитель в Российской Федерации АО «Нижфарм»), циклическую гормональную терапию (трансдермальные эстрогены и микронизированный прогестерон), а также воздействие физическими факторами (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально на аппарате BTL4000-Ppremium-G, BTL Corporate, Чехия). Группа сравнения (n=51) получала стандартное лечение в виде гистероскопического адгезиолизиса и циклической гормонотерапии (трансдермальные эстрогены и микронизированный прогестерон). Эффективность лечения оценивали через 3 мес в ходе контрольной офисной гистероскопии с использованием эндоскопического оборудования Karl Storz.
Результаты. Средний возраст пациенток с рецидивами ВМС составил 37,36 года (Q₁–Q₃: 32,54–38,84). Частота рецидивов ВМС в группе, получавшей комплексное лечение, оказалась в 3,5 раза ниже по сравнению с пациентками, получивших традиционную терапию (p<0,001).
Выводы. Разработанный метод комплексного лечения ВМС, включающий гистероскопический адгезиолизис с последующей имплантацией противоспаечного барьерного геля (Антиадгезин 3,0 мл), циклическую гормонотерапию и воздействие физическими факторами (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально), демонстрирует значимое (p<0,001) превосходство над традиционным подходом: более низкая частота рецидивов через 3 мес наблюдения (в 3,5 раза, 14,0% против 49,0%).
Ключевые слова: внутриматочные синехии, рецидив, лечение, гиалуронат натрия.
Для цитирования: Оразов М.Р., Михалева Л.М., Исмаилзаде С.Я. Эффективность лечения и профилактика рецидивов внутриматочных синехий в репродуктивном возрасте. Клинический разбор в общей медицине. 2026; 7 (2): 62–66. DOI: 10.47407/kr2026.7.2.00771
Цель. Оценить эффективность комплексного метода лечения и профилактики рецидивов внутриматочных синехий (ВМС) в репродуктивном возрасте.
Материалы и методы. В проспективное исследование вошла 101 пациентка с верифицированным диагнозом N85.6 «ВМС (рецидив, возникший в течение 3–6 мес после гистероскопического адгезиолизиса)». В ходе исследования методом слепой рандомизации пациентки были стратифицированы на две группы: основную группу (n=50) и группу сравнения (n=51). Основная группа (n=50) получала комплексное лечение по оригинальному методу (патент RU 2830460 C1), включающее гистероскопический адгезиолизис с введением противоспаечного геля на основе гиалуроната натрия в объеме 3,0 мл (Антиадгезин, производитель Genewel Co., Ltd., Корея, представитель в Российской Федерации АО «Нижфарм»), циклическую гормональную терапию (трансдермальные эстрогены и микронизированный прогестерон), а также воздействие физическими факторами (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально на аппарате BTL4000-Ppremium-G, BTL Corporate, Чехия). Группа сравнения (n=51) получала стандартное лечение в виде гистероскопического адгезиолизиса и циклической гормонотерапии (трансдермальные эстрогены и микронизированный прогестерон). Эффективность лечения оценивали через 3 мес в ходе контрольной офисной гистероскопии с использованием эндоскопического оборудования Karl Storz.
Результаты. Средний возраст пациенток с рецидивами ВМС составил 37,36 года (Q₁–Q₃: 32,54–38,84). Частота рецидивов ВМС в группе, получавшей комплексное лечение, оказалась в 3,5 раза ниже по сравнению с пациентками, получивших традиционную терапию (p<0,001).
Выводы. Разработанный метод комплексного лечения ВМС, включающий гистероскопический адгезиолизис с последующей имплантацией противоспаечного барьерного геля (Антиадгезин 3,0 мл), циклическую гормонотерапию и воздействие физическими факторами (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально), демонстрирует значимое (p<0,001) превосходство над традиционным подходом: более низкая частота рецидивов через 3 мес наблюдения (в 3,5 раза, 14,0% против 49,0%).
Ключевые слова: внутриматочные синехии, рецидив, лечение, гиалуронат натрия.
Для цитирования: Оразов М.Р., Михалева Л.М., Исмаилзаде С.Я. Эффективность лечения и профилактика рецидивов внутриматочных синехий в репродуктивном возрасте. Клинический разбор в общей медицине. 2026; 7 (2): 62–66. DOI: 10.47407/kr2026.7.2.00771
Intrauterine adhesion recurrence treatment and prevention efficacy at fertile age
Mekan R. Orazov1, Liudmila M. Mikhaleva2, Sevinc Ya. Ismayilzade31 Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2 Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery, Moscow, Russia;
3 POLYCLINIC.RU, Moscow, Russia
omekan@mail.ru
Abstract
Aim. To assess the efficacy of a complex treatment and prevention method for recurrent intrauterine synechiae (IUS) in fertile age.
Methods. A prospective study included 101 patients with the verified diagnosis N85.6 “IUS (relapse within 3–6 months post hysteroscopic adhesiolysis)”. During the study the patients were stratified into two groups by blinded randomization: index group (n=50) and comparison group (n=51). The index group (n=50) received combination treatment based on the original method (patent RU 2830460 C1) that included hysteroscopic adhesiolysis with administration of 3.0 mL of the sodium hyaluronate-based anti-adhesive gel (Antiadgezin, manufacturer Genewel Co., Ltd., Korea, representative for the Russian Federation Nizhpharm OJSC), cyclic hormone therapy (transdermal estrogens and micronized progesterone), as well as exposure to physical factors (ultrasound therapy targeting the pelvic organ projection zone and dermatoparamic iodine electrophoresis with galvanic current targeting the abdominal-vaginal-sacral region performed using the BTL4000-Premium-G system, BTL Corporate, Czech Republic). The comparison group (n=51) received standard treatment in the form of hysteroscopic adhesiolysis and cyclic hormone therapy (transdermal estrogens and micronized progesterone). The treatment efficacy was assessed within 3 months during the follow-up office hysteroscopy performed using the Karl Storz endoscopic equipment.
Results. The average age of patients with recurrent IUS was 37.36 years (Q₁–Q₃: 32.54–38.84). The IUS recurrence rate in the group receiving combination treatment was 3.5 times lower compared to that in patients, who received conventional therapy (p<0.001).
Conclusions. The developed IUS complex treatment method involving hysteroscopic adhesiolysis with subsequent implantation of the anti-adhesive barrier gel (Antiadgezin 3.0 mL), cyclic hormone therapy, and exposure to physical factors (ultrasound therapy targeting the pelvic organ projection zone and dermatoparamic iodine electrophoresis with galvanic current targeting the abdominal-vaginal-sacral region) demonstrates significant (p<0.001) superiority over the traditional approach: lower recurrence rate within 3 months of follow-up (3.5 times lower, 14.0% vs. 49.0%).
Keywords: intrauterine synechiae, relapse, treatment, sodium hyaluronate.
For citation: Orazov M.R., Mikhaleva L.M., Ismayilzade S.Ya. Intrauterine adhesion recurrence treatment and prevention efficacy at fertile age. Clinical review for general practice. 2026; 7 (2): 62–66 (In Russ.). DOI: 10.47407/kr2026.7.2.00771
Актуальность проблемы
В настоящее время одной из нерешенных проблем репродуктивной медицины во всем мире остаются внутриматочные синехии (ВМС) – мультифакториальный полигенный синдром с различными формами клинических детерминант, от асимптомного течения до абсолютной инфертильности и осложнений имплантации и гестации [1, 2].
Распространенность ВМС в мире достигает 19,1% (95% доверительный интервал 12,8–27,5%). При этом частота рецидива ВМС после лечения варьирует от 21 до 41,9% (W. Lee и соавт., 2021; A. Richtárová и соавт., 2022), что указывает на недостаточную эффективность существующих методов профилактики повторного формирования синехий [3].
Клиническая значимость проблемы определяется также широким спектром симптомов, включая скудные менструации, аменорею, бесплодие и другие осложнения [4]. Многофакторность этиологии, низкая результативность лечения адгезивного процесса полости матки определяют приоритетность поиска новых методов не только терапии, но и прежде всего прогнозирования исходов и профилактики ВМС, при этом исследования по оценке эффективности того или иного метода должны отличаться высоким качеством [5].
Решение этих вопросов позволит оптимизировать тактику ведения пациенток с ВМС, снизить частоту рецидивов и улучшить их репродуктивные исходы. Все перечисленное выше определило цель настоящего исследования: оценить эффективность комплексного метода лечения и профилактики рецидивов ВМС в репродуктивном возрасте.
Материалы и методы
Исследование выполнено в период 2021–2025 гг. на клинической базе кафедры акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН (заведующий кафедрой – заслуженный деятель науки РФ академик РАН профессор В.Е. Радзинский). В проспективный лечебный этап настоящего исследования вошла 101 пациентка с верифицированным диагнозом N85.6 «ВМС (рецидив, возникший в течение 3–6 мес после гистероскопического адгезиолизиса)».
Критерии включения:
• фертильный возраст (15–49 лет);
• верифицированный на основании гистероскопического исследования диагноз ВМС (код Международной классификации болезней 10-го пересмотра N85.6), рецидив ВМС (для основной группы);
• наличие информированного согласия на участие в исследовании.
Критерии исключения:
• отказ пациентки от участия в исследовании;
• сопутствующие заболевания матки (подслизистая миома матки, полипы эндометрия, гиперплазия эндометрия, аденомиоз, врожденные аномалии развития матки);
• злокачественные новообразования матки и шейки матки;
• острые воспалительные заболевания органов малого таза, тяжелое течение ВМС Va и Vb по классификации ESGE (European Society of Gynecological Endoscopy, 1995);
• атрезия цервикального канала;
• беременность на момент исследования (включая эктопическую).
Рецидивом ВМС считали вновь возникшие адгезии, верифицированные в ходе контрольного гистероскопического исследования через 6 мес после адгезиолизиса.
Все участницы планировали в ближайшее время реализацию репродуктивной функции и дали информированное согласие на участие. В ходе исследования методом слепой рандомизации пациентки были стратифицированы на две группы: основную группу (n=50) и группу сравнения (n=51). Основная группа (n=50) получала комплексное лечение по оригинальному методу (патент RU 2830460 C1) [6], включающее гистероскопический адгезиолизис с введением противоспаечного геля на основе гиалуроната натрия в объеме 3,0 мл (Антиадгезин производства компании Genewel Co., Ltd., Корея), циклическую гормональную терапию (трансдермальные эстрогены и микронизированный прогестерон), а также воздействие физическими факторами (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально на аппарате BTL4000-Ppremium-G, BTL Corporate, Чехия). Группа сравнения (n=51) получала стандартное лечение в виде гистероскопического адгезиолизиса и циклической гормонотерапии (трансдермальные эстрогены и микронизированный прогестерон). Эффективность лечения оценивали через 3 мес в ходе контрольной офисной гистероскопии с использованием эндоскопического оборудования Karl Storz.
Статистический анализ массива данных производили с помощью программ IBM SPSS v. 23.0 (IBM Corporation, США) и StatTech («Статтех», Россия). Для проверки нормальности распределения количественных данных использовали тесты Шапиро–Уилка при n<50 и Колмогорова–Смирнова при n>50. Для выявления независимых предикторов рецидива проводился многофакторный логистический регрессионный анализ с пошаговым включением переменных. В модель включались факторы, продемонстрировавшие значимость p<0,1 при однофакторном анализе. Качество модели оценивалось с помощью критерия Хосмера–Лемешова и площади под ROC-кривой (AUC).
Результаты и обсуждение
В ходе исследования было установлено, что медианный возраст пациенток с рецидивами ВМС составил 37,36 года (Q₁–Q₃: 32,54–38,84), статистически значимых различий установлено не было (p=0,063). При анализе социально-демографических характеристик не выявлено значимых межгрупповых различий по уровню образования (p=0,998) и брачному статусу (p=0,800).
В ходе исследования выявлены ключевые гистероскопические предикторы риска рецидива ВМС:
• атрофия эндометрия (отношение шансов – ОШ 4,51; 95% ДИ 1,40–14,64);
• частичная либо полная облитерация истмического отдела (ОШ 3,90; 95% ДИ 1,52–10,01);
• микрополипоз эндометрия (ОШ 2,91; 95% ДИ 1,05–8,07);
• отсутствие визуализации устьев маточных труб (ОШ 2,72; 95% ДИ 1,26–5,88);
• диффузная гиперемия эндометрия (ОШ 2,39; 95% ДИ 1,06–5,35);
• тяжелая степень адгезивно-фиброзных поражений (ОШ 2,15; 95% ДИ 1,15–4,31).
Вышеуказанные эндоскопические маркеры свидетельствуют о прогрессирующем характере фиброзирующих изменений при рецидивах заболевания и имеют важное значение для прогнозирования риска рецидива [7].
Анализ распределения степени тяжести ВМС в исследуемых группах продемонстрировал преобладание пациенток с легкой степенью адгезивного процесса как в основной группе, так и в группе сравнения. Меньшую долю составили пациентки со средней степенью тяжести, и наименьшая часть участниц исследования имели тяжелую степень патологического процесса. Статистический анализ с применением критерия хи-квадрат подтвердил отсутствие значимых межгрупповых различий (p=0,852), что свидетельствует об однородности, статистической гомогенности выборки и корректности проведенной рандомизации. Таким образом, группы были сопоставимы по исходной тяжести заболевания, что позволяет провести объективную оценку эффективности предложенного комплексного метода лечения в сравнении с традиционным подходом.
Контрольная офисная гистероскопия, проведенная через 3 мес после окончания лечения в рамках second look, позволила объективно оценить эффективность используемых терапевтических подходов (рис. 1).
 Согласно результатам, частота рецидивирования ВМС в группе традиционной терапии была в 3,5 раза выше, чем в группе комплексного лечения. Полученные данные убедительно демонстрируют преимущества разработанного комплексного подхода в профилактике рецидивов ВМС. Корреляционный анализ с использованием метода ранговой корреляции Спирмена выявил наличие статистически значимой положительной связи между исходной степенью тяжести внутриматочного адгезивного процесса и частотой развития рецидивов заболевания (ρ=0,642, p<0,001), что свидетельствует о значимом влиянии исходной тяжести патологического процесса на прогноз заболевания.
Согласно результатам, частота рецидивирования ВМС в группе традиционной терапии была в 3,5 раза выше, чем в группе комплексного лечения. Полученные данные убедительно демонстрируют преимущества разработанного комплексного подхода в профилактике рецидивов ВМС. Корреляционный анализ с использованием метода ранговой корреляции Спирмена выявил наличие статистически значимой положительной связи между исходной степенью тяжести внутриматочного адгезивного процесса и частотой развития рецидивов заболевания (ρ=0,642, p<0,001), что свидетельствует о значимом влиянии исходной тяжести патологического процесса на прогноз заболевания.При стратификационном анализе частоты рецидивов в зависимости от исходной степени тяжести синехий установлена отчетливая градация эффективности лечения в обеих исследуемых группах (рис. 2).
В группе комплексной терапии наблюдалась прямая связь между тяжестью процесса и частотой рецидивов ВМС, однако сила этой корреляции была существенно ниже, чем в группе традиционного лечения.
Сравнительный анализ эффективности терапевтических подходов позволил установить достоверное преимущество разработанного комплексного метода лечения независимо от степени выраженности адгезивного процесса (p<0,001). Наиболее выраженный профилактический эффект комплексной терапии наблюдался у пациенток с легкой степенью адгезивного процесса, где частота рецидивов была ниже в 4,1 раза по сравнению с группой традиционного лечения. При средней степени тяжести синехий использование комплексного подхода обеспечивало снижение частоты рецидивов в 3,1 раза. Особого внимания заслуживает тот факт, что даже при тяжелой степени адгезивного процесса предложенный метод позволил добиться значимого терапевтического эффекта, снижая частоту рецидивов в 2,5 раза.
Проблема ВМС остается одним из наиболее сложных вызовов современной репродуктивной медицины, что обусловлено не только высокой частотой встречаемости данной нозологии, варьирующей от 3 до 13% в структуре внутриматочных заболеваний, но и значительным риском рецидивирования после лечения. Особую актуальность приобретают поиск предикторов рецидивирования и разработка эффективных методов профилактики повторного формирования синехий, учитывая, что частота рецидивов может достигать 21–41,9% в зависимости от распространенности первичного адгезивного процесса [8].
Механизм действия комплексного метода может быть объяснен с позиций современных представлений о патогенезе заболевания: персистирующее аномальное воспаление является основным драйвером/коунфандером эндометриального фиброза. Использование физических факторов, противоспаечного барьера на основе гиалуроната натрия (Антиадгезин в объеме 3,0 мл) в сочетании с циклической гормонотерапией позволяет воздействовать на различные звенья патогенеза, включая подавление экспрессии NF-κB-опосредованных механизмов воспаления [9].
Полученные результаты свидетельствуют о том, что:
• риск рецидива ВМС прямо пропорционален исходной степени тяжести адгезивного процесса;
• предложенный комплексный метод лечения эффективен при всех степенях тяжести адгезий;
• наибольшее клиническое преимущество метода наблюдается у пациенток с тяжелой степенью адгезивного процесса;
• раннее начало лечения при легкой степени адгезий позволяет достичь наилучших результатов (частота рецидивов менее 10%).
В современной гинекологической хирургии ключевым методом профилактики послеоперационных спаек является применение биорезорбируемых барьеров на основе гиалуроновой кислоты (ГК) в гелевой форме. Важным преимуществом таких гелевых форм является их способность за счет уникальной реологии обеспечивать формирование непрерывного равномерного покрытия всей площади операционной раны, включая анатомически сложные зоны (например, полость матки, поверхности яичников, интерстициальные отделы маточных труб).
ГК – эндогенный линейный гликозаминогликан, структурная единица внеклеточного матрикса, отвечающая в том числе за пролиферацию и миграцию различных клеток. Ее противоспаечный эффект реализуется за счет мультимодального действия, которое включает как механическое разделение серозных поверхностей, так и влияние на фибринолиз, ремезотелиализацию и модуляцию воспалительного каскада.
Принцип использования механических барьеров в современной хирургии заключается в размещении в операционной области барьера, который изолирует ее от окружающих тканей, предотвращая прикрепление фибриновых сгустков и дальнейшее формирование спаек. Таким образом, подходящий механический барьер должен быть биоразлагаемым, сохраняться в течение всего процесса заживления и быть инертным к иммунному ответу [10].
Ключевыми фармакологическими преимуществами ГК являются ее эндогенное происхождение, биосовместимость, биоразлагаемость и отсутствие антигенности. Эти свойства обеспечивают высокий профиль безопасности и неограниченные возможности для клинического применения.
ГК, как правило, применяется в противоспаечных барьерах в комбинации с другими компонентами, например с карбоксиметилцеллюлозой (КМЦ), образуя полимерный комплекс, который кинетически стабилизирует молекулу ГК, ингибируя ее ферментативный гидролиз, что приводит к увеличению периода биологической активности и, как следствие, к пролонгированному барьерному и противовоспалительному действию в зоне хирургического вмешательства [11, 12].
В настоящее время в Российской Федерации зарегистрирован и разрешен к применению противоспаечный барьер в виде геля на основе ГК Антиадгезин (производитель Genewel Co., Ltd., Корея, представитель в РФ АО «Нижфарм»). Гель Антиадгезин представляет собой комбинацию высокоочищенной натриевой соли ГК и КМЦ, разрешен к применению при различных оперативных вмешательствах, в том числе внутриматочных.
Антиадгезин механически разделяет серозные поверхности в течение критического периода заживления (до 7 сут), что предотвращает контакт и последующее слипание поврежденных тканей, сводя к минимуму риск развития фиброзных адгезий, не влияя при этом на нормально протекающие процессы регенерации. Гель прост в использовании, безопасен и инертен.
Послеоперационные внутриматочные спайки представляют собой важную клиническую проблему, поскольку могут привести к бесплодию, повторным выкидышам, нерегулярным циклам с дисменореей и тазовым болям [13].
Внутриматочное введение барьеров на основе ГК после внутриматочных вмешательств позволяет улучшить репродуктивные исходы, повышая частоту наступления беременности. Так, по данным проспективного рандомизированного исследования V. Tsapanos и соавт., внутриматочное введение противоспаечного барьерного средства, содержащего ГК и КМЦ, не только позволяет предотвратить формирование или уменьшить выраженность внутриматочного спаечного процесса, но и способствует сохранению репродуктивной функции. Внутриматочное введение геля с ГК и КМЦ после раздельного диагностического выскабливания повысило частоту наступления беременности в течение 8 мес до 100% против 54% в контроле. При этом у небеременных пациенток после раздельного диагностического выскабливания внутриматочное введение геля с ГК и КМЦ снизило частоту формирования синехий по данным гистеросальпингографии до 10% против 50% в контроле [14].
В проспективном рандомизированном клиническом исследовании (J. Do и соавт.) применение геля с ГК и КМЦ после внутриматочных вмешательств снизило частоту синехий через 4 нед до 13% против 26% в контроле [15].
Согласно данным систематического обзора и метаанализа, проведенного Л.В. Адамян и соавт., применение геля на основе ГК для профилактики спаек после гинекологических операций достоверно снижает частоту формирования умеренных и тяжелых послеоперационных спаек у женщин репродуктивного возраста (p=0,0010). При этом доля участков со спайками была статистически значимо выше в контрольной группе по сравнению с экспериментальной группой (p<0,00001) [11].
Современные исследования методов, направленных на профилактику образования спаек, сосредоточены на использовании механических барьеров и противоспаечных адъювантов. Использование комбинированных стратегий, включающих механические барьеры, адъюванты (например, гормоны) и др., представляется многообещающим вариантом [10].
Заключение
Предложенный оригинальный комплексный метод лечения, включающий гистероскопический адгезиолизис, имплантацию противоспаечного барьерного геля на основе гиалуроната натрия (Антиадгезин в объеме 3,0 мл), циклическую гормонотерапию и физиотерапевтическое воздействие (ультразвуковая терапия на зону проекции органов малого таза и дерматопарамибный электрофорез йода гальваническим током абдоминально-вагинально-сакрально), продемонстрировал значительное превосходство над традиционным подходом, что выразилось в достоверном снижении частоты рецидивов в 3,5 раза (14,0% против 49,0%, p<0,05).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru;
ORCID: 0000-0002-1767-5536
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-1767-5536
Михалева Людмила Михайловна – чл.-кор. РАН, д-р мед. наук, проф., дир. НИИМЧ им.
акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского», засл. деят. науки РФ.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Liudmila M. Mikhaleva – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director of Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Исмаилзаде Севиндж Ядулла кызы – канд. мед. наук, врач акушер-гинеколог ООО «КДЦ «ПОЛИКЛИНИКА.РУ». E-mail: sevka_monika@mail.ru; ORCID: 0000-0002-7428-0469
Sevinc Ya. Ismayilzade – Cand. Sci. (Med.), gynecologist, POLYCLINIC.RU.
E-mail: sevka_monika@mail.ru; ORCID: 0000-0002-7428-0469
Поступила в редакцию: 13.01.2026
Поступила после рецензирования: 19.01.2026
Принята к публикации: 22.01.2026
Received: 13.01.2026
Revised: 19.01.2026
Accepted: 22.01.2026
Список исп. литературыСкрыть список1. Оразов М.Р., Михалева Л.М., Исмаилзаде С.Я. Внутриматочные синехии: старая проблема, новый взгляд. Клинический разбор в общей медицине. 2023;4(9):36-40.
Orazov M.R., Mikhaleva L.M., Ismailzade S.Ya. Intrauterine adhesions: an old problem, a new look. Clinical review in general medicine. 2023;4(9):36-40 (in Russian).
2. Оразов М.Р., Михалева Л.М., Хамошина М.Б. и др. Внутриматочные спайки: от патогенеза к эффективным технологиям преодоления. Медицинский совет. 2023;17(5):72-80.
Orazov M.R., Mikhaleva L.M., Khamoshina M.B. et al. Intrauterine adhesions: from pathogenesis to effective treatment technologies. Medical Council. 2023;17(5):72-80 (in Russian).
3. Hooker AB. Prevention of Intrauterine Adhesions: The Way to Go. BJOG 2025;132(2):165-6. DOI: 10.1111/1471-0528.17968
4. Hong W, Wu Z, Li L et al. Intrauterine adhesions treated with hysteroscopic adhesiolysis and subsequent obstetric outcome: A retrospective matched cohort study. BJOG 2025;132(2):155-64. DOI: 10.1111/1471-0528.17793
5. Оразов М.Р., Михалева Л.М., Исмаилзаде С.Я. Прогнозирование рецидивирования внутриматочных синехий. Трудный пациент. 2021;(7).
Orazov M.R., Mikhaleva L.M., Ismailzade S.Ya. Predicting the recurrence of intrauterine adhesions. Difficult patient. 2021;(7) (in Russian).
6. Оразов М.Р., Михалева Л.М., Исмаилзаде С.Я. и др. Способ комплексного лечения внутриматочных синехий. Патент 2830460 C1, Российская Федерация; заявитель и патентообладатель. №2024101444 заявл. 22.01.2024; опубл. 19.11.2024.
Orazov M.R., Mikhaleva L.M., Ismailzade S.Ya. et al. Method for the complex treatment of intrauterine adhesions. Patent 2830460 C1, Russian Federation; applicant and patent holder. No. 2024101444 filed January 22, 2024; published November 19, 2024 (in Russian).
7. Оразов М.Р., Михалева Л.М., Исмаилзаде С.Я. Рецидивирующие внутриматочные синехии в репродуктивном возрасте. Гистероскопические предикторы. Акушерство и гинекология. 2024;12(спецвып.):48-54.
Orazov M.R., Mikhaleva L.M., Ismailzade S.Y. Recurrent intrauterine adhesions in reproductive age. Hysteroscopic predictors. Obstetrics and Gynecology. 2024;12(special issue):48-54 (in Russian).
8. Liang Y, Meng J, Yu Z et al. Ru single-atom nanozymes targeting ROS-ferroptosis pathways for enhanced endometrial regeneration in intrauterine adhesion therapy. Biomaterials 2025;(315):122923. DOI: 10.1016/j.biomaterials.2024.122923
9. Sánchez-Ruiz R, Hernández-Chico I, Lara-Del-Río B et al. Chronic endometritis and fertility: A binomial linked by microorganisms. Eur J Obstet Gynecol Reprod Biol 2025;(305):86-91. DOI: 10.1016/j.ejogrb.2024.11.032
10. Capella-Monsonís H, Kearns S, Kelly J et al. Battling adhesions: from understanding to prevention. BMC Biomed Eng 2019;1(5). DOI:10.1186/s42490-019-0005-0
11. Adamyan L et al. Hyaluronic acid in the prevention of adhesions after gynecological surgery: systematic review and meta-analysis. J Endometriosis Uterine Disord 2024;6. DOI: 10.1016/j.jeud.2024.100070
12. Sirovy M, Odlozilova S, Kotek J et al. Current options for the prevention of postoperative intra-abdominal adhesions. Asian J Surg 2023 Oct 26:S1015-9584(23)01613-5. DOI: 10.1016/j.asjsur.2023.10.001. Epub ahead of print.
13. Torres-De La Roche LA, Campo R, Devassy R et al. Adhesions and Anti-Adhesion Systems Highlights. Facts Views Vis Obgyn 2019;11(2):137-49.
14. Tsapanos VS, Stathopoulou LP, Papathanassopoulou VS, Tzingounis VA. The role of Seprafilm bioresorbable membrane in the prevention and therapy of endometrial synechiae. J Biomed Mater Res 2002;63(1):10-4. DOI: 10.1002/jbm.10040
15. Do JW. The effectiveness of Hyaluronic acid + Sodium Carboxymethyl Cellulose in the prevention of intrauterine adhesion after intrauterine surgery. J Korean Gynecol Endoscopy Minimally Invasive Surg 2005;(17):2.
