Клинический разбор в общей медицине №02 2026
Yulia M. Matyavina2
1 Krasnopolsky Moscow Regional Research Institute of Obstetrics and Gynecology, Moscow, Russia;
2 Ogarev National Research Mordovian State University, Saransk, Russia
kudashkinaanna37@mail.ru
Abstract
Relevance. Endometriosis is a chronic disease characterized by the ectopic localization of endometrial tissue and is widely prevalent among women of reproductive age (up to 9%). The condition is associated with chronic pelvic pain, dysmenorrhea, dyspareunia, and infertility, leading to a significant reduction in quality of life and reproductive potential. Despite decades of research, the etiology and pathogenesis of endometriosis remain insufficiently understood, while existing treatment methods, including hormonal therapy and surgical intervention, often provide only temporary relief and are associated with adverse effects. Therefore, an in-depth investigation of the molecular mechanisms underlying endometriosis and the development of novel therapeutic approaches remains highly relevant.
Aim. To summarize current data on the etiopathogenesis of endometriosis and to analyze promising directions for its treatment.
Materials and methods. A review of Russian and international publications from the past five years was conducted using the elibrary and PubMed databases, as well as the clinical guidelines “Endometriosis” developed by the Russian Society of Obstetricians and Gynecologists.
Results. The analysis revealed increased expression of estrogen receptor alpha (ERα) and decreased activity of estrogen receptor beta (ERβ) in endometriotic lesions, which contributes to enhanced tissue proliferation, inflammatory processes, and impaired immune response.
Conclusion. The obtained data confirm the key role of hormonal imbalance, particularly alterations in the ERα/ERβ ratio, in the pathogenesis of endometriosis and highlight the potential of molecular targeted therapy. Further investigation of pathogenetic mechanisms may contribute to the development of effective treatment strategies and prevention of complications, including oncological transformation.
Keywords: endometriosis, pathogenesis, conservative treatment, laparoscopy, progestins.
For citation: Vasina A.P., Kudashkina A.M., Shubin D.Yu., Andreeva N.A., Matyavina Yu.M. Current trends in the research of the etiopathogenesis and treatment of endometriosis. Clinical review for general practice. 2026; 7 (2): 41–44 (In Russ.). DOI: 10.47407/kr2026.7.02.00p4554
Актуальность
Эндометриоз – это хроническое воспалительное заболевание, связанное с гормональным фоном, при котором эндометриоидная ткань разрастается за пределами полости матки. Это заболевание поражает около 9% женщин репродуктивного возраста по всему миру.
Эндометриоз характеризуется множеством симптомов, среди которых: существенное ухудшение общего состояния здоровья, острые и продолжительные боли в тазовой области, нарушение функционирования органов малого таза, бесплодие, а также различные психические и эмоциональные расстройства. Женщины, страдающие от этого заболевания, часто испытывают значительное снижение качества жизни, повышенную утомляемость и дискомфорт в повседневной деятельности [1].
Цель настоящего исследования – обобщить и проанализировать современные данные об этиопатогенезе эндометриоза, а также рассмотреть перспективные направления лечения, основанные на последних научных достижениях.
Материалы и методы
Исследование и сбор актуальной информации осуществлялись с использованием открытых ресурсов, таких как eLibrary, PubMed, а также клинических рекомендаций «Эндометриоз», разработанных Российским обществом акушеров-гинекологов (РОАГ). Были проанализированы данные из российских и зарубежных статей за последние 5 лет. Результаты проведенных исследований систематизированы и представлены в данной работе.
Результаты
Патогенез эндометриоза представляет собой сложное переплетение генетических, гормональных и иммунных факторов, взаимодействующих между собой и способствующих прогрессированию данного заболевания.
Одной из самых заметных теорий, способствующих изучению эндометриоза, является концепция ретроградных менструаций, предложенная Артуром Сэмпсоном в начале XX в. Согласно этой теории, менструальная кровь, содержащая жизнеспособные клетки эндометриоидной ткани, может проникать через фаллопиевы трубы в брюшную полость, где происходит их имплантация на стенки внутренних органов или в области малого таза [2]. Эта идея объясняет, почему эндометриоз чаще всего локализуется в малом тазу и проявляется сильной хронической болью, а также различными другими симптомами.
Однако, несмотря на свою популярность и признание, данная теория не является панацеей. Большинство женщин сталкиваются с явлением ретроградной менструации, но лишь у небольшого процента из них диагностируется эндометриоз. Этот факт указывает на то, что, помимо ретроградного переноса клеток, существуют иные механизмы, способствующие возникновению заболевания. Более того, случаи, когда эндометриоз наблюдается за пределами брюшной полости, бросают тень сомнения на простоту объяснений, основанных только на этой теории [3].
Следующая теория, теория метастазирования, предполагает распространение клеток эндометрия по организму через лимфатическую или гематогенную системы [4]. Это означает, что клетки могут «путешествовать» по организму с током крови или лимфы и имплантироваться в отдаленные участки, начиная расти и размножаться, формируя очаги эндометриоза вне брюшной полости, в легких, торакальных лимфатических узлах, коже.
Теория иммунной дисрегуляции. Данная теория говорит, что нарушение нормальной иммунной реакции организма играет ключевую роль в развитии и прогрессировании заболевания. Вместо того чтобы эффективно уничтожать эктопические (расположенные вне матки) клетки эндометрия, иммунная система женщин с эндометриозом проявляет сниженную или измененную реакцию, позволяя этим клеткам выживать, расти и инвазировать окружающие ткани [5].
При эндометриозе наблюдаются изменения в клеточном иммунитете, которые затрагивают перитонеальные макрофаги и нейтрофилы, также он влияет на некоторые типы Т-клеток и естественных клеток-киллеров. Эти изменения включают в себя изменение производства цитокинов, хемокинов и других межклеточных медиаторов. Кроме того, может нарушиться то, как эти клетки распознают и реагируют на окружающие их вещи [6].
Нарушение функции макрофагов. Макрофаги играют ключевую роль в иммунном надзоре и процессах тканевой регенерации в эндометрии. В норме их количество и функциональная активность изменяются в зависимости от фазы менструального цикла, обеспечивая элиминацию апоптотических клеток и клеточного детрита [7].
При эндометриозе отмечается увеличение числа макрофагов как в эутопическом эндометрии, так и в перитонеальной жидкости, при этом их активность утрачивает циклический характер [8]. Такие макрофаги демонстрируют снижение способности к фагоцитозу и иммунному контролю, одновременно усиливая продукцию провоспалительных цитокинов и факторов роста. В результате макрофаги не только не устраняют эктопические эндометриоидные клетки, но и создают микросреду, способствующую их выживанию, инвазии и поддержанию хронического воспаления, что играет важную роль в прогрессировании эндометриоза.
Нарушение баланса Т-хелперов. Одним из значимых иммунных механизмов эндометриоза является дисбаланс между различными субпопуляциями Т-хелперов. В нормальных условиях соотношение Th1- и Th2-клеток обеспечивает адекватный противовоспалительный и цитотоксический иммунный ответ [9]. У пациенток с эндометриозом выявляется смещение иммунного баланса в сторону Th2-ассоциированного ответа, что сопровождается подавлением клеточного иммунитета и снижением активности механизмов, направленных на уничтожение эктопических эндометриоидных клеток [10]. Такое состояние способствует их иммунной толерантности, персистенции и дальнейшему росту. Нарушение регуляции Т-клеточного иммунитета рассматривается как один из факторов формирования хронического воспалительного процесса, поддерживающего клинические проявления эндометриоза и способствующего его рецидивированию [11].
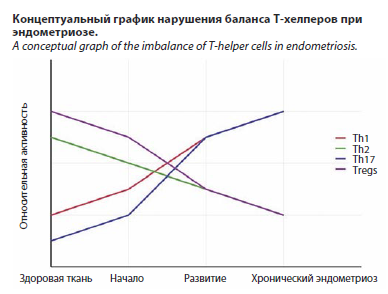 Концептуальный график нарушения баланса T-хелперов при эндометриозе представлен на рисунке. График наглядно демонстрирует, как происходит нарушение иммунного баланса при развитии эндометриоза: провоспалительные клетки (Th1 и Th17) увеличивают свою активность, в то время как регуляторные клетки (Th2 и Tregs) снижают свою активность, что приводит к развитию хронического воспаления.
Концептуальный график нарушения баланса T-хелперов при эндометриозе представлен на рисунке. График наглядно демонстрирует, как происходит нарушение иммунного баланса при развитии эндометриоза: провоспалительные клетки (Th1 и Th17) увеличивают свою активность, в то время как регуляторные клетки (Th2 и Tregs) снижают свою активность, что приводит к развитию хронического воспаления.
Теория гормонального дисбаланса. Гормональная теория эндометриоза также продолжает оставаться актуальной. Эстрогены, по мнению многих исследователей, способствуют не только распространению эндометриозной ткани, но и активации воспалительных процессов. Аномальные уровни гормонов, такие как прогестерон и тестостерон, могут взаимодействовать с клонированными эндометриальными клетками, приводя к их ненормальному поведению и адгезии к различным органам [12]. Исследования показывают, что повышенные уровни эстрогенов могут служить фактором риска для развития эндометриоза, а также способствовать его прогрессированию.
Эндометриоз характеризуется избыточной стимуляцией эстрогенами, что может приводить к увеличению числа эндометриальных клеток вне утробной полости. Дополнительные данные свидетельствуют о том, что женщины с нарушениями в метаболизме эстрогенов имеют повышенный риск развития эндометриоза, что подчеркивает важность баланса гормонов в организме [13].
Действие эстрогенов реализуется через связывание с рецепторами, расположенными на поверхности или внутри клеток. Основные типы рецепторов эстрогена – это ERα и ERβ.
ERα (эстрогеновый рецептор альфа) в основном отвечает за пролиферацию (размножение) клеток, рост тканей и регуляцию репродуктивных процессов. Стимуляция ERα часто ассоциируется с ростом эндометриоидных очагов.
ERβ (эстрогеновый рецептор бета) играет роль в модуляции воспаления, апоптозе (запрограммированной гибели клеток) и дифференцировке клеток. Влияние ERβ на эндометриоз более сложное, может оказывать как стимулирующее, так и ингибирующее действие в зависимости от контекста. При эндометриозе наблюдаются специфические изменения в экспрессии и активности рецепторов ERα и ERβ, которые способствуют развитию и прогрессированию заболевания [14].
В эндометриоидных очагах часто наблюдается повышенная экспрессия рецепторов ERα по сравнению с нормальным эндометрием. Это делает очаги более чувствительными к эстрогенам и способствует их пролиферации и росту.
В то же время экспрессия ERβ в эндометриоидных очагах может быть снижена, изменена или вовсе нарушена. Поскольку ERβ может оказывать защитное действие, подавляя рост клеток, нарушение его функции способствует развитию эндометриоза [15].
Рецепторы ERα в эндометриоидных клетках могут быть более чувствительны к эстрогенам, чем в нормальном эндометрии. Это может быть связано с изменениями в структуре рецепторов или в их сигнальных путях [16]. Даже если рецепторы ERβ присутствуют, их функция может быть нарушена, например, из-за изменений в структуре, сниженной способности связываться с эстрогенами или нарушений в их сигнальных путях.
Гормональный дисбаланс при эндометриозе на уровне рецепторов ERα и ERβ – это сложный процесс, включающий изменения в экспрессии, активности и чувствительности этих рецепторов. Сдвиг в соотношении ERα/ERβ в пользу ERα способствует пролиферации и воспалению [17]. Понимание этого механизма является ключом к разработке более эффективных стратегий диагностики и лечения эндометриоза.
Обсуждение
Современные методы лечения эндометриоза направлены на облегчение симптомов и на удаление в некоторых случаях эндометриоидных очагов. Полностью излечить эндометриоз невозможно, но можно ввести заболевание в стойкую длительную ремиссию. Лечение эндометриоза можно условно разделить на хирургическое удаление очагов поражения и небольшую группу медикаментозных методов лечения [18].
Согласно рекомендациям РОАГ, первоначальная терапия эндометриоза предполагает использование комбинированных методов, включающих эстрогены и прогестины, а также назначение прогестинов в сочетании с нестероидными противовоспалительными препаратами для облегчения болевого синдрома. Агонисты гонадотропин-рилизинг-гормона (ГнРГ) [19] рассматриваются в качестве второго этапа лечения, наряду с внутриматочными системами, содержащими левоноргестрел, и депо-прогестинами. Таким образом, комбинированные оральные контрацептивы (КОК) часто назначаются молодым женщинам, что позволяет также минимизировать риск незапланированной беременности.
Если эндометриоз проявляется бессимптомно или имеет невысокую степень выраженности, а также в случаях после хирургического вмешательства или наличии хронического воспалительного процесса в области половых органов, следует рассмотреть возможность начала лечения с применением КОК [20]. Использование КОК способствует значительному снижению объема кровотечений, ослаблению болевых симптомов и уменьшению размеров очагов эндометриоза.
КОК действуют, регулируя гормональный фон, что приводит к уменьшению активности эндометриозных тканей и снижению воспалительных реакций. Кроме того, использование таких контрацептивов может быть полезным для женщин, планирующих предотвратить беременность, поскольку они предоставляют двойную функцию: как защиту от нежелательной беременности, так и облегчение симптомов, связанных с заболеванием. Важно отметить, что выбор метода лечения должен осуществляться совместно с врачом, который сможет учесть индивидуальные особенности пациентки и возможные противопоказания к применению гормональной терапии.
Дополнительно к группе препаратов можно отнести депо-прогестины, которые используются для контроля симптомов, а также опиоидные анальгетики для более тяжелых случаев боли. Кроме того, существуют неоральные комбинированные гормональные контрацептивы, такие как трансдермальные пластыри или вагинальные кольца, которые предоставляют дополнительные опции для регулирования гормонального фона и уменьшения боли. Такие разнообразные подходы к лечению позволяют врачам выбирать наиболее подходящее решение в зависимости от индивидуальных особенностей пациента и клинической ситуации.
Агонисты ГнРГ. Эти препараты вызывают искусственную менопаузу, резко снижая уровень эстрогенов и подавляя функцию яичников, что приводит к значительному уменьшению размеров эндометриоидных очагов и облегчению боли. Однако длительное применение агонистов ГнРГ может вызвать побочные эффекты, связанные с эстрогенной недостаточностью.
При отсутствии положительного эффекта на протяжении 6 мес, наличии признаков распространенного эндометриоза, бесплодии неясного генеза в сочетании с другими предикторами эндометриоза, наличии противопоказаний к гормонотерапии, когда неинвазивный метод диагностики не позволяет идентифицировать причину боли, можно решать вопрос о целесообразности оперативного вмешательства [21].
При наружном эндометриозе, сопровождающемся образованием эндометриоидных кист, рекомендуется проводить эндоскопическое хирургическое вмешательство с аккуратной и бережной энуклеацией капсулы кисты. Основная цель такого подхода – максимальное сохранение овариального резерва, особенно у пациенток репродуктивного возраста, которые еще не реализовали свою репродуктивную функцию.
При лечении эндометриоза не следует ограничиваться исключительно хирургическим методом. Также крайне важно правильно подобрать препарат для послеоперационной терапии и определить ее длительность, чтобы предотвратить рецидивы заболевания.
Заключение
Таким образом, эндометриоз остается сложным и многогранным заболеванием, этиология которого до сих пор полностью не изучена. Несмотря на существование нескольких ведущих теорий, включающих ретроградную менструацию, иммунную дисрегуляцию, генетическую предрасположенность и гормональный дисбаланс, патогенез эндометриоза, вероятно, обусловлен сложным взаимодействием этих факторов. Отсутствие единой причины диктует необходимость комплексного подхода к лечению, который должен быть индивидуализирован с учетом тяжести симптомов, возраста пациентки, желания сохранить фертильность и индивидуальных особенностей организма.
Однако необходимы дальнейшие исследования для полного выяснения этиологии, совершенствования методов диагностики и разработки новых, более эффективных и безопасных методов лечения, направленных на предотвращение прогрессирования заболевания и улучшение качества жизни женщин, страдающих эндометриозом. Особое внимание следует уделить разработке персонализированных стратегий лечения, учитывающих индивидуальные генетические и иммунологические характеристики пациенток.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Васина Аксинья Петровна – ординатор, ГБУЗ МО «Московский областной НИИ акушерства
и гинекологии им. акад. В.И. Краснопольского». E-mail: k.vasina2018@yandex.ru;
ORCID: 0009-0013-6223-4125
Aksinya P. Vasina – Resident, Krasnopolsky Moscow Regional Research Institute of Obstetrics and Gynecology. E-mail: k.vasina2018@yandex.ru; ORCID: 0009-0013-6223-4125
Кудашкина Анна Михайловна – студентка медицинского института ФГБОУ ВО
«МГУ им. Н.П. Огарева». E-mail: kudashkina.anna37@bk.ru; ORCID: 0000-0004-3569-5826
Anna M. Kudashkina – Student, Ogarev National Research Mordovian State University.
E-mail: kudashkina.anna37@bk.ru; ORCID: 0000-0004-3569-5826
Шубин Даниил Юрьевич – ассистент каф. акушерства и гинекологии им. А.П. Марусова ФГБОУ ВО «МГУ им. Н.П. Огарева». E-mail: daniilshubin13rus@gmail.com; ORCID: 0000-0003-4582-9181
Daniil Yu. Shubin – Аssistant, Ogarev National Research Mordovian State University.
E-mail: daniilshubin13rus@gmail.com; ORCID: 0000-0003-4582-9181
Андреева Наталья Анатольевна – канд. мед. наук, доц. каф. акушерства и гинекологии
им. А.П. Марусова ФГБОУ ВО «МГУ им. Н.П. Огарева». E-mail: andreeva-77@list.ru;
ORCID: 0009-0004-0356-3158
Natalia A. Andreeva – Cand. Sci. (Med.), Associate Professor, Ogarev National Research Mordovian State University. E-mail: andreeva-77@list.ru; ORCID: 0009-0004-0356-3158
Матявина Юлия Михайловна – студентка Медицинского института ФГБОУ ВО
«МГУ им. Н.П. Огарева». E-mail: Matiayulia@yandex.ru; ORCID: 0000-0004-5236-7856
Yulia M. Matyavina – Student, Ogarev National Research Mordovian State University.
E-mail: Matiayulia@yandex.ru; ORCID: 0000-0004-5236-7856
Поступила в редакцию: 04.12.2025
Поступила после рецензирования: 24.12.2025
Принята к публикации: 22.01.2026
Received: 04.12.2025
Revised: 24.12.2025
Accepted: 22.01.2026
Клинический разбор в общей медицине №02 2026
Современные направления изучения этиопатогенеза и лечения эндометриоза
Номера страниц в выпуске:41-44
Аннотация
Актуальность. Эндометриоз – хроническое заболевание, характеризующееся эктопическим расположением эндометриальной ткани, широко распространенное среди женщин репродуктивного возраста (до 9%). Он ассоциирован с хронической тазовой болью, дисменореей, диспареунией и бесплодием, что существенно снижает качество жизни и репродуктивный потенциал пациенток. Несмотря на длительную историю изучения, этиология и патогенез эндометриоза остаются недостаточно изученными, а существующие методы лечения (гормональная терапия и хирургическое вмешательство) нередко имеют временный эффект и сопровождаются побочными явлениями. В связи с этим актуальной является необходимость углубленного анализа молекулярных механизмов заболевания и поиска новых терапевтических подходов.
Цель. Обобщить современные данные об этиопатогенезе эндометриоза и рассмотреть перспективные направления его лечения.
Материалы и методы. Проведен анализ отечественных и зарубежных публикаций за последние 5 лет, представленных в базах
eLibrary и PubMed, а также клинических рекомендаций «Эндометриоз», разработанных Российским обществом акушеров-гинекологов.
Результаты. Установлено, что в эндометриоидных очагах отмечаются повышение экспрессии рецепторов ERα и снижение активности ERβ, что способствует усилению пролиферации ткани, воспалительной реакции и нарушению иммунного ответа.
Заключение. Полученные данные подтверждают ключевую роль гормонального дисбаланса в патогенезе эндометриоза и указывают на перспективность молекулярно-таргетированной терапии. Изучение патогенетических механизмов заболевания имеет важное значение для разработки эффективных методов лечения и профилактики осложнений, включая онкологические.
Ключевые слова: эндометриоз, патогенез, консервативное лечение, лапароскопия, прогестины.
Для цитирования: Васина А.П., Кудашкина А.М., Шубин Д.Ю., Андреева Н.А., Матявина Ю.М. Современные направления изучения этиопатогенеза и лечения эндометриоза. Клинический разбор в общей медицине. 2026; 7 (2): 41–44. DOI: 10.47407/kr2026.7.02.00p4554
Актуальность. Эндометриоз – хроническое заболевание, характеризующееся эктопическим расположением эндометриальной ткани, широко распространенное среди женщин репродуктивного возраста (до 9%). Он ассоциирован с хронической тазовой болью, дисменореей, диспареунией и бесплодием, что существенно снижает качество жизни и репродуктивный потенциал пациенток. Несмотря на длительную историю изучения, этиология и патогенез эндометриоза остаются недостаточно изученными, а существующие методы лечения (гормональная терапия и хирургическое вмешательство) нередко имеют временный эффект и сопровождаются побочными явлениями. В связи с этим актуальной является необходимость углубленного анализа молекулярных механизмов заболевания и поиска новых терапевтических подходов.
Цель. Обобщить современные данные об этиопатогенезе эндометриоза и рассмотреть перспективные направления его лечения.
Материалы и методы. Проведен анализ отечественных и зарубежных публикаций за последние 5 лет, представленных в базах
eLibrary и PubMed, а также клинических рекомендаций «Эндометриоз», разработанных Российским обществом акушеров-гинекологов.
Результаты. Установлено, что в эндометриоидных очагах отмечаются повышение экспрессии рецепторов ERα и снижение активности ERβ, что способствует усилению пролиферации ткани, воспалительной реакции и нарушению иммунного ответа.
Заключение. Полученные данные подтверждают ключевую роль гормонального дисбаланса в патогенезе эндометриоза и указывают на перспективность молекулярно-таргетированной терапии. Изучение патогенетических механизмов заболевания имеет важное значение для разработки эффективных методов лечения и профилактики осложнений, включая онкологические.
Ключевые слова: эндометриоз, патогенез, консервативное лечение, лапароскопия, прогестины.
Для цитирования: Васина А.П., Кудашкина А.М., Шубин Д.Ю., Андреева Н.А., Матявина Ю.М. Современные направления изучения этиопатогенеза и лечения эндометриоза. Клинический разбор в общей медицине. 2026; 7 (2): 41–44. DOI: 10.47407/kr2026.7.02.00p4554
Current trends in the research of the etiopathogenesis and treatment of endometriosis
Aksinya P. Vasina1, Anna M. Kudashkina2, Daniil Yu. Shubin2, Natalia A. Andreeva2,Yulia M. Matyavina2
1 Krasnopolsky Moscow Regional Research Institute of Obstetrics and Gynecology, Moscow, Russia;
2 Ogarev National Research Mordovian State University, Saransk, Russia
kudashkinaanna37@mail.ru
Abstract
Relevance. Endometriosis is a chronic disease characterized by the ectopic localization of endometrial tissue and is widely prevalent among women of reproductive age (up to 9%). The condition is associated with chronic pelvic pain, dysmenorrhea, dyspareunia, and infertility, leading to a significant reduction in quality of life and reproductive potential. Despite decades of research, the etiology and pathogenesis of endometriosis remain insufficiently understood, while existing treatment methods, including hormonal therapy and surgical intervention, often provide only temporary relief and are associated with adverse effects. Therefore, an in-depth investigation of the molecular mechanisms underlying endometriosis and the development of novel therapeutic approaches remains highly relevant.
Aim. To summarize current data on the etiopathogenesis of endometriosis and to analyze promising directions for its treatment.
Materials and methods. A review of Russian and international publications from the past five years was conducted using the elibrary and PubMed databases, as well as the clinical guidelines “Endometriosis” developed by the Russian Society of Obstetricians and Gynecologists.
Results. The analysis revealed increased expression of estrogen receptor alpha (ERα) and decreased activity of estrogen receptor beta (ERβ) in endometriotic lesions, which contributes to enhanced tissue proliferation, inflammatory processes, and impaired immune response.
Conclusion. The obtained data confirm the key role of hormonal imbalance, particularly alterations in the ERα/ERβ ratio, in the pathogenesis of endometriosis and highlight the potential of molecular targeted therapy. Further investigation of pathogenetic mechanisms may contribute to the development of effective treatment strategies and prevention of complications, including oncological transformation.
Keywords: endometriosis, pathogenesis, conservative treatment, laparoscopy, progestins.
For citation: Vasina A.P., Kudashkina A.M., Shubin D.Yu., Andreeva N.A., Matyavina Yu.M. Current trends in the research of the etiopathogenesis and treatment of endometriosis. Clinical review for general practice. 2026; 7 (2): 41–44 (In Russ.). DOI: 10.47407/kr2026.7.02.00p4554
Актуальность
Эндометриоз – это хроническое воспалительное заболевание, связанное с гормональным фоном, при котором эндометриоидная ткань разрастается за пределами полости матки. Это заболевание поражает около 9% женщин репродуктивного возраста по всему миру.
Эндометриоз характеризуется множеством симптомов, среди которых: существенное ухудшение общего состояния здоровья, острые и продолжительные боли в тазовой области, нарушение функционирования органов малого таза, бесплодие, а также различные психические и эмоциональные расстройства. Женщины, страдающие от этого заболевания, часто испытывают значительное снижение качества жизни, повышенную утомляемость и дискомфорт в повседневной деятельности [1].
Цель настоящего исследования – обобщить и проанализировать современные данные об этиопатогенезе эндометриоза, а также рассмотреть перспективные направления лечения, основанные на последних научных достижениях.
Материалы и методы
Исследование и сбор актуальной информации осуществлялись с использованием открытых ресурсов, таких как eLibrary, PubMed, а также клинических рекомендаций «Эндометриоз», разработанных Российским обществом акушеров-гинекологов (РОАГ). Были проанализированы данные из российских и зарубежных статей за последние 5 лет. Результаты проведенных исследований систематизированы и представлены в данной работе.
Результаты
Патогенез эндометриоза представляет собой сложное переплетение генетических, гормональных и иммунных факторов, взаимодействующих между собой и способствующих прогрессированию данного заболевания.
Одной из самых заметных теорий, способствующих изучению эндометриоза, является концепция ретроградных менструаций, предложенная Артуром Сэмпсоном в начале XX в. Согласно этой теории, менструальная кровь, содержащая жизнеспособные клетки эндометриоидной ткани, может проникать через фаллопиевы трубы в брюшную полость, где происходит их имплантация на стенки внутренних органов или в области малого таза [2]. Эта идея объясняет, почему эндометриоз чаще всего локализуется в малом тазу и проявляется сильной хронической болью, а также различными другими симптомами.
Однако, несмотря на свою популярность и признание, данная теория не является панацеей. Большинство женщин сталкиваются с явлением ретроградной менструации, но лишь у небольшого процента из них диагностируется эндометриоз. Этот факт указывает на то, что, помимо ретроградного переноса клеток, существуют иные механизмы, способствующие возникновению заболевания. Более того, случаи, когда эндометриоз наблюдается за пределами брюшной полости, бросают тень сомнения на простоту объяснений, основанных только на этой теории [3].
Следующая теория, теория метастазирования, предполагает распространение клеток эндометрия по организму через лимфатическую или гематогенную системы [4]. Это означает, что клетки могут «путешествовать» по организму с током крови или лимфы и имплантироваться в отдаленные участки, начиная расти и размножаться, формируя очаги эндометриоза вне брюшной полости, в легких, торакальных лимфатических узлах, коже.
Теория иммунной дисрегуляции. Данная теория говорит, что нарушение нормальной иммунной реакции организма играет ключевую роль в развитии и прогрессировании заболевания. Вместо того чтобы эффективно уничтожать эктопические (расположенные вне матки) клетки эндометрия, иммунная система женщин с эндометриозом проявляет сниженную или измененную реакцию, позволяя этим клеткам выживать, расти и инвазировать окружающие ткани [5].
При эндометриозе наблюдаются изменения в клеточном иммунитете, которые затрагивают перитонеальные макрофаги и нейтрофилы, также он влияет на некоторые типы Т-клеток и естественных клеток-киллеров. Эти изменения включают в себя изменение производства цитокинов, хемокинов и других межклеточных медиаторов. Кроме того, может нарушиться то, как эти клетки распознают и реагируют на окружающие их вещи [6].
Нарушение функции макрофагов. Макрофаги играют ключевую роль в иммунном надзоре и процессах тканевой регенерации в эндометрии. В норме их количество и функциональная активность изменяются в зависимости от фазы менструального цикла, обеспечивая элиминацию апоптотических клеток и клеточного детрита [7].
При эндометриозе отмечается увеличение числа макрофагов как в эутопическом эндометрии, так и в перитонеальной жидкости, при этом их активность утрачивает циклический характер [8]. Такие макрофаги демонстрируют снижение способности к фагоцитозу и иммунному контролю, одновременно усиливая продукцию провоспалительных цитокинов и факторов роста. В результате макрофаги не только не устраняют эктопические эндометриоидные клетки, но и создают микросреду, способствующую их выживанию, инвазии и поддержанию хронического воспаления, что играет важную роль в прогрессировании эндометриоза.
Нарушение баланса Т-хелперов. Одним из значимых иммунных механизмов эндометриоза является дисбаланс между различными субпопуляциями Т-хелперов. В нормальных условиях соотношение Th1- и Th2-клеток обеспечивает адекватный противовоспалительный и цитотоксический иммунный ответ [9]. У пациенток с эндометриозом выявляется смещение иммунного баланса в сторону Th2-ассоциированного ответа, что сопровождается подавлением клеточного иммунитета и снижением активности механизмов, направленных на уничтожение эктопических эндометриоидных клеток [10]. Такое состояние способствует их иммунной толерантности, персистенции и дальнейшему росту. Нарушение регуляции Т-клеточного иммунитета рассматривается как один из факторов формирования хронического воспалительного процесса, поддерживающего клинические проявления эндометриоза и способствующего его рецидивированию [11].
 Концептуальный график нарушения баланса T-хелперов при эндометриозе представлен на рисунке. График наглядно демонстрирует, как происходит нарушение иммунного баланса при развитии эндометриоза: провоспалительные клетки (Th1 и Th17) увеличивают свою активность, в то время как регуляторные клетки (Th2 и Tregs) снижают свою активность, что приводит к развитию хронического воспаления.
Концептуальный график нарушения баланса T-хелперов при эндометриозе представлен на рисунке. График наглядно демонстрирует, как происходит нарушение иммунного баланса при развитии эндометриоза: провоспалительные клетки (Th1 и Th17) увеличивают свою активность, в то время как регуляторные клетки (Th2 и Tregs) снижают свою активность, что приводит к развитию хронического воспаления.Теория гормонального дисбаланса. Гормональная теория эндометриоза также продолжает оставаться актуальной. Эстрогены, по мнению многих исследователей, способствуют не только распространению эндометриозной ткани, но и активации воспалительных процессов. Аномальные уровни гормонов, такие как прогестерон и тестостерон, могут взаимодействовать с клонированными эндометриальными клетками, приводя к их ненормальному поведению и адгезии к различным органам [12]. Исследования показывают, что повышенные уровни эстрогенов могут служить фактором риска для развития эндометриоза, а также способствовать его прогрессированию.
Эндометриоз характеризуется избыточной стимуляцией эстрогенами, что может приводить к увеличению числа эндометриальных клеток вне утробной полости. Дополнительные данные свидетельствуют о том, что женщины с нарушениями в метаболизме эстрогенов имеют повышенный риск развития эндометриоза, что подчеркивает важность баланса гормонов в организме [13].
Действие эстрогенов реализуется через связывание с рецепторами, расположенными на поверхности или внутри клеток. Основные типы рецепторов эстрогена – это ERα и ERβ.
ERα (эстрогеновый рецептор альфа) в основном отвечает за пролиферацию (размножение) клеток, рост тканей и регуляцию репродуктивных процессов. Стимуляция ERα часто ассоциируется с ростом эндометриоидных очагов.
ERβ (эстрогеновый рецептор бета) играет роль в модуляции воспаления, апоптозе (запрограммированной гибели клеток) и дифференцировке клеток. Влияние ERβ на эндометриоз более сложное, может оказывать как стимулирующее, так и ингибирующее действие в зависимости от контекста. При эндометриозе наблюдаются специфические изменения в экспрессии и активности рецепторов ERα и ERβ, которые способствуют развитию и прогрессированию заболевания [14].
В эндометриоидных очагах часто наблюдается повышенная экспрессия рецепторов ERα по сравнению с нормальным эндометрием. Это делает очаги более чувствительными к эстрогенам и способствует их пролиферации и росту.
В то же время экспрессия ERβ в эндометриоидных очагах может быть снижена, изменена или вовсе нарушена. Поскольку ERβ может оказывать защитное действие, подавляя рост клеток, нарушение его функции способствует развитию эндометриоза [15].
Рецепторы ERα в эндометриоидных клетках могут быть более чувствительны к эстрогенам, чем в нормальном эндометрии. Это может быть связано с изменениями в структуре рецепторов или в их сигнальных путях [16]. Даже если рецепторы ERβ присутствуют, их функция может быть нарушена, например, из-за изменений в структуре, сниженной способности связываться с эстрогенами или нарушений в их сигнальных путях.
Гормональный дисбаланс при эндометриозе на уровне рецепторов ERα и ERβ – это сложный процесс, включающий изменения в экспрессии, активности и чувствительности этих рецепторов. Сдвиг в соотношении ERα/ERβ в пользу ERα способствует пролиферации и воспалению [17]. Понимание этого механизма является ключом к разработке более эффективных стратегий диагностики и лечения эндометриоза.
Обсуждение
Современные методы лечения эндометриоза направлены на облегчение симптомов и на удаление в некоторых случаях эндометриоидных очагов. Полностью излечить эндометриоз невозможно, но можно ввести заболевание в стойкую длительную ремиссию. Лечение эндометриоза можно условно разделить на хирургическое удаление очагов поражения и небольшую группу медикаментозных методов лечения [18].
Согласно рекомендациям РОАГ, первоначальная терапия эндометриоза предполагает использование комбинированных методов, включающих эстрогены и прогестины, а также назначение прогестинов в сочетании с нестероидными противовоспалительными препаратами для облегчения болевого синдрома. Агонисты гонадотропин-рилизинг-гормона (ГнРГ) [19] рассматриваются в качестве второго этапа лечения, наряду с внутриматочными системами, содержащими левоноргестрел, и депо-прогестинами. Таким образом, комбинированные оральные контрацептивы (КОК) часто назначаются молодым женщинам, что позволяет также минимизировать риск незапланированной беременности.
Если эндометриоз проявляется бессимптомно или имеет невысокую степень выраженности, а также в случаях после хирургического вмешательства или наличии хронического воспалительного процесса в области половых органов, следует рассмотреть возможность начала лечения с применением КОК [20]. Использование КОК способствует значительному снижению объема кровотечений, ослаблению болевых симптомов и уменьшению размеров очагов эндометриоза.
КОК действуют, регулируя гормональный фон, что приводит к уменьшению активности эндометриозных тканей и снижению воспалительных реакций. Кроме того, использование таких контрацептивов может быть полезным для женщин, планирующих предотвратить беременность, поскольку они предоставляют двойную функцию: как защиту от нежелательной беременности, так и облегчение симптомов, связанных с заболеванием. Важно отметить, что выбор метода лечения должен осуществляться совместно с врачом, который сможет учесть индивидуальные особенности пациентки и возможные противопоказания к применению гормональной терапии.
Дополнительно к группе препаратов можно отнести депо-прогестины, которые используются для контроля симптомов, а также опиоидные анальгетики для более тяжелых случаев боли. Кроме того, существуют неоральные комбинированные гормональные контрацептивы, такие как трансдермальные пластыри или вагинальные кольца, которые предоставляют дополнительные опции для регулирования гормонального фона и уменьшения боли. Такие разнообразные подходы к лечению позволяют врачам выбирать наиболее подходящее решение в зависимости от индивидуальных особенностей пациента и клинической ситуации.
Агонисты ГнРГ. Эти препараты вызывают искусственную менопаузу, резко снижая уровень эстрогенов и подавляя функцию яичников, что приводит к значительному уменьшению размеров эндометриоидных очагов и облегчению боли. Однако длительное применение агонистов ГнРГ может вызвать побочные эффекты, связанные с эстрогенной недостаточностью.
При отсутствии положительного эффекта на протяжении 6 мес, наличии признаков распространенного эндометриоза, бесплодии неясного генеза в сочетании с другими предикторами эндометриоза, наличии противопоказаний к гормонотерапии, когда неинвазивный метод диагностики не позволяет идентифицировать причину боли, можно решать вопрос о целесообразности оперативного вмешательства [21].
При наружном эндометриозе, сопровождающемся образованием эндометриоидных кист, рекомендуется проводить эндоскопическое хирургическое вмешательство с аккуратной и бережной энуклеацией капсулы кисты. Основная цель такого подхода – максимальное сохранение овариального резерва, особенно у пациенток репродуктивного возраста, которые еще не реализовали свою репродуктивную функцию.
При лечении эндометриоза не следует ограничиваться исключительно хирургическим методом. Также крайне важно правильно подобрать препарат для послеоперационной терапии и определить ее длительность, чтобы предотвратить рецидивы заболевания.
Заключение
Таким образом, эндометриоз остается сложным и многогранным заболеванием, этиология которого до сих пор полностью не изучена. Несмотря на существование нескольких ведущих теорий, включающих ретроградную менструацию, иммунную дисрегуляцию, генетическую предрасположенность и гормональный дисбаланс, патогенез эндометриоза, вероятно, обусловлен сложным взаимодействием этих факторов. Отсутствие единой причины диктует необходимость комплексного подхода к лечению, который должен быть индивидуализирован с учетом тяжести симптомов, возраста пациентки, желания сохранить фертильность и индивидуальных особенностей организма.
Однако необходимы дальнейшие исследования для полного выяснения этиологии, совершенствования методов диагностики и разработки новых, более эффективных и безопасных методов лечения, направленных на предотвращение прогрессирования заболевания и улучшение качества жизни женщин, страдающих эндометриозом. Особое внимание следует уделить разработке персонализированных стратегий лечения, учитывающих индивидуальные генетические и иммунологические характеристики пациенток.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Васина Аксинья Петровна – ординатор, ГБУЗ МО «Московский областной НИИ акушерства
и гинекологии им. акад. В.И. Краснопольского». E-mail: k.vasina2018@yandex.ru;
ORCID: 0009-0013-6223-4125
Aksinya P. Vasina – Resident, Krasnopolsky Moscow Regional Research Institute of Obstetrics and Gynecology. E-mail: k.vasina2018@yandex.ru; ORCID: 0009-0013-6223-4125
Кудашкина Анна Михайловна – студентка медицинского института ФГБОУ ВО
«МГУ им. Н.П. Огарева». E-mail: kudashkina.anna37@bk.ru; ORCID: 0000-0004-3569-5826
Anna M. Kudashkina – Student, Ogarev National Research Mordovian State University.
E-mail: kudashkina.anna37@bk.ru; ORCID: 0000-0004-3569-5826
Шубин Даниил Юрьевич – ассистент каф. акушерства и гинекологии им. А.П. Марусова ФГБОУ ВО «МГУ им. Н.П. Огарева». E-mail: daniilshubin13rus@gmail.com; ORCID: 0000-0003-4582-9181
Daniil Yu. Shubin – Аssistant, Ogarev National Research Mordovian State University.
E-mail: daniilshubin13rus@gmail.com; ORCID: 0000-0003-4582-9181
Андреева Наталья Анатольевна – канд. мед. наук, доц. каф. акушерства и гинекологии
им. А.П. Марусова ФГБОУ ВО «МГУ им. Н.П. Огарева». E-mail: andreeva-77@list.ru;
ORCID: 0009-0004-0356-3158
Natalia A. Andreeva – Cand. Sci. (Med.), Associate Professor, Ogarev National Research Mordovian State University. E-mail: andreeva-77@list.ru; ORCID: 0009-0004-0356-3158
Матявина Юлия Михайловна – студентка Медицинского института ФГБОУ ВО
«МГУ им. Н.П. Огарева». E-mail: Matiayulia@yandex.ru; ORCID: 0000-0004-5236-7856
Yulia M. Matyavina – Student, Ogarev National Research Mordovian State University.
E-mail: Matiayulia@yandex.ru; ORCID: 0000-0004-5236-7856
Поступила в редакцию: 04.12.2025
Поступила после рецензирования: 24.12.2025
Принята к публикации: 22.01.2026
Received: 04.12.2025
Revised: 24.12.2025
Accepted: 22.01.2026
Список исп. литературыСкрыть список1. Filip L, Duică F, Prădatu A et al. Endometriosis associated Infertility: a critical review and analysis on etiopathogenesis and therapeutic approaches. Medicina (Kaunas) 2020;56:9:460. DOI: 10.3390/medicina56090460
2. Keettel WC, Stein RJ. The viability of the cast-off menstrual endometrium. Am J Obstetrics Gynecol 1951;61(2):440-2.
3. Yovich JL, Rowlands PK, Lingham, S et al.Pathogenesis of endometriosis: Look no further than John Sampson. Reprod Biomed Online 2020;40:7-11.
4. Howkins & Bourne Shaw’s Textbook of Gynecology. 16th edition. Published by Reed Elsevier India Private Limited, 2015.
5. Beste MT, Pfaffle-Doyle N, Prentice EA et al. Endometriosis: Molecular network analysis of endometriosis reveals a role for c-Jun-regulated macrophage activation. Sci Translational Med 2014;6:222. DOI: 10.1126/scitranslmed.3007988.222ra16
6. Kapoor R, Stratopoulou CA, Dolmans MM. Pathogenesis of endometriosis: New insights into prospective therapies. Int J Mol Sci 2021;22:11700.
7. Vallvé-Juanico J, Houshdaran S, Giudice LC. The endometrial immune environment of women with endometriosis. Hum Reprod Update 2019;25:565-92.
8. Abramiuk M, Grywalska E, Małkowska P et al. The role of the immune system in the development of endometriosis. Cells 2022;11:2028.
9. Berbic M, Schulke L, Markham R et al.Macrophage expression in endometrium of women with and without endometriosis. Hum Reprod 2009;24:325-32.
10. Smolarz B, Szyłło K, Romanowicz H. Endometriosis: Epidemiology, classification, pathogenesis, treatment and genetics (Review of literature). Int J Mol Sci 2021;22:10554.
11. Rizner TL. Estrogen metabolism and action in endometriosis. Mol Cell Endocrinol 2009;307: 8-18.
12. Marquardt RM, Kim TH, Shin JH, Jeong JW. Progesterone and estrogen signaling in the endometrium: What goes wrong in endometriosis? Int J Mol Sci 2019;20:3822.
13. Koukoura O, Sifakis S, Spandidos DA. DNA methylation in endometriosis (Review). Mol Med Rep 2016;13:2939-48.
14. Jiang L, Yan Y, Liu Z, Wang Y. Inflammation and endometriosis. Front Biosci 2016;21:941-8.
15. Asghari S, Valizadeh A, Aghebati-Maleki L et al. Endometriosis: Perspective, lights, and shadows of etiology. Biomed Pharmacother 2018;106:163-74.
16. Kim JJ, Kurita T, Bulun SE. Progesterone action in endometrial cancer, endometriosis, uterine fibroids, and breast cancer. Endocr Rev 2013;34:130-62.
17. Saunders PTK, Horne AW. Endometriosis: Etiology, pathobiology, and therapeutic prospects. Cell 2021;184:2807-24
18. Taylor HS, Kotlyar AM, Flores VA. Endometriosis is a chronic systemic disease: clinical challenges and novel innovations. Lancet 2021;397(10276):839-52.
19. Эндометриоз. Клинические рекомендации Минздрава России. М., 2024. URL: http://www.medico.crimea.com/cprot/endometr.pdf. Klinicheskie rekomendatsii
Endometriosis. Clinical recommendations, Ministry of Health of the Russian Federation. Moscow, 2024. URL: http://www.medico. crimea.com/cprot/endometr.pdf (in Russian).
20. Vercellini P, Buggio L, Berlanda N et al. Estrogen-progestins and progestins for the management of endometriosis. Fertil Steril 2016;106(7):1552-71.e2. DOI: 10.1016/j. fertnstert.2016.10.022
21. Jacobson TZ, Duffy JM, Barlow DH et al. WITHDRAWN: Laparoscopic surgery for pelvic pain associated with endometriosis. Cochrane Database Syst Rev 2014;2014(8):CD001300. DOI: 10.1002/14651858. CD001300.pub3.
21 апреля 2026
Количество просмотров: 175
